Журнал неорганической химии, 2022, T. 67, № 2, стр. 216-223
Триангуляция в системе Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7
М. А. Петрова a, *, О. Ю. Синельщикова a
a Институт химии силикатов им. И.В. Гребенщикова РАН
199034 Санкт-Петербург, наб. Макарова, 2, Россия
* E-mail: maya_petrova@inbox.ru
Поступила в редакцию 31.05.2021
После доработки 28.07.2021
Принята к публикации 04.08.2021
- EDN: KITRBP
- DOI: 10.31857/S0044457X2202012X
Аннотация
Целесообразность изучения фазовых диаграмм состояния фосфатных систем щелочных элементов
и цинка определяется перспективой их использования в качестве катализаторов, ионных
проводников, люминофоров, твердотельных лазеров, пьезоэлектрических и других материалов
c ценными для практики свойствами. Методом рентгенофазового анализа исследовано фазообразование
в частных разрезах LiNaZnP2O7–NaKZnP2O7 и LiNaZnP2O7–K2ZnP2O7 тройной системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 на образцах, полученных твердофазным синтезом. На основании анализа совокупности
данных по фазовым равновесиям ранее изученных систем ${\text{M}}_{2}^{{\text{'}}}$ZnP2O7–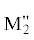 ZnP2O7 (M', M" = Li, Na, K) и LiKZnP2O7–LiNaZnP2O7 (NaKZnP2O7, Na2ZnP2O7), а также данных, полученных в настоящей работе, проведена триангуляция тройной системы
Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 в области, ограниченной соединениями Na2ZnP2O7, LiNaZnP2O7, LiKZnP2O7 и K2ZnP2O7. Установлено образование твердых растворов, содержащих три щелочных элемента: LixNayK2 – (x + y)ZnP2O7 (0 ≤ x ≤ 0.8, 0.2 ≤ y ≤ 1.0) на основе NaKZnP2O7 (пр. гр. P21/n) и LixNayK2 – (x + y)ZnP2O7 (0 ≤ x ≤ 0.17, 0 ≤ y ≤ 0.42) на основе K2ZnP2O7 (пр. гр. P42/mnm). По результатам исследования уточнена диаграмма состояния системы Li2ZnP2O7–K2ZnP2O7.
ZnP2O7 (M', M" = Li, Na, K) и LiKZnP2O7–LiNaZnP2O7 (NaKZnP2O7, Na2ZnP2O7), а также данных, полученных в настоящей работе, проведена триангуляция тройной системы
Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 в области, ограниченной соединениями Na2ZnP2O7, LiNaZnP2O7, LiKZnP2O7 и K2ZnP2O7. Установлено образование твердых растворов, содержащих три щелочных элемента: LixNayK2 – (x + y)ZnP2O7 (0 ≤ x ≤ 0.8, 0.2 ≤ y ≤ 1.0) на основе NaKZnP2O7 (пр. гр. P21/n) и LixNayK2 – (x + y)ZnP2O7 (0 ≤ x ≤ 0.17, 0 ≤ y ≤ 0.42) на основе K2ZnP2O7 (пр. гр. P42/mnm). По результатам исследования уточнена диаграмма состояния системы Li2ZnP2O7–K2ZnP2O7.
ВВЕДЕНИЕ
Исследование фосфатов щелочных металлов и цинка обусловлено их значением для практики, например, для получения стекол, керамики [1–7], ионных проводников [8–11], сегнето- и пьезоэлектрических материалов [1], люминофоров, в том числе применимых для лазерной техники [6, 12–19] и в других специальных областях. Одна из возможностей расширения круга новых индивидуальных фаз и фаз переменного состава с ценными свойствами – использование различных типов изоморфных замещений как в катионной, так и в анионной подрешетке [20–24]. С этой точки зрения определенный интерес представляет изучение фазовых соотношений в соответствующих фосфатных системах, что открывает большие возможности для целенаправленного синтеза новых неорганических материалов, в том числе и композиционных.
В предшествующих работах по цинкофосфатам щелочных металлов [25–29] изучены фазовые соотношения в бинарных дифосфатных системах, которые графически могут быть представлены наружными и внутренними сторонами концентрационного треугольника Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 (рис. 1). Краткое описание ранее изученных систем приведено ниже.
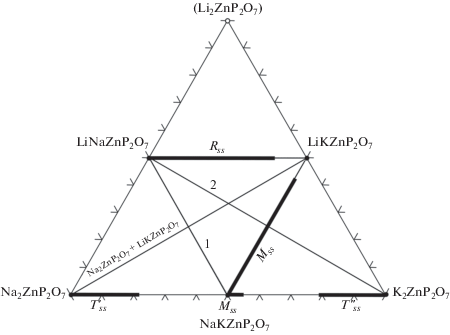
Рис. 1.
Фазовый треугольник системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7. Полужирными линиями указаны твердые растворы при 25°С: тетрагональные Na2 –xKxZnP2O7 (0.0 < х ≤ 0.46) – $T_{{ss}}^{'}$ и NaxK2 –xZnP2O7 (0 < x ≤ 0.42) – 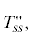 моноклинные Na1 –xK1 +xZnP2O7 (0 ≤ x ≤ 0.1) и LixNa1 –xKZnP2O7 (0 ≤ x ≤ 0.8) – Mss, орторомбический LiNa1 –xKxZnP2O7 (0 ≤ x ≤ 0.85) – Rss; 1 и 2 – исследуемые разрезы.
моноклинные Na1 –xK1 +xZnP2O7 (0 ≤ x ≤ 0.1) и LixNa1 –xKZnP2O7 (0 ≤ x ≤ 0.8) – Mss, орторомбический LiNa1 –xKxZnP2O7 (0 ≤ x ≤ 0.85) – Rss; 1 и 2 – исследуемые разрезы.
Системы ${\text{M}}_{2}^{'}$ZnP2O7–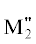 ZnP2O7 (M', M" = Li, Na, K) образованы смешанными дифосфатами цинка и являются наружными сторонами треугольника
Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 [25, 26] на рис. 1.
ZnP2O7 (M', M" = Li, Na, K) образованы смешанными дифосфатами цинка и являются наружными сторонами треугольника
Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 [25, 26] на рис. 1.
В системах образуется по одному эквимолярному соединению с двумя щелочными катионами LiNaZnP2O7 (Cmcm), α- и β-LiKZnP2O7 (Pc и Pmc21 соответственно) и NaKZnP2O7 (P21/n). Кроме того, в системе Na2ZnP2O7–K2ZnP2O7 установлено образование трех типов твердых растворов на основе Na2ZnP2O7 (P42/mnm) и K2ZnP2O7 (P42/mnm) с предельной растворимостью второго компонента при комнатной температуре 23 и 21 мол. % соответственно, а также на основе соединения NaKZnP2O7 с содержанием до 5 мол. % K2ZnP2O7.
Соединения со стехиометрией, подобной М2ZnP2O7 (M = Na, K), для лития не установлены. Согласно фазовой диаграмме состояния системы Zn2P2O7–Li4P2O7 [25], составу Li2ZnP2O7 соответствует смесь двух фаз: соединения Li12Zn4(P2O7)5 и твердого раствора Li2xZn2 –xP2O7 (0.3 $ \leqslant $ х $ \leqslant $ 0.56). Исходя из этого субсолидусные фазовые соотношения между несуществующей фазой Li2ZnP2O7 и соответствующими соединениями LiNaZnP2O7 и LiКZnP2O7 (рис. 1) находятся в области трехфазных равновесий, так как данные части систем являются политермическими сечениями в поле тройных систем (Li12Zn4(P2O7)5 + + Li2хZn2 –хP2O7 + LiМZnP2O7 (М = Na, K)).
Системы LiKZnP2O7–LiNaZnP2O7 (NaKZnP2O7, Na2ZnP2O7) являются внутренними сечениями концентрационного треугольника Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 (рис. 1). В системах LiKZnP2O7–LiNaZnP2O7 и LiKZnP2O7–NaKZnP2O7 установлены обширные области ограниченных твердых растворов, содержащих одновременно три щелочных катиона: ромбический. LiNa1 –xKxZnP2O7 (0 ≤ x ≤ 0.85) на основе LiNaZnP2O7 (пр. гр. Cmcm) и моноклинный LixNa1 –xKZnP2O7 (0 ≤ x ≤ 0.80) на основе NaKZnP2O7 (пр. гр. P21/n) [24, 25]. На рис. 1 они обозначены как Rss и Mss соответственно.
Система LiKZnP2O7–Na2ZnP2O7 является эвтектической. Субсолидусные фазовые соотношения в ней представлены смесью исходных компонентов; взаимодействие между ними не обнаружено [29].
С целью разбиения упомянутой тройной системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 на элементарные треугольники в настоящей работе в дополнение к ранее изученным системам исследовано фазообразование в системах LiNaZnP2O7–NaKZnP2O7 и LiNaZnP2O7–K2ZnP2O7 (разрезы 1 и 2 на рис. 1).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Образцы в разрезах 1 и 2 готовили из предварительно синтезированных соответствующих исходных компонентов систем LiNaZnP2O7, NaKZnP2O7 и K2ZnP2O7, которые, в свою очередь, были получены по методике, описанной в [24, 25] с использованием следующих реактивов: ZnO, Li2CO3, NaPO3, KPO3 (х. ч.) и NH4H2PO4 (ос. ч.). Смеси исходных компонентов, взятых в необходимых соотношениях, прессовали в таблетки и обжигали при температуре 550°С в течение 11 ч. Образцы после обжига исследовали с помощью рентгенофазового анализа (РФА). Съемку проводили на дифрактометре ДРОН-3М (излучение CuKα) при комнатной температуре в интервале брэгговских углов 2θ 10°–70° с шагом 0.02°.
Результаты РФА образцов в указанных системах представлены на рис. 2, 3 и в табл. 1.
Рис. 2.
Дифрактограммы (1 – x)LiNaZnP2O7 : xNaKZnP2O7 (разрез 1) при комнатной температуре. $T_{{ss}}^{'}$ (Na2 ‒ yKyZnP2O7 при 0 ≤ y ≤ 0.46) и Na2ZnP2O7 (Na2 –yKyZnP2O7 при y = 0) (1), α-LiKZnP2O7 (2).
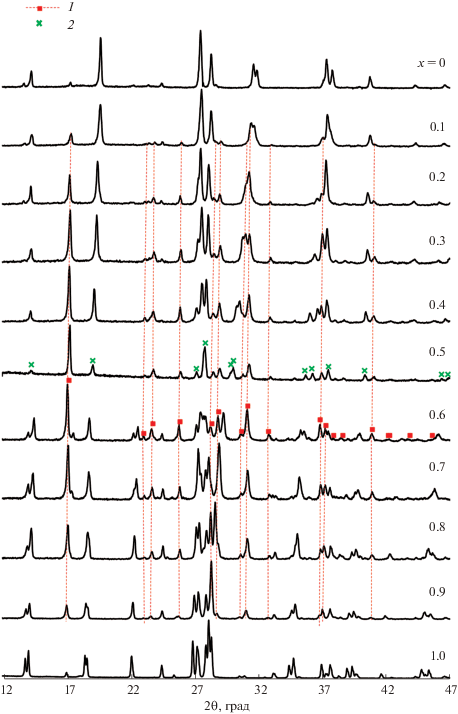
Рис. 3.
Дифрактограммы (1 – x)LiNaZnP2O7 : xK2ZnP2O7 (разрез 2) при комнатной температуре. Mss (LixNayK2 – (x+y)ZnP2O7 при 0 ≤ x ≤ 0.74, 0.26 ≤ y ≤ 1.0) (1); $T_{{ss}}^{'}$ (Na2 –yKyZnP2O7 при 0 ≤ y ≤ 0.46) и Na2ZnP2O7 (Na2 –yKyZnP2O7 при y = 0.0) (2); α-LiKZnP2O7 (3).
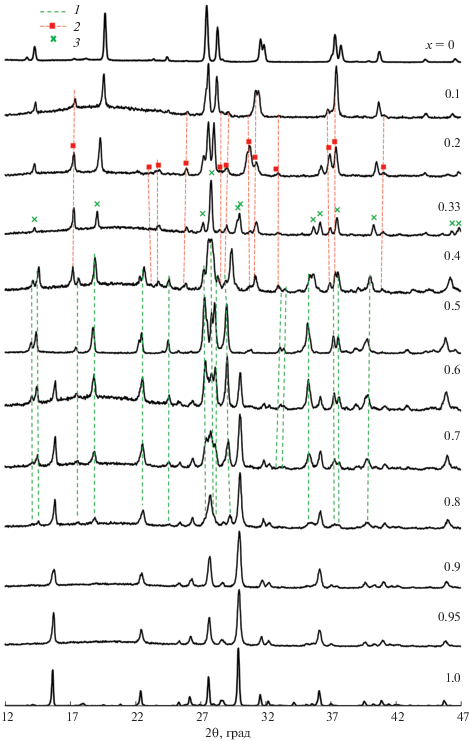
Таблица 1.
Фазовый состав в системах LiNaZnP2O7–NaKZnP2O7 и LiNaZnP2O7–K2ZnP2O7
| LiNaZnP2O7–NaKZnP2O7 | LiNaZnP2O7–K2ZnP2O7 | ||
|---|---|---|---|
| хNaKZnP2O7 | cостав | хK2ZnP2O7 | cостав |
| 0.1; 0.2; 0.3; 0.4 | Na2ZnP2O7 + Rss | 0.1; 0.2 | Na2ZnP2O7 + Rss |
| 0.5 | Na2ZnP2O7 + LiKZnP2O7 | 0.33 | Na2ZnP2O7 + LiKZnP2O7 |
| 0.6 | $T_{{{\text{ss}}}}^{'}$ + LiKZnP2O7 | 0.4 | $T_{{{\text{ss}}}}^{'}$ + Mss + LiKZnP2O7 |
| 0.7; 0.8; 0.9 | $T_{{{\text{ss}}}}^{'}$ + Mss | 0.5 | Mss |
| 0.6 | Mss + 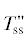 |
||
| 0.7; 0.8 | 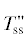 + LiKZnP2O7 + LiKZnP2O7 |
||
| 0.9; 0.95 | 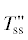 |
||
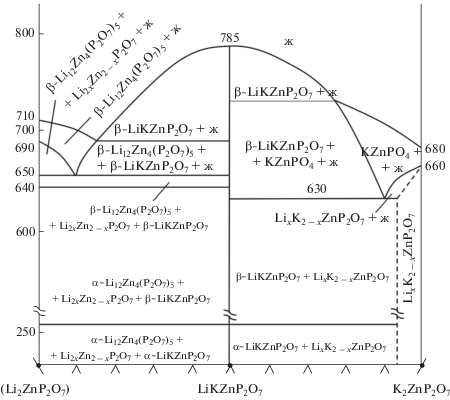
В системе LiNaZnP2O7–K2ZnP2O7 обнаружена область гомогенности на основе K2ZnP2O7 с содержанием LiNaZnP2O7 до 10 мол. % (рис. 2). Образование твердых растворов в указанной системе и в системе Na2ZnP2O7–K2ZnP2O7 [25] свидетельствует о возможности их существования и в системе Li2ZnP2O7–K2ZnP2O7 [28]. Для проверки существования подобных твердых растворов и в системе Li2ZnP2O7–K2ZnP2O7 были синтезированы образцы с содержанием Li2ZnP2O7 0.05, 0.075 и 0.1 мол. % (рис. 1) при температуре 550°С (11 ч). По данным РФА, у двух первых образцов все рефлексы отвечали структуре K2ZnP2O7, примесных фаз не обнаружено, в отличие от состава 0.1 мол. % Li2ZnP2O7. Оба образца затем были обожжены при температуре 635°С в течение 2 ч (выше температуры эвтектики (630°С) в данной системе). Дифракционная картина после обжига сохранилась, подплавление образцов не наблюдалось. Таким образом, в системе Li2ZnP2O7–K2ZnP2O7 установлено существование тетрагонального твердого раствора LixK2 –xZnP2O7 (0 $ \leqslant $ x $ \leqslant $ 0.17) на основе K2ZnP2O7 (рис. 4).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Обнаружение тетрагональных твердых растворов в системе Li2ZnP2O7–K2ZnP2O7 вносит коррективы в изученную нами ранее систему Li2ZnP2O7–K2ZnP2O7 [25]; уточненный вариант диаграммы приведен на рис. 4.
Таким образом, твердые растворы на основе K2ZnP2O7 установлены в трех системах: Na2ZnP2O7–K2ZnP2O7, Li2ZnP2O7–K2ZnP2O7 и LiNaZnP2O7–K2ZnP2O7, что дает основание выделить в плоскости концентрационного треугольника Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 область гомогенности с тетрагональной структурой (пр. гр. P42/mnm). В координатах тройной системы поле упомянутой тетрагональной фазы может быть записано как LixNayK2 – (x+y)ZnP2O7 (0 $ \leqslant $ x $ \leqslant $ $ \leqslant $ 0.17, 0 $ \leqslant $ y $ \leqslant $ 0.42).
В тройной системе Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 выделен также твердый раствор с моноклинной структурой (пр. гр. P21/n). Предпосылкой для его существования является наличие твердых растворов на основе NaKZnP2O7, которые реализуются в системах Na2ZnP2O7–K2ZnP2O7 и LiKZnP2O7–NaKZnP2O7. Положение моноклинного твердого раствора на фазовом треугольнике может быть записано формулой LixNayK2 – (x+y)ZnP2O7 (0 $ \leqslant $ x $ \leqslant $ 0.8, 0.2 $ \leqslant $ y $ \leqslant $ 1.0).
Как следует из данных табл. 1, изученные системы LiNaZnP2O7–NaKZnP2O7 и LiNaZnP2O7–K2ZnP2O7 не являются истинными, так как фазовые соотношения в них представлены фазами, не находящимися на соединительной прямой между исходными компонентами. Оба сечения проходят через несколько фазовых полей с одно-, двух- и трехфазными равновесиями. Однофазному равновесию соответствуют моноклинный твердый раствор на основе NaKZnP2O7 и тетрагональный на основе K2ZnP2O7.
На основании результатов рентгенофазового анализа разрезов LiNaZnP2O7–NaKZnP2O7 и LiNaZnP2O7–K2ZnP2O7 с учетом данных по фазовым равновесиям в ранее изученных вышеупомянутых системах [25–29] проведена триангуляция системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 в области, ограниченной соединениями Na2ZnP2O7, LiNaZnP2O7, LiKZnP2O7 и K2ZnP2O7. Эта область может быть разбита на 10 элементарных треугольников (рис. 5), где в равновесии находятся фазы, указанные в табл. 2.
Рис. 5.
Триангуляция системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7 в области, ограниченной соединениями Na2ZnP2O7, LiNaZnP2O7, LiKZnP2O7 и K2ZnP2O7; 1–10 – элементарные фазовые треугольники, 6 – моноклинный твердый раствор LixNayK2 – (x+y)ZnP2O7 (0 ≤ x ≤ 0.8, 0.2 ≤ y ≤ 1.0) – Mss; 10 – тетрагональный твердый раствор LixNayK2 – (x+y)ZnP2O7 (0 ≤ x ≤ 0.17, 0 ≤ y ≤ 0.42) – 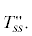
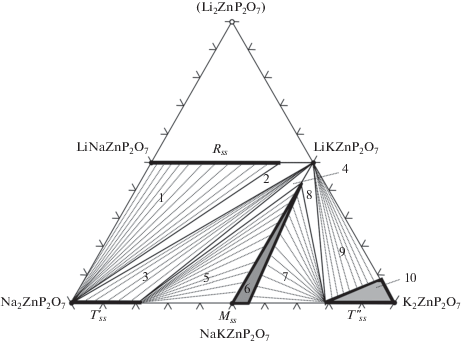
Таблица 2.
Фазовый состав в элементарных треугольниках системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7
| Номер элементарного треугольника | Состав | Номер элементарного треугольника | Состав |
|---|---|---|---|
| 1 | Rss + Na2ZnP2O7 | 6 | Mss |
| 2 | Rss + Na2ZnP2O7 + LiKZnP2O7 | 7 | Mss + 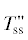 |
| 3 | $T_{{{\text{ss}}}}^{'}$ + LiKZnP2O7 | 8 | Mss + 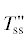 + LiKZnP2O7 + LiKZnP2O7 |
| 4 | $T_{{{\text{ss}}}}^{'}$ + LiKZnP2O7 + Mss | 9 | 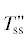 + LiKZnP2O7 + LiKZnP2O7 |
| 5 | $T_{{{\text{ss}}}}^{'}$ + Mss | 10 | 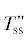 |
ЗАКЛЮЧЕНИЕ
Анализ совокупности данных, полученных в работах [25–29], а также в настоящей работе по изучению фазовых соотношений в частных разрезах тройной системы Li2ZnP2O7–Na2ZnP2O7–K2ZnP2O7, позволил провести разбиение указанной системы в области, ограниченной соединениями Na2ZnP2O7, LiNaZnP2O7, LiKZnP2O7 и K2ZnP2O7, на 10 элементарных треугольников с одно-, двух- и трехфазными равновесиями. В плоскости фазового треугольника данной системы установлено существование двух твердых растворов состава LixNayK2 – (x+y)ZnP2O7 (0 $ \leqslant $ x $ \leqslant $ 0.17, 0 $ \leqslant $ y $ \leqslant $ $ \leqslant $ 0.42) с тетрагональной (пр. гр. P42/mnm) и LixNayK2 – (x+y)ZnP2O7 (0 $ \leqslant $ x $ \leqslant $ 0.8, 0.2 $ \leqslant $ y $ \leqslant $ 1.0) с моноклинной (пр. гр. P21/n) структурой.
Список литературы
Kharroubi M., Assad H., Gacem L., Henn F. // Int. J. Emerging Technol. Adv. Engineer. 2014. V. 4. № 7. P. 49.
Сычева Г.А. // Физика и химия стекла. 2018. Т. 44. № 6. C. S27. https://doi.org/10.1134/S013266511807017X
Caldiño U., Lira A., Meza-Rocha A.N. et al. // J. Lumin. 2018. V. 194. P. 231. https://doi.org/10.1016/j.jlumin.2017.10.028
Soriano-Romero O., Lozada-Morales R., Meza-Rocha A.N. et al. // J. Lumin. 2020. V. 217. P. 116791. https://doi.org/10.1016/j.jlumin.2019.116791
Shwetha M., Eraiah B. // J. Non-Cryst. Solids. 2021. V. 555. P. 120622. https://doi.org/10.1016/j.jnoncrysol.2020.120622
Kundu H.K., Massand O.P., Marathe P.K., Venkataraman G. // Nucl. Instrum. Methods. 1980. V. 175. P. 363. https://doi.org/10.1016/0029-554X(80)90749-1
Quinn C.J., Beall G.H., Dickenson J.E. // Bull. Span. Soc. Ceram. Glasses. 1992. V. 4. P. 79.
Sunitha A.M., Gopalakrishna G.S., Byrappa K. // J. Int. Acad. Res. Multidisciplinary. 2016. V. 4. № 2. P. 329.
Kalai C., Kharroubi M., Gacem L. et al. // Glass. Phys. Chem. 2019. V. 45. P. 503. https://doi.org/10.1134/S1087659619060087
Voronin V.I., Sherstobitova E.A., Blatov V.A., Shekhtman G.Sh. // J. Solid State Chem. 2014. V. 211. P. 170. https://doi.org/10.1016/j.jssc.2013.12.015
Saha S., Rousse G., Fauth F. et al. // Inorg. Chem. 2019. V. 58. № 3. P. 1774. https://doi.org/10.1021/acs.inorgchem.8b01800
Kumar B.V., Vithal M. // Physica B. 2012. V. 407. № 12. P. 2094. https://doi.org/10.1016/j.physb.2012.02.013
Rim B., Lakhdar G., Bachir B. et al. // Luminescence. 2021. V. 36. № 2. P. 489. https://doi.org/10.1002/bio.3968
Bhake A.M., Parauha Y.R., Dhoble S.J. // J. Mater. Sci. –Mater. Electron. 2020. V. 31. P. 548. https://doi.org/10.1007/s10854-019-02559-4
Guerbous L., Gacem L. // Acta Phys. Pol., A. 2012. V. 122. № 3. P. 535. https://doi.org/10.12693/APhysPolA.122.535
Amara A., Gacem L., Gueddim A. et al. // Phys. B. 2018. V. 545. P. 408. https://doi.org/10.1016/j.physb.2018.07.008
Fhoula M., Dammak M. // J. Lumin. 2019. V. 210. P. 1. https://doi.org/10.1016/j.jlumin.2019.01.058
Gacem L., Artemenko A., Ouadjaout D. et al. // Solid State Sci. 2009. V. 11. P. 1854. https://doi.org/10.1016/j.solidstatesciences.2009.08.006
Belbal R., Gacem L., Bentria B. // Inorg. Chem. Commun. 2018. V. 97. P. 39. https://doi.org/10.1016/j.inoche.2018.09.007
Chen Z., Fang Y., Zhang W. et al. // Inorg. Chem. 2018. V. 57. № 17. P. 10568. https://doi.org/10.1021/acs.inorgchem.8b01140
Dong L., Ge X., Zhang P. et al. // Z. Anorg. Allg. Chem. 2019. V. 645. № 14. P. 944. https://doi.org/10.1002/zaac.201900045
Song H., Zhang S., Li Y. et al. // Solid State Sci. 2019. V. 95. 105940. https://doi.org/10.1016/j.solidstatesciences.2019.105940
Song Z., Yu H., Wu H. et al. // Inorg. Chem. Front. 2020. V. 7. № 18. P. 3482. https://doi.org/10.1039/D0QI00689K
Wang H., Geng L., Wang Y.-J. et al. // J. Alloys Compd. 2020. V. 820. Art. 153176. https://doi.org/10.1016/j.jallcom.2019.153176
Петрова М.А., Микиртичева Г.А., Гребенщиков Р.Г. // Неорган. материалы. 2007. Т. 43. № 9. С. 1141. [Petrova M.A., Mikirticheva G.A., Grebenshchikov R.G. // Inorg. Mater. 2007. V. 43. № 9. P. 1024. https://doi.org/10.1134/S0020168507090208]
Лапшин А.Е., Петрова М.А. // Физика и химия стекла. 2012. Т. 38. № 6. С. 718. [Lapshin A.E., Petrova M.A. // Glass Phys. Chem. 2012. V. 38. № 6. P. 491. https://doi.org/10.1134/S108765961206003X]
Петрова М.А., Волков С.Н., Бубнова Р.С. // Физика и химия стекла. 2014. Т. 40. № 4. С. 592. [Petrova M.A., Volkov S.N., Bubnova R.S. // Glass Phys. Chem. 2014. V. 40. № 4. P. 447. https://doi.org/10.1134/S1087659614040087]
Volkov S., Petrova M., Sinel’shchikova O. et al. // J. Solid State Chem. 2019. V. 269. P. 486. https://doi.org/10.1016/j.jssc.2018.10.029
Петрова М.А., Попова В.Ф. // Физика и химия стекла. 2017. Т. 43. № 4. С. 431. [Petrova M.A., Popova V.F. // Glass Phys. Chem. 2017. V. 43. № 4. P. 380. https://doi.org/10.1134/S1087659617040125]
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии