Микроэлектроника, 2020, T. 49, № 4, стр. 251-261
Параметры плазмы и кинетика активных частиц в смеси CHF3 + O2 + Ar
А. М. Ефремов a, *, Д. Б. Мурин a, K.-H. Kwon b
a Федеральное государственное бюджетное образовательное учреждение высшего образования
“Ивановский государственный химико-технологический университет”, кафедра технологии приборов и материалов электронной техники
г. Иваново, Шереметевский проспект, 7, Россия
b Korea University, Department of Control and Instrumentation Engineering
339-700 Sejong, South Korea
* E-mail: efremov@isuct.ru
Поступила в редакцию 01.11.2019
После доработки 01.11.2019
Принята к публикации 02.12.2019
Аннотация
Изучено влияние соотношения компонентов O2/Ar в смеси CHF3 + O2 + Ar на электрофизические параметры плазмы, кинетику активных и их стационарные концентрации в условиях индукционного ВЧ (13.56 МГц) разряда. При совместном использовании методов диагностики и моделирования плазмы: 1) выявлены особенности состава плазмы в бескислородной системе CHF3 + Ar; 2) установлены механизмы влияния кислорода на стационарные концентрации активных частиц через кинетику процессов при электронном ударе и реакции атомно-молекулярного взаимодействия; и 3) проведен модельный анализ кинетики гетерогенных процессов (травление, полимеризация, деструкция полимерной пленки), определяющих режим травления и его выходные характеристики.
1. ВВЕДЕНИЕ
Фторуглеродные газы вида CxHyFz активно используются в технологии интегральной микро- и наноэлектроники, электроники при проведении процессов реактивно-ионного травления кремния и его соединений [1–3]. Выходные характеристики процесса травления в плазме таких газов в значительной степени зависят от соотношения числа атомов фтора к числу атомов углерода в исходной молекуле, которое определяет соотношение концентраций F/CFx в газовой фазе и, как следствие, баланс скоростей процессов травления и поверхностной полимеризации. Широкое применение, в частности, получили плазмообразующие смеси на основе CF4, который в силу высокого значения F/C = 4 обеспечивает доминирование травления над полимеризацией [3, 4]. Это позволяет высокие скорости травления и чистоту обрабатываемой поверхности. Тем не менее, в работах [5–7] было показано, что трифторметан (CHF3) существенно превосходит CF4 по селективности травления в системе SiO2/Si. Это обуславливает высокий интерес к практическому использованию и, как следствие, к изучению физико-химических свойств плазменных систем на основе CHF3.
На протяжении последних лет было опубликовано несколько работ, посвященных исследованию электрофизических параметров и состава плазмы CHF3 [8–12]. По их результатам: 1) определены механизмы процессов, формирующих стационарный состав плазмы; 2) выявлены зависимости концентраций нейтральных и заряженных частиц от условий возбуждения разряда; и 3) скомпонованы кинетические схемы (наборы процессов и соответствующих констант скоростей), обеспечивающие адекватное описание кинетики плазмохимических реакций. К сожалению, все эти данные относятся либо к плазме чистого CHF3, либо к смесям CHF3 + Ar фиксированного или переменного состава. В то же время, хорошо известно, что добавка кислорода к фторуглеродному газу является эффективным инструментом регулирования кинетики травления и полимеризации за счет увеличения скорости генерации атомов фтора, связывания фторуглеродных радикалов в соединения вида CFxOy и травление пленки атомами кислорода [4]. Так, например, в работе [13] было показано, что варьирование соотношений различных компонентов в смеси CF4 + O2 + Ar позволяет получать комбинации параметров плазмы и концентраций активных частиц, не доступные в соответствующих бинарных смесях. Этот факт и определил направление исследований в данной работе.
Целью данной работы являлось исследование электрофизических параметров и состава плазмы индукционного ВЧ (13.56 МГц) разряда в смеси CHF3 + O2 + Ar. Основное внимание было направлено на 1) выявление механизмов влияния соотношения компонентов O2/Ar на кинетику и концентрации активных частиц; и 2) установление взаимосвязей между параметрами газовой фазы и гетерогенными характеристиками процесса травления.
2. МЕТОДИЧЕСКАЯ ЧАСТЬ
2.1. Оборудование и методики эксперимента
Эксперименты проводились при возбуждении индукционного ВЧ (13.56 МГц) разряда в смеси CHF3 + O2 + Ar в реакторе планарного типа сцилиндрической ($r$ = 13 см, $l$ = 16 см) рабочей камерой из анодированного алюминия [14]. В качестве неизменных параметров процесса выступали общее давление и расход плазмообразующего газа ($p$ = 10 мторр, $q$ = 40 станд. см3/мин), вкладываемая мощность ($W$ = 700 Вт) и мощность смещения (${{W}_{{dc}}}$ = 200 Вт). В качестве варьируемого параметра использовалось соотношение начальных концентраций Ar/O2, которое устанавливалось изменением индивидуальных расходов этих компонентов при постоянном ${{q}_{{{\text{CH}}{{{\text{F}}}_{{\text{3}}}}}}}$ = 20 станд. см3/мин. Таким образом, содержание CHF3 в смеси всегда составляло 50%, при этом изменение ${{q}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ = 0–40 станд. см3/мин (${{y}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ = ${{{{q}_{{{{{\text{O}}}_{{\text{2}}}}}}}} \mathord{\left/ {\vphantom {{{{q}_{{{{{\text{O}}}_{{\text{2}}}}}}}} q}} \right. \kern-0em} q}$ = 0–0.5, или 0–50%) соответствовало полному замещению аргона на кислород.
Диагностика плазмы осуществлялась двойным зондом Лангмюра DLP2000 (Plasmart Inc., Korea). Для минимизации погрешности измерений зондовых вольт-амперных характеристик (ВАХ) из-за полимеробразования на зондах применялась система импульсной очистки зондов ионной бомбардировкой. Предварительные эксперименты показали отсутствие значимых искажений ВАХ, последовательно измеряемых в системах 50% CHF3 + 50% Ar и 50% CHF3 + 50% O2 в течение ~5 мин после зажигания разряда. Обработка зондовых ВАХ базировалась на известных положениях теории двойного зонда [15–17] с использованием максвелловской функции распределения электронов по энергиям (ФРЭЭ). Результатом обработки выступали данные по температуре электронов (${{T}_{e}}$) и плотности ионного тока (${{J}_{ + }}$). Суммарная концентрация положительных ионов (${{n}_{ + }}$) определялась из соотношения ${{J}_{ + }}$ ≈ $0.61e{{n}_{ + }}{{\upsilon }_{B}}$ [16, 17], где ${{\upsilon }_{B}}$ ≈ $\sqrt {{{e{{T}_{e}}} \mathord{\left/ {\vphantom {{e{{T}_{e}}} {{{m}_{i}}}}} \right. \kern-0em} {{{m}_{i}}}}} $ – скорость ионов на внешней границе двойного электрического слоя у поверхности зонда без учета отрицательных ионов. Допустимость такого подхода показана в наших работах [18, 19]. Эффективная масса ионов $\left( {{{m}_{i}}} \right)$ оценивалась по соотношению ${{m}_{i}}$ = ${{\left( {\sum {{{{y}_{{X_{i}^{ + }}}}} \mathord{\left/ {\vphantom {{{{y}_{{X_{i}^{ + }}}}} {{{m}_{{X_{i}^{ + }}}}}}} \right. \kern-0em} {{{m}_{{X_{i}^{ + }}}}}}} \right)}^{{ - 1}}},$ где ${{y}_{{X_{i}^{ + }}}}$ и ${{m}_{{X_{i}^{ + }}}}$ – парциальные мольные доли и массы ионов. Для каждого типа положительного иона полагалось, что ${{y}_{{{{X}^{ + }}}}}$ ~ ${{{{k}_{{iz}}}{{y}_{X}}} \mathord{\left/ {\vphantom {{{{k}_{{iz}}}{{y}_{X}}} {\sqrt {{1 \mathord{\left/ {\vphantom {1 {{{m}_{{{{X}^{ + }}}}}}}} \right. \kern-0em} {{{m}_{{{{X}^{ + }}}}}}}} }}} \right. \kern-0em} {\sqrt {{1 \mathord{\left/ {\vphantom {1 {{{m}_{{{{X}^{ + }}}}}}}} \right. \kern-0em} {{{m}_{{{{X}^{ + }}}}}}}} }},$ где ${{k}_{{iz}}}$ и ${{y}_{X}}$ – константа скорости ионизации и мольная доля соответствующей нейтральной частицы.
Величина отрицательного смещения на нижнем электроде $ - {{U}_{{dc}}}$ при ${{W}_{{dc}}}$ = const измерялась высоковольтным зондом AMN-CTR (YoungsinEng, Korea). В предварительных экспериментах было установлено, что варьирование ${{W}_{{dc}}}$ в пределах 0–200 Вт не оказывает влияния на вид зондовых ВАХ и, следовательно, на параметры газовой фазы разряда.
2.2. Моделирование плазмы
Для получения данных по стационарному составу плазмы использовалась кинетическая 0‑мерная модель, оперирующая усредненными по объему реактора величинами [18, 19]. Кинетическая схема (набор реакций и соответствующих констант скоростей) для нейтральных частиц, представленная в табл. 1, была сформирована по результатам предшествующих исследований систем CHF3 + Ar [8, 11], O2 + Ar [20, 21] и CHF3 + O2 + Ar [22]. В последней работе было отмечено, что стационарные концентрации нейтральных частиц при комбинировании CHF3 и O2 в одной смесив значительной степени определяются процессами ступенчатой диссоциации вида CHFx + O → COFx + H и CFx + + O → COFx– 1 + F. На основании этого кинетическая схема была дополнена реакциями образования и гибели атомов O и O(1D) с участием метастабильных молекул O2(a1Δ) и O2(b1Σ). Алгоритм моделирования базировался на совместном решении уравнений химической кинетики нейтральных и заряженных частиц с учетом следующих допущений:
Таблица 1.
Реакции с участием нейтральных частиц в плазме смеси CHF3 + O2 + Ar
| Реакция | k, см3/с | Реакция | $k$, см3/с | ||
|---|---|---|---|---|---|
| 1. | CHF3 + e → F + CHF2 + e | $f\left( {{{T}_{e}}} \right)$ | 60. | CF2 + O(1D)→ CO + 2F | 3.98 × 10–12 |
| 2. | CHF3 + e → H + CF3 + e | $f\left( {{{T}_{e}}} \right)$ | 61. | CF + F → CF2 | 5.01 × 10–15 |
| 3. | CHF3 + e → HF + CF2 + e | $f\left( {{{T}_{e}}} \right)$ | 62. | CF + H → C + HF | 1.20 × 10–11 |
| 4. | CHF2 + e → CHF + F + e | $f\left( {{{T}_{e}}} \right)$ | 63. | CF + O → CO + F | 6.31 × 10–11 |
| 5. | CHF2 + e → H + CF2 + e | $f\left( {{{T}_{e}}} \right)$ | 64. | CF + O(1D) → CO + F | 2.00 × 10–11 |
| 6. | CHF + e → H + CF + e | $f\left( {{{T}_{e}}} \right)$ | 65. | CF + O2 → CFO + O | 3.16 × 10–11 |
| 7. | CF4 + e → CF3 + F + e | $f\left( {{{T}_{e}}} \right)$ | 66. | CH + HF → CF + H2 | 3.23 × 10–11 |
| 8. | CF4 + e → CF2 + 2F + e | $f\left( {{{T}_{e}}} \right)$ | 67. | CH + O → CO + H | 1.06 × 10–10 |
| 9. | CF4 + e → CF3+ + F + 2e | $f\left( {{{T}_{e}}} \right)$ | 68. | CH + F → C + HF | 1.02 × 10–12 |
| 10. | CF3 + e → CF2 + F + e | $f\left( {{{T}_{e}}} \right)$ | 69. | H2 + F → HF + H | 1.60 × 10–11 |
| 11. | CF2 + e → CF + F + e | $f\left( {{{T}_{e}}} \right)$ | 70. | FO + O → F + O2 | 2.51 × 10–11 |
| 12. | CF2 + e → C + 2F + e | $f\left( {{{T}_{e}}} \right)$ | 71. | FO + O(1D) → F + O2 | 5.01 × 10–11 |
| 13. | CF + e → C + F + e | $f\left( {{{T}_{e}}} \right)$ | 72. | FO + FO → 2F + O2 | 2.51 × 10–12 |
| 14. | HF + e → H + F + e | $f\left( {{{T}_{e}}} \right)$ | 73. | 2FO → F2 + O2 | 2.51 × 10–16 |
| 15. | F2 + e → 2F + e | $f\left( {{{T}_{e}}} \right)$ | 74. | CFO + CF3 → CF4 + CO | 1.00 × 10–11 |
| 16. | H2 + e → 2H + e | $f\left( {{{T}_{e}}} \right)$ | 75. | CFO + CF3 → CF2O + CF2 | 1.00 × 10–11 |
| 17. | CH + e → C + H + e | $f\left( {{{T}_{e}}} \right)$ | 76. | CFO + CF2 → CF3 + CO | 3.16 × 10–13 |
| 18. | O2 + e → 2O + e | $f\left( {{{T}_{e}}} \right)$ | 77. | CFO + CF2 → CF2O + CF | 3.16 × 10–13 |
| 19. | O2 + e → O + O(1D)+e | $f\left( {{{T}_{e}}} \right)$ | 78. | CFO + O → CO2 + F | 1.00 × 10–10 |
| 20. | O + e → O(1D) + e | $f\left( {{{T}_{e}}} \right)$ | 79. | CFO + O(1D) → CO2 + F | 1.00 × 10–10 |
| 21. | O2 + e → O2(a) + e | $f\left( {{{T}_{e}}} \right)$ | 80. | 2CFO → CF2O + CO | 1.00 × 10–11 |
| 22. | O2 + e → O2(b) + e | $f\left( {{{T}_{e}}} \right)$ | 81. | CFO + F → CF2O | 7.94 × 10–11 |
| 23. | O2(a) + e → O2 + e | $f\left( {{{T}_{e}}} \right)$ | 82. | CF2O + O(1D) → F2 + CO2 | 2.00 × 10–11 |
| 24. | O2(a) + e → 2O + e | $f\left( {{{T}_{e}}} \right)$ | 83. | C + O2 → CO + O | 1.58 × 10–11 |
| 25. | O2(a) + e → O + O(1D) + e | $f\left( {{{T}_{e}}} \right)$ | 84. | CO + F → CFO | 1.29 × 10–11 |
| 26. | O2(a) + e → O2(b) + e | $f\left( {{{T}_{e}}} \right)$ | 85. | F → Fads | $f\left( \gamma \right)$ |
| 27. | O2(b) + e → O2 + e | $f\left( {{{T}_{e}}} \right)$ | Fads + CHFx → CHFx + 1 | γ = 0.02 | |
| 28. | O2(b) + e → 2O+ e | $f\left( {{{T}_{e}}} \right)$ | Fads + CFx → CFx + 1 | ||
| 29. | O2(b) + e → O + O(1D) + e | $f\left( {{{T}_{e}}} \right)$ | Fads + F → F2 | ||
| 30. | CO2 + e → CO + O + e | $f\left( {{{T}_{e}}} \right)$ | Fads + C → CF | ||
| 31. | CO + e → C + O + e | $f\left( {{{T}_{e}}} \right)$ | Fads + O → FO | ||
| 32. | FO + e → F + O + e | $f\left( {{{T}_{e}}} \right)$ | Fads + H → HF | ||
| 33. | CFO + e → CO + F + e | $f\left( {{{T}_{e}}} \right)$ | 86. | H → Hads | $f\left( \gamma \right)$ |
| 34. | CF2O + e → CFO + F + e | $f\left( {{{T}_{e}}} \right)$ | Hads + CFx → CHFx | γ = 0.05 | |
| 35. | CHF3 + F → HF + CF3 | 1.58 × 10–13 | Hads + F → HF | ||
| 36. | CHF3 + H → H2 + CF3 | 1.60 × 10–19 | Hads + C → CH | ||
| 37. | CHF2 + F → HF + CF2 | 3.16 × 10–11 | Hads + H → H2 | ||
| 38. | CHF2 + H → HF + CHF | 3.22 × 10–10 | 87. | CF3 → CF3ads | $f\left( \gamma \right)$ |
| 39. | CHF2 + H → CF2 + H2 | 3.20 × 10–14 | CF3ads + F → CF4 | γ = 0.05 | |
| 40. | CHF2 + CF3 → CHF3 + CF2 | 1.58 × 10–12 | CF3ads + H → CHF3 | ||
| 41. | CHF2 + O → CF2O + H | 1.05 × 10–11 | 88. | CF2 → CF2ads | $f\left( \gamma \right)$ |
| 42. | CHF + F → HF + CF | 3.25 × 10–11 | CF2ads + F → CF3 | γ = 0.1 | |
| 43. | CHF + H → HF + CH | 3.10 × 10–10 | CF2ads + H → CHF2 | ||
| 44. | CHF + O → HF + CO | 3.25 × 10–11 | CF2ads + O → CF2O | ||
| 45. | F2 + CF3 → CF4 + F | 6.31 × 10–14 | 89. | CF → CFads | $f\left( \gamma \right)$ |
| 46. | F2 + CF2 → CF3 + F | 7.94 × 10–14 | CFads + F → CF2 | γ = 0.1 | |
| 47. | F2 + CF → CF2 + F | 3.98 × 10–12 | CFads + H → CHF | ||
| 48. | F2 + H → HF + F | 8.20 × 10–12 | CFads + O → CFO | ||
| 49. | F2 + O(1D) → FO + F | 7.94 × 10–12 | 90. | C → Cads | $f\left( \gamma \right)$ |
| 50. | F2 + CFO → CF2O + F | 5.01 × 10–14 | Cads + F → CF | γ = 1 | |
| 51. | CF3 + F → CF4 | 1.00 × 10–12 | Cads + H → CH | ||
| 52. | CF3 + H → CF2 + HF | 7.94 × 10–11 | Cads + O → CO | ||
| 53. | CF3 + O → CF2O + F | 3.16 × 10–11 | 91. | O → Oads | $f\left( \gamma \right)$ |
| 54. | CF3 + O(1D) → CF2O + F | 3.16 × 10–11 | Oads + O → O2 | γ = 0.1 | |
| 55. | CF2 + F → CF3 | 4.17 × 10–13 | Oads + F → FO | ||
| 56. | CF2 + H → HF + CF | 3.20 × 10–11 | Oads + C → CO | ||
| 57. | CF2 + O → CFO + F | 3.16 × 10–11 | Oads + CFx → CFxO | ||
| 58. | CF2 + O(1D) → CFO + F | 3.16 × 10–11 | 92. | O(1D) → O | $f\left( \gamma \right)$ |
| 59. | CF2 + O → CO + 2F | 3.98 × 10–12 | γ = 1 | ||
1) Энергетическое распределение электронов в условиях высоких степеней ионизации газа (${{{{n}_{ + }}} \mathord{\left/ {\vphantom {{{{n}_{ + }}} N}} \right. \kern-0em} N}$ ~ 10–4, где $N$ = ${p \mathord{\left/ {\vphantom {p {{{k}_{B}}{{T}_{{gas}}}}}} \right. \kern-0em} {{{k}_{B}}{{T}_{{gas}}}}}$ – общая концентрация частиц при температуре ${{T}_{{gas}}}$) формируется при существенном вкладе равновесныхэлектрон-электронных соударений. Таким образом, константы скоростей процессов R1–R34 могут быть найдены по соотношениям вида $k$ = $AT_{e}^{B}{\text{exp}}\left( {{{ - C} \mathord{\left/ {\vphantom {{ - C} {{{T}_{e}}}}} \right. \kern-0em} {{{T}_{e}}}}} \right)$ [8, 9, 20], полученным при интегрировании сечений соответствующих процессов с Максвелловской ФРЭЭ.
2) Варьирование начального состава смеси CHF3 + O2 + Ar в условиях $p,W$ = const не сопровождается существенными изменениями температуры газа. Это позволяет пренебречь влиянием соотношения Ar/O2 на константы скоростей объемных атомно-молекулярных процессов R35–R84. Значения последних брали из открытой базы данных [23] для ${{T}_{{gas}}}$ = 600 К.
3) Гетерогенная рекомбинация атомов и радикалов подчиняется механизму Или-Ридила. Соответственно, константы скоростей процессов R85–R92 могут быть определены как $k$ ≈ ${{\gamma {{\upsilon }_{T}}} \mathord{\left/ {\vphantom {{\gamma {{\upsilon }_{T}}} {2r}}} \right. \kern-0em} {2r}},$ где $r$ – радиус рабочей камеры реактора, ${{\upsilon }_{T}}$ = = ${{\left( {{{8{{k}_{B}}{{T}_{{gas}}}} \mathord{\left/ {\vphantom {{8{{k}_{B}}{{T}_{{gas}}}} {\pi m}}} \right. \kern-0em} {\pi m}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}$ и $\gamma $ вероятность рекомбинации [8, 9, 22].
Концентрация электронов оценивалась по измеренному значению ${{n}_{ + }}$ с использованием соотношения
полученного при совместном решении кинетического уравнения для отрицательных ионов и уравнения квазинейтральности плазмы [11]. Константы скоростей ион-ионной рекомбинации ${{k}_{{ii}}}$ принимались равными для всех типов положительных ионов [11, 13]. При расчете суммарной частоты диссоциативного прилипания ${{\nu }_{{da}}}$ = $N\sum y{{k}_{{da}}}$ (где $y$ – мольная доля частицы, характеризующейся константой скорости диссоциативного прилипания ${{k}_{{da}}}$) принимались во внимание HF, CHFx (x = = 1–3), CFx (x = 1–3), O2, CO2 и CF2O.
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Из данных рис. 1a можно видеть, что замещение Ar на O2 в смеси CHF3 + O2 + Ar при$~{{y}_{{{\text{CH}}{{{\text{F}}}_{{\text{3}}}}}}}$ = = const вызывает монотонное снижение средней энергии (температуры) электронов в диапазоне 4.8–3.0 эВ при 0–50% O2. Причиной данного эффекта является увеличение потерь энергии электронами в процессах низкопорогового (колебательного, электронного) возбуждения O2 и молекулярных продуктов плазмохимических реакций. Действительно, первый потенциал возбуждения атомов Ar составляет ∼11.6 эВ, в то время как кислород, например, характеризуется непрерывным спектром не упругого рассеяния электронов, начиная с ~0.2 эВ [24]. Последнее обеспечивается колебательным возбуждением молекул O2 (${{\varepsilon }_{{th}}}$ = = 0.16 эВ, где ${{\varepsilon }_{{th}}}$ – пороговая энергия возбуждения), а также образованием метастабильных электронно-возбужденных состояний O2(a1Δ) с ${{\varepsilon }_{{th}}}$ = 0.98 эВ и O2(b1Σ) с${{\varepsilon }_{{th}}}$ = 1.64 эВ [24]. Результаты диагностики плазмы показали также, что замещение аргона на кислород приводит к снижению суммарной концентрации положительных ионов (${{n}_{ + }}$ = 6.2 × 1010–3.0 × 1010 см–3 при 0–50% O2, см. рис. 1а) и плотности ионного тока (${{J}_{ + }}$ = = 1.94–0.86 мА/см2 при 0–50% O2, см. рис. 1б). Расчетное значение ${{n}_{e}}$ следует поведению ${{n}_{ + }}$ и изменяется в диапазоне 6.2 × 1010–2.5 × 1010 см–3 при 0–50% O2. Такое изменение концентраций заряженных частиц обусловлено уменьшением скоростей их генерации из-за снижения эффективной частоты ионизации ${{\nu }_{{iz}}}$ = $N\sum y{{k}_{{iz}}}$ (1.6 × 105–1.2 × × 104 с–1, или в ~1.3 раза при 0–50% O2) и скорости ионизации ${{\nu }_{{iz}}}{{n}_{e}}$ (9.6 × 1015–2.9 × 1014 см–3 с–1, или в ~3.3 раза при 0–50% O2). Причинами здесь являются 1) снижение констант скоростей ионизации нейтральных частиц, ${{k}_{{iz}}},$ из-за снижения ${{T}_{e}}$ (табл. 2); и 2) увеличение доли нейтральных частиц с низкими ${{k}_{{iz}}}$ (рис. 2 и табл. 2). Было найдено также, что замещение аргона на кислород сопровождается увеличением абсолютной (${{n}_{ - }}$ = 2.3 × × 108–5.2 × 109 при 0–50% O2) и относительной (${{{{n}_{ - }}} \mathord{\left/ {\vphantom {{{{n}_{ - }}} {{{n}_{e}}}}} \right. \kern-0em} {{{n}_{e}}}}$ = 0.04–0.21 при 0–50% O2) концентрации отрицательных ионов. Оба эффекта связаны с ростом суммарной частоты и скорости диссоциативного прилипания из-за увеличения концентраций электроотрицательных кислородсодержащих частиц. Отметим, что выполнение условия ${{{{n}_{ - }}} \mathord{\left/ {\vphantom {{{{n}_{ - }}} {{{n}_{e}}}}} \right. \kern-0em} {{{n}_{e}}}} \ll 1$ подтверждает применимость допущения $~{{n}_{e}}$ ≈ ${{n}_{ + }},$ использованного в работе [12] при моделировании плазмы в смеси CHF3 + Ar.
Рис. 1.
Экспериментальные (точки + сплошные линии) и расчетные (пунктир) параметры плазмы в смеси CHF3 + O2 + Ar: 1 – температура электронов; 2 – суммарная концентрация положительных ионов; 3 – концентрация электронов; 4 – плотность ионного тока; 5 – отрицательное смещение на нижнем электроде в условиях ${{W}_{{dc}}}$ = const.
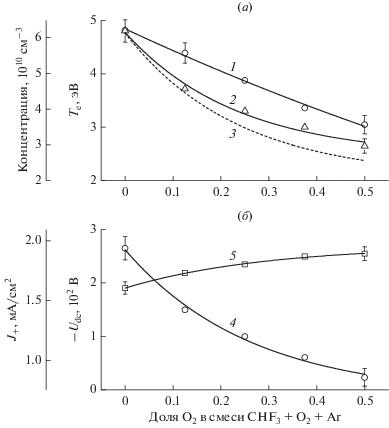
Таблица 2.
Константы скоростей ионизации (${{k}_{{iz}}},$ 10–10 см3/с) основных нейтральных частиц в плазме смеси CHF3 + O2 + Ar
| ${{y}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ | CHF3 | CF4 | CF3 | CF2 | F2 | HF | F | Ar | O2 | CF2O | CO2 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 0% | 5.64 | 13.4 | 21.8 | 20.1 | 1.84 | 3.96 | 4.18 | 25.2 | 10.4 | 6.30 | 16.9 |
| 50% | 0.51 | 1.15 | 5.0 | 4.70 | 0.15 | 0.46 | 0.58 | 2.66 | 1.82 | 1.45 | 2.39 |
Рис. 2.
Стационарные концентрации нейтральных компонентов газовой фазы в плазме смеси CHF3 + O2 + Ar.
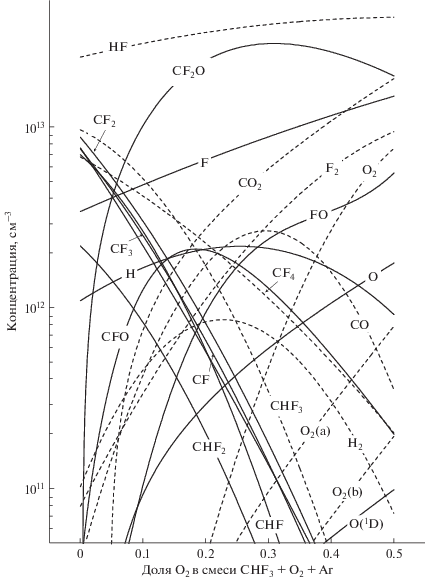
Расчеты показали, что основными компонентами газовой фазы в плазме 50% CHF3 + 50% Ar являются HF, CHFx (x = 1, 3) и СFx (x = 1–4) (рис. 2). Доминирование HF над другими типами частиц (что не противоречит экспериментальным данным [25, 26]) обеспечивается 1) прямым образование HF из исходных молекул CHF3 по R3; и 2) высокими скоростями объемных процессов CHFx + F → CFx + HF (R35, R37, R42), CHFx + + H → CHFx –1 + HF (R38, R43) и CFх + H → → CFх – 1+ HF (R52, R56). Отметим также, что эффективная генерация радикалов CFx (x = 1–3) по реакциям R35, R37 и R42 в сочетании с гетерогенными процессами вида CFx + F → CFх + 1 (R85, R88 и 89) обуславливает выполнение условия ${{n}_{{{\text{C}}{{{\text{F}}}_{x}}}}}$ > ${{n}_{{{\text{CH}}{{{\text{F}}}_{x}}}}}$ для суммарных концентраций этих частиц. Основными каналами образования атомов фтора являются процессы электронного удара с участием СFx (R9–R11) и HF (R14) при определяющей (~50% от общей скорости, в силу ${{n}_{{{\text{HF}}}}}$ > ${{n}_{{{\text{C}}{{{\text{F}}}_{x}}}}}$) роли R14 (рис. 3а). Пренебрежимо малый (менее 1% от общей скорости) вклад молекул CHF3 через R1 обусловлен низким значением константы скорости данного процесса (3.4 × 10–11 см3/с vs. 4.9 × 10–10 см3/с для R10 и 1.4 × 10–9 см3/с для R14) из-за высокой пороговой энергии (~13.0 эВ vs. ~3.8 эВ для R10 и ~5.9 эВ для R14). Характерной особенностью кинетики гибели атомов фтора в исследованном диапазоне условий является заметный (~25% от общей скорости) вклад объемных процессов R35, R37, R42 (рис. 3б). Последний эффект является основной причиной значительно более низких концентраций атомов фтора по сравнению с плазмой CF4 в аналогичном диапазоне условий [11].
Рис. 3.
Кинетика атомов фтора в плазме смеси CHF3 + O2 + Ar: а – скорости процессов образования атомов фтора и суммарная скорость образования; б – частоты процессов гибели атомов фтора и суммарная частота гибели. Цифры на кривых соответствуют номерам реакций в табл. 1. Пунктиром показаны гетерогенные процессы.
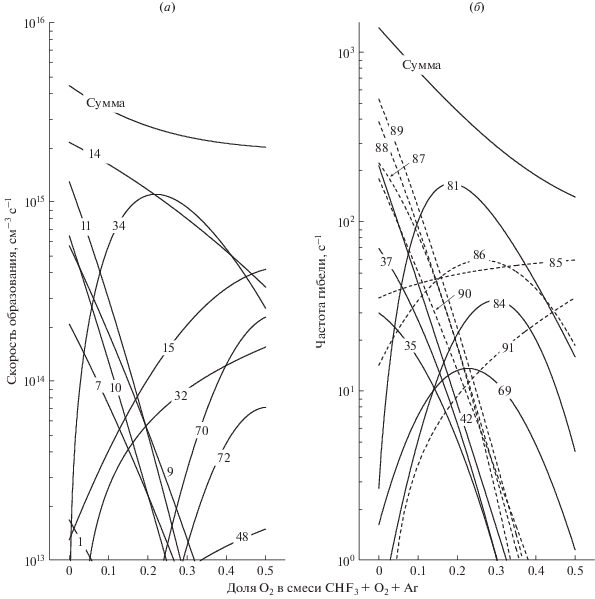
Замещение Ar на O2 в смеси CHF3 + O2 + Ar сопровождается существенными изменениями концентраций (рис. 2) и кинетики (рис. 3) нейтральных частиц, наиболее значимыми из которых являются снижение эффективности процессов при электронном ударе, резкое падение концентраций компонентов вида CFx и CHFx, а также увеличение концентрации атомов фтора. Резкое падение ${{n}_{{{\text{C}}{{{\text{F}}}_{3}}}}}$ (6.3 × 1012–7.0 × 109 см–3, или в ~900 раз при 0–50% O2) и ${{n}_{{{\text{C}}{{{\text{F}}}_{2}}}}}$ (7.3 × 1012–5.3 × 109 см–3, или в ~1400 раз при 0–50% O2) обусловлено сочетанием двух факторов, а именно: 1) ростом скоростей гибели этих частиц за счет процессов вида CFx + O → CFx– 1O + F (R53, R57) и CFx + O(1D) → → CFx – 1 O + F (R54, R58); и 2) снижением скоростей их образования по механизмам R35, R37 и R42 из-за аналогичного изменения концентраций CHFx. Причиной последнего эффекта также являются объемные процессы с участием атомов кислорода R41 и R44. Поэтому, принимая во внимание снижение частот диссоциирующих столкновений электронов (например, ${{k}_{{11}}}{{n}_{e}}$ = 148–17 с–1 при 0–50% O2), увеличение ${{y}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ эффективно подавляет образование атомов фтора по механизмам R9–R11 (рис. 3а). Отметим, что высокая скорость генерации молекул HF по R44 вызывает незначительный рост концентрации этих частиц (2.4 × 1013–4.0 × 1013 см–3, или в ~1.7 раз при 0–50% O2, см. рис. 2) и обуславливает более медленное снижение R14 сравнению с R9–R11. Тем не менее, суммарная скорость генерации атомов фтора в процессах R9–R11 и R14 монотонно снижается (4.2 × 1015–3.3 × 1014 см–3 с–1, или в ~13 раз при 0–50% O2), при этом величина снижения не компенсируется появлением дополнительных механизмов генерации атомов с участием молекул F2 (R15) и кислородсодержащих частиц (R32, R34, R70). Причиной резкого роста скорости R15 является аналогичное изменение ${{n}_{{{{{\text{F}}}_{{\text{2}}}}}}}$ (8.2 × 1010–9.3 × 1012 см–3, или в ~115 раз при 0–50% O2, см. рис. 2) обусловленное эффективным образованием этих молекул по R82 с участием CF2O. Поэтому скорости R15 и R34 в кислородсодержащей плазме фактически лимитируются скоростью образования CF2O в объемных (R81) и гетерогенных (R89, R90 и R91) процессах. Расчеты показали, что суммарная скорость образования и концентрация CF2O имеют максимальные значения в области 20–30% O2 из-за противоположного изменения концентраций обеспечивающих частиц – CFx и CHFx с одной стороны и O и O(1D) с другой. Аналогично, невысокая эффективность генерации атомов фтора по R32 и R70 является следствием лимитирования образования FO скоростями гетерогенных процессов R85 и R91. Последние, в свою очередь, ограничиваются низкими концентрациями атомов кислорода, которые активно гибнут в объеме плазмы при взаимодействии с CHFx (R41, R44) и CFx (R53, R57, R59). Таким образом, замещение Ar на O2 в условиях ${{y}_{{{\text{CH}}{{{\text{F}}}_{{\text{3}}}}}}}$ = const приводит к уменьшению суммарной скорости генерации атомов фтора (4.5 × 1015–2.0 × 1015 см–3 с–1, или в ∼2.3 раза при 0–50% O2, см. рис. 3а). В то же время, снижение концентраций CHFx и CFx обуславливает еще более резкое падение частот гибели атомов фтора в объемных (R35, R37, R42) и гетерогенных (R87–R90) процессах (рис. 3б). Данный эффект и является причиной роста концентрации атомов F, отмеченного на рис. 2. Аналогичным образом изменяется и плотность потока атомов на обрабатываемую поверхность ${{{\Gamma }}_{{\text{F}}}}$ (рис. 4).
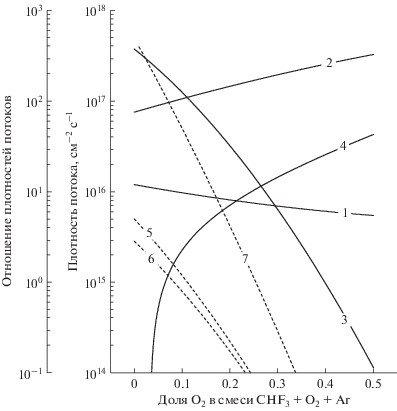
Рис. 4.
Плотности потоков (сплошные линии) и отношения плотностей потоков (пунктир) активных частиц в плазме смеси CHF3 + O2 + Ar: 1 – ${{{\Gamma }}_{ + }};$ 2 – ${{{\Gamma }}_{F}};$ 3 – ${{{\Gamma }}_{{pol}}} = {{{\Gamma }}_{{{\text{C}}{{{\text{F}}}_{{\text{2}}}}}}}$ + ${{{\Gamma }}_{{{\text{CF}}}}} + {{{\Gamma }}_{{{\text{CHF}}}}};$ 4 – ${{{\Gamma }}_{{\text{O}}}};$ 5 – ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{F}}}}}};$ 6 – ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}$ (×10–17); 7 – ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{F}}}}{{{\Gamma }}_{{\text{O}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{F}}}}{{{\Gamma }}_{{\text{O}}}}}}$ (×10–17).
Известно, что при проведении процессов травления в плазме галогенсодержащих газов, характер зависимости скорости травления от условий обработки определяется не только плотностью потока атомов галогенов, но зависит от ряда факторов, влияющих на эффективную вероятность взаимодействия атомов с обрабатываемой поверхностью [4]. Кроме температуры поверхности, во фторуглеродной плазме к таким и факторам относят процессы, затрудняющие доступ атомов фтора к поверхностным активным центрам: образование труднолетучих продуктов взаимодействия и маскирование поверхности фторуглеродной полимерной пленкой. Предшествующие исследования механизмов ионно-стимулированной химической реакции в полимеробразующей фторсодержащей плазме (например – [27–32]) могут быть обобщены в виде следующих положений:
1) Процессы взаимодействия ионов с поверхностью характеризуется скоростью ${{Y}_{S}}{{{\Gamma }}_{ + }}$ [31, 32], где ${{Y}_{S}}$ – выход процесса (атом/ион) и ${{{\Gamma }}_{ + }}$ – плотность потока ионов. В диапазоне ${{\varepsilon }_{i}}$ < 500 эВ можно полагать, что ${{Y}_{S}}$ ~ $\sqrt {{{m}_{i}}{{\varepsilon }_{i}}} $ или $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} $ [11–13], где ${{\varepsilon }_{i}}$ = $e\left| { - {{U}_{f}} - {{U}_{{dc}}}} \right|$ – энергия бомбардирующих ионов, $~ - {{U}_{f}}$ ≈ $0.5{{T}_{e}}{\text{ln}}\left( {{{{{m}_{e}}} \mathord{\left/ {\vphantom {{{{m}_{e}}} {2.3{{m}_{i}}}}} \right. \kern-0em} {2.3{{m}_{i}}}}} \right)$ – плавающий потенциал, $ - {{U}_{{dc}}}$ – отрицательное смещение на подложкодержателе при ${{W}_{{dc}}}$ = const, и ${{M}_{i}}$ эффективная молярная масса ионов, определяемая аналогично ${{m}_{i}}.$ Таким образом, изменение скорости любого ионного процесса при варьировании условий обработки отслеживается параметром $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{{ + ~}}}$ [12, 13].
2) Образование полимерной пленки обеспечивается CHxFy радикалами с $x + y$ ≤ 2, при этом вероятность полимеризации увеличивается при снижении концентрации атомов фтора [27, 28]. Поэтому изменение скорости связывания радикалов с поверхностью отслеживается отношением ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{F}}}}}},$ где ${{{\Gamma }}_{{pol}}}$ – суммарная плотность потока полимеробразующих радикалов. Деструкция полимерной пленки происходит за счет ионного распыления и травления атомами кислорода [4, 30]. Таким образом, относительное изменение толщины пленки ${{h}_{{pol}}}$ за счет действия физического и химического факторов характеризуется параметрами ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {\sqrt {{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {\sqrt {{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}$ и ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{O}}}}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{O}}}}{{{\Gamma }}_{{\text{F}}}}}}$ соответственно, где ${{{\Gamma }}_{{\text{O}}}}$ – плотность потока атомов кислорода.
3) Скорость взаимодействия атомов фтора с обрабатываемой поверхностью определяется соотношением ${{\gamma }_{R}}{{{\Gamma }}_{F}},$ где ${{\gamma }_{R}}$ – эффективная вероятность взаимодействия. При постоянной температуре поверхности можно полагать, что в области ${{h}_{{pol}}}$ < 2 нм справедливо соотношение ${{\gamma }_{R}}$ ~ ${1 \mathord{\left/ {\vphantom {1 {{{h}_{{pol}}}}}} \right. \kern-0em} {{{h}_{{pol}}}}}$ [27].
Расчеты показали, что замещение Ar на O2 в смеси CHF3 + O2 + Ar вызывает резкое снижение как плотности потока полимеробразующих радикалов ${{{\Gamma }}_{{pol}}} = {{{\Gamma }}_{{{\text{C}}{{{\text{F}}}_{{\text{2}}}}}}}$ + ${{{\Gamma }}_{{{\text{CF}}}}} + {{{\Gamma }}_{{{\text{CHF}}}}}$ (3.1 × 1017–1.5 × × 1014 см–2 с–1, или в ~2000 раз при 0–50% O2) из-за аналогичного изменения концентраций соответствующих частиц, так и параметра ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{F}}}}}}$ (4.1–0.0005, или в ~8000 раз при 0–50% O2) (рис. 4). Данный факт однозначно свидетельствует о снижении полимеризационной нагрузки газовой фазы на контактирующие с ней поверхности. Существенное падение плотности потока ионов с ростом ${{y}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ не компенсируется ростом их энергии ($ - {{U}_{{dc}}}$ = 190–254 В и ${{\varepsilon }_{i}}$ = 219–272 эВ при 0–50% O2, см. рис. 1б), что обуславливает монотонное снижение параметра $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}$ (1.8 × 1017–8.8 × × 1016 эВ1/2 см–2 с–1, или в ~2 раза при 0–50% O2). Тем не менее, формальное снижение эффективности деструкции полимерной пленки по физическому механизму не означает роста толщины пленки на обрабатываемой поверхности. Во-первых, снижение $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}$ (фактически – плотности потока энергииионов) с избытком компенсируется еще более резким падением полимеризационной активности газовой фазы. Соответственно, характер изменения отношения ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}$ (2.2 × 10–17–5.3 × 10–21 эВ–1/2 см2 с при 0–50% O2, см. рис. 4) однозначно свидетельствует о смещении баланса скоростей процессов осаждения и распыления полимерной пленки в направлении уменьшения ее толщины. И, во-вторых, рост плотности потока атомов кислорода обеспечивает увеличение скорости химической деструкции полимера, что также способствует снижению ${{h}_{{pol}}}.$ Это подтверждается соответствующим изменением параметра ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{O}}}}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{O}}}}{{{\Gamma }}_{{\text{F}}}}}}$ (рис. 4).
На основании выше сказанного можно с достаточной степенью уверенности полагать, что замещение Ar на O2 в смеси CHF3 + O2 + Ar сопровождается снижением ${{h}_{{pol}}}.$ Предположение о пропорциональном характере изменения величин ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}{{{\Gamma }}_{{\text{F}}}}}}$ и ${{{{{\Gamma }}_{{pol}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{pol}}}} {{{{\Gamma }}_{{\text{O}}}}{{{\Gamma }}_{{\text{F}}}}}}} \right. \kern-0em} {{{{\Gamma }}_{{\text{O}}}}{{{\Gamma }}_{{\text{F}}}}}}$ с одной стороны и толщины полимерной пленки с другой, позволяет говорить о снижении ${{h}_{{pol}}}$ до двух порядков величины при ${{y}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ ~ 20%. Очевидно, что такая ситуация способствует протеканию процесса травления в кинетическом режиме при отсутствии определяющего влияния ${{h}_{{pol}}}$ на эффективную вероятность взаимодействия атомов фтора. Фактически, это соответствует “классическому” режиму ионно-стимулированной химической реакции, в котором характер зависимости скорости травления от условий обработки формируется только изменениями ${{{\Gamma }}_{{\text{F}}}}$ и $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}.$ На наш взгляд, использование более богатых кислородом смесей может вызвать ухудшение выходных характеристик процесса травления из-за увеличения отношения ${{{{{\Gamma }}_{{\text{F}}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{\text{F}}}}} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}}}} \right. \kern-0em} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}}}$ (0.43–3.6 эВ–1/2 при 0–50% O2), отражающего вклады спонтанного и ионно-стимулированного химического взаимодействия в общую скорость процесса. Согласно многочисленным экспериментальным данным [2, 3], более высокие значения параметра ${{{{{\Gamma }}_{{\text{F}}}}} \mathord{\left/ {\vphantom {{{{{\Gamma }}_{{\text{F}}}}} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}}}} \right. \kern-0em} {\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{\Gamma }}_{ + }}}}$ отвечают низкой анизотропии травления и высокой шероховатости обработанных поверхностей.
4. ЗАКЛЮЧЕНИЕ
Проведено исследование электрофизических параметров плазмы, кинетики плазмохимических процессов и стационарного состава газовой фазы в системе CHF3 + O2 + Ar с переменным соотношением компонентов O2/Ar в условиях индукционного ВЧ (13.56 МГц) разряда. Показано, что в бескислородной системе CHF3 + Ar выполняется условие ${{n}_{{{\text{HF}}}}}$> ${{n}_{{{\text{C}}{{{\text{F}}}_{x}}}}}$ > ${{n}_{{{\text{CH}}{{{\text{F}}}_{x}}}}},$ которое обеспечивается эффективным протеканием процессов вида CHFx + F → CFx + HF, CHFx + H → → CHFx – 1 + HF и CFх + H → CFх –1 + HF. Установлено, что замещение аргона на кислород сопровождается резким снижением концентраций компонентов CHFx и CFх из-за их диссоциации при взаимодействии с атомами кислорода, а также ростом концентрации атомов фтора по причине снижения частоты гибели этих частиц в объемных процессах. При модельном анализе кинетики гетерогенных процессов подтверждено, что увеличение доли кислорода в плазмообразующей смеси приводит к снижению полимеризационной нагрузки газовой фазы на контактирующие с ней поверхности, а также вызывает резкое (до двух порядков величины при ~20% О2) уменьшение толщины фторуглеродной полимерный пленки.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта 19-07-00804А.
Список литературы
Wolf S., Tauber R.N. Silicon Processing for the VLSI Era. Volume 1. Process Technology. Lattice Press, New-York, 2000. 416 p.
Rooth J.R. Industrial Plasma Engineering. IOP Publishing LTD. Philadelphia. 2001. 658 p.
Roosmalen A.J., Baggerman J.A.G., Brader S.J.H. Dry etching for VLSI. Plenum Press, New-York, 1991. 490 p.
Lieberman M.A., Lichtenberg A.J. Principles of plasma discharges and materials processing. John Wiley & Sons Inc., New-York, 1994. 757 p.
Yeom G.Y., Kushner M.J. Si/SiO2 etch properties using CF4 and CHF3 in radio frequency cylindrical magnetron discharges // Appl. Phys. Lett. 1990. V. 56. P. 857–859.
Rossnagel S.M., Cuomo J.J., Westwood W.D. (Eds.). Handbook of plasma processing technology. Noyes Publications, ParkRidge, 1990. 338 p.
Cartry F.G., Peignon M.-C., Cardinaud Ch. Selective and deep plasma etching of SiO2: Comparison between different fluorocarbon gases (CF4, C2F6, CHF3) mixed with CH4 or H2 and influence of the residence time // J. Vac. Sci. Technol. B. 2002. V. 20. P. 1514–1521.
Ho P., Johannes J.E., Buss R.J. Modeling the plasma chemistry of C2F6 and CHF3 etching of silicon dioxide, with comparisons to etch rate and diagnostic data // J. Vac. Sci. Technol. A. 2001.V. 19. P. 2344–2367.
Bose D., Rao M.V.V.S., Govindan T.R., Meyyappan M. Uncertainty and sensitivity analysis of gas-phase chemistry in a CHF3 plasma // Plasma Sources Sci. Technol. 2003. V. 12. P. 225–234.
Proshina O., Rakhimova T.V., Zotovich A., Lopaev D.V., Zyryanov S.M., Rakhimov A.T. Multifold study of volume plasma chemistry in Ar/CF4 and Ar/CHF3 CCP discharges // Plasma Sources Sci. Technol. 2017. V. 26. P. 075005.
Ефремов А.М., Мурин Д.Б., Kwon K.-H. Параметры плазмы и кинетика активных частиц в смесях CF4 (CHF3) + Ar переменного начального состава // Микроэлектроника. 2018. Т. 47. № 6. С. 414–423.
Ефремов А.М., Мурин Д.Б., Kwon K.-H.Особенности кинетики объемных и гетерогенных процессов в плазме смесей CHF3 + Ar и C4F8 + Ar // Микроэлектроника. 2019. Т. 48. № 2. С. 125–133.
Efremov A., Lee J., Kim J. On the control of plasma parameters and active species kinetics in CF4 + O2 + Ar gas mixture by CF4/O2 and O2/Ar mixing ratios // Plasma Chem. PlasmaProcess. 2017. V. 37. P. 1445–1462.
Son J., Efremov A., Yun S.J., Yeom G.Y., Kwon K.-H. Etching characteristics and mechanism of SiNxfilms for Nano-Devices in CH2F2/O2/Ar inductively coupled plasma: Effect of O2 mixing ratio // J. Nanosci. Nanotech. 2014. V. 14. P. 9534–9540.
Johnson E.O., Malter L. A floating double probe method for measurements in gas discharges // Phys. Rev. 1950. V. 80. P. 58–70.
Shun’ko V. Langmuir probe in theory and practice. Universal Publishers. Boca Raton. 2008. 245 p.
Caneses J.F., Blackwell B. RF compensation of double Langmuir probes: modelling and experiment. Plasma Sources Sci. Technol. 2015. V. 24. P. 035024.
Kwon K.-H., Efremov A., Kim M., Min N.K., Jeong J., Kim K. A model-based analysis of plasma parameters and composition in HBr/X (X = Ar, He, N2) inductively coupled plasmas // J. Electrochem. Soc. 2010. V. 157. P. H574–H579.
Efremov A., Min N.K., Choi B.G., Baek K.H., Kwon K.-H. Model-based analysis of plasma parameters and active species kinetics in Cl2/X (X = Ar, He, N2) inductively coupled plasmas // J. Electrochem. Soc. 2008. V. 155. P. D777–D782.
Hsu C.C., Nierode M.A., Coburn J.W., Graves D.B. Comparison of model and experiment for Ar, Ar/O2 and Ar/O2/Cl2 inductively coupled plasmas // J. Phys. D. Appl. Phys. 2006. V. 39. № 15. P. 3272–3284.
Lee B.J., Efremov A., Yang J.W., Kwon K.-H. Etching characteristics and mechanisms of MoS2 2D Crystals in O2/Ar inductively coupled plasma // J. Nanosci. Nanotechnol. 2016. V. 16. № 11. P. 11201–11209.
Lim N., Efremov A., Yeom G.Y., Kwon K.-H. On the etching characteristics and mechanisms of HfO2 thin films in CF4/O2/Ar and CHF3/O2/Ar Plasma for Nano-Devices // J. Nanosci. Nanotechnol. 2014. V. 14. № 12. P. 9670–9679.
NIST Chemical Kinetics Database. https://kinetics. nist.gov/kinetics/welcome.jsp
Chistophorou L.G., Olthoff J.K. Fundamental electron interactions with plasma processing gases. Springer Science + Business Media. New York. 2004. 780 p.
Turban G., Grolleau B., Launay P., Briaud P. A mass spectrometric diagnostic of C2F6 and CHF3 plasmas during etching of SiO2 and Si // Revue Phys. Appl. 1985. V. 20. P. 609–620.
Takahashi K., Hori M., Goto T. Characteristics of fluorocarbon radicals and CHF3 molecule in CHF3 electron cyclotron resonance downstream plasma // Jpn. J. Appl. Phys. 1994. V. 33. P. 4745–4758.
Standaert T.E.F.M., Hedlund C., Joseph E.A., Oehrlein G.S. Role of fluorocarbon film formation in the etching of silicon, silicon dioxide, silicon nitride, and amorphous hydrogenated silicon carbide // J. Vac. Sci. Technol. A. 2004. V. 22. P. 53–60.
Stoffels W.W., Stoffels E., Tachibana K. Polymerization of fluorocarbons in reactive ion etching plasmas // J. Vac. Sci. Tech. A. 1998. V. 16. P. 87–95.
Kay E., Coburn J., Dilks A. Plasma chemistry of fluorocarbons as related to plasma etching and plasma polymerization. In: Veprek S., Venugopalan M. (eds) Plasma Chemistry III. Topics in Current Chemistry. V. 94. Springer, Berlin, Heidelberg. 1980.
Jansen M., Gardeniers H., de Boer M., Elwenspoek M., Fluitman J. A survey on the reactive ion etching of silicon in microtechnology // J. Micromech. Microeng. 1996. V. 6. P. 14–28.
Gray D.C., Tepermeister I., Sawin H.H. Phenomenological modeling of ion enhanced surface kinetics in fluorine-based plasma etching // J. Vac. Sci. Technol. B. 1993. V. 11. P. 1243–1257.
Lee C., Graves D.B., Lieberman M.A. Role of etch products in polysilicon etching in a high-density chlorine discharge // Plasma Chem. Plasma Proc. 1996. V. 16. P. 99–118.
Дополнительные материалы отсутствуют.
Инструменты
Микроэлектроника


