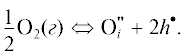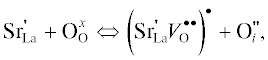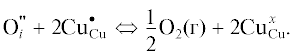Журнал неорганической химии, 2022, T. 67, № 6, стр. 678-685
Высокотемпературные свойства слоистых оксидов (La,Tb,Sr)2CuO4 ± δ со структурой T*-фазы
С. Я. Истомин a, *, А. В. Морозов a, Н. В. Лысков b, С. М. Казаков a, Е. В. Антипов a
a Московский государственный университет им. М.В. Ломоносова, Химический факультет
119991 Москва, Ленинские горы, 1, Россия
b Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, пр-т Академика Семенова, 1, Россия
* E-mail: isserge71@gmail.com
Поступила в редакцию 12.10.2021
После доработки 08.11.2021
Принята к публикации 15.11.2021
- EDN: JZZJZI
- DOI: 10.31857/S0044457X22060113
Аннотация
Впервые проведено исследование высокотемпературного термического расширения и электропроводности купратов La1.2 –хSrхTb0.8CuO4 ± δ (x = 0, 0.05) со структурой Т*-фазы для оценки возможности их использования в качестве катодного материала твердооксидного топливного элемента. Методом дилатометрии установлено, что коэффициент термического расширения (КТР) оксидов на воздухе в интервале температур 303–1123 K составляет 12.2 (х = 0) и 12.7 ppm K–1 (x = 0.05). Исследование высокотемпературной кристаллической структуры La1.2Tb0.8CuO4 ± δ выявило наличие анизотропии КТР вдоль кристаллографических осей (КТР(с)/КТР(а) = 1.35). Анализ данных высокотемпературной электропроводности соединений при различном парциальном давлении кислорода показал, что дырочные носители заряда являются доминирующими. Электропроводность при 973 K на воздухе составила 0.3–0.6 См/см. Вероятной причиной относительно невысоких величин проводимости может являться образование катионов Tb4+ в области высоких температур, которые выполняют роль ловушек для основных носителей заряда. Из результатов проведенного исследования можно сделать вывод, что La1.2 –хSrхTb0.8CuO4 ± δ могут найти лишь ограниченное применение в качестве катодного материала ТОТЭ, например, в виде тонкопленочных функциональных покрытий.
ВВЕДЕНИЕ
Сложные оксиды 3d-металлов с перовскитоподобной структурой привлекают повышенное внимание с целью практического использования в качестве электродных материалов различных высокотемпературных электрохимических устройств, в частности, твердооксидных топливных элементов (ТОТЭ) [1–5]. Среди оксидов, удовлетворяющих требованиям к катодным материалам среднетемпературных ТОТЭ, работающих в интервале 500–800°С, наибольший интерес вызывают перовскиты, содержащие 3d-металлы конца ряда (Fe, Co, Ni и Cu). Это связано с их высокой кислород-ионной проводимостью, которая способствует повышению производительности катода в области средних температур [3].
Слоистые купраты Ln2СuO4 с перовскитоподобной структурой относительно недавно стали исследоваться в качестве катодного материала среднетемпературных ТОТЭ [6–16]. Среди изученных соединений большой интерес представляет Pr2CuO4, имеющий простой химический состав и сочетающий низкую величину коэффициента термического расширения (КТР) (11.8 ppm K–1) c высокой общей электропроводностью (∼100 См/см при 1173 K) [6]. Этот оксид, однако, имеет относительно низкую величину кислород-ионной проводимости, что связано с присутствием в его кристаллической структуре (Т'-фаза) сжатого флюоритного блока Pr2O2 [6]. В то же время La2CuO4 со структурой K2NiF4 (Т-фаза), имеющий в своем составе блок со структурой каменной соли, обладает более высокой (на несколько порядков) кислород-ионной проводимостью, но демонстрирует низкую электропроводность (∼15 См/см при 1273 K), которая практически не зависит от температуры [17]. Среди купратов (A,A')2CuO4 – δ, содержащих в составе два различных по размеру А‑катиона, существуют фазы (T*-фаза), в кристаллической структуре которых содержатся одновременно блоки со структурой каменной соли и флюорита (рис. 1). Такие соединения известны, в частности, среди купратов Pr2 –xSrxCuO4 – δ (x = = 0.3, 0.4) [18]. Исследование высокотемпературных свойств этих оксидов показало, что они обладают приемлемой величиной электропроводности на воздухе (∼34 См/см при 993 K для состава Pr1.6Sr0.4CuO4 – δ), а также более высокой кислород-ионной проводимостью, чем Pr2CuO4, что связано с присутствием в их структуре блока каменной соли [19]. Следует отметить, что недостатком таких фаз в качестве катодного материала среднетемпературного ТОТЭ может стать присутствие в их составе катионов Sr2+. Их наличие может способствовать повышенной реакционной способности при контакте с электролитом ТОТЭ на основе кислотного оксида – Zr0.84Y0.16O1.92 (8YSZ). Среди купратов существуют также оксиды, кристаллизующиеся в структуре T*-фазы, при этом содержащие в качестве А-катиона исключительно катионы РЗЭ. К таким фазам относятся La2 –xTbxCuO4 (x = 0.6–0.8) и La2 –xDyxCuO4 (x = 0.8–0.9) [20].
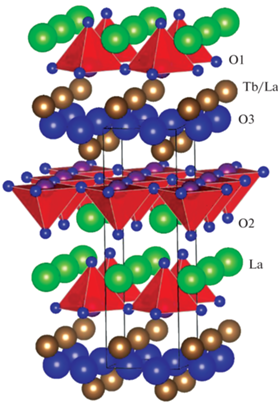
Рис. 1.
Кристаллическая структура Т*-фазы. Обозначения атомов даны для структуры La1.2Tb0.8CuO4 ± δ. Красные полиэдры – тетрагональная пирамида CuO5. Синим цветом обозначены атомы кислорода, зеленым – La, коричневым – Tb/La.
Цель настоящей работы – синтез купратов La1.2 –хSrхTb0.8CuO4 ± δ (x = 0 и 0.05) со структурой Т*-фазы и исследование их высокотемпературных физико-химических свойств, а именно термического расширения и электропроводности.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез образцов La1.2 –хSrхTb0.8CuO4 ± δ (x = 0 и 0.05) проводили цитратным методом в соответствии с методикой [20]. Для этого в расплав моногидрата лимонной кислоты C6H8O7 ⋅ H2O (50-кратный мольный избыток) добавляли водный раствор, полученный растворением стехиометрических количеств La2O3 (99.999%), CuO (99.999%) и Tb4O7 в горячей концентрированной азотной кислоте, а также Sr(NO3)2. Оксид лантана перед использованием прокаливали при температуре 1173 K на воздухе в течение 12 ч с целью разложения образовавшихся при длительном хранении на воздухе карбонатов. Полученную смесь упаривали в фарфоровой чашке на газовой горелке до образования густой карамелеобразной массы. Полученные прекурсоры обжигали при 923 K в течение 12 ч. Затем синтезированные порошки перетирали в агатовой ступке в среде ацетона, прессовали в таблетки и обжигали в трубчатой печи в токе кислорода при 1273 K в течение 48 ч, скорость нагрева составляла 1 град/мин. Далее таблетки повторно перетирали, перепрессовывали и повторяли процедуру обжига еще 3–4 раза.
Рентгенофазовый анализ поликристаллических образцов проводили при комнатной температуре в камере Гинье Huber G670 Guinier (CuKa1-излучение, λ = 1.5406 Å, детектор Image Plate) и на дифрактометре Bruker D8-Advance (CuKα-излучение, λ = 1.5418 Å). Фазовый анализ образцов осуществляли с использованием базы данных ICDD PDF-2. Для уточнения параметров элементарных ячеек использовали программный пакет STOE “WinXPOW”.
Высокотемпературную рентгенографию применяли для изучения температурной зависимости параметров элементарной ячейки La1.2Tb0.8CuO4 ± δ в интервале 298–1073 K. Рентгенограммы регистрировали на дифрактометре Bruker D8-Advance, оснащенном высокотемпературной камерой XRK Anton Paar (Германия). Кристаллические структуры полученных соединений были уточнены с использованием программного пакета TOPAS.
Термомеханические измерения и определение коэффициентов термического расширения проводили при помощи дилатометра NETZSCH DIL 402C. Для калибровки прибора использовали образцовую меру (эталонный материал, представляющий собой стержень из сапфира высотой 4.72 мм). Образцы представляли собой таблетки с плоскопараллельными гранями. Диаметр таблетки ≤6 мм, высота от 4.5 до 5.5 мм. Измерения проводили в статической воздушной атмосфере в температурном интервале 303–1123 K со скоростью нагрева 5 град/мин и под нагрузкой 20 сН. Полученные данные обрабатывали с помощью программного обеспечения Proteus Analysis.
Термогравиметрические эксперименты проводили при помощи термоанализатора Netzsch STA 449C в атмосфере искусственного воздуха (20% O2, 80% Ar) и Ar/H2 (8%) в температурном интервале от 298 до 1073 K со скоростью нагрева 10 град/мин.
Электропроводность керамических образцов измеряли четырехзондовым методом на постоянном токе с использованием потенциостата P-30S (ООО “Элинс”, Россия). Измерения проводили в режиме циклической развертки потенциала в интервале от –100 до +100 мВ со скоростью 20 мВ/с в интервале температур от 373 до 1173 K на воздухе и при варьировании парциального давления кислорода от 0.21 атм до 2 × 10–4 атм. Образцы для измерений представляли собой плотноспеченную керамику цилиндрической формы (диаметр 8 мм, высота ~12 мм). Потенциальные контакты формировали на боковой поверхности образца с помощью платиновой пасты. Организацию токовых контактов осуществляли нанесением платиновой пасты на торцевые поверхности цилиндра. После этого образец сушили при 373 K в течение 1 ч и затем отжигали при 1173 K в течение 5 ч для полного удаления органических составляющих пасты. Температуру контролировали с помощью Pt–Pt/Rh-термопары, расположенной вблизи образца. Парциальное давление кислорода определяли потенциометрическим датчиком кислорода на основе стабилизированного ZrO2.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Дифрактограммы La1.2 –хSrхTb0.8CuO4 ± δ (x = 0 и 0.05) проиндицированы в тетрагональной сингонии в пр. гр. P4/nmm с параметрами элементарных ячеек a = 3.862(3), c = 12.426(1) Å для La1.2Tb0.8CuO4 ± δ и a = 3.866(2), c = 12.466(3) Å для La1.15Sr0.05Tb0.8CuO4 ± δ. Из литературы известно, что в структуре T*-фазы могут присутствовать как кислородные вакансии, так и сверхстехиометрический кислород, локализованный в тетраэдрических междоузлиях блока со структурой каменной соли [20]. В настоящей работе точное содержание кислорода в полученных купратах не определяли, однако, учитывая, что при их синтезе была воспроизведена методика [15], можно высказать предположение, что их кислородный состав также близок к стехиометрическому: La1.2Tb0.8CuO4.05(3) и La1.15Sr0.05Tb0.8CuO4.01(4).
Высокотемпературное термическое расширение
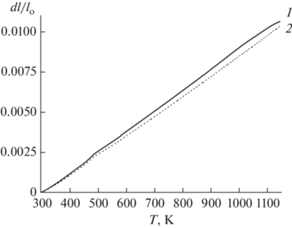
На рис. 2 приведены температурные зависимости относительного удлинения образцов La1.2 –хSrхTb0.8CuO4 ± δ (x = 0 и 0.05). Для обоих составов наблюдается практически линейное термическое расширение в исследуемом температурном интервале. Полученные величины линейных КТР близки и составляют 12.2 ppm K–1 для La1.2Tb0.8CuO4 ± δ и 12.7 ppm K–1 для La1.15Sr0.05Tb0.8CuO4 ± δ. Они сопоставимы с КТР стандартных электролитов ТОТЭ на основе стабилизированного диоксида циркония 8YSZ (10.8 ppm K–1 [21]) и допированного оксида церия Ce0.8Gd0.2O1.9 (20GDC, 12.8 ppm K–1 [22]). Необходимо отметить, что на дилатометрических кривых отсутствует ярко выраженный эффект химического расширения, который проявляется в виде роста КТР с температурой и связан преимущественно с потерей оксидом части кислорода. Такое поведение демонстрируют, например, купраты Pr2 –xSrxCuO4 – δ (x = 0.3, 0.4) со структурой T*-фазы [21]. Отсутствие яркого эффекта химического расширения в случае купратов La1.2 –хSrхTb0.8CuO4 ± δ (x = 0, 0.05), по всей видимости, связано с тем, что степень окисления катионов Cu в них близка к +2, что существенно затрудняет потерю ими кислорода с ростом температуры.
Рис. 2.
Температурные зависимости относительного расширения образцов La1.15Sr0.05Tb0.8CuO4 ± δ (1) и La1.2Tb0.8CuO4 ± δ (2) на воздухе.
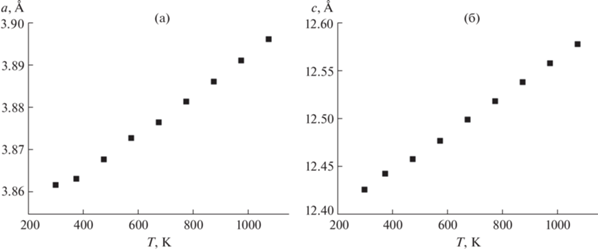
Кристаллическую структуру La1.2Tb0.8CuO4 ± δ при различной температуре уточняли методом Ритвельда по данным высокотемпературной порошковой рентгеновской дифракции, полученным на воздухе в интервале температур 298–1173 K. В качестве исходных атомных координат использовали данные [20]. На рис. 3 приведены температурные зависимости параметров a и с элементарной ячейки La1.2Tb0.8CuO4 ± δ. Расчетные величины КТР вдоль кристаллографических направлений а и с составляют 11.7 и 15.8 ppm K–1 соответственно. Таким образом, фаза демонстрирует анизотропию КТР c коэффициентом КТР(с)/КТР(а) = = 1.35. Линейный КТР, вычисленный из температурной зависимости объема элементарной ячейки в виде V1/3, равен 13.0 ppm K–1 и близок к величине КТР, полученной из данных дилатометрии (12.2 ppm K–1).
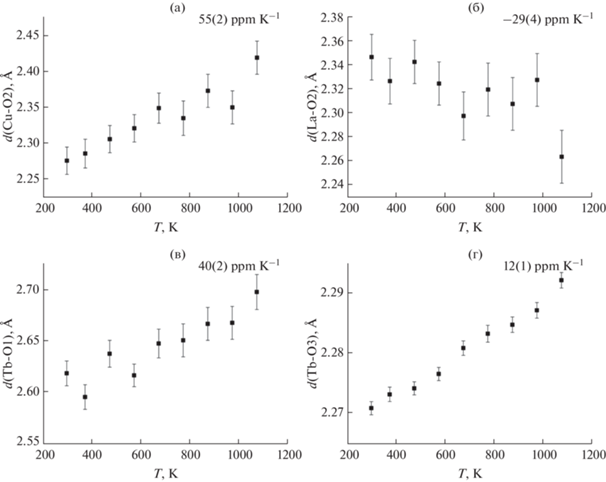
Помимо расчета величин КТР также были проанализированы температурные зависимости основных межатомных расстояний в структуре La1.2Tb0.8CuO4 ± δ (рис. 4). Учитывая высокие погрешности в определении положения атомов кислорода по рентгенографическим данным, имеет смысл обсудить лишь тенденции в изменении расстояний между катионами и ионами кислорода в кристаллической структуре La1.2Tb0.8CuO4 ± δ. С увеличением температуры наибольшее расширение демонстрирует связь Cu–O2 (55(2) ppm K–1), отвечающая расстоянию между катионом меди и аксиальным атомом кислорода в пирамиде CuO5, а также связь Tb–O1 (40(2) ppm K–1), соответствующая расстоянию между катионом Tb, принадлежащим флюоритному блоку, и атомом кислорода O1 из расположенного над ним слоя CuO2 (рис. 1). Интересно отметить, что очень быстрое увеличение длины связи Cu–O2 приводит к тому, что связь между катионом La, принадлежащим блоку со структурой каменной соли, и этим же атомом кислорода O2, наоборот, быстро сокращается с ростом температуры (КТР(La–O2) = = –29.4 ppm K–1). Подобное поведение часто демонстрируют и другие оксиды со структурой Т-фазы, например, Pr1.25Sr0.75Cu0.25Co0.75O4 – δ [23]. Следует также отметить быстрый рост длины связи Tb–O1 (рис. 4в) с температурой. Из литературы известно, что в купратах со структурой T'-фазы внутри флюоритного блока R2O2 присутствуют короткие связи R–O, что приводит к их слабому удлинению с ростом температуры. В то же время длинные связи между катионом R и атомами кислорода, принадлежащими слою CuO2, демонстрируют более сильное удлинение с ростом температуры. Так, в Sm2CuO4 указанные связи на ∼50% длиннее связей внутри флюоритного блока [6]. Для изученного в настоящей работе купрата La1.2Tb0.8CuO4 ± δ они отличаются в 3.7 раза (рис. 4в и 4г). Вероятной причиной этого может быть наличие переменной степени окисления у катионов Tb, что может сказываться на природе химической связи Tb–O.
Рис. 4.
Температурные зависимости основных межатомных расстояний в кристаллической структуре La1.2Tb0.8CuO4 ± δ. Обозначения атомов соответствуют рис. 1.
Высокотемпературная электропроводность
Температурные зависимости электропроводности для La1.2 –хSrхTb0.8CuO4 ± δ (x = 0, 0.05) на воздухе представлены на рис. 5. Они подчиняются модифицированному уравнению Аррениуса для термоактивационного поведения с учетом того, что носителями заряда в исследуемых соединениях являются поляроны малого радиуса:
где T – абсолютная температура; k – константа Больцмана; А – предэкспоненциальный множитель; Ea – энергия активации.Рис. 5.
Температурные зависимости электропроводности La1.2 –хSrхTb0.8CuO4 ± δ (х = 0 (1) и 0.05 (2)) на воздухе.
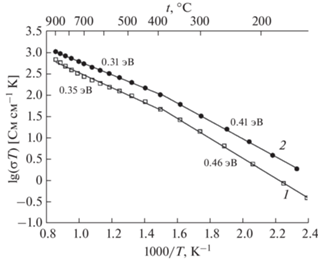
Электропроводность обоих соединений демонстрирует полупроводниковое поведение во всем исследованном интервале температур при парциальном давлении кислорода. При температуре ~673 K наблюдается уменьшение наклона зависимостей электропроводности, сопровождаемое снижением величины энергии активации (Еа) от 0.46 до 0.35 эВ и от 0.41 до 0.31 эВ для La1.2Tb0.8CuO4 ± δ и La1.15Sr0.05Tb0.8CuO4 ± δ соответственно. Немного более высокая электропроводность Sr-содержащего состава (при 973 K 0.28 См/см для La1.2Tb0.8CuO4±δ и 0.56 См/см для La1.15Sr0.05Tb0.8CuO4 ± δ) обусловлена, по-видимому, гетеровалентным замещением катионов La3+ на Sr2+, что способствует увеличению концентрации дырочных носителей заряда (${{h}^{ \bullet }}$) согласно следующим квазихимическим уравнениям:
(2)
$\begin{gathered} 2{\text{SrO}} + {\text{CuO}}\xrightarrow{{{\text{L}}{{{\text{a}}}_{{\text{2}}}}{\text{Cu}}{{{\text{O}}}_{{\text{4}}}}}} \\ \to \,\,2{\text{Sr}}_{{{\text{La}}}}^{'} + {\text{Cu}}_{{{\text{Cu}}}}^{x} + 3O_{{\text{O}}}^{x} + V_{{\text{O}}}^{{ \bullet \bullet }}, \\ \end{gathered} $(3)
$V_{{\text{O}}}^{{ \bullet \bullet }} + \frac{1}{2}{{O}_{2}}({\text{г}}) \to O_{{\text{O}}}^{x} + 2{{h}^{ \bullet }},$С целью изучения природы носителей заряда в купратах La1.2 –хSrхTb0.8CuO4 ± δ нами исследована температурная зависимость электропроводности при различном парциальном давлении кислорода (рис. 6). Следует отметить, что с повышением парциального давления кислорода наблюдается небольшой рост электропроводности изученных образцов. Это также указывает на то, что основными носителями заряда в исследованных соединениях являются дырки, локализованные на ионах меди (${\text{Cu}}_{{{\text{Cu}}}}^{ \bullet }$):
(4)
$2{\text{Cu}}_{{{\text{Cu}}}}^{x} + V_{{\text{O}}}^{{ \bullet \bullet }} + \frac{1}{2}{{{\text{O}}}_{2}}({\text{г}}) \to 2{\text{Cu}}_{{{\text{Cu}}}}^{ \bullet } + {\text{O}}_{{\text{O}}}^{x}.$Рис. 6.
Температурные зависимости электропроводности La1.2 –хSrхTb0.8CuO4 ± δ, где х = 0 (а) и 0.05 (б), при различном парциальном давлении кислорода.
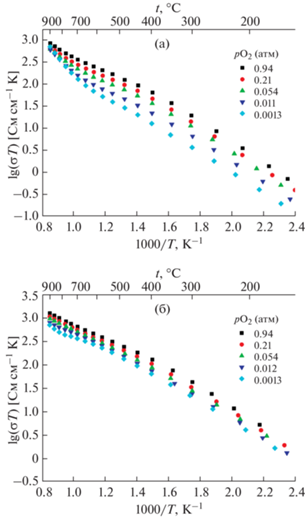
Наличие кислородных вакансий в этих соединениях может быть обусловлено процессами потери кислорода как с ростом температуры, так и вследствие понижения парциального давления кислорода в газовой фазе. Кроме того, в случае Sr-содержащего состава образование кислородных вакансий также обусловлено гетеровалентным замещением катионов лантана на стронций (уравнение (2)).
Следует отметить, что для La1.2Tb0.8CuO4 ± δ до 973 K температурные зависимости электропроводности при варьировании парциального давления кислорода ведут себя одинаково. Однако при дальнейшем повышении температуры электропроводность становится практически независимой от рО2. Для La1.15Sr0.05Tb0.8CuO4 ± δ можно отметить симбатное поведение температурных зависимостей электропроводности при изменении парциального давления кислорода.
Для детального анализа изменения электропроводности от рО2 и установления механизма взаимодействия кислорода из газовой фазы с твердым телом были построены изотермы проводимости в билогарифмических координатах (рис. 7). Полученные зависимости lgσ–lg(${{p}_{{{{{\text{O}}}_{{\text{2}}}}}}}$) имеют линейный вид. В случае La1.2Tb0.8CuO4 ± δ (рис. 7a) тангенс угла наклона в температурном интервале 373–873 K составляет ~1/4. Такое поведение $\left( {\sigma \infty p_{{{{{\text{O}}}_{{\text{2}}}}}}^{{\frac{1}{4}}}} \right)$ может отвечать процессу внедрения кислорода в вакантные кислородные позиции в кислородной подрешетке, описываемому уравнением (3) [24].
Рис. 7.
Зависимости электропроводности La1.2 ‒ хSrхTb0.8CuO4 ± δ, где х = 0 (а) и 0.05 (б), от парциального давления кислорода при различной температуре: 1 – 1173, 2 – 1093, 3 – 1013, 4 – 933, 5 – 843, 6 – 753, 7 – 673 K (цифрами указан тангенс угла наклона соответствующих прямых).
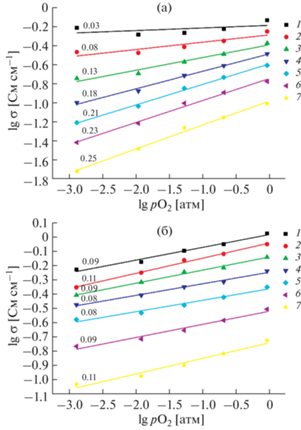
Повышение температуры от 873 до ~1023 K приводит к уменьшению тангенса угла наклона изотерм проводимости до ~1/6, в результате чего внедрение кислорода из газовой фазы в кристаллическую решетку может осуществляться за счет образования междоузельного кислорода [25]:
Дальнейшее повышение температуры до 1173 K приводит к нивелированию зависимости проводимости от рО2. Возможной причиной такого поведения может быть частичный переход катионов Tb из степени окисления +3 (${\text{Tb}}_{{{\text{Tb}}}}^{x}$) в степень окисления +4 (${\text{Tb}}_{{{\text{Tb}}}}^{ \bullet }$):
(6)
${\text{Tb}}_{{{\text{Tb}}}}^{x} \Leftrightarrow {\text{Tb}}_{{{\text{Tb}}}}^{ \bullet } + e{\kern 1pt} '.$В результате термической активации дырки, локализованные на атомах меди, могут выступать в качестве ловушек для образующихся свободных электронов (e'):
(7)
${\text{Cu}}_{{{\text{Cu}}}}^{ \bullet } + e{\kern 1pt} ' \Leftrightarrow {\text{Cu}}_{{{\text{Cu}}}}^{x},$Поведение электропроводности соединения La1.15Sr0.05Tb0.8CuO4 ± δ в зависимости от рО2 (рис. 7б) отличается от описанного выше поведения купрата La1.2Tb0.8CuO4 ± δ. Наклон изотерм проводимости от рО2 практически не изменяется при варьировании температуры. Тангенс угла наклона составляет 0.10 ± 0.02, что соответствует, по-видимому, доминированию процесса внедрения кислорода из газовой фазы в кристаллическую решетку с образованием междоузельного кислорода (уравнение (5), $\sigma \infty p_{{{{{\text{O}}}_{{\text{2}}}}}}^{{\frac{1}{6}}}$). Вместе с тем присутствие катионов Sr2+ может вызывать процесс ассоциации кислородных вакансий, приводящий к дополнительной генерации междоузельного кислорода [10]:
наличие которого может несколько снижать концентрацию дырочных носителей заряда вследствие процесса перехода его в газовую фазу:По всей видимости, возможность протекания данных процессов и обусловливает явно выраженное отсутствие изменения наклона изотерм проводимости от рО2 при варьировании температуры. На реализацию подобного механизма указывают структурные данные работы [20], полученные при помощи низкотемпературной нейтронографии. Из них следует, что частичное замещение катионов Tb на Sr приводит к образованию кислородных вакансий в аксиальной позиции пирамиды CuO5 (кислород О2, рис. 1) и одновременному увеличению содержания междоузельного кислорода в блоке NaCl.
ЗАКЛЮЧЕНИЕ
Исследование высокотемпературного термического расширения слоистых купратов La1.2 –хSrхTb0.8CuO4 ± δ (х = 0, 0.05) со структурой T*-фазы выявило, что они имеют линейные КТР (12.2 и 12.7 ppm K–1 для x = 0.0 и 0.05 соответственно), сопоставимые с КТР стандартных электролитов ТОТЭ на основе флюоритоподобных оксидов 8YSZ и 20GDC. Полученные значения КТР значительно ниже, чем для купратов Pr2 –xSrxCuO4 – δ с аналогичной кристаллической структурой (например, для x = 0.4 КТР составляет 14.9 ppm K–1 при 423–773 K и 17.3 ppm K–1 при 773–1273 K [19]).
Исследование высокотемпературных электропроводящих свойств показало, что основными носителями заряда в изученных сложных оксидах являются дырки, локализованные на ионах меди. Данные соединения имеют более низкие величины электропроводности (0.3–0.6 См/см при 973 K), чем исследованные ранее оксиды Pr2 –xSrxCuO4 – δ со структурой T*-фазы (34 См/см при 993 K для Pr1.6Sr0.4CuO4 – δ [19]). Вероятная причина такой аномально низкой электропроводности – образование катионов Tb4+ c ростом температуры, которые выполняют роль ловушек для основных носителей заряда. Таким образом, вследствие низкой проводимости оксидные фазы La1.2 –хSrхTb0.8CuO4 ± δ (х = 0, 0.05) могут найти лишь крайне ограниченное применение в качестве катодного материала среднетемпературного ТОТЭ, например, в виде очень тонких пленок.
Список литературы
Aguadero A., Fawcett L., Taub S. et al. // J. Mater. Sci. 2012. V. 47. P. 3925. https://doi.org/10.1007/s10853-011-6213-1
Jacobson A.J. // Chem. Mater. 2010. V. 22. P. 660. https://doi.org/10.1021/cm902640j
Istomin S.Ya., Antipov E.V. // Russ. Chem. Rev. 2013. V. 82. P. 686. https://doi.org/10.1070/RC2013v082n07ABEH004390
Istomin S.Ya., Lyskov N.V., Mazo G.N. et al. // Russ. Chem. Rev. 2021. V. 90. № 6. P. 644. https://doi.org/10.1070/RCR4979
Tarutin A.P., Lyagaeva J.G., Medvedev D.A. et al. // J. Mater. Chem. A. 2021. V. 9. P. 154 https://doi.org/10.1039/D0TA08132A
Kaluzhskikh M.S., Kazakov S.M., Mazo G.N. et al. // J. Solid State Chem. 2011. V. 184. P. 698. https://doi.org/10.1016/j.jssc.2011.01.035
Lyskov N.V., Kaluzhskikh M.S., Leonova L.S. et al. // Int. J. Hydrogen Energy. 2012. V. 37. P. 18357. https://doi.org/10.1016/j.ijhydene.2012.09.099
Zheng K., Gorzkowska-Sobas A., Swierczek K. // Mater. Res. Bull. 2012. V. 47. P. 4089. https://doi.org/10.1016/j.materresbull.2012.08.072
Lyskov N.V., Mazo G.N., Leonova L.S. et al. // Russ. J. Electrochem. 2013. V. 49. № 8. P. 747. https://doi.org/10.1134/S1023193513080120
Kolchina L.M., Lyskov N.V., Pestrikov P.P. et al. // Mater. Chem. Phys. 2015. V. 165. P. 91. https://doi.org/10.1016/j.matchemphys.2015.08.059
Mukherjee K., Hayamizu Y., Kim C.S. et al. // ACS Appl. Mater. Interfaces. 2016. V. 8. P. 34295. https://doi.org/10.1021/acsami.6b08977
Khandale A.P., Pahune B.S., Bhoga S.S. et al. // Int. J. Hydrogen Energy. 2019. V. 44. P. 15417. https://doi.org/10.1016/j.ijhydene.2019.04.055
dos Santos-Gomez L., Porras-Vazquez J.M., Hurtado J. et al. // J. Alloys Compd. 2019. V. 788. P. 565. https://doi.org/10.1016/j.jallcom.2019.02.237
Niemczyk A., Olszewska A., Du Z. et al. // Int. J. Hydrogen Energy. 2018. V. 43. P. 15492. https://doi.org/10.1016/j.ijhydene.2018.06.119
Chaudhari V.N., Khandale A.P., Bhoga S.S. // Ionics. 2017. V. 23. P. 2553. https://doi.org/10.1007/s11581-017-1999-8
Li H., Cai Zh., Li. Q. et al. // J. Alloys Compd. 2016. V. 688. P. 972. https://doi.org/10.1016/j.jallcom.2016.05.350
Boehm E., Bassat J.-M., Steil M.C. et al. // Solid State Sci. 2013. V. 5. P. 973. https://doi.org/10.1016/S1293-2558(03)00091-8
Hwang H.Y., Cheong S.-W., Cooper A.S. et al. // Physica C. 1992. V. 192. P. 362. https://doi.org/10.1016/0921-4534(92)90842-Z
Mazo G.N., Kazakov S.M., Kolchina L.M. et al. // Solid State Ionics. 2014. V. 257. P. 67. https://doi.org/10.1016/j.ssi.2014.01.039
Lappas A., Prasides K. // J. Solid State Chem. 1995. V. 115. P. 332. https://doi.org/10.1006/jssc.1995.1142
Stochniol G., Gupta A., Naoumidis A. et al. // Proceedings of the 5th International Symposium on Solid Oxide Fuel Cells (SOFC-V) / Eds. Stimming U. et al. N.J.: Electrochemical Society, Pennington, 1997. P. 888.
Tietz F. // Ionics. 1999. V. 5. P. 129. https://doi.org/10.1007/BF02375916
Mazo G.N., Kazakov S.M., Kolchina L.M. et al. // J. Alloys Compd. 2015. V. 639. P. 381. https://doi.org/10.1016/j.jallcom.2015.03.081
Hong D.J.L., Smyth D.M. // J. Solid State Chem. 1993. V. 102. P. 250. https://doi.org/10.1006/jssc.1993.1029
Hong D.J.L., Smyth D.M. // J. Solid State Chem. 1992. V. 97. P. 427. https://doi.org/10.1016/0022-4596(92)90052-W
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии