Журнал неорганической химии, 2021, T. 66, № 10, стр. 1457-1468
Система FeS–Ga2S3–In2S3
Ф. М. Мамедов a, *, Д. М. Бабанлы b, c, И. Р. Амирасланов d, Д. Б. Тагиев a, М. Б. Бабанлы a
a Институт катализа и неорганической химии им. акaд. М. Нагиева НАН Азербайджана
AZ-1143 Баку, пр-т Г. Джавида, 113, Азербайджан
b Азербайджанский государственный университет нефти и промышленности
AZ-1010 Баку, пр-т Азадлыг, 20, Азербайджан
c Азербайджано-французский университет
AZ-1010 Баку, ул. Низами, 183, Азербайджан
d Институт физики НАН Азербайджана
AZ-1143 Баку, пр-т Г. Джавида, 131, Азербайджан
* E-mail: faikmamadov@mail.ru
Поступила в редакцию 11.02.2021
После доработки 21.04.2021
Принята к публикации 27.04.2021
Аннотация
Представлены результаты исследования фазовых равновесий в системе FeS–Ga2S3–In2S3 методами дифференциального термического и рентгенофазового анализа. Построены некоторые политермические сечения и изотермические сечения при 900 и 1070 K фазовой диаграммы, а также проекция поверхности ликвидуса. Определены типы и координаты нон- и моновариантных равновесий. Установлено, что данная система квазитройная, ликвидус состоит из полей первичной кристаллизации шести фаз. На основе исходных бинарных и тройных (FeGa2S4, FeIn2S4) соединений выявлены широкие области твердых растворов, представляющие интерес как магнитные материалы.
ВВЕДЕНИЕ
Халькогениды переходных элементов типа АВ2Х4 (А = Mn, Fe; B = Ga, In, Sb, Bi; X = S, Se, Te), относящиеся к группе разбавленных магнитных полупроводников, проявляют интересные физические свойства и на протяжении многих лет привлекают внимание исследователей [1–11]. Это связано прежде всего с перспективностью их использования для создания приборов различного назначения: диодов Шоттки, переключателей, лазеров, модуляторов света и других устройств, управляемых магнитным полем. Установлено, что некоторые соединения указанного типа являются магнитными топологическими изоляторами и очень перспективны для создания супербыстрых элементов памяти, устройств спинтроники, квантовых компьютеров, детекторов темной материи и т.д. [12–18].
Поиск и дизайн новых сложных фаз основаны на данных по фазовым равновесиям и термодинамическим характеристикам соответствующих систем [1, 19–25]. При этом особый интерес представляют системы, содержащие соединения – структурные или формульные аналоги, в которых можно ожидать образования широких областей твердых растворов. Изменяя состав соединений путем получения твердых растворов различных типов замещения, можно существенно улучшить их функциональные характеристики [26–31].
Настоящая работа является продолжением наших исследований в области физико-химического анализа сложных систем на основе халькогенидов переходных металлов [32–34] и посвящена изучению фазовых равновесий в системе FeS–Ga2S3–In2S3.
Характеристики исходных соединений и граничных квазибинарных систем
Соединение FeS плавится конгруэнтно при 1461 K и претерпевает полиморфные переходы при 411 и 588 K [35]. Высокотемпературная модификация FeS кристаллизуется в тетрагональной структуре [36, 37], а низкотемпературная модификация имеет гексагональную структуру [38] (табл. 1).
Таблица 1.
Кристаллографические данные для соединений системы FeS–Ga2S3–In2S3
| Соединение | Тип, пр. гр. и параметры решетки, нм | Литература |
|---|---|---|
| FeS-ht | Тетрагональная, пр. гр. P4/nmm, а = 0.3768, c = 0.5039, или а = 0.36735, c = 0.50328 | [36] [37] |
| FeS-rt | Гексагональная, пр. гр. P63/mmc, а = 0.34436(1), c = 0.57262(2) | [38] |
| Ga2S3-ht | Гексагональная, пр. гр. P61, а = 0.374, c = 0.614 | [45] |
| Ga2S3-rt | Моноклинная, пр. гр. C1c1. а = 1.1107, b = 0.6411, c = 0.7021 | [46] |
| In2S3-ht1 | Тригональная, пр. гр. Pm1, а = 0.38656(2), c = 0.91569(5) | [47] |
| In2S3-ht2 | Кубическая, Fdm, а = 1.08315(2) | [47] |
| In2S3-rt | Тетрагональная, пр. гр. I1/amd, а = 0.76231(4), c = 3.2353(3) | [47] |
| Fe2Ga2S5 | Ромбоэдрическая, пр. гр. R3m, а = 0.36508(7), с = 4.4843 | [40] |
| FeGa2S4-ht | Ромбическая, пр. гр. $F\bar {4}3m$, а = 1.289, b = 0.751, с = 0.609 | [40] |
| FeGa2S4-rt | Тригональная, пр. гр. Pm1, а = 0.3654, c = 1.2056(5) | [40] |
| FeIn2S4 | Кубическая, пр. гр. Fdm, а = 1.0598 и a = 1.053 | [48] [41] |
| FeGaInS4 | Тригональная, пр. гр. Pm1,a = 0.37765(1), c = 1.22257(3) | [52] |
| GaInS3 | Гексагональная, пр. гр. P61, а = 0.6653(2), c = 1.7921(8), или а = 0.386, c = 1.740 | [49] [42] |
| Ga2In4S9 | Гексагональная, пр. гр. Pm1, а = 0.7589(5), c = 3.670(5) | [50] |
Соединение Ga2S3 плавится конгруэнтно при 1395 K и претерпевает фазовые переходы при 823 и 1293 K [38].
Соединение In2S3 плавится конгруэнтно при 1375 K и претерпевает полиморфные превращения при 411 и 588 K [35].
Типы и параметры кристаллических решеток различных модификаций FeS, Ga2S3 и In2S3, а также тройных соединений системы FeS–Ga2S3–In2S3 приведены в табл.1.
Боковые квазибинарные составляющие системы FeS–Ga2S3–In2S3 исследованы в работах [39–41].
Система FeS–Ga2S3 изучена в работах [39, 40]. По данным [39], она характеризуется образованием двух тройных соединений – FeGa2S4 и Fe2Ga2S5. Первое плавится с открытым максимумом при 1418 K и образует эвтектики с обоими бинарными соединениями. Эвтектики имеют координаты 46 мол. % FeS, 1363 K и 74 мол. % FeS, 1070 K. Соединение Fe2Ga2S5 устойчиво ниже температуры 1043 K, при которой разлагается по твердофазной реакции. В более ранней работе [40] была представлена ориентировочная фазовая диаграмма, согласно которой в системе образуется ряд промежуточных фаз переменного состава, устойчивых в узких интервалах температур, а соединения FeGa2S4 и Fe2Ga2S5 плавятся с разложением по перитектическим реакциям при 1343 и 1385 K соответственно. Первое имеет две модификации – высокотемпературную ромбическую и низкотемпературную тригональную (табл. 1).
Система FeS–In2S3 [41] характеризуется образованием соединения FeIn2S4 с конгруэнтным плавлением при 1398 K. Эвтектика имеет состав 73 мол. % FeS и кристаллизуется при 1373 K. FeIn2S4 образует непрерывный ряд твердых растворов с In2S3-ht1 с кубической структурой, который охватывает область концентраций 0–45% In2S3, что находится в соответствии с изоструктурностью указанных соединений (табл. 1). Образование твердых растворов на основе In2S3 сопровождается резким повышением температуры фазового перехода ht1 ↔ ht2 (1025 K) и установлением перитектоидного равновесия при 1300 K [41]. На кривых ликвидуса и солидуса, отвечающих β-фазе, существует точка минимума (M) при 85 мол. % In2S3 и 1285 K.
Система Ga2S3–In2S3 изучена в работах [42–44]. Согласно [42], она характеризуется наличием одного тройного соединения GaInS3, которое плавится с разложением по перитектической реакции при 1183 K и образует эвтектику (35 мол. % In2S3 и 1113 K) с твердыми растворами на основе Ga2S3.
В [43] представлена близкая к описанной в [42] картина фазовых равновесий в данной системе. Подтверждено существование инконгруэнтно плавящегося соединения GaInS3 (1183 K) и эвтектики при составе 35 мол. % In2S3. Однако, по данным [43], эвтектика кристаллизуется при более высокой температуре (1183 K), а указанное соединение является фазой переменного состава с широкой областью гомогенности. Практически одновременно с [43] была опубликована работа [44], в которой сообщалось о полученной методом газотранспортных реакций смеси кристаллов тройных фаз составов Ga2In4S9, Ga2In8S15 и Ga6In4S15. Позже была определена кристаллическая структура одной из них – Ga2In4S9 (табл. 1).
В работах [51, 52] нами были изучены квазибинарные разрезы FeGa2S4–FeIn2S4 и FeS–FeGaInS4 системы FeS–Ga2S3–In2S3 и из порошковых дифракционных данных уточнена кристаллическая структура и параметры решетки фазы FeGaInS4 (табл. 1). Недавно мы представили данные по квазитройным подсистемам FeS–FeGa2S4–FeGaInS4 [53] и FeS–FeGaInS4–FeIn2S4 [54]. Установлено, что первая подсистема относится к системам с моновариантными эвтектическим и перитектоидным равновесиями, а вторая – к типу с тройной эвтектикой и ограниченными твердыми растворами на основе исходных соединений.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез. Для проведения исследований вначале были синтезированы соединения FeS, Ga2S3, In2S3, FeGa2S4 и FeIn2S4 с использованием высокочистых элементов: железа (99.995%), индия (99.999%), галлия (99.999%) и серы (99.99%), приобретенных у “Alfa Aesar” (Германия). Стехиометрические смеси элементов помещали в кварцевые ампулы, которые вакуумировали до остаточного давления ~10–2 Па. Синтез проводили в двухзонном режиме. В случае FeS нижнюю “горячую” зону медленно нагревали от комнатной температуры до 1470 K, а в случае соединений Ga2S3, In2S3, FeGa2S4 и FeIn2S4 – на 30–50 K выше их точек плавления. При синтезе часть ампулы находилась вне печи и охлаждалась водой (“холодная” зона). Взаимодействие компонентов происходило в “горячей” зоне, а в “холодной” зоне газообразная сера конденсировалась и возвращалась в зону взаимодействия. В результате реакции в “холодной” зоне количество серы халькогена постепенно уменьшалось, и в течение 1–2 ч она расходовалась практически полностью. После этого ампулу полностью помещали в печь и выдерживали при указанной температуре в течение 3–4 ч. Полученные образцы подвергали термообработке при 900 K в течение 100 ч, это позволяло достичь полноты взаимодействия и увеличить степень кристалличности синтезируемых соединений.
Индивидуальность синтезированных соединений контролировали методами ДТА и РФА. Температуры плавления FeS, Ga2S3, In2S3, FeGa2S4 и FeIn2S4, определенные по термограммам нагревания с точностью ±3 K, были равны 1465, 1395, 1375, 1418 и 1398 K соответственно, что совпадает с данными работ [35, 39, 40].
В результате расшифровки порошковых рентгенограмм получены следующие кристаллографические данные:
FeS – гексагональная решетка, пр. гр. P63/mmc, a = 0.34440(4), c = 0.57260(7) нм;
Ga2S3 – моноклинная решетка, пр. гр. C1c1, а = 1.1109(4), b = 0.6414(5), c = 0.7024(7) нм;
In2S3 – тетрагональная решетка, пр. гр. I1/amd, a = 0.76232(4), c = 3.2355(2) нм;
FeGa2S4 – тригональная решетка, пр. гр. P3m1, a = 0.36543(3), c = 1.20558(8) нм;
FeIn2S4 – кубическая решетка, пр. гр. Fd3m, a = 1.0607(2) нм,
которые хорошо согласуются с литературными данными (табл. 1).
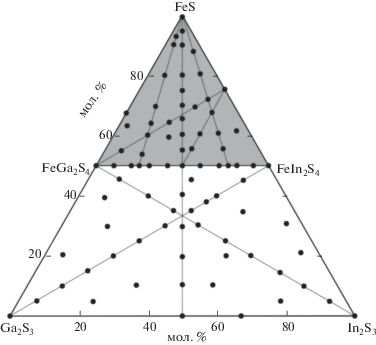
Сплавы исследуемой системы (рис. 1) каждый массой 0.5 г готовили сплавлением исходных соединений в различных соотношениях в вакуумированных кварцевых ампулах с последующим гомогенизирующим отжигом при 900 K в течение ∼600 ч. Некоторые сплавы после выдерживания при 1070 или 900 K закаливали вбрасыванием в холодную воду.
Методы исследования. Дифференциальный термический анализ выполняли на установке Netzsch 404 F1 Pegasus system (хромель-алюмелевые термопары) в интервале температур от комнатной до ~1480 K со скоростью нагревания 10 град/мин. Рентгенофазовые и структурные исследования проводили на основе порошковых дифрактограмм, полученных на дифрактометре D2 Phaser (CuKα1-излучение).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Совместная обработка полученных экспериментальных результатов, а также имеющихся данных по граничным квазибинарным системам и подсистеме FeS–FeGa2S4–FeIn2S4 [51–53] позволила установить полную взаимосогласованную картину фазовых равновесий в системе. При этом нами в основном подтверждены данные [39, 40, 43] по фазовым равновесиям в граничных квазибинарных системах. Небольшие расхождения, касающиеся координат некоторых нонвариантных точек (табл. 2), учтены при обработке данных ДТА сплавов системы FeS–Ga2S3–In2S3.
Таблица 2.
Нонвариантные равновесия в системе FeS–Ga2S3–In2S3
| Точка или кривая на рис. 5 | Равновесие | Т, K | Состав, мол. % | |
|---|---|---|---|---|
| FeS | In2S3 | |||
| D1 D2 D* p1 p2 p3 |
L ↔ γ (FeGa2S4) L ↔ β2 (FeIn2 S4) L ↔ β2 (FeGaInS4) L + β2 ↔ δ L + $\beta _{2}^{'}$ ↔ β2 L + $\beta _{2}^{'}$ ↔ β2 |
1420 1410 1375 1190 1310 1300 |
50 50 50 – 7 – |
– 50 25 43 93 90 |
| M e1 e2 e3 e4 |
L ↔ β2 L ↔ β1 + δ L ↔ β1 + γ L ↔ α + γ L ↔ α + β2 |
1290 1180 1363 1328 1373 |
12 – 44 74 72 |
88 32 – – 28 |
| e5 e6 U E1 E2 |
L ↔ γ + β2 L ↔ α + β2 L + β2 ↔ γ + δ L ↔ β1 + γ + δ L ↔ α + β2 + γ |
1340 1310 1168 1105 1290 |
50 68 10 9 65 |
35 16 38 31 24 |
В таблицах и на рисунках, а также в тексте статьи использованы следующие обозначения твердых растворов на основе соединений и их различных модификаций: α – FeS-ht, β1 – Ga2S3, $\beta _{{\text{2}}}^{'}$ – In2S3‑ht2, γ – FeGa2S4, β2 – FeIn2S4, δ – GaInS3, ε – Ga2In4S9.
Твердофазные равновесия в системе FeS–Ga2S3–In2S3
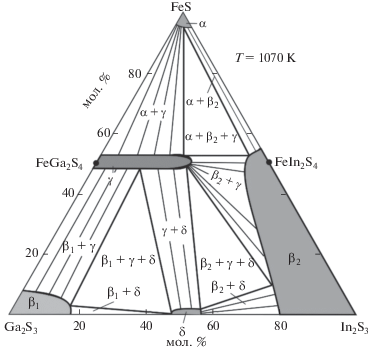
На рис. 2 представлена диаграмма твердофазных равновесий в системе FeS–Ga2S3–In2S3 при 900 K. Из диаграммы видно, что система характеризуется образованием широких областей твердых растворов на основе исходных бинарных и тройных соединений. Характер фазовых равновесий и соответствующие экспериментальные данные по подсистеме FeS–FeGa2S4–FeIn2S4 приведены и рассмотрены в работах [51–54].
Рис. 2.
Диаграмма твердофазных равновесий системы FeS–Ga2S3–In2S3 при 900 K. Красные кружки (1–7) – сплавы, для которых на рис. 3 приведены порошковые дифрактограммы.
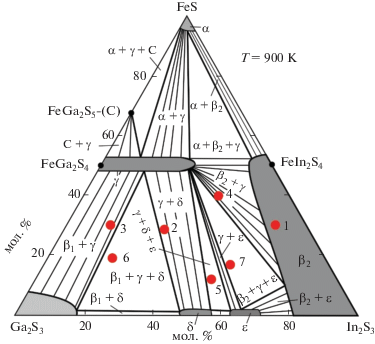
Как видно из рис. 2, подсистема Ga2${\text{S}}_{{\text{3}}}^{'}$–FeGa2S4–FeIn2S4–In2S3, которая может быть представлена как взаимная система Ga2${\text{S}}_{{\text{3}}}^{'}$ + FeIn2S4 ↔ ↔ In2S3 + FeGa2S4, является обратимо-взаимной, т.е. не имеет стабильной диагонали. В формировании фазовых областей определяющую роль играют не исходные соединения, а твердые растворы, особенно γ-фаза на основе FeGa2S4, которая образует коноды со всеми другими фазами системы.
Наличие широких областей гомогенности на основе исходных соединений по разрезу FeGa2S4–FeIn2S4 (рис. 2, γ- и β2-фазы) установлено нами в работе [51], где представлены кристаллографические данные твердых растворов.
Следует также отметить образование непрерывных твердых растворов между In2S3-ht1 и FeIn2S4, имеющими кубическую структуру. Мы установили, что область гомогенности этой фазы растворов проникает вглубь концентрационного треугольника и занимает значительную часть его площади (рис. 2, область β2). На основании данных порошковых дифрактограмм мы определили значения периода решетки для различных составов β2-фазы, которые монотонно меняются в интервале a = 1. 05152–1.08315 нм.
Все фазовые области в подсистеме Ga2S3–FeGa2S4–FeIn2S4–In2S3 подтверждены рентгенографически. На рис. 3 приведены порошковые дифрактограммы выборочных сплавов из ряда одно-, двух- и трехфазных областей с указанием фазовых составов. Видно, что дифракционные картины всех этих образцов находятся в соответствии с фазовой диаграммой.
Рис. 3.
Порошковые дифрактограммы и фазовые составы сплавов 1–7 системы FeS–Ga2S3–In2S3, указанных на рис. 2.
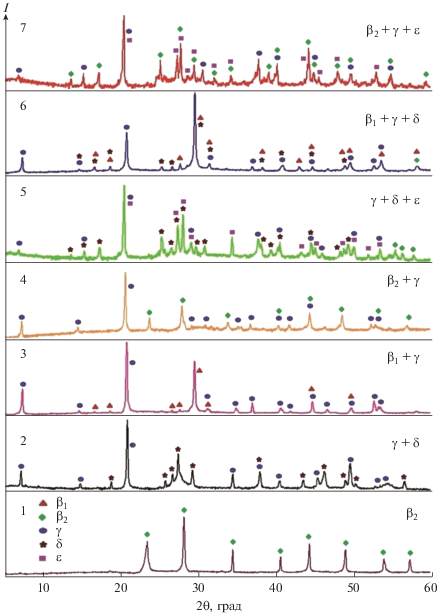
Диаграмма твердофазных равновесий при 1070 K (рис. 4) отличается от таковой при 900 K отсутствием соединения Fe2Ga2S5 и ε-фазы, которые существуют ниже 1043 [51] и 990 K соответственно, а также фазовых полей с их участием.
Поверхность ликвидуса
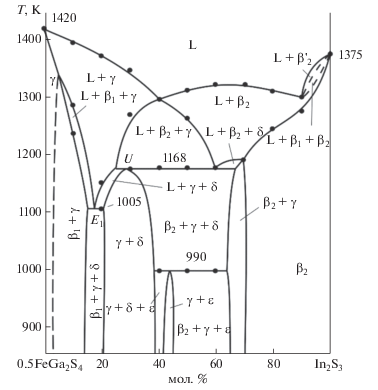
На рис. 5 представлена проекция поверхности ликвидуса системы FeS–Ga2S3–In2S3 с указанием изотерм с шагом 50 K. Видно, что ликвидус состоит из шести полей, отвечающих первичной кристаллизации α-, γ-, β1-, β2-, δ- и $\beta _{{\text{2}}}^{'}$-фаз. Эти поля разграничены рядом кривых моновариантных равновесий и точек нонвариантных равновесий. Типы и координаты нонвариантных равновесий приведены в табл. 2, а типы и температурные интервалы моновариантных равновесий – в табл. 3.
Рис. 5.
Проекция поверхности ликвидуса системы FeS–Ga2S3–In2S3. Пунктиры – квазибинарные разрезы. Поля первичной кристаллизации фаз: 1 – α; 2 – γ; 3 – β1; 4 – β2; 5 – δ; 6 – $\beta _{2}^{'}.$
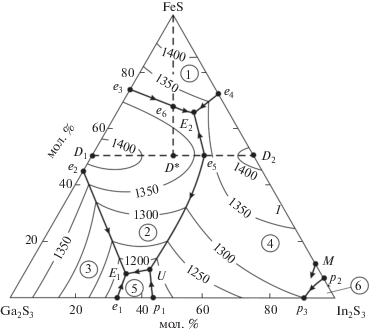
Таблица 3.
Моновариантные равновесия в системе FeS–Ga2S3–In2S3
| Кривая на рис. 5 |
Равновесие | Температурный интервал, K |
|---|---|---|
| p2p3 p1U e5U UE1 e1E1 |
L + $\beta _{2}^{'}$ ↔ β2 L+ β2 ↔ δ L ↔ γ + β2 L ↔ γ + δ L ↔ β1 + δ |
1310–1300 1190–1168 1340–1168 1168–1105 1165–1105 |
| e2E1 e3e6 e6E2 e4E2 e5E2 |
L ↔ β1 + γ L ↔ α + γ L ↔ α + γ L ↔ α + β2 L ↔ β2 + γ |
1163–1105 1328–1310 1310–1290 1373–1290 1340–1290 |
Квазибинарные разрезы FeGa2S4–FeIn2S4 и FeS–FeGaInS4 (рис. 5, пунктирные прямые) делят концентрационный треугольник FeS–Ga2S3–In2S3 на три самостоятельные подсистемы. Подсистемы FeS–FeGa2S4–FeGaInS4 и FeS–FeGaInS4–FeIn2S4 относятся к типам с моновариантной и нонвариантной эвтектиками соответственно. Третья подсистема, Ga2S3–FeGa2S4–FeIn2S4–In2S3, конгруэнтно не триангулируется, что, как показано выше, связано с образованием в ней ряда фаз переменного состава с широкими областями гомогенности.
Как видно из рис. 5, наибольшие протяженности по составу и температуре имеют поля первичной кристаллизации β2-, γ- и β1-фаз, что открывает возможность варьировать составы раствор-расплавов и температурных режимов при выращивании монокристаллов указанных твердых растворов.
Политермические разрезы
Для уточнения положения изотерм на поверхностях ликвидуса фаз, хода кривых моновариантных равновесий и координат точек нонвариантных равновесий нами построен ряд политермических сечений фазовой диаграммы системы А. Ниже представлены и кратко описаны некоторые из них.
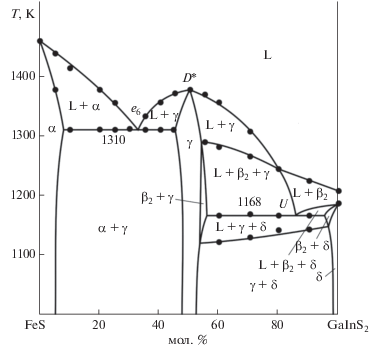
Разрез FeS–GaInS3 (рис. 6) частично квазибинарный. В области составов FeS–FeGaInS4 он относится к эвтектическому типу. Отметим, что точка максимума (D*), отвечающая плавлению γ-фазы состава FeGaInS4, не является таковой по разрезу FeGa2S4–FeIn2S4 [53]. Поэтому она, по-видимому, не является дистектической точкой в классическом понимании. Однако мы установили [52, 53], что γ-фаза состава FeGaInS4 плавится при постоянной температуре (1375 K) и, образуя нонвариантные эвтектики (е5, е6) с α- и β2-фазами на основе FeS и FeIn2S4, триангулирует систему А.
В области составов >50 мол. % GaInS3 ликвидус состоит из ветвей, отвечающих первичной кристаллизации γ- и β2-фаз. Ниже ликвидуса в области 55–85 мол. % GaInS3 кристаллизация протекает моновариантно по эвтектической (табл. 3, кривая e5U), а в области >85 мол. % GaInS3 – по перитектической (P1U) реакциям. Горизонталь при 1168 K соответствует нонвариантной переходной реакции (U). Далее кристаллизация продолжается по эвтектической кривой UE1 и завершается образованием двухфазной области γ + δ (рис. 6).
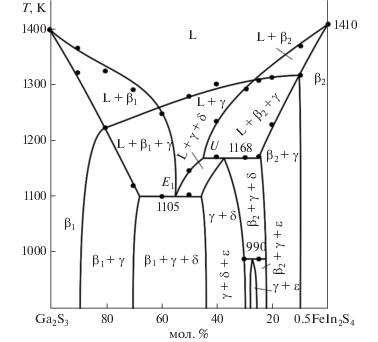
Разрез Ga2S3–0.5FeIn2S4 (рис. 7) пересекает поля первичной кристаллизации β1-, γ- и β2-фаз. В интервалах составов 0–10 и 85–100 мол. % Ga2S3 кристаллизация завершается образованием однофазных β2- и β1-твердых растворов соответственно. В промежуточном интервале составов ниже ликвидуса протекают равновесные эвтектические реакции по кривым e5U (10–45 мол. % Ga2S3), UE1 (45–55 мол. % Ga2S3) и e2Е1 (55–80 мол. % Ga2S3). В определенных концентрационных интервалах кристаллизация завершается этими реакциями и на Т–х-диаграмме формируются двухфазные области β2 + γ, γ + δ и β1 + γ. Горизонталь при 1168 K отвечает нонвариантной переходной реакции U, а при 1105 K – кристаллизации тройной эвтектики β1 + γ + δ (Е1). Термический эффект при 990 K относится к твердофазной реакции β2 + δ ↔ ε. Существование ε-фазы и соответствующих фазовых областей при 900 K подтверждено нами рентгенографически (рис. 2).
Разрез 0.5FeGa2S4–In2S3 (рис. 8) проходит через поля первичной кристаллизации γ-, β2- и $\beta _{{\text{2}}}^{'}$-фаз. Сравнение с рис. 5 показывает, что при составах >90 мол. % In2S3 после первичной кристаллизации $\beta _{{\text{2}}}^{'}$-фазы протекает перитектоидная реакция L + $\beta _{{\text{2}}}^{'}$ ↔ β2 (рис. 5, табл. 3, кривая Р2Р3) и кристаллизация завершается по схеме L → β2. Этим же процессом завершается кристаллизация образцов, содержащих >70 мол. % In2S3. В области составов 5–70 мол. % In2S3 ниже ликвидуса кристаллизация продолжается моновариантно по эвтектическим е2Е1 (5–18 мол. % In2S3), UЕ1(18–25 мол. % In2S3), е5U (25–60 мол. % In2S3) и перитектической P1U (60–70 мол. % In2S3) кривым. Горизонтали при 1168, 1105 и 990 K отвечают соответственно нонвариантным переходному (U), эвтектическому (E1) равновесиям и твердофазной реакции β2 + δ ↔ ε. В субсолидусе данный разрез проходит через ряд областей, фазовые составы и границы которых находятся в соответствии с диаграммами твердофазных равновесий (рис. 2, 4).
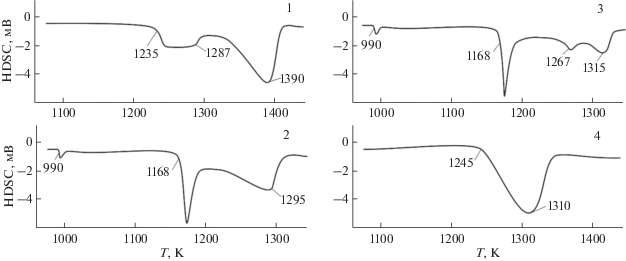
В заключение рассмотрим кривые ДТА нагревания некоторых образцов по разрезу 0.5FeGa2S4–In2S3 (рис. 9) в контексте рис. 5 и 8. Образец 1 (10 мол. % In2S3) в твердом состоянии двухфазный – β1 + γ. Согласно рис. 5 и 8, размытый эндотермический эффект в интервале температур 1235–1287 K отвечает его моновариантному плавлению по эвтектической схеме L ↔ β1 + γ (е2Е1). После этой реакции избыток β1-фазы полностью переходит в жидкое состояние при 1390 K. На кривой ДТА образца 2 (40 мол. % In2S3) видны четкие эндоэффекты при 990 и 1168 K, относящиеся к твердофазному разложению ε-фазы и переходному равновесию U. Плавление завершается при 1295 K по эвтектической схеме е2Е1 (рис. 5, табл. 3). Термограмма нагревания образца 3 (50 мол. % In2S3 ) кроме этих трех процессов отражает также завершение плавления при 1315 K (рис. 8). Кривая нагревания образца 4 (80 мол. % In2S3) содержит один размытый эндоэффект, отвечающий плавлению β2-твердого раствора.
ЗАКЛЮЧЕНИЕ
На основании результатов ДТА и РФА свыше 50 синтезированных и отожженных сплавов впервые получена полная взаимосогласованная картина фазовых равновесий в квазитройной системе FeS–Ga2S3–In2S3. Построены проекция поверхности ликвидуса, некоторые политермические сечения и изотермические сечения при 900 и 1070 K фазовой диаграммы. Определены поля первичной кристаллизации шести фаз, а также типы и координаты нон- и моновариантных равновесий. В системе выявлены широкие области твердых растворов на основе бинарных и тройных соединений, представляющие практический интерес как потенциальные магнитные материалы.
Список литературы
Haeuseler H., Srivastava S.K. // Z. Kristallogr. 2000. V. 215. № 4. P. 205. https://doi.org/10.1524/zkri.2000.215.4.205
Ranmohotti K.G.S., Djieutedjeu H., Lopez J. et al. // J. Am. Chem. Soc. 2015. V. 137. № 2. P. 691. https://doi.org/10.1021/ja5084255
Djieutedjeu H., Makongo J., Rotaru A. et al. // Eur. J. Inorg. Chem. 2011. V. 26. P. 3969. https://doi.org/10.1002/ejic.201100364
Torresa T., Sagredoa V., de Chalbauda L.M. et al. // Phys. B. 2006. V. 384. P. 100. https://doi.org/10.1016/j.physb.2006.05.162
Боднарь И.В., Викторов И.А., Павлюковец С.А. // Неорган. материалы. 2010. Т. 46. № 6. С. 681. [Bodnar I.V., Viktorov I.A., Pavlyukovets S.A. // Inorg. Mater. 2010. V. 46. № 6. P. 604. https://doi.org/10.1134/S0020168510060087]
Боднарь И.В., Труханов С.В. // ФТП. 2011. Т. 45. № 7. С. 890. [Bodnar I.V., Trukhanov S.V. // Semiconductors. 2011. V. 45. № 7. Р. 861. https://doi.org/10.1134/S1063782611070050]
Nowka C., Gellesch M., Enrique Hamann Borrero J. et al. // J. Cryst. Growth. 2017. V. 459. P. 81. https://doi.org/10.1016/j.jcrysgro.2016.11.090
Myoung B.R., Lim J.T., Kim C.S. // J. Magn. Magn. Mater. 2017. V. 438. P. 121. https://doi.org/10.1016/j.jmmm.2017.04.05624
Yang J., Zhou Z., Fang J. et al. // Appl. Phys. Lett. 2019. V. 115. № 22. P. 222101. https://doi.org/.1063/1.5126233
Karthikeyan N., Aravindsamy G., Balamurugan P., Sivakumar K. // Mater. Res. Innovations. 2017. P. 278. https://doi.org/10.1080/14328917.2017.1314882
Аминов Т.Г., Бушева Е.В., Шабунина Г.Г. // Журн. неорган. химии. 2019. Т. 64. № 12. С. 1340. [Aminov T.G., Busheva E.V., Shabunina G.G. // Russ. J. Inorg. Chem. 2019. V. 64. № 12. P. 1592. https://doi.org/10.1134/S0036023619120039]https://doi.org/10.1134/S0044457X19120031
Otrokov M.M., Klimovskikh I.I., Bentmann H. et al. // Nature. 2019. V. 576. P. 416. https://doi.org/10.1038/s41586-019-1840-9
Xu L., Mao Y., Wang H. et al. // Science Bull. 2020. V. 65. № 24. P. 2086. https://doi.org/10.1016/j.scib.2020.07.032
Klimovskikh I.I., Otrokov M.M., Estyunin D. et al. // Quantum Mater. 2020. V. 5. № 54. P. 1. https://doi.org/10.1038/s41535-020-00255-9
Estyunin D.A., Klimovskikh I.I., Shikin A.M. et al. // APL Materials. 2020. V. 8. P. 021105. https://doi.org/10.1063/1.5142846
Yonghao Y., Xintong W., Hao L. et al. // Nano Lett. 2020. V. 20. P. 3271. https://doi.org/10.1021/acs.nanolett.0c00031
Zhou L., Tan Z., Yan D. et al. // Phys. Rev. B. 2020. V. 102. P. 085114. https://doi.org/10.1103/PhysRevB.102.085114
Yujun D., Yijun Y., Meng Z. et al. // Science. 2020. V. 367. № 6480. P. 895. https://doi.org/10.1126/science.aax8156
Zlomanov V.P., Khoviv A.M., Zavrazhnov A.Yu. // Tech. Mater. Sci. Adv. Topics. 2013. P. 103.
Imamaliyeva S.Z., Babanly D.M., Tagiev D.B., Babanly M.B. // Russ. J. Inorg. Chem. 2018. V. 63. № 13. P. 1704. https://doi.org/10.1134/S0036023618130041
Babanly M.B., Mashadiyeva L.F., Babanly D.M. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 13. P. 1649. https://doi.org/10.1134/S0036023619130035
Кертман А.В., Русейкина А.В. // Журн. неорган. химии. 2020. Т. 65. № 11. С. 1544. [Kertman A.V., Ruseikina A.V. // Russ. J. Inorg. Chem. 2020. V. 65. № 11. P. 1756. https://doi.org/10.1134/S003602362011008X]https://doi.org/10.31857/S0044457X20110082
Имамалиева С.З., Мехдиева И.Ф., Бабанлы Д.М. и др. // Журн. неорган. химии. 2020. Т. 65. № 11. С. 1550. [Imamaliyeva S.Z., Mekhdiyeva I.F., Babanly D.M. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 11. P. 1762. https://doi.org/10.1134/S0036023620110066]https://doi.org/10.31857/S0044457X20110069
Асадов М.М., Ахмедова Н.А., Мамедова С.Р., Тагиев Д.Б. // Журн. неорган. химии. 2020. Т. 65. № 7. С. 974. [Asadov M.M., Akhmedova N.A., Mamedova S.R. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 7. Р. 1061. https://doi.org/10.1134/S0036023620070013]https://doi.org/10.31857/S0044457X20070016
Исмаилова Э.Н., Машадиева Л.Ф., Бахтиярлы И.Б., Бабанлы М.Б. // Журн. неорган. химии. 2019. Т. 64. № 6. С. 646. [Ismailova E.N., Mashadieva L.F., Bakhtiyarly I.B. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 6. Р. 801. https://doi.org/10.1134/S0036023619060093]https://doi.org/10.1134/S0044457X19060096
Ranmohotti K.G.S., Djieutedjeu H., Poudeu P.F.P. // J. Am. Chem. Soc. 2012. V. 134. № 34. P. 14033. https://doi.org/10.1021/ja303952w
Moroz N.A., Lopez J.S., Djieutedjeu H., Ranmohotti K.G.S. et al.// Chem. Mater. 2016. V. 28. № 23. P. 8570. https://doi.org/10.1021/acs.chemmater.6b03293
Боднарь И.В., Труханов С.В // ФТП. 2011. Т. 45. № 11. С. 1464. [Bodnar I. V., Trukhanov S.V. // Semiconductors. 2011. V. 45. № 11. P. 1408. https://doi.org/10.1134/s106378261111008x]
Рудь В.Ю., Рудь Ю.В., Осипова М.А., Боднарь И.В. // ФТП. 2010. Т. 44. № 1. С. 48. [Rud V.Y., Rud Y.V., Osipova M.A., Bodnar I.V. // Semiconductors. 2010. V. 44. № 1. Р. 45.] https://doi.org/10.1134/S1063782610010070
Djieutedjeu H., Zhou X., Chi H., Haldolaarachchige N. et al. // J. Mater. Chem. C. 2014. V. 2. P. 6199. https://doi.org/10.1039/C4TC00672K
Orujlu E.N. // Phys. Chem. Solid State. 2020. V. 21. № 1. P. 113. https://doi.org/10.15330/pcss.21.1.113-116
Mammadov F.M., Amiraslanov I.R., Imamaliyeva S.Z. et al. // J. Phase Equilib. Diffus. 2019. V. 40. № 6. P. 787. https://doi.org/10.1007/s11669-019-00768-2
Мамедов Ф.М., Бабанлы Д.М., Амирасланов И.Р. и др. // Журн. неорган. химии. 2020. Т. 65. № 11. С. 1535. [Mamedov F.M., Babanly D.M., Amiraslanov I.R. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 11. P. 1747. https://doi.org/10.1134/S0036023620110121]10.1134/S0036023620110121
Mammadov F.M., Amiraslanov I.R., Aliyeva Y.R. et al. // Acta Chim. Slovenica. 2019. V. 66. P. 466. https://doi.org/10.17344/acsi.2019.4988
Binary alloy phase diagrams / Ed. Massalski T.B. Ohio, 1990. 3875 p.
Bertaut E.F., Burlet P., Chappert J. // Solid State Commun. 1965. V. 3. P. 335.
Lennie A.R., Redfern S.A., Schofield P.F., Vaughan D.J. // Mineralogical Magazine.1995. V. 59. P. 677.
Kuhn S.J., Kidder M.K., Parker D.S. et al. // Phys. C: Superconductivity and Its Applications. 2017. V. 534. P. 29. https://doi.org/10.1016/j.physc.2016.12.006
Allazov M.R. // Bull. Baku State University. 2009. № 2. P. 42.
Pardo M.P., Dogguy-Smiri L., Flahaut J. // Mater. Res. Bull. 1980. № 7. V. 16. P. 1375.
Рустамов П.Г., Бабаева Б.К., Аллазов М.Р. // Журн. неорган. химии. 1979. № 24. P. 2208.
Заргарова М.И., Гамидов Р.С. // Изв. АН СССР. Неорган. материалы. 1969. Т. 5. № 2. С. 371.I.
Muschinsky V.P., Ambross V.P. // Kristall Technic. 1970. V. 5. I. 4. P. 5.
Kramer V., Nitsche R., Ottemann J. // J. Cryst. Growth. 1970. V. 7. P. 285.
Camille Y.J., Jimmie G.E. // J. Phys. Chem. B. 2001. V. 105. P. 2718. https://doi.org/10.1021/jp003312x
Jones C.Y., Bryan J.C., Kirschbaum K., Edwards J.G. // Z. Kristallogr. 2001. V. 216. P. 327. https://doi.org/10.1524/ncrs.2001.216.14.349
Paul P., Jose M.M.A., Maximo L. et al. // Acta Crystallogr. B. 2016. V. 72. P. 410. https://doi.org/10.1107/S2052520616007058
Hahn H., Klingler W. // Z. Anorg. Allg. Chem. 1950. V. 263. P. 177.
Гусейнов Г.Г., Амирасланов И.Р., Кулиев А.С., Maмедов K.С. // Неорган. материалы. 1987. Т. 23. С. 854.
Schulte M., Kramer V. // Z. Naturforsch. 1982. V. 37b. P. 390.
Mammadov F.M., Amiraslanov I.R., Efendiyeva N.N., Imamaliyeva S.Z. // Chem. Problems. 2019. V. 17. P. 58. https://doi.org/10.32737/2221-8688-2019-1-58-65
Mammadov F.M., Niftiyev N.N., Mammadov F.I. // Azerb. Chem. J. 2017. № 2. P. 56.
Mammadov F.M. // Chem. Problems. 2020. V. 18. № 2. P. 214. https://doi.org/10.32737/2221-8688-2020-2-214-221
Mammadov F.M. // Azerb. Chem. J. 2020. № 3. P. 29. https://doi.org/10.32737/0005-2531-2020-3-29-33
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии