Журнал неорганической химии, 2021, T. 66, № 1, стр. 63-68
Новые гексабромоплатинаты органилтрифенилфосфония [Ph3PR]2[PtBr6], R = CH3, CH=CH2, CH2CH=CH2
А. Р. Зыкова a, *, В. В. Шарутин a, О. К. Шарутина a
a Южно-Уральский государственный университет (национальный исследовательский университет)
454080 Челябинск, пр-т им. В.И. Ленина, 76, Россия
* E-mail: aesya@mail.ru
Поступила в редакцию 02.07.2020
После доработки 19.08.2020
Принята к публикации 25.08.2020
Аннотация
C целью расширения знаний об ионных гексабромсодержащих комплексах платины(IV), перспективных в качестве катализаторов химических реакций и биологически активных веществ, синтезирован следующий ряд соединений: [Ph3PCH3]2[PtBr6] (I), [Ph3PCH=CH2]2[PtBr6] (II), [Ph3PCH2CH=CH2]2[PtBr6] (III). Комплексы I–III представляют собой кристаллы красного цвета, полученные из гексабромоплатината калия и бромидов органилтрифенилфосфония в ацетонитриле с выходом 90–94%. Строение полученных соединений установлено с помощью рентгеноструктурного анализа и инфракрасной спектроскопии. В кристаллах комплексов I−III присутствуют тетраэдрические катионы фосфония. Тетраэдрическая конфигурация катионов приближается к идеальной. В гексабромоплатинатных октаэдрических анионах транс-углы BrPtBr равны 180°, цис-углы близки к теоретическому значению 90°. Структура кристаллов образована слабыми водородными связями Br…H–C между катионами и анионами.
ВВЕДЕНИЕ
Октаэдрическая координационная сфера платины обусловливает широкие возможности для точной настройки фармакологических свойств соединения [1, 2]. Комплексы четырехвалентной платины являются кинетически инертными по сравнению с аналогичными комплексами двухвалентной платины [3]. Препараты на основе платины(IV) обладают рядом преимуществ: более высокой стабильностью свойств, более длительным периодом полураспада в крови и более низкой токсичностью [4]. Функциональность препаратов, как полагают, зависит от восстановления Pt(IV) до Pt(II) in vivo, в результате чего образуются реакционноспособные интермедиаты, которые могут взаимодействовать с ДНК, приводящие к запрограммированной гибели опухолевой клетки [5, 6].
Гексахлороплатинаты(IV) проявляют противоопухолевую активность против клеточной линии аденокарциномы легкого человека (A549) и клеточной линии карциномы носоглотки человека (CNE-2) [7]. Ранее нами была выявлена антимикробная активность гексахлороплатинатов(IV) аммония в отношении Escherichia coli штамма М-17 [8]. Гексахлороплатинаты(IV) применяют также в качестве катализаторов реакций, проводимых в ионных жидкостях [9, 10].
В литературе известно только несколько гексабромоплатинатных комплексов, содержащих в качестве катионов протонированные гетероциклические соединения (замещенный имидазол, фенантролин, пиридин) [11–15], которые успешно применяются в качестве катализатора гидросилилирования фенилацетилена триэтилсиланом [11]. Другой пример практического применения заключается в получении твердых растворов на основе термического разложения бинарных комплексов, содержащих тугоплавкие металлы [15].
С целью установления особенностей синтеза и строения гексабромоплатинатных комплексов фосфония нами получены и структурно охарактеризованы ионные комплексы платины(IV) [Ph3PCH3]2[PtBr6], [Ph3PCH=CH2]2[PtBr6] и [Ph3PCH2CH=CH2]2[PtBr6].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез [Ph3PCH3]2[PtBr6] (I). К раствору 47 мг (0.1 ммоль) бромида метилтрифенилфосфония в 3 мл ацетонитрила приливали раствор 50 мг (0.06 ммоль) гексабромоплатината калия в 3 мл ацетонитрила. После сливания растворов смесь выдерживали в течение 48 ч, фильтровали, промывали ацетонитрилом. Раствор медленно испаряли до объема 0.5 мл, наблюдали образование кристаллов. Выход 72 мг (90%), красные кристаллы, tпл = 234°С. ИК-спектр (ν, см–1): 3058, 2971, 2905, 2361, 1584, 1479, 1436, 1403, 1342, 1332, 1317, 1163, 1115, 1025, 995, 974, 893, 782, 747, 717, 690, 515, 502, 475, 429.
Соединения II и III синтезировали аналогично.
[Ph3PCH=CH2]2[PtBr6] (II). Красные кристаллы, выход 93%, tразл = 219°С. ИК-спектр (ν, см–1): 3058, 3015, 2988, 2955, 2852, 2361, 1584, 1481, 1434, 1386, 1340, 1313, 1265, 1186, 1161, 1113, 1017, 995, 979, 848, 755, 738, 725, 689, 599, 536, 490, 480, 437, 419.
[Ph3PCH2CH=CH2]2[PtBr6] (III). Красные кристаллы, выход 94%, tпл = 238°С. ИК-спектр (ν, см–1): 3034, 3011, 2981, 2865, 2361, 1632, 1603, 1582, 1481, 1435, 1388, 1312, 1186, 1161, 1111, 995, 975, 924, 836, 810, 783, 753, 743, 720, 689, 616, 598, 538, 516, 505, 457, 437.
ИК-спектры регистрировали на инфракрасном спектрометре Shimadzu IR Affinity-1S в таблетках KBr в области 4000–400 см–1.
Рентгеноструктурный анализ монокристаллов I–III (CCDC 1 988 380 для I, 1 988 472 для II, 1 989 018 для III, deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk) выполнен на дифрактометре D8 QUEST фирмы Bruker (MoKα-излучение, λ = 0.71073 Å, графитовый монохроматор) при 296(2) K. Обработку данных, редактирование и уточнение параметров элементарной ячейки и структур проводили по программам SMART и SAINT-Plus [16], SHELXL/PC [17] и OLEX2 [18]. Кристаллографические данные и результаты уточнения структур приведены в табл. 1.
Таблица 1.
Кристаллографические данные, параметры эксперимента и уточнения структур I–III
| Параметр | I | II | III |
|---|---|---|---|
| М | 1229.16 | 1253.18 | 1281.23 |
| Сингония | Моноклинная | Триклинная | Триклинная |
| Пр. гр. | P21/n | P$\bar {1}$ | P$\bar {1}$ |
| a, Å | 10.214(6) | 9.968(9) | 10.297(9) |
| b, Å | 13.023(6) | 14.533(11) | 10.705(10) |
| c, Å | 15.219(7) | 14.784(15) | 10.882(10) |
| α, град | 90.00 | 94.50(5) | 80.92(4) |
| β, град | 97.64(2) | 102.86(5) | 69.47(4) |
| γ, град | 90.00 | 93.05(4) | 73.95(5) |
| V, Å3 | 2006.4(17) | 2076(3) | 1077.1(18) |
| Z | 4 | 2 | 1 |
| ρвыч, г/см3 | 2.035 | 2.005 | 1.975 |
| μ, мм−1 | 9.577 | 9.259 | 8.925 |
| F(000) | 1164.0 | 1188.0 | 610.0 |
| Размер кристалла, мм | 0.49 × 0.24 × 0.19 | 0.17 × 0.15 × 0.13 | 0.34 × 0.21 × 0.12 |
| Область сбора данных по θ, град | 6.24−68.98 | 6.00−50.12 | 6.55−56.99 |
| Интервалы индексов отражений | –16 ≤ h ≤ 16, –20 ≤ k ≤ 20, –24 ≤ l ≤ 24 |
–11 ≤ h ≤ 11, –17 ≤ k ≤ 17, –17 ≤ l ≤ 17 |
–13 ≤ h ≤ 13, –14 ≤ k ≤ 14, –14 ≤ l ≤ 14 |
| Измерено отражений | 57 080 | 53 254 | 30 583 |
| Rint | 0.0736 | 0.0484 | 0.0453 |
| Независимых отражений | 8434 | 7328 | 5465 |
| Переменных уточнения | 215 | 445 | 239 |
| GOOF | 1.010 | 1.027 | 1.108 |
| R-факторы по F 2 > 2σ(F 2) | R1 = 0.0450, wR2 = 0.0859 | R1 = 0.0261, wR2 = 0.0594 | R1 = 0.0401, wR2 = 0.0748 |
| R-факторы по всем отражениям | R1 = 0.1002, wR2 = 0.1056 | R1 = 0.0399, wR2 = 0.0654 | R1 = 0.0503, wR2 = 0.0792 |
| Остаточная электронная плотность (min/max), e/Å3 | 1.95/–3.39 | 0.81/–0.94 | 2.04/–1.46 |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Синтез комплексов I–III осуществляли взаимодействием бромидов органилтрифенилфосфония с гексабромоплатинатом калия в ацетонитриле (мольное соотношении реагентов 2 : 1). Преимуществами данного метода синтеза являются одностадийность, высокий выход и чистота целевого продукта.
При испарении растворителя наблюдали образование красных кристаллов с выходом до 94%.
Известно, что поглощение связей P–CPh проявляется в интервале частот 1450–1435 cм–1 [19]. Так, в ИК-спектрах соединений I–III присутствуют полосы поглощения при 1436, 1434 и 1435 см–1, соответствующие колебаниям связей фосфор–углерод фенильных колец в катионах. В полученных спектрах наблюдаются полосы поглощения при 3058 (I), 3058 (II) и 3034 см–1 (III), которые отвечают колебаниям CAr–H и проявляются в области 3080–3030 см–1. Присутствуют также полосы поглощений, связанные с валентными колебаниями алкильных и алкенильных групп: –CH3 2971 (I), –СH2 2852, 1481 (II), 2865, 1481 (III), ‒CH=CH2 995 см–1 (III) [20].
Кристаллическая структура комплексов I–III состоит из тетраэдрических катионов и октаэдрических анионов. В катионах кристаллов I–III атомы углерода СAr и СR, связанные с фосфором, лежат в вершинах искаженного тетраэдра (рис. 1–3). Алкильная группа в катионах метилтрифенилфосфония I статиcтически разупорядочена по двум положениям. В структуре комплекса II присутствуют два типа кристаллографически независимых катионов [Ph3PCH=CH2]2+. Углы CPC отклоняются от теоретического значения: 108.4(3)°−111.4(2)° (I), 107.8(2)°−111.0(2)°, 106.8(2)°−111.3(2)° (II), 107.8(3)°−112.3(3)° (III). Длины связей P−CPh (1.788(5)−1.794(5) Å (I), 1.792(5)−1.797(5), 1.799(5)−1.804(5) Å (II), 1.786(6)−1.792(6) Å (III)) равнозначны, как и расстояния P−CR (1.800(6) Å (I), 1.776(5), 1.781(5) Å (II), 1.792(6) Å (III)). Геометрические параметры совпадают со значениями аналогичных фосфониевых катионов [21–25]. Центральный атом платины координирует шесть атомов брома, которые образуют октаэдр. В анионах всех исследованных комплексов атомы платины находятся в частных позициях – координаты платины совпадают с координатами центра инверсии, из-за этого октаэдрический фрагмент симметричен. В октаэдрических анионах транс-углы BrPtBr равны теоретическому значению (180.0° (I); 180.0° (II), 180.0° (III)), цис-углы составляют 89.52(4)°−90.48(4)° в I, 89.36(7)°−90.64(7)°, 88.90(6)°−91.10(6)° в II, 89.32(6)°−90.68(6)° в III. Связи Pt−Br сопоставимы по длине и составляют 2.4626(11)−2.4694(12) Å в I, 2.4688(18)−2.4721(19), 2.458(2)−2.4638(18) Å в II, 2.4621(18)−2.4655(18) Å в III, что меньше суммы ковалентных радиусов атомов платины и брома (2.56 Å [26]).
Рис. 1.
Геометрия катиона и аниона в комплексе I, атомы показаны в виде эллипсоидов тепловых колебаний с вероятностью 40%.
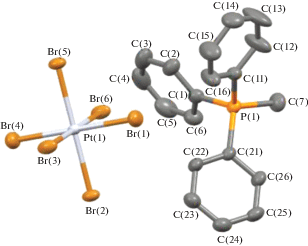
Рис. 2.
Геометрия катиона и аниона в комплексе II, атомы показаны в виде эллипсоидов тепловых колебаний с вероятностью 40%.
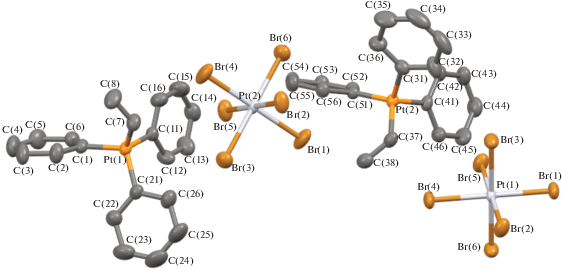
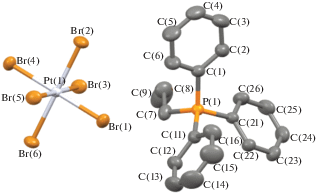
Рис. 3.
Геометрия катионов и анионов в комплексе III, атомы показаны в виде эллипсоидов тепловых колебаний с вероятностью 40%.
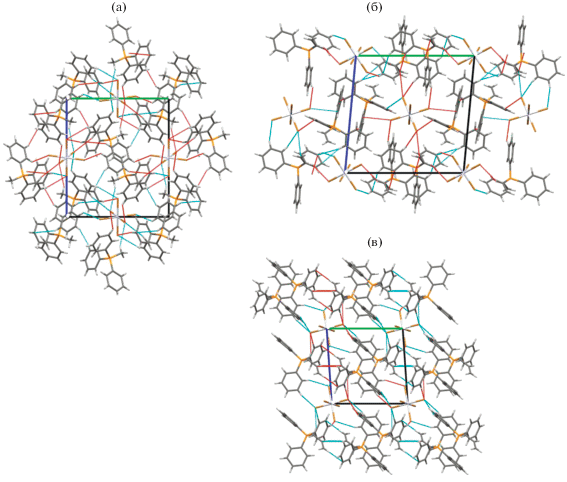
В кристаллах комплексов I–III присутствуют слабые водородные связи Br…H–C (2.964–3.033, 2.863–2.913, 2.908–3.010 Å) (рис. 4). Каждый катион в I и III имеет короткие контакты с четырьмя анионами, а в II – с двумя анионами. В кристаллах I и III в цепочках из катионов присутствуют короткие контакты H…H (2.26 Å). Анионные цепочки Br…Br в кристаллах отсутствуют, возможно, из-за большого размера фосфониевых катионов.
Список литературы
Wheate N.J., Walker S., Craig G.E., Oun R. // Dalton Trans. 2010. V. 39. P. 8113. https://doi.org/10.1039/C0DT00292E
Galanski M., Keppler B.K. // Anti-Cancer Agents Med. Chem. 2007. V. 7. P. 55. https://doi.org/10.2174/187152007779314017
Petruzzella E., Sirota R., Solazzo I. et al. // Chem. Sci. 2018. V. 9. P. 4299.
Li Z., Chen Y., Zhifang Liu Z. // Monatshefte für Chemie – Chemical Monthly. 2020. V. 151. P. 353. https://doi.org/10.1007/s00706-020-02561-1
Lakomska I., Wojtczak A., Sitkowski J. et al. // Polyhedron. 2008. V. 27. P. 2765. https://doi.org/10.1016/j.poly.2008.05.032
Alvarado-Soto1 L., Ramirez-Tagle R. // J. Struct. Chem. 2020. V. 61. № 5. P. 688. https://doi.org/10.1134/S0022476620050030
Zhao J., Chen F., Han Y. et al. // Molecules. 2018. V. 23. P. 1397. https://doi.org/10.3390/molecules230613972018
Tkacheva A.R., Sharutin V.V., Sharutina O.K. et al. // Russ. J. Gen. Chem. 2020. V. 90. № 4. P. 1. [Ткачёва А.Р., Шарутин В.В., Шарутина О.К. и др. // Журн. общ. химии. 2020. Т. 90. № 4. С. 599.]https://doi.org/10.1134/S1070363220040155
Elmali A., Elerman Y., Eren G. et al. // Z. Naturforsch., B: Chem. Sci. 2005. V. 60. P. 164. https://doi.org/10.1515/znb-2005-0206
Bell K.J., Westra A.N., Warr R.J. et al. // Angew. Chem., Int. Ed. 2008. V. 47. P. 1745.
Hu J.J., Li F., Hor T.S. // Organomet. Chem. 2009. V. 28. P. 1212. https://doi.org/10.1021/om800978j
Kim N., Ha K. // Z. Kristallogr. - New Cryst. Struct. 2010. V. 225. P. 37. https://doi.org/10.1524/ncrs.2010.0014
Ha K. // Z.Kristallogr. – New Cryst. Struct. 2013. P. 228.
Rosokha S.V., Kumar A. // J. Mol. Struct. 2017. V. 1138. P. 129. https://doi.org/10.1016/j.molstruc.2017.03.0090022-2860
Yoshida T. // CSD Commun. (Priv. Commun.) 2016.
SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc. 1998. Madison, Wisconsin, USA.
SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc. 1998. Madison, Wisconsin, USA.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Crystallogr. 2009. V. 42. P. 339. https://doi.org/10.1107/S0021889808042726
Преч Э., Бюльцманн Ф., Аффольтер К. Определение строения органических соединений М.: Мир, 2006.
Тарасевич Б.Н. ИК спектры основных классов органических соединений. М.: Изд-во Моск. ун-та, 2012.
Kuznetsov M.L., Bokach N.A., Kukushkin V.Yu. et al. // J. Chem. Soc., Dalton Trans. 2000. № 24. P. 4683.
Шарутин В.В., Сенчурин В.С., Шарутина О.К. // Вестник ЮУрГУ. 2011. Т. 6. № 33.
Li H.H., Chen Z.R., Wang C. et al. // Chin. J. Struct. Chem. 2005. V. 24. P. 1318.
Tkacheva A.R., Sharutin V.V., Sharutina O.K., Slepukhin P.A. // Russ. J. Gen. Chem. 2019. V. 89. № 9. P. 1816. [Ткачёва А.Р., Шарутин В.В., Шарутина О.К., Слепухин П.А. // Журн. общ. химии. 2019. Т. 89. № 9. С. 1414.]https://doi.org/10.1134/S1070363219090147
Sharutin V.V., Sharutina O.K., Senchurin V.S., Andreev P.V. // Russ. J. Inorg. Chem. 2018. V. 63. № 9. P. 1178. [Шарутин В.В., Шарутина О.К., Сенчурин В.С., Андреев П.В. // Журн. неорган. химии. 2018. V. 63. № 9. С. 1153.]https://doi.org/10.1134/S0036023618090188
Cordero B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. V. 21. P. 2832. https://doi.org/10.1039/B801115J
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии