Микроэлектроника, 2019, T. 48, № 1, стр. 3-15
Атомно-слоевoе осаждение Y2O3 с использованием трис(бутилциклопентадиенил)иттрия и воды
А. И. Абдулагатов 1, Р. Р. Амашаев 1, Кр. Н. Ашурбекова 1, Ш. М. Рамазанов 1, Д. К. Палчаев 1, А. М. Максумова 1, М. Х. Рабаданов 1, И. М. Абдулагатов 1, *
1 Дагестанский государственный университет
367000 г. Махачкала, ул. Гаджиева, д. 43-а, Россия
* E-mail: ilmutdina@gmail.com
Поступила в редакцию 20.05.2018
После доработки 20.05.2018
Принята к публикации 20.05.2018
Аннотация
Получены пленки оксида иттрия (Y2O3) методом атомно-слоевого осаждения (АСО) с использованием трис(бутилциклопентадиенил)иттрия (Y(CpBut)3) и H2O. Прекурсор иттрия показал термическую стабильность и высокую реакционную способность в поверхностных реакциях с H2O. In situ мониторинг процесса осаждения методом кварцевого пьезоэлектрического микровзвешивания (КПМ) показал, что рост оксида сопровождается абсорбцией воды в толщу пленки, которая может привести к процессам по типу химического осаждения из газовой фазы (ХОГФ). Снижение объема напускаемой воды и увеличение времени продувки в АСО-цикле позволили снизить эффект ХОГФ. Толщина Y2O3 пленки, приходящаяся на один АСО-цикл (постоянная роста), при температуре 230°С менялась в зависимости от количества циклов и имела максимальное значение равное 1.7 Å/цикл. Покрытия, полученные при 230°С, имели поликристаллическую кубическую структуру и среднюю плотность 96% от объемной плотности Y2O3. Метод рентгеновской фотоэлектронной спектроскопии (РФС) показал, что содержание примесей углерода в пленке ниже предела чувствительности инструмента (~0.2 ат. %). С помощью спектроскопии резерфордовского обратного рассеивания (СРОР) было получено отношение атомной концентрации О/Y равное ~1.58. Полученные пленки Y2O3 имели показатель преломления света равный 1.85 (при 632.8 нм), а с защитной пленкой АСО Al2O3 эта величина составляла 1.73.
ВВЕДЕНИЕ
Благодаря уникальной комбинации диэлектрических, оптических и термических свойств оксид иттрия и его сплавы в течение уже многих лет являются предметом исследований. Оксид иттрия имеет высокое значение диэлектрической проницаемости равное 10 [1], широкий диапазон оптической передачи 0.25–8 мкм [2] и высокую температуру плавления ~2439°C [1, 3]. В связи с близостью параметров кристаллической решетки и высокой химической совместимостью с кремнием, Y2O3 рассматривался как материал, способный потенциально заменить оксид кремния в качестве диэлектрического затвора в транзисторах [4, 5]. Пленки Y2O3 успешно опробованы в металл–изолятор–металл (МИМ) устройствах [6, 7]. Была продемонстрирована перспективность применения данного материала в качестве диэлектрика в электронных устройствах на основе графена и карбоновых нанотрубок [8]. Он также использовался в качестве волновода в оптических устройствах [9, 10], как буферный слой для сверхпроводников [11, 12] и как высокотемпературное защитное покрытие [13, 14].
Пленки Y2O3 осаждаются как газофазными, так и жидкофазными методами. Как правило процессы нанесения пленок из паровой фазы включают в себя различные модификаци методов физического осаждения из газовой фазы (ФОГФ) [15, 16] или химического осаждения из газовой фазы [17, 18]. Несмотря на то, что этими методами можно получать высококачественные пленки, низкий уровень контроля толщины покрытий и высокие температуры осаждения являются их существенными недостатками. С относительно недавних пор стало возможным осаждать оксид иттрия методом атомно-слоевого осаждения. Под названием “молекулярное наслаивание”, этот метод был разработан в начале шестидесятых годов прошлого столетия научной школой член-корр. АН СССР Валентина Борисовича Алесковского [19]. В отличие от других газофазных методов, в АСО рост пленок осуществляется “снизу–вверх” посредством повторяющихся, самоограничивающихся поверхностных реакций. Эта особенность позволяет равномерно покрывать наноструктурированные подложки и дисперсные материалы с контролем толщины на уровне Ангстрема [20].
В предыдущих работах по термическому АСО Y2O3 осаждение достигалось с использованием следующих типов прекурсоров иттрия: β-дикетонат – трис(2,2,6,6-тетраметил-3,5-гептандион)иттрия (Y(thd)3) [4, 21–23], Y(thd)3(бипиридил) [23], Y(thd)3(1,10-фенантролин) [23]; циклопентадиенил – трис(циклопентадиенил)иттрий (YCp3) [24], трис(метилциклопентадиенил)иттрий (Y(CpMe)3) [24], трис(этилциклопентадиенил)иттрий (Y(CpEt)3) [25]; трис(изопропилциклопентадиенил)иттрий (Y(iPrCp)3) [26], ацетамидинат – трис(N,N'-диизопропилацетамидинат)иттрия (Y(iPr2amd)3) [27], трис(N,N'-диизопропил-2-диметиламино-гуанидинато) (Y(DPDMG)3) [28], а также комбинация циклопентадиенил и ацетамидината (iPrCp)2Y(iPr-amd) [29–31]. В этих экспериментах О2, озон (О3), радикалы кислорода или H2O использовались в качестве прекурсоров кислорода. Низкая реакционная способность β-дикетонатов иттрия, используемых в сочетании с О2 [22], О3 [4, 22, 23] и кислородными радикалами [21], приводит к осаждению пленок с относительно высоким содержанием примесного углерода (>1 ат. %). Прогресс в осаждении АСО пленок Y2O3 был достигнут благодаря применению циклопентадиенил [24, 25] и ацетамидинат [27] прекурсоров в сочетании с H2O, где уровень примесей углерода был ≤0.5 ат. %. В последнее время значительное внимание уделялось прекурсору с гетеролитическими лигандами (iPrCp)2Y(iPr-amd), так как этот реагент находится в жидком состоянии при комнатной температуре и при нагревании обладает высоким давлением паров [29, 30, 32]. Однако при схожих режимах осаждения, используя (iPrCp)2Y(iPr-amd) и H2O, исследователями были получены не согласующиеся данные по содержанию примесей углерода. Так, в одном случае сообщалось о содержании примесей углерода ниже чувствительности РФС (0.5–1 ат. %) [29, 30], а в другом ~3.7 ат. % [31]. Применение О3 вместо H2O с (iPrCp)2Y(iPr-amd) привело к увеличению содержания углерода до ~5.6 ат. % [31]. Присутствие углерода указывает на неидеальность протекающих на поверхности химических реакций. В процессах с использованием озона, из-за его высокой окислительной способности, между осаждаемой пленкой и кремниевой подложкой, может образоваться слой SiOx или/и силиката иттрия с низким коэффициентом диэлектрической проницаемости [4, 26, 33]. В целом, циклопентадиениловые (Cp) реагенты демонстрируют более подходящую химию поверхности. Процессы АСО Y2O3 с использованием Cp прекурсоров иттрия оставляют за собой минимальное количество примесей углерода и показывают относительно высокие темпы роста в пределах 1.2–1.8 Å/цикл [24–26].
В данной работе был изучен процесс АСО Y2O3 с использованием трис(бутилциклопентадиенил)иттрия (Y(CpBut)3) и воды. Y(CpBut)3 является привлекательным, коммерчески доступным реагентом поскольку находится в жидком состоянии при комнатной температуре. Жидкие прекурсоры обладают более высокой летучестью и реакционной способностью по сравнению с другими прекурсорами иттрия, находящимися в твердом состоянии [29]. Предлагаемая схема осаждения АСО Y2O3, состоящая из двух А–Б поверхностных реакций, представлена ниже.
где скобками обозначена поверхность, x – доля лигандов оставшихся после дозирования прекурсоров, а HCpBut – побочный продукт поверхностных реакций (обозначено произвольно). В отличие от ранее опубликованных работ по АСО Y2O3, данный процесс АСО был исследован в режиме реального времени (in situ) с использованием кварцевого пьезоэлектрического микрорезонатора (КПМ). Это позволило детально изучить механизм роста пленки Y2O3. В частности, с помощью КПМ была обнаружена абсорбция H2O в толщу осаждаемой пленки. Данные мониторинга роста пленки позволили оптимизировать процесс осаждения для минимизации негативных последствий данного эффекта. В данной работе впервые демонстрируется АСО Y2O3 с использованием Y(CpBut)3 и воды. На основании полученных экспериментальных данных был предложен примерный механизм осаждения пленки.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
АСО пленки Y2O3 осаждались на оборудовании компании АСО НаноТех (г. Махачкала, Россия). Установка снабжена вакуумной камерой с горячими стенками, куда натекает вязкий поток инертного газа. В качестве газа-носителя использовался азот ультравысокой чистоты (УВЧ, 99.999%). В процессе АСО давление N2 в реакторе поддерживалось на уровне ~1.0 Торр. Чистота Y(CpBut)3 (CAS номер 312739-77-8, Sigma-Aldrich) составляла 99.9%. Вода использовалась хроматографического класса чистоты. Из-за чувствительности прекурсора иттрия к кислороду и влаге его загружали в контейнер для напуска в перчаточном пакете в атмосфере УВЧ N2. Для создания достаточного давления паров, Y(CpBut)3 нагревали в барботере из нержавеющей стали до температуры 170°C. Прекурсор дозировался путем перенаправления части потока газа-носителя через барботер. Контейнер с водой находился при комнатной температуре. Перед началом процесса реагенты подвергались дегазации.
Оборудование, использованное для КПМ-мониторинга, было схоже с тем, что использовалось в других работах [34]. Разрешение КПМ по массе составляет примерно 0.3 нг/см2. До начала АСО Y2O3, КПМ сенсор покрывали в том же реакторе и при той же температуре пленкой АСО Al2O3, толщиной примерно 60 Å, для чего использовались триметилалюминий (97%, CAS номер 75-24-1, Sigma-Aldrich) и H2O. Осаждение Al2O3 проводилось для получения однородной, чистой поверхности. Погрешности для каждой из точек кривых насыщения прекурсора иттрия рассчитывались по стандартным отклонениям значений для 10–15 АСО-циклов.
В качестве подложек для осаждения Y2O3 использовали полированные с одной стороны кремниевые пластины Si 〈100 〉 размером 2.5 × 2.5 см. Подложки очищались ацетоном, изопропанолом, высушивались потоком УВЧ азота и выдерживались в реакционной камере до начала осаждения в течение ~30 минут. Все использованные пластины Si 〈100 〉 имели естественный слой оксида кремния толщиной ~20 Å.
Для определения толщины и показателя преломления полученных пленок использовали спектроскопический эллипсометр. Толщину измеряли при угле падения 75° для трех длин волн 418.5, 594.6 и 763.2 нм. Данные показателя преломления света определяли для диапазона длин волн от 418.5 до 754.7 нм. Представленные значения погрешности толщины АСО-пленок рассчитывались из значений толщины для трех образцов, напыляемых одновременно и расположенных по направлению потока газа на расстоянии примерно 1 см друг от друга. Показатель преломления определяли фиксацией в модели точных данных по толщине пленки АСО Y2O3 и подслоев, полученных методом отражения рентгеновских лучей (ОРЛ).
Данные отражения и дифракции рентгеновских лучей (ОРЛ и ДРЛ) были получены с помощью дифрактометра высокого разрешения с рентгеновской медной трубкой, работающей при λ = 1.54 Å и током нити 40 мА. ОРЛ анализ использовался для определения плотности, поверхностной среднеквадратичной шероховатости и толщины полученных Y2O3 пленок. Для ДРЛ анализа образцы держали при ω = 1°, а сканирование детектором проводили от 25° до 60° (2θ). ДРЛ измерения проводились для определения кристаллической структуры и размера зерен пленок Y2O3.
Данные рентгеновской фотоэлектронной спектроскопии были получены с использованием монохроматического AlKα рентгеновского источника (1486.6 эВ) с возможностью распыления Ar+. Энергия ионов аргона при травлении составляла примерно 1.5 кэВ. Фотоэлектроны собирали с помощью полусферического анализатора. Данные РФС позволили определить состав и уровень примесей углерода в пленках.
Метод спектроскопии резерфордовского обратного рассеивания использовался для определения отношения концентрации атомов кислорода и иттрия в полученных пленках. Анализ проводился на оборудовании RBS 400 компании Analytical endstation (США). Энергия ионов 4He+ составляла 2 MэВ, а угол падения 165°.
Время введения прекурсоров в камеру и их продувки обозначены как t1/t2/t3/t4, где t1 – время напуска Y(CpBut)3, t3 – время напуска H2O и t2, t4 – время продувки после напуска первого и второго реагентов, в секундах.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
А) Результаты КПМ мониторинга и оптимизация АСО Y2O3
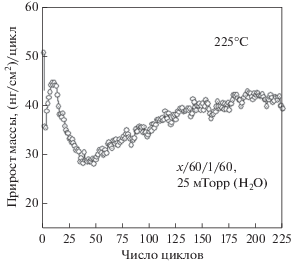
На рис. 1 представлены данные изменения прироста массы, приходящиеся на один АСО цикл Y2O3, в процессе осаждения пленки на аморфном Al2O3, предварительно нанесенном на кристалл КПМ. Осаждение проводилось при 225°С с временем напуска и продувки реагентов в цикле 1/60/1/60. Парциальное давление Y(CpBut)3 при напуске через барботер в течение 1с составляло 300 мТорр, а H2O – примерно 25 мТорр. Как видно из рис. 1, процесс осаждения начинается значительным приростом массы на первом АСО циклe Y2O3 (50.6 нг/см2). Предположительно, относительно высокая концентрация поверхностных (–OH) групп аморфного АСО Al2O3 [35] способствует эффективной реакции Y(CpBut)3 с поверхностью. Данное поведение характерно для “поверхностно-стимулированного” механизма нуклеации АСО пленок [36]. Однако он быстро сменяется на тип-2 “поверхностно-ингибированный” механизм характерный для процессов осаждения поликристаллических пленок [37]. На третьем цикле система проходит через первый локальный минимум. Период роста от первого локального минимума до максимума характеризуется ростом островков оксида и их разрастанием в сплошную пленку [38]. Чем выше плотность нуклеационных зародышей, тем меньше АСО циклов требуется для достижения локального максимума [39]. Через 40 циклов процесс проходит через второй минимум и после примерно 200 циклов прирост массы стабилизируется на уровне ~42.3 нг/см2 за цикл. Появление второго локального минимума ранее объясняли разницей в темпах роста различных кристаллографических плоскостей зародышей [37]. После прохождения второго минимума выход на линейный рост потребовал значительного количества циклов.
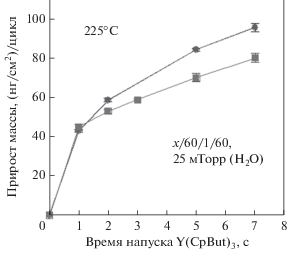
После стабилизации прироста массы за цикл были проведены эксперименты по определению самоограничиваемости реакции Y(CpBut)3 с поверхностными гидроксильными группами (реакции А). На рис. 2 представлены КПМ данные двух попыток установления зависимости прироста массы, приходящейся на один цикл, от времени напуска Y(CpBut)3. Данные были получены при параметрах цикла х/60/1/60, где х – изменяемое время напуска Y(CpBut)3 при фиксированном времени напуска H2O, равное 1 с. При этом парциальное давление при напуске воды составляло ~25 мТорр, что соответствует 25 × 103 L (1 L = 1 × 10–6 Торр с). Из рис. 2 видно, что с увеличением времени напуска Y(CpBut)3 прирост массы не достигал насыщения, это говорит о не самоограничивающемся характере поверхностной реакции, т.е. не выполняется одно из ключевых условий проведения АСО процесса. Данный результат мотивировал к более детальному изучению процессов, происходящих при осаждении пленки.
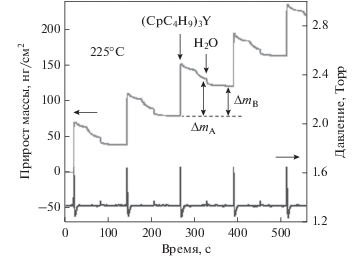
На рис. 3 приведен сигнал КПМ, наблюдаемый в результате поочередного напуска Y(CpBut)3 и H2O в процессе АСО Y2O3, который проводили с использованием параметров цикла 1/60/1/60 при температуре 225°C. Данные были получены на начальном этапе (первые 15 циклов) роста пленки. Как видно из рисунка, напуск Y(CpBut)3 ведет к приросту массы, а напуск воды к ее потере. Это происходит в соответствии с предложенным выше механизмом осаждения АСО Y2O3, где напуск Y(CpBut)3 приводит к росту массы (реакция А), а замена поверхностных CpBut лигандов на гидроксильные группы (реакция Б) – к ее снижению. Прирост массы после напуска Y(CpBut)3 составлял 51 нг/см2 (ΔmA), а потеря массы после H2O – примерно 7 нг/см2, с общим приростом в 44 нг/см2 (ΔmB). При этом, на шаге продувки Y(CpBut)3 происходит значительное снижение массы, что связано с потерей лигандов в результате поверхностной рекомбинации, причем эти процессы возможно проходят в два этапа.
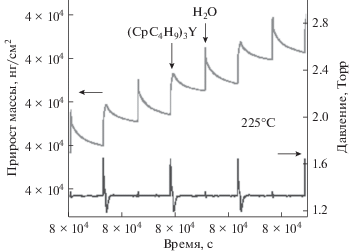
Рис. 4 иллюстрирует сигнал КПМ после примерно 500 АСО циклов при параметрах цикла 8/60/1/60. Если напуск воды на начальном этапе осаждения Y2O3 приводил к потере массы (рис. 3), то с увеличением количества АСО-циклов, потеря массы сменилась ее ростом. Данное поведение объясняется абсорбцией воды в толщу осаждаемой пленки, что выражается резким скачком массы во время напуска и последующей диффузией воды из пленки на этапе продувки. Как видно из рисунка, на стадии продувки вода удаляется не полностью (масса не стабилизировалась). В результате каждый последующий напуск Y(CpBut)3 реагирует в газовой фазе с диффундирующей из пленки водой, что приводит к эффекту химического осаждения из газовой фазы, а значит и к неконтролируемому росту пленки. Процесс абсорбции воды постепенно начинался уже на стадии нуклеации пленки и усиливался с увеличением толщины пленки.
В ранних работах по термическому АСО Y2O3, с использованием Y(iPr2amd)3 и H2O, также упоминается влияние абсорбции H2O на процесс осаждения [27]. Однако никаких подтверждающих данный эффект экспериментальных результатов авторами предоставлено не было. При этом авторами отмечалась необходимость продолжительной продувки после напуска воды для ее полной десорбции до напуска прекурсора иттрия [27]. Отсюда следует, что абсорбция воды происходит вне зависимости от типа прекурсора иттрия и связана со свойствами самой пленки. Известно, что Y2O3 может реагировать с H2O с образованием оксигидроокиси (YOOH) и гидроксидa иттрия (Y(OH)3) даже при комнатной температуре [40]. Это связывают прежде всего с тем, что оксид иттрия химически активен и обладает основными свойствами [40, 41]. В кристаллической решетке Y2O3 имеются присущие ему дефекты в виде кислородных вакансий и дислокаций [42]. Эти дефекты могут служить центрами разложения H2O. По одному из механизмов, при диссоциативном растворении молекулы воды, кислород заполняет вакансии в кислородной подрешетке, а протоны локализуются в позициях вблизи ионов кислорода, образуя центры (OH)− [43]. При этом протонирование оксида иттрия ведет к модификации его электрических свойств [44]. Интересно, что термохимические расчеты указывают на то, что протекание реакции по схеме Y 2O3 + 3H2O(г) → 2Y(OH)3 ($\Delta {{G}_{{225^\circ {\text{C}}}}}$ = 9.45 ккал/мол) [45] является маловероятным. Другие оксиды редкоземельных металлов также обладают основными свойствами [46]. Один из таких примеров – реакция пленки оксида лантана (La2O3) с H2O с образованием гидроксида лантана в процессе термического АСО с использованием воды [47, 48]. Оксид иттрия обладает менее выраженными основными свойствами, чем оксид лантана [46], поэтому можно предположить, что удаление воды на стадии ее продувки в случае АСО Y2O3 будет более эффективным, чем для La2O3.
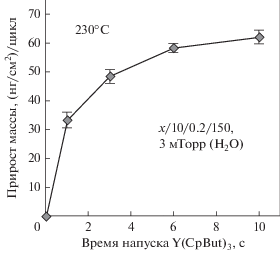
Во избежание осложнений, связанных с абсорбцией воды, дальнейший процесс АСО Y2O3 проводили с меньшей дозой напускаемой воды и большим временем ее продувки. На рис. 5 представлены КПМ данные повторного исследования зависимости прироста массы за цикл от времени напуска Y(CpBut)3. Эксперимент проводился при 230°С, где время напуска и продувки в цикле составляло х/10/0.2/150, х – изменяемое время напуска Y(CpBut)3, а 0.2 с – фиксированное время напуска H2O. Парциальное давление напускаемой воды при этом составляло 3 мТорр, что соответствует размеру дозы 6 × 102 Л. Этот объем более чем в 40 раз ниже объема воды, использованного в предыдущих экспериментах. Время продувки после напуска воды было продлено с 60 с до 150 с. Как видно из графика, с увеличением времени напуска Y(CpBut)3 происходит плавное насыщение поверхности.
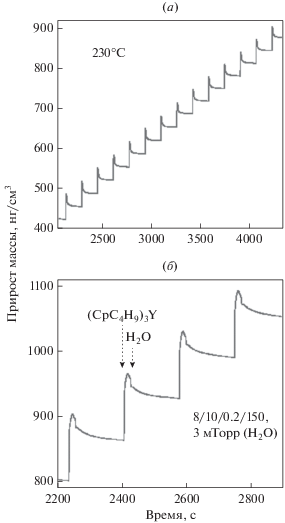
На рис. 6 представлены КПМ данные процесса осаждения Y2O3 при 230°С с использованием оптимальных параметров цикла 8/10/0.2/150. Длительный напуск реагента иттрия необходим для достижения полного насыщения поверхности реакцией гидроксильных групп и Y(CpBut)3. На рис. 6а показан сигнал КПМ, наблюдаемый после 350 циклов. Данные демонстрируют линейность роста пленки и высокую воспроизводимость процесса от цикла к циклу. Приближенный вид КПМ данных показан на рис. 6б. Здесь напуск Y(CpBut)3 приводит к увеличению массы на 102 нг/см2, а доза H2O – к ее снижению на 31 нг/см2, где результирующий прирост массы составляет 62 нг/см2 за цикл. Пик абсорбции воды на данном этапе не наблюдали, однако, он было заметным после примерно 500 АСО-циклов.
Рис. 6.
КМП-данные процесса АСО Y2O3: a – наблюдаемые на протяжении 14 циклов; б – приближенный вид 4-х циклов.
Используя данные рис. 3, где отношение ΔmB/ΔmA = 0.87 и рассчитанные из (A–Б) реакций атомные массы ΔmA(YO1.5) = 113 а. е. м. и ΔmB(Y(CpBut)3 – xHCpBut) = 452–122x, откуда находим, что х = 2.6. Получается, что доля CpBut лигандов, оставшихся после реакции (А), равна примерно 13.3%. Схожий результат был получен в другой работе, где проводился КПМ-мониторинг процесса АСО Y2O3 с использованием Y(CH3Cp)3 и H2O [49]. Согласно этим данным ~17% лигандов CH3Cp остаются на поверхности пленки после дозирования Y(CH3Cp)3 [49]. Различие в количестве остаточных лигандов после напуска Y(CH3Cp)3 и Y(CpBut)3 предположительно связано с разницей в размере лигандов и связанными с этим стерическими эффектами. Из приведенных данных можно предположить, что в результате реакции (А) на несколько атомов иттрия приходится один CpBut лиганд, т.е. осаждение протекает с частичным разложением прекурсора иттрия.
Б) Рост АСО Y2O3 пленки на кремниевой подложке
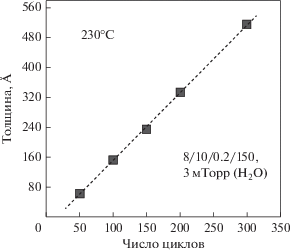
В представленных ниже данных, пленки оксида иттрия осаждались с оптимальным временем дозирования и продувки в цикле 8/10/0.2/150. Зависимость толщины пленки Y2O3, от числа АСО-циклов представлена на рис. 7. Осаждение проводилось при 230°С на кремниевой подложке Si 〈100 〉 со слоем естественного оксида кремния. Толщина пленок измерялась спектроскопическим эллипсометром. Данные рис. 7 указывают на характер роста пленки близкий к линейному с увеличением количества АСО-циклов. Расчеты постоянной роста, полученные отношением толщины к количеству АСО-циклов для каждой точки рис. 7, показали, что ее значение увеличивается от 1.4 до 1.7 Å/цикл при осаждении от 50 до 200 циклов соответственно. Выше 200 циклов постоянная роста не меняется. Увеличение постоянной роста с количеством циклов часто наблюдается при АСО-кристаллических пленок. Причина такого поведения системы может быть в длительном нуклеационном периоде, увеличении размера зерен и шероховатости с увеличением толщины пленки [50]. Разница по толщине между образцами, распложенными на расстоянии примерно 10 см друг от друга по направлению потока газа, после 300 АСО-циклов, составляла примерно 7.8%.
Рис. 7.
Зависимость толщины пленки Y2O3 от количества АСО циклов. Данные спектроскопического эллипсометра.
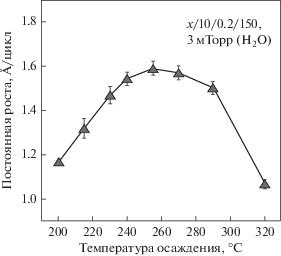
Зависимость постоянной роста от температуры осаждения исследовалась в пределах от 200 до 320°C. Полученные результаты представлены на рис. 8. В этом эксперименте на кремниевые подложки наносили по 50 циклов АСО Y2O3. При температуре 255°C постоянная роста достигла максимального значения в ~1.6 Å/цикл, в связи с чем данная температура может считаться оптимальной для АСО Y2O3 с использованием Y(CpBut)3 и H2O. Снижение постоянной роста при температуре выше 270°С может быть связано с уменьшением концентрации поверхностных реакционных групп в результате термического разложения прекурсора иттрия. Полученные значения постоянной роста близки к данным приведенным в научной литературе для термического АСО Y2O3, проводимого в диапазоне температур 225–300°С с использованием циклопентадиениловых прекурсоров YCp3/H2O (1.4–1.6 Å/цикл) [24], Y(CpMe)3/H2O (~1.3 Å/цикл) [24], Y(CpEt)3/H2O (1.7 Å/цикл) [25], Y(iPrCp)3/O3 (1.7 Å/цикл) [26]. Эти результаты говорят о том, что удлинение алкильной группы на Ср-лиганде не влияет заметным образом на реакционную способность прекусрсора иттрия, и соответственно, на постоянную роста. Полученные нами значения темпа роста пленки выше чем для АСО систем Y(thd)3/O3 (~0.23 Å/цикл) [23], Y(iPr2amd)3/H2O (0.8 Å/цикл) [27], (iPrCp)2Y(iPr-amd)/H2O (0.6 или 1.3 Å/цикл) [29, 31], (iPrCp)2Y(iPr-amd)/О3 (1.3 Å/цикл) [31], Y(DPDMG)3/H2O (1.3 Å/цикл) при их осаждении в интервале 225–350°С.
В) Анализ полученных АСО Y2O3 пленок (ОРЛ, ДРЛ, РФС, СРОР)
Плотность и среднеквадратичную шероховатость полученных покрытий Y2O3 определяли с помощью ОРЛ. Пленки, полученные осаждением при 230°C, имели плотность в пределах 93–98% от справочных данных для объемного Y2O3 (5.03 г/см3) [1]. Для сравнения, плотность АСО-пленок оксида иттрия, полученных с использованием Y(DPDMG)3 и H2O, в диапазоне температур от 175 до 250°C, варьироваться в пределах 83.5–87.5%. Полученная нами пленка толщиной 340 Å имела шероховатость 11.8 Å, а пленка толщиной 60 Å – чуть ниже 7 Å. Шероховатость пленки может варьироваться в зависимости от ее толщины и температуры осаждения [24]. Данные по шероховатости АСО Y2O3 пленок, полученные в других работах, значительно разнятся. Так, в одном случае пленки толщиной 500 Å, полученные при 250°С с использованием Y(CpEt)3/H2O, имели шероховатость 4 Å [25], а в другом случае при 280°С с использованием Y(iPr2amd)3/H2O – 28 Å [27]. Соответствие значений толщины пленок, полученных эллипсометрией было подтверждено методом ОРЛ.
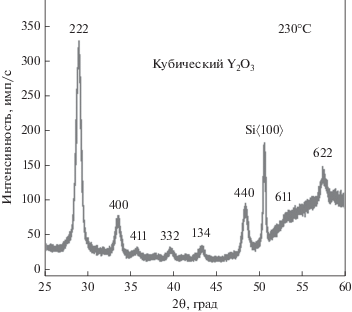
Кристаллическую структуру полученных пленок Y2O3 определяли методом дифракции рентгеновских лучей (ДРЛ). Дифрактограмма АСО пленки Y2O3 толщиной 455 Å, полученной при 230°С, приведена на рис. 9. До осаждения пленки Y2O3 на подложку предварительно наносили пленку АСО Al2O3 толщиной 48 Å. Расположение индексов Миллера и относительная интенсивность дифракционных линий совпадают со справочными данным для кубического поликристаллического Y2O3 (PDF-номер 88-5592, JCPDS-ICDD, 2002). На рис. 9 видно, что дифракционные линии кристаллографических плоскостей (222) и (440) имеют наибольшую интенсивность. Используя формулу Шеррер и данные полной ширины на уровне половинной амплитуды (FWHM) наиболее интенсивной дифракционной линии (222) рассчитан размер зерна равный примерно 11.2 нм. Пики кристаллического Y(OH)3, которые могли бы сформироваться как продукты реакции Y2O3 с водой, обнаружены не были. Кристаллическая структура полученной нами пленки совпадает с данными, представленными в других работах по термическому АСО Y2O3. Как правило, Y2O3 пленки полученные термическим АСО имеют кубическую структуру с преференциальными плоскостями роста (222), (400) и (440). Полученные нами пленки и с использованием YCp3/H2O или Y(CpEt)3/H2O при 250°С имели наиболее интенсивный пик (222), однако, в случае Y(CpMe)3/H2O получали пленки с наиболее интенсивным пиком (400) [24, 25]. При схожих температурных режимах осаждения, в отдельных случаях, пленки Y2O3, полученные с использованием О3, демонстрировали более низкую кристалличность в сравнении с АСО-системами, в которых использовалась вода [31]. Кубическая пленка оксида иттрия может потенциально применяться в оптике, поскольку поликристаллические материалы с иной кристаллической структурой демонстрируют большее рассеивание света [2].
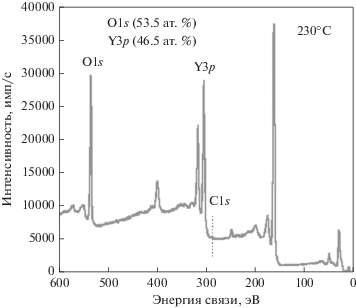
Элементный анализ полученной при 230°С пленки Y2O3 проводили с помощью рентгеновской фотоэлектронной спектроскопии. В связи с тем, что влага и углерод могут быть адсорбированы на поверхности Y2O3 пленки [27], РФС сканирование проводили после травления ионами аргона. На рис. 10 показан РФС спектр оксида иттрия толщиной ~150 Å после травления. Как видно из рисунка, на спектре отсутствует остовный пик углерода (C1s) с энергией связи ~285 эВ, что свидетельствует о содержании примесей углерода в пленке ниже чувствительности инструмента (~0.2 ат. %). Схожий результат был получен для пленок термического АСО Y2O3 с использованием YCp3, Y(CpMe)3 [24], Y(CpEt)3 [25], Y(iPr2amd)3 [27] в комбинации с H2O и для случая Y(iPrCp)3 с O3 [26] Использование гетеролитического регента (iPrCp)2Y(iPr-amd) и H2O в одном случае приводило к содержанию примесей углерода на уровне 3.7 ат. % [31], а в другом – ниже разрешения РФС-инструмента (0.5–1 ат. %) [29, 30]. Пленки, полученные с использованием Y(DPDMG)3/H2O имели примеси углерода и азота на уровне ~2 и ~3 ат. % [28], а в случае и Y(thd)3/O3 ~1.4 и ~0.2 ат. % [23] соответственно. Полученный нами результат еще раз демонстрирует, что с использованием Ср прекурсоров иттрия в комбинации с H2O можно получить пленки без примесей углерода. Во многих работах по термическому АСО Y2O3 были подробно исследованы РФС спектры высокого разрешения пиков иттрия (Y2p) и кислорода (O1s). В частности показанo раздвоение пика О1s, связанное с поверхностной гидроксилацией и присутствием поверхностных углеродных примесей [27]. Модификация поверхности происходит в результате контакта пленки Y2O3 с воздухом [10]. В данной работе также наблюдали раздвоение пика кислорода (данные не показаны). После примерно 4-х минут травления двойной пик кислорода постепенно перешел в остовый пик (О1s) с энергией связи соответствующей кислороду в Y2O3.
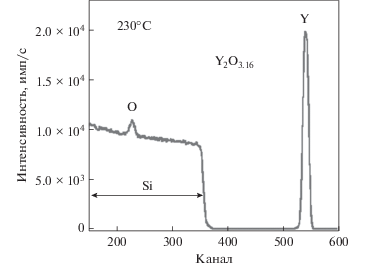
РФС анализ также позволил получить информацию о количественном содержании атомов иттрия и кислорода. После травления ионами аргона, концентрация атомов иттрия и кислорода была 44.1 и 55.9 ат. % соответственно. Отсюда, отношение O/Y равно 1.3, что ниже значения 1.5 для стехиометрического Y2O3. Схожее расхождение ранее наблюдалось при РФС анализe АСО Y2O3 покрытий, полученных с использованием Y(DPDMG)3/H2O, где отношение Y/O равнялось 1.24 [28]. Данное отклонение, скорее всего, связано с преференциальным травлением легких элементов ионами аргона [51]. Для более точного определения атомной концентрации элементов пленки использовали спектрометрию резерфордовского обратного рассеивания для чего выбрали пленку толщиной 520 Å полученной при 230°С. Спектр СРОР представлен на рис. 11. В данном случае отношение O/Y равнялось 1.58, что ближе к стехиометрическому значению. СРОР анализ пленок АСО Y2O3 полученных с использованием Y(iPr2amd)3/H2O [27] и Y(DPDMG)3/H2O [28] также показал избыток кислорода на ~33% от стехиометрического. Повышенное содержание кислорода объясняется присутствием физисорбированной воды и/или поверхностного слоя гидроксида иттрия, который образуется в результате контакта с воздухом [10]. В соответствии с РФС-данными, в СРОР-спектре также отсутствует пик примесей углерода.
Г) Оптические свойства АСО Y2O3 пленки
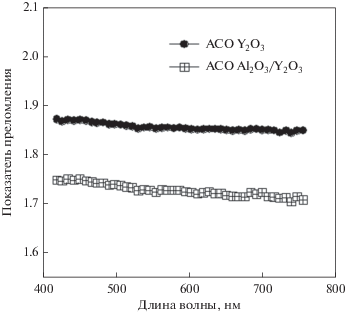
Данные зависимости показателя преломления света (n) от длины волны для полученной нами пленки АСО Y2O3 представлены на рис. 12. На данном рисунке также представлены данные оптических свойств АСО Y2O3 с защитным АСО покрытием Al2O3. Пленки осаждались при 230°С с использованием времени напуска и продувки 8/10/0.2/150 для АСО Y2O3 и 1/25/1/25 – для АСО Al2O3. ОРЛ данные для толщины пленок использовались при моделировании их оптических свойств. Пленка АСО Y2O3 толщиной 335.7 Å, без защитного покрытия, имела показатель преломления ~1.85 (632.8 нм), что незначительно ниже справочных данных для объемного Y2O3 (1.93) [52]. Схожие значения показателя преломления были получены для АСО Y2O3, осажденных с использованием Y(iPrCp)3/O3 (1.77) [26], Y(iPr2amd)3/H2O (1.8, при 632.8 нм) [27], (iPrCp)2Y(iPr-amd)/H2O (<1.8, при 632.8 нм) [29]. Ранее отмечалось, что показатель преломления пленок Y2O3 зависит от метода их осаждения и, как правило, их значение на 2–10% ниже значений для объемного Y2O3 [53]. Увеличить показатель преломления АСО-пленок Y2O3 можно путем их высокотемпературного отжига (600–800°С) за счет увеличения их плотности и снижения содержания примесей. При этом необходимо учитывать, что пленка Y2O3 может реагировать с подложкой [26]. Оптические свойства поликристаллического Y2O3 во многом определяются отражением и рассеиванием света с его поверхности [2, 53]. Более того, абсорбция значительного количества воды на воздухе, или после обмакивания в воде, ведет к деградации оптических свойств Y2O3 в инфракрасной области спектра [53, 54]. В данной работе пленка АСО Al2O3 использовалась в качестве антиотражательного и защитного покрытия. Пленку АСО Al2O3 наносили в режиме in situ сразу после осаждения АСО Y2O3. Из ОРЛ анализа толщина полученной пленки Y2O3 составляла ~310 Å, а оксида алюминия – ~30 Å. Плотность пленки оксида иттрия была 93%. Как видно из рис. 12, присутствие оксида алюминия ведет к снижению показателя преломления в среднем на 7% в сравнении с образцом без покрытия Al2O3. Интересно, что эти данные хорошо согласуются с ранее опубликованными показателями преломления для Y2O3 в вакууме ~1.7 (580 нм) [15, 55]. Полученный результат говорит о том, что тонкая АСО Al2O3 пленка эффективно снижает влияние рассеивания и абсорбированной воды на оптические свойства АСО Y2O3. Показатель поглощения света (k) пленки Y2O3 как с покрытием Al2O3, так и без него, в измеренной области длины волны, равнялся нулю.
ЗАКЛЮЧЕНИЕ
АСО кристаллических Y2O3 пленок с постоянной роста 1.7 Å/цикл было продемонстрировано с использованием Y(CpBut)3 и H2O. In situ мониторинг процесса при 230°С позволил определить период нуклеации пленки Y2O3 на Al2O3, а также наблюдать побочный процесс абсорбции воды. Абсорбция воды усиливалась с увеличением толщины пленки, что приводило к неконтролируемому осаждению Y2O3 по типу ХОГФ. Для достижения самоограничивающейся поверхностной реакции Y(CpBut)3 потребовалось снижение объема напускаемой воды и ее длительная продувка. Необходимость контроля напуска воды говорит о затруднительности проведения процесса в самоограничивающемся режиме по воде. Возможно, что для осаждения относительно тонких пленок размер дозируемой воды не критичен. Полученные результаты указывают на важность in situ мониторинга АСО процессов, в особенности при осаждении оксидов редкоземельных металлов, проводимых с использованием H2O. Несмотря на наблюдаемые побочные процессы в ходе осаждения, Y(CpBut)3 показал высокую реакционную способность в поверхностных реакциях с H2O, что позволило получить высококачественные АСО Y2O3 пленки при 230°С с содержанием примесей углерода ниже чувствительности РФС. Оптимальной температурой осаждения пленки является 255°С, где постоянная роста имеет максимальное значение. Было также продемонстрировано, что осаждение пленки Al2O3 является эффективным способом снижения влияния рассеивания и поверхностной адсорбции воды на оптические свойства АСО Y2O3.
Список литературы
CRC Hand Book of Chemistry and Physics, 89th Edition. Ed. Lide D.R. CRC Press, Boca Raton, FL. 2008–2009.
Harris D.C. Durable 3–5 mu m transmitting infrared window materials // Infrared Physics & Technology. 1998. V. 39. № 4. P. 185–201.
Swamy V., Dubrovinskaya N.A., Dubrovinsky L.S. High-temperature powder x-ray diffraction of yttria to melting point // J. Materials Research. 1999. V. 14. № 2. P. 456–459.
Gusev E.P., Cartier E., Buchanan D.A., Gribelyuk M., Copel M., Okorn-Schmidt H., D’Emic C. Ultrathin high-K metal oxides on silicon: processing, characterization and integration issues // Microelectronic Engineering. 2001. V. 59. № 1–4. P. 341–349.
Wilk G.D., Wallace R.M., Anthony J.M. High-kappa gate dielectrics: Current status and materials properties considerations // J. Applied Physics. 2001. V. 89. № 10. P. 5243–5275.
Tsui B.Y., Hsu H.H., Cheng C.H. High-Performance Metal-Insulator-Metal Capacitors With HfTiO/Y2O3 Stacked Dielectric // Ieee Electron Device Letters. 2010. V. 31. № 8. P. 875–877.
Wu Y.H., Lin C.C., Hu Y.C., Wu M.L., Wu J.R., Chen L.L. High-Performance Metal-Insulator-Metal Capacitor Using Stacked TiO2/Y2O3 as Insulator // Ieee Electron Device Letters. 2011. V. 32. № 8. P. 1107–1109.
Wang Z., Xu H., Zhang Z., Wang S., Ding L., Zeng Q., Yang L., Pei T., Liang X., Gao M., Peng L.-M. Growth and Performance of Yttrium Oxide as an Ideal High-kappa Gate Dielectric for Carbon-Based Electronics // Nano Letters. 2010. V. 10. № 6. P. 2024–2030.
Huignard A., Aron A., Aschehoug P., Viana B., Théry J., Laurent A., Perrière J. Growth by laser ablation of Y2O3 and Tm : Y2O3 thin films for optical applications // J. Materials Chemistry. 2000. V. 10. № 2. P. 549–554.
Niu D., Ashcraft R.W., Parsons G.N. Water absorption and interface reactivity of yttrium oxide gate dielectrics on silicon // Applied Physics Letters. 2002. V. 80. № 19. P. 3575–3577.
Jollet F., Noguera C., Gautier M., Thromat N., Duraud J.P. Influence of Oxygen Vacancies on the Electronic-Structure of Yttrium-Oxide // J. American Ceramic Society. 1991. V. 74. № 2. P. 358–364.
Mui D., Martinez J.C., Wiehl L., Raitieri R., Adrian H. Alpha-Axis growth of ferroelectric SrBi2Ta2O9 thin films on silicon // Materials Letters. 2005. V. 59. № 10. P. 1243–1247.
Lu F.X.,Guo H.B., Guo S.B., He Q., Li C.M., Tang W.Z., Chen G.C. Magnetron sputtered oxidation resistant and antireflection protective coatings for freestanding diamond film IR windows. // Diamond and Related Materials. 2009. V. 18. № 2–3. P. 244–248.
Dukel’skii K.V., Evstrop’ev S.K. Forming protective nanosize Y(2)O(3) coatings on crystal phosphors // J. Optical Technology. 2008. V. 75. № 11. P. 737–740.
Atanassov G., Thielsch R., Popov D. Optical-Properties of TiO2, Y2O3 and CeO2 Thin-Films Deposited by Electron-Beam Evaporation // Thin Solid Films. 1993. V. 223. № 2. P. 288–292.
Matsumoto M., Yamaguchi N., Matsubara H. Low thermal conductivity and high temperature stability of ZrO2–Y2O3–La2O3 coatings produced by electron beam PVD // Scripta Materialia. 2004. V. 50. № 6. P. 867–871.
Bakovets V.V., Levashova T.M., Ratushnyak V.T., Bakhturova L.F. Chemical vapor deposition of Y2O3 films using Y(dpm)(3) // Inorganic Materials. 2002. V. 38. № 4. P. 371–373.
Pulver M., Nemetz W., Wahl G. CVD of ZrO2, Al2O3 and Y2O3 from metalorganic compounds in different reactors // Surface & Coatings Technology. 2000. V. 125. № 1–3. P. 400–406.
Malygin A.A., Drozd V.E., Malkov A.A., Smirnov V.M. From V. B. Aleskovskii’s “Framework” Hypothesis to the Method of Molecular Layering/Atomic Layer Deposition // Chemical Vapor Deposition. 2015. V. 21. № 10–12. P. 216–240.
George S.M. Atomic Layer Deposition: An Overview. // Chemical Reviews. 2010. V. 110. № 1. P. 111–131.
Van T.T., Chang J.P. Radical-enhanced atomic layer deposition of Y2O3 via a beta-diketonate precursor and O radicals // Surface Science. 2005. V. 596. № 1–3. P. 1–11.
Mölsä H., Niinistö L., Utriainen M. Growth of yttrium oxide thin films from β-diketonate precursor // Advanced Materials for Optics and Electronics. 1994. V. 4. № 6. P. 389–400.
Putkonen M., Sajavaara T., Johansson L.S., Niinistö L. Low-temperature ALE deposition of Y2O3 thin films from beta-diketonate precursors // Chemical Vapor Deposition. 2001. V. 7. № 1. P. 44–50.
Niinisto J., Putkonen M., Niinisto L. Processing of Y2O3 thin films by atomic layer deposition from cyclopentadienyl-type compounds and water as precursors // Chemistry of Materials. 2004. V. 16. № 15. P. 2953–2958.
Majumder P., Jursichb G., Kueltzob A., Takoudis C. Atomic layer deposition of Y2O3 films on silicon using tris(ethylcyclopentadienyl) yttrium precursor and water vapor // J. Electrochemical Society. 2008. V. 155. № 8. P. G152–G158.
Xu R.S., Selvaraj S.K., Azimi N., Takoudis C.G. Growth Characteristics and Properties of Yttrium Oxide Thin Films by Atomic Layer Deposition from Novel Y(iPrCp)(3) Precursor and O-3 // Atomic Layer Deposition Applications 8. 2012. V. 50. № 13. P. 107–116.
de Rouffignac P., Park J.S., R.G. Gordon. Atomic layer deposition of Y(2)O(3) thin films from yttrium tris(N,N'-diisopropylacetamidinate) and water // Chemistry of Materials. 2005. V. 17. № 19. P. 4808–4814.
Mai L.K., Boysen N., Subaşı E., de los Arcos T., Rogalla D., Grundmeier G., Bock C., Lu H-L., Devi A. Water assisted atomic layer deposition of yttrium oxide using tris(N,N'-diisopropyl-2dimethylamido-guanidinato) yttrium(III): process development, film characterization and functional properties // Rsc Advances. 2018. V. 8. № 9. P. 4987–4994.
Park I.S., Jung Y.C., Seong S., Ahn J., Kang J., Nohd W., Lansalot-Matrasd C. Atomic layer deposition of Y2O3 films using heteroleptic liquid (iPrCp)(2)Y(iPr-amd) precursor. // J. Materials Chemistry C. 2014. V. 2. № 43. P. 9240–9247.
Lee J.S., Kim W.H., Oh I.K., Kim M.K., Lee G., Lee C.W., Park J., Lansalot-Matras C., Noh W., Kim H. Atomic layer deposition of Y2O3 and yttrium-doped HfO2 using a newly synthesized Y(iPrCp)(2)(N-iPr-amd) precursor for a high permittivity gate dielectric // Applied Surface Science. 2014. V. 297. P. 16–21.
Seppälä S., Niinistö J., Blanquart T., Kaipio M., Mizohata K., Räisänen J., Lansalot-Matras C., Noh W., Ritala M., Leskelä M. Heteroleptic Cyclopentadienyl-Amidinate Precursors for Atomic Layer Deposition (ALD) of Y, Pr, Gd, and Dy Oxide Thin Films // Chemistry of Materials. 2016. V. 28. № 15. P. 5440–5449.
Kang J.H., Jung Y.C., Seong S., Taehoon L., Ahn J., Noh W., Park I.S. Structural, chemical, and electrical properties of Y2O3 thin films grown by atomic layer deposition with an (iPrCp)(2)Y(iPr-amd) precursor // Materials Science in Semiconductor Processing. 2017. V. 63. P. 279–284.
Lim B.S., Rahtu A., de Rouffignac P., Gordon R.G. Atomic layer deposition of lanthanum aluminum oxide nano-laminates for electrical applications // Applied Physics Letters. 2004. V. 84. № 20. P. 3957–3959.
Elam J.W., Groner M.D., George S.M. Viscous flow reactor with quartz crystal microbalance for thin film growth by atomic layer deposition // Review of Scientific Instruments. 2002. V. 73. № 8. P. 2981–2987.
Ott A.W., Klaus J.W., Johnson J.M., George S.M. Al3O3 thin film growth on Si(100) using binary reaction sequence chemistry // Thin Solid Films. 1997. V. 292. № 1–2. P. 135–144.
Elliott S.D. Improving ALD growth rate via ligand basicity: Quantum chemical calculations on lanthanum precursors // Surface & Coatings Technology. 2007. V. 201. № 22–23. P. 9076–9081.
Nilsen O., Karlsen O., Kjekshus A., Fjellvag H. Simulation of growth dynamics in atomic layer deposition. Part II. Polycrystalline films from cubic crystallites // Thin Solid Films. 2007. V. 515. № 11. P. 4538–4549.
Puurunen R.L., Vandervorst W. Island growth as a growth mode in atomic layer deposition: A phenomenological model // J. Applied Physics. 2004. V. 96. № 12. P. 7686–7695.
Wind R.W., Fabreguette F.H., Sechrist Z.A., George S.M. Nucleation period, surface roughness, and oscillations in mass gain per cycle during W atomic layer deposition on Al2O3 // J. Applied Physics. 2009. V. 105. № 7. P. 074309-1–074309-13.
Kuroda Y., Hamano H., Mori T., Yoshikawa Y., Nagao M. Specific adsorption behavior of water on a Y2O3 surface // Langmuir. 2000. V. 16. № 17. P. 6937–6947.
Kurushkin M., Kurushkin D. Acid–Base Behavior of 100 Element Oxides: Visual and Mathematical Representations // J. Chemical Education. 2018. V. 95. № 4. P. 678–681.
Zheng J.X., Ceder G., Maxisch T., Chim W.K., Choi W.K. Native point defects in yttria and relevance to its use as a high-dielectric-constant gate oxide material: First-principles study // Physical Review B. 2006. V. 73. № 10. P. 104101-1–104101-7.
Putilov L.P., Varaksin A.N., Tsidilkovski V.I. Defect formation and water incorporation in Y2O3 // J. Physics and Chemistry of Solids. 2011. V. 72. № 9. P. 1090–1095.
Norby T., Kofstad P. Direct-Current Conductivity of Y2O3 as a Function of Water-Vapor Pressure // J. American Ceramic Society. 1986. V. 69. № 11. P. 780–783.
HSC Chemistry // 2002. Outotec. P. Version 5.1.
Moeller T., Kremers H.E. The Basicity Characteristics of Scandium, Yttrium, and the Rare Earth Elements // Chemical Reviews. 1945. V. 37. № 1. P. 97–159.
Nolan M., Elliott S.D. Competing Mechanisms in Atomic Layer Deposition of Er2O3 versus La2O3 from Cyclopentadienyl Precursors // Chemistry of Materials. 2010. V. 22. № 1. P. 117–129.
Päiväsaari J., Dezelah C.L., Back D., El-Kaderi H.M., Heeg M.J., Putkonen M., Niinistöa L., Winter C.H. Synthesis, structure and properties of volatile lanthanide complexes containing amidinate ligands: application for Er2O3 thin film growth by atomic layer deposition // J. Materials Chemistry. 2005. V. 15. № 39. P. 4224–4233.
Elam J.W. Emerging Applications for ALD in Energy Technologies. ALD workshop at 8th International Conference on Atomic Layer Deposition // ALD – 2008. June 29–July 2, Bruges, Belgium. 2008.
Elam J.W., Martinson Alex B.F., Pellin M.J., Joseph T. Hupp J.T. Atomic layer deposition of In2O3 using cyclopentadienyl indium: A new synthetic route to transparent conducting oxide films // Chemistry of Materials. 2006. V. 18. № 15. P. 3571–3578.
Greene J.E., Klinger R.E., Barr T.L., Welsh L.B. Auger and X-Ray Photoelectron-Spectroscopy Studies of Preferential Sputtering in Y2O3-Doped ZrO2 Films // Chemical Physics Letters. 1979. V. 62. № 1. P. 46–50.
Nigara Y. Measurement of Optical Constants of Yttrium Oxide // Japanese J. Applied Physics. 1968. V. 7. № 4. P. 404–408.
Tropf W.J., Thomas M.E. Yttria (Y2O3) // Handbook of Optical Constants of Solids. Ed. Palik E.D. Academic Press. University of Maryland. 1991. V. 2. P. 1081–1098.
Bezuidenhout D.F., Pretorius R. The Optical-Properties of Evaporated Y2O3 Films // Thin Solid Films. 1986. V. 139. № 2. P. 121–132.
Arnon O., Chou T.J. Wide Band Measurement of the Refractive-Index of Optical Thin-Films during Their Deposition // Thin Solid Films. 1982. V. 91. № 1. P. 23–31.
Дополнительные материалы отсутствуют.
Инструменты
Микроэлектроника