Журнал физической химии, 2020, T. 94, № 8, стр. 1149-1152
Термодинамические свойства расплавов тройной системы Ag–Al–Yb
Л. А. Романова a, В. Г. Кудин b, *, В. С. Судавцова a, **, П. П. Левченко a, М. И. Иванов a
a Национальная академия наук Украины, Институт проблем материаловедения
Киев, Украина
b Киевский национальный университет имени Тараса Шевченко
Киев, Украина
* E-mail: dir@ipms.kiev.ua
** E-mail: sud.materials@ukr.net
Поступила в редакцию 16.10.2018
После доработки 11.04.2019
Принята к публикации 10.12.2019
Аннотация
Методом изопериболической калориметрии определены энтальпии смешения жидких сплавов системы Ag–Al–Yb вдоль двух лучевых сечений с постоянным соотношением атомных долей алюминия и серебра: 1) xAg/xAl = 0.46/0.54 при 1271 ± 1 K, 2) xAg/xAl = 0.19/0.81 при 1454 ± 5 K до xYb ∼ 0.2. Установлено, что расплавы изученной системы образуются с выделением небольшого количества теплоты (ΔНmin = –29 кДж/моль), а минимум ΔН приходится на средину концентрационного треугольника. С помощью “геометрических” и “аналитической” модели Редлиха–Кистера выполнены расчеты ΔН расплавов тройной системы Ag–Al–Yb из аналогичных данных для двойных граничных подсистем.
Сплавы двойных и тройных систем, содержащих алюминий, d- и f-металлы, склонны к аморфизации, обратимо поглощают водород, проявляют магнитные свойства. Поэтому для научно обоснованного получения сплавов, содержащих такие металлы, необходимо знать их термодинамические свойства в жидком состоянии, поскольку их получают путем непосредственного сплавления.
В настоящее время термодинамические свойства фаз большинства двойных систем исследованы довольно хорошо, однако, тройные и более сложные расплавы – изучены недостаточно. Это обусловлено тем, что исследование многокомпонентных систем является сложной задачей, так как требует большого количества материалов, времени и трудовых затрат.
Поэтому значительный практический интерес представляет возможность оценки термодинамических свойств тройных систем на основе аналогичных данных о граничных двойных системах. В настоящее время разработаны методы, которые позволяют в определенной степени решать эту задачу. Это позволяет существенно уменьшить количество экспериментов и выбрать двойные сплавы с оптимальным соотношением концентраций, в которые целесообразно вводить третий компонент.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для проведения расчетов термодинамических свойств расплавов тройных с использованием “геометрических” и “аналитической” модели необходима достоверная информация об аналогичных данных для граничных подсистем Ag–Al, Ag–Yb, Al–Yb.
Термодинамические характеристики жидких сплавов системы Al–Ag исследованы в широкой концентрационной области. Энтальпии смешения, определенные методом ЭДС [1, 2], а также с использованием адиабатического калориметра [3] согласуются между собой. Точность определения $\Delta H$ из температурной зависимости ЭДС не всегда является достаточно высокой. Предпочтительным, особенно при высоких температурах, является определение этой величины методом калориметрии. Поэтому для дальнейших расчетов тройной системы были взяты энтальпии смешения этой граничной подсистемы из работы [3].
Энтальпии смешения расплавов двойных систем Al–Yb и Ag–Yb исследованы нами ранее [4, 5]. Они являются умеренными отрицательными величинами, достигающими в минимуме близких значений –22.6 ± 0.5 (при xYb = 0.37 и Т = 1300–1463 K) и –21.5 ± 1.9 (при xAg = 0.55 и Т = 1300 K) кДж/моль соответственно.
Мы оценили энтальпии смешения расплавов тройной системы Ag–Al–Yb по моделям Колера [6], Тупа [7], Бонье–Кабо [8]. Оказалось, что последние два расчета примерно одинаковы, а по методу Колера немного отличаются ходом линий изоэнтальпий смешения жидких сплавов в центральной части концентрационного треугольника. Чтобы выяснить, какая из моделей наиболее точно описывает термодинамические свойства расплавов системы Ag–Al–Yb, мы изучили их термохимические свойства по двум лучевым сечениям с xAg/xAl = 0.46/0.54 (1271 ± 1 K) и xAg/xAl = = 0.19/0.81 (1454 ± 1) методом калориметрии.
Методика эксперимента заключалась в постепенном введении в двойной сплав (с заданным соотношением мольных долей алюминия и серебра) твердых образцов иттербия. Непосредственно перед сбросом в калориметрическую ванну образец находился при комнатной температуре в барабанном дозаторе. При добавлении образца в расплав регистрировали соответствующие термические кривые, связанные с нагреванием его до температуры опыта и растворением в расплаве. Парциальные энтальпии смешения иттербия рассчитывали по формуле:
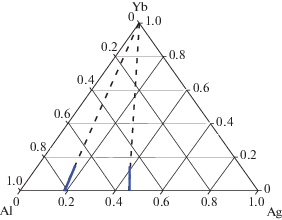
где K – коэффициент теплообмена калориметра, Si – площадь пика под термической кривой, $\Delta H_{{298}}^{{{{T}_{д}}}}$ – энтальпия нагревания одного моля образца от 298 K до температуры опыта Tд, ni – количество моль иттербия в образце. В каждом опыте калориметр калибровали сбрасыванием в тигель более тяжелого металла серебра в начале и эталонного вещества – молибдена в середине и конце опыта. Полученную зависимость коэффициента теплообмена (K) калориметра от массы расплава (рис. 1) использовали для дальнейших расчетов парциальных и интегральных энтальпий смешения жидких растворов. Для проведения исследований использованы алюминий марки АВОО (99.999%), серебро марки “ос. ч.” (99.99%) и иттербий (99.0%).Рис. 1.
Пример зависимости обратного коэффициента теплообмена калориметра от массы исследуемых сплавов.
Методом высокотемпературной калориметрии исследованы энтальпии смешения расплавов тройной системы Ag–Al–Yb вдоль двух лучевых сечений (рис. 2).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
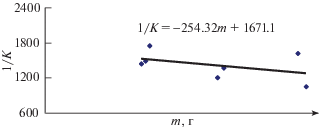
Результаты экспериментально изученных парциальных энтальпий смешения иттербия ($\Delta {{\bar {H}}_{{{\text{Yb}}}}}$) расплавов тройной системы Ag–Al–Yb приведены на рис. 3. Видно, что все расплавы образуются с выделением теплоты, а $\Delta \bar {H}_{{{\text{Yb}}}}^{\infty }$ = –159 ± 7 и –206 ± ± 8 кДж/моль соответственно, а при xYb > 0.6 $\Delta {{\bar {H}}_{{{\text{Yb}}}}}$ становятся небольшими положительными величинами. Погрешности изученных парциальных энтальпий смешения иттербия определяли из среднеквадратичных отклонений экспериментальных точек относительно сглаживающих кривых.
Рис. 3.
Парциальные энтальпии смешения иттербия в расплавах системы Ag–Al–Yb лучевых сечений с xAg/xAl = = 0.46/0.54 (а) и 0.19/0.81 (б).
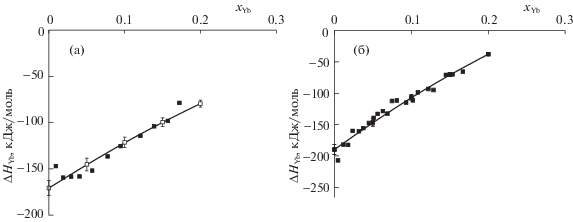
Образование жидких сплавов системы в исследованной области концентраций характеризуется отрицательными значениями интегральных энтальпий смешения (рис. 4). С увеличением содержания иттербия в тройном сплаве вдоль исследованного сечения наблюдается постепенное увеличение, а затем снижение значений $\Delta H$ по абсолютной величине. Минимальные значения энтальпий смешения расплавов для этих сечений равны –29.8 ± 0.2 и –27.2 ± 0.2 кДж/моль, соответственно, приходятся на состав xYb = 0.4.
Рис. 4.
Интегральные энтальпии смешения расплавов системы Ag–Al–Yb для лучевых сечений xAg/xAl = 0.46/0.54 (а) и 0.19/0.81 (б); 1 – экспериментальные данные при Т = 1271 (а) и 1454 (б), 2 – рассчитанные по модели Редлиха–Кистера с L = –250.
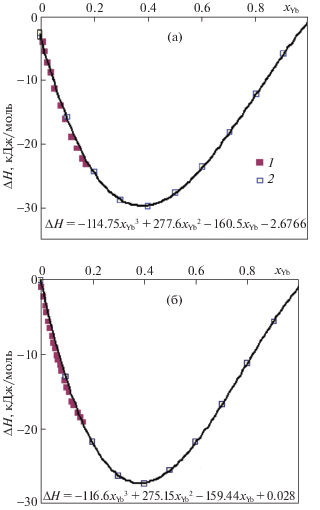
Полученные экспериментально энтальпии смешения изученных расплавов несколько отличаются от рассчитанных по “геометрическим” моделям, что дает основание предположить наличие тройного взаимодействия в исследованной системе. На рис. 5 представлены расчеты по модели Редлиха–Кистера с учетом параметра тройного вклада L1 = –250, который оценен из экспериментальных данных. Как видно из рис. 5, минимум энтальпий смешения приходится на центральную область концентрационного треугольника (xYb = 0.38, xAl = xAg = 0.31) и составляет –29 кДж/моль. Это обусловлено образованием тернарного соединения YbAg1.5Al0.5 [9], которое, вероятнее всего, плавится конгруэнтно при Т ≈ ≈ 1500–1700 K. Хотя в [9] была исследована структура еще соединения Yb8Ag21Al45, но оно, по-видимому, легкоплавкое.
Рис. 5.
Изоэнтальпии смешения расплавов тройной системы Ag–Al–Yb, рассчитанные по уравнению Редлиха–Кистера (L = –250) при Т = 1363 K.
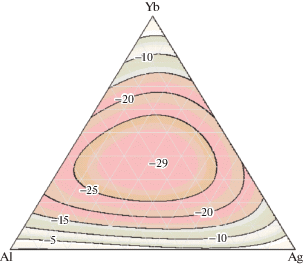
Таким образом, модель Редлиха–Кистера с параметром тройного взаимодействия L = –250 позволяет удовлетворительно описать концентрационную зависимость энтальпий смешения расплавов тройной системы Ag–Al–Yb. Поэтому эту модель можно использовать для расчета других термодинамических свойств расплавов этой и других подобных систем.
Список литературы
Wilder T.C., Elliot J.F. // J. Electrochem. Soc. 1960. V. 107. P. 1202.
Massart G., Desre P., Bonnier E. // J. Chem. Phys. 1970. V. 67. P. 1485.
Itagaki K., Jazawa A. // J. Jap. Inat. Metals. 1968. V. 32. P. 1294.
Судавцова В.С., Иванов М.И., Березуцкий В.В. и др. // Журн. физ. химии. 2012. Т. 86. № 8. С. 1311.
Ivanov M.I., Berezutski V.V., Usenko N.I. // Intern. J. of Materials Research. 2009. V. 100. № 7. P. 1001.
Kohler F. // Monatshefte für Chemie. 1960. V. 91. № 4. P. 738. https://doi.org/10.1007/BF00899814
Toop G.W. // Transactions of the Metallurgical Society of AIME. 1965. V. 233. P. 850.
Bonnier E., Caboz R. // Comptes rendus Acad. Sci., Paris. 1960. V. 250. № 3. P. 527.
Gordier G., Henselei R. // Intern. J. of Modern Physics B. 1993. V. 7. № 3. P. 391.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии