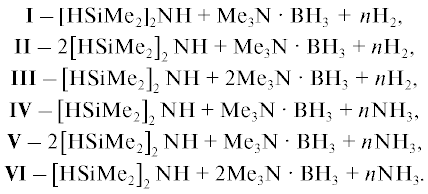Журнал неорганической химии, 2021, T. 66, № 11, стр. 1585-1592
Термодинамический анализ процессов получения пленок SiBCN с использованием газовой смеси триметиламинборана и тетраметилдисилазана
В. А. Шестаков a, *, М. Л. Косинова a
a Институт неорганической химии им. А.В. Николаева СО РАН
630090 Новосибирск, пр-т Академика Лаврентьева, 3, Россия
* E-mail: vsh@niic.nsc.ru
Поступила в редакцию 29.03.2021
После доработки 27.04.2021
Принята к публикации 10.05.2021
Аннотация
Проведено термодинамическое моделирование процесса химического осаждения из газовой фазы (chemical vapor deposition, CVD) пленок сложного состава в системе Si–B–N–C–H при пониженном давлении (0.01 Торр) в широком интервале температур (от 400 до 1200 K) с использованием летучих элементоорганических соединений – тетраметилдисилазана [HSiMe2]2NH и триметиламинборана Me3N · BH3 – в качестве исходных веществ. Согласно CVD-диаграммам, пленки могут представлять собой фазовые комплексы, содержащие в себе фазы Si3N4, BN, SiC и C в различных сочетаниях. Результаты работы могут быть использованы для управления процессом CVD в системе Si–B–N–C–H.
ВВЕДЕНИЕ
Интерес, проявляемый в настоящее время к покрытиям из кремнийсодержащей керамики (SiC, Si3N4, Si–C–N, Si–B–C–N), обусловлен их физико-химическими свойствами, такими как высокая твердость, химическая стабильность и инертность, термическая и коррозионная стойкость, а также высокая температура плавления и низкая плотность. Высокопрочные и легкие материалы с улучшенными эксплуатационными характеристиками нужны для развития практически всех отраслей экономики, что стимулирует исследования, направленные на разработку новых эффективных методов синтеза покрытий SiBCN. Регулярное появление обзоров по этой теме свидетельствует о большом интересе к ней исследователей [1–4]. Среди известных методов создания неорганических пленок и покрытий на поверхности твердых тел ведущее место занимают методы химического осаждения из газовой фазы (CVD) [5–8]. Широкое распространение метода CVD в промышленном производстве обусловлено его относительной аппаратурной простотой и безопасностью, технологичностью и высоким качеством покрытий, получаемых в оптимальных условиях. Для изготовления пленок с требуемыми параметрами необходимым условием является знание закономерностей изменения их функциональных характеристик от условий формирования и послеростовой обработки, химического и фазового состава образцов, их структуры, стабильности и т.д.
Согласно имеющимся в литературе данным, для получения покрытий SiBCN используют следующие газовые смеси: SiMe4 + H2 + BF3 + Ar + + N2 + He [9], SiCl3Me + NH3 + BCl3 + H2 + Ar [10, 11], (SiMe3)2 + Me3N · BH3 + Ar [12] и летучие кремний-борорганические соединения в смеси с азотом и аргоном [13–15]. Для оптимизации параметров осаждения покрытий из сложных газовых смесей – температуры осаждения, общего давления в системе и состава исходной газовой смеси – полезно предварительно провести термодинамический анализ процесса CVD [16–19]. Термодинамическое моделирование системы Si–B–C–N–Cl–H проведено в работе [20], где показана возможность получения керамики SiBCN из смеси SiCl3Me + NH3 + BCl3 + H2 + Ar и установлено, что преобладающими конденсированными фазами являются SiC, Si3N4, BN, B4C и C.
Ранее нами проведено моделирование процессов осаждения пленок карбонитрида кремния SiCxNy из газовых смесей ряда кремнийорганических соединений с N2, NH3, H2 и He в температурном интервале 800–2300 K [21] и нитрида BN и карбонитрида бора BCxNy из газовых смесей боразина, алкиламинборанов или триалкилборатов с N2, NH3, H2 и He в температурном интервале 800–2000 K при пониженном давлении в системе [22, 23]. Система Si–B–N–C–H была исследована на примере смесей тетраметилсилана SiMe4 (Si : C : N : H = 1 : 4 : 0 : 12) и гексаметилдисилана (SiMe3)2 (Si : C : N : H = 2 : 6 : 0 : 18) с триметиламинбораном Me3N ⋅ BH3 или триэтиламинбораном Et3N ⋅ BH3. Показана возможность получения пленок SiBCN различного состава: от нитридов бора и кремния до их смесей с карбидами и/или углеродом. Согласно расчетным CVD-диаграммам, преобладающими конденсированными фазами в равновесии были различные фазовые комплексы11, содержащие SiC, Si3N4, BN и C [24]. Отметим, что в проведенном ранее экспериментальном исследовании CVD-процесса в аналогичной системе [12] были найдены те же фазовые комплексы. Это свидетельствует о том, что термодинамическое моделирование может быть использовано для прогноза результатов эксперимента.
Механизмы химических реакций в газовой фазе и на поверхности подложки определяются природой реагентов, что приводит к изменению химического и фазового состава пленки и отражается на ее нано- и микроструктуре, а также на физико-химических, функциональных и эксплуатационных свойствах. Набор конденсированных фаз, находящихся в равновесии с газовой фазой, существенно зависит от параметров процесса: температуры реактора, общего давления в системе, соотношения компонентов исходной газовой смеси. Однако в работе [24] влияние соотношения исходных элементоорганических веществ на количественный состав фазовых комплексов не рассматривалось. Эти обстоятельства делают целесообразным изучение этого вопроса для процессов CVD получения пленок SiBCN в химических системах с разными кремний- и борсодержащими реагентами.
В настоящей работе рассмотрена возможность получения пленок SiBCN в системе Si–B–C–N–H с использованием тетраметилдисилазана [HSiMe2]2NH (Si : C : N : H = 2 : 4 : 1 : 15) и триметиламинборана Me3N ⋅ BH3 (B : C : N : H = 1 : 3 : 1 : : 12) в качестве исходных веществ в смесях с водородом или аммиаком при различном соотношении элементоорганических соединений в исходной газовой смеси.
ТЕРМОДИНАМИЧЕКИЙ РАСЧЕТ
В качестве исходных веществ мы рассматривали кремнийорганическое (тетраметилдисилазан [HSiMe2]2NH) и борорганическое (триметиламинборан Me3N ⋅ BH3) соединения. Расчеты проводили для ряда исходных газовых смесей:
Целью термодинамического анализа является определение состава газовой фазы и находящихся в равновесии с ней конденсированных фаз, изучение влияния соотношения исходных кремний- и борорганических веществ на количественный состав фазовых комплексов, построение CVD-диаграмм, определяющих условия образования тех или иных фазовых комплексов. Используемый нами метод расчета основан на минимизации свободной энергии Гиббса рассматриваемой системы. Принималось, что газообразные соединения подчиняются закону идеального газа, а конденсированные фазы являются фазами постоянного состава. Предполагается, что подложка является инертной по отношению как к газообразным веществам, находящимся в реакторе, так и к пленке. В качестве исходной термодинамической информации использовали стандартные термодинамические характеристики индивидуальных веществ: ΔfH°(298 K), S°(298 K), $C_{p}^{0} = f(T).$ Набор согласованных термодинамических свойств для всех соединений был взят из Банка данных свойств материалов электронной техники [25]. В процессе расчета учитывали следующие конденсированные фазы: Si, Si3N4, SiC(2), C(графит), BN(3), B4C, B(2), а также 88 молекулярных форм газовой фазы22.
Для исходных газовых смесей I–VI проведено термодинамическое моделирование процессов осаждения индивидуальных конденсированных фаз или их смесей в интервале температур 400–1200 K при pобщ = 0.01 Торр. Значение параметра n в системе варьировали в интервале от 1 до 10. Результаты расчета представлены в виде соответствующих сечений CVD-фазовой диаграммы Si–B–C–N–H, а также таблиц, позволяющих проследить изменение содержания отдельных фаз в получаемых фазовых комплексах в зависимости от состава исходной смеси газов и температуры.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
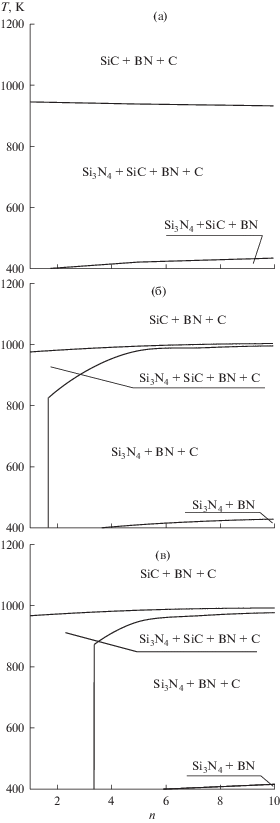
Система I. На рис. 1а представлена CVD-диаграмма системы I, показывающая влияние содержания водорода в исходной смеси на температурные интервалы существования фазовых комплексов Si3N4 + SiC + BN, Si3N4 + SiC + BN + C и SiC + BN + C.
Положение пограничной линии Si3N4 + SiC + + BN | Si3N4 + SiC + BN + C определяется здесь химическим равновесием CH4 = C + 2H2, а положение линии Si3N4 + SiC + BN + C | SiC + BN + C – равновесием Si3N4 + C = 3SiC + 2N2. Отметим находящуюся в нижней части диаграммы область условий образования свободного от графита фазового комплекса Si3N4 + SiC + BN. Весь углерод в этой области условий находится в газовой фазе в виде метана.
Содержание конденсированных фаз, а также основных компонентов газовой фазы в системе I при n = 5 в зависимости от температуры реактора показано в табл. 1. Видно, что содержание нитрида и карбида кремния в фазовом комплексе остается практически постоянным в интервале температур 400–800 K, тогда как содержание нитрида бора остается постоянным во всем температурном интервале. Метан при повышении температуры разлагается на водород и графит. Содержание графита в фазовом комплексе достигает максимума в районе 800 K. При температурах выше 900 K в газовой фазе появляется азот.
Таблица 1.
Содержание кристаллических фаз и основных молекулярных форм газовой фазы в системе I при n = 5
| Т, K | Кристаллические фазы, моль | Молекулярные формы газовой фазы, моль | |||||
|---|---|---|---|---|---|---|---|
| Si3N4 | SiC | BN | C | CH4 | H2 | N2 | |
| 400 | 0.25 | 1.25 | 1.00 | 0.00 | 5.75 | 8.00 | 0.00 |
| 500 | 0.25 | 1.25 | 1.00 | 5.16 | 0.59 | 18.32 | 0.00 |
| 600 | 0.25 | 1.25 | 1.00 | 5.73 | 0.02 | 19.45 | 0.00 |
| 700 | 0.25 | 1.25 | 1.00 | 5.74 | 0.00 | 19.50 | 0.00 |
| 800 | 0.25 | 1.25 | 1.00 | 5.75 | 0.00 | 19.50 | 0.00 |
| 900 | 0.21 | 1.37 | 1.00 | 5.63 | 0.00 | 19.50 | 0.08 |
| 1000 | 0.00 | 2.00 | 1.00 | 5.00 | 0.00 | 19.50 | 0.50 |
| 1100 | 0.00 | 2.00 | 1.00 | 5.00 | 0.00 | 19.50 | 0.50 |
| 1200 | 0.00 | 2.00 | 1.00 | 5.00 | 0.00 | 19.50 | 0.50 |
Система II. CVD-диаграмма системы II отличается от диаграммы, представленной на рис. 1а, только тем, что пограничная линия Si3N4 + SiC + + BN + C | SiC + BN + C смещена в ней на 7–11 K в область высоких температур, а пограничная линия Si3N4 + SiC + BN | Si3N4 + SiC + BN + C смещена на 7–9 K в область низких температур. Поэтому она здесь не представлена.
Содержание конденсированных фаз, а также основных компонентов газовой фазы в системе II при n = 5 в зависимости от температуры реактора показано в табл. 2.
Таблица 2.
Содержание кристаллических фаз и основных молекулярных форм газовой фазы в системе II при n = 5
| Т, K | Кристаллические фазы, моль | Молекулярные формы газовой фазы, моль | |||||
|---|---|---|---|---|---|---|---|
| Si3N4 | SiC | BN | C | CH4 | H2 | N2 | |
| 400 | 0.50 | 2.50 | 1.00 | 0.00 | 8.50 | 9.00 | 0.00 |
| 500 | 0.50 | 2.50 | 1.00 | 7.71 | 0.79 | 24.42 | 0.00 |
| 600 | 0.50 | 2.50 | 1.00 | 8.47 | 0.03 | 25.93 | 0.00 |
| 700 | 0.50 | 2.50 | 1.00 | 8.50 | 0.00 | 25.99 | 0.00 |
| 800 | 0.50 | 2.50 | 1.00 | 8.50 | 0.00 | 26.00 | 0.00 |
| 900 | 0.45 | 2.66 | 1.00 | 8.34 | 0.00 | 26.00 | 0.11 |
| 1000 | 0.00 | 4.00 | 1.00 | 7.00 | 0.00 | 26.00 | 1.00 |
| 1100 | 0.00 | 4.00 | 1.00 | 7.00 | 0.00 | 26.00 | 1.00 |
| 1200 | 0.00 | 4.00 | 1.00 | 7.00 | 0.00 | 26.00 | 1.00 |
Отметим, что основные тенденции, отмеченные ранее при описании системы I, сохраняются и в системе II. Однако при одинаковом содержании в фазовых комплексах нитрида бора в них будет большее содержание остальных компонентов комплексов: нитрида и карбида кремния, а также графита.
Система III. CVD-диаграмма системы III отличается от диаграммы, представленной на рис. 1a, тем, что пограничная линия Si3N4 + SiC + BN + + C | SiC + BN + C смещена в ней на 5–9 K в область низких температур, а пограничная линия Si3N4 + SiC + BN | Si3N4 + SiC + BN + C – на 13–15 K также в область низких температур.
Содержание конденсированных фаз, а также основных компонентов газовой фазы в системе III при n = 5 в зависимости от температуры реактора показано в табл. 3.
Таблица 3.
Содержание кристаллических фаз и основных молекулярных форм газовой фазы в системе III при n = 5
| Т, K | Кристаллические фазы, моль | Молекулярные формы газовой фазы, моль | |||||
|---|---|---|---|---|---|---|---|
| Si3N4 | SiC | BN | C | CH4 | H2 | N2 | |
| 400 | 0.25 | 1.25 | 2.00 | 0.00 | 8.75 | 7.00 | 0.00 |
| 500 | 0.25 | 1.25 | 2.00 | 8.01 | 0.74 | 23.01 | 0.00 |
| 600 | 0.25 | 1.25 | 2.00 | 8.71 | 0.03 | 24.44 | 0.00 |
| 700 | 0.25 | 1.25 | 2.00 | 8.75 | 0.00 | 24.50 | 0.00 |
| 800 | 0.25 | 1.25 | 2.00 | 8.75 | 0.00 | 24.50 | 0.00 |
| 900 | 0.20 | 1.41 | 2.00 | 8.59 | 0.00 | 24.50 | 0.10 |
| 1000 | 0.00 | 2.00 | 2.00 | 8.00 | 0.00 | 24.50 | 0.50 |
| 1100 | 0.00 | 2.00 | 2.00 | 8.00 | 0.00 | 24.50 | 0.50 |
| 1200 | 0.00 | 2.00 | 2.00 | 8.00 | 0.00 | 24.50 | 0.50 |
Основные тенденции, отмеченные ранее при описании системы I, сохраняются и в системе III. Однако при одинаковом содержании в фазовых комплексах нитрида и карбида кремния в них будет большее содержание других компонентов комплексов – нитрида бора и графита.
Система IV. На рис. 1б представлена CVD-диаграмма системы IV, показывающая влияние содержания аммиака в исходной смеси на температурные интервалы существования фазовых комплексов Si3N4 + BN, Si3N4 + BN + C, Si3N4 + + SiC + BN + C и SiC + BN + C.
Положение пограничной линии Si3N4 + + BN | Si3N4 + BN + C определяется здесь химическим равновесием CH4 = C + 2H2, а положение линий Si3N4 + BN + C | Si3N4 + SiC + BN + C и Si3N4 + SiC + BN + C | SiC + BN + C – равновесием Si3N4 + C = 3SiC + 2N2. Таким образом, хотя пограничные линии в системах I и IV разделяют области существования различных фазовых комплексов, их положение определяется одними и теми же равновесиями. Отметим, что на диаграмме системы IV также есть область условий, в которой не образуется графит. Однако она представлена другим фазовым комплексом – Si3N4 + BN. В области низких температур нитрид кремния термодинамически более устойчив, чем карбид кремния. Поэтому в данной температурной области карбид кремния образуется только при n < 1.66, где азота в системе недостаточно, чтобы весь кремний перевести в нитрид. При высоких температурах ситуация становится обратной.
Содержание конденсированных фаз, а также основных компонентов газовой фазы в системе IV при n = 5 в зависимости от температуры реактора показано в табл. 4. При n = 5 содержание в фазовых комплексах нитрида и карбида кремния, а также нитрида бора в своих температурных интервалах остается постоянным. Содержание графита в фазовом комплексе по мере разложения метана с температурой возрастает, а затем падает в связи с переходом нитрида кремния в карбид.
Таблица 4.
Содержание кристаллических фаз и основных молекулярных форм газовой фазы в системе в системе IV при n = 5
| Т, K | Кристаллические фазы, моль | Молекулярные формы газовой фазы, моль | |||||
|---|---|---|---|---|---|---|---|
| Si3N4 | SiC | BN | C | CH4 | H2 | N2 | |
| 400 | 0.67 | 0.00 | 1.00 | 0.00 | 7.00 | 7.00 | 1.67 |
| 500 | 0.67 | 0.00 | 1.00 | 6.41 | 0.59 | 19.81 | 1.67 |
| 600 | 0.67 | 0.00 | 1.00 | 6.98 | 0.02 | 20.95 | 1.67 |
| 700 | 0.67 | 0.00 | 1.00 | 7.00 | 0.00 | 21.00 | 1.67 |
| 800 | 0.67 | 0.00 | 1.00 | 7.00 | 0.00 | 21.00 | 1.67 |
| 900 | 0.67 | 0.00 | 1.00 | 7.00 | 0.00 | 21.00 | 1.67 |
| 1000 | 0.00 | 2.00 | 1.00 | 5.00 | 0.00 | 19.50 | 3.00 |
| 1100 | 0.00 | 2.00 | 1.00 | 5.00 | 0.00 | 19.50 | 3.00 |
| 1200 | 0.00 | 2.00 | 1.00 | 5.00 | 0.00 | 19.50 | 3.00 |
Система V. На рис. 1в представлена CVD-диаграмма системы V, показывающая влияние содержания аммиака в исходной смеси на температурные интервалы существования фазовых комплексов Si3N4 + BN, Si3N4 + BN + C, Si3N4 + SiC + BN + C и SiC + BN + C.
Переход между областями существования фазовых комплексов Si3N4 + BN + C и Si3N4 + SiC + + BN + C в области низких температур осуществляется здесь при n = 3.3 по той причине, что относительное содержание кремния в этой системе больше, чем в системе IV. Отметим также уменьшение области существования фазового комплекса Si3N4 + BN в системе V по сравнению с аналогичной областью системы IV.
Содержание конденсированных фаз, а также основных компонентов газовой фазы в системе V при n = 5 в зависимости от температуры реактора показано в табл. 5.
Таблица 5.
Содержание кристаллических фаз и основных молекулярных форм газовой фазы в системе V при n = 5
| Т, K | Кристаллические фазы, моль | Молекулярные формы газовой фазы, моль | |||||
|---|---|---|---|---|---|---|---|
| Si3N4 | SiC | BN | C | CH4 | H2 | N2 | |
| 400 | 1.33 | 0.00 | 1.00 | 0.34 | 10.66 | 7.18 | 0.83 |
| 500 | 1.33 | 0.00 | 1.00 | 10.15 | 0.84 | 26.82 | 0.83 |
| 600 | 1.33 | 0.00 | 1.00 | 10.97 | 0.03 | 28.43 | 0.83 |
| 700 | 1.33 | 0.00 | 1.00 | 11.00 | 0.00 | 28.50 | 0.83 |
| 800 | 1.33 | 0.00 | 1.00 | 11.00 | 0.00 | 28.50 | 0.83 |
| 900 | 1.33 | 0.00 | 1.00 | 11.00 | 0.00 | 28.50 | 0.83 |
| 1000 | 0.00 | 4.00 | 1.00 | 7.00 | 0.00 | 28.50 | 3.50 |
| 1100 | 0.00 | 4.00 | 1.00 | 7.00 | 0.00 | 28.50 | 3.50 |
| 1200 | 0.00 | 4.00 | 1.00 | 7.00 | 0.00 | 28.50 | 3.50 |
Как видно из табл. 4 и 5, при одинаковом содержании нитрида бора в фазовых комплексах систем IV и V содержание в них остальных компонентов (Si3N4, SiC и С) в системе V больше, чем в системе IV.
Система VI. CVD-диаграмма системы VI отличается от диаграммы, представленной на рис. 1б, следующими особенностями: а) пограничная линия Si3N4 + SiC + BN + C | SiC + BN + C смещена в ней на 5–9 K в область низких температур; б) пограничная линия Si3N4 + BN + C | Si3N4 + SiC + + BN + C смещена на 6 K в область низких температур при n = 1.66 и на 2 K в область высоких температур при n = 10; в) пограничная линия Si3N4 + + BN | Si3N4 + BN + C смещена на 9 K в область низких температур33.
Содержание конденсированных фаз, а также основных компонентов газовой фазы в системе VI при n = 5 в зависимости от температуры реактора показано в табл. 6.
Таблица 6.
Содержание кристаллических фаз и основных молекулярных форм газовой фазы в системе VI при n = 5
| Т, K | Кристаллические фазы, моль | Молекулярные формы газовой фазы, моль | |||||
|---|---|---|---|---|---|---|---|
| Si3N4 | SiC | BN | C | CH4 | H2 | N2 | |
| 400 | 0.67 | 0.00 | 2.00 | 0.00 | 10.00 | 7.00 | 1.67 |
| 500 | 0.67 | 0.00 | 2.00 | 9.22 | 0.77 | 25.45 | 1.67 |
| 600 | 0.67 | 0.00 | 2.00 | 9.97 | 0.03 | 26.94 | 1.67 |
| 700 | 0.67 | 0.00 | 2.00 | 10.00 | 0.00 | 26.94 | 1.67 |
| 800 | 0.67 | 0.00 | 2.00 | 10.00 | 0.00 | 27.00 | 1.67 |
| 900 | 0.67 | 0.00 | 2.00 | 10.00 | 0.00 | 27.00 | 1.67 |
| 1000 | 0.00 | 2.00 | 2.00 | 8.00 | 0.00 | 27.00 | 3.00 |
| 1100 | 0.00 | 2.00 | 2.00 | 8.00 | 0.00 | 27.00 | 3.00 |
| 1200 | 0.00 | 2.00 | 2.00 | 8.00 | 0.00 | 27.00 | 3.00 |
Основные тенденции, отмеченные ранее при описании системы IV, сохраняются и в системе VI. Однако при одинаковом содержании в фазовых комплексах нитрида и карбида кремния в них будет большее содержание других компонентов комплексов: нитрида бора и графита.
ЗАКЛЮЧЕНИЕ
В работе проведено термодинамическое моделирование процесса осаждения из газовой фазы в системе Si–B–C–N–H фазовых комплексов на основе нитридов бора и кремния, карбида кремния, а также графита. Построены соответствующие CVD-диаграммы, показывающие области существования этих комплексов. Исследована зависимость содержания отдельных фаз в фазовых комплексах от состава исходной газовой смеси и температуры.
Обобщая результаты моделирования с использованием смесей триметиламинборана, триэтиламинборана и трех различных кремнийорганических соединений: SiMe4, (SiMe3)2 [24] и [HSi(Me)2]2NH (наст. работа), можно сказать, что CVD-диаграммы в основном подобны, и сделать следующие выводы:
– повышение общего давления в реакторе приводит к смещению пограничных линий на CVD-диаграммах в область более высоких температур, а также способствует образованию смеси нитридов бора и кремния в системах с аммиаком при низких температурах;
– в области низких температур при увеличении содержания водорода или аммиака в системе можно ожидать появление безуглеродных фазовых комплексов Si3N4 + SiC + BN или Si3N4 + BN;
– в области низких температур нитрид кремния термодинамически более устойчив, чем карбид кремния, поэтому в данной температурной области карбид кремния образуется только в той области составов системы, где азота в системе недостаточно, чтобы весь кремний перевести в нитрид;
– в области высоких температур нитрид кремния отсутствует в связи с образованием карбида кремния;
– следует отметить, что во всем изученном интервале температур в фазовых комплексах присутствует нитрид бора, и только при весьма высоких температурах можно ожидать появление карбида бора;
– содержание отдельных фаз в фазовых комплексах существенно зависит от температуры и соотношения реагентов в исходной газовой смеси (табл. 1–6);
– определены фазовые равновесия, определяющие положение пограничных линий на CVD-диаграммах. Как показано в [22], эти равновесия могут использоваться для управления процессом CVD.
Проведенное моделирование химического осаждения из газовой фазы в системе Si–B–C–N–H позволяет рекомендовать кремний- и борорганические соединения, рассмотренные в наших работах, для получения покрытий SiBCN. Как правило, в процессах разложения элементоорганических соединений экспериментаторы сталкиваются с проблемой соосаждения углерода в пленках. С целью получения пленок, не содержащих фазы углерода, в данной системе можно использовать сравнительно низкие температуры и повышенное давление процесса, а также увеличить содержание водорода или аммиака в исходной газовой смеси. С другой стороны, для получения покрытий, обогащенных углеродом (carbon-rich), следует проводить синтез при средних температурах (700–900 K). Зависимости содержания фаз в фазовых комплексах от температуры и состава исходной газовой смеси, представленные в табл. 1–6, могут быть полезны при выборе условий формирования покрытий заданного состава.
Список литературы
Barroso G., Li Q., Bordia R.K., Motz G. // J. Mater. Chem. A. 2019. V. 7. P. 1936. https://doi.org/10.1039/c8ta09054h
Jia D., Liang B., Yang Z., Zhou Y. // Prog. Mater. Sci. 2018. V. 98. P. 1. https://doi.org/10.1016/j.pmatsci.2018.05.006
Zhang P., Jia D., Yang Z. et al. // J. Adv. Ceram. 2012. V. 1. P. 157. https://doi.org/10.1007/s40145-012-0017-x
Colombo P., Mera G., Riedel R., Soraru G.D. // J. Am. Ceram. Soc. 2010. V. 93. P. 1805. https://doi.org/10.1111/j.1551-2916.2010.03876.x
Ashurbekova K., Ashurbekova K., Botta G. et al. // Nanotechnology. 2020. V. 31. P. 342001. https://doi.org/10.1088/1361-6528/ab8edb
Fraga M., Pessoa R. // Micromachines. 2020. V. 11. P. 799. https://doi.org/10.3390/mi11090799
Lozanov V.V., Il’in I.Yu., Morozova N.B. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 11. P. 1781. [Лозанов В.В., Ильин И.Ю., Морозова Н.Б. и др. // Журн. неорган. химии. 2020. Т. 65. № 11. С. 1570.]https://doi.org/10.1134/S0036023620110108
Koponen S.E., Gordon P.G., Barry S.T. // Polyhedron. 2016. V. 108. P. 59. https://doi.org/10.1016/j.poly.2015.08.024
Samra H.A., Kumar A., Xia J. et al. // Surf. Coat. Technol. 2013. V. 223. P. 52. https://doi.org/10.1016/j.surfcoat.2013.02.028
Wang C., Liu Y., Zhao M. et al. // Ceram. Int. 2018. V. 44. P. 22830. https://doi.org/10.1016/j.ceramint.2018.09.074
Qin H., Liu Y., Ye F. et al. // J. Alloys Compd. 2019. V. 771. P. 747. https://doi.org/10.1016/j.jallcom.2018.08.006
Merenkov I.S., Katsui H., Khomyakov M.N. et al. // J. Eur. Ceram. Soc. 2019. V. 39. P. 5123. https://doi.org/10.1016/j.jeurceramsoc.2019.08.006
Hegemann D., Riedel R., Oehr C. // Chem. Vap. Deposition. 1999. V. 5. P. 61. https://doi.org/0948-1907/99/0203-0061
Wilden J., Wank A., Bykava A. // Surf. Coat. Technol. 2005. V. 200. P. 612. https://doi.org/10.1016/j.surfcoat.2005.01.027
Sunn X., Liu H., Li J., Cheng H. // Ceram. Int. 2016. V. 42. P. 82. https://doi.org/10.1016/j.ceramint.2015.07.116
Cheimarios N., Kokkoris G., Boudouvis A.G. // Archives of Computational Methods in Engineering. 2021. V. 28. P. 637. https://doi.org/10.1007/s11831-019-09398-w
Shavelkina M.B., Ivanov P.P., Bocharov A.N., Amirov R.Kh. // High Energ. Chem. V. 54. № 5. P. 374. [Шавелкина М.Б., Иванов П.П., Бочаров А.Н., Амиров Р.Х. // Химия высоких энергий. 2020. Т. 54. № 5. С. 411.]https://doi.org/10.1134/S0018143920050136
Shabarova L.V., Sennikov P.G., Kornev R.A. et al. // High Energ. Chem. V. 54. P. 469. [Шабарова Л.В., Сенников П.Г., Корнев Р.А., Плехович А.Д., Кутьин А.М. // Химия высоких энергий. 2019. Т. 53. № 6. С. 489.]https://doi.org/10.1134/S0018143920060132
Nikonova K.S., Il’yasova A.S., Brekhovskikh M.N. // Russ. J. Inorg. Chem. 2020. V. 65. P. 1366. [Нико-нов К.С., Ильясов А.С., Бреховских М.Н. // Журн. неорган. химии. 2020. Т. 65. № 9. С. 1222.]https://doi.org/10.1134/S0036023620090120
Dong N., Chai N., Liu Y. et al. // J. Eur. Ceram. Soc. 2016. V. 36. P. 3581. https://doi.org/10.1016/j.jeurceramsoc.2016.05.030
Shestakov V.A., Kosyakov V.I., Kosinova M.L. // Russ. J. Inorg. Chem. 2020. V. 65. № 6. P. 898. [Шестаков В.А., Косяков В.И., Косинова М.Л. // Журн. неорган. химии. 2020. Т. 65. № 6. P. 829.]https://doi.org/10.1134/S0036023620060212
Shestakov V.A., Kosyakov V.I., Kosinova M.L. // Russ. Chem. Bull. 2019. V. 68. P. 1983. https://doi.org/1066-5285/19/6811-1983 [Шестаков В.А., Косяков В.И., Косинова М.Л. // Изв. АН. Сер. хим. 2019. Т. 11. С. 1983.]
Kosyakov V.I., Shestakov V.A., Kosinova M.L. // Russ. J. Inorg. Chem. 2018. V. 63. P. 822. [Косяков В.И., Шестаков В.А., Косинова М.Л. // Журн. неорган. химии. 2018. Т. 63. С. 777. https://doi.org/10.7868/S0044457X1806017X]https://doi.org/10.1134/S0036023618060153
Shestakov V.A., Kosinova M.L. // Russ. Chem. Bull., Int. Edv. 2021. V. 70. № 2. P. 283. [Шестаков В.А., Косинова М.Л. // Изв. АН. Сер. хим. 2021. № 2. С. 283.]https://doi.org/10.1007/s11172-021-3083-9
Kuznetsov F.A., Titov V.A. Proc. Int. Symp. Advanced Materials (September 24–30, 1995). Jpn. P. 16.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии