Микроэлектроника, 2021, T. 50, № 6, стр. 419-427
О механизмах плазменного травления оксидов титана, индия, олова и цинка в смеси HBr + Ar
А. М. Ефремов a, b, *, С. А. Смирнов a, b, В. Б. Бетелин b, K.-H. Kwon c
a ФГБОУ ВО “Ивановский государственный химико-технологический университет”
153000 Иваново,
Шереметевский просп., 7, Россия
b ФГУ ФНЦ НИИСИ РАН
Москва, Нахимовский просп., 36, корп. 1, Россия
c Korea University
339-700 Sejong, South Korea
* E-mail: amefremov@mail.ru
Поступила в редакцию 05.04.2021
После доработки 15.05.2021
Принята к публикации 01.06.2021
Аннотация
Проведено исследование кинетики и механизмов реактивно-ионного травления оксидов титана (TiO2), индия (In2O3), олова (SnO2) и цинка (ZnO) в плазме HBr + Ar. Установлено, что увеличение доли Ar сопровождается снижением скоростей травления всех исследованных материалов, при этом абсолютные значения скоростей при любом составе смеси коррелируют с величиной энергии разрыва оксидной связи и/или летучестью продуктов взаимодействия. При совместном использовании методов диагностики и моделирования плазмы определены стационарные концентрации активных частиц и плотности их потоков на обрабатываемую поверхность. Использование этих данных для анализа кинетики гетерогенных процессов показало, что а) доминирующим механизмом травления в диапазоне 0–75% Ar является ионно-стимулированная химическая реакция; и б) эффективная вероятность взаимодействия атомов брома увеличивается (для TiO2) или снижается (для In2O3, SnO2 и ZnO) с ростом степени разбавления HBr аргоном. Сделаны предположения о причинах такой зависимости.
1. ВВЕДЕНИЕ
Современные исследования в области технологии микро- и нано-электроники все чаще имеют дело с альтернативными материалами, которые используются в приборах нового типа и/или замещают традиционные материалы в кремниевых интегральных структурах. Одним из показательных направлений здесь является оптоэлектроника, где технология изготовления элементов солнечных батарей и светоизлучающих устройств (например – светодиодов) требует оптически прозрачных проводящих и полупроводниковых слоев [1]. Большие перспективы в этом плане имеют оксиды некоторых металлов, в частности – титана, индия, олова и цинка [1, 2]. Известно, что неотъемлемым этапом любой планарной технологии является структурирование (размерное травление) предварительно сформированных сплошных слоев [3, 4]. Поэтому разработка и оптимизация методов плазменного (т.е. сухого, без использования жидких реагентов) травления тонких пленок TiO2, In2O3, SnO2 и ZnO является актуальным направлением совершенствования технологии для повышения качества и функциональности конечных изделий. Очевидно, что решение таких задач невозможно без систематических научных исследований, направленных на выявление взаимосвязей между условиями проведения процесса, внутренними параметрами плазмы и механизмами гетерогенных процессов в системе плазма/обрабатываемая поверхность.
В настоящее время существует достаточное количество работ (например, [5–16]) посвященных исследованиям закономерностей плазменного травления TiO2, In2O3, SnO2 и ZnO в среде фтор-, хлор-, и бром-содержащих газов в условиях реактивно-ионного процесса (давление газа <20 мторр, энергия ионной бомбардировки >100 эВ). Основной особенностью таких процессов является реализация двух механизмов газификации атомов поверхности – физического распыления и химической реакции. Это обеспечивает получение технологически приемлемых скоростей травления для материалов, образующих нелетучие галогениды металлов. В целом, по результатам существующих работ для каждого из перечисленных оксидов выявлены зависимости выходных характеристик процесса (скорость, анизотропия, селективность по отношению к материалу маски) от условий его проведения (давление, вкладываемая мощность, мощность смещения); б) предложены плазмообразующие газы и/или смеси, обеспечивающие достижение наилучших значений одного или нескольких выходных параметров; и в) изучены механизмы деградации электрических свойств поверхности после плазменного воздействия. В то же время, существует ряд проблем, которые требуют особого внимания. Во-первых, большинство имеющихся работ значительно различаются по диапазонам исследованных условий и типам плазмохимических реакторов. Как результат, невозможность корректного сравнения кинетики травления различных материалов существенно затрудняет выбор оптимального плазмообразующего газа для целей конкретного процесса. Во-вторых, многие исследования носят феноменологический характер, основанный на описании экспериментальных данных без объяснений наблюдаемых эффектов. Очевидно, что игнорирование взаимосвязей гетерогенного взаимодействия с параметрами газовой фазы, являющейся источником активных частиц, не способствует пониманию механизма процесса и путей его оптимизации. И, в-третьих, основное внимание было уделено фтор- и хлор-содержащим плазмообразующим газам. На этом фоне, информация по бром-содержащим газам более бедна и явно не достаточна для оценки их перспектив в советующих процессах.
Цель данной работы – сравнительное исследование кинетики и механизмов реактивно-ионного травления тонких пленок TiO2, In2O3, SnO2 и ZnO в смесях HBr + Ar переменного начального состава. Выбор варьируемого параметра обусловлен тем, что увеличение доли Ar в смеси неизбежно сопровождается изменением режима травления и переходом к доминированию физических каналов гетерогенного взаимодействия. Такая ситуация способствует эффективному выявлению вкладов химической реакции и физического распыления в общую скорость процесса и, как следствие, формированию адекватных представлений о его механизме.
2. МЕТОДИЧЕСКАЯ ЧАСТЬ
2.1. Получение пленок TiO2, In2O3, SnO2 и ZnO
Пленки TiO2 толщиной ∼200 нм получали на подложках Si(100) методом центрифугирования. В качестве жидкого прекурсора использовался Ti(i-C3H7O)4, растворенный в смеси бутил ацетата и изопропилового спирта. Формирование твердого покрытия обеспечивалось на этапах термической обработки (∼10 мин при 120°С) и выжигания растворителя (∼30 мин при 420°С). Стехиометрический состав оксида подтверждается анализом поверхности методом Оже-спектроскопии [8].
Пленки In2O3, SnO2 и ZnO толщиной ∼150 нм формировали на подложках Si(100) при магнетронном распылении соответствующих мишеней. Чистота материала мишени во всех случаях составляла 99.99%. Процесс осаждения In2O3 и SnO2 проводили в среде аргона при давлении 0.01 мторр и мощности 100 Вт. В случае ZnO, в качестве рабочего газа выступала смесь 75% Ar + + 25% O2 при давлении 5 мторр.
2.2. Исследование кинетики травления и диагностика плазмы
Эксперименты проводились в реакторе планарного типа в условиях индукционного ВЧ (13.56 МГц) разряда [8, 9, 16]. В качестве постоянных внешних параметров плазмы выступалиобщий расход ($q$ = 40 станд. см3/мин) и давление ($p$ = 6 мторр) плазмообразующего газа, вкладываемая мощность ($W$ = 800 Вт) и мощность смещения на нижнем электроде (${{W}_{{dc}}}$ = 200 Вт). Величину потенциала смещения $ - {{U}_{{dc}}}$ контролировали высоковольтным зондом AMN-CTR (YoungsinEng, Korea). В качестве варьируемого параметра выступал начальный состав смеси HBr + Ar, задаваемый соотношением парциальных расходов компонентов смеси. Соответственно, изменение ${{q}_{{{\text{Ar}}}}}$ в диапазоне 0–30 станд. см3/мин обеспечивало увеличение доли Ar в плазмообразующей смеси ${{y}_{{{\text{Ar}}}}} = {{{{q}_{{{\text{Ar}}}}}} \mathord{\left/ {\vphantom {{{{q}_{{{\text{Ar}}}}}} q}} \right. \kern-0em} q}$ до 75%.
Диагностика плазмы осуществлялась с помощью двойного зонда Лангмюра DLP2000 (PlasmartInc., Korea). Обработка измеренных вольт-амперных характеристик (ВАХ) проводилась с использованием известных положений зондовой теории для разрядов низкого давления [17, 18]. Результатом обработки являлись данные по температуре электронов (${{T}_{e}}$) и плотности ионного тока (${{J}_{ + }}$).
Подвергаемые травлению образцы размером ∼2 × 2 см располагались в центральной части нижнего электрода, изготовленного из анодированного алюминия. Встроенная система водяного охлаждения обеспечивала поддержание постоянной температуры электрода $~{{T}_{S}}$ (а, следовательно, и температуры образца) после зажигания плазмы. Скорость травления определяли как $R = {{\Delta h} \mathord{\left/ {\vphantom {{\Delta h} \tau }} \right. \kern-0em} \tau },$ где $~\tau ~$ – время травления и $\Delta h$ – высота ступеньки травления на границе маскированной и немаскированной областей обрабатываемой поверхности. Величина $\Delta h$ измерялась профилометром Alpha-stepD-500 (KLA-Tencor, USA). В качестве маскирующего покрытия использовался фоторезист AZ1512 толщиной ∼1.5 мкм. В предварительных экспериментах было найдено, что а) кинетические зависимости $\Delta h = f\left( \tau \right)$ для всех исследованных материалов имеют квази-линейный характер; и б) увеличение площади обрабатываемой поверхности (числа одновременно загружаемых образцов) для каждого материала не приводит к снижению скорости травления и не сопровождается заметными изменениями зондовых ВАХ. Это позволяет заключить, что процесс травления протекает стационарно, в кинетическом режиме и характеризуется пренебрежимо малым влиянием продуктов травления на параметры газовой фазы.
2.3. Моделирование плазмы
Для получения данных по составу плазмы использовалась 0-мерная кинетическая модель, подробно описанная в наших работах [19–22]. Алгоритм моделирования базировался на совместном решении уравнений химической кинетики нейтральных и заряженных частиц c использованием типовых допущений для области давлений $p$ < 20 мторр [4]. В частности, полагалось, что:
1) функция распределения электронов по энергиям (ФРЭЭ) в условиях ${{{{n}_{ + }}} \mathord{\left/ {\vphantom {{{{n}_{ + }}} N}} \right. \kern-0em} N}$ ∼ 10–4 (где ${{n}_{ + }}$ – концентрация положительных ионов, а $N = {p \mathord{\left/ {\vphantom {p {{{k}_{B}}{{T}_{{gas}}}}}} \right. \kern-0em} {{{k}_{B}}{{T}_{{gas}}}}}$ – общая концентрация частиц при температуре газа ${{T}_{{gas}}}$), формируется при существенном вкладе равновесных электрон-электронных соударений. Поэтому аппроксимация ФРЭЭ функцией Максвелла обеспечивает адекватное описание кинетики процессов при электронном ударе;
2) гетерогенная рекомбинация атомов Br и H описывается механизмом Или-Ридила. Соответствующие константы скоростей (частоты) рекомбинации могут быть определены как $k \approx {{\gamma {{\upsilon }_{T}}} \mathord{\left/ {\vphantom {{\gamma {{\upsilon }_{T}}} {2r}}} \right. \kern-0em} {2r}},$ где $\gamma $ – вероятность рекомбинации [23, 24], $r$ – радиус рабочей камеры реактора, а ${{\upsilon }_{T}} = {{\left( {{{8{{k}_{B}}{{T}_{{gas}}}} \mathord{\left/ {\vphantom {{8{{k}_{B}}{{T}_{{gas}}}} {\pi m}}} \right. \kern-0em} {\pi m}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}.$ Величина ${{T}_{{gas}}}$ в первом приближении может полагаться независимой от состава плазмообразующей смеси [20, 21];
3) высокая электроотрицательность плазмы HBr обуславливает запись уравнения квазинейтральности в виде ${{n}_{ + }} = {{n}_{e}} + ~{{n}_{ - }},$ где слагаемые в правой части представляют концентрации электронов и отрицательных ионов. Концентрация электронов при этом может быть определена как
(1)
${{n}_{e}} \approx \frac{{{{k}_{{ii}}}n_{ + }^{2}}}{{{{\nu }_{{da}}} + {{k}_{{ii}}}{{n}_{ + }}}},$(2)
${{n}_{ + }} \approx \frac{{{{J}_{ + }}}}{{0.61e\sqrt {{{e{{T}_{e}}} \mathord{\left/ {\vphantom {{e{{T}_{e}}} {{{m}_{i}}}}} \right. \kern-0em} {{{m}_{i}}}}} }}~,$Базовая кинетическая схема процессов с участием нейтральных частиц (табл. 1) была заимствована из наших работ [19–21]. Выходными параметрами модели служили усредненные по объему реактора скорости процессов образования и гибели частиц, их концентрации и плотности потоков на поверхность, контактирующую с плазмой.
Таблица 1.
Кинетическая схема с участием нейтральных частиц в плазме HBr
| Реакция | $k$, см3/с | Реакция | $k$, см3/с | ||
|---|---|---|---|---|---|
| 1. | HBr + e → H + Br + e | $f\left( {{{T}_{e}}} \right)$ | 8. | Br → Brads | $f\left( \gamma \right)$, $\gamma $ = 0.1 |
| 2. | H2 + e → 2H + e | $f\left( {{{T}_{e}}} \right)$ | Brads + H → HBr | ||
| 3. | Br2 + e → 2Br + e | $f\left( {{{T}_{e}}} \right)$ | Brads + Br → Br2 | ||
| 4. | HBr + H → H2 + Br | 1.2 × 10–11 | 9. | H → Hads | $f\left( \gamma \right)$, $\gamma $ = 0.01 |
| 5. | HBr + Br → Br2 + H | 1.4 × 10–29 | Hads + Br → HBr | ||
| 6. | Br2 + H → HBr + Br | 1.2 × 10–10 | Hads + H → H2 | ||
| 7. | H2 + Br → HBr + H | 1.6 × 10–18 | |||
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Из анализа имеющихся работ [4, 25–27] можно заключить, что кинетика травления оксидных материалов в галогенсодержащей плазме определяется не только условиями процесса (типом газа и внешними параметрами плазмы), но и в значительной степени зависит от физико-химических свойств самого материала. Наиболее критичными из таких свойств являются а) летучесть продуктов взаимодействия, определяющая механизм их десорбции с обрабатываемой поверхности; и б) соотношение сил химических связей в оксиде и галогениде металла, влияющее на вероятность спонтанной химической реакции. Из табл. 2 можно видеть, что энергия разрыва оксидной связи убывает в ряду TiO2–SnO2–In2O3–ZnO, при этом только для In2O3 выполняется условие ${{\varepsilon }_{{dis}}}$(In–Br) > ${{\varepsilon }_{{dis}}}$(In–O). Фактически это означает, что химическое взаимодействие атомов брома с остальными материалами может протекать лишь по ионно-стимулированному механизму, когда ионная бомбардировка обеспечивает деструкцию оксидных связей. В то же время, насыщенные бромиды индия характеризуются максимальной температурой плавления, и, следовательно, минимальной летучестью по сравнению с продуктами травления остальных оксидов. Поэтому потенциал спонтанной химической реакции в системе In2O3 + Br ограничивается ионно-стимулированной десорбцией продуктов взаимодействия.
Таблица 2.
Энергии разрыва химических связей (${{\varepsilon }_{{dis}}}$) и температуры плавления насыщенных бромидов металлов (${{T}_{{mp}}}$), характеризующие их летучесть
| ${{\varepsilon }_{{dis}}}$, кДж/моль | |||||||
|---|---|---|---|---|---|---|---|
| Ti–O | Ti–Br | In–O | In–Br | Sn–O | Sn–Br | Zn–O | Zn–Br |
| 672 | 439 | 346 | 409 | 528 | 337 | 159 | 138 |
| ${{T}_{{mp}}}$, °C | |||||||
| 38 | 420 | 29 | 402 | ||||
На рис. 1а представлены экспериментальные данные по влиянию начального состава смеси HBr + Ar на скорости травления TiO2, In2O3, SnO2 и ZnO. Эти результаты могут быть обобщены в виде следующих положений:
Рис. 1.
Скорость травления (а) и относительное изменение эффективной вероятности гетерогенного взаимодействия атомов брома (б) в зависимости от начального состава смеси HBr + Ar: 1 – TiO2; 2 – In2O3; 3 – SnO2; 4 – ZnO; и 5 – фоторезист.
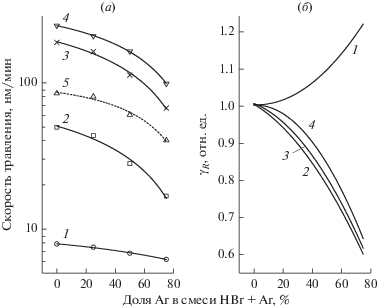
1) качественно идентичные формы кривых $R = f\left( {{{y}_{{{\text{Ar}}}}}} \right)~$ указывают на то, что процессы травления всех исследуемых материалов обеспечиваются одним типом активных частиц и/или имеют общую лимитирующую стадию. Отсутствие принципиальных различий в режимах травления обуславливает одинаковые методы регулирования выходных характеристик при варьировании внешних параметров плазмы;
2) максимальная скорость травления для ZnO (246.4–99.1 нм/мин при 0–75% Ar) и минимальная для TiO2 (7.9–6.2 нм/мин при 0–75% Ar) согласуются с различиями энергий разрыва оксидных связей (табл. 2). Более высокие скорости травления SnO2по сравнению с In2O3 внутри этого интервала формально противоречат условию ${{\varepsilon }_{{dis}}}$ (In–O) < ${{\varepsilon }_{{dis}}}$(Sn–O), но однозначно отражают значительно более высокую летучесть бромидов олова;
3) селективность травления по отношению к фоторезисту превышает единицу только для ZnO (2.9–2.1 при 0–75% Ar) и SnO2 (2.2–1.0 при 0–75% Ar), при этом для всех четырех оксидов имеет место снижение селективности с ростом ${{y}_{{{\text{Ar}}}}}.$ Такая ситуация в целом соответствует полученным ранее данным для широкого круга материалов и плазменных систем [26, 27]. Очевидно, что в реальных технологических процессах для оксидов титана и индия необходимо использование альтернативных масок, обладающих большей стойкостью к действию плазмы HBr. В частности, эксперименты с диоксидом кремния показали, что в исследованном диапазоне условий величина $\Delta h$ определяется на уровне ошибки измерений, что обуславливает пренебрежимо малую скорость травления данного материала. Таким образом, SiO2 является одним из достойных кандидатов на роль маскирующего покрытия при структурировании пленок TiO2 и In2O3.
Известно, что скорость реактивно-ионного процесса может быть представлена как сумма двух составляющих – физического распыления (${{R}_{{{\text{физ}}}}}$) и химической реакции (${{R}_{{{\text{хим}}}}}$) [4, 28, 29]. Таким образом, снижение скорости травления $R = {{R}_{{{\text{физ}}}}} + {{R}_{{{\text{хим}}}}}$ с ростом ${{y}_{{{\text{Ar}}}}}$ может иметь место при доминировании как химического, так и физического механизмов травления. В первом случае причиной может служить снижение концентрации и плотности потока атомов брома (как основных химически активных частиц) в условиях ${{R}_{{{\text{хим}}}}}$ > ${{R}_{{{\text{физ}}}}},$ а во втором – уменьшение интенсивности ионной бомбардировки поверхности при ${{R}_{{{\text{физ}}}}}$ > ${{R}_{{{\text{хим}}}}}.$ Последний фактор также может влиять и на ${{R}_{{{\text{хим}}}}}$ при протекании химической реакции по ионно-стимулированному механизму, в режиме лимитирования потоком ионов. Поэтому для получения дополнительной информации по режимам и механизмам травления необходимы данные по электрофизическим параметрам и составу плазмы.
Электрофизические параметры и состав плазмы HBr + Ar являлись предметом подробного изучения в наших ранних работах [20, 21]. Поэтому ниже мы ограничимся кратким обсуждением лишь тех данных, которые имеют принципиальное значение для целей данного исследования. При диагностике плазмы было найдено, что увеличение ${{y}_{{{\text{Ar}}}}}$ в условиях $p,~W$ = const сопровождается ростом как температуры электронов (рис. 2а), так и концентраций заряженных частиц (рис. 2б). Отмеченное изменение ${{T}_{e}}$ является следствием снижения потерь энергии электронов в процессах колебательного и электронного возбуждения при снижении доли молекулярных компонентов в газовой фазе. Увеличение концентраций электронов (3.8 × 1010–1.6 × × 1011 см–3 при 0–75% Ar) и положительных ионов (8.9 × 1010–1.8 × 1011 см–3 при 0–75% Ar) обусловлено действие двух механизмов, а именно а) ростом эффективной частоты ионизации ${{\nu }_{{iz}}} \approx {{k}_{{iz,{\text{HBr}}}}}\left[ {{\text{HBr}}} \right] + {{k}_{{iz,{\text{Ar}}}}}\left[ {{\text{Ar}}} \right]$ (6.5 × 104–1.0 × 105 c–1 при 0–75%Ar) по причине ${{k}_{{iz,{\text{Ar}}}}}$ > ${{k}_{{iz,{\text{HBr}}}}};$ и б) снижением скоростей гибели электронов и положительных ионов в процессах диссоциативного прилипания и ион-ионной рекомбинации, соответственно. Причиной последнего эффекта является уменьшение доли электроотрицательных частиц и концентрации отрицательных ионов (${{{{n}_{ - }}} \mathord{\left/ {\vphantom {{{{n}_{ - }}} {{{n}_{e}}}}} \right. \kern-0em} {{{n}_{e}}}}$ = 1.33–0.16 при 0–75% Ar). Величина плотности ионного тока следует изменению ${{n}_{ + }}$ (рис. 2в), при этом увеличение потока ионов ${{{{\Gamma }}}_{ + }} \approx {{{{J}_{ + }}} \mathord{\left/ {\vphantom {{{{J}_{ + }}} e}} \right. \kern-0em} e}$ более значимо (в ∼2.5 раза при 0–75% Ar) по сравнению с противоположными тенденциями напряжения смещения на нижнем электроде $ - {{U}_{{dc}}}$ (в ∼1.3 раза при 0–75% Ar) (рис. 2а) и энергии ионов ${{\varepsilon }_{i}} = - e\left( {{{U}_{{dc}}} + {{U}_{f}}} \right),$ где ${{U}_{f}} = 0.5{{T}_{e}}{\text{ln}}\left( {{{{{m}_{i}}} \mathord{\left/ {\vphantom {{{{m}_{i}}} {2\pi {{m}_{e}}}}} \right. \kern-0em} {2\pi {{m}_{e}}}}} \right).$ Такая ситуация обеспечивает монотонное увеличение параметра $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }}$ (где ${{M}_{i}} = {{N}_{A}}{{m}_{i}}$ – эффективная молярная масса ионов), характеризующего интенсивность ионной бомбардировки обрабатываемой поверхности (рис. 2в) [20, 21].Из сравнения данных рис. 1а и 2в следует, что увеличение доли Ar сопровождается противоположными изменениями скорости травления и параметра $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }}.$ Это позволяет предположить, что для всех исследованных материалов а) физическое распыление не вносит принципиального вклада в наблюдаемую скорость взаимодействия; и б) скорость ионно-стимулированной химической реакции не лимитируется процессами с участием ионов. Более точное разделения вкладов ${{R}_{{{\text{физ}}}}}$ и ${{R}_{{{\text{хим}}}}}$ в наблюдаемую скорость травления каждого материала возможно при корректировке скоростей травления в плазме чистого аргона ${{R}_{{{\text{физ}},~0}}}$ (5.5 нм/мин для TiO2, 6.5 нм/мин для In2O3, 33.4 нм/мин для SnO2 и 70.2 нм/мин для ZnO) в предположении о прямо-пропорциональной взаимосвязи величин ${{R}_{{{\text{физ}}}}}$ и $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }}.$ Это позволяет в первом приближении полагать, что для смеси любого состава
(3)
${{R}_{{{\text{физ}}}}} = {{R}_{{{\text{физ,0}}}}}\frac{{\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }}}}{{\sqrt {40{{\varepsilon }_{{i,0}}}} {{{{\Gamma }}}_{{ + ,0}}}}}~,$Рис. 2.
Измеренные (сплошные линии) и расчетные (пунктир) параметры газовой фазы в зависимости от начального состава смеси HBr + Ar: 1 – температура электронов (${{T}_{e}}$); 2 – отрицательное смещение на обрабатываемой поверхности ($ - {{U}_{{dc}}}$); 3 – суммарная концентрация положительных ионов (${{n}_{ + }}$); 4 – концентрация электронов (${{n}_{e}}$); 5 – плотность ионного тока (${{J}_{ + }}$); 6 – параметр$\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }},$ характеризующий интенсивность ионной бомбардировки; 7 – плотность потока атомов брома (${{{{\Gamma }}}_{{{\text{Br}}}}}$); 8 – плотность потока атомов водорода (${{{{\Gamma }}}_{{\text{H}}}}$).
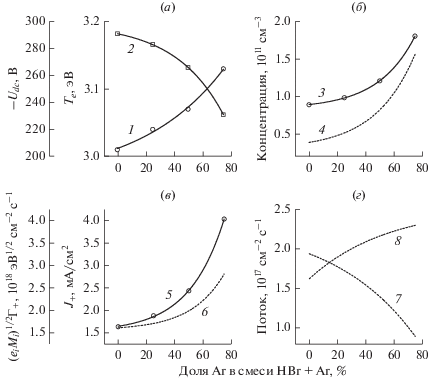
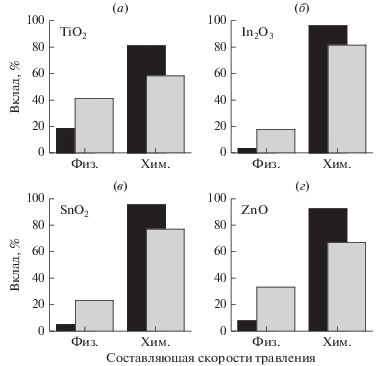
Рис. 3.
Вклады физического распыления (физ.) и ионно-стимулированной химической реакции (хим.) в наблюдаемую скорость травления в плазме чистого HBr (черные столбцы) и в смеси 25% HBr + 75% Ar (серые столбцы).
Анализ закономерностей процессов образования и гибели нейтральных частиц в плазме HBr + Ar показал, что смеси любого состава характеризуются идентичными базовыми свойствами [19–21]. В частности, генерация атомов брома обеспечивается преимущественно за счет R1 (∼20%), R3 (∼50%) и R6 (∼20%), при этом доминирующая роль R3 обусловлена а)высокими концентрациями молекул Br2 из-за быстрой конверсии 2Br → Br2 по механизму R8; и б) условием ${{k}_{3}}$ ∼ 1.3 × 10–8 см3/с > ${{k}_{1}}$ ∼ 1.6 × 10–9 см3/с (при ${{T}_{e}}$ = 3 эВ) из-за различий в пороговых энергиях и сечениях соответствующих процессов.Более высокие концентрации атомов брома по сравнению с атомами водорода ([Br]/[H] = 11.1–3.5 при 0–75% Ar, рис. 4) также являются результатом действия двух факторов. Во-первых, это значительно более низкие скорости генерации атомов H, обусловленные различием скоростей процессов R2 и R3 из-за ${{k}_{2}}$ ∼ 8.1 × 10–10 см3/с < ${{k}_{3}}.$ Соответственно, при равных скоростях образования атомов обоих сортов по R1, имеет место ситуация ${{R}_{1}} + {{R}_{2}}$ < ${{R}_{1}} + {{R}_{3}}.$ И, во-вторых, суммарная частота гибели атомов водорода в атомно-молекулярных процессах R4 и R6 практически на порядок величины превышает аналогичное значение для гетерогенной рекомбинации R8 и R9. Увеличение доли Ar в смеси HBr + Ar приводит к росту эффективность генерации атомов брома в реакциях R1 (${{k}_{1}}{{n}_{e}}$ = 60–270 с–1 при 0–75% Ar) и R3 (${{k}_{3}}{{n}_{e}}$ = 450–1900 с–1 при 0–75% Ar) за счет изменения температуры и концентрации электронов. Это приводит к тому, что концентрация (рис. 4) и плотность потока ${{{{\Gamma }}}_{{{\text{Br}}}}} \approx 0.25[{\text{Br}}]{{\upsilon }_{{T,{\text{Br}}}}}$ (рис. 2г) атомов брома снижаются значительно медленнее (в ∼2 раза при 0–75% Ar), чем это следовало бы ожидать из простого эффекта разбавления. Что касается атомов водорода, аналогичное изменение эффективности их образования в R1 и R2 дополняется снижением частоты гибели в объемных в реакциях R4 и R6. Поэтому увеличение ${{y}_{{{\text{Ar}}}}}$ в диапазоне 0–75% сопровождается монотонным ростом величин [H] (рис. 4) и ${{{{\Gamma }}}_{{\text{H}}}}$ (рис. 2г).
Рис. 4.
Концентрации нейтральных частиц в плазме чистого HBr (черные столбцы) и в смеси 25% HBr + 75% Ar (серые столбцы).

Сравнение данных рис. 1а и 2г позволяет заключить, что изменение скоростей травления всех исследованных материалов отражает поведение величины ${{{{\Gamma }}}_{{{\text{Br}}}}},$ при этом отношение ${{{{R}_{{{\text{хим}}}}}} \mathord{\left/ {\vphantom {{{{R}_{{{\text{хим}}}}}} {{{{{\Gamma }}}_{{{\text{Br}}}}}}}} \right. \kern-0em} {{{{{\Gamma }}}_{{{\text{Br}}}}}}}$ отслеживает изменение эффективной вероятности взаимодейстия $~{{\gamma }_{R}}.$ Из рис. 1б можно видеть, что увеличение доли аргона в плазмообразующей смеси сопровождается ростом ${{\gamma }_{R}}$ в системе TiO2 + Br, но приводит к близкому по характеру снижению этой величины для SnO2, In2O3 и ZnO. Очевидно, что в первом случае имеет место явная корреляция в изменениях ${{\gamma }_{R}}$ и параметра $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }},$ характеризующего интенсивность ионной бомбардировки обрабатываемой поверхности. Поэтому естественно предположить, что причиной роста ${{\gamma }_{R}}$ для TiO2, как для наиболее прочной молекулы (т.е. обладающей максимальной величиной ${{\varepsilon }_{{dis}}},$ см. табл. 2), является активация химической реакции за счет разрыва оксидных связей. Очевидно, что увеличение скорости ионного процесса TiOx → Ti + xO способствует росту числа центров хемосорбции для атомов брома и создает благоприятные условия для химической реакции Ti + xBr → TiBrx, протекающей в условиях избытка активных частиц. Снижение вероятности взаимодействия для трех остальных оксидов противоречит как характеру изменения $\sqrt {{{M}_{i}}{{\varepsilon }_{i}}} {{{{\Gamma }}}_{ + }},$ так и условию ${{T}_{S}}$ ≈ const. По нашему мнению, причиной такого поведения ${{\gamma }_{R}}$ может служить пассивация поверхности, обусловленная ростом плотности потока атомов водорода в условиях ${{{{\Gamma }}}_{{\text{H}}}}$ > ${{{{\Gamma }}}_{{{\text{Br}}}}}$ (рис. 2г). Механизм данного эффекта можно представить в виде конкурентной адсорбции атомов водорода, снижающей долю центров адсорбции, доступных для атомов брома. Вопрос о том, почему аналогичные процессы не приводят к снижению ${{\gamma }_{R}}$ для TiO2 на данном этапе остается открытым. Можно лишь предположить, что в силу максимальной разности величин ${{\varepsilon }_{{dis}}}$ для связей Ti–Br (∼439 кДж/моль) и Ti–H (∼204 кДж/моль), последние эффективно разрушаются при взаимодействии с атомами брома. Тем не менее, однозначная интерпретация роли атомов водорода в процессе травления требует дальнейших исследований.
4. ЗАКЛЮЧЕНИЕ
Проведено сравнительное исследование кинетики реактивно-ионного травления оксидов титана, индия, олова и цинка в плазме смесей HBr + Ar переменного начального состава. Установлено, что абсолютные значения скоростей травления возрастают в ряду TiO2–In2O3–SnO2–ZnO при любом фиксированном составе смеси (что согласуется с величиной энергии разрыва оксидной связи и/или летучестью продуктов взаимодействия), но снижаются с увеличением содержания Ar. Анализ этих данных с привлечением результатов диагностики и моделирования плазмы позволил заключить, что основным механизмом травления во всех случаях является ионно-стимулированная химическая реакция в режиме лимитирования потоком нейтральных частиц. Найдено, что эффективная вероятность гетерогенного взаимодействия атомов брома с ростом доли Ar в смеси увеличивается в системе TiO2 + Br, но снижается для SnO2, In2O3 и ZnO. Предположено, что причинами наблюдаемых эффектов являются активация химической реакции ионной бомбардировкой (для TiO2, как для наиболее прочной молекулы) или пассивация поверхности атомами водорода.
Публикация выполнена в рамках государственного задания ФГУ ФНЦ НИИСИ РАН (проведение фундаментальных научных исследований) по теме № 0580-2021-0006 “Фундаментальные и прикладные исследования в области литографических пределов полупроводниковых технологий и физико-химических процессов травления 3D нанометровых диэлектрических структур для развития критических технологий производства ЭКБ. Исследование и построение моделей и конструкций элементов микроэлектроники в расширенном диапазоне температур (от –60 до +300°С)”.
Список литературы
Advances in optoelectronic technology and industry. London, Taylor & Francis Group. 2020. 242 p.
Saji K.J., Jayarai M.K. Oxide thin film transistors. N.Y., Nova Science Publishers. 2017. 150 p.
Advanced plasma processing technology. John Wiley & Sons Inc. N.Y. 2008, 479 p.
Lieberman M.A., Lichtenberg A.J. Principles of plasma discharges and materials processing. N.Y., John Wiley & Sons Inc. 2005, 757 p.
Garay A.A., Hwang S.M., Chung C.W. Inductive coupled plasma reactive ion etching characteristics of TiO2 thin films // Thin Solid Films. 2015. V. 587. P. 20–27
Joo Y.-H., Woo J.-C., Kim C.-I. Dry etching properties of TiO2 thin film using inductively coupled plasma for resistive random access memory application // Trans. Electr. Electron. Mater. 2012. V. 13. № 3. P. 144–148.
Norasetthekul S., Park P.Y., Baik K.H., Lee K.P., Shin J.H., Jeong B.S., Shishodia V., Lambers E.S., Norton D.P., Pearton S.J. Dry etch chemistries for TiO2 thin films // Appl. Surf. Sci. 2001. V. 185. P. 27–33.
Lee J., Efremov A., Lee B.J. et al. Etching Characteristics and Mechanisms of TiO2 Thin Films in CF4 + Ar, Cl2 + Ar and HBr + Ar Inductively Coupled Plasmas // Plasma Chem. Plasma Process. 2016. V. 36. P. 1571–1588.
Kwon K.-H., Efremov A., Kim M., Min N.K., Jeong J., Kim K. Etching characteristics of In2O3 and SnO2 thin films in an inductively coupled HBr/Ar plasma: Effects of gas mixing ratio and bias power // Jpn. J. Appl. Phys. 2010. V. 49. P. 031103.
Park J.C., Kim J.K., Kim T.G., Lee D.W., Cho H., Kim H.S., Yoon S.J., Jung Y.-G. Dry etching of SnO2 and ZnO films in halogen-based inductively coupled plasmas // Int. J. Modern Phys. B. 2011. V. 25. № 31. P. 4237–4240.
Woo J.C., Kim G.H., Kim J.G., Kim C.I. Etching characteristic of ZnO thin films in inductively coupled plasma // Surface Coatings Technol. 2008. V. 202. P. 5705–5708.
Lee J.-M., Chang K.-M., Kim K.-K., Choi W.-K., Park S.-J. Dry etching of ZnO using an inductively coupled plasma // J. Electrochem. Soc. 2001. V. 148. № 1. P. G1–G3.
Nordheden K.J., Dineen M., Welch C. Inductively coupled plasma etching of ZnO // Proc. SPIE 6474, Zinc Oxide Materials and Devices II, 64740P (20 February 2007).
Nordheden K.J. Plasma etching of ZnO: a review // Proc. SPIE 5359, Quantum Sensing and Nanophotonic Devices, (6 July 2004).
Na S.W., Shin M.H., Chung Y.M., Han J.G., Jeung S.H., Boo J.H., Lee N.-E. Etching characteristics of ZnO thin films inchlorine-containing inductively coupled plasmas // Microelectronic Engineering. 2006. V. 83. P. 328–335.
Ham Y.-H., Efremov A., Yun S.J., Kim J.K., Min N.-K., Kwon K.-H. Etching characteristics and mechanism of ZnO thin films in inductively coupled HBr/Ar plasma // Thin Solid Films. 2009. V. 517. P. 4242–4245.
Johnson E.O., Malter L. A floating double probe method for measurements in gas discharges // Phys. Rev. 1950. V. 80. P. 58–70.
Shun’ko E.V. Langmuir probe in theory and practice. Universal Publishers. Boca Raton. 2008. 245 p.
Efremov A., Choi B.G., Nahm S., Lee H.W., Min N.K., Kwon K.H. Plasma parameters and active species kinetics in an inductively coupled HBr plasma // J. Korean Phys. Soc. 2008. V. 52. № 1. P. 48–55.
Efremov A., Lee J., Kwon K.-H. A comparative study of CF4, Cl2 and HBr + Ar inductively coupled plasmas for dry etching applications // Thin Solid Films. 2017. V. 629. P. 39–48.
Kwon K.-H., Efremov A., Kim M., Min N.K., Jeong J., Kim K. A model-based analysis of plasma parameters and composition in HBr/X (X = Ar, He, N2) inductively coupled plasmas // J. Electrochem. Soc. 2010. V. 157(5). P. H574–H579.
Efremov A., Kim J.H., Kwon K.H. A model-based comparative study of HCl and HBrplasma chemistries for dry etching purposes // Plasma Chem. Plasma. Process. 2015. V. 35. P. 1129–1142.
Curley G.A., Gatilova L., Guilet S., Bouchoule S., Gogna G.S., Sirse N., Karkari S., Booth J.P. Surface loss rates of H and Cl radicals in an inductively coupled plasma etcher derived from time-resolved electron density and optical emission measurements // J. Vac. Sci. Technol. A. 2010. V. 28. № 2. P. 360–372.
Kota G.P., Coburn J.W., Graves D.B. Heterogeneous recombination of atomic bromine and fluorine // J. Vac. Sci. Technol. A. 1999. V. 17. № 1. P. 282–290.
Rooth J.R. Industrial Plasma Engineering. IOP Publishing LTD, Philadelphia, 1995. 620 p.
Roosmalen A.J., Baggerman J.A.G., Brader S.J.H. Dry etching for VLSI. Plenum Press, N.Y., 1991, 490 p.
Sugavara M. Plasma etching: Fundamentals and applications. Oxford University Press, N.Y., 1998. 469 p.
Gray D.C., Tepermeister I., Sawin H.H. Phenomenological modeling of ion enhanced surface kinetics in fluorine-based plasma etching // J. Vac. Sci. Technol. B. 1993. V. 11. P. 1243–1257.
Efremov A.M., Rybkin V.V., Betelin V.B., Kwon K.-H. On mechanisms of oxygen influence on gas-phase parameters and silicon reactive-ion etching kinetics in HBr + Cl2 + O2 plasma // Izv. Vyssh. Uchebn. Zaved. Khim. Khim. Tekhnol. 2019. V. 62. № 10. P. 76–83.
Дополнительные материалы отсутствуют.
Инструменты
Микроэлектроника


