Химическая физика, 2022, T. 41, № 7, стр. 39-46
Влияние содержания магния и механической активации на горение в системе Ni + Al + Mg
Н. А. Кочетов *
Институт структурной макрокинетики и проблем материаловедения
им. А.Г. Мержанова Российской академии наук
Черноголовка, Россия
* E-mail: kolyan_kochetov@mail.ru
Поступила в редакцию 11.10.2021
После доработки 16.11.2021
Принята к публикации 20.11.2021
- EDN: QLXAVS
- DOI: 10.31857/S0207401X2207007X
Аннотация
Изучено влияние содержания магния и механической активации исследуемой системы Ni + Al + Mg на удлинение образцов в процессе горения, максимальную температуру и скорость горения, размеры композитных частиц и выход смеси после активации, фазовый состав и морфологию продуктов реакции. Определены параметры синтеза, при которых в полученных продуктах присутствует тройная фаза Ni2Mg3Al. Экспериментально показано, что активация приводит к увеличению скорости реакции и снижает максимальную температуру горения смеси. С увеличением содержания магния в смеси Ni + Al + Mg скорость горения сначала возрастает (при 10%-ном содержании Mg), затем уменьшается, а максимальная температура реакции убывает во всем исследованном диапазоне значений. Наблюдаемые зависимости среднего размера композитных частиц, выхода смеси после механической активации и удлинения образцов в процессе горения от содержания Mg в смеси Ni + Al + Mg не монотонны. Механическая активация приводит к образованию высокопористых продуктов синтеза.
ВВЕДЕНИЕ
Интерметаллиды на основе алюминида никеля являются перспективными конструкционными материалами и находят широкое применение благодаря сочетанию прочности при высоких температурах, высокой теплопроводности и хорошей коррозионной стойкости [1, 2]. Данные материалы получают методами порошковой металлургии, механосинтезом и самораспространяющимся высокотемпературным синтезом [1–4].
Одним из способов улучшения эксплуатационных характеристик интерметаллидов на основе смеси Ni–Al является введение в состав материала дополнительных элементов [5, 6]. Магниевые сплавы являются одними из самых легких, обладают большим значением модуля упругости, высокой механической прочностью и низкой плотностью [7, 8]. Снижение веса сплава на 10% может привести к уменьшению расхода топлива транспортного средства на 3–7% [9–11].
В системе Ni–Al–Mg, кроме двойных интерметаллидов, возможно также образование тройных фаз, в том числе фазы Гейслера – Mg2NiAl [12]. Материалы на основе фаз Гейслера привлекают интерес благодаря высокой жаропрочности и жаростойкости, трещиностойкости, низкой плотности, низкой ползучести при повышенных температурах [12–14].
Одним из распространенных способов управления реакционной способностью порошковых смесей является метод механической активации (МА) [5, 6, 15–20]. В процессе МА порошковая смесь обрабатывается в шаровой мельнице, формируются композитные частицы, состоящие из слоев исходных компонентов [18–20]. Кроме того, происходит интенсивная пластическая деформация материала, создающая высокую концентрацию дефектов кристаллической структуры и внутренние напряжения. Также после МА обычно наблюдаются увеличение площади контакта компонентов смеси и удаление оксидных и адсорбционных слоев с поверхности частиц. Благодаря этим факторам после МА возникает возможность реализовать процесс горения в смесях, не горящих в обычных условиях [19, 20].
В литературе практически отсутствует информация о влиянии содержания магния и МА на горение системы Ni + Al + Mg. Поэтому была поставлена цель – экспериментально выявить влияние содержания магния и механической активации на горение системы Ni + Al + Mg.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали образцы порошков алюминия АСД-4 (чистота 99.2 мас.%, средний размер частиц – 10 мкм), карбонильного никеля марки ПНК (чистота 99.9 мас.%, средний размер частиц – 10 мкм), и порошка магния марки МПФ-3 (чистота – 99%, средний размер частиц – 170 км). Для получения смеси Ni + Al + хMg исходные порошки перемешивали в фарфоровой ступке до визуального отсутствия неоднородностей. Коэффициент х меняли от 0 до 50 мас.%.
Механическую активацию смесей порошков проводили в механоактиваторе АГО-2 [18–23] с водяным охлаждением в атмосфере воздуха при ускорении 90g в течение 5 мин. Соотношение массы шаров к массе смеси составляло 20 : 1.
В процессе МА часть порошковой смеси налипает (“наклепывается”) на поверхность шаров и стенки барабанов активатора [18]. За выход смеси после МА принималось отношение массы не налипшей активированной смеси, которую можно легко извлечь после МА из барабана, к массе исходной порошковой смеси, закладываемой в барабан перед МА [5].
Из исходной и активированной смесей методом двухстороннего холодного прессования получали цилиндрические образцы высотой 10–20 мм и диаметром 10 мм. Давление прессования и масса образцов исходных смесей составляли 80–100 Кг/см2 и 1.5–3.9 г, для активированных смесей – 110–140 кг/см2 и 2.5–3 г. Разности давлений прессования и масс образцов обусловлены изменениями прессуемости смесей после МА, а также расчетной плотности при варьировании содержания магния в смесях.
Процесс горения спрессованных образцов протекал в инертной среде аргона при давлении 760 Торр в камере постоянного давления [5, 6, 18–23]. Видеозапись процесса фиксировали на видеокамеру через смотровое стекло. Горение образцов инициировали с верхнего торца нагретой вольфрамовой спиралью через поджигающую таблетку состава Ti + 2B, что обеспечивало стабильные условия зажигания. Измерения максимальных температур горения проводили с использованием вольфрам-рениевой термопары ВР5/ВР20 с толщиной спая 0.2 мм. Термопара вводилась с нижнего торца образца по его оси на 4 мм. При покадровой обработке видеозаписей определяли скорость горения образцов.
За относительное удлинение образцов принималось отношение высоты сгоревших к высоте исходных образцов. Значения максимальной температуры, скорости горения, относительного удлинения образцов и выхода смеси после МА рассчитывали, как среднее результатов нескольких экспериментов. Погрешность измерений не превышала 10%.
Фракционный состав и распределение частиц смеси по размерам определяли по стандартной методике на лазерном анализаторе размера частиц “Микросайзер-201C” (Россия). Погрешность измерений не превышала 1.2%.
Рентгенофазовый анализ активированных смесей, а также продуктов синтеза исходных и активированных смесей проводили на дифрактометре “Дрон-3М” (Россия), Cu(Kα)-излучение, диапазон углов 2θ от 20° до 90°. Полученные данные анализировали с использованием базы порошковых дифракционных данных PDF-2.
Морфологию частиц активированных смесей, а также микроструктуру продуктов горения, изучали методом сканирующей электронной микроскопии (СЭМ) на микроскопе “Ultra Plus” фирмы Carl Zeiss (Германия). Для исследования микроструктуры из продуктов синтеза изготавливали шлифы.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты рентгенофазового анализа активированных смесей (Ni + Al + Mg) не выявили образования новых фаз в процессе МА. Сравнительный анализ рентгенограмм активированных и исходных смесей показал уменьшение отношения интенсивности рефлексов к интенсивности фона и уширение рефлексов никеля, алюминия и магния после активации. Эти факты свидетельствуют об увеличении дефектности кристаллической структуры компонентов смесей [19, 20].
Исходные частицы никеля и алюминия имеют характерный размер порядка 10 мкм, магния – 170 мкм. В процессе МА частицы исходных металлов разрушаются, деформируются и агломерируются, формируя композитные частицы [15–21]. Фотографии композитных частиц, образовавшихся в процессе МА смеси Ni + Al + Mg с различным содержанием магния, представлены на рис. 1а–в. На фотографиях видно, что добавление в смесь Ni + Al 10 мас.% магния приводит к значительному увеличению размера композитных частиц, образующихся в процессе МА (рис. 1а, б). Увеличение содержания Mg в смеси до 20 мас.% приводит к уменьшению размеров композитных частиц, однако они по прежнему превышают размеры частиц, образовавшихся после МА смеси Ni + Al без магния (рис. 1в). На основании этих данных построена кривая зависимости среднего размера композитных частиц от содержания магния в активированной смеси Ni + Al + Mg (рис. 2а).
Рис. 1.
Фотографии композитных частиц, образовавшихся в процессе МА образцов смесей Ni + Al + Mg с различным содержанием магния (мас.%): а – 0, б – 10, в – 20.

Рис. 2.
а – Зависимость среднего размера частиц образцов активированной смеси; б – зависимость выхода смеси после МА от содержания магния в смеси Ni + Al + Mg.
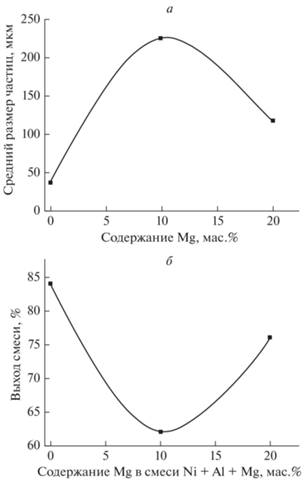
Выход смеси после МА уменьшается при добавлении в активируемую смесь 10 мас.% Mg, т.е. смесь в процессе МА налипает на стенки барабана и шары сильнее. При увеличении содержания Мg в смеси Ni + Al до 20 мас.% выход активированной смеси увеличивается (рис. 2б), т.е. на шары и стенки барабана налипает меньшее количество смеси.
Экспериментально измеренные зависимости скорости и максимальной температуры горения от процентного содержания Mg в исходной и активированной смесях Ni + Al + Mg представлены на рис. 3а, б. Благодаря увеличению площади контакта и удалению диффузионных затруднений между компонентами реакционной смеси после МА значительно (в разы) увеличивается скорость горения смеси.
Рис. 3.
Зависимости скорости горения (а), максимальной температуры горения (б), относительного удлинения образца в процессе горения (в) от различного содержания магния в образцах: ◼ – исходной смеси Ni + Al + Mg, ⚪ – активированной смеси Ni + Al + Mg.
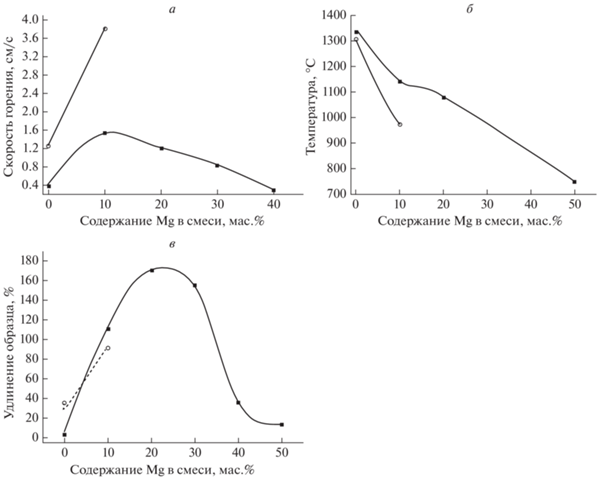
При этом максимальная температура горения смесей после их активации уменьшается, что наблюдалось и в предыдущих работах [21]. Наиболее вероятным объяснением снижения максимальных температур горения активированных смесей является предположение об образовании в процессе МА нестабильных твердых растворов [24, 25]. Было показано, что МА может приводить к образованию неравновесных перенасыщенных растворов с малым размером кристаллитов, которые, вследствие изменений структуры, могут обладать уникальными реакционными свойствами [21, 24]. Если предположить, что уменьшение максимальной температуры горения активированных смесей связано с образованием продукта из нестабильных твердых растворов в процессе МА, этот факт находит свое объяснение в рамках классической теории горения [26].
При добавлении в смесь Ni + Al 10% магния скорость горения образцов возрастала, при дальнейшем увеличении содержания магния скорость горения монотонно уменьшалась (рис. 3а). При этом максимальная температура горения уменьшалась с увеличением содержания Mg во всем исследованном диапазоне значений (рис. 3б). Магний, с одной стороны, в большинстве случаев не вступает в реакцию и, являясь инертным разбавителем, уменьшает максимальную температуру и скорость горения. С другой стороны, магний обладает достаточно низкой температурой кипения (1090 °С) и, как следствие, частично выделяется при горении в виде газа. Вероятно, из-за значительных размеров частиц (170 мкм) и высоких скоростей горения (1.5 см/с при содержании в смеси 10 мас.% Mg), магний не успевает полностью прогреваться и закипать перед фронтом горения. Соответственно, основное газовыделение Mg (кипение) происходит за фронтом горения. Дополнительное газовыделение за фронтом горения, согласно конвективно-кондуктивной модели, может привести к увеличению скорости горения [27–30], что, по-видимому, и наблюдается при добавлении в смесь Ni + Al 10% магния. При дальнейшем увеличении содержания магния в смеси начинает преобладать фактор влияния его, как инертного разбавителя, уменьшающий скорость и максимальную температуру горения.
Известно, что после МА количество примесных газов в смеси увеличивается [22, 31, 32]. Дополнительное увеличение выделения газов в процессе горения за счет магния приводит к тому, что если содержание Mg в активированной смеси достигает 20 мас.%, то сгорает небольшой фрагмент образца, который “отлетает” в процессе горения и горение прекращается. Таким образом, максимальное содержание магния в активированных смесях, при котором образец сгорал до конца, составило 10 мас.%.
В ранее опубликованных работах отмечается, что в процессе горения образцов, как правило, происходит изменение их геометрических размеров – усадка или удлинение [18, 31–33]. Удлинение образца происходит из-за выделения примесных газов за фронтом горения [18, 22, 27, 34, 35]. На рис. 3в представлена кривая зависимости относительного удлинения образцов от содержания магния в смеси. Из рисунка следует, что увеличение содержания магния до 20 мас.% приводит к увеличению удлинения образцов в процессе горения. Это происходит из-за увеличения газовыделения за фронтом горения, обусловленного кипением магния, как отмечалось выше. При дальнейшем возрастании количества магния в смеси (>20%) максимальная температура реакции становится ниже температуры кипения магния (рис. 3б). Это приводит к уменьшению газовыделения и, соответственно, роста образцов в процессе горения (рис. 3в).
Также следует отметить, что МА смеси Ni + Al + + Mg практически не повлияла на удлинение активированных образцов в процессе горения, несмотря на то что после МА, как правило, увеличивается количество примесных газов в смеси. Вероятно, это происходит из-за того, что примесные газы, вносимые в смесь Ni + Al + Mg в процессе МА, выделяются перед фронтом горения и не приводят к дополнительному удлинению образца, однако приводят к отрыву горящей части и прекращению горения образца, если содержание магния в смеси достигает 20 мас.%.
Фотографии продуктов горения исходных и активированных смесей Ni + Al + Mg с различным содержанием магния показаны на рис. 4а, б. Следует отметить, что образец из неактивированной смеси Ni + Al + 50% магния не догорел до конца (рис. 4а). На фотографиях можно видеть, что при добавлении в смесь 10 и 20% Mg возрастает удлинение образцов продуктов реакции исходных смесей. При дальнейшем увеличении количества магния в смеси рост образцов продуктов уменьшается, как отмечалось выше (рис. 4а).
Рис. 4.
Фотографии продуктов горения исходной (а) и активированной (б) смесей Ni + Al + Mg. Содержание Mg в образцах (мас.%): 1 – 0, 2 – 10, 3 – 20, 4 – 30, 5 – 40, 6 – 50 мас.%.

В процессе МА в обрабатываемую реакционную смесь вносятся дополнительные примесные газы [31, 32]. Выделение этих газов при горении образцов приводит к образованию высокопористых и непрочных продуктов синтеза (рис. 4б).
Рентгенограммы продуктов горения исходных и активированных смесей представлены на рис. 5. Основными фазами в продуктах синтеза исходных смесей являются интерметаллид NiAl и непрореагировавший Mg (в случаях, когда магний содержится в составе исходной смеси). Также в случае реакции смеси Ni + Al без магния в продуктах наблюдаются следы оксида Al2O3 и интерметаллида Ni2Al3 (рис. 5а). В случае реакции смесей Ni + Al + Mg в продуктах синтеза присутствуют следы оксида магния MgO (рис. 5а). Небольшое количество кислорода могло содержаться в аргоне, в атмосфере которого протекал процесс горения.
Рис. 5.
Результаты рентгенофазового анализа продуктов синтеза исходной (а) и активированной (б) смесей Ni + Al + Mg с различным содержанием магния. Цифрами обозначены рефлексы фаз: 1 – NiAl, 2 – Ni2Al3, 3 –Al2O3, 4 – MgO, 5 – Mg, 6 – NiMgAl.
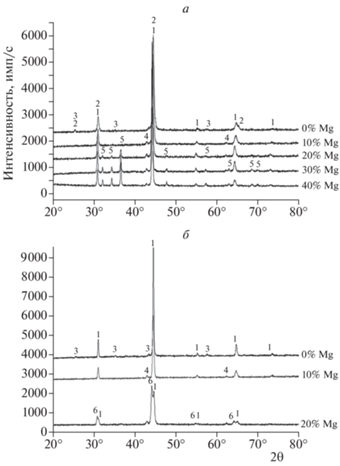
На рентгенограммах продуктов реакции активированных смесей наблюдаются рефлексы интерметаллида NiAl и следы оксидов – Al2O3 (в случае горения смеси Ni + Al без магния) и MgO (в случае горения смесей Ni + Al + Mg). Наиболее интенсивными рефлексами на рентгенограмме продуктов синтеза активированной смеси Ni + + Al + 20% Mg являются рефлексы тройной фазы NiMgAl (рис. 5б).
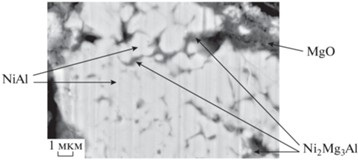
Из продуктов горения активированных смесей были изготовлены шлифы. Фотография микроструктуры продуктов синтеза активированной смеси Ni + Al + 20% Mg представлена на рис. 6. Согласно фазовой диаграмме из работы [36], многокомпонентная система Ni–Al–Mg характеризуется наличием нескольких твердых растворов со сложным составом, поэтому точная идентификация фаз затруднена. По результатам элементного энергодисперсионного анализа на фотографиях микроструктуры продуктов удалось идентифицировать фазы: NiAl (более светлые зерна) и Ni2Mg3Al (более темная область), а также MgO.
Результаты данной работы могут быть использованы при получении интерметаллидов в системе Ni + Al + Mg.
ВЫВОДЫ
1. Изучено влияние механической активации и содержания магния в системе Ni + Al + Mg на скорость и максимальную температуру горения, удлинение образцов в процессе синтеза, размеры композитных частиц и выход смеси после МА, фазовый состав и морфологию продуктов реакции.
2. Показано, что зависимости скорости горения, среднего размера композитных частиц, выхода смеси после МА и удлинения образцов в процессе горения от содержания Mg в смеси Ni + Al + + Mg не монотонны.
3. С увеличением содержания магния в смеси Ni + Al + Mg уменьшается максимальная температура горения.
4. После механической активации порошковой смеси возрастает скорость реакции и снижается максимальная температура горения образцов; кроме того, увеличивается пористость продуктов синтеза.
5. В результате синтеза системы Ni + Al + Mg получен продукт, содержащий тройную фазу Ni2Mg3Al.
6. Предложено объяснение большинству определенных зависимостей.
Автор работы признателен И.Д. Ковалеву, О.Д. Боярченко, Р.А. Кочеткову, С.Г. Вадченко, М.Л. Бусуриной, Н.И. Мухиной за помощь в экспериментах, Б.С. Сеплярскому и А.С. Щукину – за проявленный интерес и обсуждение.
Список литературы
Pogozhev Yu.S., Sanin V.N., Ikornikov D.M. et al. // Intern. J. Self-Propag. High-Temp. Synth. 2016. V. 25. № 3. P. 186; https://doi.org/10.3103/S1061386216030092
Sanin V.N., Ikornikov D.M., Andreev D.E. et al. // Ibid. 2014. V. 23. № 4. P. 232; https://doi.org/10.3103/S1061386214040098
Suryanarayana C. // Prog. Mater. Sci. 2001. V. 46. P. 1.
Wang J. // J. Alloys Compd. 2008. V. 456. P. 139.
Кочетов Н.А., Сычев А.Е. // Физика горения и взрыва. 2019. Т. 55. № 6. С. 58; https://doi.org/10.15372/FGV20190608
Кочетов Н.А., Сычев А.Е. // Физика горения и взрыва. 2020. Т. 56. № 5. С. 32; https://doi.org/10.15372/FGV20200502
Manladan S., Yusof F., Ramesh S. et al. // Intern. J. Adv. Manuf. Technol. 2016. V. 86. № 5. P. 1805; https://doi.org/10.1007/s00170-015-8258-9
Лазарев П.А., Сычев А.Е., Кочетов Н.А. и др. // Неорган. материалы. 2021. Т. 57. № 3. С. 343; https://doi.org/10.31857/S0002337X21030076
Kim H.C., Wallington T.J. // Environ. Sci. Technol. 2013. V. 47. № 12. P. 6089; https://doi.org/10.1021/es3042115
Humpenöder F., Popp A., Stevanovic M. et al. // Ibid. 2015. V. 49. № 11. P. 6731; https://doi.org/10.1021/es506201
Modaresi R., Pauliuk S., Løvik A.N. et al. // Ibid. 2014. V. 48. № 18. P. 10776; https://doi.org/10.1021/es502930
Graf T., Felser C., Parkin S.S.P. // Prog. Solid State Chem. 2011. V. 39. № 1. P. 1; https://doi.org/10.1016/j.progsolidstchem.2011.02.001
Sreenivasa Reddy P.V., Kanchana V. // J. Alloys Compd. 2014. V. 616. P. 527; https://doi.org/10.1016/J.JALLCOM.2014.07.020
Lin W., Freeman A.J. // Phys. Rev. B. 1992. V. 45. № 1. P. 61; https://doi.org/10.1103/PhysRevB.45.61
Корчагин М.А., Филимонов В.Ю., Смирнов В.Е. и др. // Физика горения и взрыва. 2010. Т. 46. № 1. С. 48.
Корчагин М.А. // Там же. 2015. Т. 51. № 5. С. 77; https://doi.org/10.15372/FGV20150509
Корчагин М.А., Григорьева Т.Ф., Бохонов Б.Б. и др. Там же. 2003. Т. 39. № 1. С. 51.
Кочетов Н.А. // Хим. физика. 2016. Т. 35. № 7. С. 49; https://doi.org/10.7868/S0207401X16070049
Кочетов Н.А., Сеплярский Б.С. // Физика горения и взрыва. 2020. Т. 56. № 3. С. 69; https://doi.org/10.15372/FGV20200307
Кочетов Н.А., Сеплярский Б.С., Щукин А.С. // Там же. 2019. Т. 55. № 3. С. 63; https://doi.org/10.15372/FGV20190308
Кочетов Н.А., Сеплярский Б.С. // Хим. физика. 2020. Т. 39. № 9. С. 39; https://doi.org/10.31857/S0207401X20090058
Кочетов Н.А., Сеплярский Б.С. // Хим. физика. 2018. Т. 37. № 10. С. 44; https://doi.org/10.1134/S0207401X18100059
Кочетов Н.А., Студеникин И.А. // Хим. физика. 2018. Т. 37. № 1. С. 43; https://doi.org/10.7868/S0207401X18010089
Wen C.E., Kobayashi K., Sugiuama A. et al. // J. Mater. Sci. 2000. V. 35. P. 2099.
Рогачёв А.С., Мукасьян А.С. // Физика горения и взрыва. 2010. Т. 46. № 3. С. 3.
Зельдович Я.Б., Баренблатт Г.И., Либрович В.Б. и др. Математическая теория горения. М.: Наука, 1980.
Сеплярский Б.С. // Докл. РАН. 2004. Т. 396. № 5. С. 640.
Сеплярский Б.С., Абзалов Н.И., Кочетков Р.А. и др. // Хим. физика. 2021. Т. 40. № 3. С. 23; https://doi.org/10.31857/S0207401X21030109
Сеплярский Б.С., Кочетков Р.А., Лисина Т.Г. и др. // Хим. физика. 2020. Т. 39. № 1. С. 31; https://doi.org/10.31857/S0207401X20010136
Сеплярский Б.С., Кочетков Р.А., Лисина Т.Г. и др. // Хим. физика. 2019. Т. 38. № 3. С. 24; https://doi.org/10.1134/S0207401X19030063
Vadchenko S.G. // Intern. J. Self-Propag. High-Temp. Synth. 2016. V. 25. № 4. P. 210; https://doi.org/10.3103/S1061386216040105
Vadchenko. S.G. // Ibid. 2015. V. 24. № 2. P. 90; https://doi.org/10.3103/S1061386215020107
Kochetov N.A., Sytschev A.E. // Mater. Chem. Phys. 2021. V. 257. P. 123727; https://doi.org/10.1016/j.matchemphys.2020.123727
Kamynina O.K., Rogachev A.S., Sytschev A.E. et al. // Intern. J. Self-Propag. High-Temp. Synth. 2004. V. 13. № 3. P.193.
Камынина О.К., Рогачев А.С., Умаров Л.М. // Физика горения и взрыва. 2003. Т. 39. № 5. С. 69.
Landolt–Börnstein – Group IV: Physical Chemistry. V. 11 (Ternary Alloy Systems). Subvolume A (Light Metal Systems). Berlin Heidelberg: Springer, 2005. Part 3. P. 154; https://doi.org/10.1007/10915998_16
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика