Журнал физической химии, 2020, T. 94, № 8, стр. 1248-1255
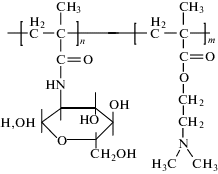
Синтез, морфология и спектральные характеристики медь-, серебро- и селенсодержащих гибридных наносистем на основе сополимера 2-деокси-2-метакриламидо-D-глюкозы с 2-диметиламиноэтилметакрилатом
С. В. Валуева a, *, М. Э. Вылегжанина a, Л. Н. Боровикова a, О. В. Назарова a, М. А. Безрукова a, Ю. И. Золотова a, Е. Ф. Панарин a, b
a Российская академия наук, Институт высокомолекулярных соединений
199004 Санкт-Петербург, Россия
b Федеральное государственное автономное образовательное учреждение высшего образования
“Санкт-Петербургский политехнический университет Петра Великого”
195251 Санкт-Петербург, Россия
* E-mail: svalu67@mail.ru
Поступила в редакцию 10.10.2019
После доработки 10.10.2019
Принята к публикации 12.11.2019
Аннотация
Синтезированы гибридные наносистемы на основе наночастиц нуль-валентной меди (Cu0), нуль-валентного серебра (Ag0) и нуль-валентного селена (Se0). Наночастицы стабилизированы водорастворимым статистическим сополимером 2-деокси-2-метакриламидо-D-глюкозы с 2-диметиламиноэтилметакрилатом. Методами УФ/видимой спектроскопии и атомно-силовой микроскопии проведено их сравнительное исследование. Показано влияние природы наночастицы на морфологические и спектральные характеристики сформировавшихся наносистем. Установлено, что восстановление в воде ионов биогенных элементов в присутствии указанного сополимера за счёт достаточно хорошей экранировки позволяет получать наноструктуры сферической формы диаметром от 80 до 250 нм.
Нанодисперсные системы биогенных элементов таких как медь, серебро и селен представляют особый интерес. Важно отметить, что переход от макро- к микро- и наноразмерам приводит к появлению новых неспецифичных видов биологической активности у этих элементов [1]. Так, медь в нанодисперсном состоянии обладает антимикробными, противовирусными, противоопухолевыми и фунгицидными свойствами, и в то же время характеризуется сравнительно низкой токсичностью (медь в нуль-валентной форме (Cu0) в 7–50 раз менее токсична, чем медь в ионной форме) [2–9]. Кроме того, наночастицы (НЧ) Cu0 стимулируют обменные процессы и проявляют полифункциональную биологическую активность [4]. Соединения меди являются контактными фунгицидами в отношении большинства фитопатогенов, ими обрабатывают сады, виноградники и овощные культуры [6–9].
НЧ нуль-валентного серебра (Ag0) проявляют сильно выраженные антимикробные свойства, причем степень антибактериального эффекта в значительной мере определяется морфологией НЧ [10, 11].
Селен – жизненно важный микроэлемент входит в состав многих ферментов-антиоксидантов и выполняет в организме функцию антиоксиданта с иммуностимулирующим и противоопухолевым действием. Существует зависимость между содержанием селена во внешней среде и частотой поражения населения злокачественными опухолями [12–15]. В клинической медицине показана эффективность использования НЧ селена в нуль-валентной форме (Se0) в комбинации с известными противоопухолевыми веществами [16].
Известно, что НЧ кинетически неустойчивы в растворе и имеют тенденцию как к агломерации, так и к окислению, поэтому их необходимо стабилизировать. Известными стабилизаторами являются высокомолекулярные соединения. Стабилизация НЧ полимерами может осуществляться как по стерическому, так и по электростерическому механизму [17], при этом тип стабилизации определяется, как природой НЧ, так и природой полимера.
Известно, что некоторые аминосодержащие полимеры [18, 19], полисахариды [20] и сополимеры на их основе, например, статистические сополимеры 2-деокси-2-метакриламидо-D-глюкозы (МАГ) с 2-диметиламиноэтилметакрилатом (ДМАЭМ) [21], способны не только выполнять функцию стабилизатора образующихся НЧ, но и служить одновременно восстановителями, например, ионов серебра и золота. В присутствии сополимеров МАГ-ДМАЭМ процесс восстановления ионов протекает с более высокой скоростью, чем в случае соответствующих гомополимеров, и образующиеся при этом НЧ характеризуются высокой стабильностью. Поэтому несомненный интерес представляет исследование как возможности использования таких сополимеров в процессе восстановления ионов биогенных элементов, так и физико-химических свойств образующихся НЧ.
Цель настоящей работы – синтез и сравнительное исследование спектральных и морфологических характеристик гибридных наносистем на основе НЧ биогенных элементов Cu0, Ag0 и Se0, стабилизированных водорастворимым сополимером (СП) 2-деокси-2-метакриламидо-D-глюкозы с 2-диметиламиноэтилметакрилатом (МАГ-ДМАЭМ)
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы
Для синтеза НЧ меди, серебра и селена использовались сульфат меди и аммиак водный (“Реахим”, Москва), гидразин гидрат (“ЭкросХим”, Москва); нитрат серебра (“ЭкросХим”, Москва) и боргидрид натрия (“Вектон”, Санкт-Петербург); селенистая и аскорбиновая кислоты (“Вектон”, Санкт-Петербург). Вещества растворялись в апирогенной воде для инъекций.
Синтез сополимера 2-деокси-2-метакриламидо-D-глюкозы с 2-диметиламиноэтилметакрилатом (МАГ-ДМАЭМ)
2-деокси-2-метакриламидо-D-глюкозу (МАГ) получали по известной методике [22]. Синтез статистического сополимера МАГ-ДМАЭМ осуществляли методом свободно-радикальной сополимеризации мономеров в запаянных ампулах в атмосфере аргона при 60°C в течение 24 ч в растворе N,N-диметилформамида в присутствии инициатора – 2,2'-азо-бис-изобутиронитрила [23]. Выход сополимера составил 81 мас. %. Состав сополимера МАГ-ДМАЭМ определяли методом 1Н ЯМР спектроскопии и потенциометрического титрования звеньев ДМАЭМ 0.1 N раствором HCl, результаты обоих методов совпадали в пределах погрешности ±3% [23]. Состав сополимера МАГ:ДМАЭМ – 31:69 мол. %.
Регистрация спектров поглощения
Спектры оптического поглощения в УФ- и видимой областях для синтезированных наносистем измеряли с помощью спектрофотометра “Specord M-40” (Карл Цейс Йена, Германия) в рабочем диапазоне от 200 до 900 нм в кварцевых кюветах с толщиной фотометрического слоя 1 см. Относительная суммарная погрешность при регистрации спектров не превышала 2%.
Диффузия и скоростная седиментация
Для исследования молекулярно-конформационных характеристик синтезированного сополимера МАГ-ДМАЭМ использовались гидродинамические методы – поступательная диффузия и скоростная седиментация. Гидродинамические характеристики определяли в водном растворителе (0.1 N HCl + 0.1 N NaCl). Коэффициент поступательной диффузии D был определен методом дисперсии границы раствор-растворитель на поляризационном диффузометре Цветкова [24] при температуре 24°С. Образование границы раствор-растворитель выполняли в подслаивающей оптической кювете длиной 3 см по ходу луча света. Фотографии интерференционных полос границы раствор-растворитель обрабатывали методом максимальной ординаты и площади под интерференционной полосой [25]. По площадям под интерференционными кривыми рассчитывали инкремент показателя преломления dn/dc (dn/dc = 0.168 см3/г). По измеренным коэффициентам диффузии D рассчитали гидродинамический радиус эквивалентной сферы Rh по уравнению Эйнштейна–Стокса: Rh = kT/6πDη0, где k – константа Больцмана, η0 – вязкость растворителя, T – температура. Коэффициенты седиментации s макромолекул в центробежном поле измерены на ультрацентрифуге фирмы МОМ 3180 (Венгрия), оборудованной поляризационно-интерферометрической приставкой [26], при скорости вращения ротора 40 × × 103 об./мин при температуре 24°С. Использовали двухсекторную кювету с образованием искусственной границы методом наслаивания. Толщина кюветы по ходу луча света 12 мм. Поляризационно-интерферометрическая оптика, установленная на ультрацентрифуге и диффузометре, позволила проводить измерения при концентрациях, не превышающих 0.15 × 10–2 г/см3, и не исследовать концентрационные зависимости. По данным седиментационно-диффузионных измерений определена абсолютная молекулярная масса MsD сополимера методом Сведберга: MsD = = (s/D)NAkT/(1 – ${v}$ρ0) , где k – постоянная Больцмана, T – абсолютная температура, ρ0 – плотность растворителя. Для фактора плавучести (1 – ${v}$ρ0) сополимера приняли значение 0.254 [25]. Значения гидродинамического инварианта Цветкова–Кленина рассчитывали по формуле [26]: А0 = = (η0D/T)(MsD[η]/100)1/3.
Изучение морфологии гибридных наносистем методом атомно-силовой микроскопии (АСМ)
Исследование морфологии гибридных наносистем сополимер/НЧ проводили методом АСМ на атомно-силовом микроскопе Nanotop NT-206 (ОДО “Микротестмашины”, Беларусь). Измерения выполняли в контактном режиме в атмосферных условиях с использованием кремниевых кантилеверов NSC11/AlBS без покрытия с коэффициентом жесткости k = 3.0 Н/м и радиусом кривизны кончика острия 10 нм. Экспериментальные данные обрабатывали с помощью программы Surface Explorer. В качестве подложки использовали слюду.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Синтез наночастиц нуль-валентной меди
НЧ нуль-валентной меди получали восстановлением сульфата меди CuSO4 · 5H2O гидразин гидратом N2H4 · H2O в водном растворе в присутствии сополимера МАГ-ДМАЭМ по реакции:
(1)
${\text{C}}{{{\text{u}}}^{{2 + }}} + {{{\text{N}}}_{{\text{2}}}}{{{\text{H}}}_{{\text{4}}}} + 4{\text{O}}{{{\text{H}}}^{ - }} \to 2{\text{C}}{{{\text{u}}}^{0}} + {{{\text{N}}}_{2}}{\kern 1pt} \uparrow \; + \;4{{{\text{H}}}_{{\text{2}}}}{\text{O}}.$Согласно работе [27], помимо наночастиц Cu0, могут образоваться в качестве примесей и НЧ оксидов меди. Чтобы избежать образования примесей реакцию восстановления проводили в два этапа. Сначала к водному раствору CuSO4 и сополимера (ССП = 0.2 мас. %) добавляли водный аммиак до рН 10.8 (цвет раствора становился ярко синим), чтобы обеспечить полное связывание Cu2+ в комплексный ион
(1')
$\begin{gathered} 2{\text{CuS}}{{{\text{O}}}_{4}} + 4{\text{N}}{{{\text{H}}}_{3}} + {{{\text{N}}}_{{\text{2}}}}{{{\text{H}}}_{{\text{4}}}} = \\ = 2{\text{C}}{{{\text{u}}}^{0}} + 2{{{\text{N}}}_{2}}{\kern 1pt} \uparrow \; + \;2{{({\text{N}}{{{\text{H}}}_{4}})}_{2}}{\text{S}}{{{\text{O}}}_{4}}. \\ \end{gathered} $рН медь-содержащих растворов составляла 10.8.
Синтез наночастиц нуль-валентного серебра
Наночастицы нуль-валентного серебра получали в результате окислительно-восстановительной реакции нитрата серебра (AgNO3) с боргидридом натрия (NaBH4):
(2)
$\begin{gathered} {\text{AgN}}{{{\text{О}}}_{3}} + {\text{NaB}}{{{\text{H}}}_{4}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} \to \\ \to {\text{A}}{{{\text{g}}}^{0}} + {\text{NaN}}{{{\text{O}}}_{3}} + {\text{B}}{{({\text{OH}})}_{3}} + {{{\text{H}}}_{2}}{\kern 1pt} \uparrow {\kern 1pt} . \\ \end{gathered} $рН серебро-содержащих растворов составляла 10.5.
Синтез наночастиц нуль-валентного селена
Синтез НЧ нуль-валентного селена осуществлялся в результате реакции между селенистой (H2SeO3) и аскорбиновой (C6H8O6) кислотами:
(3)
${{{\text{H}}}_{{\text{2}}}}{\text{Se}}{{{\text{O}}}_{3}} + 2{{{\text{C}}}_{{\text{6}}}}{{{\text{H}}}_{{\text{8}}}}{{{\text{O}}}_{6}} \to {\text{S}}{{{\text{e}}}^{0}} + 3{{{\text{H}}}_{{\text{2}}}}{\text{O}} + 2{{{\text{C}}}_{{\text{6}}}}{{{\text{H}}}_{{\text{6}}}}{{{\text{O}}}_{6}}.$Таким образом, с использованием реакций (1')–(3) были получены относительно гидрофильные НЧ металлов (Cu0 и Ag0) и гидрофобные НЧ металлоида (Se0); рН селен-содержащих растворов составляла 3.4.
Коллоидные дисперсии металлов в растворах имеют полосы поглощения в ультрафиолетовой/видимой области спектра в диапазоне 200–900 нм. Это связано с возбуждением поверхностного плазмона и является характерным свойством металлической природы частиц.
На спектрах поглощения, полученных для медь-содержащей наносистемы МАГ-ДМАЭМ/Cu0 появлялась характерная для НЧ Cu0 полоса поверхностного плазмонного резонанса (ППР) при λ = 575 нм (рис. 1) (согласно литературным данным [28] для НЧ меди ППР наблюдается в диапазоне длин волн λ = 570–590 нм). Полосы поглощения, характерные для оксидов меди, обычно наблюдаемые в диапазонах λ = 300–450 и 700–750 нм [29, 30], на данном спектре отсутствовали. Следует отметить, что МАГ-ДМАЭМ в данном диапазоне длин волн не поглощает (см. вставку на рис. 1).
Рис. 1.
Спектр поглощения для медь-содержащей наносистемы на основе сополимера МАГ-ДМАЭМ (СCu = 0.01 мас. %, CСП = 0.2 мас. %). На вставке показан спектр поглощения свободного сополимера МАГ-ДМАЭМ.
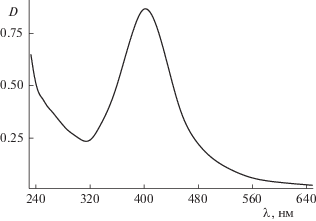
На рис. 2 приведены оптические спектры поглощения для серебро-содержащей наносистемы (МАГ-ДМАЭМ)/Ag0. Максимум полосы ППР для этой наносистемы наблюдается при λ = 400 нм, что свидетельствует об образовании в водном растворе НЧ серебра в нуль-валентном состоянии [31]. Известно, что на форму и интенсивность ППР для серебросодержащих систем влияет несколько факторов: размер и форма НЧ Ag0, их диэлектрическое окружение и тип стабилизации [32].
В случае гибридных наносистем (МАГ-ДМАЭМ)/Cu0 и (МАГ-ДМАЭМ)/Ag0 максимум полосы ППР можно объяснить межмолекулярными взаимодействиями поверхностного плазмона НЧ меди или серебра с гидрофобными группами молекул СП (с метильными и метиленовыми группами) по стерическому механизму, так как в щелочной области рН сополимер не заряжен [16].
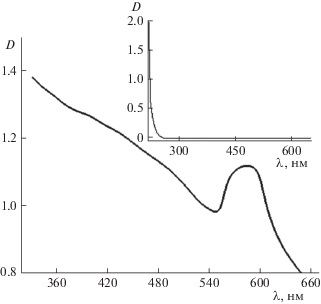
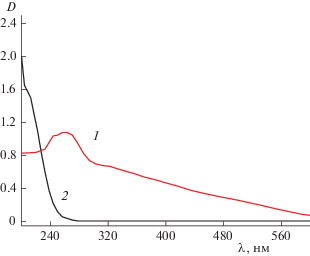
На рис. 3 представлены оптические спектры поглощения для селен-содержащей наносистемы (МАГ-ДМАЭМ)/Se0. Максимум на спектре поглощения для НЧ селена (кривая 1) наблюдался при λ = 250–265 нм, что свидетельствует об образовании в водном растворе НЧ селена в нуль-валентном состоянии (согласно литературным данным пик поглощения для свободных НЧ Se0 наблюдается при на λ = 256 нм [33]. При введении в реакционную среду сополимера МАГ-ДМАЭМ наблюдался сдвиг максимума поглощения в коротковолновую область (гипсохромный сдвиг): λ = 210–220 нм, при этом несколько изменялась и форма пика. Это свидетельствует о сильном взаимодействии между НЧ Se0 и сополимером МАГ-ДМАЭМ. Учитывая гидрофобную природу НЧ селена и наличие заряженных в кислой среде групп на СП, можно предположить, что НЧ Se0 будут взаимодействовать по электростерическому механизму как с гидрофобными группами СП (например, CH2- и CH3-группами), так и с заряженными в кислой среде группами ДМАЭМ, например, –N+(CH3)2H.
Рис. 3.
Спектры поглощения для селена без стабилизатора (1) и для системы (МАГ-ДМАЭМ)/Se0 (СSe = = 0.01 мас. %, CСП = 0.1%) (2).
В гидродинамических экспериментах для исходного сополимера были определены значения характеристической вязкости [η] = 0.30 дл/г, коэффициентов поступательной диффузии D = = 4.6 × 10–7 cм2/c (dn/dc = 0.168 см3/г) и скоростной седиментации S = 2.0 Св., оценен гидродинамический радиус Rh = 4.7 нм, рассчитаны молекулярная масса MsD = 43 000 и гидродинамический инвариант A0 = 3.6 × 10–10 эрг/град. Найденная величина A0 характерна для гибкоцепных полимеров в хороших растворителях и согласуется с результатами работы [25].
На рис. 4 представлены 3D-изображения поверхности тонкой пленки, отлитой из водного раствора медь-содержащей наносистемы на основе СП, полученные в контактном режиме при комнатной температуре на слюде методом атомно-силовой микроскопии (АСМ). На 3D-изображении наблюдаютcя структуры двух морфологических типов: во-первых, отдельные органо-неорганические сферические наноструктуры на основе НЧ Cu0 и сополимера с архитектурой типа “ядро–оболочка” (НЧ меди, окруженные органической фазой) диаметром ∼100–150 нм (табл. 1) и высотой над поверхностью подложки около 8 нм (I тип); во-вторых, эти наноструктуры собраны в агрегаты микронных размеров, имеющие сложную морфологию (II тип структуры). Между собой агрегаты соединены тяжами (“тяжевая структура” пленки), имеющими толщину 100–150 нм и высоту над поверхностью подложки не более 2 нм. В ряде случаев эти тяжи содержат сферические наноструктуры I типа. Расчетные математические параметры шероховатости пленки невелики и имеют следующие значения: средне-арифметическая шероховатость Ra = 1.0 нм, средне-квадратичная шероховатость Rq = 1.4 нм (для матрицы сканирования 5 × 5 мкм) (табл. 1). Методом малоуглового рентгеновского рассеяния для медь-содержащей наносистемы (МАГ-ДМАЭМ)/Cu0 было показано, что в этой системе формируются наноструктуры диаметром до 100 нм, а также мелкие наночастицы меди от 1 до 5 нм (наблюдали унимодальное и узко дисперсное распределение с максимумом при 3.4 нм). Последний результат свидетельствует о достаточно хорошей экранировке сополимером НЧ меди.
Рис. 4.
АСМ-изображения поверхности тонких пленок, полученных из водных растворов медь-содержащей наносистемы на основе сополимера МАГ-ДМАЭМ на слюде.
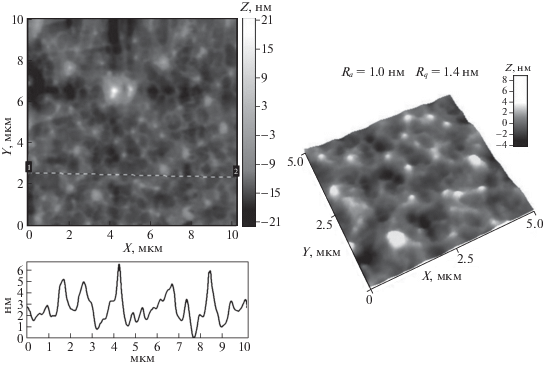
Таблица 1.
Данные по размерам и параметрам шероховатости для гибридных наносистем на основе сополимера МАГ-ДМАЭМ и НЧ Cu0, Ag0 и Se0
| Наносистема | DАСМ, нм | Ra, нм | Rq, нм |
|---|---|---|---|
| (МАГ-ДМАЭМ)/Cu0 | 100–150 | 1.0 | 1.4 |
| (МАГ-ДМАЭМ)/Ag0 | 80–150 | 2.4 | 4.3 |
| (МАГ-ДМАЭМ)/Se0 | 120–250 | 10.2 | 15.8 |
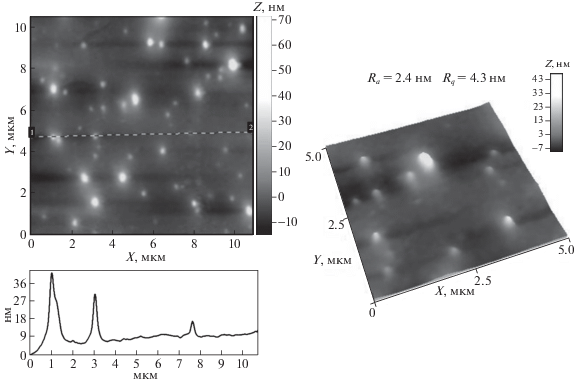
Совсем иная морфологическая картина наблюдается для серебро-содержащей наносистемы (рис. 5). Поверхность пленки менее гладкая, чем в случае медь-содержащей наносистемы: параметры шероховатости составляют Ra = 2.4 нм и Rq = 4.3 нм (для матрицы сканирования 5 × 5 мкм) (табл. 1). На поверхности пленки наблюдаются преимущественно дискретные сферические серебросодержащие наноструктуры диаметром 80–150 нм (табл. 1) и высотой над поверхностью подложки ∼13 нм, а также их агрегаты размером ∼200–400 нм и высотой над поверхностью подложки ∼40 нм.
Рис. 5.
АСМ-изображения поверхности тонких пленок, полученных из водных растворов серебро-содержащей наносистемы на основе сополимера МАГ-ДМАЭМ на слюде.
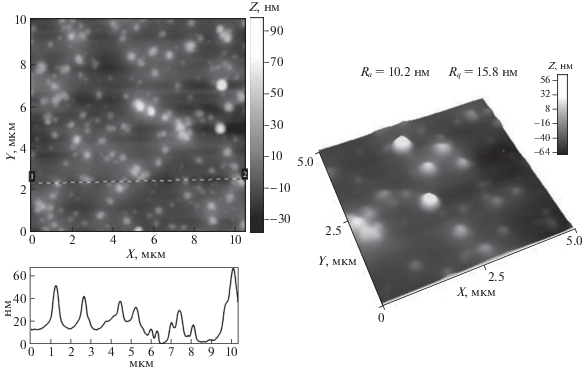
Морфологическая картина для селен-содержащей наносистемы (рис. 6) похожа на таковую для серебро-содержащей наносистемы (рис. 5). Однако, размерные характеристики и величины параметров шероховатости имеют существенно большие значения: диаметр изолированных сферических структур составляет DАСМ = 120–250 нм, а параметры шероховатости – Ra = 10.2 нм и Rq = = 15.8 нм (табл. 1); высота над поверхностью подложки ∼20 нм (для матрицы сканирования 5 × × 5 мкм). На поверхности пленки, которая имеет рыхлую структуру наблюдаются так же агрегаты размером ∼300–500 нм и высотой над поверхностью подложки ∼55 нм.
ВЫВОДЫ
1. Синтезированы новые органо-неорганические наносистемы на основе высокомолекулярного водорастворимого стабилизатора – сополимера 2-деокси-2-метакриламидо-D-глюкозы с 2-диметиламиноэтилметакрилатом и биогенных элементов меди, серебра и селена, которые продемонстрировали достаточно хорошую экранировку макромолекулами сополимера НЧ в нуль-валентном состоянии (Cu0, Ag0 и Se0).
2. Установлено, что в водном растворе изученных наносистем формируются сферические наноструктуры. Показано, что размеры (DАСМ) и параметры шероховатости (Ra и Rq) наносистем существенно зависят от природы наночастицы: медь- и серебро-содержащие наносистемы имеют меньшие значения DАСМ, Ra и Rq, чем селен-содержащие наносистемы.
Список литературы
Панарин Е.Ф. // Изв. АН. Сер. химическая. 2017. № 10. С. 1812.
Borkow G., Gabbay J. // Current Chemical Biology. 2009. V. 3. № 3. P. 272. https://doi.org/10.2174/2212796810903030272
Lansdown A.B.G., Sampson B., Rowe A. // J. Anat. 1999. V. 195. P. 375. https://doi.org/10.1046/j.1469-7580.1999.19530375.x
Shende S., Ingle A.P., Gade A., Rai M. // World J. of Microbiology and Biotechnology. 2015. V. 31. № 6. P. 865. https://doi.org/10.1007/s11274-015-1840-3
Halevas E.G., Pantazaki A.A. // Nanomed Nanotechnol J. 2018. V. 2. № 1. P. 119.
Saharan V., Sharma G., Yadav M. et al. // J. Biol. Macromol. 2015. V. 75. P. 346. https://doi.org/10.1016/j.ijbiomac.2015.01.027
Cioffi N., Torsi L., Ditaranto N. // Appl. Phys. Lett. 2004. V. 85. № 12. P. 2417. https://doi.org/10.1063/1.1794381
Abd-Elsalam K.A., Vasil’kov A.Y., Said-Galiev E.E. et al. // Eur. J. Plant Pathol. 2018. V. 151. P. 57. https://doi.org/10.1007/s10658-017-1349-8
Mekahlia S., Buzid B. // Physics Procedia. 2009. V. 2. P. 1045. https://doi.org/10.1016/j.phpro.2009.11.061
Афиногенов Г.Е., Панарин Е.Ф. Антимикробные полимеры. СПб.: Гиппократ, 1993. 264 с.
Водорастворимая серебросодержащая бактерицидная композиция и способ ее получения: Пат. 2128047 РФ, МПК 51А 61 К 31/79, А 61 К 33/38 / Афиногенов Г.Е., Копейкин В.В., Панарин Е.Ф.; заявитель и патентообладатель Афиногенов Геннадий Евгеньевич. № 95119636/14; заявл. 21.06.1995; опубл. 27.03.1999. 4 с.
Yoshizawa K., Willett W.C., Morris S.J. // J. Natl. Cancer Inst. 1998. V. 90. № 16. P. 1219. https://doi.org/10.1093/jnci/90.16.1219
Kok F.J., Hofman A., Witteman J.C.M. et al. // JAMA. 1989. V. 261. № 10. P. 1161. https://doi.org/10.1093/ajcn/45.2.462
Валуева С.В., Боровикова Л.Н., Коренева В.В. и др. // Журн. физ. химии. 2007. Т. 81. № 1. С. 1329. ISSN: 0044-4537.
Валуева С.В., Азизбекян С.Г., Кучинский М.П. и др. // Журн. “Нанотехника”. 2012. № 4(32). С. 53.
Wang Y., Hang H., Yan L. // Colloids and Surfaces B: Biointerfaces. 2016. V. 140. P. 297. https://doi.org/10.1016/j.colsurfb.2016.02.025
Mayer A.B.R. // Polym. Adv. Technol. 2001. V. 12. P. 96. https://doi.org/10.1002/1099-1581(200101/02)12:1/2<96::AID-PAT943>3.0.CO;2-G
Sun H., Gao Z., Yang L., Gao L. // Collod Polym. Sci. 2010. V. 288. P. 1713.
Ishii T., Otsuka H., Kataoka K., Nagasaki Y. // Langmuir. 2004. V. 20. P. 561.
Yakout S.M., Mostafa A.A. // Int. J. Clin. Exp. Med. 2015. V. 8. № 3. P. 3538.
Некрасова Т.Н., Золотова Ю.И., Назарова О.В. и др. // Докл. АН. 2012. Т. 446. № 5. С. 527.
Korzhikov V., Diederichs S., Nazarova O.V. et al. // J. Appl. Polymer Sci. 2008. V. 108. № 4. P. 2386. https://doi.org/10.1002/app.27292
Nazarova O.V., Leontyeva E.A., Nekrasova T.N. et al. // J. Carbohydrate Chem. 2009. V. 28. № 1. P. 37.
Eskin V.E., Frenkel S.Ya. Structure of macromolecules in solutions, National Lending Library for Sci. and Technol., Boston Spa, Yorkshire, England, 1979, 750 p.
Андреева Л.Н., Безрукова М.А., Бушин С.В. и др.// ВМС. А. 2014. Т. 56. № 4. С. 372.
Tsvetkov V.N., Lavrenko P.N., Bushin S.V. // J. Polym. Sci.: Polym. Chem. Ed. 1984. V. 22. № 11. P. 3447. https://doi.org/10.1002/pol.1984.170221160.
AL-Thabaiti S.A., Obaid A.Y., Khan Z. // Colloid Polym Sci. 2015. P. 12. https://doi.org/10.1007/s00396-015-3633-5
Guzman A., Arroyoa J., Verdea L., Rengifoa J. // Procedia Materials Science. 2015. V. 9. P. 298. https://doi.org/10.1016/j.mspro.2015.04.038
Sundaramurthy N., Parthiban C. // IRJET (International Research Journal of Engineering and Technology). 2015. V. 2. № 6. P. 332.
Rodriguez O.P., Pal. U. // J. Opt. Soc. Am. (B). 2008. V. 28. № 11. P. 2375.
Низамов Т.Р., Евстафьев И.В., Оленин А.Ю., Лисичкин Г.В. // Коллоидный журнал. 2014. Т. 76. № 4. С. 513. https://doi.org/10.7868/S0023291214040120
Moores A., Goettmann F. // New J. Chem. 2006. V. 30. № 8. P. 1121. https://doi.org/10.1039/B604038C
Бусев А.И. Колориметрические (фотометрические) методы определения неметаллов. М.: Изд-во иностр. лит-ры, 1963. 467 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии