Акустический журнал, 2022, T. 68, № 2, стр. 204-217
Подход к обнаружению аберраций при транскраниальной ультразвуковой визуализации
Д. В. Леонов a, b, *, Н. С. Кульберг a, c, **, Т. В. Яковлева c, ***, П. Д. Соловьёва b
a Научно-практический клинический центр диагностики и телемедицинских технологий ДЗ г. Москвы
127051 Москва, ул. Петровка 24, стр. 1, Россия
b Национальный исследовательский университет “МЭИ”
111250 Москва, ул. Красноказарменная 14, Россия
c Федеральный исследовательский центр “Информатика и управление” РАН
119333 Москва, ул. Вавилова 44, корп. 2, Россия
* E-mail: LeonovD.V@ya.ru
** E-mail: kulberg@ya.ru
*** E-mail: tan-ya@bk.ru
Поступила в редакцию 23.08.2021
После доработки 27.11.2021
Принята к публикации 30.11.2021
- EDN: IYSPAL
- DOI: 10.31857/S0320791922020046
Аннотация
При работе систем ультразвуковой медицинской диагностики присутствие черепных костей на пути распространения ультразвука серьезно осложняет визуализацию тканей и сосудов мозга, поскольку кости искажают ультразвуковое поле, внося в него фазовые и амплитудные аберрации. Такие искажения не всегда очевидны, поскольку полная информация об исследуемом объекте принципиально недоступна. В статье развивается новый подход к обнаружению аберраций волнового фронта, основанный на методе синтезированной апертуры. Предложен количественный параметр, характеризующий присутствие аберраций и основанный на измерении среднеквадратичной ширины углового распределения интенсивности. Приведены экспериментальные результаты на частоте 2 МГц, полученные с использованием фантома и при транскраниальном исследовании in vivo. Показано, что в присутствии аберраций величина предложенного параметра возрастает по отношению к теоретическому значению для случая без аберраций на 22–45%.
ВВЕДЕНИЕ
Транскраниальный ультразвук используется как для диагностики патологических изменений тканей и сосудов головного мозга, так и в качестве средства неинвазивного хирургического вмешательства. В диагностике используют небольшие фазированные датчики и тонкие акустические окна в черепе, а в хирургии применяют мощные излучатели большого размера в форме полусферы, способные создать поле, проходящее даже через толстые кости [1‒7]. Однако преломление волн в черепе и на границе мягких тканей снижает качество фокусировки, ведет к ухудшению контрастной и пространственных разрешающих способностей и, как следствие, потере диагностической информации [1]. Это происходит из-за различий в скорости звука и плотности между костными и мягкими тканями [2]. При транскраниальной диагностике часто используют височное окно прозрачности, поскольку оно является наиболее тонким (2.7 ± 0.9 мм соответствует хорошей акустической проницаемости [3]) и дает широкую область обзора, а его отличие от мягких тканей по скорости звука (2570–3030 м/с), при этом большое затухание (от 379 до 1210 Нп/м) и неровная поверхность вносят вклад в возникновение аберраций [4].
Существует ряд подходов, позволяющих оценить качество фокусировки ультразвукового излучения при транскраниальных исследованиях [7‒14]. Одна из первых попыток выполнить эту оценку была предложена М. Финком [15]. При этом требовалось в область интереса ввести гидрофон, который бы являлся точечным источником. Сигнал от гидрофона принимался приложенным к черепу фазированным датчиком, принятый фронт сравнивался со сферическим, рассчитывались задержки и затухание и делался вывод о качестве фокусировки. Из-за инвазивности такая процедура не получила повсеместного клинического внедрения, но стала “золотым стандартом” в научных исследованиях и получила ряд модификаций [16‒18].
Благодаря совершенствованию технологий проектирования и методов возбуждения многоэлементные фазированные решетки нашли широкое применение в хирургии [5‒7]. Однако используемые в хирургии решетки работают только на излучение, поэтому многообещающим инструментом в развитии технологий коррекции аберраций стало компьютерное моделирование распространения акустического поля от цели через ткани мозга и кости черепа до ультразвукового преобразователя [19‒22]. Этот подход основан на предварительной оценке акустических свойств черепа, получаемой из компьютерных или магниторезонансных томограмм. В рамках подхода применяются три основные категории методов численного моделирования: трассировка лучей [23], метод углового спектра [24], моделирование с учетом формы импульса [25, 26]. Последняя из перечисленных категорий методов дает наиболее точную оценку [27], но на моделирование уходит несколько часов, что затрудняет клиническое использование. В другом способе [28] градиенты магнитно-резонансной томографии, чувствительные к движению, используются для регистрации смещения тканей, вызванного акустической радиационной силой импульса, излученного фазированной решеткой ультразвукового прибора. Томограф регистрирует величину смещения тканей. Затем в сигналы, излучаемые ультразвуковым преобразователем, вводятся дополнительные задержки, и измерение повторяется. Процесс повторяется многократно. Сравнение величины смещения тканей для различных итераций позволяет оценить относительное качество фокусировки.
В статье предлагается новый подход к обнаружению искажений волнового фронта при транскраниальной ультразвуковой визуализации, основанный на методе синтеза апертуры [29]. Способ обнаружения искажений основан на оценке ширины луча; если луч достаточно узок – искажения отсутствуют. Под термином “луч” понимается область, в которой сконцентрирована наибольшая энергия излучения. Эта область характеризуется шириной луча, которая меняется с отдалением от излучателя и принимает наименьшее значение в фокусе. Расширение происходит из-за расфокусировки, вызванной прохождением луча через аберратор, вносящий дополнительные задержки, не учитываемые при формировании луча, заключающемся в когерентном суммировании сигналов со всех элементов фазированной решетки. Существенным преимуществом предлагаемого подхода является то, что для его осуществления достаточно лишь одного фазированного датчика, исследуемая область не должна непременно содержать точечные источники.
МАТЕРИАЛЫ И МЕТОДЫ
Способ обнаружения аберраций
Новый подход к обнаружению аберраций в процессе получения данных заключается в том, что ультразвуковой преобразователь прикладывают к поверхности исследуемого объекта, для улучшения контакта промежуточное пространство заполняют ультразвуковым гелем или иным звукопроводящим веществом. Затем ультразвуковой преобразователь в режиме синтезированной апертуры излучает и принимает сигналы, которые проходят предварительную обработку в тракте ультразвукового прибора.
Традиционная схема сканирования с использованием синтезированной апертуры состоит в выполнении следующих шагов:
– выбирают угол направления и формируют луч передатчика в этом направлении;
– формируют луч приемника в направлении, совпадающем с направлением луча передатчика;
– записывают в память значение принятого сигнала;
– повторяют предыдущие шаги для всех углов в диапазоне, соответствующем области интереса.
Существенным отличительным признаком предлагаемого подхода является применение особой диагностической схемы сканирования, которая состоит в выполнении следующих шагов:
– выбирают угол направления, для которого будет осуществляться коррекция;
– при формировании луча на передачу луч фиксируют на заданном угле;
– при формировании луча на прием выбирают любое направление в области интереса, не обязательно совпадающее с углом передатчика;
– записывают в память значение принятого сигнала;
– повторяют предыдущий шаг, меняя направление формирования луча на прием, и таким образом сканируют всю область зондирования.
Если аберрации отсутствуют, то при такой схеме сканирования будет получено изображение, в котором наиболее яркая область соответствует выбранному углу коррекции. Наличие аберраций приведет к расширению яркой области, т.к. аберрации расширяют луч как передатчика, так и приемника. Иллюстрация для пояснения этого принципа дана на рис. 1. На изображении слева искажающая пластина отсутствует, поэтому угловая ширина луча Δ здесь меньше, чем на изображении справа.
Рис. 1.
Пояснение способа обнаружения аберраций: 1 – секторный ультразвуковой датчик; 2 – звукопроводящее вещество; 3 – искажающий слой; Δ – угловая ширина луча.

Таким образом, в предлагаемом способе обнаружения аберраций строится функция отклика множества виртуальных точечных источников, расположенных один за одним так, что каждый обладает уникальной радиальной координатой, но угловая координата у всех одинакова. Виртуальные точечные источники формируются методом синтезированной апертуры, при этом сначала излучает первый элемент решетки, и все элементы принимают, потом излучает второй элемент, и все принимают, и т.д. для каждого элемента. Для синтеза апертуры характерно выполнение фокусировки на прием и передачу на этапе постобработки. Наличие аберраций приводит к расширению функции отклика, причем это расширение по угловой координате можно выразить через количественный параметр.
Оборудование для экспериментальной апробации
Главным элементом экспериментальной установки являлся прибор Сономед-500 производства фирмы Спектромед (г. Москва) с секторным фазированным датчиком 3.0S19 фирмы Меделком (Литва, г. Вильнюс), содержащим 64 пьезокерамических элемента с шагом 290 мкм, поперечным размером 13 мм и полосой 1.6–3.7 МГц по уровню –3 дБ. Используемый ультразвуковой диагностический прибор обладает возможностью передачи для последующей обработки на компьютере “сырых” сигналов из тракта B-визуализации, выполняемой в режиме синтезированной апертуры. Сигналы прошли некоторую предварительную обработку в тракте прибора (усиление, полосовая фильтрация, преобразование Гильберта). Сигналы сохраняются в память до поступления на вход формирователя луча. Зондирование во всех опытах выполнялось на несущей частоте 2 МГц.
Для наблюдений использовался многоцелевой фантом ATS Laboratories Model 539 [30]. Его габаритные размеры 23.4 × 20.5 × 9.5 см, скорость звука в фантоме равна 1450 м/с и коэффициент затухания ультразвука 0.5 дБ/см/МГц. Фантом изготовлен из уретанового каучука и включает в себя комбинацию нейлоновых моноволоконных линейных мишеней диаметром 120 мкм, предназначенных для точности измерения расстояний, и тканеимитирующих мишенных структур, имеющих различные размеры и контрастность. Фантом предназначен для контроля следующих характеристик: глубина проникновения, оценка осевой и поперечной разрешающей способности, разрешение по толщине, контрастная разрешающая способность. Схема расположения объектов в фантоме представлена на рис. 2.
В большинстве опытов датчик закреплялся на штативе, чтобы минимизировать влияние случайных вибраций. Аберрации вносились с помощью специально изготовленных искажающих пластин. Пластины изготавливались из силиконового геля “ЭКОН” (г. Москва), водостойкий, скорость распространения звука в котором после застывания равна 1200 м/с. При изготовлении пластин жидкий гель заливался в формы. Формы были распечатаны на 3D принтере из PLA пластика. Аберраторы представляют собой пластины размером 35 × 26 мм и толщиной от 3 до 5 мм. Форма аберратора задается гармонической функцией $A\sin ({{2\pi nl} \mathord{\left/ {\vphantom {{2\pi nl} L}} \right. \kern-0em} L})$, где $A = 1$ мм – амплитуда отклонения поверхности, $L = 20$ мм – ширина апертуры фазированного датчика, $n$ – число периодов синусоиды, помещающихся на поверхности датчика. Были изготовлены 2 аберратора: № 1 (n = 1.5) и № 2 (n = 2.5). Для крепления пластин к ультразвуковому датчику был изготовлен крепежный элемент, распечатанный на 3D принтере из PLA пластика.
Аберратор № 3 представлял собой ex-vivo височную кость, которая перед проведением исследования помещалась в барокамеру для дегазации. Как и другие аберраторы, височная кость прикладывалась к фантому ATS Laboratories Model 539, а пространство между височной костью, фантомом и датчиком заполнялось гелем для ультразвуковых исследований.
В одном из экспериментов фазированный ультразвуковой датчик через звукопроводящий гель прикладывался к голове добровольца в области височного окна акустической прозрачности. Проводилось сканирование в режиме синтеза апертуры.
При помощи устройства и способа, описанного в [16], были получены профили фазовых искажений, вносимых каждым из аберраторов. При этом сигнал от одноэлементного датчика карандашного типа, расположенного на оси, проходящей через центр сонограммы с противоположной стороны фантома или головы и выполняющего роль калибровочного источника, проходил исследуемый объект насквозь и приходил на апертуру фазированного датчика. В случае отсутствия аберратора на апертуре фазированного датчика регистрируют сферический фронт волны, излученной одноэлементным датчиком, причем радиус сферического фронта соответствует расстоянию между датчиками. Искажающие слои вносят задержки в фазовый фронт, регистрируемые по отклонению от сферичности; на основе этих задержек были получены профили, представленные на рис. 3.
Ход эксперимента
Секторный фазированный ультразвуковой датчик прикладывается к фантому так, что в область обзора попадают объекты для проверки пространственной разрешающей способности, как показано на рис. 1. Пространство между излучающей поверхностью датчика и фантомом заполняется дегазированной водой. Ультразвуковой прибор выполняет сканирование в режиме синтезированной апертуры и формирует в памяти прибора массив данных, который может быть передан на персональный компьютер для дальнейшей обработки и формирования сонограммы. В процессе сканирования сначала сигнал излучается первым элементом датчика, распространяется в фантоме, отражается, принимается всеми элементами датчика, каждый из которых записывает принятый сигнал в свой канал. После этого процедура излучения и приема повторяется для каждого из элементов датчика. В результате формируется массив P размером $K \times K \times N$, где K – число элементов датчика, N – число отсчетов по глубине.
Затем в пространство между зондирующей поверхностью датчика и фантомом помещается искажающий слой – аберратор. Процедура сканирования, описанная в предыдущем абзаце, повторяется для каждой из искажающих пластин. В результате получают B + 1 массивов данных P, где B – количество искажающих пластин. Таким образом, был получен набор данных без аберратора и 3 набора данных с различными аберраторами. Пятый набор был получен при ультразвуковом исследовании (УЗИ) головы добровольца, в других наборах использовались искажающие слои, описанные в разделе “Оборудование для экспериментальной апробации”. Полученные данные передаются на персональный компьютер для дальнейшей обработки.
На персональном компьютере в среде Microsoft Visual Studio запускается код, считывающий данные и строящий сонограмму для каждого из массивов P. Для построения сонограммы используются традиционная и предлагаемая схемы сканирования с использованием синтезированной апертуры, описанные в разделе “Способ обнаружения аберраций”. Формируются 2B + 2 сонограммы, для каждой из которых оцениваются параметры:
а) среднеквадратичная ширина углового распределения интенсивности:
(1)
$\alpha = \sqrt {\frac{{\int\limits_a^b {A\left( \varphi \right){{{\left( {\varphi - {{\varphi }_{0}}} \right)}}^{2}}d\varphi } }}{{\int\limits_a^b {A\left( \varphi \right)d\varphi } }}} ,$б) интегральная интенсивность, нормированная на значение в пике:
(2)
$\beta = \frac{{\int\limits_{ - 45^\circ }^{45^\circ } {A\left( \varphi \right)d\varphi } }}{{{{A}_{{\max }}}}},$в) центральное значение функции углового распределения интенсивности:
г) ширина главного лепестка углового распределения интенсивностей эхо-сигналов по уровню 0.707 от величины интенсивности в центре распределения:
(4)
$\left\{ \begin{gathered} \delta = {{\varphi }_{R}} - {{\varphi }_{L}}, \hfill \\ {{\varphi }_{R}} = \varphi ,\,\,\,\,{\text{если}}\,\,\,\,A\left( \varphi \right) = 0.707{{A}_{{\max }}} \wedge \varphi < 0^\circ , \hfill \\ {{\varphi }_{L}} = \varphi ,\,\,\,\,{\text{если}}\,\,\,\,A\left( \varphi \right) = 0.707{{A}_{{\max }}} \wedge \varphi > 0^\circ , \hfill \\ \end{gathered} \right.$(д) мода ε как наиболее часто встречающееся значение в наборе данных:
(5)
$\varepsilon = max\left( {\operatorname{hist} \left( {\operatorname{LPF} \left( {A\left( \varphi \right)} \right)} \right)} \right),$е) среднеквадратичная ширина углового распределения интенсивности после вычитания моды:
(6)
$\zeta = \sqrt {\frac{{\int\limits_a^b {\left( {A\left( \varphi \right) - \varepsilon } \right){{{\left( {\varphi - {{\varphi }_{0}}} \right)}}^{2}}d\varphi } }}{{\int\limits_a^b {\left( {A\left( \varphi \right) - \varepsilon } \right)d\varphi } }}} .$Параметры оценивают по угловому распределению интенсивностей, полученому на расстоянии 100 мм от апертуры ультразвукового датчика.
РЕЗУЛЬТАТЫ
Результаты исследования представлены в таблицах 1–3. Можно видеть, что в случае использования предлагаемой схемы сканирования значение параметров α, β, δ, ε и ζ больше тогда, когда есть аберрации, а значение γ, напротив, понижается. Так, наличие аберраций повышает величину среднеквадратичной ширины углового распределения интенсивности α на 31%, если сравнивать случаи отсутствия аберратора и УЗИ через кости черепа. Что касается традиционной схемы сканирования, то при ее применении не всегда удавалось определить ширину распределения δ, параметр α практически не менялся при добавлении аберратора, γ понижался, остальные параметры повышаются.
Таблица 1.
Сопоставление традиционной и предлагаемой схем сканирования
| Традиционная схема сканирования | Предлагаемая схема сканирования | |
|---|---|---|
| Сонограмма/Угловое распределение интенсивностей эхо-сигналов | Сонограмма/Угловое распределение интенсивностей эхо-сигналов | |
| Без аберраций |  |
 |
 |
 |
|
| Аберратор № 1 |  |
 |
 |
 |
|
| Аберратор № 2 | 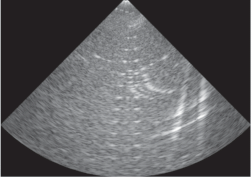 |
 |
 |
 |
|
| Аберратор № 3 |  |
 |
 |
 |
|
| УЗИ мозга |  |
 |
 |
 |
Таблица 2.
Критерии наличия аберраций при использовании предлагаемой схемы сканирования
| Среднеквадратичная ширина углового распределения интенсивности (α), градусы | Нормированная интегральная интенсивность (β), отн. ед. | Значение функции в центре (γ), отн. ед. | Ширина распределения по пороговому уровню 0.707 (δ), градусы | Значение моды (ε) | Среднеквадратичная ширина углового распределения интенсивности после вычитания моды (ζ), градусы | |
|---|---|---|---|---|---|---|
| Без аберраций | 6.2 | 27 | 147 | 4.3 | 0.101 | 5.29 |
| Аберратор № 1 | 7.5 | 47 | 45 | 5.0 | 0.260 | 6.34 |
| Аберратор № 2 | 7.9 | 63 | 54 | 17.0 | 0.293 | 7.54 |
| Аберратор № 3 | 8.0 | 77 | 7 | 9.2 | 0.511 | 7.12 |
| УЗИ мозга | 8.2 | 79 | 4 | 5.7 | 0.506 | 7.52 |
Таблица 3.
Критерии наличия аберраций при использовании традиционной схемы сканирования (символ “–" означает, что параметр не определен)
| Среднеквадратичная ширина углового распределения интенсивности (α), градусы | Нормированная интегральная интенсивность (β), отн. ед. | Значение функции в центре (γ), отн. ед. | Ширина распределения по пороговому уровню 0.707 (δ), градусы | Значение моды (ε) | Среднеквадратичная ширина углового распределения интенсивности после вычитания моды (ζ), градусы | |
|---|---|---|---|---|---|---|
| Без аберраций | 8.5 | 59 | 170 | – | 0.046 | 4.81 |
| Аберратор № 1 | 8.5 | 61 | 50 | 14.9 | 0.249 | 8.39 |
| Аберратор № 2 | 8.2 | 73 | 74 | 12.8 | 0.253 | 7.98 |
| Аберратор № 3 | 8.4 | 63 | 13 | – | 0.306 | 8.74 |
| УЗИ мозга | 8.6 | 70 | 17 | 0.7 | 0.378 | 8.72 |
ОБСУЖДЕНИЕ
Фазовые аберрации возникают, когда на пути распространения волны есть среда, скорость распространения звука в которой отлична от основной среды, и граница сред не является гладкой. Энергетические потери возникают, когда акустический импеданс одной из сред отличен от импеданса другой среды. В используемых нами аберраторах наблюдались оба эти явления.
Поскольку аберраторы № 1 и № 2 изготовлены из одного материала, коэффициент затухания ультразвуковой волны в них одинаков, но различается профиль вносимых фазовых искажений. Как видно из рис. 3, аберратор № 2 вносит больший фазовый набег, чем аберратор № 1. Количественно это подтверждается параметрами α, β и δ при использовании предлагаемой схемы сканирования. Параметр γ, напротив, возрос, хотя расширение лепестка должно было привести к его снижению. Такой результат может быть обусловлен перемещением датчика при замене аберратора и влиянием ярких точечных рассеивателей – нейлоновых струн для проверки разрешающей способности.
Ширина распределения δ, рассчитанная по пороговому уровню 0.707, как видно из табл. 2, является возможным дополнительным критерием наличия аберраций при использовании предлагаемой схемы сканирования. Присутствие аберраторов приводит к увеличению этого параметра на 16.3–295.3%. Параметр δ очень чувствителен к выбору порогового уровня и неприменим для традиционной схемы сканирования ввиду невозможности учесть существенную часть углового спектра вне порогового уровня, заданного для расчета параметра δ.
На рассчитываемые параметры могут оказывать влияние не только фазовые искажения, но и потери энергии, неизменно возникающие на границах сред и в самих средах. Если перемножить β и γ, то можно получить оценку энергетических потерь. Так, добавление аберратора № 1 привело к потере 46% интенсивности, если сравнивать со случаем без аберратора. При использовании аберратора № 3 потерялось 87% интенсивности сигнала.
Из вышеизложенного следует, что именно параметр α при использовании предлагаемой схемы сканирования может служить эффективным количественным критерием при определении наличия аберраций предлагаемым методом, поскольку в наших экспериментах он стабильно меняется на 20–31% при возникновении аберраций, тогда как в традиционной схеме он неинформативен.
Единственным требованием для осуществления предлагаемого способа обнаружений аберраций является наличие не менее двух наборов данных, полученных при использовании предлагаемой схемы сканирования и одинаковых настройках ультразвукового прибора. Причем один из наборов непременно должен содержать эталонные данные, полученные при исследовании объекта без аберраций. Второй и последующие наборы могут содержать аберрации. Именно сравнение их с эталонным набором описанным способом позволит говорить о наличии или отсутствии аберраций. Но это требование не является обязательным, поскольку можно выполнять сравнение с теоретическим значением, рассчитываемым для наших условий.
Распределение акустического давления в пространстве описывается уравнением Гельмгольца [31]:
где $\Delta = {{\nabla }^{2}}$ – это оператор Лапласа; $k = \frac{\omega }{c}$ – модуль волнового вектора; $f\left( {t,x} \right)$ – характеристика источника; t – время; $p\left( {t,x} \right)$ – искомое распределение давления, которое после регистрации фазированным датчиком можно представить в частотной области следующей функцией:(8)
$p\left( {\omega ,x} \right) = \int\limits_{ - {D \mathord{\left/ {\vphantom {D 2}} \right. \kern-0em} 2}}^{{D \mathord{\left/ {\vphantom {D 2}} \right. \kern-0em} 2}} {a\left( {x{\kern 1pt} '} \right)G\left( {\omega ,x - x{\kern 1pt} '} \right)} dx{\kern 1pt} ',$(9)
$G\left( {\omega ,r} \right) = \frac{{\exp \left( {i\frac{\omega }{c}r} \right)}}{r} = \frac{{\exp \left( {i\frac{\omega }{c}\sqrt {{{{\left( {x - x{\kern 1pt} '} \right)}}^{2}} + {{z}^{2}}} } \right)}}{{\sqrt {{{{\left( {x - x{\kern 1pt} '} \right)}}^{2}} + {{z}^{2}}} }},$Формулу (8) в приближении Френеля можно представить в следующем виде:
(10)
$p\left( {\omega ,x} \right) = \int\limits_{ - {{\xi }_{0}}}^{{{\xi }_{0}}} {\tilde {a}\left( \xi \right)\exp \left( { - ix\xi } \right)d\xi } {\kern 1pt} ,$В нашей реализации способа использовалась прямоугольная функция аподизации:
(11)
$a\left( {x{\kern 1pt} '} \right) = \left\{ \begin{gathered} 1,~\,\,\,{\text{если}}\,\,\,\frac{{ - D}}{2} < x < \frac{D}{2}, \hfill \\ 0,~\,\,\,\,{\text{иначе,}} \hfill \\ \end{gathered} \right.$(12)
$p\left( {\omega ,~x} \right) = \int\limits_{ - {{\xi }_{0}}}^{{{\xi }_{0}}} {{\text{exp}}\left( { - ix\xi } \right)d\xi } = 2\frac{{{\text{sin}}\left( {x{{\xi }_{0}}} \right)}}{x},$(14)
$p\left( {\omega ,x} \right) = 2\frac{{{\text{sin}}\left( {\frac{{x\omega D}}{{2zc}}} \right)}}{x}.$Затем рассчитывается величина параметра α относительно x, называемая ${{\alpha }_{{{\text{лин}}}}}$:
(15)
${{\alpha }_{{{\text{лин}}}}} = \sqrt {\frac{{\int\limits_{{{x}_{l}}}^{{{x}_{r}}} p \left( {{{\omega }_{0}},x} \right){{{\left( {x - {{x}_{0}}} \right)}}^{2}}dx}}{{\int\limits_{{{x}_{l}}}^{{{x}_{r}}} p \left( {{{\omega }_{0}},x} \right)dx}}} ,$(16)
$\left\{ {\begin{array}{*{20}{c}} {{{x}_{r}} = z{\text{tg}}\left( b \right),} \\ {{{x}_{l}} = z{\text{tg}}\left( a \right).} \end{array}} \right.$Далее переходим к расчету среднеквадратичной ширины (1) углового распределения интенсивности эхосигнала через рассчитанное значение :
Значение α сравнивается с полученным в результате эксперимента и делается вывод о наличии аберраций. Для наших параметров теоретическое значение среднеквадратичной ширины углового распределения интенсивности, полученное в результате численных расчетов по формуле (17), равно 5.2°. Это значение на 19% меньше, чем полученное экспериментально для фантома без аберратора. От полученных экспериментально значений для аберраторов и УЗИ мозга теоретическое значение отличается на 44–58%.
Полученное отличие экспериментального от теоретического значений достаточно велико и может быть связано с неточным заданием размера апертуры, возможным смещением несущей частоты и присутствием спекл-шума. В ходе эксперимента также рассчитывался параметр ζ, отличающийся от α смещением на значение моды. Значение моды учитывает вклад, вносимый спекл-шумом, поэтому сравнение экспериментального ζ и теоретического α дает близкие результаты. Так, теоретическое значение среднеквадратичной ширины углового распределения интенсивности α, полученное в результате численных расчетов по формуле (17), на 1.7% меньше, чем полученное экспериментально значение ζ для фантома без аберратора. От полученных экспериментально значений для аберраторов и УЗИ мозга теоретическое значение отличается на 22–45%.
Сравнение теоретического значения среднеквадратичной ширины углового распределения интенсивности α и полученного экспериментально значения ζ для традиционной схемы проводить некорректно, поскольку при традиционной схеме сканирования точечного источника в центре может и не быть, как, например, в представленном случае без аберрации, именно поэтому эмпирическое значение ζ оказалось меньше теоретического предела.
Полагаем, что предлагаемый способ обнаружения аберраций может быть особенно полезен тогда, когда недостаток априорных знаний о внутренней структуре исследуемого объекта не позволяет сделать вывод о наличии аберраций, основываясь лишь на визуальном анализе сонограммы, полученной при использовании традиционной схемы сканирования. Также он может быть полезен для развития способов коррекции аберраций. Например, нашим коллективом был разработан итеративный способ исправления аберраций, работающий на основе аппроксимации фазовых искажений полиномами малых порядков [29], в котором предлагаемый подход к обнаружению аберраций позволяет количественно определить качество коррекции и, таким образом, рассчитать, на какой итерации стоит завершить работу алгоритма коррекции. Предлагаемый способ выиграет, если подобрать функцию аподизации так, чтобы боковые лепестки убывали быстрее.
Одним из направлений развития предлагаемого способа может служить расширение его на весь кадр за счет выполнения оценки аберраций во множественных областях и построения карты качества фокусировки, как это было сделано в работе [33]. В упомянутой статье в качестве количественного критерия качества фокусировки взята ширина функции отклика точечного источника по уровню половинной интенсивности, нормированная на теоретически достижимую величину так, что при наличии аберраций качество фокусировки будет меньше единицы. Аналогичный критерий качества в нашей работе обозначен δ. Мы предпочли использовать среднеквадратичную ширину углового распределения интенсивности, как более устойчивую к шумовому влиянию.
Необходимо сказать, что если доступно несколько сонограмм, полученных с одного объекта при одинаковых условиях, то накопление для борьбы с шумами стоит выполнять путем усреднения угловых распределений интенсивности эхо-сигналов, полученных на одной глубине, но в разные моменты времени.
ЗАКЛЮЧЕНИЕ
В статье развивается новый подход к обнаружению аберраций в системах ультразвуковой диагностической визуализации, основанный на использовании метода синтезированной апертуры. В работе был исследован ряд параметров количественной оценки наличия аберраций. Из полученных результатов можно сделать вывод, что в рамках предлагаемого подхода величина среднеквадратичной ширины углового распределения интенсивности, рассчитанная после вычитания моды, является эффективным количественным критерием наличия аберраций, в то время как использование данного параметра в традиционной схеме некорректно и не позволяет обнаружить аберрации. Качественным критерием наличия искажений в исследуемой среде является расширение луча: если луч достаточно узок – искажения отсутствуют. В работе продемонстрирована возможность обнаружения аберраций предлагаемым способом на примере фантома и силиконовых пластин, моделирующих искажения, вносимые черепом, а также на примере височной кости ex vivo и с участием добровольца.
Эксперименты проводились на частоте 2 МГц и показали, что среднеквадратичная ширина углового распределения интенсивности после вычитания моды при появлении аберраций возрастает по отношению к теоретическому значению для случая без аберраций на 22–45%, когда исследования проводились по предлагаемой схеме сканирования.
Существенным преимуществом данного подхода является то, что для его осуществления достаточно лишь одного фазированного датчика, исследуемая область не должна непременно содержать точечные источники. Данный способ обнаружения аберраций не требует проведения дополнительных исследований, таких как КТ или МРТ, достаточно лишь УЗИ. Значимым является также тот факт, что с помощью разработанного подхода можно выявлять аберрации более чем на одном участке сонограммы.
Данная статья подготовлена авторским коллективом в рамках научно-исследовательской работы (№ ЕГИСУ: АААА-А20-120071090054-9) в соответствии с Программой Департамента здравоохранения города Москвы “Научное обеспечение столичного здравоохранения” на 2020–2022 года. Авторы выражают благодарность проф. Осипову Льву Васильевичу и Скосыреву Сергею Вадимовичу за предоставление сырых радиочастотных сигналов из тракта предварительной обработки ультразвукового прибора, за помощь в получении аберраторов, а также врачу ультразвуковой диагностики Григорьеву Григорию Константиновичу за обследование добровольца.
Список литературы
Fry F.J., Barger J.E. Acoustical properties of the human skull // J. Acoust. Soc. Am. 1978. V. 63. № 5. P. 1576–1590. https://doi.org/10.1121/1.381852
Clement G.T., Hynynen K. Correlation of ultrasound phase with physical skull properties // Ultrasound Med. Biol. 2002. V. 28. № 5. P. 617–624. https://doi.org/10.1016/s0301-5629(02)00503-3
Del Brutto O.H., Mera R.M., de la Luz Andrade M., Espinosa V., Castillo P.R., Zambrano M., Nader J.A. Temporal bone thickness and texture are major determinants of the high rate of insonation failures of transcranial Doppler in Amerindians (the Atahualpa Project) // J. Clin. Ultrasound. 2016. V. 44. № 1. P. 55–60. https://doi.org/10.1002/jcu.22284
Ammi A.Y., Mast T.D., Huang I.H., Abruzzo T.A., Coussios C.C., Shaw G.J., Holland C.K. Characterization of ultrasound propagation through ex-vivo human temporal bone // Ultrasound Med. Biol. 2008. V. 34. № 10. P. 1578–1589. https://doi.org/10.1016/j.ultrasmedbio.2008.02.012
Росницкий П.Б., Сапожников О.А., Гаврилов Л.Р., Хохлова В.А. Метод создания абсолютно плотных фазированных решеток для неинвазивной ультразвуковой хирургии с контролем степени нерегулярности расположения элементов // Акуст. журн. 2020. Т. 66. № 4. С. 366–376. https://doi.org/10.31857/S0320791920040097
Пестова П.А., Карзова М.М., Юлдашев П.В., Крайдер У., Хохлова В.А. Влияние траектории перемещения фокуса на равномерность температурного поля при импульсном воздействии мощного ультразвукового пучка на биологическую ткань // Акуст. журн. 2021. Т. 67. № 3. С. 250–259. https://doi.org/10.31857/S0320791921030126
Kyriakou A., Neufeld E., Werner B., Paulides M.M., Szekely G., Kuster N. A review of numerical and experimental compensation techniques for skull-induced phase aberrations in transcranial focused ultrasound // Int. J. Hyperthermia. 2014. V. 30. P. 36–46.
Rau R., Schweizer D., Vishnevskiy V., Goksel O. Ultrasound aberration correction based on local speed-of-sound map estimation // IEEE Int. Ultrasonics Symp. 2019. P. 2003–2006. https://doi.org/10.1109/ULTSYM.2019.8926297
Escoffre J.M., Bouakaz A. Therapeutic Ultrasound. Switzerland, Springer International Publishing, 2016. https://doi.org/10.1007/978-3-319-22536-4
Eames M.D., Hananel A., Snell J.W., Kassell N.F., Aubry J.F. Trans-cranial focused ultrasound without hair shaving: feasibility study in an ex vivo cadaver model // J. Ther. Ultrasound. 2014. https://doi.org/10.1186/2050-5736-1-24
Mozaffarzadeh M., Minonzio C., de Jong N., Verweij M.D., Hemm S., Daeichin V. Lamb waves and adaptive beamforming for aberration correction in medical ultrasound imaging // IEEE Trans. Ultrason. Ferroelectr. Freq. Contr. 2021. V. 68. № 1. P. 84–91. https://doi.org/10.1109/TUFFC.2020.3007345
Ferri M., Bravo J.M., Redondo J., Sánchez-Pérez J.V. Enhanced 3D-printed holographic acoustic lens for aberration correction of single-element transcranial focused ultrasound. arXiv:1805.10007.
Deng L., Hughes A., Hynynen K. A Noninvasive ultrasound resonance method for detecting skull induced phase shifts may provide a signal for adaptive focusing // IEEE Trans. Biomed. Eng. 2020. V. 67. № 9. P. 2628–2637. https://doi.org/10.1109/TBME.2020.2967033
Clement G.T., Hynynen K. A non-invasive method for focusing ultrasound through the human skull // Phys. Med. Biol. 2002. V. 47. № 8. P. 1219–1236.
Fink M. Time reversed acoustics // Phys. Today. 1997. V. 50. № 3. P. 34–40.
Osipov L.V., Kulberg N.S., Skosyrev S.V., Leonov D.V., Grigorev G.K., Vladzimirskiy A.V., Morozov S.P. Transcranial beam steering with aberration correction // Biomedical Engineering. 2021. V. 54. № 6. P. 438–442. https://doi.org/10.1007/s10527-021-10057-3
Lindsey B.D., Smith S.W. Pitch-catch phase aberration correction of multiple isoplanatic patches for 3-D transcranial ultrasound imaging // IEEE Trans. Ultrason. Ferroelectr. Freq. Contr. 2013. V. 60. P. 463–480.
Pernot M., Montaldo G., Tanter M., Fink M. ‘Ultrasonic stars’ for time-reversal focusing using induced cavitation bubbles // Appl Phys Lett. 2006. V. 88. № 3. P. 034102. https://doi.org/10.1063/1.2162700
Wu N., Shen G., Qu X., Wu H., Qiao S., Wang E., Chen Y., Wang H. An efficient and accurate parallel hybrid acoustic signal correction method for transcranial ultrasound // Phys. Med. Biol. 2020. V. 65. № 21. https://doi.org/10.1088/1361-6560/abaa25
Maimbourg G., Guilbert J., Bancel T., Houdouin A., Raybaud G., Tanter M., Aubry J.F. Computationally effective transcranial ultrasonic focusing: taking advantage of the high correlation length of the human skull // IEEE Trans. Ultrason. Ferroelectr. Freq. Contr. V. 67. № 10. P. 1993–2002. https://doi.org/10.1109/TUFFC.2020.2993718
Rosnitskiy P.B., Yuldashev P.V., Sapozhnikov O.A., Gavrilov L.R., Khokhlova V.A. Simulation of nonlinear trans-skull focusing and formation of shocks in brain using a fully populated ultrasound array with aberration correction // J. Acoust. Soc. Am. 2019. V. 146. № 3. https://doi.org/10.1121/1.5126685
Jin C., Moore D., Snell J., Paeng D.G. An open-source phase correction toolkit for transcranial focused ultrasound // BMC Biomed. Eng. 2020. https://doi.org/10.1186/s42490-020-00043-3
Winkler-Skalna A., Nowoświat A. Use of n-perturbation interval ray tracing method in predicting acoustic field distribution // Appl. Math. Modelling. 2021. V. 93. P. 426–442.
Schoen S., Arvanitis C.D. Heterogeneous angular spectrum method for trans-skull imaging and focusing // IEEE Trans. Medical Imaging. 2020. V. 39. № 5. P. 1605–1614. https://doi.org/10.1109/TMI.2019.2953872
Haqshenas S.R., Gélat P., van’t Wout E., Betcke T., Saffari N. A fast full-wave solver for calculating ultrasound propagation in the body // Ultrasonics. 2021. V. 110. https://doi.org/10.1016/j.ultras.2020.106240
Almquist S., Parker D.L., Christensen D.A. Rapid full-wave phase aberration correction method for transcranial high-intensity focused ultrasound therapies // J. Ther. Ultrasound. 2016. V. 30. № 4. https://doi.org/10.1186/s40349-016-0074-7
Marsac L., Chauvet D., La Greca R., Boch A.L., Chaumoitre K., Tanter M., Aubry J.F. Ex vivo optimisation of a heterogeneous speed of sound model of the human skull for non-invasive transcranial focused ultrasound at 1 MHz // Int. J. Hyperthermia. 2017. V. 33. № 6. P. 635–645. https://doi.org/10.1080/02656736.2017.1295322
McDannold N., Maier S.E. Magnetic resonance acoustic radiation force imaging // Med. Phys. 2008. V. 35. P. 3748–3758.
Кульберг Н.С., Леонов Д.В. Способ исправления фазовых искажений в сигналах при транскраниальной ультразвуковой визуализации. Патент на изобретение RU 2744313.
Multi-Purpose Phantom Model ATS 539. CIRS. DataSheet #041621. https://www.cirsinc.com/products/ultrasound/ats-urethane/multi-purpose-phantom/
Sommerfeld A. Partial Differential Equations in Physics. New York: Academic Press. 1949.
Duffy D.G. Green’s Functions with Applications. 2nd edition. CRC Press. 2016.
Lambert W., Cobus L.A., Couade M., Fink M., Aubry A. Reflection matrix approach for quantitative imaging of scattering media // Phys. Rev. X. 2020. V. 10. № 2. https://doi.org/10.1103/PhysRevX.10.021048
Дополнительные материалы отсутствуют.
Инструменты
Акустический журнал




