Агрохимия, 2022, № 8, стр. 69-77
Распределение мышьяка и фосфора в системе почва–растение при выращивании амаранта на почвах разных типов
М. А. Ефремова 1, *, Ф. Адимале 1
1 Санкт-Петербургский государственный аграрный университет
196601 Санкт-Петербург–Пушкин, Петербургское шоссе, 2, Россия
* E-mail: marina_efremova@mail.ru
Поступила в редакцию 28.02.2022
После доработки 31.03.2022
Принята к публикации 16.05.2022
- EDN: HBDUEX
- DOI: 10.31857/S0002188122080051
Аннотация
В лабораторном опыте на искусственно загрязненных мышьяком почвах (дерново-подзолистой среднесуглинистой почве (Albic Retisols, WRB) и солонце гидроморфном (Gleyic Solonetz Albic, WRB)) выращивали амарант (Amaranthus cruentus L.) для сравнительной оценки распределения фосфатов и As-содержащих соединений в почвах и выявлении закономерностей накопления As растениями. В почвах был определен групповой и фракционный состав фосфатов и содержание As в полученных вытяжках. При увеличении содержания мышьяка в дерново-подзолистой почве масса амаранта существенно возрастала (r = 0.90). Мышьяк, внесенный в солонец, ингибировал рост амаранта (r = –0.94). Содержание металлоида в растениях на изученных почвах изменялось прямо пропорционально его содержанию в почве. Коэффициенты накопления As амарантом из солонца гидроморфного в среднем в опыте были больше в 3.3 раза, чем из дерново-подзолистой почвы. Содержание гидролизуемых фосфатов в дерново-подзолистой почве составило 52% от валового содержания фосфора, в солонце гидроморфном – 23%. При этом в солонце 77% гидролизуемых фосфатов входило в наиболее растворимые фракции однозамещенных и двухзамещенных фосфатов, в дерново-подзолистой почве – 49% активных фосфатов. Содержание гидролизуемых As-содержащих соединений в дерново-подзолистой почве было в 3.8 раза меньше, чем в солонце при сопоставимом валовом содержании элемента в обеих почвах. В целом это обеспечило высокую доступность As растениям амаранта на солонце по сравнению с дерново-подзолистой почвой.
ВВЕДЕНИЕ
С точки зрения санитарно-гигиенической безопасности продукции растениеводства необходимо изучать влияние различных компонентов педосферы на поведение экотоксикантов в системе почва–растение. Мышьяк относится к токсикантам 1-го класса опасности. Его содержание в организме человека на 40% обусловлено потреблением продуктов, содержащих этот металлоид [1]. Таким образом, мышьяк мигрирует по пищевой цепи, первоначально накапливаясь в растениях.
Фоновые уровни содержания As в почвах мира варьируют от 0.1 до 95 мг/кг [2, 3]. Распределение мышьяка в системе почва–растение зависит от свойств почвы, в которой элемент может находиться в виде индивидуальных химических соединений различной растворимости, в адсорбированном состоянии, в составе первичных и вторичных минералов, в соединениях с органическими веществами. А.И. Перельман отнес мышьяк к слабоподвижным элементам [4]. Комплексные анионы AsO$_{2}^{ - }$, AsO$_{4}^{{3 - }}$, HAsO2–, H2AsO$_{3}^{ - }$ рассматриваются как подвижные формы As в почве [3], из них наиболее распространенная форма соединений мышьяка в условиях окружающей среды – арсенат-ион (AsO$_{4}^{{3 - }}$); мышьяк в форме арсенит-иона (AsO$_{3}^{{3 - }}$) доминирует при низких показателях окислительно-восстановительного потенциала и рН почвы. Показано, что величина показателя рН почвы оказывает важнейшее влияние на накопление мышьяка растениями из почвы [3, 5]. При этом в почвенных условиях с близкими величинами рН мышьяк менее доступен растениям из почвы с аэробной средой и высоким окислительно-восстановительным потенциалом, чем из почвы с анаэробной средой.
Мышьяк может удерживаться в твердой фазе почвы полуторными оксидами железа и алюминия путем осаждения с ними [6, 7], а также органическим веществом [8]. Гидроксиды железа наиболее активно удерживают мышьяк при рН 8.0, гидроксиды алюминия – при рН 4.0. В аналогичных условиях сорбируется почти в 3 раза больше арсенат-ионов, чем арсенит-ионов. Адсорбция As гуминовыми кислотами высока в диапазоне рН 5.0–7.0, а также при большом содержании кальция в гуминовых кислотах [9–12]. В кислой среде гуминовые кислоты могут внести больший вклад в удержание As, чем глинистые минералы и оксиды металлов [13, 14].
На поведение микроэлементов в системе почва–растение существенное влияние оказывают их химические элементы-аналоги. Химические свойства фосфора и мышьяка схожи. Элементы входят в 5-ю группу периодической системы, имеют близкие размеры атомного радиуса, величины потенциала ионизации и электроотрицательности. Оба элемента образуют оксианионы в степени окисления +5. Согласно литературным данным [6], мышьяк поступает в корневую систему растений в форме арсенатов, которые нарушают метаболизм фосфатов в организме растений (фосфорилирование и синтез АТФ). Доказательством схожести геохимического поведения мышьяка и фосфора является тот факт, что в фосфатных горных породах относительно высоко содержание As (от 6.6 до 121 мг/кг) по сравнению со средним содержанием мышьяка в нефосфатных породах (от 1.8 до 6.6 мг/кг) [2]. Фосфаты способны конкурировать с As за места сорбции в почвенной среде в экологически важных диапазонах рН [15, 16]. По данным [16, 17], конкуренция со стороны анионов PO$_{4}^{{3 - }}$ препятствует прочному закреплению оксианионов мышьяка при адсорбции частицами гидроксидов железа. Увеличение подвижности мышьяка в почве при возрастании содержания в ней фосфатов способствует накоплению металлоида растениями [18]. По другим данным, фосфор способствует снижению накопления растениями мышьяка из почвы [2, 3].
Цель работы – сравнительная оценка распределения фосфатов и As-содержащих соединений в пахотном горизонте дерново-подзолистой почвы (Albic Retisols, WRB) и солонца гидроморфного (Gleyic Solonetz Albic, WRB) и выявление закономерностей накопления As растениями амаранта (Amaranthus cruentus L.) из этих почв.
МЕТОДИКА ИССЛЕДОВАНИЯ
Опыт по исследованию накопления As амарантом из дерново- подзолистой среднесуглинистой почвы и солонца гидроморфного был заложен в лабораторных условиях. Схема опыта состояла из 6-ти вариантов, в которых были созданы различные уровни загрязнения почвы мышьяком (табл. 1). Опыт проводили в пластиковых сосудах, масса абсолютно сухой почвы в каждом сосуде составляла 300 г. Повторность опыта трехкратная.
Таблица 1.
Схема опыта
| Вариант | Доза* As, мг/кг абсолютно-сухой почвы | Валовое содержание As в почве после загрязнения (Cп), мг/кг абсолютно сухой почвы | |
|---|---|---|---|
| дпп** | солонец | ||
| 1. N200P250K250 (фон) | – | 5.2 | 4.4 |
| 2. Фон + As1 | 2 | 7.2 | 6.4 |
| 3. Фон + As2 | 4 | 9.2 | 8.4 |
| 4. Фон + As3 | 6 | 11.2 | 10.4 |
| 5. Фон + As4 | 8 | 13.2 | 12.4 |
| 6. Фон + As5 | 10 | 15.2 | 14.4 |
Валовое содержание мышьяка в почвах, отобранных для опыта, было больше предельно-допустимой концентрации элемента (ПДК) более чем в 2 раза и составляло в солонце 4.4 мг/кг почвы, в дерново-подзолистой почве – 5.2 мг/кг. Искусственное загрязнение почв экотоксикантом создавали на 5-ти уровнях за счет внесения в почву раствора Na3AsO3. В результате, валовое содержание As в почвах опыта превышало ПДК элемента в 2–7 раз.
Согласно литературным данным, овощные виды амаранта, к которым относится и Amaranthus cruentus L., требуют высокого уровня удобренности почвы [19]. В связи с этим в качестве фона в почву были внесены минеральные удобрения (мочевина, простой суперфосфат и калий сернокислый) в дозах, рекомендованных для выращивания овощных культур в вегетационных опытах [20]. После загрязнения мышьяком и внесения удобрений почву инкубировали в течение 1 мес. при комнатной температуре в лабораторном помещении, влажность почвы в течение опыта поддерживали на уровне 70% ПВ. Далее в сосуды были высеяны семена амаранта. После прорастания амаранта в каждом сосуде было оставлено по 10 растений. Уборку амаранта проводили на 27-е сут вегетации. После уборки и учета массы растений в каждом опытном варианте составляли объединенную растительную пробу для определения содержания мышьяка. К химическому анализу растения были подготовлены путем мокрого озоления в смеси концентрированных кислот НNO3 и HClO4 (1 : 5). Содержание As в подготовленных растворах определяли на атомно-абсорбционном спектрометре Varian AAS-240 VGA-77. Коэффициент накопления (КН) As амарантом определен как отношение содержания элемента в абсолютно сухой массе растений к валовому содержанию в абсолютно сухой почве. Вынос элемента растениями из почвы рассчитан как произведение их массы в сосуде на содержание в них мышьяка.
В почвах 2-х вариантов опыта, загрязненных мышьяком в количестве 6 и 10 мг/кг, был определен групповой и фракционный состав фосфатов (по методу Гинзбург и Лебедевой) [21]. Фосфаты последовательно извлекали из почвы различными растворителями. В ходе анализа сначала выделяли фракцию наиболее растворимых форм фосфатов щелочных и щелочноземельных элементов (Са-РI – аммонийно-молибдатная вытяжка). Затем извлекали фракцию менее растворимых форм фосфатов, связанных с кальцием и магнием, а также c закисными формами железа (Са-РII – ацетатно-молибдатная вытяжка). После этого выделяли фосфаты, связанные с алюминием и железом (Al-P, Fe-P – фтораммонийная и щелочная вытяжки соответственно) и, наконец, фракцию высокоосновных труднорастворимых фосфатов (Са-РIII – сернокислая вытяжка). Фосфаты всех вышеуказанных вытяжек в сумме относят к гидролизуемым или активным фосфатам почвы. Наименее растворимая часть фосфатов, оставшаяся в почве после всех химических обработок, – это негидролизуемые фосфаты. В выделенных фракциях было определено содержание мышьяка на эмиссионном спектрометре с индуктивно-связанной плазмой “Оптима-2100 DV”.
Основные результаты, полученные в исследовании, подвергали математической обработке методами корреляционного и дисперсионного анализов.
Для постановки опыта использовали солонец гидроморфный луговой нитратный высокосолончаковатый слабозасоленный глубокий малогумусный глыбистый легкого гранулометрического состава [22]. Почва для опыта была отобрана на участке приморской низменности Бенина с глубиной залегания грунтовых вод ≈3 м от поверхности и верхней границей солевых выделений на уровне 48 см от поверхности. Почва была извлечена из надсолонцового пахотного горизонта глубиной 18–20 см. Содержание органических веществ в солонце было низким (0.88%), рН$_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}$ 8.4, содержание обменного Na – 7.85 ммоль(экв)/100 г почвы, емкость катионного поглощения почвы – 23.5 ммоль(экв)/100 г [23]. Содержание подвижных соединений фосфора и калия в почве составляло соответственно: 543 мг Р2О5/кг и 215 мг K2О/кг почвы. Очень высокое содержание фосфора могло быть связано с насыщенностью верхнего горизонта почвы остатками раковин морских животных. Для солонца характерен нитратный тип засоления (табл. 2), анионы CO$_{3}^{{2 - }}$ и SO2– в водной вытяжке не обнаружены. Среди водорастворимых веществ почвы бóльшая доля приходилась на органические вещества – ≈62%.
Таблица 2.
Характеристика водной вытяжки солонца гидроморфного
| Сухой остаток | Прокаленный остаток | Анионы | Катионы | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| HCO$_{3}^{ - }$ | Cl– | NO$_{3}^{ - }$ | Σ | Ca2+ | Mg2+ | Na+ | K+ | Σ | ||
| % | ммоль/100 г почвы | |||||||||
| 0.24 | 0.09 | 0.92 | 0.88 | 1.77 | 3.57 | 0.62 | 0.27 | 2.39 | 0.55 | 3.83 |
Дерново-подзолистая среднесуглинистая почва была отобрана для опыта в Гатчинском р-не Ленинградской обл. из пахотного горизонта, мощность которого составляла 27 см. Агрохимические показатели дерново-подзолистой почвы были определены по методикам ГОСТ. Почва хорошо окультурена, для нее характерны повышенное содержание органического вещества (4.9%), нейтральная реакция среды (рHKCl 6.2), очень высокое содержание подвижного фосфора – 350 мг/кг и высокое содержание обменного калия – 185 мг/кг. Емкость катионного поглощения почвы составляла 20 ммоль(экв)/100 г.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Масса амаранта, выращенного на дерново-подзолистой почве (табл. 3), увеличивалась при возрастании содержания в ней мышьяка (r = 0.90). Эффект стимуляции роста растений под действием мышьяка наблюдали и ранее [15]. Предполагается, что он частично обусловлен стерилизацией почвы, уничтожением патогенной микрофлоры. Достоверное увеличение массы амаранта в опыте отмечено, начиная с варианта, где доза внесения As составила 6 мг/кг почвы, а общее содержание элемента равна 10.4 мг/кг абсолютно сухой почвы.
Таблица 3.
Воздушно-сухая масса амаранта и показатели накопления As амарантом из дерново-подзолистой почвы и солонца гидроморфного
| Вариант | Дерново-подзолистая почва | Солонец гидроморфный | ||||
|---|---|---|---|---|---|---|
| Мр, г/сосуд | Ср, мг/кг | Ар, мкг/сосуд | Мр, г/сосуд | Ср, мг/кг | Ар, мкг/сосуд | |
| 1. NPK (фон) | 0.067 | – | – | 0.247 | – | – |
| 2. Фон + As1 | 0.071 | 0.02 | 0.001 | 0.168 | 0.06 | 0.010 |
| 3. Фон + As2 | 0.111 | 0.09 | 0.010 | 0.140 | 0.43 | 0.060 |
| 4. Фон + As3 | 0.227 | 0.17 | 0.039 | 0.106 | 0.65 | 0.069 |
| 5. Фон + As4 | 0.202 | 0.26 | 0.053 | 0.096 | 0.65 | 0.062 |
| 6. Фон + As5 | 0.212 | 0.32 | 0.068 | 0.083 | 0.80 | 0.066 |
| Среднее | 0.148 | 0.17 | 0.034 | 0.140 | 0.52 | 0.053 |
| σ* | 0.074 | 0.12 | 0.028 | 0.061 | 0.29 | 0.024 |
| НСР05 | 0.083 | – | – | 0.127 | – | – |
| r (от Mр) | – | 0.85 | 0.89 | – | –0.98 | –0.83 |
| r (от Cп) | 0.90 | 1.0 | 0.99 | –0.94 | 0.93 | 0.74 |
Мышьяк, внесенный в солонец, ингибировал рост амаранта, масса растений снижалась при увеличении содержания As в почве (r = –0.94). При загрязнении этой почвы мышьяком в дозе 2 мг/кг (валовое содержание As равно 6.4 мг/кг) фитотоксический эффект составил 32%, достоверное снижение массы растений (57%) зафиксировано при загрязнении почвы мышьяком в количестве 6 мг/кг почвы.
Таким образом, несмотря на то что валовое содержание мышьяка в солонце гидроморфном и дерново-подзолистой почве было сопоставимым, фитотоксичность мышьяка проявилась только на солонце.
Содержание мышьяка в растениях амаранта на дерново-подзолистой почве было в среднем в 3 раза меньше, чем на солонце. Доступное для растений количество этого микроэлемента в солонце могло быть больше, чем в дерново-подзолистой почве из-за значительной щелочности почвенной среды, в которой мышьяк подвижнее в условиях хорошей аэрации обеих почв [24], созданных при проведении опыта. Кроме этого, в дерново-подзолистой почве значительно больше содержание органического вещества, которое играло существенную роль в сорбции мышьяка [3]. Следует добавить, что произрастающие на солонце растения были ослаблены солевым стрессом, и это, вероятно, снижало избирательную способность корневой системы растений по отношению к токсичному элементу.
Концентрация As в растениях амаранта возрастала прямо пропорционально валовому содержанию металлоида как в дерново-подзолистой почве (r = 1.0), так и в солонце (r = 0.93).
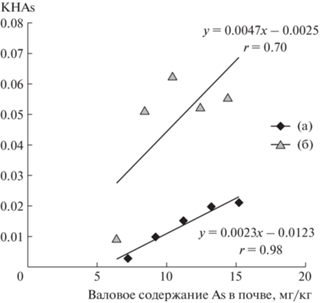
Связь между коэффициентами накопления мышьяка амарантом и валовым содержанием элемента в дерново-подзолистой почве также описали прямолинейной зависимостью (рис. 1), корреляционная связь между этими показателями была тесной (r = 0.98), существенная на 5%-ном уровне значимости. Для солонца линейная зависимость между данными показателями была менее выражена, корреляционная связь несущественна. При увеличении валового содержания мышьяка в солонце >10.4 мг/кг концентрация As в растениях, коэффициент накопления и вынос этого элемента амарантом не изменялись на фоне снижения массы растений.
Рис. 1.
Зависимость коэффициентов накопления As амарантом от его валового содержания в почве (а – дерново-подзолистая почва, б – солонец).
Согласно литературным данным [5, 15–18], поведение химических элементов-аналогов – фосфора и мышьяка в системе почва–растение имеет общие черты, что способствует изучению механизма распределения мышьяка в почве через распределение фосфора. В двух вариантах опыта, при загрязнении почвы As в дозах 6 и 10 мг/кг почвы определили фракционный и групповой состав фосфатов. Увеличение загрязнения дерново-подзолистой почвы мышьяком привело к возрастанию 2-х активных фракций гидролизумых фосфатов: однозамещенных фосфатов кальция (Ca-PI) и фосфатов алюминия (Al-P). Наиболее заметно, в 2.5 раза, возросло содержание однозамещенных фосфатов (табл. 4). Сравнительный анализ этих данных позволил предположить, что внесение мышьяка в дерново-подзолистую почву способствовало снижению активности сообщества микроорганизмов, в том числе микроорганизмов, мобилизующих фосфор из почвы. В итоге, в варианте с более высокой степенью загрязнения почвы мышьяком для растений стала доступной более значимая, с точки зрения их питания, доля общего количества макроэлемента. В этих условиях достоверно возрастала масса амаранта (табл. 3).
Таблица 4.
Фракции фосфатов и As-содержащих соединений в почвах разных типов
| Доза As, мг/кг почвы | Вытяжки | Σ | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| аммонийно- молибдатная | ацетатно- молибдатная | фтор- аммонийная | щелочная | сернокислая | |||||||
| Ca-PI | Ca-PII | Al-P | Fe-P | Ca-PIII | |||||||
| Фосфаты | |||||||||||
| Дерново-подзолистая среднесуглинистая почва | |||||||||||
| мг/кг | %* | мг/кг | % | мг/кг | % | мг/кг | % | мг/кг | % | мг/кг | |
| 6 | 214 | 7.2 | 454 | 15.2 | 213 | 7.1 | 251 | 8.4 | 395 | 13.2 | 1527 |
| 10 | 534 | 17.8 | 334 | 11.2 | 245 | 8.2 | 219 | 7.3 | 267 | 8.9 | 1599 |
| Среднее | 374 | 12.5 | 394 | 13.2 | 229 | 7.6 | 235 | 7.9 | 331 | 11.0 | 1563 |
| σ | 226 | – | 85 | – | 23 | – | 23 | 90 | – | 51 | |
| Солонец гидроморфный | |||||||||||
| 6 | 533 | 9.4 | 517 | 9.1 | 182 | 3.2 | 25.8 | 0.4 | 93.8 | 1.6 | 1352 |
| 10 | 533 | 9.4 | 493 | 8.7 | 164 | 2.9 | 18.7 | 0.3 | 90.6 | 1.6 | 1299 |
| Среднее | 533 | 9.4 | 517 | 9.1 | 182 | 3.2 | 25.8 | 0.4 | 93.8 | 1.6 | 1352 |
| σ | 0.0 | – | 17 | – | 13 | – | 5.0 | – | 2.3 | – | 38 |
| As-содержащие соединения | |||||||||||
| Дерново-подзолистая среднесуглинистая почва | |||||||||||
| мг/кг | %* | мг/кг | % | мг/кг | % | мг/кг | % | мг/кг | % | мг/кг | |
| 6 | 1.8 | 16.2 | –** | – | – | – | – | – | 1.5 | 13.4 | 3.3 |
| 10 | 1.2 | 7.8 | – | – | – | – | – | – | 1.5 | 9.7 | 2.7 |
| Среднее | 1.5 | 12.0 | – | – | – | – | – | – | 1.5 | 11.5 | 3.0 |
| σ | 0.5 | 5.9 | – | – | – | – | – | – | 0.0 | – | 0.4 |
| Солонец гидроморфный | |||||||||||
| 6 | 9.7 | 93.6 | – | – | – | – | – | – | – | – | 9.7 |
| 10 | 9.9 | 68.8 | – | – | – | – | 0.7 | 4.9 | 1.7 | 11.5 | 12.3 |
| Среднее | 9.8 | 81.2 | – | – | – | – | – | – | – | – | 11.0 |
| σ | 0.1 | 17.5 | – | – | – | – | – | – | – | – | 1.8 |
В среднем в 2-х вариантах отмечено высокое содержание гидролизуемых фосфатов в дерново-подзолистой почве – 52.2% от общего содержания почвенных фосфатов (рис. 2), что объясняется внесением удобрений. Гидролизуемые фосфаты были относительно равномерно распределены по выделенным фракциям (рис. 3).
Рис. 2.
Групповой состав фосфатов почв разных типов (% от валового содержания фосфора в почве): (а) – дерново-подзолистая почвы, (б) – солонец.

Рис. 3.
Фракционный состав фосфатов в почвах разных типов, % от общего содержания гидролизуемых фосфатов.

Несмотря на применение удобрений на солонце, в групповом составе фосфатов гидролизуемые соединения фосфора составили только 23% (рис. 2). Количество негидролизуемых фосфатов в солонце было в 3 раза больше, чем в дерново-подзолистой почве. Можно предположить, что запас нерастворимых соединений фосфора обеспечен большим содержанием в солонце обломков раковин морских животных, содержащих этот элемент в своем составе.
Среди гидролизуемых фосфатов в солонце гидроморфном наибольшую долю занимали их наиболее растворимые фракции: однозамещенные и двухзамещенные фосфаты, которые включали 77% активного фосфора почвы (рис. 3). Абсолютное содержание этих фракций фосфатов в солонце было в 1.4 раза больше, чем в дерново-подзолистой почве. По-видимому, к ним относятся не только фосфаты кальция, но в значительной степени – фосфаты натрия, т.к. этот элемент преобладал в водной вытяжке из почвы (табл. 2).
Данные содержания мышьяка в вытяжках, выполненных по методу Гинзбург и Лебедевой, показали, что после загрязнения дерново-подзолистой почвы As прочно закрепился в ее твердой фазе, т.к. доля активных соединений As была невысокой и в среднем в 2-х вариантах опыта составила 23.5% (табл. 4). При этом мышьяк гидролизуемых соединений равномерно распределился между легкорастворимой фракцией однозамещенных фосфатов кальция и фракцией труднорастворимых трехосновных фосфатов кальция. Предположительно, к этим фракциям приурочены соответственно однозамещенные арсенаты (арсениты) кальция и трехзамещенные арсенаты. Содержание микроэлемента в других фракциях было меньше предела обнаружения.
В варианте с максимальным загрязнением солонца мышьяком количество гидролизуемых соединений мышьяка составило 85% от общего содержания этого элемента в почве (рис. 4). Среди гидролизуемых соединений металлоида наиболее велика была доля As-содержащих соединений во фракции однозамещенных фосфатов почвы (рис. 5). Значительное содержание мышьяка в составе наиболее подвижной фракции было связано с высоким показателем рН почвы, что согласовалось с данными работы [24]. По-видимому, мышьяк этой фракции солонца был представлен днозамещенными арсенатами кальция и натрия. В среднем в 2-х вариантах опыта количество гидролизуемых соединений As в солонце было в 3.8 раза больше, чем в дерново-подзолистой почве (рис. 4). Вследствие этого средняя в опыте величина КН As растениями амаранта на этой почве была в 3.4 раза больше, чем на дерново-подзолистой почве.
Рис. 4.
Содержание мышьяка в разных группах фосфатов: (а) – гидролизуемые фосфаты, (б) – негидролизуемые фосфаты (на примере варианта с максимальным загрязнением почвы мышьяком).

Рис. 5.
Содержание мышьяка в разных фракциях гидролизуемых фосфатов (на примере варианта с максимальным загрязнением почвы мышьяком).

Так как масса амаранта, произраставшего на почвах 2-х типов, в среднем существенно не различалась (табл. 2), то на единицу массы растений на солонце в среднем приходилось в 6.5 раза больше легкоподвижного мышьяка (аммонийно-молибдатная вытяжка), чем на дерново-подзолистой почве.
ВЫВОДЫ
1. При увеличении содержания мышьяка в дерново-подзолистой почве масса растений амаранта существенно возрастала (r = 0.90). Мышьяк, внесенный в солонец, ингибировал рост амаранта (r = –0.94), при этом достоверное снижение массы растений по отношению к контролю зарегистрировано при валовом содержании As в почве равном 10.4 мг/кг.
2. Содержание As в растениях амаранта как на дерново-подзолистой почве, так и на солонце, возрастало прямо пропорционально степени загрязнения почвы токсикантом (r = 1.0 и r = 0.93 соответственно).
3. Коэффициенты накопления As амарантом из солонца гидроморфного в среднем в опыте были в 3.3 раза больше, чем из дерново-подзолистой почвы. По-видимому, доступное для растений количество мышьяка в солонце гидроморфном было больше, чем в дерново-подзолистой среднесуглинистой почве из-за более высокого показателя рН солонца, более высокого содержания органического вещества в дерново-подзолистой почве, а также из-за условий солевого стресса, в которых оказались растения амаранта при выращивании на солонце.
4. Через 2 мес после внесения простого суперфосфата содержание гидролизуемых фосфатов в дерново-подзолистой почве составило 52% от валового содержания фосфора, в солонце гидроморфном – 23%. В солонце на долю наиболее растворимых фракций однозамещенных и двухзамещенных фосфатов пришлось 77% гидролизуемых фосфатов, в дерново-подзолистой почве – 49% активных фосфатов.
5. Содержание гидролизуемых As-содержащих соединений в дерново-подзолистой почве было в 3.8 раза меньше, чем в солонце гидроморфном при сопоставимом валовом содержании элемента в обеих почвах. В солонце однозамещенные соединения мышьяка составили 89% от общего количества гидролизуемых соединений металлоида. Вероятно, это обеспечило высокую доступность As растениям амаранта на солонце по сравнению с дерново-подзолистой почвой.
Список литературы
Colangelo E.P., Guerinot M.L. Put the metal to the petal: metal uptake and transport throughout plants // Curr. Opin. Plant Biol. 2006. V. 9. P. 322–330.
Саркар Д., Датта Р. Концентрация и биодоступность мышьяка в почвах с разными свойствами: исследование почв во Флориде // Микроэлементы в окружающей среде: биогеохимия, биотехнология и биоремедиация / Под ред. Прасада М.Н.В., Саджвана К.С., Найду Р. М.: ФИЗМАТЛИТ, 2009. С. 104–122.
Кабата-Пендиас А., Пендиас Х. Микроэлементы в почвах и растениях. М.: Изд-во “Мир”, 1989. 439 с.
Перельман А.И. Геохимия. М.: Высш. шк., 1989. 527 с.
Talukder A.S.M.H.M., Meisner C.A., Sarkar M.A.R., Islam M.S., Sayre K.D., Duxbury J.M., Lauren J.G. Effect of water management, arsenic and phosphorus levels on rice in a high-arsenic soil–water system: II. Arsenic uptake // Ecotoxicol. Environ. Saf. 2012. V. 80. P. 145–151.
Awasthi S., Chauhan R., Srivastava S., Tripathi R.D. The journey of arsenic from soil to rice // Front. Plant Sci. V. 8: 1007. https://doi.org/10.3389/fpls.2017.01007
Jacobs L.W., Syers J.K., Keeney D.R. Arsenic sorption by soils // Soil Sci. Soc. Amer. J. 1970. V. 34. Is. 5. P. 750–754.
Beesley L., Inneh O.S., Norton G.J., Moreno-Jimenez E., Pardo T., Clementer R., Dawson J.J.C. Assessing the influence of compost and biochar amendments on the mobility and toxicity of metals and arsenic in a naturally contaminated mine soil // Environ. Pollut. 2014. V. 186. P. 195–202.
Виноградов А.П. Геохимия редких и рассеянных элементов в почвах. М.: Изд-во АН СССР, 1982. 283 с.
Hu H., Allard B., Grimvall A. Influence of pH and organic substance on the adsorption of As(V) on geologic materials // Water Air Soil Pollut. 1988. V. 40. P. 293–305.
Weng L., Van Riemsdijk W.H., Hiemstra T. Effects of fulvic and humic acids on arsenate adsorption to goethite: experiments and modeling // Environ. Sci. Technol. 2009. V. 43(19). P. 7198–7204.
Ильин В.Б., Сысо А.И. Микроэлементы и тяжелые металлы в почвах и растениях Новосибирской области. Новосибирск: Изд-во СО РАН, 2001. 229 с.
Thanabalasingam P., Pickering W.F. Arsenic sorption by humic acids // Environ. Pollut. Ser. B. 1986. V. 12. P. 233–246.
Zayre I., Gonzalez A., Krachler M., Cheburkin A.K., Shotyk W. Spatial distribution of natural elements of arsenic, selenium, and uranium in a minerotrophic peatland, Cola di Lago, Canton Ticino, Switzerland // Environ. Sci. Technol. 2006. V. 40. P. 6568–6574.
Химия тяжелых металлов, мышьяка и молибдена в почвах / Под ред. Зырина Н.Г., Садовниковой Л.К. М.: Изд-во МГУ, 1985. 208 с.
Manning B.A., Goldberg S. Modeling competitive adsorption of arsenate with phosphate and molybdate on oxide minerals // Soil Sci. Amer. J. 1996. V. 60. P. 121–131.
Jackson B.P., Miller W.P. Effectiveness of phosphate and hydroxide for desorption of arsenic and selenium species from iron oxides // Soil Sci. Amer. J. 2000. V. 64. P. 1616–1622.
Cao X., Ma Lena Q. Effects of compost and phosphate on plant arsenic accumulation from soils near pressure-treated wood // Environ. Pollut. 2004. V. 132. Is. 3. P. 435–442.
Бреус И.П. Продуктивность, химический состав и удобрение амаранта, выращиваемого на зеленую массу // Агрохимия. 1997. № 10. С. 62–74.
Журбицкий З.И. Теория и практика вегетационного метода. М.: Наука, 1968. 266 с.
Агрохимические методы исследования почв / Под ред. Соколова А.В. М.: Наука, 1975. 656 с.
Егоров В.В., Иванова Е.Н., Фридланд В.М., Розов Н.И. Классификация и диагностика почв СССР. М.: Колос, 1977. 225 с.
Аринушкина Е.В. Руководство по химическому анализу почв. М.: Изд-во МГУ, 1970. 244 с.
Глазовская М.А. Геохимия природных и техногенных ландшафтов СССР. М.: Высш. шк., 1988. 328 с.
Дополнительные материалы отсутствуют.


