НЕФТЕХИМИЯ, 2023, том 63, № 5, с. 720-734
УДК 66.088:66.097.3:66.092.088
ПЕРЕРАБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ
ПЛАЗМЫ В ПРИСУТСТВИИ МАГНИЙ-ЦЕРИЕВЫХ КАТАЛИЗАТОРОВ
С РАЗЛИЧНОЙ МОРФОЛОГИЕЙ
© 2023 г. О. В. Голубев1,*, П. С. Ильчук1, А. А. Садовников1, А. Л. Максимов1
1 Институт нефтехимического синтеза им. А.В. Топчиева РАН, Москва, 119991 Россия
*E-mail: golubev@ips.ac.ru
Поступила в редакцию 8 ноября 2023 г.
После доработки 20 ноября 2023 г.
Принята к публикации 4 декабря 2023 г.
Синтезирован ряд CeO2-MgO-катализаторов с различным мольным соотношением для плазменно-ката-
литического разложения CO2 до CO и О2. Катализаторы были приготовлены золь-гель методом и охарак-
теризованы физико-химическими методами анализа (рентгенофазовый анализ, растровая электронная
микроскопия, рентгенофотоэлектронная спекроскопия, низкотемпературная адсорбция-десорбция азота,
термопрограммированная десорбция CO2). Установлено, что наивысшая конверсия CO2 (31%) дости-
гается в присутствии катализатора с наибольшим содержанием CeO2. Исследовано также введение в
систему H2; показано, что метанирования CO2 в присутствии синтезированных образцов не происходит,
однако конверсия CO2 до CO увеличивается вследствие повышения мощности разряда в присутствии
молекулярного водорода.
Ключевые слова: переработка CO2, плазменный катализ, цериевые катализаторы, барьерный разряд
DOI: 10.31857/S0028242123050106, EDN: RZWDAI
В связи с проблемой растущих выбросов СО2
замкнуть углеродный цикл, конвертируя выбросы
возрастает потребность в новых технологиях для
CO2 в ценные продукты.
ее решения. Технологии улавливания, хранения и
Один из перспективных способов превращения
утилизации углерода (CCSU) стали перспектив-
CO2 в химические вещества с высокой добавлен-
ным подходом, позволяющим не только сократить
ной стоимостью или в «строительные блоки» для
выбросы CO2, но и в перспективе превратить их в
таких продуктов - низкотемпературный плазмен-
ценные ресурсы. Утилизация углерода предпола-
но-каталитический подход. Химические реакции
гает преобразование CO2 в полезные продукты с
в плазме протекают при умеренных температурах
помощью химических, биологических или элек-
и атмосферном давлении и являются высокоэнер-
трохимических процессов. В качестве примеров
гетическими за счет образующихся при этом элек-
можно привести производство синтетического то-
тронов, ионов и других активных частиц. Высокие
плива [1, 2], химических веществ [3], строитель-
уровни энергии плазмы могут расщеплять сложные
ных материалов [4] и даже сырья для выращивания
молекулы с высокой энергией связи, такие как CO2,
водорослей [5]. Утилизация CO2 не только откры-
на более простые соединения. Плазмохимические
вает перспективы для экономики, но и помогает
и плазменно-каталитические процессы утилизации
CO2 в настоящее время широко исследуются, что
отражено в нескольких недавних обзорных статьях
# Дополнительные материалы для этой статьи доступны по
[6-9]. Для активации СО2 применяют различные
doi
10.31857/S0028242123050106 для авторизованных
источники плазмы; среди них - сверхвысокочастот-
пользователей.
ный [10-12], скользящий дуговой [13-15] источни-
720
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
721
Таблица 1. Обозначения синтезированных образцов
Цели данной работы - синтез ряда новых нена-
несенных катализаторов MgO-CeO2 с различным
Состав катализатора
Обозначение
молярным соотношением и исследование их вли-
10 мол. % MgO - 90 мол. % CeO2
Mg10Ce90
яния на конверсию CO2 в процессе плазменно-ка-
25 мол. % MgO - 75 мол. % CeO2
Mg25Ce75
талитического разложения, а также возможность
50 мол. % MgO - 50 мол. % CeO2
Mg50Ce50
проведения гидрирования СО2 при тех же условиях.
75 мол. % MgO - 25 мол. % CeO2
Mg75Ce25
90 мол. % MgO - 10 мол. % CeO2
Mg90Ce10
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
К настоящему времени известны различные
способы синтеза ненанесенных адсорбентов
ки и барьерный разряды (БР) [16-22]. Наиболее
MgO-CeO2 для адсорбции CO2 [32-35]. Выбор зо-
часто используется плазма барьерного разряда, что
ль-гель метода синтеза с использованием лимонной
обусловлено простотой реактора и низкой рабочей
кислоты обусловлен низкой стоимостью реагентов,
температурой.
отсутствием вредных темплатов и многостадийной
При добавлении катализатора конверсия CO2
подготовки.
может быть повышена за счет взаимодействия
Материалы. Для синтеза катализаторов без до-
CO2 с поверхностью катализатора и последующей
полнительной очистки были использованы следую-
диссоциации связи C=O в молекуле. На основании
щие реагенты: магний азотнокислый шестиводный
проведенного ранее обзора литературы [23] было
(ч.д.а., АО «Ленреактив», Россия), церий(III) азот-
выявлено, что перспективные материалы, способ-
нокислый шестиводный (х.ч., ООО «Центр Техно-
ствующие плазменно-каталитической диссоциации
логий Лантан», Россия), кислота лимонная моно-
CO2, можно разделить на две группы.
гидрат (ч., ООО «Компонент-Реактив», Россия).
Одна из них - группа оксидов металлов с ос-
Катализаторы были получены методом золь-гель
новными свойствами, в частности оксиды щелоч-
синтеза по методике [33]. Образцы с различным
ноземельных металлов. Основные свойства таких
мольным соотношением MgO-CeO2 имели следу-
оксидов способствуют адсорбции CO2 на поверх-
ющие обозначения (табл. 1).
ности. Перспективные материалы для адсорбции
Для синтеза образцов расчетные количества
CO2 - CaO и MgO, описанные в работах [24-26].
Mg(NO3)2 · H2O, Ce(NO3)3 · 6H2O и лимонной
Вторая группа веществ для плазменно-ката-
кислоты растворяли в расчетном количестве дис-
литического удаления CO2 - оксиды, обладаю-
тиллированной воды в плоскодонной колбе и пе-
щие кислородными вакансиями, например, CeO2.
ремешивали в течение 3 ч при 80°С на водяной
Благодаря наличию дефектов в кристаллической
бане. Полученный раствор упаривали, сушили при
структуре и способности накапливать кислород
110°С в течение 8 ч, затем прокаливали при 150°С
можно в присутствии CeO2 проводить различные
в течение 10 ч. После этого образец нагревали от
каталитические процессы утилизации CO2 [27-29].
25 до 450°С (2 ч) и прокаливали при этой темпе-
Сочетание CeO2 и MgO в катализаторе может быть
ратуре 450°С в течение 6 ч. Количества реагентов,
эффективным для плазменно-каталитической дис-
использованных для синтеза, приведены в табл. S1.
социации, что было предварительно исследовано в
Был получен порошок от бледно-желтого до свет-
работах [30, 31]. Установлено, что более высокая
ло-серого цвета. Перед проведением плазменно-ка-
каталитическая активность катализатора на осно-
талитического эксперимента порошкообразный ка-
ве MgO-CeO2 (по сравнению с CaO-CeO2, CeO2 и
тализатор под давлением формировали в таблетки,
MgO) объясняется сочетанием слабых основных
дробили, а затем просеивали на ситах для получе-
центров и кислородных вакансий на поверхности
ния фракции 1.0-1.5 мм.
катализатора. Однако более детальное изучение
влияния основных центров и кислородных вакан-
Физико-химический анализ. Текстурные ха-
сий на плазменно-каталитическую конверсию CO2
рактеристики (SБЭТ, Vпор, dпор) полученных образ-
в таких бинарных системах осталось за рамками
цов определяли методом низкотемпературной ад-
упомянутых исследований.
сорбции N2 на приборе Belsorp miniX (Microtrac
НЕФТЕХИМИЯ том 63 № 5 2023
722
ГОЛУБЕВ и др.
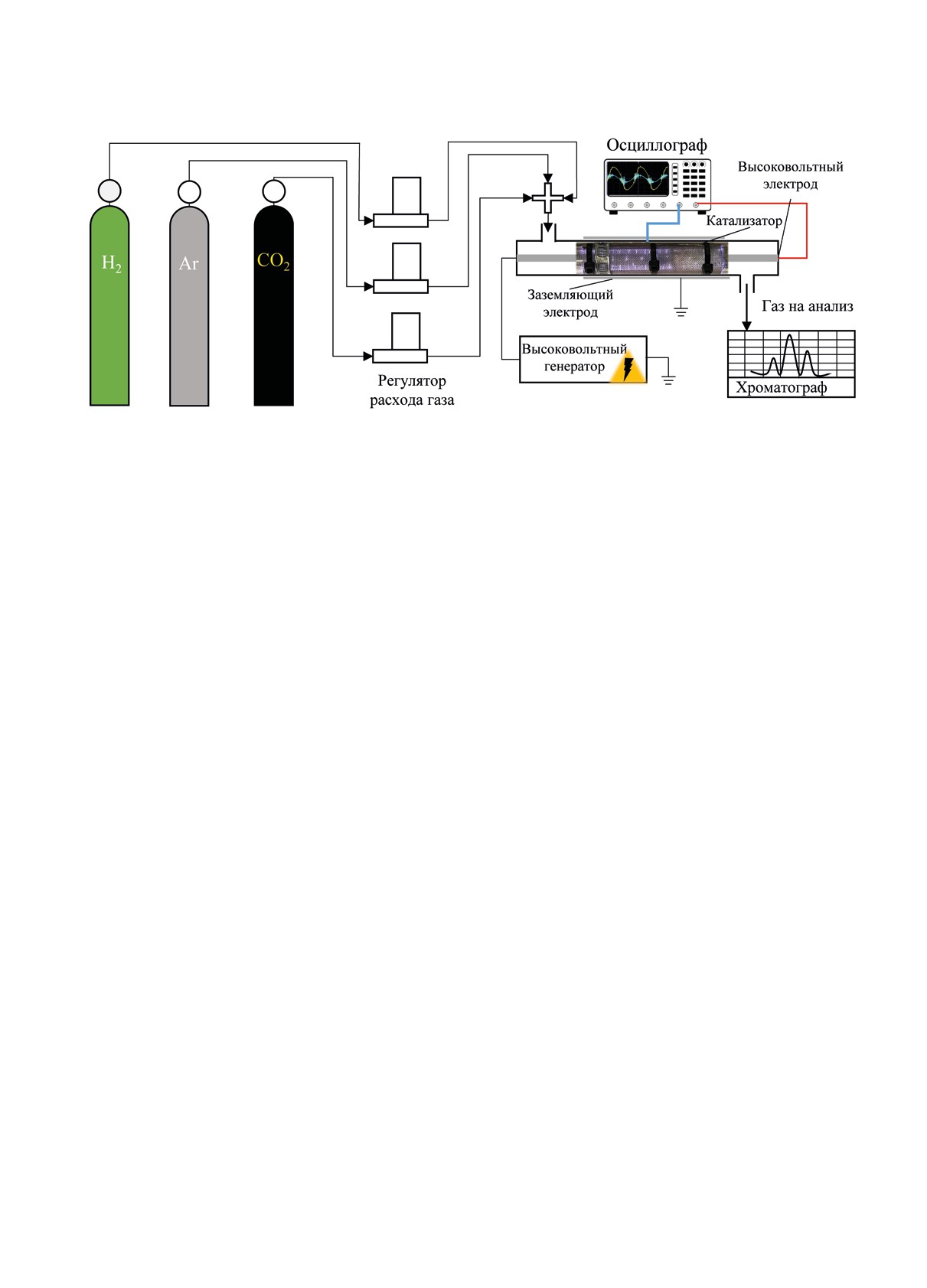
Рис. 1. Схема реактора барьерного разряда.
MRB, Германия). Перед анализом образец дегази-
нии УСГА-101 (ООО «Юнисит», Россия). Обра-
ровали при Т = 250°С и Р=10 Па в течение 24 ч.
зец катализатора нагревали в токе He при 512°С в
Для расчета площади поверхности применяли те-
течение 40 мин для удаления молекул H2O и O2, а
орию Брунауэра-Эммета-Теллера (БЭТ) в диапа-
затем насыщали CO2 при температуре 60°С в тече-
зоне относительных давлений (P/P0) = 0.05-0.20.
ние 24 мин. Адсорбированный CO2 затем удаляли
Общий объем пор рассчитывали по количеству ад-
при температуре 102°С, а процесс десорбции CO2
сорбированного N2 при P/P0 = 0.95. Для определе-
анализировали с помощью детектора по теплопро-
ния диаметра пор по ветви десорбции применяли
водности.
метод Барретта-Джойнера-Халенды. Рентгено-
Морфологию поверхности и элементный ана-
граммы образцов регистрировали в диапазоне 2θ =
лиз образцов исследовали методом растровой элек-
10°-90° на дифрактометре Rigaku Rotaflex RU-200
тронной микроскопии (РЭМ) в сочетании с энерго-
(Япония) с CuKα-излучением, оснащенном гони-
дисперсионной рентгеновской спектроскопией
ометром Rigaku D/Max-RC (скорость вращения
(ЭДС) на микроскопе Carl Zeiss NVision 40 (Герма-
1°/мин; шаг 0.04°). Идентификацию дифракто-
ния), оснащенном детектором Oxford Instruments
грамм осуществляли по базе данных PDF-2 ICDD.
X-Max EDX, работающим при напряжении 20 кВ.
Регистрацию рентгеновских фотоэлектронных
Отложение углерода на катализаторах оцени-
спектров (XPS) проводили на электронном спект-
вали методом CHNS-анализа на анализаторе Flash
рометре PREVAC EA15 (Польша). В качестве
2000 (Thermo, Великобритания). Образец массой
источника первичного излучения использовали
1-2 мг нагревали до 2000°С в потоке О2 с после-
AlKα (hν = 1486.74 эВ, 150 Вт). Деконволюцию пи-
дующим хроматографическим анализом оксидов,
ков проводили с помощью программы PeakFit с вы-
образовавшихся в процессе горения.
читанием фона Ширли и последующей подгонкой
Термогравиметрический анализ с дифференци-
к функциям Фойгта. Содержание элементов (Mg и
альной сканирующей калориметрией (ТГА-ДСК)
Ce) определяли методом рентгенофлуоресцентной
проводился на анализаторе TGA/DSC 3+ (Mettler
спектроскопии (РФЭС) на приборе ARL Perform’x
Toledo) в диапазоне температур 30-900°С в атмос-
Sequential XFR (Швейцария), оснащенном рентге-
фере воздуха.
новской трубкой мощностью 2500 Вт. Перед анали-
зом каждый образец измельчали и прессовали в таб-
Плазменно-каталитические эксперименты
летку с H3BO3. Основные свойства катализаторов
Оценку активности катализаторов проводили с ис-
оценивали методом CO2-температурной програм-
пользованием лабораторной плазменно-каталити-
мированной десорбции (CO2-ТПД) на оборудова-
ческой установки (рис. 1).
НЕФТЕХИМИЯ том 63 № 5 2023
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
723
Таблица 2. Текстурные характеристики синтезированных образцов и реальное содержание оксидов металлов в них
Текстурные характеристики
Содержание оксидов, мол. %
Образец
S
БЭТ
, м2/г
Vпор, см3/г
dпор, нм
MgO
CeO2
Mg10Ce90
25
0.07
15
13
87
Mg25Ce75
20
0.07
9
29
71
Mg50Ce50
45
0.17
14
53
47
Mg75Ce25
72
0.21
10
78
22
Mg90Ce10
142
0.35
9
93
7
Установка состояла из блока подачи газов, ре-
вали на газовом хроматографе ПИА (ООО «НПФ
актора, высоковольтного источника питания и из-
МЭМС», Россия) с детектором по теплопроводно-
мерительных приборов. В качестве реактора и ди-
сти. Колонки: для определения CO2 - адсорбент
электрического барьера использовали кварцевую
Hayesep N, длина 2 м; для определения H2, O2,
трубку (внешний диаметр 16 мм, толщина стенки
N2, CH4 и CO - молекулярные сита 13Å, длиной
2 мм, длина 160 мм). Стальной стержень (d = 8 мм)
2 м. Следует отметить, что содержание Ar в газо-
с винтовой резьбой внутри реактора служил вы-
вой смеси не определяли, поскольку он служил
соковольтным электродом, стальная сетка (размер
газом-носителем в хроматографе. Конверсию CO2
ячейки 0.5 мм, длина 80 мм) располагалась с внеш-
(%) рассчитывали по следующему уравнению:
ней стороны реактора и служила заземляющим
электродом.
(2)
Газовые смеси, состоящие из CO2 и Ar (10 об. %
CO2 - 90 об. % Ar) или CO2, H2 и Ar (10 об. % CO2 -
40 об. % H2 - 50 об. % Ar), подавали в реактор с
помощью регуляторов массового расхода РРГ-20
где ν(CO2)на входе - количество CO2, поданного в
(ООО «Элточприбор», Россия). Образец катали-
реактор, ν(CO2)на выходе - количество CO2 в выходя-
затора (2 см3) помещали в реактор в зоне разряда
щем потоке.
и фиксировали кварцевой ватой с обоих концов
слоя. Высоковольтный источник питания генери-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
ровал синусоидальный сигнал с частотой 23 кГц.
Физико-химические характеристики катали-
Эксперименты проводили в диапазоне напряжений
заторов. По результатам низкотемпературной ад-
3.4-4.8 кВ. Продолжительность эксперимента со-
ставляла 2 ч для получения и анализа трех проб
сорбции N2 можно установить, что с увеличением
газовой смеси на выходе из реактора. Регистра-
содержания MgO в образце площадь поверхности
цию электрических сигналов (тока и напряжения)
увеличивается с 25 до 142 м2/г, а также увеличива-
осуществляли с помощью осциллографа Tektronix
ется объем пор (табл. 2). Это объясняется использо-
TDS 2012B (Tektronix, США). По площади обра-
ванием лимонной кислоты при синтезе катализато-
зующихся на экране фигур Лиссажу рассчитывали
ра. Лимонная кислота играет роль хелатирующего
поглощенную мощность плазмы по следующему
агента для ионов Mg2+, а также порообразователя
уравнению [36]:
[37]. Таким образом, чем выше содержание Mg2+
на стадии приготовления катализатора, тем более
P = fW = fCnA,
(1)
развитая поверхность и более крупные поры обра-
где Cn - емкость конденсатора, подключенного по-
зуются в образце после прокаливания.
следовательно с реактором, f - частота приложен-
Изученные изотермы адсорбции образцов в
ного напряжения, A - площадь фигуры Лиссажу.
соответствии с классификацией ИЮПАК отно-
Газообразные продукты реакции (CO, O2, CH4)
сятся к изотермам IV типа с петлей гистерезиса
вместе с исходной смесью (CO2, H2) анализиро-
(рис. S1). Таким образом, образец содержит мезо-
НЕФТЕХИМИЯ том 63 № 5 2023
724
ГОЛУБЕВ и др.
Рис. 2. РЭМ-микрофотографии полученных образцов.
поры, и сила взаимодействия между поверхностью
ленными по низкотемпературной адсорбции N2),
образцов и адсорбтивом относительно слабая. Из-
так и макропорами (определенными по РЭМ).
менение морфологии поверхности образцов также
Анализ РЭМ-изображений подтверждает утверж-
наблюдается на РЭМ-изображениях (рис. 2).
дение о том, что с увеличением содержания Mg2+
в исходном растворе формируется широкопори-
Образец Mg10Ce90 характеризовался хлопье-
стая структура за счет добавления лимонной кис-
видной структурой, которая в дальнейшем преоб-
лоты в процессе синтеза катализатора. Для оценки
разовывалась в губчатую пористую структуру в
элементного состава на поверхности образца был
образце Mg90Ce10 с размером ячеек 50-200 нм.
применен энергодисперсионный рентгеновский
Образцы Mg75Ce25 и Mg90Ce10 можно охарак-
анализ (рис. S2-S6, табл. 3). Было обнаружено, что
теризовать как мезо-макропористые материалы,
соотношение Mg : Ce близко к расчетным данным
поскольку они обладают как мезопорами (опреде-
и согласуется с данными РФА.
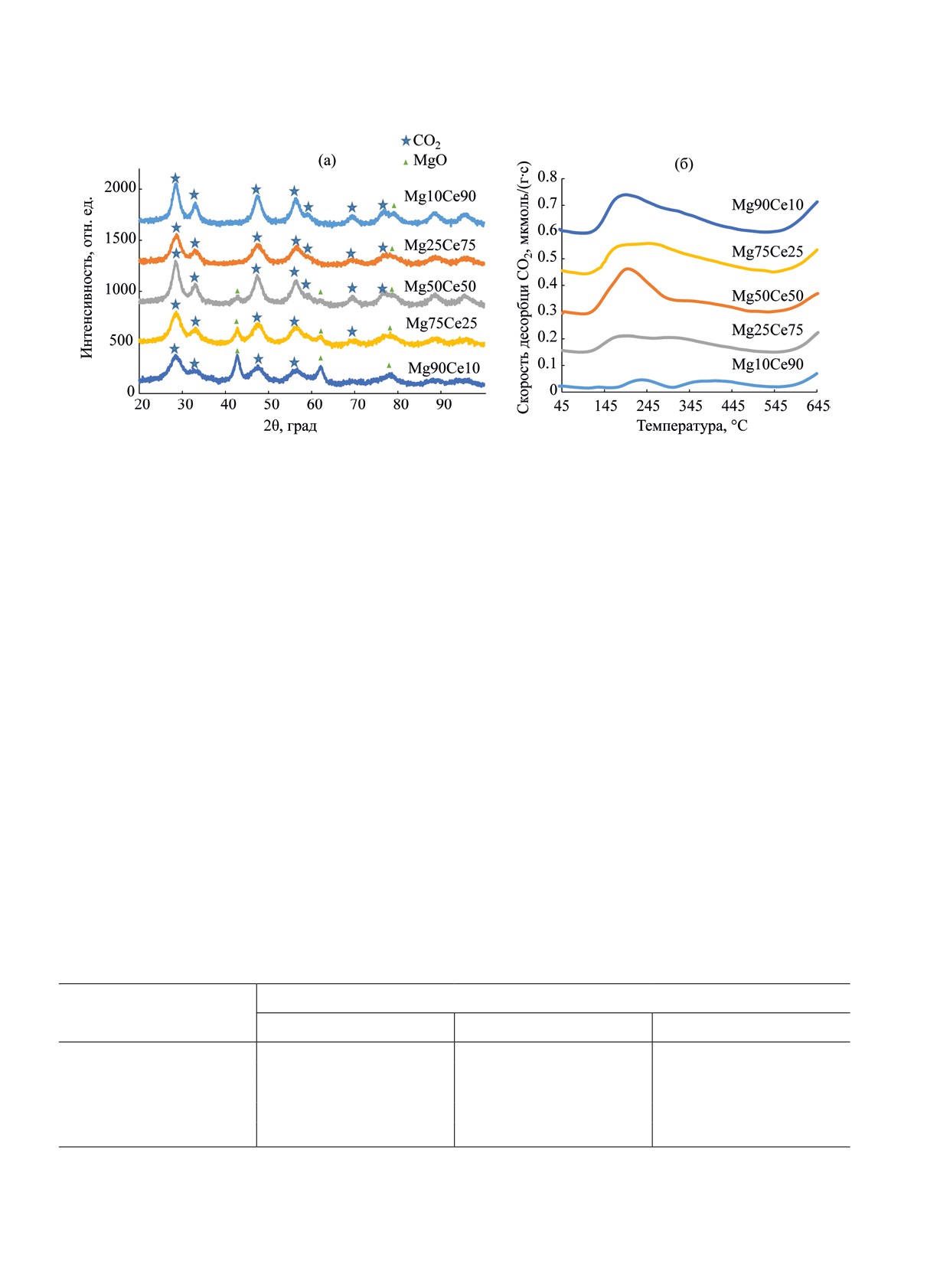
Фазовый состав полученных катализаторов
Таблица 3. Содержание элементов на поверхности ката- был определен методом РФА. Из дифрактограмм
лизаторов, определенное с помощью энергодисперсион-
(рис. 3а) видно, что характерные сигналы MgO при
ной спектроскопии
2θ = 43° и 62.5° отсутствуют на дифрактограммах
Ат., %
Mg10Ce90 и Mg25Ce75, но появляются на дифрак-
Образец
тограммах образцов с бóльшим содержанием MgO.
O
Mg
Ce
Возможным объяснением этого факта может быть
Mg10Ce90
70.5
1.9
27.7
то, что, с уменьшением содержания MgO в образ-
Mg25Ce75
70.2
6.9
22.9
це, фаза MgO становится преимущественно аморф-
Mg50Ce50
62.9
22.1
15.0
ной, чем обуславливается высокая дисперсность
Mg75Ce25
63.6
26.3
10.0
фазы. Пики при 2θ = 28°, 33°, 48°, 57°, 70° и 77°
Mg90Ce10
69.5
27.0
3.5
соответствуют фазе CeO2 [38]. Следует также от-
НЕФТЕХИМИЯ том 63 № 5 2023
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
725
Рис. 3. Дифрактограммы (а) и кривые термопрограммируемой десорбции (б) синтезированных образцов.
метить, что по данным РФА, смешанные оксиды не
(898 эВ), v'' (888 эВ), v (882 эВ), которые относят-
образуются.
ся к Ce4+ (CeO2), и пики u' (903 эВ), v' (885 эВ),
которые относятся к Ce3+ (Ce2O3). Исходя из пло-
При определении основности катализаторов
щади пиков Ce4+ и Ce3+ рассчитывали содержание
методом CO2-ТПД установлено (рис. 3б), что с по-
CeO2. Площади пиков после деконволюции для
вышением мольной доли MgO в катализаторе уве-
каждого образца, полуширина и рассчитанное со-
личивается содержание основных центров. Наи-
держание CeO2 приведены в табл. S2. Видно, что
меньшая концентрация основных центров была
наибольшее содержание CeO2 составило 92% (об-
характерна для образца Mg10Ce90 (табл. 4), что
разец Mg50Ce50), а наименьшее - 68% (образец
связано с наименьшим содержанием MgO в ката-
Mg75Ce25). Таким образом, строгой зависимости
лизаторе. Следует отметить, что в ряду Mg50Ce50-
между молярным соотношением MgO : CeO2 и со-
Mg75Ce25-Mg90Ce10 основные свойства изменя-
держанием Ce4+ не наблюдается. В спектрах O1s
ются незначительно, что может быть связано со
наблюдаются два пика. Пик при 532 эВ соответ-
схожим содержанием атомов Mg на поверхности,
ствует MgO, а пик при 529 эВ - CeO2 (табл. S3). Из
что определено по результатам ЭДС (табл. 3).
спектров хорошо видно, что пик при 532 эВ возрас-
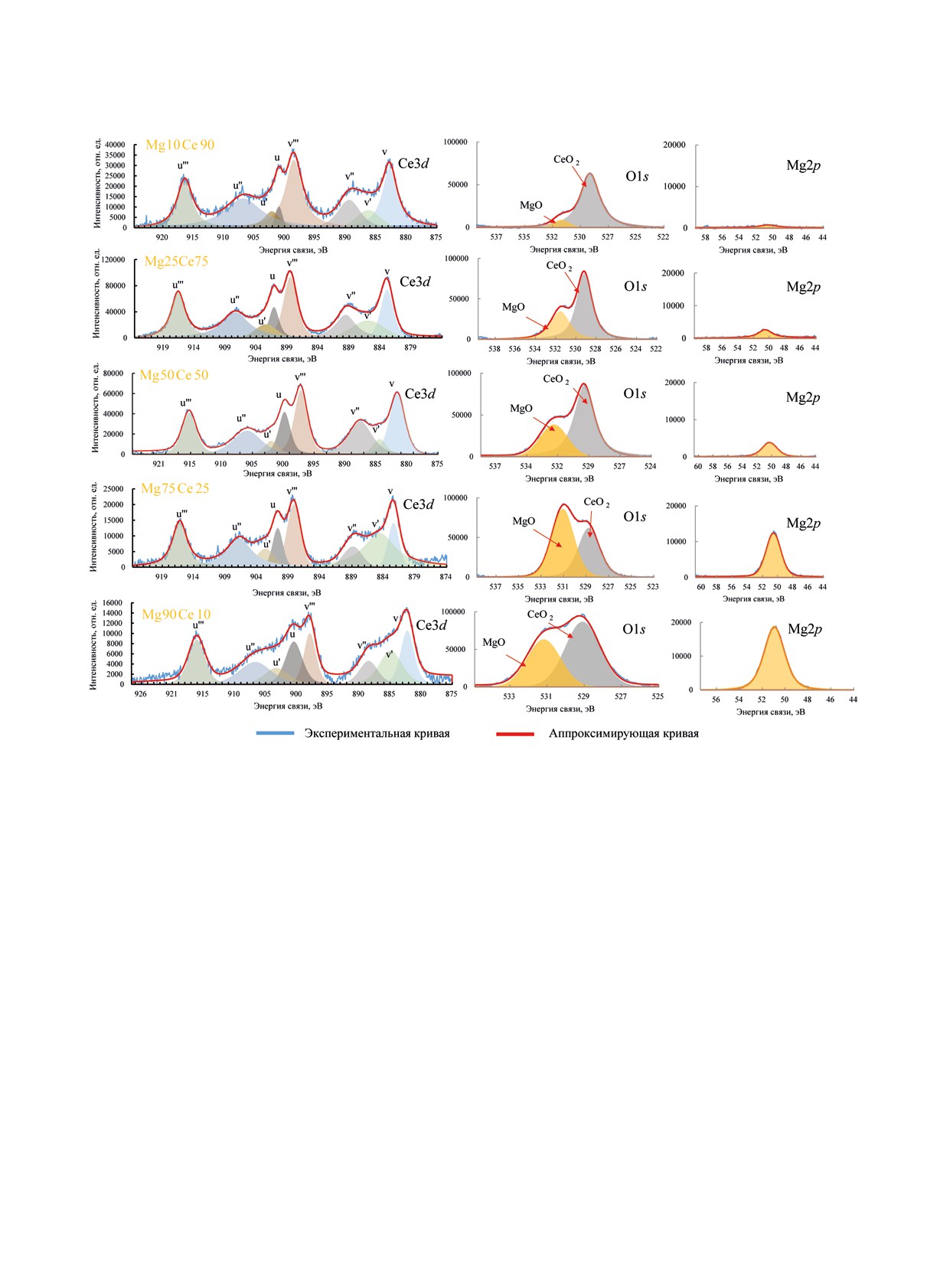
По данным РФЭС, образцы содержат на по-
тает по мере увеличения содержания MgO в образ-
верхности атомы Ce, Mg и O (рис. 4). На спектре
це. Такая же тенденция наблюдается и на спектрах
Ce3d после деконволюции присутствуют следую-
Mg2p. Здесь присутствует только один пик, кото-
щие пики: u''' (917 эВ), u'' (907 эВ), u (901 эВ), v'''
рый относится к MgO. С увеличением содержания
Таблица 4. Характеристики основных центров, определенные методом термопрограммируемой десорбции CO2
Концентрация основных центров, мкмоль/г
Образец
слабые (100-300°C)
сильные (300-500°C)
всего
Mg10Ce90
16
25
41
Mg25Ce75
52
65
117
Mg50Ce50
190
-
190
Mg75Ce25
198
-
198
Mg90Ce10
200
-
200
НЕФТЕХИМИЯ том 63 № 5 2023
726
ГОЛУБЕВ и др.
Рис. 4. РФЭ-спектры синтезированных катализаторов.
MgO в катализаторе площадь пика увеличивается
мой мощности разряда объясняется составляющей
(табл. S4).
напряжения.
Плазменно-каталитические эксперименты
Плазменно-каталитическое разложение CO2
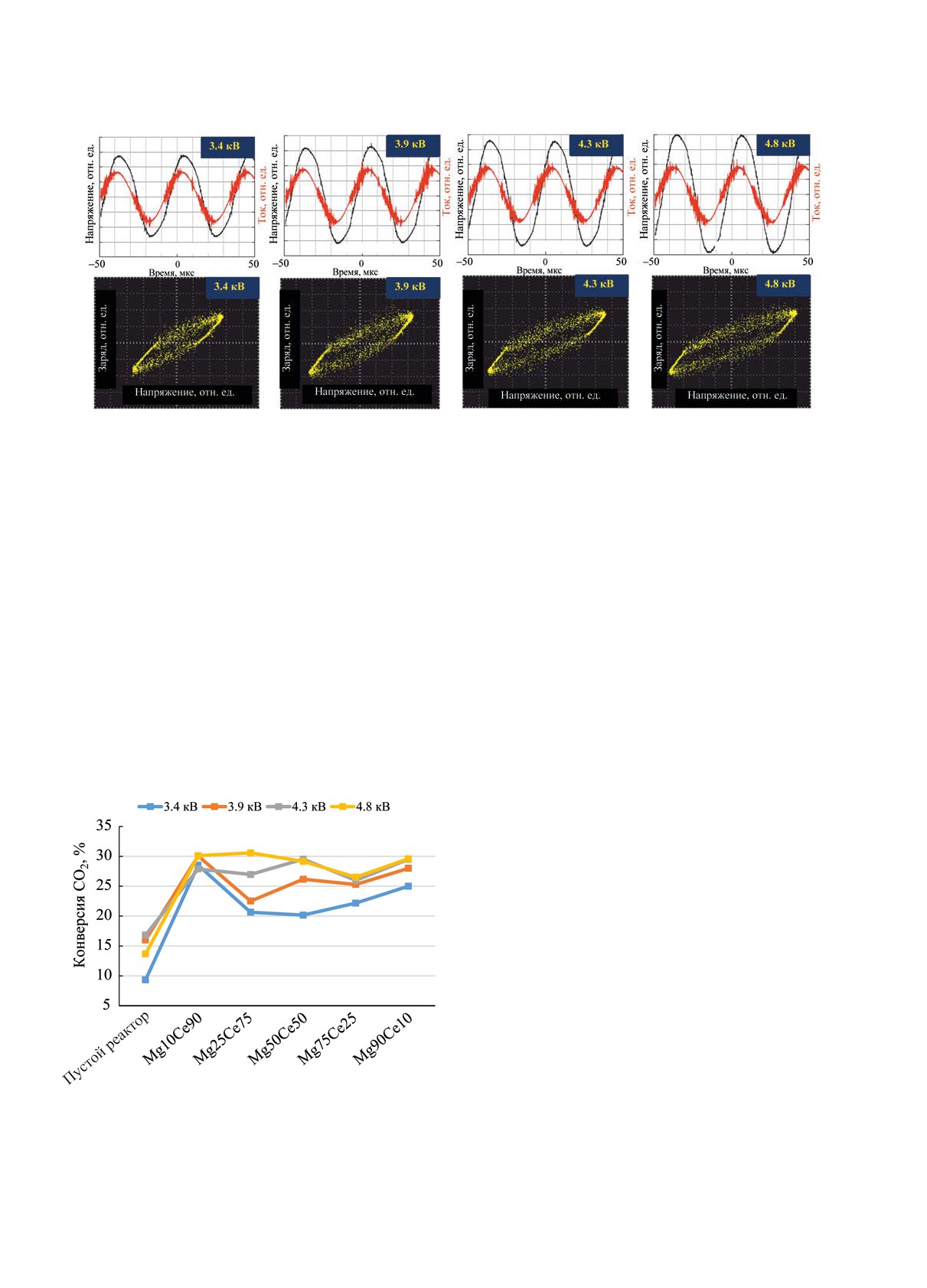
На рис. 5б представлены осциллограммы напря-
Разложение диоксида углерода осуществляли в
жения и тока. Амплитуда синусоидального сигнала
реакторе барьерного разряда, заполненном синте-
напряжения увеличивается при повышении зна-
зированными катализаторами, в течение 2 ч с по-
чения входного напряжения. На осциллограммах
степенным повышением напряжения от 3.4 кВ до
тока разряда хорошо видны микроразряды. Ампли-
4.8 кВ. Из рис. 6 видно, что в отсутствие катали-
туда токового сигнала остается неизменной, как и
затора (холостой опыт) конверсия CO2 достигает
плотность микроразрядов при увеличении напря-
9-17%, в зависимости от потребляемой мощности.
жения. Видно, что фигура Лиссажу растягивается
Это согласуется с предыдущими полученными ре-
по горизонтальной оси, что связано с увеличением
зультатами [31], где конверсия CO2 в отсутствие
напряжения. Сигнал заряда остается практически
катализатора составляла 11%. При добавлении ка-
неизменным независимо от величины входного на-
тализатора конверсия CO2 увеличивалась до 31%.
пряжения. Таким образом, увеличение поглощае-
Наибольшая конверсия была достигнута в присут-
НЕФТЕХИМИЯ том 63 № 5 2023
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
727
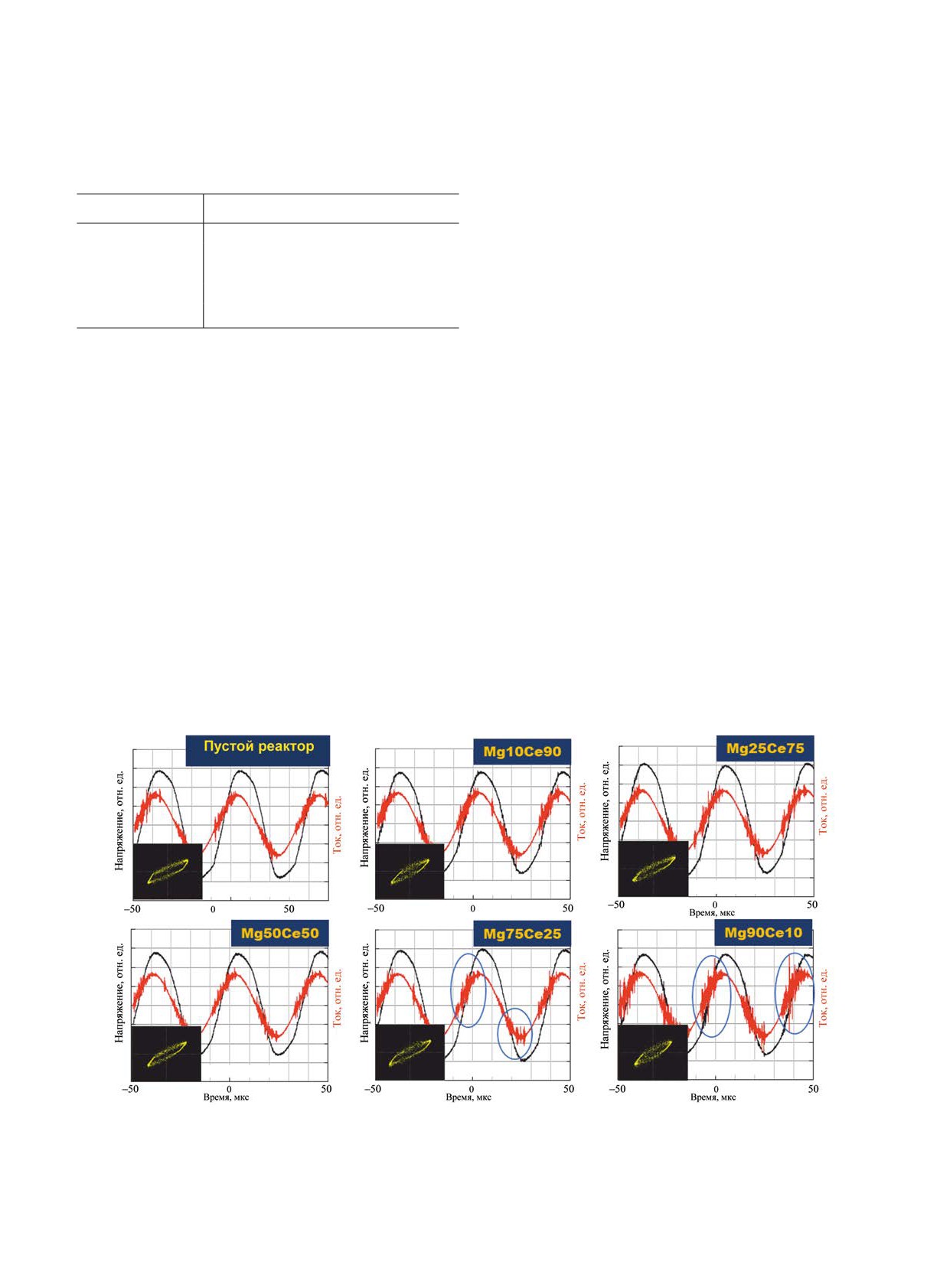
Рис. 5. Осциллограммы тока и напряжения и фигуры Лиссажу, снятые при плазменно-каталитическом разложении CO2 в
присутствии образца Mg10Ce90. Шкала сигнала напряжения - 5 В/дел., шкала сигнала тока - 2 В/дел.
ствии образцов Mg10Ce90 и Mg25Ce75 при на-
Газовая смесь на выходе из реактора состояла
пряжении 4.8 кВ. Можно сделать вывод, что более
из CO2, CO, O2 и N2. После вычитания доли N2 и
развитая поверхность образцов катализаторов не
O2 (полученных из примеси воздуха), было рассчи-
играет важной роли в плазменно-каталитическом
тано соотношение [CO]/[O-2], которое составило
разложении CO2, поскольку Mg10Ce90 и Mg25Ce75
2±0.2. Это соотношение указывает на то, что ос-
характеризуются наименьшими значениями удель-
новным продуктом разложения CO2 является CO,
ной площади поверхности (20-25 м2/г) и объема
а не твердый углерод. В данных условиях реакции
пор (0.07 см3/г). Аналогичное наблюдение приво-
образование твердого углерода маловероятно, по-
дится в работе [24], а которой показано, что высо-
скольку реакция разложения СО2 до С и О2 требует
кая удельная поверхность Al2O3 не оказывает влия-
чрезвычайно высоких температур (6000-7000°С).
ния на плазменно-каталитическую конверсию CO2.
Тем не менее, после реакции был проведен анализ
катализаторов с целью выявления осаждения угле-
рода, о чем будет описано далее.
При увеличении поглощаемой мощности
(с ~5.5 до ~6.5 Вт) конверсия CO2 возрастает,
что в первую очередь связано с усилением элек-
трического поля и образованием в плазме бо-
лее активных частиц. В данном исследовании
было достаточно сложно сравнить активность
MgO-CeO2-катализаторов при повышенной мощ-
ности, поэтому была поставлена задача не по
достижению максимально возможной конвер-
сии, а по сравнению активности катализаторов
MgO-CeO2 в схожих условиях. Как видно из рис. 6,
при напряжении 3.4-3.8 кВ наибольшую актив-
ность в диссоциации CO2 проявляет образец
Mg10Ce90, в присутствии Mg25Ce75 и Mg50Ce50
Рис. 6. Конверсия CO2 в барьерном разряде при на-
конверсия снижается с последующим увеличением
пряжении 3.4-4.8 кВ в присутствии синтезированных
в присутствии Mg75Ce25 и Mg90Ce10. Предполо-
катализаторов.
жительно, при сочетании основных свойств MgO и
НЕФТЕХИМИЯ том 63 № 5 2023
728
ГОЛУБЕВ и др.
Таблица 5. Содержание кислородных вакансий в фазе
Другой вероятный эффект в увеличении кон-
, рассчитанное по данным рентгенофотоэлектрон-
CeO2
версии CO2 в присутствии образцов Mg75Ce25 и
ной спектроскопии
Mg90Ce10 (по сравнению с Mg50Ce50) может сле-
Образец
Количество кислородных вакансий
довать из морфологии поверхности катализатора.
Согласно РЭМ-изображениям (рис. 2), указанные
Mg10Ce90
0.11
образцы обладают макропорами, образовавшими-
Mg25Ce75
0.15
Mg50Ce50
0.08
ся в процессе синтеза. В работе [40] сообщалось
Mg75Ce25
0.32
о микроразрядах, которые могут образовываться
Mg90Ce10
0.23
внутри пор катализатора размером 4-100 нм. Такие
микроразряды усиливают локальное электриче-
ское поле и тем самым могут повышать конверсию
CO2. На рис. 7 видно, что в присутствии образцов
Mg75Ce25 и Mg90Ce10 плотность микроразрядов
кислородно-дефицитной структуры CeO2 домини-
рующая роль в разложении CO2 принадлежит кис-
выше, чем в присутствии других катализаторов:
наблюдается большее количество пиков на осцил-
лородным вакансиям, а не основным центрам. Из
данных РФЭС и деконволюции площади пика было
лограмме тока с большей амплитудой (выделено на
рассчитано содержание кислородных вакансий по
рис. 7). Это наблюдение может свидетельствовать
о преимуществе пористой структуры в плазмен-
соотношению [Ce3+/(Ce3++ Ce4+)] [39]. Из табл. 5
видно, что в образцах Mg75Ce25 и Mg90Ce10 со-
но-каталитическом процессе в данных условиях.
держание кислородных вакансий в оксиде церия
Для обобщения вышеперечисленных свойств
выше, чем в других образцах, однако, вследствие
катализатора, влияющих на процесс плазменно-ка-
наибольшего содержания оксида церия в катализа-
талитического разложения CO2, была рассчитана
торе Mg10Ce90, конверсия CO2 в присутствии ука-
удельная каталитическая активность. Поскольку ка-
занного образца являлась наивысшей. Это объясня-
тализаторы с различным содержанием CeO2 имели
ется тем, что при одинаковом объеме катализатора
разную плотность, масса катализатора в реакторе
в реакторе масса катализатора будет разной.
варьировалась (катализатор загружали по объему).
Рис. 7. Осциллограммы тока и напряжения и фигуры Лиссажу, снятые при плазменно-каталитическом разложении CO2 при
напряжении 3.4 кВ. Шкала сигнала напряжения - 5 В/дел., шкала сигнала тока - 2 В/дел.
НЕФТЕХИМИЯ том 63 № 5 2023
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
729
вывод, что образцы на основе MgO более эффек-
тивны в разложении CO2 на единицу массы ката-
лизатора, а образцы на основе CeO2 - на единицу
объема катализатора.
Разложение CO2 в присутствии H2. Поскольку
перспективным процессом утилизации углекисло-
го является его конверсия в метан и углеводороды,
было проведено исследование влияния добавления
в систему H2 для выявления возможности мета-
нирования CO2 при тех же условиях реакции. Ре-
зультаты экспериментов показали, что полученные
катализаторы не проявляют активность в процессе
метанирования CO2. Селективность по CH4 была
относительно низкой (2-4%), а образование CH4
происходило скорее плазменным, чем каталитиче-
ским путем. Восстановление CO2 до CH4 является
восьмиэлектронным процессом, поэтому в каче-
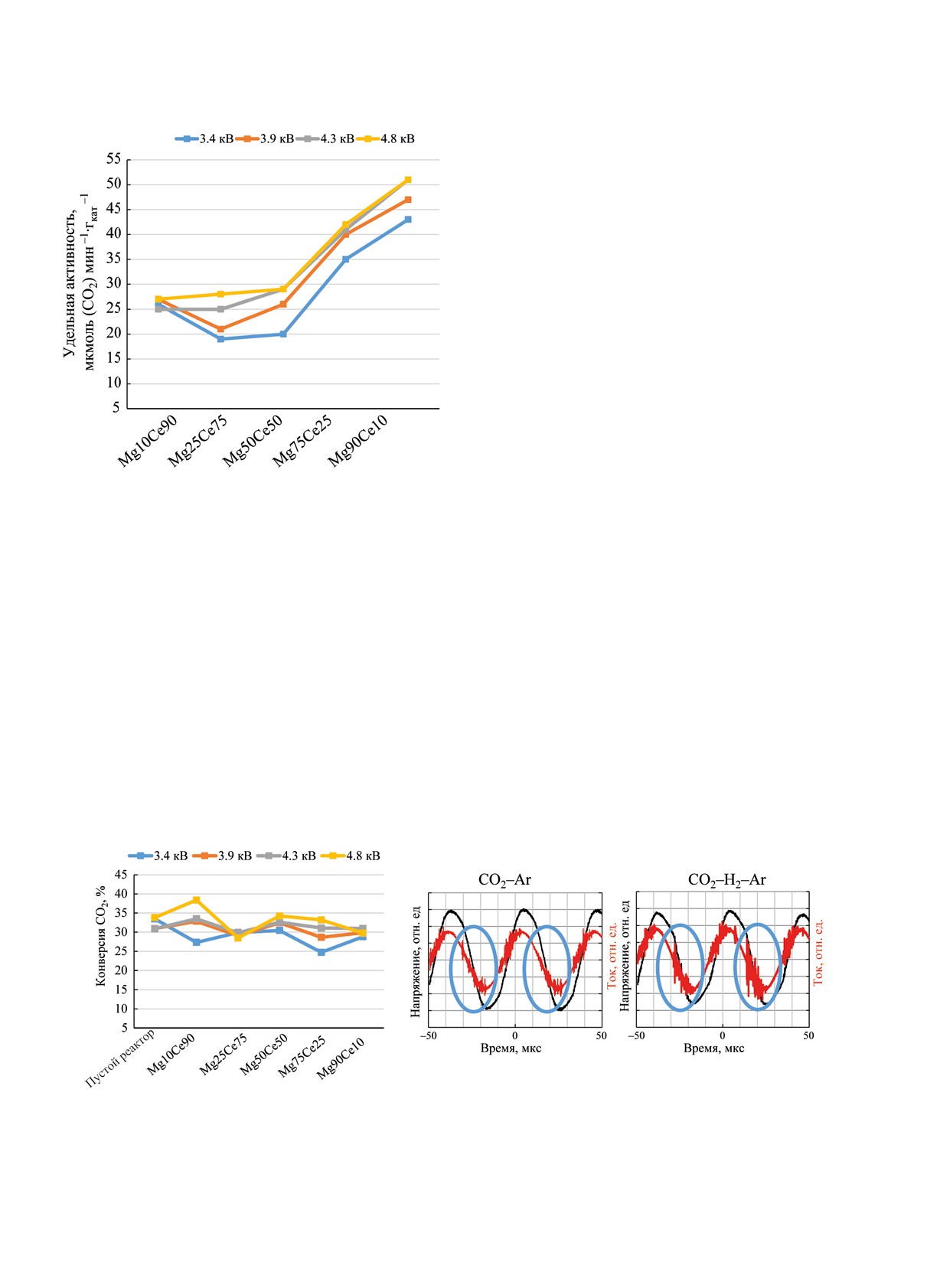
Рис. 8. Удельная каталитическая активность образцов в
стве каталитического активного центра необходи-
процессе плазменно-каталитического разложения CO2.
мы переходные металлы, например Ni, Ru, Pt и др.
Отмечено, однако, что конверсия CO2 была выше,
Для определения активности 1 г образца (т.е. какое
чем в отсутствие H2 (40% в присутствии Mg10Ce90
количество CO2 преобразуется на 1 г катализатора
против 31% в газовой смеси CO2-Ar). Следует
в минуту) была проведена нормализация графиков
также отметить, что в отсутствие катализатора (в
активности (рис. 8).
пустом реакторе) конверсия CO2 была сопостави-
Как видно, удельная активность растет с увели-
ма с таковой в присутствии исследуемых образцов
чением содержания MgO в образце. Однако прово-
(рис. 9), что свидетельствует об отсутствии эффекта
дить сравнение образцов с одинаковой массой за-
от введения катализатора. Более высокая конверсия
труднительно, поскольку параметры разряда будут
CO2 в присутствии H2 может быть объяснена уве-
отличаться при различном объеме образца внутри
личением мощности в присутствии молекулярного
зоны плазмы. Другая причина заключается в том,
газа. Как объясняется в работах [41, 42], изменение
что время взаимодействия газа с катализатором
состава газа в достаточной степени влияет на физи-
будет различаться. Таким образом, можно сделать
ческие характеристики плазмы: температуру газа,
Рис. 9. Результаты эксперимента по разложению CO2 в присутствии H2 и разрядные характеристики процесса в отсутствие
(смесь CO2-Ar) и в присутствии H2 (смесь CO2-H2-Ar) при напряжении 3.4 кВ (образец Mg75Ce25). Шкала сигнала напря-
жения - 5 В/дел., шкала сигнала тока - 2 В/дел.
НЕФТЕХИМИЯ том 63 № 5 2023
730
ГОЛУБЕВ и др.
Таблица 6. Баланс газовых смесей во входном и выходном потоке при проведении процесса с использованием образ-
ца Mg10Ce90 при напряжении 3.4 кВт
Концентрация, об. %
CO2
CO
O2
H2
CH4
Ar
Всего (без Ar)
До реакции
10.5
-
-
43
-
ост.
53.5
После реакции
8.2
2.1
0.1
39.2
0.7
ост.
50.2
Таблица 7. Содержание углерода в катализаторах до и после экспериментов
Содержание углерода и водорода, мас. %
Образец
до реакции
после реакции
С
H
C
H
Mg10Ce90
0.33
0.28
0.34
0.21
Mg25Ce75
0.76
0.46
0.62
0.24
Mg50Ce50
1.28
0.66
1.00
0.31
Mg75Ce25
1.25
0.89
1.54
0.42
Mg90Ce10
1.58
1.77
2.48
0.80
напряженность приведенного электрического поля
ца между этими значениями может быть связана с
и среднюю энергию электронов. Таким образом,
образованием Н2О.
добавка Н2 приводит к появлению более активных
Характеристики образцов катализаторов
частиц плазмы, которые оказывают большее вли-
после реакции. После проведения плазменно-ка-
яние на диссоциацию СО2, чем каталитические
талитических экспериментов были определены
реакции на поверхности катализатора. Последний
характеристики поверхности катализаторов. Для
факт проиллюстрирован характеристиками разря-
оценки количества кокса после разложения CO2
да в присутствии и в отсутствие Н2 (рис. 9). При
использовали элементный анализ образцов мето-
введении в газовую смесь H2 на осциллограмме
дом CHNS. Присутствие углерода, определенное в
тока наблюдаются более плотные микроразряды,
образцах до реакции, связано с использованием ли-
а также расширяются фигуры Лиссажу. Другое
монной кислоты в процессе синтеза катализаторов.
возможное объяснение усиления конверсии CO2
Чем выше содержание MgO в образце, тем боль-
может заключаться в захвате O2 радикалами H, как
шее количество лимонной кислоты требовалось
описано в работе [43]. Введение H2 в поток CO2 в
для синтеза. Таким образом, содержание углерода в
присутствии плазмы приводит к образованию H2O
синтезированных образцах увеличивается (табл. 7).
и, тем самым, ограничивает обратную реакцию:
Из анализа катализаторов после реакции следует,
CO + 0.5O2 → CO2.
что характеристики поверхности (табл. 8) и содер-
В описанных условиях не представляется воз-
жание углерода практически не изменились в слу-
можным оценить образование Н2О вследствие осо-
чае образцов Mg10Ce90 и Mg25Ce75. Напротив, в
бенностей конструкции установки для отбора проб
случае образцов Mg75Ce25 и Mg90Ce10 происхо-
газа. Однако можно косвенно оценить его содер-
дит резкое снижение удельной поверхности и уве-
жание при сравнении содержания O2 на выходе из
личение содержания углерода. Данные явления,
реактора. Отмечено, что при проведении процесса
по всей видимости, связаны с превращением MgO
в смеси CO2-H2-Ar, концентрация O2 в выходящем
либо в MgCO3, либо в Mg(OH)2.
потоке стремится к нулю (концентрация O2 в слу-
чае CO2-Ar составляла 0.5-1.0 об. %). Из табл. 6
Для выявления природы снижения удельной
видно, что концентрация Н2 на выходе уменьшает-
площади был проведен термогравиметрический
ся по сравнению с концентрацией на входе. Разни-
анализ (рис. S6-S10). На кривой ТГА наблюдаются
НЕФТЕХИМИЯ том 63 № 5 2023
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
731
Таблица 8. Текстурные характеристики образцов после реакции разложения CO2
Текстурные характеристики
Образец после реакции
S
БЭТ
, м2/г
изм. SБЭТ, м2/г
Vпор, см3/г
dпор, нм
Mg10Ce90
21
↓ 4
0.08
18
Mg25Ce75
19
-
0.08
12
Mg50Ce50
22
↓ 23
0.12
19
Mg75Ce25
26
↓ 46
0.15
16
Mg90Ce10
74
↓ 69
0.26
10
три стадии разложения материала. Первая стадия
бóльшая роль в разложении CO2 отводится CeO2 и
разложения происходит при ~100°С и объясняет-
кислородным вакансиям в структуре оксида церия.
ся удалением физически адсорбированной воды.
Конверсия CO2 также увеличивалась при нали-
Вторая стадия при ~350°С связана с разложением
чии макропористой структуры образцов Mg75Ce25
Mg(OH)2 [44], который мог образоваться из MgO в
и Mg90Ce10 за счет образования микроразрядов
условиях эксперимента. Следует отметить, что ам-
внутри пор. Тем не менее, конверсия CO2 в присут-
плитуда этого пика незначительна в случае образца
ствии этих катализаторов ниже, чем в присутствии
Mg10Ce90 (в котором содержание MgO наимень-
Mg10Ce90, содержащего наибольшее количество
шее) и увеличивается с ростом содержания MgO.
CeO2. Установлено, что полученные катализаторы
Потеря массы образца Mg90Ce10 на второй стадии
не эффективны для реакции метанирования CO2,
составляет ~12%. Кроме того, третья стадия разло-
добавление H2 приводило лишь к увеличению кон-
жения при ~565°С может быть связана с разложе-
версии CO2 за счет увеличения поглощаемой мощ-
нием MgCO3 до исходного MgO, а также с выгора-
ности плазмы и улавливания кислорода.
нием углерода из лимонной кислоты. Потеря массы
Можно заключить, что положительный эффект
на этой стадии наименьшая для образца Mg10Ce90
от сочетания основного оксида металла (MgO) с
(1.00%) и наибольшая для образца Mg90Ce10
CeO2 может проявляться при небольшом количе-
(2.88%), что коррелирует с содержанием углерода
по данным анализа CHNS.
стве MgO в катализаторе (Mg10Ce90). При сниже-
нии содержания церия эффективность разложения
Таким образом, можно заключить, что образцы
CO2 также снижается. Было отмечено, что катали-
с высоким содержанием MgO менее стабильны в
заторы с более высоким содержанием CeO2 более
ходе плазменно-каталитической реакции и нужда-
стабильны, чем содержащие преимущественно
ются в реактивации для восстановления физико-хи-
MgO. Результаты, полученные в данной работе,
мических характеристик. Катализаторы с высоким
могут быть использованы при дальнейшей разра-
содержанием церия (Mg10Ce90 и Mg25Ce75) ока-
ботке катализаторов для разложения СО2, метани-
зались стабильными в указанных условиях и, сле-
рования СО2, риформинга СО2 и других процессов,
довательно, могут сохранять свою каталитическую
связанных с утилизацией СО2 в плазме. Дальней-
активность в течение более длительного времени.
шее исследование плазменно-каталитического раз-
ложения CO2 может быть связано с мезо-макропо-
ЗАКЛЮЧЕНИЕ
ристыми катализаторами CeO2 с целью сочетания
В настоящей работе была синтезирована серия
эффектов от кислородных вакансий и микроразря-
катализаторов MgO-CeO2, которые применяли
дов, которые могут образовываться внутри мезо- и
для плазменно-каталитического разложения CO2.
макропор.
В присутствии катализаторов конверсия CO2 уве-
личивалась по сравнению с таковой в отсутствие
ФИНАНСИРОВАНИЕ РАБОТЫ
катализатора с 17 до 31%. Установлено, что конвер-
сия CO2 не связана с высокой площадью поверх-
Работа выполнена в рамках Государственного
ности и сильной основностью катализаторов, а
задания ИНХС РАН.
НЕФТЕХИМИЯ том 63 № 5 2023
732
ГОЛУБЕВ и др.
БЛАГОДАРНОСТИ
technologies in cement-based materials // Constr.
Авторы выражают благодарность д.ф.-м.н.
org/10.1016/j.conbuildmat.2020.121660
Лебедеву Ю.А. и к.х.н. Голубевой М.А. за помощь
5.
Saravanan A., Deivayanai V.C., Senthil Kumar P.,
в подготовке публикации.
Rangasamy G., Varjani S. CO2 bio-mitigation using
Работа выполнена с использованием оборудова-
genetically modified algae and biofuel production
ния ЦКП «Аналитический центр глубокой перера-
towards a carbon net-zero society // Bioresour. Technol.
ботки нефти и нефтехимии» ИНХС РАН.
biortech.2022.127982
Съемка микрофотографий РЭМ проводи-
6.
Snoeckx R., Bogaerts A. Plasma technology - a novel
лась с использованием оборудования ЦКП ФМИ
solution for CO2 conversion? // Chem. Soc. Rev. 2017.
ИОНХ РАН.
7.
Adwek G., Shen B., Craven M., Wang Y., Kang D., Wu C.,
КОНФЛИКТ ИНТЕРЕСОВ
Tu X. A review of non-thermal plasma technology: a
novel solution for CO2 conversion and utilization //
А.Л. Максимов является главным редакто-
Renew. Sust. Energ. Rev. 2021. V. 135. ID 109702.
ром журнала «Нефтехимия/Petroleum Chemistry».
Остальные авторы заявляют об отсутствии
8.
Chen G., Snyders R., Britun N. CO2 conversion using
конфликта интересов.
catalyst-free and catalyst-assisted plasma-processes:
recent progress and understanding // J. CO2 Util.
ИНФОРМАЦИЯ ОБ АВТОРАХ
jcou.2021.101557
9.
Debjyoti R., Ye P., Yu J.C., Song C. Recent progress in
org/0000-0002-8558-3094
plasma-catalytic conversion of CO2 to chemicals and
fuels // Catal. Today. 2022. V. 423. ID 113973. https://
0008-9459-8934
doi.org/10.1016/j.cattod.2022.12.004
10.
Kozák T., Bogaerts A. Evaluation of the energy efficiency
of CO2 conversion in microwave discharges using a
0002-3574-0039
reaction kinetics model // Plasma Sources Sci. Technol.
Максимов А.Л., д.х.н., чл.-корр. РАН, ORCID:
0252/24/1/015024
11.
Lebedev Yu.A., Shakhatov V.A. Decomposition of carbon
.СПИСОК ЛИТЕРАТУРЫ
dioxide in microwave discharges (an analytical review) //
1. Schlager S., Fuchsbauer A., Haberbauer M., Neuge-
org/10.1134/S1070427222010018
bauer H., Sariciftci N.S. Carbon dioxide conversion
12.
Ong M.Y., Nomanbhay S., Kusumo F., Show P.L.
to synthetic fuels using biocatalytic electrodes //
Application of microwave plasma technology to convert
carbon dioxide (CO2) into high value products: a review //
org/10.1039/C6TA07571A
2. Chen Y., Guan B., Wu X., Guo J., Ma Z., Zhang J., Jiang X.,
org/10.1016/j.jclepro.2022.130447
Bao S., Cao Y., Yin C., Ai D., ChenY., Lin H., Huang Z.
Research status, challenges and future prospects of
13.
Nunnally T., Gutsol K., Rabinovich A., Fridman A.,
renewable synthetic fuel catalysts for CO2 photocatalytic
Gutsol A., Kemoun A. Dissociation of CO2 in a low
reduction conversion // Environ. Sci. Pollut. Res. 2023.
current gliding arc plasmatron // J. Phys. D: Appl. Phys.
022-24686-y
3727/44/27/274009
3. Li J., Wang L., Cao Y., Zhang C., He P. Li H. Recent
14.
Liu J.-L., Wang X., Li X.-S., Likozar B., Zhu A.-M. CO2
advances on the reduction of CO2 to important C2+
conversion, utilisation and valorisation in gliding arc
oxygenated chemicals and fuels // Chin. J. Chem. Eng.
plasma reactors // J. Phys. D. Appl. Phys. 2020. V. 53.
cjche.2018.07.008
15.
Zhang H., Li L., Xu R., Huang J., Wang N., Li X., Tu X.
4. Liu B., Qin J., Shi J., Jiang J., Wu X., He Z. New
Plasma-enhanced catalytic activation of CO2 in a
perspectives on utilization of CO2 sequestration
modified gliding arc reactor // Waste Dispos. Sustain.
НЕФТЕХИМИЯ том 63 № 5 2023
ПЕРЕР
АБОТКА ДИОКСИДА УГЛЕРОДА С ИСПОЛЬЗОВАНИЕМ ПЛАЗМЫ
733
discharge reactor // J. Environ. Chem. Eng. 2021. V. 9.
s42768-020-00034-z
16.
Bogaerts A., Kozak T., van Laer K., Snoeckx R. Plasma-
27.
Ebrahimi P., Kumar A., Khraisheh M.A. A review
based conversion of CO2: current status and future
of CeO2 supported catalysts for CO2 reduction to
challenges // Faraday Discuss. 2015. V. 183. ID 217.
CO through the reverse water gas shift reaction //
17.
Ray D., Subrahmanyam Ch. CO2 decomposition in
catal12101101
a packed DBD plasma reactor: influence of packing
28.
Ijaz H., Gazali T., Shakeel A., Chennampilly U.A.,
materials // RSC Adv. 2016. V. 6. P. 39492-37499.
Alasiri H., Alhooshani K. A review of the indispensable
role of oxygen vacancies for enhanced CO2 methanation
18.
Michielsen I., UytdenhouwenY., Pype J., Michielsen B.,
activity over CeO2-based catalysts: uncovering,
Mertens J., Reniers F., Meynen V., Bogaerts A. CO2
influencing, and tuning strategies // Int. J. Hydrog.
dissociation in a packed bed DBD reactor: first steps
org/10.1016/j.ijhydene.2022.08.086
towards a better understanding of plasma catalysis //
29.
Ahn S.-Y., Jang W.-J., Shim J.-O., Jeon B.-H., Roh H.-S.
CeO2-based oxygen storage capacity materials in
org/10.1016/j.cej.2017.05.177
environmental and energy catalysis for carbon neutrality:
19.
Xu S., Whitehead C.J., Martin P.A. CO2 conversion
extended application and key catalytic properties // Catal.
in a non-thermal, barium titanate packed bed plasma
reactor: the effect of dilution by Ar and N2 // Chem. Eng.
614940.2022.2162677
30.
Lebedev Yu.A., Golubev O.V., Batukaev T.S., Maximov A.L.
cej.2017.06.090
Decomposition of CO2 in a barrier discharge in the
20.
Lu N., Sun D., Zhang C., Jiang N., Shang K., Bao X.,
presence of cerium oxide catalysts // Tech. Phys.
Li J., Wu Y. CO2 conversion in non-thermal plasma and
plasma/g-C3N4 catalyst hybrid processes // J. Phys.
TPL.2023.05.56015.19521
31.
Golubev O., Maximov A. Hybrid plasma-catalytic CO2
org/10.1088/1361-6463/aaa919
dissociation over basic metal oxides combined with
21.
Ashford B., Wang Y., Poh C.-K., Chen L., Tu X. Plasma-
catalytic conversion of CO2 to CO over binary metal
org/10.3390/pr11051553
oxide catalysts at low temperatures // Appl. Catal. B
32.
Jin S., Bang G., Liu L., Lee C.-H. Synthesis of
mesoporous MgO-CeO2 composites with enhanced CO2
apcatb.2020.119110
capture rate via controlled combustion // Microporous
22.
Wang L., Du X., Yi Y., Wang H., Gul M., Zhu Y., Tu X.
Plasma-enhanced direct conversion of CO2 to CO over
org/10.1016/j.micromeso.2019.109587
oxygen-deficient Mo-doped CeO2 // Chem. Commun.
33.
Jin S., Ko K.-J., Lee C.-H. Direct formation of
hierarchically porous MgO-based sorbent bead for
D0CC06514E
enhanced CO2 capture at intermediate temperatures //
23.
Golubev O.V., Maksimov A.L. Plasma-assisted catalytic
decomposition of carbon dioxide // Russ. J. Appl.
org/10.1016/j.cej.2019.04.020
34.
Pawar A.A., Lee D., Kim H. Understanding the synergy
S1070427222050019
between MgO-CeO2 as an effective promoter and ionic
24.
Duan X., Hu Z., Li Y., Wang B. Effect of dielectric
liquids for high dimethyl carbonate production from
packing materials on the decomposition of carbon
CO2 and methanol // Chem. Eng. J. 2020. V. 395. ID
dioxide using DBD microplasma reactor // AIChE
35.
Ruhaimi A.H, Aziz M.A.A. Fabrication of mesoporous
aic.14682
CeO2-MgO adsorbent with diverse active sites via
25.
Mei D., He Y., Liu S., Yan J., Tu X. Optimization of CO2
eggshell membrane-templating for CO2 capture // Appl.
conversion in a cylindrical dielectric barrier discharge
reactor using design of experiments // Plasma Process.
s00339-021-05182-5
36.
Holub M. On the measurement of plasma power in
ppap.201500159
atmospheric pressure DBD plasma reactors // Int. J.
26.
Wang B., Li X., Wang X., Zhang B. Effect of filling
Appl. Electromagn. Mech. 2012. V. 39. P. 81-87. https://
materials on CO2 conversion with a dielectric barrier
doi.org/10.3233/JAE-2012-1446
НЕФТЕХИМИЯ том 63 № 5 2023
734
ГОЛУБЕВ и др.
37. Xu C., Shi S., Dong Q., Zhu S., Wang Y., Zhou H., Wang
аргона и оптически возбужденных паров натрия //
X., Zhu L., Zhang G., Xu D. Citric-acid-assisted sol-
Журнал технической физики. 1999. № 4. С. 361-366
gel synthesis of mesoporous silicon-magnesium oxide
[Gorbunov N.A., Mel’nikov A.S. Effect of molecular
ceramic fibers and their adsorption characteristics //
nitrogen on the electron mobility in a mixture of argon
and optically excited sodium vapor // Tech. Phys. 1999.
org/10.1016/j.ceramint.2019.12.279
38. Parameswaram G., Rao P.S.N., Srivani A., Nageswara
42. Смирнов С.А., Титов В.А., Шикова Т.Г., Овцын А.А.,
Rao G., Lingaiah N. Magnesia-ceria mixed oxide
Кадников Д.В. Влияние газообразных продуктов ге-
catalysts for the selective transesterification of glycerol
терогенных реакций на параметры плазмы аргона //
to glycerol carbonate // Mol. Catal. 2018. V. 451.
Прикладная физика. 2016. № 4. С. 43-48.
43. Aerts R., Snoeckx R., Bogaerts A. In-situ chemical
39. Zheng X., Li Y., Zhang L., Shen L., Xiao Y., Zhang
trapping of oxygen in the splitting of carbon dioxide
Y., Jiang L. Insight into the effect of morphology on
by plasma // Plasma Process. Polym. 2014. V. 11.
catalytic performance of porous CeO2 nanocrystals for
H2S selective oxidation // Appl. Catal. B. 2019. V. 252.
44. Морозов С.А., Малков А.А., Малыгин А.А. Синтез
пористого оксида магния термическим разложением
40. Zhang Y., Wang H.-Y., Zhang Y.-R., Bogaerts A.
основного карбоната магния // Журн. общей химии.
Formation of microdischarges inside a mesoporous
catalyst in dielectric barrier discharge plasmas // Plasma
2003. Т. 73. № 1. С. 37-42 [Morozov S.A., Malkov A.A.,
Sources Sci. Technol. 2017. V. 26. ID 054002. https://
Malygin A.A. Synthesis of porous magnesium oxide by
doi.org/10.1088/1361-6595/aa66be
thermal decomposition of basic magnesium carbonate //
41. Горбунов Н.А., Мельников А.С. Влияние молеку-
лярного азота на подвижность электронов в смеси
org/10.1023/a:1023466200445].
НЕФТЕХИМИЯ том 63 № 5 2023