Химия твердого топлива, 2021, № 4, стр. 27-33
ИЗМЕНЕНИЕ СОСТАВА И СВОЙСТВ ГУМИНОВЫХ ВЕЩЕСТВ ПРИ МЕХАНООБРАБОТКЕ УГЛЕЙ С МИНЕРАЛЬНЫМИ СОЛЯМИ
Н. В. Юдина 1, *, А. В. Савельева 1, **, Е. В. Линкевич 1, ***
1 ФГБУН Институт химии нефти СО РАН
634055 Томск, Россия
* E-mail: natal@ipc.tsc.ru
** E-mail: anna@ipc.tsc.ru
*** E-mail: maltseva2@gmail.ru
Поступила в редакцию 11.12.2020
После доработки 10.02.2021
Принята к публикации 06.04.2021
Аннотация
При механообработке (МО) бурых углей в присутствии комплекса окислительно-щелочных реагентов и минеральных солей повышается выход водорастворимых гуминовых веществ (ГВ) на 20–30%. Состав углей и реагентов при МО оказывает влияние на содержание кислых функциональных групп в гуминовых кислотах. Ионообменные процессы при МО углей с минеральными солями сопровождаются повышением в составе ГВ макро- и микроэлементов. Установлено значительное увеличение антиоксидантной активности гуминовых кислот при МО с фосфорнокислым аммонием и сульфатом аммония. Минеральные элементы в составе ГВ проявляют физиологическую активность, оказывая влияние на развитие корней и проростков пшеницы.
ВВЕДЕНИЕ
Гуминовые вещества (ГВ), содержащиеся во всех природных средах, выполняют две очень важные функции для регуляции роста и развития растений: защитную и физиологическую. В [1–3] изучено защитное действие ГВ по отношению к проросткам пшеницы в условиях неблагоприятных температур, водного дефицита, химического стресса, зависящее от структурных особенностей ГВ и биодоступности.
Повышение продуктивности посевов сельскохозяйственных культур связано с физиологической функцией ГВ. Среди природных стимуляторов роста определенным физиологическим эффектом характеризуются хорошо усваиваемые растениями растворимые соли гуминовых кислот (ГК) с одновалентными металлами, полученные щелочным гидролизом. Гидролиз и окисление являются эффективными методами химической деструкции гуминсодержащего сырья для получения биологически активных препаратов с заданными свойствами [4].
Для придания специфических свойств гуминовым веществам предложены разные способы модификации их структуры. Благодаря высокому содержанию функциональных групп ГК являются перспективными веществами для создания комплексов с металлами. Комплекс ГК с железом оказывает положительное влияние на функциональное состояние, антиоксидантный статус растений, выращенных в условиях дефицита железа [5]. Показана возможность использования угольных и торфяных ГВ и их силанольных производных в качестве стимуляторов роста растений с замедленным высвобождением доступного азота [6].
Модификация ГК при механохимических способах обработки углей сопровождается окислительной деструкцией, приводящей к изменению выхода и состава экстрагируемых веществ [7–11]. Наиболее изучена твердофазная обработка бурого угля в присутствии окислительно-щелочных реагентов, в результате которой увеличивается содержание фенольных и карбоксильных групп в структуре гуминовых кислот [12–15].
Повышение физиологической активности гуминовых препаратов возможно путем обогащения ГК макро- и микроэлементами при механообработке угля. В результате стимулирующего действия ГК усиливается поступление в растения минеральных элементов в виде катионов и анионов через корневую систему. Как было показано ранее [16], добавки минеральных солей при механообработке окисленного угля вызывают изменения ионного состава ГК, поверхностной и физиологической активности.
Цель настоящего исследования заключалась в получении из бурых углей разного состава водорастворимых гуминовых веществ, обогащенных микро- и макроэлементами.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В табл. 1 приведена характеристика бурого угля (БУ Чинг-Чай, Китай) и окисленного угля (ОУ Баганур, Монголия). Видно, что угли существенно различаются зольностью и влажностью.
Таблица 1.
Характеристика окисленного и бурого углей
| Уголь | А, мас. % | W, мас. % | Содержание элементов, мас. % | |||
|---|---|---|---|---|---|---|
| Са | Mg | K | P | |||
| ОУ | 12.7 | 14.8 | 0.35 | 0.10 | 0.05 | 0.19 |
| БУ | 29.9 | 6.7 | 0.45 | 0.14 | 0.05 | 0.10 |
Количественное определение элементов в ОУ и БУ проводили методом атомно-эмиссионной спектрометрии АЭС с МАЭС (комплекс “Гранд”, НПО “Оптоэлектроника”, Россия). Пробы помещали в предварительно прокаленные и взвешенные кварцевые тигли, добавляли 20 мкл H2SО4 (конц.) и обрабатывали в муфельной печи до постоянной массы золы при постепенном повышении температуры до 450–500°С. Навески анализируемых, холостых проб и стандартных образцов состава графитового коллектора микропримесей СОГ-37 (ГСО 8487-2013) испаряли из канала анодного электрода. Катодом служил графитовый электрод марки ОСЧ-7–4. Параметры регистрации спектров: постоянный ток 13 А; расстояние между электродами – 0.003 м; ширина щели – 3.0 ⋅ 10–5 м; диафрагма – 0.005 м; накоплений – 160; длительность накоплений – 125 мс; полная экспозиция – 20 с.
Механообработку (МО) углей проводили в планетарной мельнице АГО–2 [15]. Для создания окислительно-щелочных условий при МО углей использовали химически чистые (х. ч.) и чистые (ч.) реагенты (Россия). Количество и чистота реагентов, используемых при МО углей, приведены в табл. 2.
Таблица 2.
Состав реагентов и чистота реагентов, используемых при МО
| № образца | Окислительно- щелочной реагент | Минеральная соль | Качество реактива, поставщик |
|---|---|---|---|
| 1 | 0.1 н. раствор NaOH | – | Х.ч., “Реахимприбор” |
| 2 | 5 мас. % NaOH | – | Х.ч., “ХПК-Групп” |
| 3 мас. % Na4P2O7 | – | Х.ч., “Перкарбонат” | |
| 3 мас. % Na2CO3 ⋅ 1.5⋅ H2O2 | – | – | |
| 3 | То же | 1 мас. % NH4H2PO4 | Х.ч., “ХПК-Групп” |
| 4 | – | 5 мас. % NH4H2PO4 | То же |
| 5 | – | 1 мас. % (NH4)SO4; | – |
| 6 | – | 5 мас. % (NH4)SO4 | – |
| 7 | – | 0.5 мас. % СаCl2 | – |
| 8 | – | 2 мас. % СаCl2 | – |
| 9 | – | 0.5 мас. % MgSO4 | – |
| 10 | – | 2 мас. % MgSO4 | – |
Гуминовые кислоты выделяли из исходных углей 0.1 н NaОН при температуре 90°С и перемешивании в течение 1 ч. Щелочную экстракцию повторяли трижды. Гуминовые кислоты в щелочном растворе осаждали 10%-ным раствором HCl. Бурый аморфный осадок ГК отделяли центрифугированием, затем отмывали дистиллированной водой до значения рН 7 и высушивали в чашке Петри в вакуумном шкафу до постоянной массы.
Гуминовые вещества из механообработанных углей экстрагировали дистиллированной водой. Водные растворы ГВ (рН 8–9) центрифугировали, фильтровали и высушивали до постоянной массы.
Методом потенциометрического титрования определяли содержание кислых ионогенных групп. Во время титрования ГК ионную силу раствора поддерживали на постоянном уровне насыщенным раствором хлорида натрия. На полученных кривых титрования выделяли три четких перегиба в области рН 10–11 (фенольные гидроксилы Ar-OH), рН 6.5–9.5 (карбоксильные группы при ароматическом кольце Ar-COOH), рН 2.5–6.5 (карбоксильные группы при углеводородных цепочках Alk-COOH). Расчет точки эквивалентности проводили с помощью численной интерполяции.
Вольтамперометрическим методом катодного восстановления кислорода с использованием ртутного пленочного электрода определяли антиоксидантные свойства ГК. Фоновым электролитом являлся фосфатный буфер (рН 6.8). По результатам определений строился график зависимости функции (1 – I/I0) от времени (t). Данный график обрабатывался методом наименьших квадратов, и находился тангенс угла наклона этого графика по линейной части кривой d(1–I/I0)/dt. По линейной части графика и по тангенсу угла наклона касательной к данному участку кривой рассчитывался кинетический критерий К, мкмоль/(л·мин) согласно формуле:
где I – ток электровосстановления (ЭВ О2) в присутствии ГК в растворе, мкА; I0 – ток ЭВ О2 в отсутствие ГК в растворе, мкА; ${\text{C}}_{{{{{\text{O}}}_{2}}}}^{0}$– исходная концентрация кислорода в растворе, мкмоль/л; t – время протекания процесса, мин.Критерий К отражает количество кислорода и активных кислородных радикалов, прореагировавших с антиоксидантом в течение 1 мин [17].
Методом капиллярного электрофореза установлен анионный и катионный состав гумата натрия и водорастворимых ГВ. Метод основан на разделении заряженных компонентов сложной смеси вкварцевом капилляре под действием приложенного электрического поля. Анализируемый раствор вводили в кварцевый капилляр, предварительно заполненный буфером-электролитом. В качестве буферного электролита использовали раствор бензимидазола в винной кислоте с добавлением раствора эфира 18-краун-6. После подачи высокого напряжения (до 30 кВ) в капилляре быстро устанавливается стационарное состояние: через капилляр протекает постоянный электроосмотический поток, на который накладывается взаимно противоположная электромиграция катионов и анионов. На электрофореграмме, полученной с помощью фотометрического детектора, по времени миграции идентифицируются катионы и анионы, а их содержание определяется по площади соответствующего пика.
Физиологическую активность гуминовых веществ оценивали по их влиянию на длину корня, высоту стебля проростка семян пшеницы негенномодифицированного сорта Самурай через 10 дней развития. Семена обрабатывали растворами, содержащими 0.05 мас. % гумата натрия и водорастворимых ГВ.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Окисленный и бурый уголь отличаются не только технической характеристикой, но и выходом ГК при щелочной экстракции (рис. 1 и 2). Условия механообработки и количество реагентов при МО углей приведены в табл. 2. Ранее было показано, что МО углей при увеличении количества NaOH с 3 до 8–12 мас. % позволяет извлечь водорастворимые ГВ, что объясняется максимальным замещением водорода в СООН-группах на неорганический катион [18]. Слабое поглощение катионов щелочных металлов при низкой концентрации связано с тем, что карбоксильные группы в ГК имеют значительно большее сродство к протонам.
Рис. 1.
Зависимость выхода ГВ и ГК из окисленного угля от условий механообработки (условия МО см. в табл. 2).
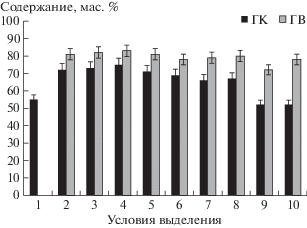
Рис. 2.
Зависимость выхода ГВ и ГК из бурого угля от условий механообработки (условия МО см. в табл.2).

При МО с комплексом окислительно-щелочных реагентов выход ГВ из ОУ составляет 78 мас. %, из БУ – 60 мас. % (рис. 1, 2). Добавки фосфорнокислого аммония (образцы 3 и 4) и сульфата аммония (образцы 5 и 6) при механическом воздействии на окисленный уголь незначительно повышают выход ГК и ГВ, при этом из бурого угля количество извлекаемых ГК на 20–27 мас. % больше, чем при щелочном гидролизе (образец 1). МО углей с хлористым кальцием (образцы 7 и 8) и сульфатом магния (образец 9 и 10) оказалась менее результативной, выходы ГК снизились и составили 53–65 мас. % для ОУ и 45–53 мас. % для БУ.
Условия МО углей влияют на функциональный состав ГК (табл. 3). Гуминовые кислоты, выделенные из БУ после МО с комплексом щелочно-окислительных реагентов, характеризуются более значительным повышением содержания фенольных и карбоксильных групп за счет реализации механизма радикального окисления в присутствии перкарбоната натрия (образцы 2).
Таблица 3.
Содержание функциональных групп в ГК углей, мг-экв/г
| № образца* | ОУ | БУ | ||||
|---|---|---|---|---|---|---|
| ArOH | ArСОOH | CnCOOH | ArOH | ArСОOH | CnCOOH | |
| 1 | 9.1 ± 0.3 | 6.3 ± 0.3 | 1.6 ± 0.1 | 9.3 ± 0.7 | 4.8 ± 0.3 | 1.1 ± 0.1 |
| 2 | 10.0 ± 0.2 | 7.3 ± 0.2 | 2.1 ± 0.2 | 11.0 ± 0.9 | 7.0 ± 0.2 | 2.6 ± 0.4 |
| 3 | 9.2 ± 0.3 | 5.4 ± 0.4 | 1.9 ± 0.3 | 11.8 ± 0.4 | 6.8 ± 0.3 | 2.4 ± 0.1 |
| 4 | 9.6 ± 0.2 | 5.9 ± 0.3 | 1.8 ± 0.2 | 12.6 ± 0.2 | 6.7 ± 0.2 | 2.7 ± 0.3 |
| 5 | 10.5 ± 0.4 | 6.0 ± 0.2 | 1.9 ± 0.1 | 12.9 ± 0.2 | 6.8 ± 0.2 | 2.3 ± 0.3 |
| 6 | 10.6 ± 0.2 | 6.0 ± 0.3 | 1.9 ± 0.3 | 12.7 ± 0.3 | 6.9 ± 0.3 | 2.5 ± 0.1 |
| 9 | 12.7 ± 0.2 | 7.6 ± 0.3 | 2.9 ± 0.2 | 10.6 ± 0.2 | 7.6 ± 0.3 | 2.9 ± 0.1 |
| 10 | 12.1 ± 0.4 | 7.8 ± 0.2 | 2.9 ± 0.1 | 11.4 ± 0.2 | 7.9 ± 0.2 | 2.9 ± 0.1 |
* Номер образца соответствует обозначению в табл. 2.
Добавки минеральных солей в процессе МО окисленного угля изменяют кислотно-щелочное равновесие в системе реагентов. Фосфорнокислый аммоний и сульфат аммония проявляют кислотные свойства и снижают щелочность при экстракции ГК, что, очевидно, приводит к снижению в их составе фенольных и карбоксильных групп в ароматическом кольце [19].
В ГК из бурого угля после МО с комплексом окислительно-щелочных реагентов и минеральных солей отмечается рост содержания фенольных и карбоксильных групп, что может быть обусловлено снижением роли щелочной составляющей при количестве воды в угле 6.7 мас. % и реализацией механизма радикального окисления [12].
Неблагоприятные факторы окружающей среды провоцируют в клетках живых организмов неконтролируемый рост свободных радикалов, что проводит к нарушению дисбаланса между скоростью образования и элиминации активных кислородных форм, что приводит к оксидативному стрессу. Нейтрализация радикалов и прекращение цепной реакции в биологических объектах осуществляются антиоксидантами с различным механизмом действия [20]. В практике растениеводства активно применяют антиоксиданты для увеличения устойчивости растений к действию стрессоров биогенной и абиогенной природы [21, 22]. Исследования, проведенные в [23], свидетельствуют, что внесение минеральных и органических удобрений приводит к значительному увеличению антиоксидантной емкости почв.
Механизм действия ГК в процессе электровосстановления кислорода заключается в реакции диспропорционирования активных форм кислорода и оценивается по значению критерия К [17]. Антиоксидантная активность ГК из окисленного угля для всех образцов выше, чем ГК из бурого угля (табл. 4). Максимальной величины критерий К достигает в ГК, выделенных из обоих углей при МО с фосфорнокислым аммонием и сульфатом аммония (образцы 3–6). В составе этих образцов снизилось содержание карбоксильных групп при ароматическом кольце. Считается, что наличие фенольных фрагментов определяет антиоксидантную активность ГК, которая может снижаться в зависимости от расположения карбоксильных групп в фенольном кольце [24–27]. Возможно, депротонирование карбоксильной группы усилит антиоксидантную активность фенолов. В ГК из бурого угля изменения количества карбоксильных групп при ароматическом кольце менее заметны.
Таблица 4.
Критерий антиоксидантной активности ГК
| № образца* | К, мкмоль/л мин | |
|---|---|---|
| ГК ОУ | ГК БУ | |
| 1 | 0.368 | 0.271 |
| 2 | 0.397 | 0.294 |
| 3 | 0.668 | 0.568 |
| 4 | 0.805 | 0.610 |
| 5 | 0.687 | 0.423 |
| 6 | 0.705 | 0.401 |
| 7 | 0.321 | 0.278 |
| 8 | 0.365 | 0.193 |
| 9 | 0.245 | 0.194 |
| 10 | 0.237 | 0.175 |
* Номер образца соответствует обозначению в табл. 2.
Эффективность МО углей с минеральными солями оценивали по содержанию анионов и катионов в гумате натрия и водорастворимых гуминовых веществах (табл. 5 и 6). В гумате натрия обнаружены анионы ${\text{SO}}_{4}^{{2 - }}$, ${\text{PO}}_{4}^{{3 - }}$, ${\text{NO}}_{3}^{ - }$, их содержание возрастает в образце 2, полученном при МО угля с комплексом окислительно-щелочных реагентов. При МО угля с добавками фосфорнокислого аммония в образцах 3 и 4 возрастает количество фосфат- и нитрат-ионов, и появляется гидрофосфат-ион. Максимальное количество сульфат- и нитрат-ионов обнаружено в образцах 5 и 6, полученных при МО угля с сульфатом аммония.
Таблица 5.
Анионный состав гуминовых веществ ОУ и БУ
| № образца* | Концентрация анионов, мг/л | |||||||
|---|---|---|---|---|---|---|---|---|
| ОУ | БУ | |||||||
| ${\text{SO}}_{4}^{{2 - }}$ | ${\text{HPO}}_{4}^{{2 - }}$ | ${\text{PO}}_{4}^{{3 - }}$ | ${\text{NO}}_{3}^{ - }$ | ${\text{SO}}_{4}^{{2 - }}$ | ${\text{HPO}}_{4}^{{2 - }}$ | ${\text{PO}}_{4}^{{3 - }}$ | ${\text{NO}}_{3}^{ - }$ | |
| 1 | 7.51 | – | 0.50 | 0.52 | 9.83 | – | 0.50 | 0.20 |
| 2 | 12.83 | – | 12.51 | 11.90 | 10.60 | – | 11.51 | 2.91 |
| 3 | 0.60 | 9.41 | 1.50 | 15.35 | 0.56 | 5.66 | 1.81 | 10.30 |
| 4 | 0.79 | 5.86 | 8.45 | 17.41 | 0.51 | 2.59 | 3.82 | 11.42 |
| 5 | 25.87 | – | 3.12 | 21.84 | 59.13 | – | 2.49 | 22.4 |
| 6 | 111.05 | – | 3.90 | 22.36 | 22.5 | – | 1.91 | 20.51 |
* Номер образца соответствует обозначению табл. 2.
Таблица 6.
Катионный состав гуминовых веществ ОУ и БУ
| № об-разца* | Концентрация катионов, мг/л | |||||
|---|---|---|---|---|---|---|
| ОУ | БУ | |||||
| Na+ | Mg2+ | Ca2+ | Na+ | Mg2+ | Ca2+ | |
| 1 | 70.83 | 0.75 | 3.73 | 34.04 | 0.75 | 3.73 |
| 2 | 126.60 | 1.14 | 4.47 | 119.1 | 1.65 | 4.01 |
| 7 | 97.70 | 2.44 | 21.62 | 90.7 | 1.99 | 19.40 |
| 8 | 80.46 | 3.99 | 22.97 | 65.22 | 1.43 | 23.51 |
| 9 | 97.6 | 3.10 | 12.38 | 88.8 | 2.10 | 14.38 |
| 10 | 95.4 | 5.75 | 11.04 | 91.4 | 2.75 | 13.01 |
* Номер образца соответствует обозначению в табл. 2.
Условия МО оказали влияние на катионный состав полученных образцов (табл. 6). В гуматах натрия обнаружено высокое содержание ионов Na+, присутствуют ионы Mg2+ и Ca2+. МО углей с комплексом окислительно-щелочных реагентов увеличиваетв ГВ количество Na+, замещающего протоны. Добавки других реагентов приводят к перераспределению катионов. При использовании в процессе МО угля хлорида кальция и сульфата магния снижается концентрация ионов Na+ за счет замещения их в структуре ГК на ионы Са2+и Mg2+. Значения концентрационных констант обмена Na–Са и Na–Mg в ГВ свидетельствуют о преимущественной сорбции ионов кальция и значительной подвижности ионов натрия. Добавка сульфата магния при МО углей приводит к снижению в составе ГВ содержания ионов Ca2+, что объясняется реакциями ионного обмена.
По результатам биотестирования установлено, что при обработке семян пшеницы полученными препаратами отмечено интенсивное развитие проростков пшеницы (рис. 3).
Повышение количества гидрофосфат-ионов в образце 3 способствует развитию более мощной корневой системы. Максимальное увеличение высоты побегов и всхожесть семян отмечаются для образцов 3, 4, 5 и 6, обработанных с фосфорнокислым аммонием и сульфатом аммония. Сульфат-ион легко усваивается корневой системой и ускоряет рост новых побегов. Ионы кальция и магния, присутствующие в образцах 7–10, укрепляют стенки клеток и способствуют развитию более мощной корневой системы. Сульфат магния, диссоциируя на ионы, переходит в обменное состояние и становится доступен для растений.
ЗАКЛЮЧЕНИЕ
В результате МО бурых углей с окислительно-щелочными реагентами образуются водорастворимые ГВ, выход которых возрастает до 60 мас. % для бурого угля и 78 мас. % для окисленного угля. Добавки минеральных солей более эффективно повышают выход ГВ до 70 мас. % при МО бурого угля.
При МО окисленного угля с комплексом окислительно-щелочных реагентов, фосфорнокислого аммония и сульфата аммония в составе выделенных ГК снижается содержание фенольных и карбоксильных групп за счет изменения кислотно-щелочного баланса системы. Повышение количества кислых групп в составе ГК после МО бурого угля может быть связано с реализацией механизма радикального окисления за счет кислорода воздуха и перкарбоната натрия при низком содержании воды в составе угля.
Наличие в ГК кислородсодержащих функциональных групп, различных катионов и анионов способствует процессу переноса электронов и протонов в результате окислительно-восстановительных реакций. Максимальной антиоксидантной активностью характеризуются ГК, полученные после МО углей в присутствии фосфорнокислого аммония и сульфата аммония.
Механообработка углей с минеральными солями сопровождается ионообменными процессами и повышением в составе водорастворимых ГВ катионов Са2+, Mg2+ и анионов ${\text{SO}}_{4}^{{2 - }}$, ${\text{HPO}}_{4}^{{2 - }}$, ${\text{NO}}_{3}^{ - }$, что отражается на их физиологической активности.
Список литературы
Куликова Н.А., Филиппова О.И. // Агрохим. вестн. 2018. № 2. С. 33.
Куликова Н.А., Филиппова О.И., Перминова И.В. // Вестн. МГУ. Сер. 17: Почвоведение. 2018. № 2. С. 35.
Куликова Н.А., Перминова И.В., Лебедева Г.Ф. // Почвоведение. 2003. № 10. С. 1207. [Eurasian Soil Science, 2003. V. 36. № 10. P. 1074].
Томсон А.Э., Наумова Г.В., Жмакова Н.А. // ХТТ. 2017. № 5. С. 53. [Solid Fuel Chemistry, 2017. V. 51. № 5. P. 315]. https://doi.org/10.3103/S0361521917050123https://doi.org/10.7868/S0023117717050085
Аброськин Д.П., Фуентес М., Гарсиа-Мина Х.М., Кляйн О.И., Сеник С.В., Волков Д.С., Перминова И.В., Куликова Н.А. // Почвоведение. 2016. № 10. С. 1167. [Eurasian Soil Science, 2016. V. 49. № 10. P. 1049]. https://doi.org/10.1134/S1064229316100021
Филиппова О.И., Куликова Н.А., Бычкова Я.С., Воликов А.Б., Перминова И.В. // Проблемы агрохимии и экологии. 2015. № 1. С. 42.
Пройдаков А.Г. // ХТТ. 2009. № 1. С. 13. [Solid Fuel Chemistry, 2009. V. 43. № 1. P. 9]. https://doi.org/10.3103/S0361521909010030
Пройдаков А.Г., Калабин Г.А. // ХТТ. 2009. № 2. С. 28. [Solid Fuel Chemistry, 2009. V. 43. № 2. P. 86]. https://doi.org/10.3103/S0361521909020050
Пройдаков А.Г., Полубенцев А.В., Кузнецова Л.А. // Химия в интересах устойчивого развития. 2005. Т. 13. № 4. С. 641.
SkripkinaT.S., Bychkov A.L., Tikhova V.D., Smolyakov B.S., Lomovsky O.I. // Environmental Technology & Innovation. 2018. V. 11. P. 74. https://doi.org/10.1016/j.eti.2018.04.010
Urazova T.S., Bychkov A.L., Lomovskii O.I. // Rus. chem. Bull. 2015. V. 64. I. 5. P. 1183. https://doi.org/10.1007/s11172-015-0997-0.
Скрипкина Т.С., Бычков А.Л., Тихова В.Д., Ломовский О.И. // ХТТ. 2018. №. 6. С. 16. [Solid Fuel Chemistry, 2018. V. 52. № 6. P. 356]. https://doi.org/10.3103/S0361521918060101.https://doi.org/10.1134/S0023117718060117
Савельева А.В., Иванов А.А., Юдина Н.В., Ломовский О.И., Дугаржав Дж. // ЖПХ. 2013. Т. 86. №. 4. С. 592. [Russian Journal of Applied Chemistry, 2013. V. 86, no. 4, P. 552]. https://doi.org/10.1134/S1070427213040174.
Юдина Н.В., Савельева А.В., Линкевич Е.В. // ХТТ. 2019. № 1. С. 34. [Solid Fuel Chemistry, 2019. V. 53. № 1. P. 29]. https://doi.org/10.3103/S0361521919010099https://doi.org/10.1134/S0023117719010092
Юдина Н.В., Савельева А.В., Ломовский O.И. // Химия в интересах устойчивого развития. 2019. Т. 27. № 4. С. 437. https://doi.org/10.15372/KhUR2019156
Юдина Н.В., Мальцева Е.В., Смирнова А.С., Березина Е.М. // ЖПХ. 2016. Т. 89. Вып. 6. С. 812. [Russian Journal of Applied Chemistry, 2016. V. 89. no. 6. P. 969]. https://doi.org/10.1134/S1070427216060215
Юдина Н.В., Савельева А.В., Иванов А.А. Короткова Е.И., Ломовский О.И. // ЖПХ. 2004. Т. 77. Вып. 1. С. 48. [Russian Journal of Applied Chemistry, 2004. V. 77, no. 1. P. 46]. https://doi.org/10.1023/B:RJAС.0000024574.01023.fe
Савельева А.В., Мальцева Е.В., Юдина Н.В., Ломовский О.И. // Химия в интересах устойчивого развития. 2016. Т. 24. № 2. С. 263.https://doi.org/10.15372/KhUR20160221
Жеребцов С.И., Вотолин К.С., Малышенко Н.В., Смотрина О.В., Дугаржан Ж., Исмагилов З.Р. // ХТТ. 2019. № 5. С. 3. [Solid Fuel Chemistry, 2019. V. 53. № 5. P. 253]. https://doi.org/10.3103/S0361521919050124.https://doi.org/10.1134/S0023117719050128
Klein O.I., Kulikova N.A., Filimonov I.S., Koroleva O.V., Konstantinov A.I. J. Soilsand Sediments. 2018. V. 18. № 4. P. 1355. https://doi.org/10.1007/s11368-016-1538-7
Tarasova A.S., Stom D.I., Kudryasheva N.S. Environ Monit Assess. 2015. V. 187. № 3. P. 4304. https://doi.org/10.1007/s10661-015-4304-1
Пахомова В.М., Даминова А.И. // Достижения науки и техники в АПК. 2019. Т. 33. № 11. С. 26. https://doi.org/10.24411/0235-2451-2019-11106
Кляйн О.И., Николаев И.В., Куликова Н.А., Степанова Е.В., Королева О.В. // Вестн. МГУЛ - Лесной вестн. 2012. № 1. С. 109.
Aeschbacher M., Graf C., Schwarzenbach R.P., Sander M. // Environ Sci. Technol. 2012. V. 46. P. 4916. https://doi.org/10.1021/es300039h
Смирнова О.В., Ефимова И.В., Хилько С.Л., Опейда И.А., Рыбаченко В.И. // Наносистемы, наноматериалы, нанотехнологии. 2010. Т. 8. № 4. С. 835.
Abdullah G. Al-Sehemi, Ahmad Irfan, Salha Mana Aljubiri, Kamel Hussein Shaker //J. Saudi Chem. Society. 2016. V. 20. № 1. P. 521.
KhiI’ko S.L., Efimova I.V., Smirnova O.V. // Solid Fuel Chemistry. 2011. V. 45. № 6. Р. 367. https://doi.org/10.3103/S036152191106005X
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива



