Журнал аналитической химии, 2022, T. 77, № 8, стр. 734-741
Тест-системы на основе нановолокон, полученных методом электроформования, для определения ионов никеля
Н. С. Комова a, b, А. И. Данчук a, В. В. Галушка a, А. М. Павлов a, А. А. Сердобинцев a, Т. Ю. Русанова a, *
a Саратовский национальный исследовательский государственный университет
имени Н.Г. Чернышевского, Институт химии
410012 Саратов, ул. Астраханская, 8, Россия
b Федеральный исследовательский центр “Фундаментальные основы биотехнологии”
Российской академии наук”, Институт биохимии им. А.Н. Баха
119071 Москва, Ленинский просп., 33, стр. 2, Россия
* E-mail: tatyanarys@yandex.ru
Поступила в редакцию 07.08.2021
После доработки 28.10.2021
Принята к публикации 28.10.2021
- EDN: HAPXKH
- DOI: 10.31857/S0044450222080047
Аннотация
Разработаны тест-системы на основе полимерных нановолокон, полученных методом электроформования, для определения ионов никеля в природных и сточных водах. Детектирование аналитического сигнала тест-систем может проводиться как визуально, так и методом цветометрии. В качестве полимерой матрицы использовали полиакрилонитрил и фторопласт, а в качестве реагентов – рубеановодородную кислоту, пиридилазонафтол, диметилглиоксим и α-фурилдиоксим. Иммобилизацию реагентов в матрицу осуществляли путем их добавления в формовочный раствор полимера до начала процесса изготовления волокна. Выбраны оптимальные условия получения тест-систем (состав формовочного раствора, параметры элктроформования, природа полимера и реагента) и регистрации аналитического сигнала (рН, параметр цветности, время регистрации сигнала). Определены параметры градуировочных зависимостей для определения ионов никеля с использованием различных тест-систем и изучена их селективность по отношению к ионам других тяжелых металлов. Показано, что тест-система на основе полиакрилонитрила (массовая доля полимера в формовочном растворе 12%) и рубеановодородной кислоты (концентрация реагента в формовочном растворе 0.05 М) позволяет определять ионы никеля в диапазоне концентраций 1 × 10–6 M–0.01 M. Разработанные тест-системы применены для определения ионов никеля в природной, водопроводной и сточной водах. Достоинством предложенных тест-систем является простота изготовления тестов, отсутствие пробоподготовки и возможность проведения анализа в полевых условиях.
Немаловажную роль в загрязнении окружающей среды играют тяжелые металлы, к которым относится и никель. Основные источники загрязнения окружающей среды никелем – предприятия горнорудной промышленности, цветной металлургии, металлообрабатывающие и другие. Никель является необходимым микроэлементом для млекопитающих и растений, обнаруживается во всех биологических материалах. В то же время никель относится к веществам второго класса опасности и оказывает общетоксическое действие на организм. Хроническая интоксикация приводит к возникновению заболеваний носоглотки, легких, появлению злокачественных новообразований и аллергических поражений в виде дерматитов и экзем. В нашей стране установлены ПДК на никель в объектах окружающей среды. Благодаря современным достижениям в области электроники и механики стало возможным применение высокотехнологичных установок для определения ионов никеля при низких концентрациях методами спектрометрии с индуктивно связанной плазмой [1], атомно-абсорбционной спектроскопии [2] и спектрофотомерии [3]. Некоторые из перечисленных методов являются достаточно сложными, требуют дорогостоящего оборудования и непригодны для быстрого и оперативного мониторинга. В качестве альтернативы перечисленным выше методам возрастает значение тест-систем для определения ионов никеля,. Преимуществами использования тест-методов являются отсутствие высоких требований к квалификации персонала, низкая стоимость материалов, простота и экспрессность. Чаще всего такие тест-системы получают на основе фильтровальной бумаги или трубок с порошками, в которых на твердую фазу иммобилизован соответствующий аналитический реагент [4].
Для визуального определения ионов никеля предложен ряд твердофазных носителей на основе силикагеля [5, 6] и ионообменника [7], модифицированных различными реагентами. Визуальный тест-метод с иммобилизованным на силикагеле 4-(2-пиридилазо)-2-нафтолом и его комплексом с Zn(II) позволяет определять Ni(II) в питьевой воде при концентрации ≥3 мкг/л [5]. В работе [6] описана тест-методика концентрирования никеля сорбцией на модифицированном бензилдиоксимом и диметилглиоксимом силохроме СХ-120 для определения никеля в фазе сорбента прямыми методами спектроскопии диффузного отражения и цветометрии. Разработанная методика позволила достичь предела обнаружения никеля 0.3 мкг/мл (в случае бензилдиоксима) и 0.6 мкг/мл (в случае диметилглиоксима) с использованием цветометрических характеристик (светлота, яркость и цветовой тон). Методика имеет один недостаток – окраска сорбатов комплексов никеля во влажном состоянии неравномерна, что затрудняет использование цветометрического метода. Альтернативный твердофазный носитель – макросетчатый карбоксильный катионит КБ-2Э, модифицированный диметилглиоксимом для определения никеля с помощью цветометрических характеристик (R, G, B). Предложенная методика анализа исключает стадию десорбции и позволяет достичь чувствительности определения ионов Ni2+ до 0.0001 ПДК в воде водоемов [7].
В настоящее время все более популярным становится метод электроформования для получения тест-систем на основе нановолокон. Наиболее важными преимуществами данных материалов являются высокая удельная площадь поверхности, большое количество используемых полимеров, а также возможность введения широкого круга реагентов. Эти достоинства позволяют создавать уникальные материалы для различных применений. Об этом свидетельствует большое количество публикаций, посвященных разработке электрохимических сенсоров [8], ферментных биосенсоров [9, 10], флуоресцентных [11] и оптических датчиков [12].
При получении систем с иммобилизованными органическими реагентами используют различные способы внедрения индикатора в структуру волокна. Органические реагенты могут фиксироваться на полимерной матрице как физическим, так и химическим способами [13, 14]. Для иммобилизации физическими способами используют адсорбцию [14], растворение [15], ионный обмен [16] и др. Данные методы достаточно просты, но ограниченная растворимость индикатора в полимерной матрице приводит к выщелачиванию реагента. На наш взгляд, перспективным способом иммобилизации реагентов в нановолокна является введение индикатора в раствор полимера непосредственно перед процессом электроформования, что позволяет избежать вымывания реагента из полученного материала.
Цель настоящей работы − создание тест-систем на основе нановолокон, полученных методом электроформования, с иммобилизованными органическими реагентами и применение данных систем для определения ионов никеля.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и реагенты. Исходный раствор ионов никеля (10 мМ) готовили растворением твердого Ni(NO3)2·6H2O в бидистиллированной воде, рабочие растворы готовили непосредственно перед применением последовательным разбавлением исходного в бидистиллированной воде.
Использовали растворы регентов (ч.д.а.): рубеановодородной кислоты (РК), пиридилазонафтола (ПАН), диметилглиоксима (ДМГ), α-фурилдиоксима (α-ФДО), которые готовили растворением навесок в диметилформамиде (ДМФА, х.ч.).
Растворы полимеров готовили растворением навесок в ДМФА (полиакрилонитрил, ПАНИ, 150 кДа, Sigma-Aldrich) и смеси ДМФА−бутилацетат (1 : 1) (политетрафторэтилен (фторопласт, ФП) Ф42-Л, АО “Галаполимер”, Россия, 100–150 кДа). Растворы перемешивали в течение 3 ч до полного растворения.
Методика получения тест-систем на основе нановолокон с иммобилизованными органическими реагентами. Иммобилизацию реагента в волокно осуществляли путем добавления реагента к раствору полимера до начала процесса изготовления волокна. Формовочный раствор получали смешиванием в соотношении 3 : 1 раствора полимера (полиакрилонитрила или фторопласта) с определенной массовой долей (ω, %) и раствора реагента (РК, ДМГ, ПАН, α-ФДО). Постоянное электрическое напряжение 45 кВ подавали между металлической иглой (положительный электрод), через которую продавливался формовочный раствор с помощью дозатора, и металлической пластиной (отрицательный электрод, заземлен), на которой закреплялась подложка (лист офисной бумаги формата А4, 80 г/м2), на котором происходило осаждение волокон. Расстояние между иглой и подложкой составляло 30 см. Скорость истечения полимера подбирали таким образом, чтобы выталкиваемый полимер успевал переноситься электрическим полем на подложку, не образуя капель и сгустков. После процесса электроформования полученный материал высушивали в течение 1 ч. Далее подготовленный материал удаляли с подложки и нарезали полосками размером 1 × 10 см. Для проведения тест-анализа растворы ионов никеля точечно наносили на материал (объем капли 1 мкл).
Методика определения цветометрических характеристик. Изображения тест-систем получали, используя цифровой фотоаппарат Nikon D 3100. Полученные изображения обрабатывали в программе “Adobe Photoshop CS6”: выделяли пятна исследуемых образцов с помощью инструмента “Магнитное лассо”, далее усредняли цвета пятен согласно следующим операциям: “Фильтр” → → “Размытие” → “Среднее” и, наконец, выбирали цвета с помощью инструмента “Color Picker (Пипетка)”, получая соответствующие цветовые параметры изображений – R, G и B.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
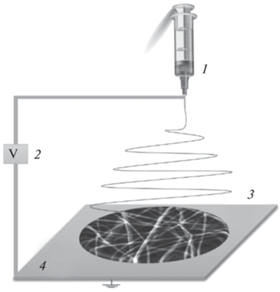
Перспективной основой для тест-систем могут стать волокна, получаемые методом электроформования, в связи с высокой удельной площадью поверхности, возможностью введения широкого круга реагентов, высокой стабильностью реагента в волокне. Такие волокна получают в результате действия электростатических сил на электрически заряженную струю полимерного раствора. Электрическое напряжение от единиц до ста киловольт прикладывается к раствору полимера, который при помощи дозатора подается через капилляр. Высокое напряжение индуцирует в растворе полимера одноименные электрические заряды, которые в результате кулоновского электростатического взаимодействия приводят к вытягиванию раствора полимера в тонкую струю. В процессе электростатического вытягивания полимерной струи она может претерпевать ряд последовательных расщеплений на более тонкие струи при определенном соотношении значений вязкости, поверхностного натяжения и плотности электрических зарядов в волокне. Полученные струи затвердевают за счет испарения растворителя или в результате охлаждения, превращаясь в волокна, и под действием электростатических сил дрейфуют к заземленной подложке, имеющей противоположное значение электрического потенциала (рис. 1).
Рис. 1.
Схема получения нановолокон методом электроформования: 1 – шприц с раствором полимера, 2 – высоковольтный источник тока, 3 – волокно, 4 – коллектор.
Для формирования нановолокон использовали такие полимеры, как полиакрилонитрил и фторопласт. В качестве реагентов выбрали ДМГ, α-ФДО, РК и ПАН как наиболее известные реагенты на ионы никеля. Иммобилизацию реагента в волокно осуществляли путем добавления раствора реагента к раствору полимера до начала процесса изготовления волокна. При этом также варьировали природу и концентрацию реагентов.
В итоге получили следующие материалы:
1) нановолокна на основе полиакрилонитрила (ω = 12%), содержащие в исходном для формования растворе 0.25, 0.125, 0.05 М РК; 2.5 мМ ПАН; 1, 0.5, 0.2 М ДМГ; 0.125 М α-ФДО.
2) нановолокна на основе фторопласта (ω = = 5%), содержащие в исходном для формования растворе 0.25 M РК; 2.5 мМ ПАН.
Морфологию полученных материалов исследовали методом сканирующей электронной микроскопии (СЭМ). В качестве примера на рис. 2 представлены изображения волокон ПАН без красителя (рис. 2а) и с красителем – РК (рис. 2б). Как видно, полученные материалы имеют гладкую и однородную поверхность без узлов. Однако диаметр волокна с красителем несколько больше (∼0.23 ± 0.03 мкм) по сравнению с волокном без красителя (∼0.18 ± 0.03 мкм). Похожая картина наблюдалась и в случае других материалов.
Рис. 2.
СЭМ-изображение волокон полиакрилонитрила без красителя (а) и с красителем – рубеановодородной кислотой (б).

Предварительные исследования полученных материалов показали, что ПАН в полиакрилонитрильном волокне при обработке ионами никелями не дает аналитический сигнал, что, возможно, связано со стерическими затруднениями при взаимодействии этого реагента с ионами металла. Остальные системы дают отклик на никель: ПАН во фторопласте образует хелаты красного цвета, РК образует с никелем голубую внутрикомплексную соль; ДМГ, реагируя с никелем в щелочной среде, образует диоксимный хелат; α-ФГО – устойчивое комплексное соединение желто-оранжевого цвета [17]. Необходимо отметить, что тест-системы на основе фторопласта требуют больше времени для проведения анализа в связи с более высокой гидрофобностью материала.
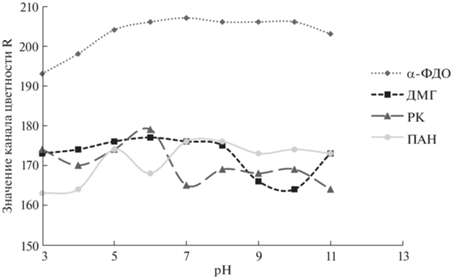
Кислотность среды является одним из важнейших факторов, определяющих направление смещения равновесий процесса комплексообразования. Изучали влияние pH среды на интенсивность окраски комплексов с Ni(II). Помимо визуальной оценки отклика определяли цветометрические характеристики окрашенной зоны. Получили зависимости интенсивностей каналов цветности от pH раствора в интервале 3–11. В качестве примера на рис. 3 представлены зависимости параметра R от рН для разных реагентов. Как видно, изменение pH среды в пределах от 3 до 11 практически не влияет на развитие окраски комплекса с α-ФДО, в то время как наиболее яркая окраска комплекса ионов никеля с РК наблюдается при рН ~7 (наиболее низкое значение параметра цветности), а с ДМГ – в диапазоне pH 9–10. Параметры G и B показывали те же результаты, хотя чувствительность каналов отличалась для различных реагентов.
Рис. 3.
Зависимость канала цветности R пятна тест-систем при определении Ni2+ (с = 1 × 10–3 М) с различными реагентами от pH среды.
Изучали кинетику образования комплексов с ионами никеля. Для этого измеряли аналитический сигнал через определенные промежутки времени после нанесения анализируемого раствора на тест-систему. В качестве примера на рис. 4 показан отклик тест-системы на основе полиакрилонитрила с РК. Для исключения влияния цвета матрицы на оси ординат показано отношение параметров цветности B/R. Установлено, что детектирование аналитического сигнала оптимально проводить через 3–5 мин после нанесения исследуемого образца на тест-полоску. Остальные исследуемые тест-системы показали аналогичное время отклика.
С помощью полученных тест-систем на основе нановолокон определяли концентрации никеля по интенсивности окрашенной зоны после контакта их с исследуемым раствором. Установили, что интенсивность окраски и площадь пятна при уменьшении концентрации никеля уменьшается. Примеры тест-систем представлены на рис. 5.
При выбранных оптимальных значениях рН построили градуировочные зависимости интенсивности различных каналов цветности от концентрации никеля в растворе. В табл. 1 представлены параметры градуировочных зависимостей для определения никеля(II). Наибольшую чувствительность и хорошее значение коэффициента аппроксимации показала система РК (0.05 М) + + полиакрилонитрил, а в качестве регистрируемого сигнала – канал R. Уменьшение концентрации реагента в волокнах позволило получить наиболее воспроизводимую систему при определении низких концентраций ионов никеля (от 1 × × 10–6 до 0.01 М). Квадрат коэффициента аппроксимации составил 0.99 для канала R.
Таблица 1.
Параметры градуировочных зависимостей для определения никеля(II)
| Система | Канал цветности | I – c | R2 | Интервал линейности градуировочной зависимости, М |
|---|---|---|---|---|
| РК (0.25 М) + полиакрилонитрил | R | y = –12756x + 170 | 0.91 | 1 × 10–5–0.01 |
| G | y = –8794x + 132 | 0.93 | 1 × 10–5–0.01 | |
| B | y = –2267x + 65 | 0.99 | 1 × 10–5–0.01 | |
| РК (0.125 М) + полиакрилонитрил | R | y = –3996x + 201 | 0.89 | 5 × 10–5–0.01 |
| G | y = –2645x + 181 | 0.88 | 5 × 10–5–0.01 | |
| B | y = –912x + 135 | 0.79 | 5 × 10–5–0.01 | |
| РК (0.05 М) + полиакрилонитрил | R | y = –4620x + 192 | 0.99 | 1 × 10–6–0.01 |
| G | y = –3825x + 186 | 0.98 | 1 × 10–6–0.01 | |
| B | y = –1427x + 163 | 0.97 | 1 × 10–6–0.01 | |
| РК (0.25 М) + фторопласт | R | y = –5784x + 146 | 0.74 | 1 × 10–6–0.01 |
| G | y = –4142x + 125 | 0.64 | 1 × 10–6–0.01 | |
| B | y = 818x + 54 | 0.12 | 1 × 10–6–0.01 | |
| ПАН (2.5 × 10–2 М) + фторопласт | R | y = 309x + 182 | 0.03 | 1 × 10–6–0.01 |
| G | y = –555x + 149 | 0.19 | 1 × 10–6–0.01 | |
| B | y = 392x + 102 | 0.28 | 1 × 10–6–0.01 | |
| α-ФДО (0.125 М) + полиакрилонитрил (ω = 12%) | R | y = –1116x + 208 | 0.91 | 1 × 10–4–0.01 |
| G | y = –3007x + 195 | 0.86 | 1 × 10–4–0.01 | |
| B | y = –3217x + 188 | 0.87 | 1 × 10–4–0.01 | |
| ДМГ (1 М) + полиакрилонитрил (ω. = 12%) | R | y = –725x + 194 | 0.95 | 1 × 10–4–0.01 |
| G | y = –2858x + 187 | 0.99 | 1 × 10–4–0.01 | |
| B | y = –1803x + 190 | 0.96 | 1 × 10–4–0.01 | |
| ДМГ (0.5 М) + полиакрилонитрил (ω = 12%) | R | y = –496x + 191 | 0.97 | 5 × 10–4–0.01 |
| G | y = 1349x + 168 | 0.73 | 5 × 10–4–0.01 | |
| B | y = 713x + 176 | 0.67 | 5 × 10–4–0.01 | |
| ДМГ (0.2 М) + полиакрилонитрил (ω = 12%) | R | y = –466x + 184 | 0.61 | 5 × 10–4–0.1 |
| G | y = 1132x + 165 | 0.88 | 5 × 10–4–0.1 | |
| B | y = 606x + 174 | 0.85 | 5 × 10–4–0.1 |
Сравнение отклика реагента, иммобилизованного в волокне и на фильтровальной бумаге, показало значительное различие в чувствительности определения. Так, бумага, обработанная РК, не дает отклик на ионы никеля при концентрации 5 × 10–5 М, в то время как волокнистый материал позволяет определять Ni2+ на уровне 1 × 10–6 М, что говорит об увеличении чувствительности нановолокон по сравнению с фильтровальной бумагой более чем в 50 раз.
В процессе анализа помимо целевых могут протекать побочные реакции с участием реагента и посторонних ионов, присутствующих в анализируемой смеси. Это может вызвать целый ряд нежелательных явлений: понижение чувствительности реакций, изменение окраски и др. Основными мешающими ионами при определения ионов никеля являются ионы меди, железа и кобальта. Для оценки селективности полученных тест-систем проанализировали растворов солей различных металлов − Cr(III), Co(II), Cu(II), Ba(II), Al(III), Pb(II), Mn(II) и Cd(II) − при варьировании их концентрации. Наблюдали, что при концентрациях ионов металлов 0.01 М тест-система с РК помимо никеля проявляла отклик на кобальт и медь, причем пятно с кобальтом окрашено в желтый цвет, с никелем и медью – в синий. При уменьшении концентрации всех металлов в анализируемом растворе в 100 раз наблюдается аналитический отклик только на никель. Тест-система на основе ДМГ не давала отклик на все исследуемые металлы, кроме Co(II). Мешающие факторы для предложенных тест-систем, зафиксированные при постоянной концентрации ионов никеля 1 × 10–5 М и переменных концентрациях ионов других металлов, представлены в табл. 2.
Таблица 2.
Мешающее влияние некоторых ионов металлов на определение Ni(II) тест-системами с рубеановодородной кислотой и диметилглиоксимом
| Мешающий ион | Fмеш |
|---|---|
| РК (0.05 М) + полиакрилонитрил (ω = 12%) | |
| Сu2+ | 10 |
| Co2+ | 100 |
| Cr3+ | >1000 |
| Ba2+ | >1000 |
| Al3+ | >1000 |
| Pb2+ | >1000 |
| Mn2+ | >1000 |
| Cd2+ | >1000 |
| ДМГ (1 М) + полиакрилонитрил (ω = 12%) | |
| Co2+ | 5 |
Тест-системы на основе полиакрилонитрила с РК (0.05 М), показавшие наилучшие результаты при определении низких концентраций ионов никеля, использовали для их определения в природной и водопроводной водах. Правильность определения подтверждали методом введено−найдено. Примеры результатов тест-определения представлены в табл. 3.
Таблица 3.
Проверка правильности определения ионов Ni(II) тест-системой полиакрилонитрил + рубеановодородная кислота (0.05 М) методом введено−найдено (n = 3, P = 0.95)
| Вода | Введено, моль/л | Найдено, моль/л | sr, % |
|---|---|---|---|
| Водопроводная | 5.0 × 10–5 | (5.2 ± 1.4) × 10–5 | 11 |
| 1.0 × 10–4 | (1.2 ± 0.3) × 10–4 | 10 | |
| 5.0 × 10–4 | (4.8 ± 1.1) × 10–4 | 9.2 | |
| Природная | 5.0 × 10–5 | (5.3 ± 1.3) × 10–5 | 9.9 |
| 1.0 × 10–4 | (1.1 ± 0.2) × 10–4 | 7.3 | |
| 5.0 × 10–4 | (5.0 ± 1.2) × 10–4 | 9.7 |
Для определения ионов никеля в сточной воде гальванического производства до и после ее очистки, где содержание никеля гораздо выше по сравнению с водопроводной или природной водами, а также находится большое количество мешающих элементов, целесообразно использовать тест-систему полиакрилонитрил + α-ФДО (0.125 М). Тест-определение проводили, используя визуальную шкалу, а также методом цветометрии (с использованием градуировочной зависимости, диапазон концентраций которой расширен за счет нелинейного участка). Результаты сравнивали с результатами, полученными методом спектрофотометрии (табл. 4).
Таблица 4.
Результаты (моль/л) определения ионов Ni2+ в сточной воде гальванического производства до и после очистки с использованием системы полиакрилонитрил + α-фурилдиоксим (0.125 М) (n = 3, P = 0.95)
| Вода | Спектрофотометрия | Тест-метод, визуальная оценка по шкале | Тест-метод, цветометрия |
|---|---|---|---|
| До очистки | (2.9 ± 0.3) × 10–5 | 3 × 10–5 | (3.1 ± 0.5) × 10–5 |
| После очистки | (2.5 ± 0.2) × 10–6 | Не обнаружен | Не обнаружен |
* * *
Таким образом, разработаны тест-системы на основе нановолокон, полученных методом электроформования, для определения ионов никеля в природных и сточных водах. Достоинством данных тест-систем являются простота изготовления тестов, отсутствие пробоподготовки и возможность проведения анализа в полевых условиях.
Работа выполнена при поддержке РНФ (проект № 21-13-00267).
Список литературы
Smirnova S.V., Ilin D.V., Pletnev I.V. Extraction and ICP-OES determination of heavy metals using tetrabutylammonium bromide aqueous biphasic system and oleophilic collector // Talanta. 2021. V. 221. Article 121485.
Ferreira S.L.C., Bezerra M.A., Santos A.S., Dos Santos W.N.L. et al. Atomic absorption spectrometry – A multi element technique // Trends Anal. Chem. 2018. V. 100. P. 1.
Zhou F., Li Ch., Zhu H., Li. Yo. A novel method for simultaneous determination of zinc, nickel, cobalt and copper based on UV–Vis spectrometry // Optik. 2019. V. 182. P. 58.
Золотов Ю.А., Иванов В.М., Амелин В.Г. Химические тест-методы анализа. М.: Едиториал УРС, 2002. 304 с.
Запорожец О.А., Петрунек Н.И., Калиниченко Е.В., Сухан В.В. Визуальный тест-метод для определения Ni(II) на основе иммобилизованного на кремнеземе 4-(2-пиридилазо)-2-нафтолата цинка // Химия и технология воды. 1999. Т. 21. № 3. С. 281.
Иванов В.М., Ершова В.И. Спектроскопия диффузного отражения иммобилизованных на силикагеле комплексом никеля с диметилглиоксимом и бензилдиоксимом // Вестн. МГУ. Сер. 2. Химия. 1999. Т. 40. № 1. С. 22.
Бобкова Л.А., Односторонцева Т.В., Козик В.В. Сорбционно-цветометрическое и тест-определение ионов марганца(II), кобальта(II), никеля(II) и меди(II) в природных водах // Ползуновский Вестник. 2009. № 3. С. 209.
Tiwari A., Terada D., Yoshikawa C., Kobayashi H. An enzyme-free highly glucose-specific assay using self-assembled aminobenzene boronic acid upon polyelectrolytes electrospun nanofibers-mat // Talanta. 2010. V. 82. № 5. P. 1725.
Cleeton C., Keirouz A., Chen Xi., Radacsi N. Electrospun nanofibers for drug delivery and biosensing // ACS Biomater. Sci. Eng. 2019. V. 5. № 9. P. 4183.
Sapountzi E., Braiek M., Vocanson F., Chateaux J.-F., Jaffrezic-Renault N., Lagarde F. Gold nanoparticles assembly on electrospun poly(vinyl alcohol)/poly(ethyleneimine)/glucose oxidase nanofibers for ultrasensitive electrochemical glucose biosensing // Sens. Actuators B. 2017. V. 238. P. 392.
Tonsomboon K., Noppakuadrittidej P., Sutikulsombat S., Petdum A., Panchan W., Wanichacheva N., Sooksimuang T., Karoonuthaisiri N. Turn-On fluorescence resonance energy transfer (FRET)-based electrospun fibrous membranes: Rapid and ultrasensitive test strips for on-site detection of Mercury (II) ion // Sens. Actuators B. 2021. V. 344. Article 130212.
Aydogdu S., Ertekin K., Suslu A., Ozdemir M., Celik E., Cocen U. Optical CO2 sensing with ionic liquid doped electrospun nanofibers // J. Fluoresc. 2011. V. 21. № 1. P. 607.
Najafi M., Frey M.W. Electrospun nanofibers for chemical separation // Nanomaterials (Basel). 2020. V. 10. № 5. P. 982.
Schoolaert E., Hoogenboom R., De Clerck K. Colorimetric nanofibers as optical sensors // Adv. Funct. Mater. 2017. V. 12. № 38. Article 1702646.
Mills A., Lepre A., Theobald B.R.C., Slade E. and Murrer B.A. Use of luminescent gold compounds in the design of thin-film oxygen sensors // Anal. Chem. 1997. V. 69. P. 2842.
Zhu Z., Wu P., Liu G., He X., Qi B., Zeng G., Wang W., Sun Y., Cui F. Ultrahigh adsorption capacity of anionic dyes with sharp selectivity through the cationic charged hybrid nanofibrous membranes // Chem. Eng. J. 2017. V. 313. P. 957.
Пешкова В.М., Савостина В.М. Аналитическая химия никеля. М.: Наука, 1966. 204 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии




