Химия высоких энергий, 2019, T. 53, № 5, стр. 396-399
Удаление сероводорода из метана в барьерном разряде с добавками жидкого углеводорода
А. Ю. Рябов a, *, С. В. Кудряшов a, А. Н. Очередько a
a Федеральное государственное бюджетное учреждение науки Институт химии нефти
Сибирского отделения РАН
634055 Томск-55, Россия
* E-mail: andrey@ipc.tsc.ru
Поступила в редакцию 08.04.2019
После доработки 29.04.2019
Принята к публикации 08.05.2019
Аннотация
Исследован процесс удаления сероводорода из метана с добавками н-алканов С6–С8 в барьерном разряде. Показано, что недостаток жидкого углеводорода в исходной смеси приводит к образованию высокомолекулярных полисульфидных соединений, избыток – тиолов и алкилсульфидов.
ВВЕДЕНИЕ
В настоящее время продолжается устойчивый рост мирового потребления углеводородных ресурсов [1]. Сероводород содержится в природном и попутном нефтяном газах, биогазе, отходящих газах нефтехимических производств, и для дальнейшего их использования, как правило, требуется предварительная очистка. В современной промышленности для решения этой задачи преимущественно используются абсорбционные методы и процесс Клауса [2–4], имеющие известные ограничения и недостатки, что объясняет значительно возросший в последнее десятилетие интерес исследователей к плазмохимическим методам конверсии сероводорода [5–11].
В работе [12] авторами показана принципиальная возможность эффективного удаления сероводорода из метана с образованием высокомолекулярных сераорганических соединений под действием барьерного разряда (БР). Анализ возможного механизма процесса показал, что образование полисульфидных органических соединений происходит на поверхности электродов реактора, а газофазные реакции преимущественно завершаются на стадии образования алкилсульфидов и элементной серы S2. Ингибирование химических процессов на поверхности электродов реактора позволит управлять направлением реакции и составом конечных продуктов. Ранее авторами было показано, например, в работах [13, 14], что добавка жидких углеводородов в поток углеводородных газов предотвращает протекание химических реакций на поверхности электродов реактора в процессе их превращения в БР.
В настоящей работе представлены результаты исследования процесса удаления сероводорода из газожидкостной смеси метана и н-алканов С6–С8 в БР.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Эксперименты проводили на лабораторной установке, общий вид которой приведен в работе [12]. В установке использовался стеклянный реактор коаксиального типа с двумя диэлектрическими барьерами с зазором между ними 1 мм, объем разрядной зоны равнялся 8.2 см3. Во всех экспериментах объемная скорость подачи смеси CH4–H2S и жидкого углеводорода составила 60 и 0.4 см3/мин соответственно. Время контакта газовой смеси с разрядной зоной 12.5 с, температура стенок реактора 20°С, атмосферное давление.
Максимальная амплитуда высоковольтных импульсов напряжения не превышала 12 кВ при частоте повторения 2 кГц и длительности 470 мкс. Активная мощность разряда (~8 Вт) рассчитана из вольт-кулоновской характеристики БР.
Анализ газообразных продуктов реакции выполнен с использованием газо-жидкостного хроматографа HP 6890, жидких продуктов с применением хромато-масс-спектрометра Thermo Scientific DFS.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В табл. 1 приведены составы газообразных продуктов и конверсия сероводорода для смесей CH4–H2S–С8H18 и CH4–H2S [12] в схожих условиях.
Таблица 1.
Состав газообразных продуктов реакции и конверсия сероводорода в зависимости от его начальной концентрации в смесях СН4–Н2S и СН4–Н2S–C8H18
| Продукт/[Н2S], об. % | СН4–Н2S [12] | СН4–Н2S–C8H18 | ||||
|---|---|---|---|---|---|---|
| 0.5 | 3 | 6 | 3 | 6 | 12 | |
| H2 | 59.3 | 73.6 | 76.0 | 31.8 | 37.9 | 40.5 |
| C2H4 | 5.1 | 4.7 | 4.1 | 9.2 | 10.2 | 10.2 |
| C2H6 | 31.6 | 19.3 | 17.2 | 34.5 | 23.9 | 20.9 |
| С3Н8 | 4.0 | 2.4 | 2.7 | 11.6 | 11.4 | 10.3 |
| С4+ | – | – | – | 12.9 | 16.6 | 18.1 |
| Конверсия, об. % | 100 | 96.6 | 95.0 | 98.5 | 94.8 | 92.3 |
Конверсия сероводорода при обработке смесей CH4–H2S в присутствии октана выше, чем без него. В газообразных продуктах значительно снижается содержание водорода, образуются алканы С4+, не обнаруженные в продуктах обработки смесей CH4–H2S. Наблюдаемые эффекты, вероятно, связаны с протеканием реакций с участием интермедиатов, образовавшихся в результате деструкции молекул октана под действием БР. В целом при увеличении концентрации сероводорода в исходной смеси изменение содержания продуктов реакции в обоих случаях имеет сходный характер, что позволяет говорить об общих стадиях механизма протекания реакций в газовой фазе.
В работе [12] нами показано, что превращение смеси СН4–Н2S под действием БР приводит к образованию различных полисульфидных органических соединений на поверхности электродов реактора. Добавка октана в исходную смесь ингибирует протекание реакций на поверхности электродов, что влияет на состав жидких продуктов (табл. 2). Продукты реакции представлены в основном насыщенными углеводородами С6–C18 преимущественно изомерного строения и сераорганическими соединениями.
Таблица 2.
Групповой состав жидких продуктов превращения смеси СН4–Н2S–C8H18 и индивидуальный состав сераорганических соединений в зависимости начальной концентрации сероводорода в смеси
| [H2S], об. % | 3 | 6 | 12 |
| Углеводороды, мас. % | 63.2 | 51.1 | 36.1 |
| Сераорганические соединения, мас. % | 36.8 | 48.9 | 63.9 |
| Тиолы | 8.61 | 17.54 | 27.31 |
| Октилтиол | 8.61 | 17.54 | 27.31 |
| Сульфиды | 21.81 | 24.92 | 26.84 |
| Дипропилсульфид | 0.11 | 0.09 | 2.57 |
| Пропилбутилсульфид | 0.71 | 1.42 | 0.89 |
| Метилоктилсульфид | 12.44 | 14.86 | 16.56 |
| Дипентилсульфид | 4.00 | 4.21 | 3.31 |
| Пропилоктилсульфид | 1.90 | 1.53 | 0.89 |
| Бутилоктилсульфид | 1.16 | 1.33 | 1.33 |
| Диоктилсульфид | 1.48 | 1.48 | 1.30 |
| Дисульфиды | 6.38 | 5.81 | 8.42 |
| Метилэтилдисульфид | 0.00 | 0.00 | 0.20 |
| Метилпропилдисульфид | 0.45 | 0.46 | 1.20 |
| Этилпропилдисульфид | 0.00 | 0.00 | 1.19 |
| Этилбутилдисульфид | 0.28 | 0.00 | 0.38 |
| Метилгексилдисульфид | 0.11 | 0.18 | 0.34 |
| Бутилизопентилдисульфид | 3.07 | 3.79 | 4.19 |
| Дипентилдисульфид | 1.84 | 1.19 | 0.89 |
| Диоктилдисульфид | 0.63 | 0.19 | 0.04 |
| Соединения с содержанием атомов S > 2 | 0.00 | 0.63 | 1.33 |
Увеличение начальной концентрации сероводорода с 3 до 12 об. % приводит к росту содержания сераорганических соединений в составе продуктов реакции с ~37 до 64 мас. %.
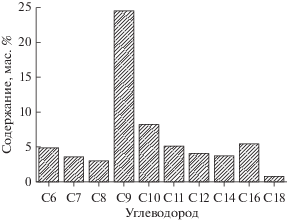
В составе жидких углеводородов значительная доля приходится на нонаны ~25 мас. %. Распределение содержания углеводородов в продуктах реакции в зависимости от количества атомов углерода в молекуле приведено на рис. 1, причем вид распределения слабо зависит от начальной концентрации сероводорода в исходной смеси.
Рис. 1.
Распределение содержания углеводородов в продуктах реакции в зависимости от количества атомов углерода в молекуле. Исходная смесь СН4–Н2S–C8H18 , [H2S] = 3 об. %.
Ранее в работе [14], посвященной изучению превращения газообразных алканов в присутствии воды в БР, выдвинуто предположение о том, что образование углеводородов С3+ преимущественно связано с реакцией встраивания CH2 радикала в С–С-связь молекулы углеводорода. В данных условиях нонаны, вероятно, образуются по похожему механизму:
(1)
${\text{С }}{{{\text{H}}}_{{\text{4}}}} + {\text{e}} \to {\text{С }}{{{\text{H}}}_{2}} + {{{\text{H}}}_{2}} + {\text{e}},\quad$(2)
${{{\text{С }}}_{{\text{8}}}}{{{\text{H}}}_{{{\text{18}}}}} + {\text{С }}{{{\text{Н }}}_{2}} \to {{{\text{С }}}_{{\text{9}}}}{{{\text{H}}}_{{20}}},$В составе сераорганических соединений идентифицированы октилтиол и различные сульфиды – преимущественно метилоктилсульфид. Содержание в продуктах дисульфидов и соединений с количеством атомов S в молекуле >2 не превышает 8.5 и 1.5 мас. % соответственно.
Содержание октилтиола в продуктах реакции практически прямо пропорционально начальной концентрации сероводорода в смеси и достигает 27.3 мас. % при [H2S] = 12 об. %. В этом случае, октилтиол и метилоктилсульфид составляют ~85% от образовавшихся сераорганических соединений. С учетом результатов, полученных в работе [12], упрощенный механизм образования этих соединений можно представить в виде следующего набора реакций:
(4)
${\text{RH}} + {\text{e}} \to {\text{R}} + {\text{H}}\,\,{\text{и л и }}\,\,{\text{R'}} + {\text{R}}'' + {\text{e}},$(7)
${\text{R}} + {{\text{S}} \mathord{\left/ {\vphantom {{\text{S}} {{{{\text{S}}}_{2}}}}} \right. \kern-0em} {{{{\text{S}}}_{2}}}} \to {{{\text{RS}}} \mathord{\left/ {\vphantom {{{\text{RS}}} {{\text{RSS}}}}} \right. \kern-0em} {{\text{RSS}}}} + {\text{R}} \to {{{\text{RSR}}} \mathord{\left/ {\vphantom {{{\text{RSR}}} {{\text{RSSR}}}}} \right. \kern-0em} {{\text{RSSR}}}},$Необходимо отметить, что метилмеркаптан не обнаружен среди продуктов реакции, хотя при удалении сероводорода из метана [12] он образуется в незначительных количествах ~0.5 об. %. По-видимому, добавка октана в исходную смесь подавляет образование метилмеркаптана, как и в случае с молекулярным водородом (табл. 1).
Представляло интерес исследовать влияние добавок жидких алканов с меньшей, чем у октана, молекулярной массой на конверсию сероводорода и состав продуктов обработки смесей CH4–H2S-алкан. Результаты экспериментов с добавками гексана и гептана приведены в табл. 3.
Таблица 3.
Конверсия сероводорода и групповой состав продуктов реакции превращении смеси СН4–Н2S в зависимости от добавки жидкого алкана, [Н2S] = 3 об. %
| Содержание, мас. % | Гексан | Гептан | Октан |
|---|---|---|---|
| Углеводороды | 58.2 | 61.8 | 63.2 |
| Сераорганические соединения | 41.8 | 38.2 | 36.8 |
| Конверсия Н2S, об.% | 92.1 | 95.8 | 98.5 |
Групповой состав продуктов реакции слабо зависит от молекулярной массы жидкого углеводорода. В ряду гексан–октан наблюдается незначительное снижение содержания сераорганических соединений в продуктах реакции. Качественный состав продуктов реакции также близок. Например, в случае добавки гексана в смесь метана и сероводорода, в составе образующихся жидких углеводородов значительная доля приходится на гептаны, а среди сераорганических соединений преобладают гексилтиол и метилгексилсульфид. Более существенное влияние добавка жидкого углеводорода оказывает на конверсию сероводорода, снижая ее до ~92 мас. % в случае гексана.
По-видимому, это связано со снижением скорости электронно-молекулярных реакций разложения сероводорода из-за понижения средней энергии электронов БР, вызванной ростом концентрации паров жидкого углеводорода в газовой смеси с уменьшением его молекулярной массы. Проведенные расчеты косвенно подтверждают это предположение: средняя энергия электронов находится в диапазоне 3.5–4 эВ для гексана и октана соответственно. Расчеты выполнены по аналогии с работой [12], интегральные сечения рассеяния электронов молекулами н-гексана и н-октана взяты из [15].
ЗАКЛЮЧЕНИЕ
Разработан одностадийный способ очистки газожидкостных смесей алканов С1–С8 от сероводорода с использованием барьерного разряда. Способ не требует применения катализаторов и химических реагентов, процесс протекает при атмосферном давлении и комнатной температуре, перспективен для подготовки природного и попутного нефтяных газов для дальнейшей переработки и применения в альтернативной энергетике.
Найден способ управления плазмохимическим процессом с образованием ценных полупродуктов нефтехимического синтеза. Недостаток жидкого углеводорода в исходной смеси приводит к образованию высокомолекулярных полисульфидных соединений, избыток – преимущественно к тиолам и алкилсульфидам.
Работа выполнена по программе фундаментальных научных исследований государственных академий наук на 2013–2020 годы. Проект V.44.3.1 “Создание научных основ переработки каустобиолитов и регулирования физико-химических свойств углеводородсодержащих коллоидных систем в условиях экстремального воздействия физических факторов (низкотемпературная плазма, механохимия и акустические методы)” № ГР AAAA-A17-117030310198-4.
Список литературы
BP Statistical Review of World Energy. June 2018. URL: https://www.bp.com/en/global/corporate/energy-economics/statistical-review-of-world-energy/ downloads.html (дата обращения 02.04.2019)
Zaman J., Chakma A. // Fuel Process. Technol. 1995. V. 41. № 2. P. 159.
Pandey R.A., Malhotra S. // Crit. Rev. Environ. Sci. Technol. 1999. V. 29. № 3. P. 229.
Yildirim Ö., Kiss A.A., Hüser N., Leßmann K., Kenig E.Y. // Chem. Eng. J. 2012. V. 213. P. 371.
Fridman A. Plasma Chemistry. New York: Cambridge University Press. 2008. 978 p.
Gutsol K., Nunnally T., Rabinovich A., Fridman A., Stari-kovskiy A., Gutsol A., Kemoun A. // Int. J. Hydrogen Energy. 2012. V. 37. № 2. P. 1335.
Huang L., Xia L., Dong W., Hou H. // Chem. Eng. J. 2013. V. 228. P. 1066.
Reddy E.L., Biju V.M., Subrahmanyam C. // Int. J. Hydrogen Energy. 2012. V.37. № 3. P. 2204.
Sekine Y., Yamadera J., Matsukata M., Kikuchi E. // Chem. Eng. Sci. 2010. V. 65. № 1. P. 487.
Gutsol K., Robinson R., Rabinovich A., Gutsol A. // Int. J. Hydrogen Energy. 2017. V. 42. № 1. P. 68.
Unseld M., Szepansk C., Lindermeir A., Maus-Friedrichs W., Dahle S. // Chem. Eng. Technol. 2017. V. 40. № 2. P. 1.
Кудряшов С.В., Очередько А.Н., Рябов А.Ю., Кривцова К.Б., Щеголева Г.С. // Химия высоких энергий. 2014. Т. 48. № 6. С. 491.
Kudryashov S.V., Ochered’ko A.N., Ryabov A.Yu., Shchyogoleva G.S. // Plasma Chemistry and Plasma Processing. 2011. V. 31. P. 649.
Кудряшов С.В., Рябов А.Ю., Очередько А.Н. // Химия высоких энергий. 2018. Т. 52. № 2. С. 150.
Sueoka O., Makochekanwa C., Tanino H., Kimura M. // Physical Review A. 2005. V.72. № 4. P. 042705.
Дополнительные материалы отсутствуют.
Инструменты
Химия высоких энергий


