Журнал неорганической химии, 2022, T. 67, № 7, стр. 896-907
Модифицирование кадмием обогащенного литием катодного материала состава Li1.2Ni0.133Mn0.534Co0.133O2
А. Е. Медведева a, *, Е. В. Махонина a, **, Л. С. Печень a, Ю. А. Политов a, А. М. Румянцев b, Ю. М. Коштял b, А. А. Курлыкин a, И. Л. Еременко a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
b Физико-технический институт им. А.Ф. Иоффе РАН
194021 Санкт-Петербург, ул. Политехническая, 26, Россия
* E-mail: anna.ev.medvedeva@gmail.com
** E-mail: elenamakhonina@mail.ru
Поступила в редакцию 26.11.2021
После доработки 03.02.2022
Принята к публикации 07.02.2022
- EDN: WNALPG
- DOI: 10.31857/S0044457X22070157
Аннотация
Обогащенный литием катодный материал для литий-ионного аккумулятора состава Li1.2Ni0.133Mn0.534Co0.133O2 синтезирован тремя различными способами. На основе этого состава получены также катодные материалы, в которых кадмий добавлен вместо части кобальта. Исследовано влияние способа получения и введения кадмия в материал на его электрохимические свойства. Оксиды получены методом соосаждения, при котором кадмий добавляли как на стадии получения прекурсора, так и на стадии твердофазной реакции прекурсора с источником лития, а также сольвотермальным синтезом. Методами масс-спектрометрии с индуктивно связанной плазмой, рентгенофазового анализа и рентгеноспектрального микроанализа доказано присутствие кадмия в полученных материалах. Бóльшая часть кадмия в модифицированных материалах существует в виде оксидного покрытия на поверхности частиц активного материала. Электрохимическое тестирование полученных материалов в полуячейках с литиевым анодом показало, что образец с наиболее равномерным покрытием, полученный при внесении кадмия на стадии синтеза прекурсора, имеет лучшие электрохимические характеристики по сравнению с исходным (обратимость на 100-ом цикле 95% по сравнению с 84%).
ВВЕДЕНИЕ
В настоящее время наряду с использованием в портативной технике литий-ионные аккумуляторы (ЛИА) применяются в электромобилях, резервных системах хранения энергии и других устройствах, требующих большой энергоемкости. Это обеспечивается постоянными исследованиями в области разработки материалов ЛИА. Одними из самых перспективных катодных материалов на данный момент являются обогащенные литием материалы (LR-материалы), чья удельная энергоемкость приближается к 270 мАч/г (900 Вт/кг) [1, 2]. В LR-материалах сосуществуют две фазы: моноклинная (пр. гр. C2/m) и тригональная ($R\bar {3}m$); и вопрос о том, представляют ли они между собой твердый раствор или композитную структуру, остается до конца не выясненным [3–5]. К сожалению, для подобных материалов характерно резкое падение емкости и среднего разрядного напряжения в процессе циклирования. Работа ЛИА основана на способности иона лития обратимо внедряться в электродные материалы, одновременно с этим происходят процессы окисления-восстановления переходных металлов (имеются в виду никель, кобальт, марганец, в дальнейшем обозначаются как ПМ), а в обогащенных литием LR-материалах также и кислорода [3, 6]; при этом происходит постоянное изменение объема кристаллической решетки активного материала катода [7]. В результате длительного циклирования катодный материал неизбежно начинает деградировать. К процессам, ведущим к его деградации, относят появление микротрещин в частицах, разрушениe агломератов, необратимые превращения, которые начинаются с поверхности частиц: паразитические реакции (окисление электролита Ni4+, растворение ПМ и др.), а также структурные и фазовые превращения. Для обогащенных литием катодных материалов большое значение имеет восстановление кислорода до молекулярного с его выделением из катодного материала [3, 6]. Процессы деградации стимулируют появление плотных поверхностных пленок нежелательных веществ на поверхности частиц электродов, что приводит к увеличению поляризационного сопротивления в процессе работы аккумулятора [3, 7, 8]. Для снижения неблагоприятного влияния вышеперечисленных процессов и улучшения электрохимических характеристик LR-материалов используют различные методы, такие как модифицирование поверхности [9], допирование [10–13] и введение различных добавок к электролиту [14]. Широко исследованы в качестве защитного покрытия оксиды (Al2O3 [15, 16], ZnO [17], ZrO2 [18, 19] и др.), фосфаты (AlPO4 [20], Co3(PO4)2 [21] и др.) и фториды (AlF3 [22], CaF2 [23, 24]) металлов, которые сдерживают деградацию катодного материала за счет подавления реакций между электролитом и активным веществом катода, уменьшая растворение ПМ в электролите и образование непроводящих пленок на поверхности электрода. Допирование в LR-материалах проводят по позициям лития и ПМ (катионное допирование) и в позиции кислорода (анионное допирование). Исследовано допирование в позиции ПМ катионами различной валентности, например, трехвалентными Fe [25], Al [23, 24] и Au [28], четырехвалентными Ti [29], Zr [30] и Ru [31, 32]. Подобное допирование улучшает электронную проводимость материала за счет увеличения межплоскостных расстояний и снижения ширины запрещенной зоны [6].
Ранее сообщалось, что модификация кадмием оказала положительный эффект на электрохимические характеристики некоторых катодных материалов (LiCoO2 [33], LiNi0.6Co0.2Mn0.2O2 [34], LiFePO4 [35] и Li2FeSiO4 [36], LiNi0.8Co0.15Al0.05O2 [37]). Авторы статьи [38] предприняли попытку совместного модифицирования обогащенных по литию материалов электрохимически неактивными элементами – кадмием и серой для создания жесткого каркаса в структуре катодного материала, что, по мнению авторов, снижает его деградацию.
Целью данного исследования было изучение влияния модифицирования кадмием LR-материала на его электрохимические свойства в зависимости от способа модифицирования. Для этого были синтезированы исходные и модифицированные LR-материалы состава Li1.2Ni0.133Mn0.534Co0.133 –xCdxO2, отличающиеся способом введения кадмия. Были исследованы их электрохимические свойства в качестве катода в полуячейках с литиевым анодом. Предполагалось, что введение кадмия с большим ионным радиусом в слой ПМ может способствовать лучшей диффузии ионов лития и улучшению электрохимических свойств катодного материала [34, 38]. Положительный эффект модифицирования проявился на материале, введение кадмия в который проводили на стадии синтеза прекурсора. При длительном циклировании при токе заряда 0.5 С обратимость модифицированного материала составила 91% по сравнению с 74% для его исходного материала.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных реагентов использовали: литий гидроксид моногидрат (99%, Sigma Aldrich), марганец(II) нитрат тетрагидрат (98%, Acros Organics), никель(II) нитрат гексагидрат (99%, Acros Organics), кобальт(II) нитрат гексагидрат (99%, Acros Organics), карбонат натрия (х. ч., Химмед), литий ацетат моногидрат (99%, Alfa Aesar), никель(II) ацетат тетрагидрат (99%+, Alfa Aesar), кобальт(II) ацетат тетрагидрат (98%, Alfa Aesar), марганец(II) ацетат тетрагидрат (Mn 22%, Alfa Aesar), кадмий нитрат тетрагидрат (ос. ч., Химмед), оксид кадмия (98.9%, Alfa Aesar), щавелевую кислоту (х. ч., Химмед), этиловый спирт абсолютный (A.C.S., Merck).
Методом соосаждения синтезировали исходные материалы LR1 и LR2 и соответствующие им материалы, модифицированные кадмием: LR1Cd и LR2Cd. Для синтеза обогащенного литием оксида LR3 и оксида, модифицированного кадмием (LR3Cd), применяли сольвотермальный метод.
В модифицированные материалы кадмий вводили в количестве 2 ат. % от общего содержания ПМ за счет уменьшения доли кобальта. Синтезы отличаются друг от друга способом внесения кадмия. Для получения LR1Cd нитрат кадмия добавляли на стадии получения прекурсора – карбоната ПМ. Введение кадмия для получения оксида LR2Cd проводили на стадии твердофазного синтеза путем добавления CdO также в количестве 2 ат. % от общего содержания ПМ за счет уменьшения кобальта. Для получения LR2 (оксида сравнения для LR2Cd) основную часть кобальта вносили на стадии синтеза карбонатного прекурсора, добавляя на стадии твердофазной реакции Со3О4 в количестве, равном содержанию добавляемого кадмия в оксиде LR2Cd. При сольвотермальном методе все элементы закладывали в реактор одновременно. При синтезе всех материалов закладывали содержание лития 1.53 (избыток 3 мас. % из-за потерь лития при отжиге) по отношению к общему содержанию других металлов (Ni, Co, Mn и Cd). Описание синтеза приведено в [39, 40] и Приложении. Соотношение элементов в прекурсорах приведено в табл. S1 .
МЕТОДЫ ИССЛЕДОВАНИЯ
Морфологию, микроструктуру, а также равномерность распределения элементов по составу полученных оксидов исследовали с помощью сканирующей электронной микроскопии (СЭМ) и рентгеноспектрального микроанализа (РСМА) на приборе NVision-40 (Carl Zeiss).
Измерение распределения частиц по размерам проводили с использованием лазерного анализатора Analysette 22 MicroTec Plus.
Для определения содержания металлов в полученных образцах использовали метод масс-спектрометрии с индуктивно связанной плазмой (ИСП-МС) на приборе Agilent 7500ce (Agilent Technologies Inc.).
Рентгенофазовый анализ (РФА) проводили при комнатной температуре на рентгеновском дифрактометре Bruker D8 Advance (CuKα-излучение, λ = 0.15418 нм, 40 кВт/40 мА) в режиме θ/2θ-сканирования в интервале углов 2θ 10°–80° с шагом 0.02°. Подробное описание приведено в Приложении.
Определение электрохимической активности полученных катодных материалов осуществляли в дисковых макетах габарита CR2032 с использованием зарядно-разрядных стендов Neware CT3008W-5V10mA. Электродный слой состоял из исследуемого катодного материала (92 мас. %), электропроводящей добавки (сажа Super C65 (Timcal) – 5 мас. %) и связующего (поливинилиденфторид Solef 5130 (Solvay) – 3 мас. %). В качестве отрицательного электрода использовали литиевую фольгу. Использованный электролит – TC-E918 (Tinci). Более подробное описание приведено в Приложении.
После сборки дисковых макетов проводили циклы формировки при токе 20 мА/г: два цикла заряда/разряда в диапазоне напряжений 2.5–4.3 В, за которыми следовала электрохимическая активация моноклинной фазы в диапазоне напряжений 2.5–4.5 В (2 цикла) и 2.5–4.6 В (2 цикла). Величина тока при гальваностатическом заряде/разряде составляла 80–100 мА/г. Работоспособность материалов оценивали также при высоких токах разряда в диапазоне 80–480 мА/г, ток заряда был постоянным – 80–100 мА/г.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Морфология и микроструктура полученных образцов сильно зависят от условий и метода синтеза. Образцы LR1 и LR1Cd очень сходны по морфологии. Первичные частицы (0.2–1.0 мкм) собраны в сферические агломераты со средним размером 13–15 мкм (рис. 1а, 2б). Для исходного материала гранулометрический анализ показывает несколько большее количество мелких частиц (рис. 2а, 2г). Материалы LR2 и LR2Cd, синтезированные методом соосаждения, но с добавлением части оксида кобальта (для LR2) и оксида кадмия (для LR2Cd) на стадии твердофазной реакции, схожи между собой по морфологии. Они содержат сферические агломераты (рис. 1в, 2г), но в отличие от предыдущей пары, в них гораздо больше мелких агломератов и отдельных первичных частиц (Приложение, рис. 1а, 2б). Размеры образовавшихся агломератов LR2 практически в два раза больше, чем LR2Cd, и составляют в среднем ~8 мкм (для LR2Cd ~4 мкм). Размеры первичных частиц для материалов LR2 и LR2Cd схожи (0.3–1.8 мкм), но для образца LR2 характерно наличие отдельных крупных частиц (2–4 мкм, рис. S1 ), а для образца LR2Cd – мелких частиц (0.3–1 мкм), лежащих россыпью. Это отразилось на дифференциальной кривой распределения частиц по размерам – появились уширения в соответствующих размерных областях (рис. 2б–2е). Морфология синтезированных частиц материалов LR3 и LR3Cd резко отличается от таковой для частиц, полученных методом соосаждения обоими способами (рис. 1д, 2е). Для них характерно образование вытянутых агломератов продолговатой формы, состоящих из первичных частиц размером 180–600 нм. Причем для исходного LR3 размеры агломератов продолговатой формы намного больше, чем для подобных агломератов в материалах LR3Cd (~10 мкм по сравнению с 1.5–5 мкм). В модифицированном материале LR3Cd присутствуют два типа агломератов: продолговатой формы (1.5–5 мкм) и большие бесформенные агломераты (9–12 мкм, рис. S1e, S1f, S2 ). Форма дифференциальной кривой распределения частиц для образца LR3 – это широкий одномодальный пик, а для образца LR3Cd характерно бимодальное распределение частиц (рис. 2в, 2е). Во всех синтезированных материалах никель, кобальт и марганец распределены равномерно, это следует из данных РСМА (рис. S3–S5 приведены для модифицированных образцов). Кадмий присутствует во всех модифицированных образцах (рис. 3). Лучшее распределение кадмия наблюдается для образца LR1Cd (рис. 3а, 3б), для образца LR2Cd характерны уже более крупные включения оксида кадмия на поверхности частиц (рис. 3в, 3г), а в случае образца LR3Cd оксид кадмия присутствует в материале в виде отдельных крупных включений (рис. 3д, 3е). Данные РСМА (рис. 4) для прекурсора R1Cd (безлитиевая форма материала LR1Cd), состоящего из смешанных карбонатов никеля, марганца, кобальта и кадмия, подтверждают равномерность распределения всех металлов в частицах прекурсора. Микрофотографии LR1Cd и R1Cd получены методом СЭМ в режиме отраженных электронов (режим, позволяющий непосредственно визуализировать области, характеризующиеся различными удельными атомными массами). И если на стадии прекурсора видно, что образец однофазный, и отдельно кадмий не визуализируется (рис. 5а–5г), то для материала LR1Cd отчетливо видна фаза оксида кадмия (рис. 5д–5з). Конечное соотношение элементов во всех полученных материалах, определенное методом ИСП-МС, представлено в табл. 1.
Рис. 1.
Микрофотографии СЭМ синтезированных LR-материалов, где а, в, д – микрофотографии исходных материалов LR1, LR2, LR3; б, г, е – микрофотографии модифицированных материалов LR1Cd, LR2Cd, LR3Cd.
Рис. 2.
Дифференциальные (а, б, в) и интегральные (г, д, е) кривые распределения агломератов по размеру для синтезированных образцов.
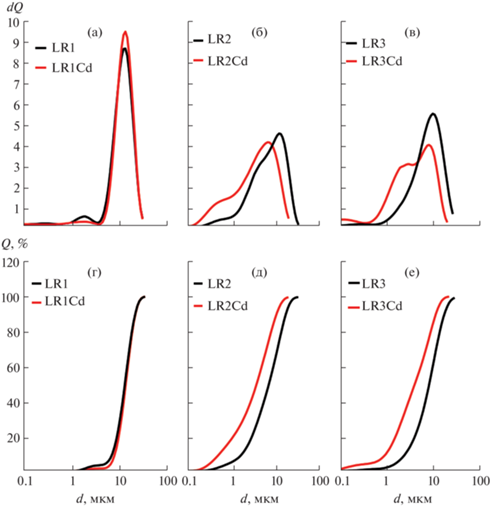
Рис. 3.
Микрофотографии СЭМ модифицированных кадмием материалов и соответствующие им карты распределения кадмия для LR1Cd (а, б), LR2Cd (в, г) и LR3Cd (д, е).

Рис. 4.
Микрофотография СЭМ образца R1Cd (а) и карты распределения элементов Cd (б), Ni (в), Co (г), O (д), Mn (е).

Рис. 5.
Микрофотографии СЭМ образцов R1Cd (а, в) и LR1Cd (д, ж) и соответствующие им микрофотографии, снятые в режиме отраженных электронов (б, г, е, з).

Таблица 1.
Соотношение элементов в полученных материалах
| Материал | Метод синтеза, способ внесения кадмия | Соотношение элементов в материалах: заложенное/по данным ИСП-МС |
||||
|---|---|---|---|---|---|---|
| Li | Ni | Mn | Co | Cd | ||
| LR1 | Соосаждение | 1.224/1.261 | 0.133/0.132 | 0.533/0.536 | 0.133/0.132 | – |
| LR1Cd | Соосаждение, стадия соосаждения прекурсора | 1.228/1.251 | 0.134/0.130 | 0.533/0.540 | 0.118/0.115 | 0.016/0.015 |
| LR2 | Соосаждение | 1.200/1.243 | 0.133/0.130 | 0.533/0.539 | 0.134/0.131 | |
| LR2Cd | Соосаждение, стадия твердофазной реакции прекурсора с источником лития | 1.224/1.287 | 0.133/0.134 | 0.534/0.534 | 0.118/0.114 | 0.015/0.018 |
| LR3 | Сольвотермальный метод | 1.240/1.209 | 0.134/0.130 | 0.533/0.538 | 0.134/0.132 | |
| LR3Cd | Сольвотермальный метод | 1.224/1.207 | 0.134/0.130 | 0.533/0.538 | 0.118/0.116 | 0.016/0.017 |
Рентгенограммы карбонатных прекурсоров исходного R1 и модифицированного R1Cd (рис. S6 ) содержат пики, отвечающие фазе карбоната марганца (PDF № 01-086-0172), и не содержат пиков примесных фаз. Рентгенограммы уточнены по методу Ритвельда. Параметры решетки модифицированного образца по сравнению с исходным незначительно увеличены: а = = 4.756(2)/4.75405(14), c = 15.5285(6)/15.5027(6), V = 304.20(2)/303.43(2). Это указывает на равномерное распределение кадмия в прекурсоре R1Cd. Рентгенограммы всех модифицированных образцов содержат дополнительную фазу – оксид кадмия (рис. 6б). Основные пики, наблюдаемые на рентгенограммах всех оксидов (рис. 6), хорошо описываются тригональной структурой (пр. гр. $R\bar {3}m$). Пики низкой интенсивности в области углов 20°–30° соответствуют моноклинной фазе Li2MnO3 (пр. гр. C2/m), характеризующейся катионным упорядочением в слоях переходного металла [22, 23]. Параметры решеток основной фазы $~R\bar {3}m,$ уточненные методом Ритвельда, во всех образцах близки друг к другу и приведены в табл. 2.
Рис. 6.
Рентгенограммы исходных LR1, LR2, LR3 (а) и модифицированных кадмием материалов LR1Cd, LR2Cd, LR3Cd (б).
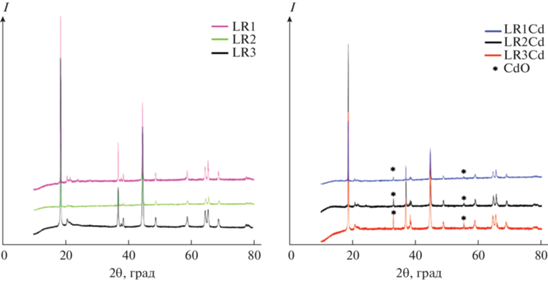
Таблица 2.
Параметры и объемы элементарной ячейки образцов
| Название образца | a, Å | c, Å | V, Å |
|---|---|---|---|
| LR1 | 2.8468(1) | 14.2180(5) | 99.788(5) |
| LR1Cd | 2.8479(1) | 14.2214(4) | 99.888(4) |
| LR2 | 2.8483(1) | 14.2221(4) | 99.923(4) |
| LR2Cd | 2.8469(1) | 14.2216(6) | 99.819(5) |
| LR3 | 2.8505(1) | 14.2184(7) | 100.049(6) |
| LR3Cd | 2.8509(1) | 14.2219(9) | 100.102(8) |
Ионный радиус Cd2+ составляет 0.95 Å, что значительно превышает ионные радиусы ПМ, входящих в состав материала (Mn4+ – 0.530 Å, Co3+ – 0.545 Å, Ni2+ – 0.69 Å), однако отмечается лишь незначительное изменение параметров решетки и объема ячейки фазы $R\bar {3}m~$ по сравнению с параметрами исходных образцов. По-видимому, это свидетельствует о том, что полного замещения ПМ кадмием не происходит, а наблюдаемые изменения могут быть связаны с различными условиями синтеза и способом введения кадмия в материал.
В работе [38] говорится об успешном допировании кадмием и серой обогащенных литием материалов, которое подтверждается увеличением параметров решетки, особенно параметра с – показателя межслоевого расстояния. Но в статье совершенно не рассмотрен тот факт, что при модифицировании кадмием и серой на рентгенограммах регистрируются пики, относящиеся к оксиду кадмия. К тому же метод синтеза модифицируемого материала аналогичен примененному нами при получении LR2Cd, в котором оксид кадмия не только располагается на поверхности частиц материала, но и образует отдельные крупные агломераты. Не исключено, что допирование кадмием может происходить при совместном допировании с серой. В нашем случае основная часть кадмия находится на поверхности полученных материалов в виде более или менее равномерного покрытия.
Все полученные материалы были электрохимически протестированы. Материалы сравнения LR1, LR2 и LR3 характеризуются совершенно различным поведением (рис. 7а). Лучшие показатели циклирования (более высокие показатели емкости, бóльшая обратимость) наблюдаются у материала, полученного традиционным методом соосаждения (LR1). Для материала LR2, также полученного методом соосаждения, но с введением части кобальта на твердофазной стадии, начальные значения емкости достигают значений материала LR1, но практически сразу падают. Стабилизация показателей емкости происходит только после 40-го цикла и составляет 85% от значения емкости материала LR1 на этом же цикле. Сближение кривых циклирования происходит к 100-му циклу, где значение емкости LR2 составляет уже 94% от значения емкости LR1. Материал LR3, синтезированный сольвотермальный методом, оказался материалом с самыми низкими электрохимическими показателями, для него характерно резкое падение значений емкости, остаток емкости к 100-му циклу для него составил только 42% от значения емкости LR1. Лучшим среди модифицированных материалов является LR1Cd, который в начале циклирования показывал чуть меньшее значение емкости по сравнению с LR1 (рис. 7б), но при этом лучше циклировался. Данный материал обладает лучшей стабильностью циклирования среди всех полученных материалов. К 130-му циклу остаточная разрядная емкость для LR1 составила 76%, для LR1Cd – 91%. Значения емкости для материала LR1Cd начинают превышать значения емкости для материала LR1 c 70-го цикла, и в дальнейшем разница между этими значениями увеличивается; значения емкости LR1 начинают сильно снижаться. Материал LR2Cd (внесение кадмия на стадии твердофазной реакции с литием) не показал изменений по сравнению с исходным материалом, показывая те же значения емкости, что и материал сравнения LR2 (рис. 7в). Начальные значения емкости для материала LR3Cd наименьшие среди всех материалов, но начиная с 60-го цикла значения емкости выравниваются со значениями емкости материала LR3 и далее в процессе циклирования немного их превышают.
Рис. 7.
Электрохимические испытания синтезированных образцов. Зависимость разрядной емкости от номера цикла при токе 80 мА/г (0.5С) в диапазоне напряжений 2.5–4.7 В для исходных LR1, LR2, LR3 (а), сравнение значений для исходных и модифицированных образцов (б, в); зависимость емкости от тока разряда для пар исходный–модифицированный материал: LR1, LR1Cd (г), LR2, LR2Cd (д), LR3, LR3Cd (е).
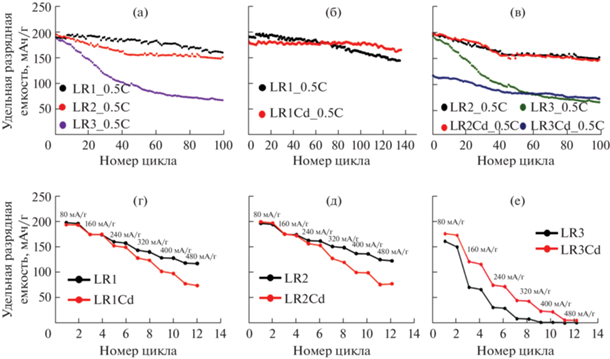
Скоростные характеристики (рис. 7г–7е) для исходных LR1 и LR2 схожи; образец LR3 гораздо быстрее теряет емкость с увеличением плотности тока разряда. Модификация кадмием в материалах LR1Cd и LR2Cd не улучшила скоростные характеристики материалов (рис. 7г, 7д); значения емкости, начиная со значения тока 240 мА/г, ниже, чем для исходных материалов, причем при увеличении тока заряда разница между значениями емкости исходного и модифицированного материала увеличивалась. Для материала LR3Cd скоростные характеристики улучшились по сравнению с характеристиками исходного материала LR3 (рис. 7е). Мы предполагаем, что эти явления связаны с морфологией образцов. Первичные частицы полученных образцов собраны в сферические агломераты для пар LR1–LR1Cd и LR2–LR2Cd и продолговатые для LR3 и LR3Cd. В образце LR3Cd имеются также бесформенные рыхлые агломераты. Форма агломератов и более мелкий размер первичных частиц образцов, полученных сольвотермальным методом, ведут к увеличению площади поверхности образцов. Этот фактор может положительно влиять на скоростные характеристики материала, но отрицательно на его циклируемость, так как такой материал подвергается более быстрому разрушению из-за протекания побочных реакций.
Во всех трех случаях модифицирования кадмий находится на поверхности частиц в виде оксида; лучшего его распределения по частицам удалось добиться в образце LR1Cd. Оксидное покрытие играет положительную роль в процессе длительного циклирования, сдерживая деградацию материала и тем самым улучшая его циклируемость, что характерно для сферических агломератов пар LR1–LR1Cd и LR2–LR2Cd. К сожалению, оно не способствовало улучшению кинетики процессов интеркаляции/деинтеркаляции лития в этих образцах.
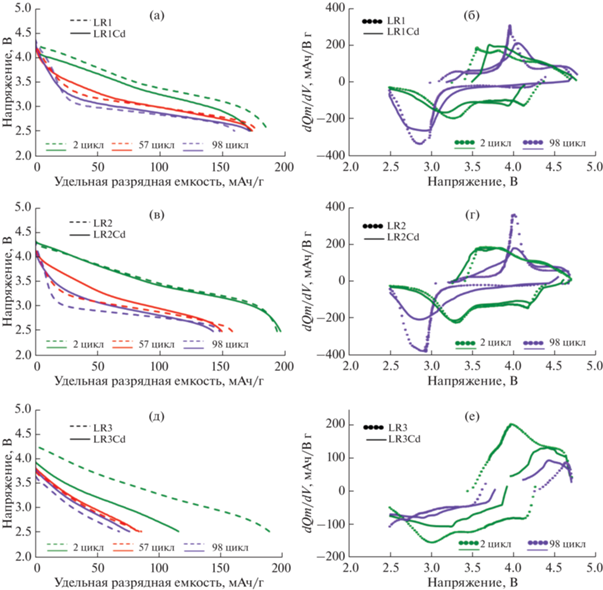
На рис. 8 представлены разрядные кривые и первые производные емкости по напряжению от напряжения (кривые dQ/dV) в разных циклах. На разрядных кривых видно, что меньшее падение напряжения в процессе циклирования наблюдается для модифицированных образцов (рис. 8а, 8в, 8д). Это, по всей видимости, свидетельствует о подавлении фазовых превращений (перехода гексагональной структуры в шпинель) в модифицированных материалах. Редокс-потенциал образующейся шпинели ниже, чем исходной структуры, чем и объясняется падение напряжения. Форма и смещение пиков на дифференциальных кривых емкости от напряжения (рис. 8б, 8г, 8е) подтверждают это предположение.
Рис. 8.
Разрядные кривые 2, 57 и 98 циклов для образцов LR1, LR1Cd (а), LR2, LR2Cd (в) и LR3, LR3Cd (д). Зависимости дифференциальной емкости по напряжению от напряжения (dQ/dV) во 2-ом и 98-ом циклах для LR1, LR1Cd (б), LR2, LR2Cd (г), LR3, LR3Cd (е). Удельный ток циклирования 80–100 мА/г.
Таким образом, в образце LR1Cd, в котором наблюдается наиболее равномерное покрытие оксидом кадмия поверхности оксида, наблюдаются и лучшие электрохимические свойства. Защитное покрытие уменьшает деградацию материала, приводя к улучшению циклирования по сравнению с исходным материалом.
ЗАКЛЮЧЕНИЕ
Изучено влияние метода получения и введения кадмия в обогащенные литием (LR) катодные материалы состава Li1.2Ni0.133Mn0.534Co0.133O2. Использованы метод соосаждения с введением кадмия на разных стадиях синтеза (осаждения прекурсора и твердофазной реакции) и сольвотермальный метод. Показано, что кадмий не входит в кристаллическую решетку оксидов, а образуется в виде CdO на поверхности материалов. Образец с наиболее равномерным покрытием, полученный при введении кадмия на стадии формирования прекурсора, показал улучшение его электрохимических характеристик по сравнению с образцом сравнения и высокую обратимость циклирования, которая составила 91% на 130-ом цикле.
Список литературы
Thackeray M.M., Kang S.-H., Johnson C.S. et al. // J. Mater. Chem. 2007. V. 17. № 30. P. 3112. https://doi.org/10.1039/b702425h
Freire M., Kosova N.V., Jordy C. et al. // Nat. Mater. 2016. V. 15. № 2. P. 173. https://doi.org/10.1038/nmat4479
He W., Guo W., Wu H. et al. // Adv. Mater. 2021. P. 2005937. https://doi.org/10.1002/adma.202005937
Long B.R., Croy J.R., Park J.S. et al. // J. Electrochem. Soc. 2014. V. 161. № 14. P. A2160. https://doi.org/10.1149/2.0681414jes
Jarvis K.A., Deng Z., Allard L.F. et al. // Chem. Mater. 2011. V. 23. № 16. P. 3614. https://doi.org/10.1021/cm200831c
Sharifi-Asl S., Lu J., Amine K. et al. // Adv. Energy Mater. 2019. V. 9. № 22. P. 1900551. https://doi.org/10.1002/aenm.201900551
Li T., Yuan X.-Z., Zhang L. et al. // Electrochem. Energy Rev. 2020. V. 3. № 1. P. 43. https://doi.org/10.1007/s41918-019-00053-3
Ji X., Xia Q., Xu Y. et al. // J. Power Sources. 2021. V. 487. P. 229362. https://doi.org/10.1016/j.jpowsour.2020.229362
Somo T.R., Mabokela T.E., Teffu D.M. et al. // Coatings. 2021. V. 11. № 7. P. 744. https://doi.org/10.3390/coatings11070744
Hebert A., McCalla E. // Mater. Adv. 2021. V. 2. № 11. P. 3474. https://doi.org/10.1039/D1MA00081K
Pechen L.S., Makhonina E.V., Medvedeva A.E. et al. // Russ. J. Inorg. Chem. 2021. V. 66. № 5. P. 777. https://doi.org/10.1134/S0036023621050144
Opra D.P., Gnedenkov S.V., Sinebryukhov S.A. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 5. P. 680. https://doi.org/10.1134/S0036023619050140
Nipan G.D., Smirnova M.N., Kornilov D.Y. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 4. P. 573. https://doi.org/10.1134/S0036023620040130
Li X., Zheng J., Engelhard M.H. et al. // ACS Appl. Mater. Interfaces. 2018. V. 10. № 3. P. 2469. https://doi.org/10.1021/acsami.7b15117
Kobayashi G., Irii Y., Matsumoto F. et al. // J. Power Sources. 2016. V. 303. P. 250. https://doi.org/10.1016/j.jpowsour.2015.11.014
Maiti S., Sclar H., Sharma R. et al. // Adv. Funct. Mater. 2021. V. 31. № 8. P. 2008083. https://doi.org/10.1002/adfm.202008083
Kong J.-Z., Zhai H.-F., Qian X. et al. // J. Alloys Compd. 2017. V. 694. P. 848. https://doi.org/10.1016/j.jallcom.2016.10.045
Wang Z., Liu E., Guo L. et al. // Surf. Coatings Technol. 2013. V. 235. P. 570. https://doi.org/10.1016/j.surfcoat.2013.08.026
Kong J.-Z., Wang S.-S., Tai G.-A. et al. // J. Alloys Compd. 2016. V. 657. P. 593. https://doi.org/10.1016/j.jallcom.2015.10.187
Wu F., Zhang X., Zhao T. et al. // ACS Appl. Mater. Interfaces. 2015. V. 7. № 6. P. 3773. https://doi.org/10.1021/am508579r
Lee S.H., Koo B.K., Kim J.-C. et al. // J. Power Sources. 2008. V. 184. № 1. P. 276. https://doi.org/10.1016/j.jpowsour.2008.05.091
Zheng J., Gu M., Xiao J. et al. // Chem. Mater. 2014. V. 26. № 22. P. 6320. https://doi.org/10.1021/cm502071h
Li M., Wang H., Zhao L. et al. // J. Solid State Chem. 2019. V. 272. P. 38. https://doi.org/10.1016/j.jssc.2019.01.022
Liu X., Huang T., Yu A. // Electrochim. Acta. 2015. V. 163. P. 82. https://doi.org/10.1016/j.electacta.2015.02.155
Hu E., Bak S.-M., Liu Y. et al. // Adv. Energy Mater. 2016. V. 6. № 3. P. 1501662. https://doi.org/10.1002/aenm.201501662
Yan W., Xie Y., Jiang J. et al. // ACS Sustain. Chem. Eng. 2018. V. 6. № 4. P. 4625. https://doi.org/10.1021/acssuschemeng.7b03634
Nayak P.K., Grinblat J., Levi M. et al. // Adv. Energy Mater. 2016. V. 6. № 8. P. 1502398. https://doi.org/10.1002/aenm.201502398
Yue B., Wang X., Wang J. et al. // RSC Adv. 2018. V. 8. № 8. P. 4112. https://doi.org/10.1039/C7RA12705G
Kam K.C., Mehta A., Heron J.T. et al. // J. Electrochem. Soc. 2012. V. 159. № 8. P. A1383. https://doi.org/10.1149/2.060208jes
Lu Y., Pang M., Shi S. et al. // Sci. Rep. 2018. V. 8. № 1. P. 2981. https://doi.org/10.1038/s41598-018-21345-6
Sathiya M., Abakumov A.M., Foix D. et al. // Nat. Mater. 2015. V. 14. № 2. P. 230. https://doi.org/10.1038/nmat4137
Tamilarasan S., Mukherjee D., Sampath S. et al. // Solid State Ionics. 2016. V. 297. P. 49. https://doi.org/10.1016/j.ssi.2016.10.003
Valanarasu S., Chandramohan R., Thirumalai J. et al. // J. Sci. Res. 2010. V. 2. № 3. P. 443. https://doi.org/10.3329/jsr.v2i3.3877
Chen Y., Li Y., Tang S. et al. // J. Power Sources. 2018. V. 395. P. 403. https://doi.org/10.1016/j.jpowsour.2018.05.088
Yang X.-L., Peng G., Zhang L.-L. et al. // J. Electrochem. Soc. 2012. V. 159. № 12. P. A2096. https://doi.org/10.1149/2.014301jes
Zhang L.-L., Duan S., Yang X.-L. et al. // Sci. Rep. 2014. V. 4. № 1. P. 5064. https://doi.org/10.1038/srep05064
Li Y., Wang S., Chen Y. et al. // Mater. Chem. Phys. 2020. V. 240. P. 122029. https://doi.org/10.1016/j.matchemphys.2019.122029
Chen G., An J., Meng Y. et al. // Nano Energy. 2019. V. 57. P. 157. https://doi.org/10.1016/j.nanoen.2018.12.049
Makhonina E.V., Maslennikova L.S., Volkov V.V. et al. // Appl. Surf. Sci. 2019. V. 474. P. 25. https://doi.org/10.1016/j.apsusc.2018.07.159
Печень Л.С., Махонина Е.В., Румянцев А.М. и др. // Журн. неорган. химии. 2018. V. 63. № 12. P. 1522.
Дополнительные материалы
- скачать ESM.docx
- Приложение 1
Инструменты
Журнал неорганической химии


