Журнал неорганической химии, 2022, T. 67, № 7, стр. 959-965
Кристаллическая структура и оптические свойства новых гибридных галовисмутатов производных 2,2'-бипиридиния
С. П. Балабанова a, П. А. Буйкин a, b, c, *, А. Б. Илюхин b, А. Ю. Руденко d, П. В. Дороватовский e, А. А. Корлюков c, В. Ю. Котов a, b
a Научно-исследовательский университет “Высшая школа экономики”
101000 Москва, ул. Мясницкая, 20, Россия
b Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
c Институт элементоорганических соединений им. А.Н. Несмеянова РАН
119991 Москва, ул. Вавилова, 28, Россия
d Институт органической химии им. Н.Д. Зелинского РАН
119991 Москва, Ленинский пр-т, 47, Россия
e Национальный исследовательский центр “Курчатовский институт”
123182 Москва, пл. Академика Курчатова, 1, Россия
* E-mail: peterzzz@mail.ru
Поступила в редакцию 27.11.2021
После доработки 22.12.2021
Принята к публикации 17.01.2022
- EDN: FYKIRE
- DOI: 10.31857/S0044457X22070030
Аннотация
Получены и структурно охарактеризованы новые гибридные галовисмутаты 2,2'-бипиридиния ([bipyH]+) I и II, 7,8-дигидро-6H-дипиридо[1,2-a:2',1'-c][1,4]диазепин-5,9-диия ([bipyC3]2+) III, 6,7,8,9-тетрагидродипиридо[1,2-a:2',1'-c][1,4]диазоцин-5,10-диия ([bipyC4]2+) IV и 1,1'-(пентандиил)бис(2,2'-бипиридиния) ((bipyH)2C5]4+) V. В структуре I присутствуют монопротонированный катион 2,2'-бипиридиния и изолированный анион [Bi2Br10]4–. Бромовисмутат 2,2'-бипиридиния II содержит полимерный анион $\left[ {{\text{BiB}}{{{\text{r}}}_{{\text{4}}}}} \right]_{n}^{{n--}}$ и изоструктурен ранее описанному иодовисмутату. Бромовисмутат III включает в свой состав анионы [BiBr6]3– и молекулы воды. Иодовисмутат [bipyC3]2[Bi2I10] (VI) изоструктурен IV. В структуре V присутствуют катионы [(bipyH)2C5]4+ и три вида анионов: [Bi2Br10]4–, [BiBr6]3– и Br–. Соединения I, III и VI выделены в чистом виде. Значения оптической ширины запрещенной зоны для них составляют 2.84, 2.88 и 2.11 эВ соответственно.
ВВЕДЕНИЕ
Гибридные галовисмутаты представляют значительный интерес для химиков и материаловедов благодаря разнообразию их физических свойств [1–8], обусловленных различным строением входящих в их состав галовисмутат-анионов [9–14]. Активное изучение гибридных галогенидов висмута началось в 90-х гг. прошлого столетия [15, 16]. В настоящее время внимание исследователей уделяется поиску новых соединений, обладающих низкими значениями ширины запрещенной зоны (Eg) [17] и хорошим оптическим поглощением [18], которые рассматриваются в качестве перспективных светопоглощающих материалов в фотовольтаике [19–21], фотодетекторах [22, 23] и фотодиодах [24]. Известно, что соединения, в кристаллической структуре которых есть полимерные линейные анионы $\left[ {{\text{Bi}}{{{\text{Х}}}_{{\text{5}}}}} \right]_{n}^{{2n--}},$ обладают низкими значениями оптической ширины запрещенной зоны. Среди этих соединений можно выделить иодовисмутат 1,1'-(1,5-пентандиил)бис(4-метилпиридиния) [25], бромовисмутат 2-бромпиридиния [26], галовисмутаты метилвиологена [27–29] и 4,4'-аминобипиридиния [30]. Производные 2,2'-бипиридина (bipy) близки по строению к катиону метилвиологена, и можно ожидать, что такие соединения будут проявлять необычные оптические свойства. Недавно был получен бромовисмутат 9,10-дигидро-8a,10a-диазонияфенантрена (схема 1 ) состава [bipyC2]6(H3O)3[BiBr5]6[BiBr6] [31], содержащий полимерные анионы $\left[ {{\text{BiB}}{{{\text{r}}}_{{\text{5}}}}} \right]_{n}^{{2n--}}.$ Кристаллы этого соединения имеют желтую окраску, что косвенно свидетельствует о достаточно низком для бромовисмутатов значении Eg.
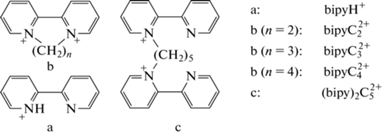
Схема 1 . Катион 2,2'-бипиридиния (а); 9,10-дигидро-8a,10a-диазонияфенантрен (b, n = 2); 7,8-дигидро-6H-дипиридо[1,2-a:2',1'-c] [1, 4]диазепин-5,9-диия (b, n = 3); 6,7,8,9-тетрагидродипиридо[1,2-a:2',1'-c] [1, 4]диазоцин-5,10-диия (b, n = 4); 1,1'-(пентандиил)бис(2,2'-бипиридиния) (в).
В литературе известно несколько галовисмутатов производных 2,2'-бипиридина. Среди них хлоровисмутаты 2,2'-бипиридиния с анионами [Bi2Cl9]3– и [Bi4Cl20]8– [32]; иодовисмутаты 2,2'-бипиридиния c анионами $[{\text{Bi}}{{{\text{I}}}_{{\text{4}}}}]_{n}^{{n--}}$ и [Bi2I10]4– [32], [Bi2I9]3– [33] и $\left[ {{\text{B}}{{{\text{i}}}_{{\text{3}}}}{{{\text{I}}}_{{{\text{11}}}}}} \right]_{n}^{{2n--}}$ [34]; а также изоструктурные хлоро- и бромовисмутаты N-метил-2,2'-бипиридиния с анионом [Bi2X10]4– [35]. В перечисленных кристаллических структурах ионы 2,2'-бипиридиния моно- и дипротонированы. В Кембриджской базе структурных данных [36] отсутствуют сведения о галовисмутатах производных 2,2'-бипиридина с алкильными цепями, содержащими более чем два атома углерода. В настоящей работе сообщается о получении новых гибридных галовисмутатов производных 2,2'-бипиридина, их кристаллической структуре и оптических свойствах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез [bipyH]4[Bi2Br10] (I). К 25 мл 0.04 М раствора BiBr3 в 2 М HBr добавляли 50 мл 0.04 М раствора 2,2'-бипиридина в 2 М HBr. Выпавший светло-желтый кристаллический осадок [bipyH]4[Bi2Br10] отфильтровывали под вакуумом, промывали этанолом и сушили на воздухе. По данным РФА, (рис. S1a ) полученный продукт является однофазным. Выход 0.77 г (83%). Детали уточнения по Ритвельду: пр. гр. $P\bar {1},$ a = 13.4421(4), b = 13.8834(5), c = = 13.9117(5) Å, α = 89.328(2)°, β = 76.115(3)°, γ = = 85.393(4)°, Rexp = 2.39%, Rwp = 5.18%, Rp = 4.02%, GOF = 2.17. Ниже приведены результаты элементного CHN-анализа.
| C | H | N | |
| Найдено, %: | 26.00; | 2.00; | 6.02. |
| Для C40H36N8Bi2Br10 (1845.78) | |||
| рассчитано, %: | 26.03; | 1.97; | 6.07. |
Изменение мольного соотношения реагентов BiBr3 и 2,2'-бипиридина с 1 : 2 на 2 : 1 приводит к образованию продукта, содержащего фазу [bipyH][BiBr4] (II) наряду с основной фазой I. По данным РФА (рис. S1b ), выделенный продукт содержит 77 (±1)% фазы I и 23 (±1)% фазы II. Детали уточнения по Ритвельду: I – пр. гр. $P\bar {1},$ a = 13.4430(6), b = 13.8829(8), c = 13.9145(9) Å, α = = 89.346(4)°, β = 76.148(5)°, γ = 85.320(6)°; II – пр. гр. ${{C2} \mathord{\left/ {\vphantom {{C2} c}} \right. \kern-0em} c}$, a = 11.9937(10), b = 17.8031(13), c = 7.4039(6) Å, β = 94.605(6)°; Rexp = 2.35%, Rwp = 5.28%, Rp = = 4.10%, GOF = 2.25.
Синтез дибромидов производных 2,2'-бипиридина. Синтез проводили путем взаимодействия 2,2'-бипиридина с соответствующими 1,n-дибромалканами (n = 3–5). В круглодонной колбе объемом 100 мл растворяли 2,2'-бипиридин (1.00 г, 6.40 ммоль) в 50 мл 1,1'-дибромалкана. Полученный раствор нагревали на магнитной мешалке с температурой рабочей поверхности 170–200°С с обратным холодильником при перемешивании в течение 6 ч. После охлаждения белый осадок отфильтровывали под вакуумом, промывали ацетоном и сушили на воздухе при температуре 95°С. В случае образования [bipyC3]Br2 выход продукта значительно превосходит выход в работе [37]. [bipyC3]Br2. Выход 2.19 г (95%). 1H ЯМР (600 МГц, ДМСО-d6), δ: 9.50 (д, 2H), 8.93 (т, 2H), 8.50 (д, 2H), 8.48 (т, 2H), 5.11 (д, 2H), 4.47 (м, 2H), 2.78 (м, 2H).
Согласно данным 1Н ЯМР, взаимодействие 2,2'-бипиридина с 1,4-дибромбутаном и 1,5-дибромпентаном в этих же условиях приводит к получению смеси продуктов [bipyC4]Br2 или [(bipy)2C5]Br2 (возможно в протонированной форме), а также бромида 2,2'-бипиридилия. Содержание [bipyC4]Br2 и [(bipy)2C5]Br2 в полученных смесях не превышает 15 мол. %.
Синтез [bipyC3]3[BiBr6]2 · H2O (III). К раствору [bipyC3]Br2 (0.358 г, 1.00 ммоль) в 25 мл 2 M HBr добавляли 0.04 М раствор BiBr3 (25 мл) в 2 М HBr. Выпавший светло-желтый осадок [bipyC3]3[BiBr6]2 · H2O отфильтровывали под вакуумом, промывали этанолом и сушили на воздухе. По данным РФА (рис. S1c ), полученный продукт является однофазным. Выход 0.49 г (49%). Детали уточнения по Ритвельду: пр. гр. $Pccn,$ a = = 22.3996(5), b = 15.4264(3), c = 15.7709(5) Å, Rexp = 1.33%, Rwp = 3.74%, Rp = 2.87%, GOF = 2.82.
| C | H | N | |
| Найдено, %: | 23.66; | 2.18; | 4.25. |
| Для C39H44N6Bi2Br12O (1989.62) | |||
| рассчитано, %: | 23.52; | 2.21; | 4.22. |
Выращивание кристаллов [bipyC4]2[Bi2I10] (IV). К раствору полученной ранее смеси дибромида [bipyC4]Br2 и бромида 2,2'-бипиридилия (0.372 г) в 40 мл H2O добавляли 60 мл раствора, содержащего Bi(NO3)3 · 5H2O (1.94 г, 4.00 ммоль) и KI (13.3 г, 78 ммоль). Выпавший оранжевый осадок отфильтровывали под вакуумом, промывали этанолом и сушили на воздухе. Из полученного оранжевого порошка механически были выделены отдельные кристаллы [bipyC4]2[Bi2I10].
Выращивание кристаллов [(bipyH)2С5]2[Bi2Br10] [BiBr6]Br · 3H2O (V). К раствору полученной ранее смеси дибромида [(bipy)2C5]Br2 и бромида 2,2'-бипиридилия (0.386 г) в 25 мл 2 M HBr добавляли 25 мл 0.04 M раствора BiBr3 в 2 M HBr. Выпавший светло-желтый осадок отфильтровывали под вакуумом, промывали этанолом и сушили на воздухе. В полученном порошке наряду с соединением I были обнаружены отдельные кристаллы [(bipyH)2С5]2[Bi2Br10][BiBr6]Br · 3H2O.
Синтез [bipyC3]2[Bi2I10] (VI). К раствору дибромида [bipyC3]Br2 (0.358 г, 1.00 ммоль) в 40 мл H2O добавляли 60 мл раствора, содержащего Bi(NO3)3 · ⋅ 5H2O (1.94 г, 4.00 ммоль) и KI (13.3 г, 78 ммоль). Выпавший оранжевый осадок [bipyC3]2[Bi2I10] отфильтровывали под вакуумом, промывали этанолом и сушили на воздухе. По данным РФА (рис. S1d ), полученный продукт является однофазным. Выход 0.84 г (81%). Детали уточнения по Ритвельду: пр. гр. ${{P{{2}_{1}}} \mathord{\left/ {\vphantom {{P{{2}_{1}}} n}} \right. \kern-0em} n},$ a = 20.149(4), b = = 11.634(3), c = 20.327(7) Å, β = 115.468(15)°, Rexp = = 1.41%, Rwp = 2.20%, Rp = 1.66%, GOF = 1.56.
Рентгеноструктурный анализ (РСА). Экспериментальные данные для соединений I–V получены на дифрактометре Bruker SMART APEX2 (λMoKα, графитовый монохроматор; ЦКП ИОНХ РАН) [38] (табл. S1 ). Поглощение учтено полуэмпирическим методом по эквивалентам (программа SADABS) [39]. Структуры определены комбинацией прямого метода и Фурье-синтезов. Уточнение проведено полноматричным анизотропно-изотропным МНК. Кристаллы I невысокого качества, что определяет высокий пик в разностном Фурье-синтезе (2.6 e/Å3). Заселенности разупорядоченных фрагментов в структуре V получены при изотропном уточнении с фиксированными тепловыми параметрами разупорядоченных атомов и в последующем уточнении фиксировались. Все расчеты выполнены по программам Shelxs и Shelxl [40].
Экспериментальные данные для структур I–V депонированы в Кембриджском банке структурных данных (CCDC № 2122720–2122724; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk).
Рентгенофазовый анализ (РФА) проведен на дифрактометре Bruker D8 Advance (CuKα-излучение, позиционно-чувствительный 1D-детектор LynxEye, геометрия на отражение). Диапазон измерений 2θ = 5°–50° для всех образцов. Полнопрофильный анализ порошков проведен с помощью программы TOPAS 4.2 [41]. Уточнение по Ритвельду проводили с использованием структурных моделей I–III.
Спектры диффузного отражения (СДО) регистрировали на спектрофотометре Ocean Optics модель QE65000 в диапазоне частот 11 000–50 000 см–1 при комнатной температуре. Спектры были перестроены в координатах зависимости функции Кубелки–Мунка [42] от энергии света (рис. S2 ). Для получения функции Кубелки–Мунка использовали уравнение:
где F(Rd) – абсолютное отражение слоя образца. Оптическую ширину запрещенной зоны (Eg) оценивали экстраполяцией линейной части соответствующей кривой на F(Rd) = 0.Спектры 1Н ЯМР регистрировали на спектрометре Bruker Avance 600 (600 МГц) в DMSO-d6 при 303 K.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В результате взаимодействия 2,2'-бипиридина (2 экв) с BiBr3 (1 экв) в сильнокислой среде получен однофазный [bipyH]4[Bi2Br10] (I) (Eg = 2.84 эВ). Структура I образована катионами монопротонированного бипиридина и центросимметричными анионами [Bi2Br10]4– (рис. 1). Каждый анион посредством водородных связей N–H⋅⋅⋅Br объединяет четыре катиона (pис. S3a). Стекинг-взаимодействия между катионами объединяют структурные единицы в слои (pис. S3b). Кратчайшие контакты Br⋅⋅⋅Br составляют 4.14 и 4.28 Å.
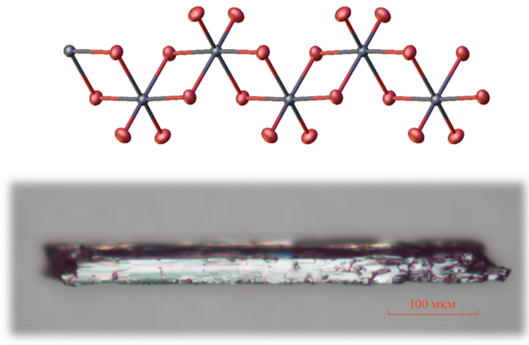
При уменьшении соотношения 2,2'-бипиридина и BiBr3 до 1 : 1 и 1 : 2 не происходит образования чистых продуктов. В последнем случае наблюдали образование кристаллов [bipyH][BiBr4] (II) наряду с основной фазой I. По данным РФА, содержание фазы II в полученной смеси составляет 23%. В структуре II катион [bipyH]+ разупорядочен вокруг оси 2, строение 1D-цепей аниона (рис. 2) характерно для подобных структур. Соединение изоструктурно иодовисмутату 2,2'-бипиридиния, описанному в [32]. Кратчайший контакт Br⋅⋅⋅Br составляет 4.03 Å.
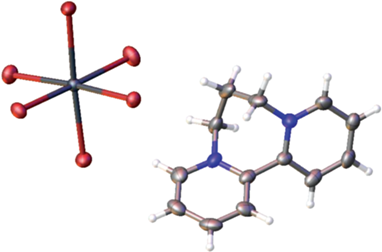
С целью изучения кристаллических структур N,N'-дизамещенных 2,2'-бипиридинов были получены галовисмутаты c катионами [bipyC3]2+, [bipyC4]2+ и [(bipyH)2C5]4+ (два последних в смеси с галовисмутатами 2,2'-бипиридилия). Однофазный бромовисмутат [bipyC3]3[BiBr6]2 · H2O (III) (Eg = 2.88 эВ) был получен при взаимодействии дибромида [bipyC3]Br2 с BiBr3 в сильнокислой среде. Один из катионов [bipyC3]2+ (рис. 3) в структуре III расположен на оси 2, кристаллизационная молекула H2O находится в обширной полости и разупорядочена вокруг центра инверсии. Анионы [BiBr6]3– расположены далеко друг от друга, в результате кратчайшие контакты Br⋅⋅⋅Br значительно больше, чем в остальных структурах, и составляют 5.10 Å.
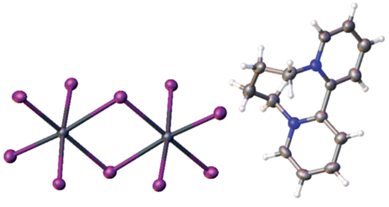
Иодовисмутаты [bipyC3]2[Bi2I10](VI) (Eg = 2.11 эВ) и [bipyC4]2[Bi2I10](IV) были выделены из слабокислых растворов, содержащих соответствующие дибромиды, Bi(NO3)3 и KI. Соединение VI кристаллизуется в пр. гр. ${{P{{2}_{1}}} \mathord{\left/ {\vphantom {{P{{2}_{1}}} n}} \right. \kern-0em} n}$ и является однофазным. Параметры кристаллической решетки при 100 K: a = 19.960, b = 11.570, c = 20.217 Å, β = 115.12° [43]. Сопоставление данных РСА и РФА для VI и IV позволяет утверждать, что эти соединения изоструктурны. В структуре IV (рис. 4) кристаллографически независимый катион находится в общей позиции, а анион – на центрах симметрии. Кратчайшие контакты I⋅⋅⋅I составляют 4.34 и 4.37 Å.
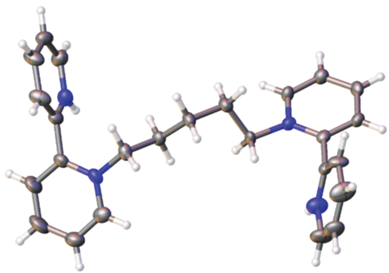
Отдельные кристаллы бромовисмутата [(bipyH)2С5]2[Bi2Br10][BiBr6]Br · 3H2O (V) были извлечены из продукта взаимодействия смеси, содержащей дибромид [(bipy)2C5]Br2 и BiBr3 в сильнокислой среде. Структура V образована катионами [(bipyH)2С5]4+ (рис. 5), анионами трех типов ([Bi2Br10]2–, [BiBr6]3–, Br–) и кристаллизационными молекулами H2O. Оба комплексных аниона расположены на центрах инверсии, анион [Bi2Br10]2– упорядочен, в то время как в анионе [BiBr6]3– атом Bi и один из атомов Br разупорядочены. Анион Br– по статистике занимает одну позицию с молекулой H2O (расстояние Br⋅⋅⋅O 0.39 Å). Кратчайшие контакты упорядоченных атомов Br⋅⋅⋅Br составляют 3.56 и 3.96 Å.
Значение оптической ширины запрещенной зоны было определено для соединений I, III и VI, выделенных в чистом виде. Для бромовисмутатов I и III оно составило 2.84 и 2.88 эВ соответственно. Указанные величины характерны для большинства известных бромовисмутатов с изолированными анионами в структуре. Более низкое значение Eg для I может быть обусловлено наличием более коротких расстояний Br⋅⋅⋅Br (4.14 и 4.28 Å в I по сравнению с 5.10 Å в III). Значение Eg для иодовисмутата VI составляет 2.11 эВ и также характерно для большинства гибридных соединений с изолированными иодовисмутат-анионами. Таким образом, в полученных соединениях отсутствуют цепи анионов, наличие которых может приводить к понижению оптической ширины запрещенной зоны, как это произошло в [bipyC2]6(H3O)3[BiBr5]6[BiBr6] [31].
Список литературы
Mencel K., Starynowicz P., Siczek M. et al. // Dalton Trans. 2019. V. 48. № 39. P. 14829. https://doi.org/10.1039/c9dt02916h
Jakubas R., Gągor A., Winiarski M.J. et al. // Inorg. Chem. 2020. V. 59. № 6. P. 3417. https://doi.org/10.1021/acs.inorgchem.9b03193
Moskwa M., Bator G., Rok M. et al. // Dalton Trans. 2018. V. 47. № 38. P. 13507. https://doi.org/10.1039/c8dt03121e
Wang Y.L., Chen X.H., Shu W. et al. // J. Coord. Chem. 2019. V. 72. № 4. P. 573. https://doi.org/10.1080/00958972.2019.1570167
Pandey S., Chattopadhyay T., Dev S. et al. // Polyhedron. 2020. V. 179. P. 114335. https://doi.org/10.1016/j.poly.2019.114335
Wang P., Sheng W.W., Chen Z.R. et al. // J. Clust. Sci. 2021. V. 32. № 3. P. 727. https://doi.org/10.1007/s10876-020-01829-0
Adonin S.A., Gorokh I.D., Samsonenko D.G. et al. // Inorg. Chim. Acta. 2018. V. 469. P. 32. https://doi.org/10.1016/j.ica.2017.08.058
Wang Y.-Y., Song L., Dai Z.-Q. et al. // J. Solid State Chem. 2021. V. 304. P. 122611. https://doi.org/10.1016/j.jssc.2021.122611
Adonin S.A., Sokolov M.N., Fedin V.P. // Coord. Chem. Rev. 2016. V. 312. P. 1. https://doi.org/10.1016/j.ccr.2015.10.010
Buikin P.A., Rudenko A.Y., Ilyukhin A.B. et al. // Russ. J. Coord. Chem. 2020. V. 46. № 2. P. 111. https://doi.org/10.1134/S1070328420020049
Buikin P.A., Rudenko A.Y., Ilyukhin A.B. et al. // Russ. J. Inorg. Chem. 2021. V. 66. № 4. P. 482. https://doi.org/10.1134/S0036023621040057
Buikin P.A., Ilyukhin A.B., Laurinavichyute V.K. et al. // Russ. J. Inorg. Chem. 2021. V. 66. № 2. P. 133. https://doi.org/10.1134/S0036023621020042
Sharutin V.V., Yegorova I.V., Klepikov N.N. et al. // Russ. J. Inorg. Chem. 2009. V. 54. № 1. P. 52. https://doi.org/10.1134/S0036023609010124
Sharutin V.V., Sharutina O.K., Khisamov R.M. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 6. P. 766. https://doi.org/10.1134/S0036023617060201
Krautscheid H. // ZAAC. 1995. V. 621. № 12. P. 2049. https://doi.org/10.1002/zaac.19956211212
Carmalt C.J., Farrugia L.J., Norman N.C. // Z. Naturforsch., Sect. B: J. Chem. Sci. 1995. V. 50. № 11. P. 1591. https://doi.org/10.1515/znb-1995-1104
Kotov V.Y., Buikin P.A., Ilyukhin A.B. et al. // New J. Chem. 2021. V. 45. № 39. P. 18349. https://doi.org/10.1039/d1nj02390j
Ganose A.M., Savory C.N., Scanlon D.O. // Chem. Commun. 2017. V. 53. № 1. P. 20. https://doi.org/10.1039/c6cc06475b
Lee L.C., Huq T.N., Macmanus-Driscoll J.L. et al. // APL Mater. 2018. V. 6. № 8. https://doi.org/10.1063/1.5029484
Stroyuk O. // Beilstein J. Nanotechnol. 2018. V. 9. № 1. P. 2209. https://doi.org/10.3762/bjnano.9.207
Waykar R., Bhorde A., Nair S. et al. // J. Phys. Chem. Solids. 2020. V. 146. P. 109608. https://doi.org/10.1016/j.jpcs.2020.109608
Usoltsev A.N., Elshobaki M., Adonin S.A. et al. // J. Mater. Chem. A. 2019. V. 7. № 11. P. 5957. https://doi.org/10.1039/c8ta09204d
Premkumar S., Liu D., Zhang Y. et al. // ACS Appl. Nano Mater. 2020. V. 3. № 9. P. 9141. https://doi.org/10.1021/acsanm.0c01787
Vassilakopoulou A., Papadatos D., Zakouras I. et al. // J. Alloys Compd. 2017. V. 692. P. 589. https://doi.org/10.1016/j.jallcom.2016.09.076
Kotov V.Y., Ilyukhin A.B., Korlyukov A.A. et al. // New J. Chem. 2018. V. 42. № 8. P. 6354. https://doi.org/10.1039/c7nj04948j
Adonin S.A., Gorokh I.D., Novikov A.S. et al. // Chem. – A Eur. J. 2017. V. 23. № 62. P. 15612. https://doi.org/10.1002/chem.201703747
Bi W., Leblanc N., Mercier N. et al. // Chem. Mater. 2009. V. 21. № 18. P. 4099. https://doi.org/10.1021/cm9016003
Leblanc N., Mercier N., Zorina L. et al. // J. Am. Chem. Soc. 2011. V. 133. № 38. P. 14924. https://doi.org/10.1021/ja206171s
Chen Y., Yang Z., Guo C.X. et al. // Eur. J. Inorg. Chem. 2010. № 33. P. 5326. https://doi.org/10.1002/ejic.201000755
Skorokhod A., Mercier N., Allain M. et al. // Inorg. Chem. 2021. V. 60. P. 17123.https://doi.org/10.1021/acs.inorgchem.1c02384
Adonin S.A., Gorokh I.D., Samsonenko D.G. et al. // Russ. J. Inorg. Chem. 2016. V. 61. № 8. P. 958. https://doi.org/10.1134/S0036023616080027
Bowmaker G.A., Junk P.C., Lee Aaron M. et al. // Aust. J. Chem. 1998. V. 51. № 4. P. 293. https://doi.org/10.1071/C97036
Oswald I.W.H., Ahn H., Neilson J.R. // Dalton Trans. 2019. V. 48. № 43. P. 16340. https://doi.org/10.1039/c9dt03207j
Goforth A.M., Tershansy M.A., Smith M.D. et al. // Acta Crystallogr., Sect. C. 2006. V. 62. № 9. P. M381. https://doi.org/10.1107/S0108270106025972
Adonin S.A., Gorokh I.D., Samsonenko D.G. et al. // Russ. J. Coord. Chem. 2016. V. 42. № 11. P. 695. https://doi.org/10.1134/S1070328416110014
Groom C.R., Bruno I.J., Lightfoot M.P. et al. // Acta Crystallogr., Sect. B. 2016. V. 72. № 2. P. 171. https://doi.org/10.1107/S2052520616003954
Popp F.D., Chesney D.K. // J. Heterocycl. Chem. 1972. V. 9. № 5. P. 1165. https://doi.org/10.1002/jhet.5570090541
Bruker // Apex II 2009. P. Bruker AXS Inc.
Sheldrick G.M. // Programs Scaling Absorpt. Correct. Area Detect. Data. 1997.
Sheldrick G.M. // Acta Crystallogr., Sect. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
Coelho A. // Bruker AXS GmbH 2009.
Kubelka P., Munk F. // Z. Tech. Phys. 1931. V. 12. № 1930. P. 593. http://www.graphics.cornell.edu/~westin/pubs/kubelka.pdf
Balabanova S., Buikin P., Ilyukhin A. et al. // CSD Commun. 2021. https://doi.org/10.5517/ccdc.csd.cc298r1d
Дополнительные материалы
- скачать ESM.docx
- Приложение 1
Инструменты
Журнал неорганической химии