Журнал неорганической химии, 2022, T. 67, № 6, стр. 843-851
Формирование в гидротермальных условиях и строение нанокомпозитов в системе ZrO2–Y2O3–Al2O3
А. И. Шуклина a, О. В. Альмяшева a, b, *
a Санкт-Петербургский государственный электротехнический университет “ЛЭТИ” им. В.И. Ульянова (Ленина)
197022 Санкт-Петербург, ул. Профессора Попова, 5, Россия
b Физико-технический институт им. А.Ф. Иоффе РАН
194021 Санкт-Петербург, ул. Политехническая, 26, Россия
* E-mail: almjasheva@mail.ru
Поступила в редакцию 08.11.2021
После доработки 10.01.2022
Принята к публикации 11.01.2022
- EDN: LRYADG
- DOI: 10.31857/S0044457X22060216
Аннотация
Исследовано взаимное влияние компонентов в системе ZrO2–Y2O3–Al2O3 на процессы формирования нанокомпозитов в условиях гидротермальной обработки. Анализ полученных результатов показал, что наличие оксида иттрия в наночастицах на основе диоксида циркония с флюоритоподобной структурой приводит к активной перекристаллизации нанокристаллов c-ZrO2(YO1.5) в системе ZrO2(YO1.5)–AlO1.5 в гидротермальных условиях. При этом оксид иттрия частично переходит из наночастиц ZrO2(YO1.5) в аморфную фазу на основе оксида алюминия. Наиболее активный перенос оксида иттрия между наночастицами ZrO2(YO1.5) и аморфной фазой наблюдается в случаях, когда оксид иттрия частично локализован на поверхности нанокристаллов c-ZrO2(YO1.5), что реализуется при содержании YO1.5 в наночастицах ZrO2(YO1.5), большем ~27 мол. %.
ВВЕДЕНИЕ
Синтез нанокомпозитов в системе ZrO2–Y2O3–Al2O3 представляет большой интерес как с точки зрения изучения процессов фазообразования в зависимости от метода и условий формирования наночастиц [1–11], так и в связи с прикладным использованием материалов на основе данной системы [12–21]. Спектр областей возможного применения материалов во многом определяется структурным состоянием ее компонентов. В частности, в работах [17, 20] показано, что в условиях пространственных ограничений, которые создают нанокристаллы ZrO2, оксид алюминия существует в рентгеноаморфном состоянии, устойчивом до 1000°С, а вся система проявляет высокую каталитическую активность в реакциях окисления водорода, сопоставимую с платина-палладиевыми промышленными катализаторами.
В связи с разнообразием функциональных материалов, реализующихся в системе ZrO2–Al2O3, разработке различных способов получения субмикронных и наноразмерных порошковых композиций на основе оксидов циркония и алюминия посвящено большое число работ [1–5, 8–10, 13–15]. Анализ результатов указанных работ показал различную степень взаимного влияния оксидов циркония и алюминия на химический состав, кристаллическую структуру, морфологию и микроструктуру образующихся материалов в зависимости от способа их получения. Это наблюдение относится ко многим оксидным системам, причем взаимное влияние компонентов на структурные превращения в них наиболее заметно, когда в композиции возможно образование твердых растворов, когерентное срастание кристаллитов по границам зерен или образование пространственных ограничений, сопоставимых по размерам с величиной минимально возможного размера зародыша кристаллической фазы [22–25].
В работах [26, 27] отмечены особенности формирования наночастиц переменного состава на основе ZrO2 в гидротермальных условиях, связанные с сегрегацией вещества в самой частице, при которой происходит перераспределение компонентов между ее объемом и поверхностью. В связи с этим представляет интерес исследование структурных и химических превращений при гидротермальной обработке композиций в системе ZrO2(YO1.5)–Al2O3, полученных осаждением гидроксида алюминия на предварительно синтезированные оксидные наночастицы ZrO2(YO1.5). В этом случае можно ожидать взаимодействия рентгеноаморфного оксида иттрия на поверхности наночастиц на основе диоксида циркония [26, 27] с аморфным оксидом алюминия, формирующимся в ходе гидротермальной обработки [1, 11, 17] и обладающим повышенной реакционной способностью.
Таким образом, цель настоящей работы заключается в определении характера фазовых превращений в системе ZrO2(YO1.5)–Al2O3 в условиях гидротермальной обработки в зависимости от соотношения компонентов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исходные композиции синтезировали прямым осаждением гидроксида алюминия Al(OH)3 в суспензии предварительно полученных наночастиц на основе диоксида циркония, допированных оксидом иттрия.
Наночастицы на основе диоксида циркония получали гидротермальной обработкой совместно осажденных гидроксидов циркония и иттрия. Смесь гидроксидов циркония и иттрия получали прямым соосаждением из водных растворов оксохлорида циркония ZrOCl2 · 8H2O (х. ч., ТУ 6-09-3677-74) и хлорида иттрия YCl3 · 6H2O (х. ч., ТУ 6-09-4773-79). В смесь растворов солей циркония и иттрия с заданным соотношением Zr : Y при постоянном перемешивании приливали раствор гидроксида аммония NH4OH (ос. ч., ГОСТ 24147-80) с концентрацией 12 моль/л до значения pH ~ 9. Полученную суспензию перемешивали в течение 1 ч, после чего осадок отделяли с помощью декантации и системы вакуумной фильтрации. После фильтрации осадок промывали дистиллированной водой до нейтральной реакции (pH ~ 7) и отсутствия ионов Cl– в фильтрате и высушивали при 90°С. Количество иттрия в системе в пересчете на оксиды ((1 – x)ZrO2 : xYO1.5) варьировали в широком диапазоне концентраций (0.06–0.50 мол. д.). Гидротермальную обработку полученных порошков осуществляли в стальных автоклавах с тефлоновым тиглем (объем тигля 16 мл). Температура обработки составляла 240°С, давление – 70 МПа, продолжительность изотермической выдержки при указанных условиях – 4 ч. В качестве гидротермального флюида использовали дистиллированную воду. Давление задавали по коэффициенту заполнения реакционного объема гидротермальным флюидом. По окончании изотермической выдержки автоклавы извлекали из печи и охлаждали на воздухе. Полученный порошок высушивали при температуре 90°С. Подробно методика получения нанокристаллов на основе диоксида циркония представлена в работах [27, 28].
Для получения нанокомпозита “наночастицы ZrO2(YO1.5)–AlO1.5” наночастицы на основе диоксида циркония диспергировали в 1.5 М водном растворе хлорида алюминия AlCl3 · 6H2O (х. ч., СТП ТУ КОМП 2-191-10) с использованием ультразвукового диспергатора (H = 22 МГц). Затем при постоянном перемешивании к полученной суспензии приливали раствор NH4OH (ос. ч., ГОСТ 24147-80) с концентрацией 12 моль/л до значения pH ~ 9. Суспензию перемешивали в течение 1 ч, затем с использованием системы вакуумной фильтрации осадок отделяли, промывали дистиллированной водой до нейтральной реакции (pH ~ 7) и отсутствия примесных ионов Cl– и высушивали при температуре 90°С. Соотношение компонентов в системе ZrO2(YO1.5)–AlO1.5 задавали равным ~22 : 78 мол. %, что соответствует эвтектическому составу системы ZrO2–AlO1.5 [29–31].
Гидротермальную обработку композиций ZrO2(YO1.5)–Al(OH)3 проводили с использованием установки для гидротермального синтеза КИ-250 (ЗАО “КемКо инжиниринг”), которая включала стальной автоклав с титановым тиглем и систему контроля параметров обработки в реакционной среде, при температуре 480°С, давлении 70 МПа и продолжительности изотермической выдержки 4 ч, гидротермальным флюидом служила дистиллированная вода. Выбор параметров обработки и более подробное описание методики синтеза представлены в работах [1, 11, 17, 32].
Композиции ZrO2(YO1.5)–Al(OH)3 также подвергали термообработке на воздухе при температуре 500°С в течение 60 мин.
Элементный состав образцов определяли методом энергодисперсионного анализа на растровом электронном микроскопе Hitachi S-570, оснащенном микрозондовой системой Bruker Quantax 200.
Фазовое состояние образцов и значения параметров элементарных ячеек определяли по данным рентгеновской дифрактометрии порошков. Доли моноклинной (m-ZrO2) и кубической (c-ZrO2) модификаций диоксида циркония в системе определяли по соотношению интегральных интенсивностей рефлексов 111 и –111 m-ZrO2 и 111 c-ZrO2 по методике, описанной в [28]. Съемку дифрактограмм осуществляли на рентгеновском дифрактометре Shimadzu XRD-7000 с использованием CuKα-излучения в диапазоне углов 2θ от 10° до 60° со скоростью съемки 2 град/мин (шаг 0.01). При определении параметров элементарной ячейки в качестве внутреннего эталона использовали кремний.
Размерные параметры кристаллитов определяли по данным о профиле линий рентгеновской дифракции, распределение кристаллитов находили с помощью программного пакета Rigaku SmartLab Studio II. Расчеты средних значений размеров кристаллитов проводили по формуле Шеррера и по данным о распределении кристаллитов по размерам.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты элементного анализа образцов “наночастицы ZrO2(YO1.5)–AlO1.5” (табл. 1) свидетельствуют об отсутствии в пределах чувствительности метода примесных элементов и о соответствии в пределах погрешности метода синтеза [27] соотношения Zr : Y заданному соотношению компонентов в пересчете на оксиды ZrO2 : YO1.5. Соотношение элементов в пересчете на оксиды ZrO2(YO1.5) : AlO1.5 отличается от заданного при синтезе, но лежит в диапазоне приблизительно от 42 до 58 мол. % AlO1.5. Отличие реального состава системы от заданного при синтезе, по-видимому, обусловлено потерями на стадии промывания осажденного Al(OH)3 от примесных ионов Cl–.
Таблица 1.
Элементный и фазовый состава композиций ZrO2(YO1.5)–AlO1.5
| Образец (количество YO1.5) | Соотношение компонентов в исходной композиции в пересчете на оксиды, мол. % | Соотношение m-ZrO2 и c-ZrO2 | Содержание YO1.5 в нанокристаллах c‑ZrO2(YO1.5)*, мол. % | Соотношение компонентов в аморфной фазе, мол. % | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| номинальное значение (задано при синтезе) | реальное значение (результаты анализа) | AlO1.5 | YO1.5 | ZrO2 | ZrO2 | YO1.5 | AlO1.5 | YO1.5 | ||
| m | c | m | c | |||||||
| гидротермальная обработка (t = 480°С, p = 3 МПа) | ||||||||||
| 6 | 10.2 (10.6)** | 47.2 | 5.4 | 3.8 | 43.6 | 7.8 | 39.6 | 7.5 | 95.6 | 4.4 |
| 15 | 18.1 | 43.7 | 10.2 | – | 46.1 | 2.6 | 43.5 | 10.0 | 90.2 | 9.8 |
| 20 | 24.3 | 60.0 | 9.7 | – | 30.3 | 0.8 | 29.5 | 14.2 | 92.3 | 7.7 |
| 25 | 32.9 | 41.9 | 19.1 | – | 39.0 | – | 39.0 | 18.8 | 80.6 | 19.4 |
| 35 | 37.1 | 56.4 | 16.2 | – | 27.5 | – | 27.5 | 25.3 | 89.2 | 10.8 |
| 50 | 56.2 | 58.2 | 23.5 | – | 18.3 | – | 18.3 | 27.8 | 78.0 | 22.0 |
| Термообработка при t = 500°C | ||||||||||
| 6 | 10.2 (10.6)* | 47.2 | 5.4 | 3.8 | 43.6 | 3.7 | 43.7 | 10.8 | 99.8 | 0.2 |
| 35 | 37.1 | 56.4 | 16.2 | – | 27.5 | – | 27.5 | 35.9 | 98.6 | 1.4 |
* Содержание YO1.5, определенное по данным о значениях параметров элементарной ячейки c-ZrO2(YO1.5) с учетом зависимости a(x(YO1.5)) для кристаллической фазы (рис. 2).
Согласно данным рентгенофазового анализа, в системе ZrO2–YO1.5 в гидротермальных условиях формируются преимущественно нанокристаллы на основе диоксида циркония со структурой флюорита (c-ZrO2), и только при 10 мол. % YO1.5 на рентгеновской дифрактограмме фиксируются рефлексы, отвечающие небольшому количеству диоксида циркония моноклинной модификации (табл. 1).
Рентгеновские дифрактограммы образцов после процедуры осаждения гидроксида алюминия представлены на рис. 1а. На этих дифрактограммах помимо фаз на основе диоксида циркония фиксируется дополнительный набор рефлексов, которые отвечают кристаллическим формам гидроксида алюминия – гиббсита (JCPDC 33-18) и байерита (JCPDC 20-11). Что касается образца с наночастицами c-ZrO2(YO1.5), содержащими максимальное количество YO1.5 (56.2 мол. %), то на его дифрактограмме не обнаруживаются рефлексы, характерные для кристаллических форм гидроксида алюминия. Следует отметить, что для нанокристаллов c-ZrO2(YO1.5) данного образца характерны и наименьшие значения их размера (рис. 2a, кривые 1, 2), составляющие ~5 нм. По-видимому, отсутствие кристаллических форм гидроксида алюминия связано с блокированием наночастицами ZrO2(YO1.5) процесса образования кристаллов Al(OH)3 по механизму, описанному в [1, 32]. В характере рефлексов, отвечающих фазам на основе диоксида циркония, никаких изменений после осаждения гидроксида алюминия и последующего высушивания образцов не наблюдается, не видны также изменения и в размере их кристаллитов (рис. 2а).
Рис. 1.
Рентгеновские дифрактограммы образцов после осаждения Al(OH)3 в суспензии наночастиц ZrO2(YO1.5) (a), после их гидротермальной обработки при 480°C (б) и после их термообработки при 500°C (в). Кривые обозначены по содержанию YO1.5 (мол. %) в наночастицах ZrO2(YO1.5) (значения округлены до целых величин).
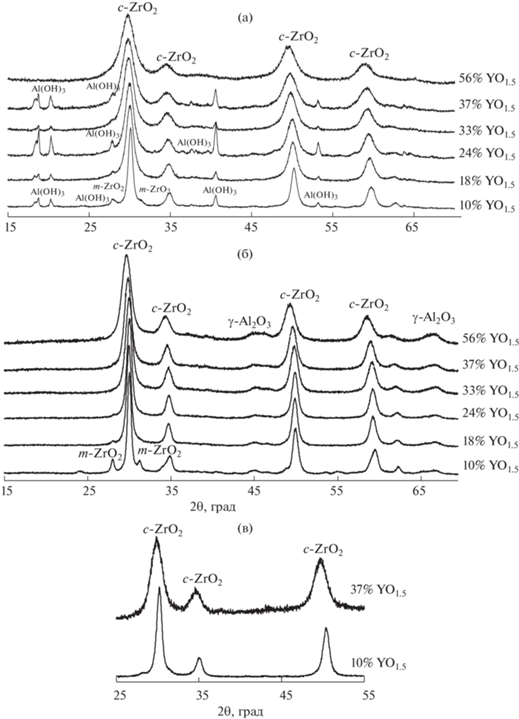
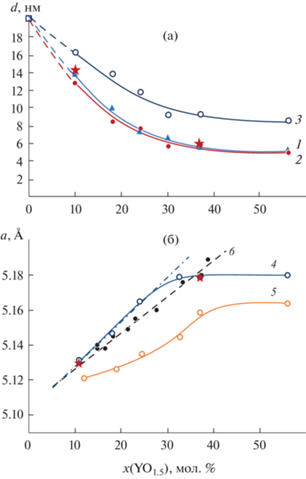
Рис. 2.
Зависимость размера кристаллитов (a) и параметра элементарной ячейки c-ZrO2(YO1.5) (б) от содержания оксида иттрия в системе: 1 – размеры кристаллитов c-ZrO2(YO1.5) исходных образцов; 2 – размеры кристаллитов c-ZrO2(YO1.5) после осаждения Al(OH)3; 3 – размеры кристаллитов c-ZrO2(YO1.5) в системе ZrO2(YO1.5)–AlO1.5 после гидротермальной обработки, квадратик – размер кристаллитов c-ZrO2 без оксида иттрия [28]; 4 – параметры элементарной ячейки c-ZrO2(YO1.5) исходных образцов; 5 – параметры элементарной ячейки c-ZrO2(YO1.5) в системе ZrO2(YO1.5)–AlO1.5 после гидротермальной обработки; 6 – параметры элементарной ячейки макрочастиц c-ZrO2(YO1.5) согласно [33, 34]; звездочки – параметры элементарной ячейки c-ZrO2(YO1.5) в системе ZrO2(YO1.5)–AlO1.5 после термообработки при t = = 500°C.
Размер кристаллитов c-ZrO2(YO1.5) уменьшается с увеличением содержания оксида иттрия в системе (рис. 2). Анализ зависимости распределения кристаллитов c-ZrO2(YO1.5) по размерам (рис. 3) свидетельствует о заметном сужении кривых распределения с увеличением содержания YO1.5 в системе, при этом значения средневзвешенного размера кристаллитов приблизительно соответствуют значениям, определенным по уширению линий рентгеновской дифракции с использованием формулы Шеррера.
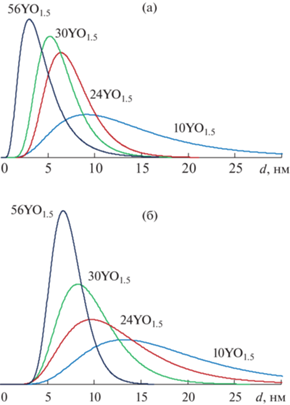
Рис. 3.
Распределение кристаллитов на основе c-ZrO2 по размерам: в системе ZrO2(YO1.5)–Al(OH)3 (a); в системе ZrO2(YO1.5)–Al2O3 (после гидротермальной обработки) (б). Кривые обозначены по содержанию YO1.5 (мол. %) в наночастицах ZrO2(YO1.5) (значения округлены до целых величин).
Значения параметров элементарной ячейки нанокристаллов на основе диоксида циркония с флюоритоподобной структурой, полученных в настоящей работе, возрастают с увеличением содержания оксида иттрия в системе. Если в диапазоне ~10–24 мол. % YO1.5 зависимость параметров элементарной ячейки c-ZrO2(YO1.5) от состава лежит приблизительно на прямой, то при бόльших количествах YO1.5 наблюдается резкое отклонение от прямолинейной зависимости (рис. 2б). На основании анализа представленной на рис. 2б зависимости можно сказать, что предельное содержание YO1.5 в нанокристаллах на основе диоксида циркония с флюоритоподобной структурой составляет около 27 мол. %. Не вошедший в структуру оксид иттрия, по-видимому, формирует аморфную фазу на поверхности наночастиц ZrO2(YO1.5). Подобный эффект отмечался в работах [26, 27].
Отклонение значений параметров элементарной ячейки нанокристаллов c-ZrO2(YO1.5) от значений параметров элементарной ячейки макроразмерных образцов [33, 34] (рис. 2б) может быть обусловлено особенностями метода синтеза, приводящими к присутствию в структуре нанокристаллов на основе c-ZrO2(YO1.5) OH–-групп, заполняющих анионные позиции вместо O2– для компенсации заряда при замещении ионов Zr4+ на ионы Y3+ [27, 35], и, как следствие, к увеличению параметров элементарной ячейки. Подтверждением этого может служить тот факт, что после термообработки данных наночастиц на воздухе при 500°C (т.е. при условиях, когда гидроксид алюминия разлагается с образованием аморфного оксида алюминия (рис. 1в) и наночастицы ZrO2(YO1.5) полностью теряют воду [27, 35]) значения параметров элементарной ячейки нанокристаллов c-ZrO2(YO1.5) практически не отличаются от значений параметров элементарной ячейки макроразмерных образцов того же состава (рис. 2б).
Гидротермальная обработка композиции ZrO2(YO1.5)–Al(OH)3 при 480°C, т.е. при температуре дегидратации с образованием AlO1.5 по данным [1, 29], приводит к исчезновению на дифрактограммах пиков, отвечающих гидроксиду алюминия (рис. 1б), т.е. происходит образование аморфной фазы, содержащей оксид алюминия. Вместе с тем следует отметить, что в образцах фиксируется некоторое повышение фона в области, которая совпадает с положением наиболее интенсивных рефлексов 400 и 440 γ‑Al2O3 (JCPDC 29-63). Кроме того, после гидротермальной обработки образца, содержащего 10.2 мол. % YO1.5, наблюдается небольшое увеличение интенсивности пиков, отвечающих моноклинной модификации диоксида циркония (рис. 1б). Для образцов, содержащих 18.1 и 24.3 мол. % YO1.5, такие рефлексы не обнаружены (рис. 1б). Количественная оценка соотношения фаз со структурой m-ZrO2 и c-ZrO2 представлена в табл. 1. Наблюдается также увеличение средних размеров кристаллитов c-ZrO2(YO1.5) в системе ZrO2(YO1.5)–AlO1.5 по сравнению с исходной (рис. 2а). Характер распределения кристаллитов по размерам тоже претерпевает заметное изменение (рис. 3). Во-первых, происходит смещение максимумов распределения в сторону более высоких значений размеров кристаллитов, что согласуется с данными об изменениях значений размеров кристаллитов, определенных по формуле Шеррера (рис. 2а). Во-вторых, после гидротермальной обработки при 480°C наблюдается уширение кривых распределения кристаллитов по размерам. Указанные изменения при гидротермальной обработке исходной композиции (ZrO2(YO1.5)–Al(OH)3, t = = 480°C) свидетельствуют о протекании в системе процесса массопереноса компонентов между частицами фазы на основе диоксида циркония. Следует отметить, что в случае гидротермальной обработки композиции “наночастицы ZrO2–Al(OH)3” при тех же условиях, т.е. без использования допанта – оксида иттрия, размер кристаллитов диоксида циркония в системе ZrO2–AlO1.5 не изменяется [1, 11, 17].
Помимо изменения размерных характеристик кристаллитов c-ZrO2(YO1.5), локализованных в рентгеноаморфной матрице, в ходе гидротермальной обработки композиции при t = 480°C наблюдается изменение параметров элементарной ячейки нанокристаллов на основе диоксида циркония с флюоритоподобной структурой (рис. 2б). Уменьшение параметров элементарной ячейки можно объяснить тем, что, во-первых, при более высокотемпературной гидротермальной обработке, как было показано в работах [27, 35], присутствующая в структуре вода покидает кристаллическую решетку, что приводит к уменьшению параметра а. Во-вторых, вследствие активного массопереноса через гидротермальный флюид происходит перераспределение оксида иттрия, первоначально локализованного как в структуре нанокристаллов c-ZrO2(YO1.5), так и на их поверхности [26, 27], между нанокристаллами c-ZrO2(YO1.5) и аморфной фазой, содержащей оксид алюминия. Отметим, что термообработка исходной композиции на воздухе при 500°C, т.е. до температуры плавления поверхностной (неавтономной) фазы [36, 37], когда межфазный перенос вещества заторможен [38–40], как показывают данные, приведенные на рис. 2 и в табл. 1, приводит лишь к незначительному увеличению средних размеров кристаллитов, а значения параметра элементарной ячейки нанокристаллов c-ZrO2(YO1.5) становятся равными (в пределах погрешности) соответствующим значениям макрокристаллов. Изменения в соотношениях фаз m-ZrO2 и c-ZrO2(YO1.5) также незначительны, а после разложения гидроксида алюминия образуется аморфная фаза на основе оксида алюминия, как и в исследованной в [1, 11, 32] композиции “наночастицы ZrO2–AlO1.5”. Причем переход оксида иттрия в аморфную фазу практически не наблюдается. Полученные значения по концентрации YO1.5 в аморфной фазе лежат в пределах погрешности расчета материального баланса в системе. Эти факты свидетельствуют об отсутствии при термообработке на воздухе при 500°C какого-либо существенного массопереноса между сосуществующими твердыми фазами, как и можно было ожидать на основании [38], в отличие от обработки исходной композиции в гидротермальных условиях, в которых массоперенос может осуществляться через гидротермальный флюид.
Поскольку растворение оксида иттрия в фазе на основе моноклинного диоксида циркония в рассматриваемом температурном диапазоне, по данным [30, 40], пренебрежимо мало, на основе баланса вещества в системе ZrO2(YO1.5)–AlO1.5 можно определить распределение компонентов между нанокристаллами c-ZrO2(YO1.5) и аморфной фазой после гидротермальной обработки при t = 480°C. Данные, приведенные в табл. 1, показывают, что с увеличением содержания YO1.5 в наночастицах на основе c‑ZrO2(YO1.5) в исходной композиции повышается доля оксида иттрия в аморфной фазе на основе оксида алюминия. Особенно это заметно для составов, в которых зависимость a(x(YO1.5)) отклоняется от прямолинейной (рис. 2б, кривая 1). Этот результат показывает, что в межфазном переносе вещества в системе ZrO2(YO1.5)–AlO1.5 в первую очередь участвуют компоненты, локализованные в аморфизированной оболочке на поверхности наночастиц ZrO2(YO1.5), затем происходит перенос оксида иттрия из нанокристаллов c-ZrO2(YO1.5) в аморфную фазу на основе оксида алюминия в процессе перекристаллизационного роста кристаллитов c-ZrO2(YO1.5). По-видимому, некоторое увеличение доли m-ZrO2 при этом связано с частичным выходом оксида иттрия из нанокристаллов c-ZrO2(YO1.5), приводящим к инициированию перехода фазы на основе диоксида циркония с флюоритоподобной структурой в фазу m-ZrO2, являющуюся равновесной при рассматриваемых условиях [30, 28, 32, 41 ]. Таким образом, наличие оксида иттрия в наночастицах ZrO2(YO1.5) кардинальным образом меняет характер процессов, протекающих в гидротермальных условиях в композитах “наночастицы ZrO2(YO1.5)–AlO1.5”, в отличие от процессов, наблюдавшихся в [1, 11, 17] в композитах “наночастицы ZrO2–AlO1.5”.
ЗАКЛЮЧЕНИЕ
Наличие оксида иттрия в наночастицах на основе диоксида циркония с флюоритоподобной структурой приводит к активной перекристаллизации нанокристаллов c-ZrO2(YO1.5) в системе ZrO2(YO1.5)–AlO1.5 в гидротермальных условиях. При этом оксид иттрия частично переходит из наночастиц ZrO2(YO1.5) в аморфную фазу на основе оксида алюминия. Наиболее активный перенос оксида иттрия между наночастицами ZrO2(YO1.5) и аморфной фазой наблюдается в случаях, когда оксид иттрия частично локализован на поверхности нанокристаллов c-ZrO2(YO1.5), т.е. при содержании YO1.5 в наночастицах ZrO2(YO1.5), большем ~27 мол. %.
Список литературы
Альмяшева О.В., Гусаров В.В. // Журн. неорган. химии. 2007. Т. 52. № 8. С. 1194. [Almjasheva O.V., Gusarov V.V. // Russ. J. Inorg. Chem. 2007. V. 52. № 8. P. 1194.] https://doi.org/10.1134/S0036023607080062
Malka I.E., Danelska A., Kimmel G. // Materials Today: Proceedings. 2016. V. 3. № 8. P. 2713. https://doi.org/10.1016/j.matpr.2016.06.018
Ульянова Т.М., Зуб Е.М., Крутько Н.П. // Поверхность. Рентгеновские, синхротронные и нейтронные исследования 2002. № 7. С. 49. [Ulyanova T.M., Zub E.M., Krutko N.P. // J. Surface Investigation. X-ray, Synchrotron and Neutron Techniques. 2002. № 7. С. 49.]
Mondal A., Ram S. // Mater. Lett. 2003. V. 57. P. 1696. https://doi.org/10.1016/S0167-577X(02)01054-6
Дудник Е.В., Шевченко А.В., Рубан А.К. и др. // Неорган. материалы. 2008. Т. 44. № 5. С. 586. [Dudnik E.V., Shevchenko A.V., Ruban A.K. et al. // Inorg. Mater. 2008. V. 44. № 5. P. 510.] https://doi.org/10.1134/S0020168508050142
Дудник Е.В., Шевченко А.В., Рубан А.К. и др. // Неорган. материалы. 2010. Т. 46. № 2. С. 212. [Dudnik E.V., Shevchenko A.V., Ruban A.K. et al. // Inorg. Mater. 2010. V. 46. № 2. P. 172.] https://doi.org/10.1134/S0020168510020159
Дудник Е.В., Цукренко В.В., Шевченко А.В. и др. // Неорган. материалы. 2011. Т. 47. № 10. С. 1217. [Dudnik E.V., Tsukrenko V.V., Shevchenko A.V. et al. // Inorg. Mater. 2011. V. 47. № 10. P. 1107.] https://doi.org/10.1134/S0020168511100050
Shi Z., Gao H., Wang X. et al. // Microporous Mesoporous Mater. 2018. V. 259. P. 26. https://doi.org/10.1016/j.micromeso.2017.09.0
Севастьянова И.Н., Саблина Е.Ю., Кульков С.Н. // Перспективные материалы. 2011. № 12. С. 455. https://elibrary.ru/download/elibrary_17561574_483-15865.pdf
Yan S., Wu D., Ma G. et al. // Ceram. Int. 2017. V. 43. № 17. P. 14742. https://doi.org/10.1016/j.ceramint.2017.07.21
Kuchuk I.S., Almjasheva O.V. // Nanosyst.: Phys. Chem. Math. 2012. V. 3. № 3. P. 123. http://nanojournal.ifmo.ru/wp-content/uploads/2012/07/NPCM_2012_3_3.pdf
Gandhi A.S., Jayaram V. // Acta Mater. 2003. V. 51. P. 1641. https://doi.org/10.1016/S1359-6454(02)00566-9
Guo Y., Hou B., Wang J. et al. // J. Fuel Chem. Technol. 2019. V. 47. № 5. P. 540. https://doi.org/10.1016/s1872-5813(19)30024-6
Hwang K.H., Zhao J., Kim J.H. et al. // Proc. Manuf. 2015 V. 2. P. 364. https://doi.org/10.1016/j.promfg.2015.07.064
Du W., AiY., He W. et al. // Ceram. Int. 2019. V. 46. № 6. P. 8452. https://doi.org/10.1016/j.ceramint.2019.12.080
Kao C.-T., Shen C.-H., Hsu H.-W. // Crystals. 2021. V. 11. № 8. P. 971. https://doi.org/10.3390/cryst11080971
Альмяшева О.В., Власов Е.А., Хабенский В.Б., Гусаров В.В. // Журн. прикл. химии. 2009. Т. 82. № 2. С. 224. [Al’myasheva O.V., Vlasov E.A., Khabenskii V.B., Gusarov V.V. // Russ. J. Appl. Chem. 2009. V. 82. № 2. P. 217.] https://doi.org/10.1134/S1070427209020104
Zhou J., Chang Q., Wang Y. et al. // Sep. Purif. Technol. 2010. V. 75. № 3. P. 243. https://doi.org/10.1016/j.seppur.2010.08.008
Li M., Yao M., Su Z. et al. // Ceram. Int. 2018. V. 44. № 17. P. 21428. https://doi.org/10.1016/j.ceramint.2018.08.202
Альмяшева О.В., Постнов А.Ю., Мальцева Н.В., Власов Е.А. // Nanosyst.: Phys. Chem. Math. 2012. V. 3. № 6. P. 75. http://nanojournal.ifmo.ru/wp-content/uploads/2013/01/NPCM2012-3_6.pdf
Yan S., Huang Y., Zhao D. et al. // Additive Manuf. 2019. V. 28. P. 120. https://doi.org/10.1016/j.addma.2019.04.024
Almjasheva O.V., Lomanova N.A., Popkov V.I. et al. // Nanosyst.: Phys. Chem. Math. 2019. V. 10. № 4. P. 428. https://doi.org/10.17586/2220-8054-2019-10-4-428-437
Смирнова Ж.Н., Гусаров В.В., Малков А.А. и др. // Журн. прикл. химии. 1995. Т. 68. № 12. С. 1950.
Tugova E.A., Krasilin A.A., Panchuk V.V. et al. // Ceram. Int. 2020. V. 46. № 15. P. 24526. https://doi.org/10.1016/j.ceramint.2020.06.239
Красилин А.А., Супрун А.М., Гусаров В.В. // Журн. прикл. химии. 2013. Т. 86. № 11. С. 1681. [Krasilin A.A., Suprun A.M., Gusarov V.V. // Russ. J. Appl. Chem. V. 86. № 11. P. 1633.] https://doi.org/10.1134/S1070427213110013
Альмяшева О.В., Смирнов А.В., Федоров Б.А. и др. // Журн. общ. химии. 2014. Т. 84. № 5. С. 710. [Almjasheva O.V., Smirnov A.V., Fedorov B.A. et al. // Russ. J. Gen. Chem. 2014. V. 84. № 5. P. 804.] https://doi.org/10.1134/S1070363214050028
Shuklina A.I., Smirnov A.V., Fedorov B.A. et al. // Nanosyst.: Phys. Chem., Math. 2020. V. 11. № 6. P. 729. https://doi.org/10.17586/2220-8054-2020-11-6-729-738
Пожидаева О.В., Корыткова Э.Н., Романов Д.П., Гусаров В.В. // Журн. общ. химии. 2002. Т. 72. № 6. С. 910. [Pozhidaeva O.V., Korytkova E.N., Romanov D.P., Gusarov V.V. // Russ. J. Gen. Chem. 2002. V. 72. № 6. P. 849.] https://doi.org/10.1023/a:1020409702215
Торопов Н.А., Барзаковский В.П., Лапин В.В., Курцева Н.Н. Диаграммы состояния силикатных систем. Справочник. Вып. 1. Л.: Наука, 1965. 546 с.
Диаграммы состояния систем тугоплавких оксидов: Справочник, Вып. 5. Двойные системы. Ч. 1. Л.: Наука, 1985. 284 с.
Lakiza S.N., Lopato L.M. // J. Am. Ceram. Soc. 1997. V. 80. № 4. P. 893. https://doi.org/10.1111/j.1151-2916.1997.tb02919.x
Альмяшева О.В., Гусаров В.В. // Физика и химия стекла. 2006. Т. 32. № 2. С. 224. [Almjashev O.V., Gusarov V.V. // Glass. Phys. Chem. 2006. V. 32. № 2. P. 162.] https://doi.org/10.1134/S1087659606020064
Dell'Agli G., Mascolo G. // J. Eur. Ceram. Soc. 2000. V. 20. № 2. P. 139. https://doi.org/10.1016/S0955-2219(99)00151-X
Strickler D.W., Carlson W.G. // J. Am. Ceram. Soc. V. 48. № 6. P. 286. https://doi.org/10.1111/j.1151-2916.1965.tb14742.x
Альмяшева О.В., Денисова Т.А. // Журн. общ. химии. 2017. Т. 87. № 1. С. 3. [Almjasheva O.V., Denisova T.A. // Russ. J. Gen. Chem. 2017. V. 87. № 1. P. 1.] https://doi.org/10.1134/S1070363217010017
Гусаров В.В., Суворов С.А. // Журн. прикл. химии. 1990. Т. 63. № 8. С. 1689. [Gusarov V.V., Suvorov S.A. // J. Appl. Chem. USSR. 1990. V. 63. № 8. P. 1560.]
Gusarov V.V. // Thermochim. Acta. 1995. V. 256. № 2. P. 467.
Гусаров В.В. // Журн. общ. химии. 1997. Т. 67. № 12. С. 1959. [Gusarov V.V. // Russ. J. Gen. Chem. 1997. V. 67. № 12. P. 1846.]
Гусаров В.В., Ишутина Ж.Н., Малков А.А., Малыгин А.А. // Докл. АН. 1997. Т. 357. № 2. С. 203. [Gusarov V.V., Ishutina Z.N., Malkov A.A., Malygin A.A. // Dokl. Akad. Nauk. 1997. V. 357. № 2. P. 203.]
Ломанова Н.А., Томкович М.В., Соколов В.В., Гусаров В.В. // Журн. общ. химии. 2016. Т. 86. № 10. С. 1605.] [Lomanova N.A., Tomkovich M.V., Sokolov V.V., Gusarov V.V. // Russ. J. Gen. Chem. 2016. V. 86. № 10. P. 2256. https://doi.org/10.1134/S1070363216100030
Yashima M., Kakihana M., Yoshimura M. // Solid State Ionics 1996. V. 86–88. P. 1131.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


