Журнал неорганической химии, 2022, T. 67, № 4, стр. 457-465
Получение люминофора CаTiO3:Pr3+ методом самораспространяющегося высокотемпературного синтеза
О. Б. Томилин a, Е. Е. Мурюмин a, *, М. В. Фадин a, С. Ю. Щипакин a
a Национальный исследовательский Мордовский государственный университет им. Н.П. Огарева
430005 Саранск,
ул. Большевистская, 68, Россия
* E-mail: mur_ee@mail.ru
Поступила в редакцию 21.02.2021
После доработки 14.10.2021
Принята к публикации 18.10.2021
- EDN: FWMPWP
- DOI: 10.31857/S0044457X22040195
Аннотация
Осуществлен самораспространяющийся высокотемпературный синтез образцов люминофора CaTiO3:Pr3+ с использованием теплового эффекта реакции взаимодействия титана с перхлоратом натрия. Изучено влияние источника кальция, содержания празеодима, а также соотношения Ti/TiO2 в шихте на люминесцентные характеристики синтезированного продукта. Фазовый состав продуктов синтеза определен методом рентгенофазового анализа, люминесцентные свойства охарактеризованы на основании спектров излучения. С помощью энергодисперсионного анализа установлен качественный и количественный состав люминофора.
ВВЕДЕНИЕ
В последнее время большое внимание уделяется разработке химически и термически стабильных, обладающих хорошими светотехническими характеристиками оксидных люминофоров красного свечения, которые приходят на смену традиционным сульфидным [1, 2] и фосфатным [3] люминофорам. Одним из таких перспективных материалов является титанат кальция, активированный Pr3+ (CaTiO3:Pr3+). Впервые о возможности использования CaTiO3:Pr3+ в качестве люминофора красного свечения было сообщено в работе [4]. Хорошая стойкость к электронному облучению высокой плотности и способность поддерживать эффективность люминесценции при длительном воздействии электрического заряда позволяют использовать CaTiO3:Pr3+ в качестве перспективного материала для светодиодных дисплеев, дисплеев на основе полевой эмиссии, плазменных панелей [5].
Люминесцентные свойства CaTiO3:Pr3+ хорошо изучены (см. работы [6–12]). При воздействии ультрафиолетовым (УФ) светом люминофор генерирует красное свечение с длиной волны излучения 612–615 нм. Координаты цветности люминофора (x = 0.68, y = 0.31) близки к “идеальному красному” [13, 14]. Люминесценция в красной области электромагнитного спектра является результатом 1D2→3H4 электронного перехода в ионах Pr3+ под действием УФ-излучения [6, 10]. Расширение области применения люминофора, а также улучшение его светотехнических характеристик возможно путем полной или частичной замены ионов Са2+ на ионы Zn2+ [6, 15], Ba2+ [16–19], Sr2+ [20–23], Ni2+ [24] и ионов Ti4+ на ионы Al3+ [25–27], Ln3+ (Ln = La, Lu, Gd) [28], Zr3+ [29, 30].
В настоящее время CaTiO3:Pr3+ получают в основном методом твердофазного спекания (см. обзор [31]), который является энергозатратным и характеризуется длительностью синтеза. Наноразмерные частицы люминофора CaTiO3:Pr3+, полученные золь–гель методом [32, 33], имеют лучшие светотехнические характеристики по сравнению с люминофором, полученным твердофазным спеканием, однако данный метод сложен в экспериментальном исполнении.
Одним из методов, который в определенной степени лишен указанных выше недостатков, является самораспространяющийся высокотемпературный синтез (СВС) [34]. Ранее данным методом были получены люминофоры CaAlSiN3:Eu2+ [35, 36], BaMgAl10O17:Eu2+ [37], Y3Al5O12:Ce3+ [38–40], Zn2SiO4:Mn2+ [40], YBO3:Eu3+ [40], (Ca,Sr,Ba)Al2O4:Eu2+ [41]. Самораспространяющийся высокотемпературный синтез люминофоров осуществляется в реакторе при повышенном давлении и в присутствии инертного газа. В работе [42] сообщалось о возможности использования для получения люминофора CaTiO3:Pr3+, Al3+ нитратно-цитратного метода горения, который является разновидностью СВС.
Цель настоящей статьи – получение люминофора красного свечения CaTiO3:Pr3+ методом СВС на воздухе при атмосферном давлении и исследование его люминесцентных свойств.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез люминофора CaTiO3:Pr3+
Для получения CaTiO3:Pr3+ методом СВС в качестве компонентов шихты использовали следующие соединения: CaO, CaCO3, Ti, TiO2, Pr(NO3)3 · 6H2O, NaClO4 марки “х. ч.”. Исходные реагенты смешивали в стехиометрическом соотношении в шаровой мельнице, затем полученную шихту насыпной плотности помещали в кварцевую лодочку. Процесс СВС инициировали волной горения вспомогательного состава (смесь BaO2 + Al). После прохождения волны горения продукт реакции охлаждали и измельчали.
Для проведения процесса СВС в данной работе использовали тепловой эффект экзотермической реакции (1) взаимодействия титана с перхлоратом натрия, для которой энтальпия реакции при стандартных условиях составляет –1916 кДж/моль (энтальпию реакции (1) рассчитывали по закону Гесса с учетом ${{\Delta }_{f}}H_{{298}}^{0}$ индивидуальных веществ, взятых из [43]):
(1)
${\text{2Ti + NaCl}}{{{\text{O}}}_{{\text{4}}}} \to {\text{2Ti}}{{{\text{O}}}_{{\text{2}}}}{\text{ + NaCl}}{\text{.}}$Получение конечного продукта можно описать схемой 1 , согласно которой кальций вводится в шихту в виде оксида кальция, и схемой 2 , где кальций вводится в виде карбоната кальция:
Схема 1 .
Схема 2 .
Сокращение ПП обозначает побочные продукты: N2, NO, NO2, O2, H2O, CO2.
Концентрация редкоземельного элемента в люминофоре может оказывать существенное влияет на его светотехнические характеристики. В связи с этим в схемах 1 и 2 для установления оптимального количества празеодима в люминофоре коэффициенты y1 и y2, отвечающие за содержание Pr в исходной шихте, принимали равными 0.001, 0.002, 0.005, 0.01 и 0.02 моль.
Варьирование стехиометрического соотношения Ti/TiO2 в исходной шихте изменяет температуру горения, что дает возможность регулировать процесс образования титаната кальция, активированного празеодимом. При протекании процесса СВС по схеме 1 значение стехиометрического коэффициента x1 изменяли в интервале от 0.3 до 0.5 моль с шагом 0.05 моль, а по схеме 2 значение стехиометрического коэффициента x2 изменяли от 0.7 до 0.9 моль с шагом 0.05 моль.
Для сравнения был получен образец люминофора CaTiO3:Pr3+ методом твердофазного спекания с содержанием празеодима в исходной шихте 0.002 моль. В этом случае готовили стехиометрическую смесь карбоната кальция, оксида титана и Pr(NO3)3 · 6H2O, которую смешивали в шаровой мельнице и затем помещали в муфельную печь. Твердофазное спекание проводили при температуре 1000°С в течение 4 ч в воздушной атмосфере, затем образующийся спек охлаждали и измельчали.
Методика экспериментальных исследований
Температуру горения измеряли вольфрам-рениевыми термопарами (ВР 5/20) диаметром 100 мкм. Сигналы от термопар непрерывно регистрировали с помощью четырехканального измерителя температуры Термодат-17.
Фазовый состав продуктов определяли методом рентгенофазового анализа (РФА) на рентгеновском дифрактометре Empyrean PANalytical c двухкоординатным детектором PIXcel3D, длина волны излучения λСuKα= 1.5418 Å, сканирование θ–2θ. Фазовый анализ проводили с использованием пакета обработки данных HighScore Plus и базы данных международного центра дифракционных данных ICDD PDF-2 (ICDD – International Centre for Diffraction Data; PDF – powder diffraction file).
Рентгеновский микроанализ и элементное картирование образцов проводили с использованием многофункционального растрового электронного микроскопа с интегрированной системой фокусированного ионного пучка Quanta 200 i 3D FEI со встроенным энергодисперсионным кремниевым дрейфовым детектором Apollo X.
Спектры фотолюминесценции были получены с использованием спектрофлуориметра RF-5301 PC (Shimadzu). В качестве источника возбуждения люминесценции использовали Xe-лампу мощностью 150 Вт.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рис. 1 представлены рентгенограммы образцов люминофора CaTiO3:Pr3+, полученного методами СВС и твердофазного спекания, которые сравнивали с рентгенограммами эталонных образцов из базы данных PDF-2. Как видно из рисунка, однофазный продукт образуется при получении люминофора методом твердофазного спекания и СВС по схеме 1 . При введении кальция в шихту в виде карбоната кальция в конечном продукте присутствует хлорид натрия, образующийся при разложении перхлората натрия.
Рис. 1.
Рентгенограммы образцов люминофора CaTiO3:Pr3+, полученного методом твердофазного спекания (а) и методом СВС по схеме 1 при введении кальция в шихту в виде оксида кальция и соотношении Ti : TiO2 = 0.3 : 0.7 (б) и по схеме 2 при введении кальция в шихту в виде карбоната кальция при соотношении Ti : TiO2 = 0.7 : 0.3 (в).
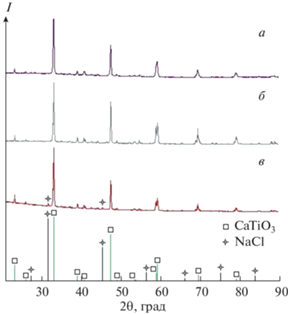
В процессе получения образцов по схемам 1 и 2 с помощью вольфрам-рениевой термопары были измерены максимальные температуры горения. При протекании СВС по схеме 1 температура горения достигала 1481°C, по схеме 2 – 1439°C. Поскольку при получении CaTiO3:Pr3+ по схеме 1 достигается температура, превышающая температуру кипения хлорида натрия (tкип(NaCl) = = 1465°C), NaCl полностью испаряется, и в итоге образуется однофазный продукт. При получении CaTiO3:Pr3+ по схеме 2 температура горения немного ниже, поэтому в конечном продукте обнаруживаются следы хлорида натрия.
На рис. 2 представлены результаты энергодисперсионного анализа (EDS) и элементное картирование однофазных образцов люминофора CaTiO3:Pr3+, полученных методами твердофазного спекания и СВС по схеме 1 . Как видно из рисунка, частицы люминофора имеют хорошую кристалличность, а элементы Сa, Ti, O и Pr, входящие в состав образцов, однородно распределены. Содержание элементов в образцах приведено в табл. 1. Результаты были получены усреднением измерений в 15 точках каждого образца. Согласно данным таблицы, содержание празеодима в люминофоре CaTiO3:Pr3+, полученном методом твердофазного спекания и методом СВС по схеме 1 , составляет 0.2 мас. %, что при пересчете соответствует ~0.002 моль.
Рис. 2.
Спектры EDS и элементное картирование образцов люминофора CaTiO3:Pr3+, полученного методом твердофазного спекания (а) и методом СВС по схеме 1 (б).
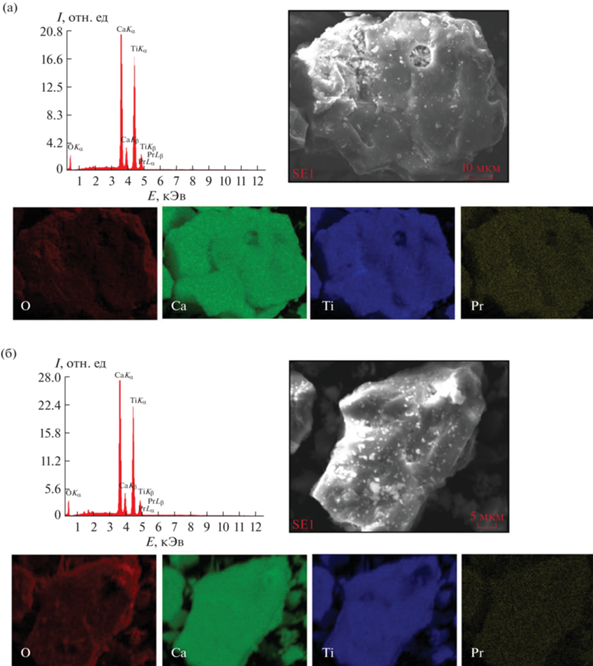
Таблица 1.
Содержание элементов (мас. %), по данным EDS-анализа, в образцах люминофора CaTiO3:Pr3+, полученного методом твердофазного спекания и методом СВС по схеме 1
| Метод | O | Ca | Ti | Pr |
|---|---|---|---|---|
| Твердофазное спекание | 35.2 | 30.5 | 34.1 | 0.2 |
| СВС по схеме 1 | 37.9 | 30.2 | 31.7 | 0.2 |
Для всех синтезированных образцов люминофора CaTiO3:Pr3+ были сняты спектры излучения люминесценции при длине волны возбуждения 330 нм. Максимум излучения люминесценции наблюдается при длине волны 614 нм, что соответствует длине волны излучения красного люминофора CaTiO3:Pr3+ [11].
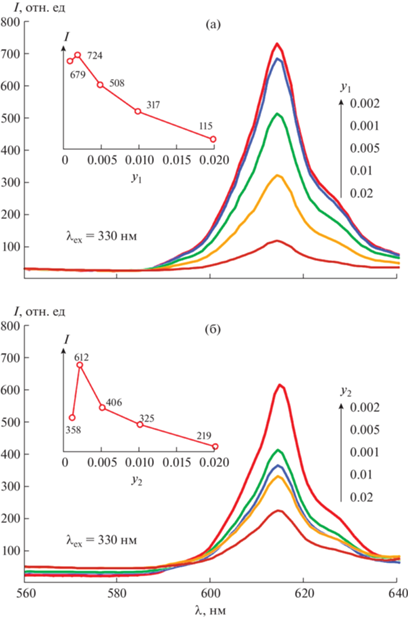
На рис. 3 представлены спектры излучения люминофора CaTiO3:Pr3+, полученного методом СВС по схемам 1 и 2 , в зависимости от содержания празеодима в исходной шихте. Независимо от источника введения кальция, максимальная интенсивность излучения соответствует количеству празеодима в шихте, равному 0.002 моль. При увеличении содержания празеодима выше указанного значения быстро происходит концентрационное тушение люминесценции. Полученный результат хорошо согласуется с выводами, сделанными в работе [12].
Рис. 3.
Спектры излучения люминофора CaTiO3:Pr3+, полученного методом СВС по схемам 1 (а) и 2 (б) в зависимости от содержания Pr (у1 и у2) в исходной шихте. На вставках показана зависимость интенсивности пика излучения при 614 нм от содержания Pr (у1 и у2) в исходной шихте.
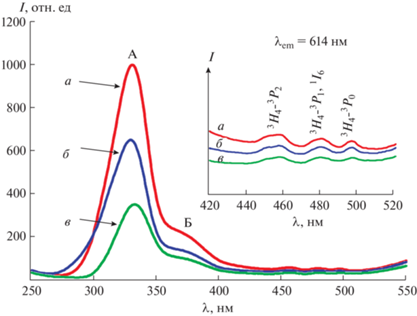
На рис. 4 представлены спектры возбуждения люминофора CaTiO3:Pr3+, полученного методом твердофазного спекания, а также методом СВС по схемам 1 и 2 , с оптимальным содержанием празеодима 0.002 моль. Спектр возбуждения содержит два широких пика, которые располагаются при 330 (А) и 370 нм (Б). Как было показано в [10], пик А возникает вследствие перехода электронов в матрице из валентной зоны в зону проводимости (Ti4+–O2– → Ti3+–O–), а пик Б – в результате межвалентного переноса заряда (Ti4+–O–Pr3+ → Ti3+–O–Pr4+). Спектр возбуждения люминофора CaTiO3:Pr3+ также содержит группу небольших пиков (см. вставку на рис. 4) при 458, 480 и 495 нм, которые соответствуют переходам 3H4–3P2, 3H4–3P1, 1I6 и 3H4–3P0 празеодима [10].
Рис. 4.
Спектры возбуждения люминофора CaTiO3:Pr3+, полученного методом СВС по схемам 1 (а) и 2 (б), а также методом твердофазного спекания (в). На вставке показан увеличенный участок спектра возбуждения в интервале от 420 до 520 нм.
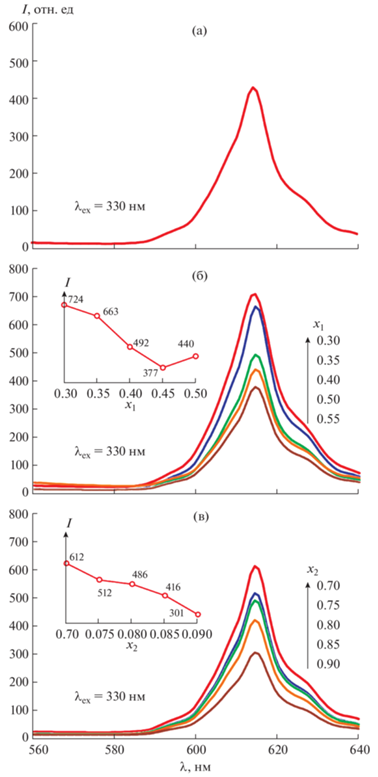
На рис. 5 представлены спектры излучения люминофора CaTiO3:Pr3+, полученного методом СВС по схемам 1 и 2 , с различным содержанием Ti в исходной шихте, а также люминофора, полученного методом твердофазного спекания, с оптимальным содержанием празеодима 0.002 моль. Как видно из рисунка, независимо от источника введения кальция в состав синтезируемого люминофора, при увеличении содержания Ti в шихте наблюдалось уменьшение относительной интенсивности люминесценции. Максимальная интенсивность излучения люминесценции соответствовала стехиометрическому соотношению Ti/TiO2, равному 0.3 : 0.7 при использовании оксида кальция и 0.7 : 0.3 при использовании карбоната кальция. При дальнейшем уменьшении содержания титана в шихте процесс СВС инициировать не удалось. Интенсивность излучения образцов люминофора, полученных по схеме 1 , выше, чем образцов, полученных по схеме 2 . Причиной этого может быть более высокая температура, достигаемая в случае синтеза люминофора по схеме 1 сравнению с синтезом по схеме 2 , а это способствует формированию более совершенной кристаллической структуры люминофора CaTiO3 : Pr3+. Из рис. 5 также видно, что интенсивность люминесценции люминофора, полученного методом СВС, выше, чем люминофора, полученного методом твердофазного спекания.
Рис. 5.
Спектры излучения люминофора CaTiO3:Pr3+, полученного методом твердофазного спекания (а), а также люминофора, полученного методом СВС по схемам 1 (б) и 2 (в) в зависимости от содержания Ti (х1 и х2) в исходной шихте. На вставках показана зависимость интенсивности пика излучения при 614 нм от содержания Ti (x1 и x2) в исходной шихте.
ЗАКЛЮЧЕНИЕ
Методом самораспространяющегося высокотемпературного синтеза получен люминофор CaTiO3:Pr3+ красного свечения. Методом РФА установлено, что однофазный продукт образуется при использовании в качестве компонента шихты оксида кальция. При введении в шихту карбоната кальция помимо основной фазы присутствует хлорид натрия. Методом EDS-анализа исследован качественный и количественный состав люминофора. Усредненное содержание празеодима в образцах люминофора, полученных методом твердофазного спекания и методом СВС при использовании в качестве компонента шихты оксида кальция, составляет 0.2 мас. %. Установлено, что максимальная интенсивность излучения соответствует концентрации празеодима в люминофоре, равной 0.002 моль. Независимо от источника кальция в шихте, при увеличении содержания Ti в шихте наблюдалось уменьшение интенсивности люминесценции образцов люминофора. Оптимальное стехиометрическое соотношение Ti/TiO2 при использовании в шихте оксида кальция равно 0.3 : 0.7, а при использовании карбоната кальция – 0.7 : 0.3.
Список литературы
Thiyagarajan P., Kottaisamy M., Sethupathi R., Rao M.S.R. // Displays. 2009. V. 30. № 4–5. P. 202. https://doi.org/10.1016/j.displa.2009.08.001
Ohnishi H. // Annu. Rev. Mater. Sci. 1989. V. 19. P. 83. https://doi.org/10.1146/annureV.ms.19.080189.000503
Steblevskaya N.I., Belobeletskaya M.V., Ustinov A.Yu., Medkov M.A. // Russ. J. Inorg. Chem. 2019. V. 64. № 2. P. 179. https://doi.org/10.1134/S0036023619020219
Vecht A., Smith D.W., Chadha S.S., Gibbons C.S. // J. Vac. Sci. Technol., B. 1994. V. 12. № 2. P. 781. https://doi.org/10.1116/1.587346
Takashima H., Shimada K., Miura N., et al. // Adv. Mater. 2009. V. 21. № 36. P. 3699. https://doi.org/10.1002/adma.200900524
Haranath D., Khan A.F., Chander H. // J. Phys. D. 2006. V. 39. № 23. P. 4656. https://doi.org/10.1088/0022-3727/39/23/009
Diallo P.T., Boutinaud P., Mahiou R., Cousseins J.C. // Phys. Status Solidi A: Appl. Res. 1997. V. 160. № 1. P.255. https://doi.org/10.1002/1521-396X(199703)160:1<255::AID-PSSA255>3.0.CO;2-Y
Tang W., Chen D. // J. Am. Ceram. Soc. 2007. V. 90. № 10. P. 3156. https://doi.org/10.1111/j.1551-2916.2007.01929.x
Zhang X., Zhang J., Ren X., Wang X.-J. // J. Solid State Chem. 2008. V. 181. № 3. P. 393. https://doi.org/10.1016/j.jssc.2007.11.022
Boutinaud P., Pinel E., Dubois M. et al. // J. Lumin. 2005. V. 111. № 1–2. P. 69. https://doi.org/10.1016/j.jlumin.2004.06.006
Zhang X., Zhang J., Wang M. et al. // J. Lumin. 2008. V. 128. № 5–6. P. 818. https://doi.org/10.1016/j.jlumin.2007.12.010
Nag Bhargavi G., Khare A. // Opt. Spectrosc. 2015. V. 118. № 6. P. 902. https://doi.org/10.1134/S0030400X15060156
Shionoya S., Yen W.M. Phosphor Handbook. Boca Raton: CRC Press, 1999.
Chadha S.S., Smith D.W., Vecht A., Gibbons C.S. // SID Digest. 1994. V. 1. P. 51.
Yu L., Xia M., Chen X. et al. // J. Mater. Res. 2013. V. 28. № 18. P. 2590. https://doi.org/10.1557/jmr.2013.225
Okamoto S., Yamamoto H. // J. Appl. Phys. 2002. V. 91. № 8. P. 5492. https://doi.org/10.1063/1.1458050
Fukuda D., Takebe H., Kuwabara M. // J. Am. Ceram. Soc. 2007. V. 90. № 8. P. 2670. https://doi.org/10.1111/j.1551-2916.2007.01811.x
Kang S.Y., Kim Y.H., Moon J. et al. // Jpn. J. Appl. Phys. 2009. V. 48. № 5R. P. 052301. https://doi.org/10.1143/JJAP.48.052301
Wang X., Xu C.N., Yamada H. et al. // Adv. Mater. 2005. V. 17. № 10. P. 1254. https://doi.org/10.1002/adma.200401406
Okamoto S., Yamamoto H. // J. Lumin. 2003. V. 102–103. P. 586. https://doi.org/10.1016/S0022-2313(02)00591-4
Okamoto S., Yamamoto H. // Appl. Phys. Lett. 2001. V. 8. № 5. P. 655. https://doi.org/10.1063/1.1343491
Kim J.S., Choi J.H., Cheon IIC., Byun J.D. // Ceram. Int. 2004. V. 30. № 7. 2029. https://doi.org/10.1016/j.ceramint.2003.12.200
Wang X., Xu C.N., Yamada H. // Jpn. J. Appl. Phys. 2005. V. 44. № 28–32. P. L912. https://doi.org/10.1143/JJAP.44.L912
Chen R., Gao Y., Gao Y. // Solid State Sci. 2019. V. 89. P. 161. https://doi.org/10.1016/j.solidstatesciences.2019.01.006
Jia W., Jia D., Rodriguez T. et al. // J. Lumin. 2006. V. 119–120. P. 13. https://doi.org/10.1016/j.jlumin.2005.12.067
Yin S.Y., Chen D.H., Tang W.J. // J. Alloys Compd. 2007. V. 441. № 1–2. P. 327. https://doi.org/10.1016/j.jallcom.2006.09.120
Tang J., Yu X., Yang L. et al. // Mater. Lett. 2006. V. 60. № 3. P. 326. https://doi.org/10.1016/j.matlet.2005.08.047
Zhang X.M., Zhang J.H., Zhang X. et al. // Chem. Phys. Lett. 2007. V. 434. № 4–6. P. 237. https://doi.org/10.1016/j.cplett.2006.12.023
Yan B., Zhou K. // J. Alloys Compd. 2005. V. 398. № 1–2. P. 165. https://doi.org/10.1016/j.jallcom.2004.08.109
Zhang J.C., Wang X.S., Yao Y. // J. Alloys Compd. 2010. V. 498. № 2. P. 152. https://doi.org/10.1016/j.jallcom.2010.03.138
Kaur J., Dubey V., Parganiha Y. et al. // Res. Chem. Intermed. 2015. V. 41. № 6. P. 3597. https://doi.org/10.1007/s11164-013-1475-7
Diallo P.T., Jeanlouis K., Boutinaud P. et al. // J. Alloys Compd. 2001. V. 323–324. P. 218. https://doi.org/10.1016/S0925-8388(01)01115-X
Meroni D., Porati L., Demartin F., Poelman D. // ACS Omega. 2017. V. 2. № 8. P. 4972. https://doi.org/10.1021/acsomega.7b00761
Pat. US 3726643 (publ. 1973). Synthesis of refractory inorganic compounds.
Chung S.-L., Huang S.-C. // Materials. 2014. V. 7. № 12. P. 7828. https://doi.org/10.3390/ma7127828
Chung S.-L., Huang S.-C. // Materials. 2016. V. 9. № 3. P. 178. https://doi.org/10.3390/ma9030178
Won C.W., Nersisyan H.H., Won H.I. et al. // J. Lumin. 2010. V. 130. № 4. P. 678. https://doi.org/10.1016/j.jlumin.2009.11.017
Won C.W., Nersisyan H.H., Won H.I., Youn J.W. // J. Lumin. 2010. V. 131. № 10. P. 2174. https://doi.org/10.1016/j.jlumin.2011.05.029
Ohyama J., Zhu C., Saito G. et al. // J. Rare Earths. 2018. V. 36. № 3. P. 248. https://doi.org/10.1016/j.jre.2017.06.014
Nersisyan H.H., Won H.I., Won C.W. et al. // Chem. Eng. J. 2012. V. 198. P. 449. https://doi.org/10.1016/j.cej.2012.05.085
Sathaporn T., Niyomwas S. // Energy Procedia. 2011. V. 9. P. 410. https://doi.org/10.1016/j.egypro.2011.09.045
Li S., Liang X. // J. Mater. Sci: Mater. Electron. 2008. V. 19. P. 1147. https://doi.org/10.1007/s10854-007-9502-3
Лидин Р.А., Андреева Л.Л., Молочко В.А. Константы неорганических веществ: справочник. М.: Дрофа, 2006.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


