Журнал неорганической химии, 2021, T. 66, № 9, стр. 1168-1175
О синтезе ферроцианидных сорбентов в полисахаридных матрицах
Л. А. Земскова a, *, А. М. Егорин a, Э. А. Токарь a
a Институт химии Дальневосточного отделения РАН
690022 Владивосток, пр-т 100-летия Владивостока, 159, Россия
* E-mail: zemskova@ich.dvo.ru
Поступила в редакцию 30.03.2021
После доработки 22.04.2021
Принята к публикации 30.04.2021
Аннотация
Систематизированы и обобщены данные, связанные с получением ферроцианидов переходных металлов – высокоселективных по отношению к цезию соединений – в полисахаридных матрицах (целлюлоза, хитин, хитозан). На основании данных электронной микроскопии установлено, что распределение сорбционно-активного компонента (ферроцианида никеля) в хитозановой матрице достаточно равномерное. Рассчитанные размеры кристаллитов, по данным рентгенофазового анализа, существенно выше для хитозанферроцианидного сорбента Zn–K, чем для хитозан-ферроцианидных сорбентов Ni–K и Cu–K. Проведен сравнительный анализ сорбционных свойств и устойчивости хитозанферроцианидных сорбентов Zn–K, Ni–K, Cu–K и сорбента марки Термоксид-35 при извлечении цезия из щелочных минерализованных растворов и морской воды.
ВВЕДЕНИЕ
Для очистки водных сред от радиоактивного цезия предложен ряд неорганических ионообменников, среди которых наиболее эффективны ферроцианиды (ФОЦ) переходных металлов. Однако использование порошков ферроцианидов в качестве сорбентов затруднительно, поскольку осадки ФОЦ легко пептизируются, а колонки, заполненные ими, имеют большое гидравлическое сопротивление. Использование подходящего носителя позволяет достичь большой механической прочности материала при малом гидравлическом сопротивлении, сохраняя при этом достаточно высокий коэффициент разделения [1].
Для синтеза композитных сорбентов используют как неорганические матрицы, так и полимеры (в качестве связующих), в том числе ионообменные смолы и природные биополимеры. Наиболее интересным неорганическим сорбентом является гранулированный ферроцианидный сорбент, получивший торговую марку Термоксид-35. Активным компонентом сорбента является ферроцианид никеля, который нанесен сорбционно-осадительным методом на устойчивый в щелочной среде гранулированный носитель – гидроксид циркония (ГЦ). Для этого гель-сферы ГЦ обрабатывают раствором сульфата никеля, а затем проводят осадительную обработку раствором ферроцианида калия с образованием в порах носителя микрокристаллов ферроцианида никеля [2, 3].
Примером композитного сорбента на основе органической матрицы (природного биополимера) является хитинсодержащий материал Микотон-Cs, полученный из высших грибов путем модификации хитин-меланин глюканового комплекса смешанным ФОЦ Cu–K, который осаждался на поверхности хитина в виде мелкокристаллического осадка [4]. К такому же типу материала можно отнести хитиновый сорбент Хизит-03 (в том числе в смеси с органическим связующим перхлорвинилом), полученный из панциря ракообразных, модифицированный ферроцианидом Cu–K [5].
В настоящее время наибольший фундаментальный и практический интерес представляет формирование наночастиц непосредственно в полимерных матрицах [6–9]. С этой точки зрения актуально исследование роста ферроцианидов в фиксирующих матрицах типа ПАН [10–12] или ионообменных смолах [13–18] и природных биополимерах. В связи с использованием последних определенный интерес представляет синтез ФОЦ в желатиновой матрице [19, 20].
Цель настоящей работы – получение и исследование сорбционных композиционных материалов на основе ферроцианидов переходных металлов путем их формирования в полисахаридной матрице, в частности, в природном биополимере хитозане.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали высокомолекулярный хитозан производства ЗАО “Восток-Бор” (ТУ 9289-092-00472124-99). Термоксид-35 – сферогранулированный неорганический сорбент на основе ферроцианида никеля на неорганическом носителе – гидроксиде циркония (содержание сорбционно-активного компонента 32–36 мас. %) – производства ЗАО “Термоксид” (TУ 6200-305-12342266–98).
Хлорид никеля(II) (NiCl2), сульфат меди(II) пятиводный (CuSO4 · 5H2O), хлорид цинка(II) (ZnCl2), ферроцианид калия трехводный (K4Fe(CN)6 · 3H2O), гидроксид натрия (NaOH) квалификации “х. ч.” были приобретены в фирме “НеваРеактив” и использованы без дополнительной очистки.
Композитные хитозанферроцианидные сорбенты (ХФС) получали путем введения в кислый раствор хитозана раствора соли переходного металла никеля(II) и последующего диспергирования полученной смеси в щелочной раствор ферроцианида калия либо, наоборот, щелочной раствор ферроцианида калия диспергировали в кислый раствор хитозана, содержащего соль никеля(II). Содержание сорбционно-активного компонента – ферроцианида переходного металла – в хитозанферроцианидных сорбентах составляет 60–80 мас. % [21].
Сорбционно-селективные характеристики ХФС в статических условиях оценивали с использованием реальной морской воды, предварительно помеченной радионуклидом 137Cs, при перемешивании в течение 24 ч. Соотношение объема морской воды к массе воздушно-сухой навески сорбента составляло 1000 мл/г. Морскую воду отделяли от сорбента на фильтре марки “синяя лента”, после чего определяли остаточную активность 137Cs. Десорбцию 137Cs проводили в статических условиях с применением раствора NH4NO3 c концентрацией 5 моль/л и объемом 50 мл (рН 4.5 ± 0.5), длительность десорбции составляла 24 ч. Предварительное замещение ${\text{NH}}_{4}^{ + }$ на Na+ позволяет повысить эффективность извлечения радионуклида, поэтому раствор NH4NO3, содержащий десорбированный 137Cs, нагревали до 70–80°С и постепенно, небольшими навесками, вносили сухой NaOH до прекращения выделения NH3 по реакции: NH4NO3 + NaOH → NaNO3 + NH3↑ + H2O. Значение рН обработанного элюата составляло 8–9.
Рентгенофазовый анализ (РФА) выполняли на дифрактометре D8 Advance с использованием программы поиска EVA с банком порошковых данных PDF-2. Рентгенограммы образцов записывали в диапазоне углов 2θ 3°–85° с шагом 0.02° при счете в точке 0.6 с.
Морфологию и распределение элементов в ХФС Ni–K определяли с помощью сканирующей электронной микроскопии (СЭМ) в сочетании с энергодисперсионным рентгеновским анализом. СЭМ-наблюдение проводили с помощью микроскопа Lyra3 ХМН (Tescan), оснащенного энергодисперсионным рентгеновским микроанализатором AZtec Energy Dispersive X-ray, автоматизированным детектором X-Max80detector (Oxford Instruments, Великобритания).
Содержание 137Cs определяли прямым радиометрическим методом с помощью гамма-радиометра РКГ-АТ1320 с детектором NaI (Tl) 63 × 63 мм (НПП Атомтех, Беларусь).
Размер частиц в композитах определяли по данным XRD с использованием уравнения Шеррера:
где β1/2 – уширение линии в радианах, θ – угол Брэгга, λ – длина волны рентгеновского излучения (CuKα, 1.5406 Å).РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Существует ряд известных работ, связанных с получением композиционных сорбентов, в которых в качестве подходящего носителя используют полисахаридные матрицы. В частности, целлюлозно-неорганические сорбенты АНФЕЖ получены путем иммобилизации смешанного ферроцианида Fe–K на поверхность гранул целлюлозы – наиболее распространенного растительного полисахарида [22, 23].
Однако проблема устойчивости целлюлозно-ферроцианидных сорбентов радикально может быть решена путем получения одностадийным методом целлюлозного волокна, объемно наполненного ФОЦ цинка и меди, когда формирование волокна и образование в его объеме ферроцианида переходного металла происходят одновременно [24, 25]. Один из способов синтеза состоит в том, что ферроцианид щелочного металла вводят в щелочной раствор целлюлозы, а соль тяжелого металла – в кислотную ванну, в которой происходит формирование волокна. Диффузия компонентов приводит одновременно с процессом регенерации целлюлозы к образованию фазы ферроцианида в объеме волокна. В работе [24] исследован волокнистый сорбент, содержащий ФОЦ цинка, который отличается простотой получения по сравнению с другими ФОЦ, так как именно сульфат цинка является обычным компонентом осадительной ванны, используемой при формировании вискозного волокна. Тот же принцип положен в основу получения целлюлозного волокна, объемно наполненного ФОЦ меди. Ферроцианид щелочного металла вносят в прядильный раствор медно-аммиачного комплекса целлюлозы, и в процессе формирования волокна образуется фаза ФОЦ меди [24]. Сорбенты были испытаны для дезактивации загрязненных вод и в процессе очистки молока от цезия.
Другим полисахаридом, который был использован для иммобилизации ферроцианидов переходных металлов, является хитин [26–28]. Несмотря на близость химического строения, он значительно превосходит целлюлозу по прочности и химической стойкости.
Иммобилизацию ФОЦ переходных металлов (Fe, Ni, Zn, Co, Cu) осуществляют при помощи производного хитина – хитозана, растворимого в кислых растворах, что позволяет применять растворные методы. Предварительно полученную по реакции двух прекурсоров (ФОЦ калия и сульфата переходного металла) суспензию вносят в раствор хитозана, затем из смеси хитозан/стабилизированная суспензия формируют гранулы в бане из жидкого азота [27] либо пену [28]. Перевод гранул или пены в хитин осуществляют реацетилированием аминогрупп хитозана.
Хитозан – полусинтетический продукт, который получают в результате деацетилирования хитина в щелочных условиях (концентрированным NaOH) или ферментативного гидролиза. Он является матрицей для иммобилизации неорганических компонентов [9, 29], в том числе ферроцианидов переходных металлов, так как обладает для этого необходимыми свойствами. Помимо низкой цены, прекрасных адсорбционных характеристик, а также биосовместимости, хитозан отличается способностью к модификации с возможностью получения новых материалов. С помощью физической модификации путем конверсии хитозанового порошка в гель (гранулы, мембраны, пленки и т.п.) или наночастицы можно увеличить его пористость, площадь поверхности, уменьшить его кристалличность и улучшить набухаемость и диффузионные свойства.
Химическая модификация может изменить подвижность (гибкость) и химическую стабильность хитозана (его производных) и уменьшить его растворимость в кислых средах. Химическая модификация включает прививку дополнительных групп или сшивку цепей полимера, которая осуществляется на функциональных группах, главным образом аминогруппах. Сшивка цепей полимера может быть выполнена методом гелирования с участием в качестве гелирующих агентов многозарядных ионов, в том числе ферроцианид- и феррицианид-ионов [30].
В литературе упоминается об использовании хитозановой смолы – сферогранулированных гранул из хитозана – для получения композитного ионообменника, состоящего из гексацианоферрата Cu–K, внедренного в матрицу хитозановой смолы [31, 32]. В этом случае предварительно проводят конверсию порошка хитозана в монодисперсные сферы, обладающие аморфизованной структурой вследствие переосаждения хитозана и повышенной сорбционной активностью по отношению к Cu(II). Гранулы насыщают медью и затем помещают в раствор K4[Fe(CN)6] с получением в фазе смолы смешанного ферроцианида K2Cu3[Fe(CN)6]2 [31].
В данной работе сорбенты получали в результате одновременного формирования ФОЦ переходного металла и осаждения хитозана в форме полиоснования. Для этого в кислый раствор хитозана вводили раствор соли переходного металла и диспергировали полученную смесь в щелочной раствор ФОЦ калия либо, наоборот, щелочной раствор ФОЦ калия добавляли в кислый раствор хитозана, содержащий хлорид никеля(II). Объемный осадок композитного материала фильтровали и сушили на воздухе при температуре 100°С с получением ксерогеля, содержащего ФОЦ переходного металла [21].
Поскольку образование неорганических компонентов в геле происходит с разной скоростью и, кроме того, осаждение хитозана (его щелочная коагуляция) и формирование комплексов идут в условиях, когда один компонент добавляется в избытке к другому, важно оценить, насколько равномерно идет формирование композиционного материала. СЭМ-изображения и карты распределения элементов, в том числе адсорбированного цезия, на поверхности частицы ХФС Ni–K (сорбент получен при мольном соотношении Ni2+ : [Fe(CN)6]4– = 3 : 1) приведены на рис. 1. Следует отметить некоторую неоднородность в распределении элементов никеля, железа и кислорода. Такая неоднородность может быть обусловлена несколькими причинами, в том числе вероятным образованием гидроксида никеля.
Рис. 1.
СЭМ-изображения во вторичных электронах поверхности композитного материала – ХФС Ni–K после сорбции Cs, энергодисперсионный спектр выделенного участка поверхности и карты распределения элементов для C, O, K, Fe, Ni и Cs.

Известно, что хитозан не сорбирует ионы щелочных металлов, следовательно, активным компонентом композитных сорбентов являются ФОЦ переходных металлов. К настоящему времени их ионообменные свойства, химическая и радиационная устойчивость достаточно хорошо изучены [33–37]. ФОЦ имеют цеолитную природу, и обменные катионы удерживаются в каналах или ячейках их кристаллической решетки за счет дисперсионных взаимодействий, имеющих неспецифический характер [34, 36]. Так, ФОЦ при несоответствии своей кристаллической структуры обменным катионам или почти не сорбирует их, или проявляет тенденцию к перестройке решетки в соответствии с требованиями поглощаемого катиона. В то же время у некоторых ФОЦ появляется способность сорбировать как небольшие по размерам ионы Na+, так и крупные ионы Cs+ и сохранять при этом почти без изменений кристаллическую решетку. В качестве примеров в работе [34] приведены ФОЦ Ni–K и ФОЦ Zn–K. Поскольку ионы Na+ и Cs+ различаются по величине эффективного радиуса более чем в 1.5 раза, предполагается, что удерживание в ячейках по существу одной и той же кристаллической решетки становится возможным вследствие участия при взаимодействии между обмениваемыми катионами и каркасом решетки молекул воды. У ФОЦ Ni–K и ФОЦ Cu–K, по-видимому, существует оптимальное соответствие размеров ячеек и ионов тяжелых щелочных металлов [34]. По этой причине для модификации хитин- и хитозансодержащих материалов выбраны ФОЦ переходных металлов (Ni, Cu, Zn, Co). В составе ФОЦ, иммобилизованных в пористый хитин, входят молекулы воды [27, 28].
Ионообменная емкость ФОЦ зависит от многих причин: от природы тяжелого металла, условий приготовления (прежде всего от соотношения реагирующих компонентов) и дальнейшей обработки полученных осадков. Немаловажное значение имеют условия применения и кислотность среды [1].
Рентгенограммы полученных хитозанферроцианидных сорбентов Ni–K, Cu–K и Zn–K приведены на рис. 2. С учетом данных химического анализа установлено, что в составе Ni-содержащего хитозанового сорбента могут присутствовать два соединения: смешанный ФОЦ K2Ni[Fe(CN)6] и простой – Ni2[Fe(CN)6]. Состав ферроцианидов переходных металлов, входящих в хитозанферроцианидные сорбенты, был установлен нами ранее в работах [38, 39] в сопоставлении с составом порошков чистых ферроцианидов переходных металлов.
Рис. 2.
Дифрактограммы композитных сорбентов: 1 – ХФС Zn–K, 2 – ХФС Ni–K, 3 – ХФС Cu–K, сорбенты получены при мольном соотношении M2+ : [Fe(CN)6]4– = 3 : 1.
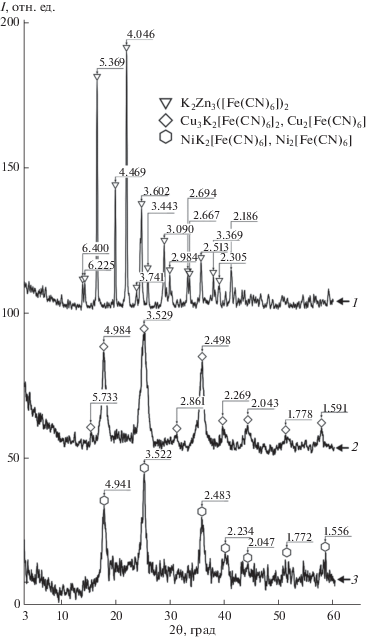
Наличие узких рефлексов на рентгенограмме ФОЦ Zn–K указывает на кристаллизацию в хитозане соли K2Zn3[Fe(CN)6]2 [40], близкой по структуре к цинковому комплексу, установленному в работе [27].
На основании данных РФА определены размеры областей когерентного рассеяния (далее размеры кристаллитов), значения которых приведены в табл. 1.
Таблица 1.
Размеры кристаллитов, оцененные на основании данных РФА
| Сорбент | Угол 2θ, град | Размер кристаллитов, нм |
|---|---|---|
| ХФС Zn–K | 13.7 16.4 19.7 21.8 |
32.73 36.48 41.22 36.77 |
| ХФС Ni–K | 17.8 25.4 |
8.05 7.40 |
| ХФС Cu–K | 17.9 25.2 |
6.17 8.69 |
Полученные сорбенты были испытаны для извлечения 137Cs из минерализованных щелочных сред [38, 39, 41] и морской воды [40]. Несмотря на устойчивость хитозана в щелочной среде, устойчивость композиционных хитозанферроцианидных сорбентов определяется природой металла, входящего в ФОЦ. В минерализованных щелочных средах ФОЦ никеля в хитозановой матрице (ХФС Ni–K) устойчивы до рН 13, тогда как ФОЦ меди разрушаются с повышением рН > 11 [38, 39].
С использованием ХФC Ni–K и ХФC Zn–K, обладающих разной способностью к концентрированию цезия и регенерации сорбента, была разработана двухстадийная схема концентрирования цезия из морской воды [40, 42]. Как следует из приведенных в табл. 2 данных, ХФС Zn–K менее эффективен, чем ХФС Cu–K и ХФС Ni–K, так как имеет наименьший коэффициент распределения (Кр) по отношению к цезию в морской воде. Однако он обладает способностью к регенерации, десорбция цезия нитратом аммония происходит практически полностью.
Таблица 2.
Cорбционно-селективные характеристики хитозанферроцианидных сорбентов в морской воде и их регенерация
| Параметр | ХФС Zn–K | ХФС Cu–K | ХФС Ni–K |
|---|---|---|---|
| Адсорбция 137Cs, % | 88.7 | 99.4 | 99.8 |
| Kр × 10–3, мл/г | 8 | 155 | 501 |
| Десорбция 137Cs, % | 98.2 | 63.7* | 8.1 |
| 49.3 | |||
| 28.8 |
Поэтому в предложенной схеме удаление цезия на первой ступени осуществляют сорбентом ХФС Zn–K, с него цезий десорбируют нитратом аммония, затем подщелачивают раствор и из щелочного элюата извлекают цезий наиболее устойчивым в щелочной среде ХФС Ni–K (табл. 3). Такая двухступенчатая схема позволяет достичь более высокой степени сжатия загрязненных отходов, чем при одноступенчатом извлечении цезия сорбентом ХФС Ni–K. При этом сорбент ХФС Ni–K проявляет неплохие характеристики в щелочном элюате даже по сравнению с сорбентом Термоксид-35 (табл. 3).
ЗАКЛЮЧЕНИЕ
При совершенствовании технологий очистки воды и разнообразных стоков, включая радиоактивные, от загрязняющих веществ отмечается тенденция к использованию нанопорошков в качестве сорбентов. Для создания новых поколений сорбентов прибегают к получению композиционных сорбционных материалов, в которых ультрадисперсные частицы (наночастицы) включены в матрицу “хозяина”. Это позволяет преодолеть трудности, препятствующие внедрению нанопорошков в технологии водоочистки, а именно: склонность частиц к агломерации, сложность отделения наноразмерных частиц от растворов, вероятность попадания наночастиц в окружающую среду с риском воздействия на живые организмы.
Использование порошков ферроцианидов в качестве сорбентов осложняется дополнительно тем, что они склонны к пептизации, не отличаются особенной устойчивостью, разрушаются и растворяются в очищаемых растворах. “Наполнение” ионообменных смол ферроцианидами переходных металлов – правильный подход к созданию сорбционных композитов. Однако смолы дороги, при формировании нужного состава ФОЦ трудно контролировать соотношения реагирующих фаз. Следование принципам “зеленой химии” предполагает замену устаревших и экологически “недружественных” полимеров на получаемые из возобновляемого природного сырья биополимеры: хитин, получаемый из него хитозан, производные целлюлозы [43]. Привлекательность методики синтеза ФОЦ в хитозане заключается не только в ее простоте, но и в возможности подстроить свойства конечного продукта под требования его конечного применения. Это возможно путем последующей химической модификации хитозана в составе композита или его термической обработки (нагрев, вымораживание и пр.). Как следует из рассмотренных литературных и собственных данных, проблема создания дешевых, стабильных композитов с высокодисперсными частицами ФОЦ может быть решена с использованием полисахаридов.
Список литературы
Тананаев И.В., Сейфер Г.Б., Харитонов Ю.Я. и др. Химия ферроцианидов. М.: Наука, 1971. 320 с.
Шарыгин Л.М., Боровкова О.Л., Калягина М.Л., Муромский А.Ю. // Радиохимия. 2013. Т. 55. № 1. С. 58. [Sharygin L.M., Borovkova O.L., Kalyagina M.L., Muromskiy A.Y. // Radiochemistry. 2013. V. 55. № 1. P. 91. https://doi.org/10.1134/S1066362213010177]
Шарыгин Л.М., Муромский А.Ю., Калягина М.Л. // Сорбц. хроматогр. процессы. 2006. Т. 6. Вып. 6. С. 965.
Косяков В.Н., Велешко И.Е., Яковлев Н.Г., Горовой Л.Ф. Получение, свойства и применение модификаций сорбента Микотон // Радиохимия. 2004. Т. 46. № 4. С. 356. [Kosyakov V.N., Veleshko I.E., Yakovlev N.G., Gorovoi L.F. // Radiochemistry. 2004. V. 46. № 4. P. 385. https://doi.org/10.1023/B:RACH.0000039117.10307.d0]
Селиверстов А.Ф. Сорбция хитином, хитозаном и хитинсодержащими материалами радиоактивных элементов из водных растворов: дис. … канд. хим. наук. М., 2004.
Помогайло А.Д., Джардималиева Г.И. Металлополимерные гибридные нанокомпозиты. М.: Наука, 2015. 494 с.
Zhang Y., Wu B., Xu H. et al. // NanoImpact. 2016. V. 3–4. P. 22. https://doi.org/http:10.1016/j.impact.2016.09.004
Sarkar S., Guibal E., Quignard F., SenGupta K. // J. Nanopart. Res. 2012. V. 14. P. 715. https://doi.org/10.1007/s11051-011-0715-2
Zhang L., Zeng Y., Cheng Z. // J. Mol. Liq. 2016. V. 214. P. 175. https://doi.org/10.1016/j.molliq.2015.12.013
Šebesta F. // J. Radioanal. Nucl. Chem. 1997. V. 220. P. 77. https://doi.org/10.1007/bf02035352
Someda H.H., ElZahhar A.A., Shehata M.K., El-Naggar H.A. // Sep. Purif. Technol. 2002. V. 29. P. 53. https://doi.org/10.1016/S1383-5866[02]00018-7
Nilchi A. // Appl. Radiat. Isot. 2007. V. 65. P. 482. https://doi.org/10.1016/j.apradiso.2006.12.003
Watari K., Imai K., Izawa M. // J. Nucl. Sci. Technol. 1967. V. 4. P. 190. https://doi.org/10.1080/18811248.1967.9732723
Watari K., Imai K., Ohmomo Y. et al. // J. Nucl. Sci. Technol. 1988. V. 25. P. 495. https://doi.org/10.1080/18811248.1988.9733618
Копырин А.А., Пяртман А.К., Кескинов В.А. и др. // Радиохимия. 1999. Т. 41. № 3. С. 236.
Копырин А.А., Пяртман А.К., Кескинов В.А. и др. // Радиохимия. 1999. Т. 41. № 3. С. 239.
Копырин А.А., Пяртман А.К., Кескинов В.А. и др. // Радиохимия. 2000. Т. 42. № 1. С. 78.
Valsala T.P., Roy S.C., Shah J.G. et al. // J. Hazard. Mater. 2009. V. 166. P. 1148. https://doi.org/10.1016/j.jhazmat.2008.12.019
Михайлов О.В. Желатин-иммобилизованные металлокомплексы. М.: Научный мир, 2004. 236 с.
Михайлов О.В. // Изв. АН. Сер. хим. 2008. № 1. С. 8.
Земскова Л.А., Егорин А.М., Сергиенко В.И. Способ получения композитных сорбентов, селективных к радионуклидам цезия. Пат. 2618705 РФ. № 2015140794; заявл. 24.09.2015; опубл. 11.05.2017 // БИ № 17.
Ремез В.П., Зеленин В.И., Смирнов А.Л. и др. // Сорбц. хроматогр. процессы. 2009. Т. 9. Вып. 5. С. 739.
Ремез В.П., Зеленин В.И., Смирнов А.Л. и др. // Сорбц. хроматогр. процессы. 2009. Т. 9. Вып. 6. С. 783.
Стрелко В.В., Яценко В.В., Марданенко В.К. и др. // Журн. прикл. химии. 1998. Т. 71. Вып. 8. С. 1295.
Тиньгаева Е.А., Глушанкова И.С., Зильберман М.В., Милютин В.В. // Журн. прикл. химии. 2012. Т. 85. Вып. 9. С. 1456.
Vincent T., Vincent C., Guibal E. // Molecules. 2015. V. 20. P. 20582. https://doi.org/10.3390/molecules201119718
Vincent T., Vincent C., Barré Y. et al. // J. Mater. Chem. A. 2014. V. 2. P. 10007. https://doi.org/10.1039/c4ta01128g
Vincent C., Hertz A., Vincent T. et al. // Chem. Eng. J. 2014. V. 236. P. 202. https://doi.org/10.1016/j.cej.2013.09.087
Shukla S.K., Mishra A.K., Arotiba O.A., Mamba B.B. // Int. J. Biol. Macromol. 2013. V. 59. P. 46. https://doi.org/10.1016/j.ijbiomac.2013.04.043
Racoviţă Ş., Vasiliu S., Popa M., Luca C. // Rev. Roum. Chim. 2009. V. 54. № 9. P. 709.
Румянцева Е.В., Велешко А.Н., Кулюхин С.А. и др. // Радиохимия. 2009. Т. 51. № 5. С. 434.
Велешко И.Е., Велешко А.Н., Румянцева Е.В. Способ. получения хитозансодержащего сорбента. Пат. 2430777 РФ. № 2010111261/05; заявл. 25.03.2010; опубл. 10.10.2011 // Б.И. № 28.
Вольхин В.В., Кощеева Е.А. // Неорган. материалы. 1968. Т. 4. № 6. С. 914.
Вольхин В.В., Шульга Е.А., Зильберман М.В. // Неорган. материалы. 1971. Т. 7. № 1. С. 77.
Вольхин В.В. // Неорган. материалы. 1979. Т. 16. № 6. С. 1086.
Вольхин В.В., Зильберман М.В., Колесова С.А. и др. // Журн. прикл. химии. 1975. Т. 48. № 1. С. 54.
Haas P.A. // Sep. Sci. Technol. 1993. V. 28. № 17–18. P. 2479. https://doi.org/10.1080/01496399308017493
Егорин А.М., Диденко Н.А., Кайдалова Т.А., Земскова Л.А. // Радиохимия. 2014. Т. 6. № 3. С. 234. [Egorin A.M., Didenko N.A., Kaidalova T.A., Zemskova L.A. // Radiochemistry. 2014. V. 56. № 3. P. 275. https://doi.org/10.1134/S1066362214030096]
Zemskova L., Egorin A., Tokar E., Ivanov V. // J. Sol-Gel Sci. Technol. 2019. V. 92. P. 459. https://doi.org/doi.org/10.1007/s10971-019-05019-x
EgorinA., Tokar E., Zemskova L. et al. // Sep. Sci. Technol. 2017. V. 52. P. 1983. https://doi.org/http:/10.1080/01496395.2017.1321669
Egorin A., Tokar E., Zemskova L. // Radiochim. Acta. 2016. V. 104. № 9. P. 657. https://doi.org/http:/10.1515/ract-2015-2536.
Егорин А.М., Токарь Э.А., Земскова Л.А. и др. Способ извлечения радионуклидов цезия из водных растворов. Пат. 2658292 РФ, заявл. 27.06.2017; опубл. 20.06.2018 // Б.И. № 17.
Кустов Л.М., Белецкая И.П. // Рос. хим. журн. 2004. Т. 48. № 6. С. 3.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


