Журнал неорганической химии, 2021, T. 66, № 8, стр. 1009-1016
ЭЛЕКТРОХИМИЧЕСКИЕ СВОЙСТВА ГОЛЛАНДИТА K1.5Fe1.5Ti6.5O16 С УГЛЕРОДНЫМ ПОКРЫТИЕМ
Н. В. Горшков a, *, Д. А. Михайлова b, М. А. Викулова a, М. В. Горбунов b, А. В. Гороховский a
a Саратовский государственный технический университет им. Ю.А. Гагарина
410054 Саратов, ул. Политехническая, 77, Россия
b Лейбницкий институт исследований твердого тела и материалов
01069 Дрезден, Гельмгольцштрассе, 20, Германия
* E-mail: gorshkov.sstu@gmail.com
Поступила в редакцию 07.02.2021
После доработки 13.03.2021
Принята к публикации 15.03.2021
Аннотация
Твердофазным методом синтезирован титанат калия, допированный железом, со структурой голландита. Для снижения контактного сопротивления и увеличения коэффициента диффузии ионов калия на поверхность полученного титаната в атмосфере аргона нанесено проводящее углеродное покрытие. Образование композиционного материала подтверждено методами рентгенофазового анализа, сканирующей электронной микроскопии и ИК-спектроскопии. Собранные на основе полученного композита полуячейки с металлическим калием в корпусе CR2025 подвержены электрохимическому тестированию с последующим расчетом удельной емкости, плотности мощности и плотности энергии. Установлено, что для малых скоростей развертки (1 и 3 мВ с–1) удельная емкость электрода с углеродным покрытием выше на 10–15%. Показано, что применение углеродных покрытий способствует увеличению коэффициента диффузии калия до 1.77 × 10–14 см2 с–1/2.
ВВЕДЕНИЕ
Совершенствование синтеза электродных материалов электрохимических накопителей энергии позволяет достичь величин удельной емкости, близких к теоретическим значениям [1–5]. С момента открытия литий-ионных аккумуляторов разработано большое число литийсодержащих положительных электродов различного состава. Последние достижения в этой области связаны с композитами LiFePO4–LiMn2O4 и LiFePO4–LiNi0.82Co0.18O2 [6] и LiTaO3 [7]. При этом альтернативой литию может быть калий как один из щелочных металлов, имеющих сходные физико-химические свойства и обильные запасы. Ионы калия обладают превосходными интеркалирующими/деинтеркалирующими свойствами в различных электроактивных материалах. Более того, потенциал калиевого анода, в отличие от натрия, наиболее близок к потенциалу литиевого анода. Следовательно, калиевые батареи могут использоваться в качестве устройства накопления альтернативной энергии, поэтому важно исследовать и разрабатывать для них новые эффективные электродные материалы [8–10].
Для электрохимических накопителей энергии применяются различные полупроводниковые сложные оксиды щелочных, щелочноземельных и переходных металлов с различной морфологией, среди которых многочисленные голландитоподобные материалы, в том числе на основе титана, привлекают внимание благодаря химической стабильности, биологической инертности, ионообмену и хорошей ионной проводимости [11], что позволяет разработать серию новых функциональных керамических материалов [12]. Многие работы направлены на исследование возможности использования калийсодержащих структур на основе TiO2 как электродных материалов с более высокой электрохимической емкостью (табл. 1).
Для материалов со столбчатой морфологией, которой зачастую обладают голландитоподобные соединения, при соотношении длины к диаметру >10 задача равномерного распределения электронного контакта по объему трехкомпонентного (активный материал–электронный проводник–полимерное связующее) электродного материала становится технологически сложной. Известны такие решения, как применение углеродных нанотрубок, сложный и многостадийный помол и др.
Титанаты калия со структурой голландита имеют высокую подвижность ионов калия в каналах титан-кислородных октаэдров, но при этом обладают низкой электропроводностью (до 10–8 См/см) [17, 18]. Варьирование методов и режимов синтеза голландита K1.5Fe1.5Ti6.5O16 позволяет получать частицы столбчатой морфологии различного размера и чистоты [18–23]. В рамках настоящей работы предлагается использовать гетероструктурированный материал на основе голландита состава K1.5Fe1.5Ti6.5O16 с углеродным покрытием.
В связи с этим целью работы является исследование электрохимических свойств материала состава K1.5Fe1.5Ti6.5O16 (KFTO(H)) со структурой голландита с углеродным покрытием, полученного с использованием электропроводящей сажи (Carbon Black (CB)).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез голландита KFTO(H) проводили по методике, описанной в работе [23], в расплаве KCl (Sigma-Aldrich) при 1200°C для стехиометрической смеси TiO2 (Sigma-Aldrich) и Fe2O3 (Sigma-Aldrich). Структуру и состав синтезированного голландита изучали методом рентгенофазового анализа (РФА) на дифрактометре ARL X’tra марки “Thermo Sciencific” (Швейцария).
Голландит с углеродным покрытием (KFTO(H)/CB) получали обработкой сухой смеси порошка KFTO(H) (95 мас. %) и сажи CB (5 мас. %) в атмосфере сухого аргона в кварцевой трубке со скоростью потока 10 л/мин в течение 10 ч при температуре 600°C аналогично методике [24]. При этом массовая доля углерода 5% для получения образцов KFTO(H)/CB была выбрана по аналогии с работой [25]. Исследование поверхности и структуры полученных материалов осуществляли при помощи сканирующего электронного микроскопа со встроенной системой для энергодисперсионного анализа EXplorer (Aspex Corporation).
Полуячейки с металлическим калием и электродом на основе KFTO(H) и KFTO(H)/CB были собраны в корпусе coin cell CR2025. Электродная масса состояла из восьми частей KFTO(H) или KFTO(H)/CB, одной части CB и одной части поливинилиденфторида (Sigma-Aldrich) и была нанесена на стальные сетки методом подпрессовки. Сепаратор Whatman (Sigma-Aldrich) был пропитан электролитом – 1М раствором KPF6 (Sigma-Aldrich) в пропиленкарбонате.
Термогравиметрические исследования проводили на приборе синхронного термического анализа Netzsch SDT 449 F3 Jupiter. Проводили электрохимическое тестирование образцов. Циклические вольтамперограммы получали с помощью потенциостата Bio-logic FRA Biologic SP-300 по двухэлектродной схеме. Из результатов циклических вольтамперограмм оценивали удельную емкость одного электрода по уравнению (1):
(1)
${{C}_{{{\text{эл}}}}} = \frac{{\mathop \smallint \nolimits^ Idv}}{{mV\Delta v}},{\text{\;Ф }}{{{\text{г}}}^{{ - 1}}},$Для расчета плотности мощности и плотности энергии использовали соответственно уравнения (2) и (3) с учетом ранее рассчитанной удельной емкости (Ф/г):
(2)
$E = \frac{{{{C}_{{{\text{эл}}}}}\Delta {{V}^{2}}}}{{7.2}},{\text{\;Вт ч к}}{{{\text{г}}}^{{ - 1}}},$Вклад диффузионной составляющей емкости и емкости двойного электрического слоя оценивали по коэффициентам уравнения для силы тока:
где a – коэффициент поверхностных емкостных эффектов, b – коэффициент процессов интеркаляции-деинтеркаляции, контролируемых диффузией.Для анализа использовали график, соответствующий зависимости:
где тангенс угла наклона прямолинейной зависимости графика (вставки на рис. 5а и 5б) соответствует коэффициенту b процессов интеркаляции-деинтеркаляции, контролируемых диффузией, а отрезок a – коэффициент поверхностных емкостных эффектов.Путем подстановки значений скорости развертки вольтамперограмм были определены процентные доли диффузионных и емкостных процессов в общей емкости электродного материала.
Электрохимическая импедансная спектроскопия была выполнена при помощи импедансметра Z1000P (ООО “Элинс”) в двухэлектродной схеме с наложением потенциала 1.3 В при переменном напряжении амплитудой 50 мВ в диапазоне частот от 100 мГц до 100 кГц.
Коэффициент диффузии ионов калия в электродном материале рассчитывали по формуле [26, 27]:
где R – постоянная Больцмана; T – температура, K; A – площадь электрода, см2; n – количество электронов; F – постоянная Фарадея; C – количество ионов K+ в электроде, моль; W – элемент Варбурга, Ом с–1/2.РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Состав и структура синтезированного голландита K1.5Fe1.5Ti6.5O16 подтверждены методом РФА (рис. 1).
На дифрактограмме полученного образца присутствуют все рефлексы, характерные для структуры голландита: 87, пр. гр. I4/m. Присутствующая вторичная фаза относится к диоксиду титана в модификации рутил, величина которой оценена в ~2%. На дифрактограмме KFTO(H)/CB имеются два рефлекса между углами 2θ = 12.0° и 12.5°, которые можно отнести к образовавшемуся слою углеродного покрытия на поверхности голландита. Согласно данным [24, 25], аналогичные углеродные покрытия имеют слоистую структуру, что может отразиться на рентгенограмме. Учитывая положение появившихся пиков, можно высказать предположение о расстоянии между слоями и соотнести его с оксиграфеновыми структурами. Так, рефлекс на меньших углах, соответствующий межслоевому расстоянию 7.23 Å, относится к внешним слоям углерода и соответствует увлажненному оксиду графена, а рефлекс на больших углах, вероятно, относится к слоям, непосредственно контактирующим с голландитом и имеющим более плотную структуру и меньшее межслоевое расстояние 7.10 Å (001). При этом природа и структура покрытий на основе углерода на голландите требуют дальнейшего изучения.
Частицы базового материала со структурой голландита (KFTO(H)) имеют столбчатую морфологию со следующими размерами: диаметр от 100 нм до 1.5 мкм, длина от 3 до 15 мкм, при этом отношение длины к диаметру составляет ~15. После нанесения углеродного покрытия морфология базового материала сохраняется, за исключением увеличения числа частиц меньшего размера. Это связано с активным ростом площади углеродного покрытия на поверхности голландита, вследствие чего происходит разрушение крупных агломератов на более мелкие (рис. 2).
Рис. 2.
Сканирующие электронные микрофотографии исходного голландита (а) и голландита с нанесенным углеродным покрытием (б).

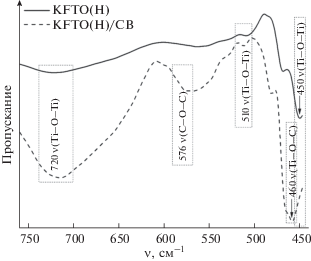
ИК-Фурье-спектр пропускания KFTO(H)/CB (рис. 3) имеет полосу поглощения при ~458 см–1, что соответствует колебаниям связей Ti–O–C, подтверждая образование композита.
В отличие от KFTO(H), на кривой ДТА KFTO(H)/CB (рис. 4а, 4б) наблюдается эндотермический пик при ~530°С, которому соответствует потеря массы 5.82%, что указывает на наличие углеродного покрытия и отсутствие потерь массы CB в процессе его формирования.
Рис. 4.
Кривые ТГ/ДСК термического поведения голландита KFTO(H) до (а) и после (б) нанесения углеродного покрытия.
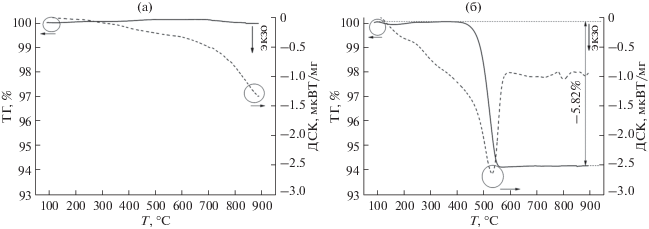
Рис. 5.
Электрохимические характеристики электрода на KFTO(H). Циклические вольтамперограммы при разных скоростях развертки потенциала KFTO(H) (а) и KFTO(H)/CB (б). Зависимость удельной емкости от скорости развертки потенциала циклических вольтамперограмм (в). Вклад емкости двойного электрического слоя и диффузионной составляющей от скорости развертки потенциала циклических вольтамперограмм (г).
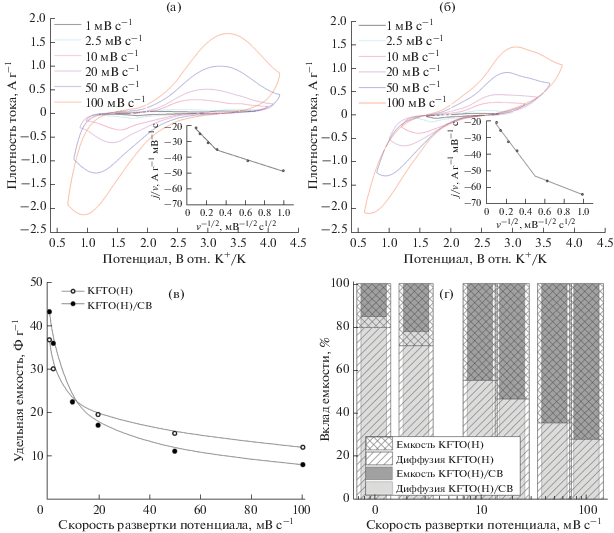
Вольтамперограммы (рис. 5а, 5б) имеют пики, характерные для обратимых процессов заряда и разряда электрода. Пики на вольтамперограммах ниже потенциала 2.0 В относительно K+/K отвечают интеркаляции калия в состав голландита и восстановлению железа. При этом обратный процесс протекает при потенциалах выше 2.0 В, смещение пиков в зависимости от скорости развертки указывает на наличие диффузионной составляющей, что типично для интеркаляционных процессов. Проведен анализ величин пиков тока при потенциалах ниже 2.0 В в координатах отношение плотности тока к скорости развертки потенциала от скорости развертки потенциала в степени –1/2; при этом наблюдаются участки с двумя наклонами. Для расчета проанализирован участок более высоких скоростей развертки потенциала, для которого вклад емкости двойного электрического слоя максимален (вставки на рис. 5а, 5б), что позволило разделить вклад емкости двойного электрического слоя и диффузионной составляющей емкости (рис. 5г). Углеродное покрытие увеличивает удельную емкость электродов для малых скоростей развертки: для 1 и 3 мВ с–1 удельная емкость электрода с углеродным покрытием выше на 10–15%, для 10 мВ с–1 значения удельной емкости близки для двух типов электродов, а для высоких скоростей (20, 50 и 100 мВ с–1) удельная емкость электродов без покрытия на 10–20% выше (рис. 5в). При этом электродную реакцию можно записать следующим образом:
Годографы импеданса электродов на основе допированного железом титаната калия со структурой голландита (рис. 6а) имеют два участка: полуокружность на средних частотах и наклонный луч на низких частотах. Импеданс ячеек можно интерпретировать схемой с последовательным сопротивлением (Rs), контактным сопротивлением электрода (Rct), элементом постоянной фазы (CPE) и элементом Варбурга (W) (вставка на рис. 6а). Низкочастотный импеданс лимитирован диффузионной составляющей, что демонстрирует наклон линейных участков реальной составляющей импеданса от угловой частоты в степени –1/2 (рис. 6б). Углеродное покрытие на KFTO(H) позволяет снизить удельное контактное сопротивление в 2.95 раза, диффузионный импеданс – элемент Варбурга – в 1.43 раза, что приводит к увеличению коэффициента диффузии ионов калия в 2.06 раза (табл. 2). При этом удельная энергия электрода на основе KFTO(H) составляет 62.1 Вт ч кг–1 для скорости развертки потенциала 1 мВ с–1, а для KFTO(H)/CB – 73.5 Вт ч кг–1. Удельная мощность электрода на основе KFTO(H) составляет 1060 Вт кг–1 для скорости развертки потенциала 100 мВ с–1, а для KFTO(H)/CB – 710 Вт кг–1. Это свидетельствует о том, что углеродное покрытие увеличивает энергетические параметры электрода, делая диффузию ионов калия более эффективной, но при этом часть открытых калиевых каналов голландита становится недоступной для быстрого обратимого ионного обмена с электролитом, что уменьшает мощностные характеристики электрода на высоких скоростях изменения потенциала.
Рис. 6.
Годографы импеданса при потенциале 1.3 В относительно K+/K (а). Зависимость реальной составляющей импеданса Z' от ω–1/2 для низкочастотной области (б).
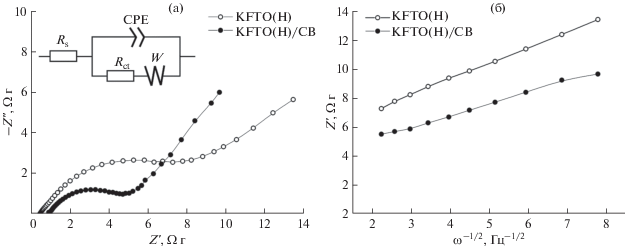
Таблица 2.
Кинетические параметры электродов на основе KFTO(H) при потенциале 1.3 В относительно K+/K
| № п/п | Материал электрода | Rct, Ω г | W, Ω с–1/2 г | ${{D}_{{{{{\text{K}}}^{ + }}}}},$ см2 с–1/2 |
|---|---|---|---|---|
| 1 | KFTO(H) | 7.70 | 3.91 | 0.86 × 10–14 |
| 2 | KFTO(H)/CB | 2.61 | 2.73 | 1.77 × 10–14 |
Полученные характеристики значительно уступают таковым для литий-ионных аналогов, что объясняется большим размером частиц голландита и низкой подвижностью ионов калия. Для дальнейших работ следует значительно уменьшить размер частиц, используя альтернативные методы синтеза. При этом голландитные структуры перспективны для использования в накопителях электрохимической энергии за счет своей высокой стабильности и ионной проводимости в каналах.
ЗАКЛЮЧЕНИЕ
Твердофазным методом синтезирован допированный железом титанат калия со структурой голландита, состав и структура которого подтверждены методом РФА. В атмосфере аргона на частицы KFTO(H) столбчатой морфологии нанесено углеродное покрытие для снижения контактного сопротивления. Его наличие наблюдается на сканирующих электронных микрофотографиях. Образование композиционного материала доказано с помощью ИК-спектроскопии – появлением полос поглощения, соответствующих связям Ti–O–C. Для электрохимического тестирования полученный композит собран в полуячейки с металлическим калием в корпусе CR2025. Показано, что углеродное покрытие на допированном железом титанате калия со структурой голландита способствует увеличению коэффициента диффузии ионов калия.
Список литературы
Ma Z., Huang X., Dou S. et al. // J. Phys. Chem. C. 2014. V. 118. № 31. P. 17231. https://doi.org/10.1021/jp502226j
Yue L., Zhang S., Zhao H. et al. // J. Alloys Compd. 2018. V. 765. P. 1263. https://doi.org/10.1016/j.jallcom.2018.06.283
Long C., Wei T., Yan J. et al. // ACS nano. 2013. V. 7. № 12. P. 11325. https://doi.org/10.1021/nn405192s
Zhu Y., Song K., Shen S. et al. // J. Alloys Compd. 2021. V. 856. P. 157992. https://doi.org/10.1016/j.jallcom.2020.157992
Шабалина А.В., Шарко Д.О., Корсакова Д.Р. и др. // Журн. неорган. химии. 2020. Т. 65. № 2. С. 271. https://doi.org/10.31857/S0044457X20020142
Медведева А.Е., Печень Л.С., Махонина Е.В. и др. // Журн. неорган. химии. 2019. Т. 64. № 7. С. 677. https://doi.org/10.1134/S0044457X19070122
Палатников М.Н., Щербина О.Б., Маслобоева С.М. и др. // Журн. неорган. химии. 2020. Т. 65. № 3. С. 413. [Palatnikov M.N., Shcherbina O.B., Masloboeva S.M., Efremov V.V. // Russ. J. Inorg. Chem. 2020. V. 65. № 3. P. 440.]https://doi.org/10.1134/S0036023620030109
Li D., Guo W., Li Y. et al. // J. Power Sources. 2019. V. 413. P. 34. https://doi.org/10.1016/j.jpowsour.2018.11.088
Kapaev R.R., Obrezkov F.A., Stevenson K.J. et al. // Chem. Commun. 2019. V. 55. № 78. P. 11758. https://doi.org/10.1039/C9CC05745E
Tang Y., Li Y., Guo W. et al. // J. Mater. Chem. A. 2018. V. 6. № 2. P. 623. https://doi.org/10.1039/C7TA09590B
Yadav M.K., Kothari A.V., Gupta V.K. // Dyes and Pigments. 2011. V. 89. № 2. P. 149. https://doi.org/10.1016/j.dyepig.2010.10.004
Ebinumoliseh I., Grosvenor A.P. // Inorg. Chem. 2018. V. 57. № 22. P. 14353. https://doi.org/10.1021/acs.inorgchem.8b02464
Noailles L.D., Johnson C.S., Vaughey J.T. et al. // J. Power Sources. 1999. V. 81. P. 259. https://doi.org/10.1016/S0378-7753(98)00244-4
Han J., Xu M., Niu Y. et al. // Chem. Commun. 2016. V. 52. № 75. P. 11274. https://doi.org/10.1039/C6CC05102B
Zhang Q., Guo Y., Guo K. et al. // Chem. Commun. 2016. V. 52. № 37. P. 6229. https://doi.org/10.1039/C6CC01057A
Gutiérrez-Flórez M.T., Kuhn A., Garcıa-Alvarado F. // Int. J. Inorg. Mater. 1999. V. 1. № 1. P. 117. https://doi.org/10.1016/S1463-0176(99)00018-6
Gorshkov N., Vikulova M., Gorbunov M. et al. // Ceram. Int. 2021. V. 47. № 4. P. 5721. https://doi.org/10.1016/j.ceramint.2020.10.158
Gorokhovsky A.V., Tretyachenko E.V., Goffman V.G. et al. // Inorg. Mater. 2016. V. 52. P. 587. https://doi.org/10.1134/S0020168516060042
Hayashi F., Furui K., Shiiba H. et al. // Front. Chem. 2020. V. 8. P. 714. https://doi.org/10.3389/fchem.2020.00714
Kong X., Wang X., Ma D. et al. // Mater. Lett. 2019. V. 237. P. 145. https://doi.org/10.1016/j.matlet.2018.11.091
Ramakrishna S., Mahender N., Reddy J.R. et al. // Indian J. Chem. 2015. V. 54A. P. 1026. http://nopr.niscair.res.in/handle/123456789/32002
Liu W., Yi H., Zheng Q. et al. // J. Mater. Chem. A. 2017. V. 5. № 22. P. 10928. https://doi.org/10.1039/C7TA03133E
Moetakef P., Larson A.M., Hodges B.C. et al. // J. Solid State Chem. 2014. V. 220. P. 45. https://doi.org/10.1016/j.jssc.2014.08.012
Su L., Jing Y., Zhou Z. // Nanoscale. 2011. V. 3. № 10. P. 3967. https://doi.org/10.1039/C1NR10550G
Fedotov S.S., Luchinin N.D., Aksyonov D.A. et al. // Nat. Commun. 2020. № 11. P. 1484. https://doi.org/10.1038/s41467-020-15244-6
Hassan Q.U., Yang D., Zhou J.P. et al. // Inorg. Chem. 2018. V. 57. № 24. P. 15187. https://doi.org/10.1021/acs.inorgchem.8b02481
Liang X., Ou X., Zheng F. et al. // ACS Appl. Mater. Interf. 2017. V. 9. № 15. P. 13151. https://doi.org/10.1021/acsami.7b00818
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии