Журнал неорганической химии, 2021, T. 66, № 5, стр. 669-677
Структура, свойства и фитопротекторные функции нанопорошков диоксида титана и водных суспензий на их основе
О. А. Шилова a, b, Г. Г. Панова c, С. В. Мякин b, d, А. С. Коваленко a, А. М. Николаев a, e, *, В. П. Челибанов f, И. В. Челибанов f, Е. А. Ясенко f, Д. Л. Корнюхин g, А. М. Артемьева g, А. С. Журавлева c, О. Р. Удалова c, А. Е. Баранчиков h, Т. В. Хамова a
a Институт химии силикатов им. И.В. Гребенщикова РАН
199034 Санкт-Петербург, наб. Макарова, 2, Россия
b Санкт-Петербургский государственный технологический институт (технический университет)
190013 Санкт-Петербург, Московский пр-т, 26, Россия
c Агрофизический научно-исследовательский институт
195220 Санкт-Петербург, Гражданский пр-т, 14, Россия
d Институт аналитического приборостроения РАН
190103 Санкт-Петербург, Рижский пр-т, 26, Россия
e Санкт-Петербургский государственный университет
199034 Санкт-Петербург, Университетская наб., 7–9, Россия
f АО “ОПТЭК” (Инструменты для научных исследований)
199178 Санкт-Петербург, Малый пр-т Васильевского острова, 58, Россия
g Всероссийский институт генетических ресурсов растений им. Н.И. Вавилова
190031 Санкт-Петербург, Большая Морская ул., 42, Россия
h Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
* E-mail: floijan@gmail.com
Поступила в редакцию 02.12.2020
После доработки 07.12.2020
Принята к публикации 08.12.2020
Аннотация
Проведено комплексное исследование фазового состава, морфологии и текстуры нанопорошка диоксида титана, полученного осаждением из водного раствора TiCl4, в сравнении с двумя коммерческими порошками. Изучены кислотно-основные свойства поверхности, заряд и изменение размера наночастиц нанопорошков диоксида титана в процессе их агрегации в водных суспензиях. Проведен сравнительный анализ влияния изученных характеристик нанопорошков на их фотокаталитическую активность и фитопротекторные свойства.
ВВЕДЕНИЕ
Диоксид титана в наноразмерном состоянии и материалы на его основе уже несколько десятилетий являются объектом многочисленных исследований [1–7]. Это связано прежде всего с его фотокаталитической активностью. Под действием ультрафиолетового излучения в материалах и покрытиях на основе наноразмерного диоксида титана, преимущественно в кристаллической фазе анатаза, происходит генерация активных форм кислорода, поверхность приобретает супергидрофильные свойства. Благодаря этому материалы и покрытия на основе нанодисперсного диоксида титана находят применение как бактерицидные, фунгицидные и обеспечивающие эффект самоочистки поверхности.
В последние годы нанодисперсный диоксид титана стали апробировать в качестве адаптогенов и стимуляторов роста в препаратах, используемых для предпосевной обработки семян и проростков растений [8–11]. Чаще всего для этой цели используют водные суспензии наночастиц диоксида титана, в том числе модифицируют поверхность наночастиц для повышения седиментационной устойчивости суспензий и/или обогащения ее полезными для растений микроэлементами. Данный подход был продемонстрирован в работе [8] на примере двух материалов на основе наночастиц диоксида титана со структурой анатаза размером ~5–10 нм, образующих в водных суспензиях агрегаты размером до ~210–240 нм и обладающих значениями ζ-потенциала от –10 до 8.5 мВ в зависимости от степени кристалличности. Полученные результаты показывают перспективность применения наночастиц диоксида титана (в определенных концентрациях) в составе биологически активных препаратов, способствующих борьбе с грибковыми инфекциями. По данным [11], использование кремнезолей на основе гидролизованного тетраэтоксисилана с добавкой нанодисперсного диоксида титана для предпосевной обработки семян пекинской капусты повышает количество эпифитных микроорганизмов на поверхности семян, увеличивая тем самым долю полезных бактерий, которые переводят органические и минеральные соединения азота в химические соединения, доступные для питания растений. Поскольку наночастицы диоксида титана используются преимущественно в виде водных суспензий, особый интерес представляет исследование свойств, приобретаемых наночастицами при взаимодействии с водной средой, включая заряд поверхности, изменение размера в процессе агрегации, а также изменение pH водной среды, оказывающее значительное влияние на растения.
Цель настоящей работы – сравнительное исследование влияния фазового состава, морфологии, текстуры и кислотно-основных свойств поверхности трех нанопорошков диоксида титана с различной структурой на их фотокаталитическую активность и изменение коллоидных характеристик при взаимодействии с водой, а также на фунгицидные, бактерицидные и фитопротекторные свойства. Полученные данные в перспективе могут найти применение при создании препаратов на основе нанопорошков диоксида титана для использования в растениеводстве открытого и защищенного грунта.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Нанопорошок диоксида титана (1) получали методом химического осаждения из водного раствора TiCl4. Для этого на первом этапе 15 мл 12 М раствора HCl растворяли в 300 мл дистиллированной воды. В полученный таким образом 2 М раствор HCl по каплям добавляли 15 мл охлажденного до 5°С TiCl4 при постоянном перемешивании при 0°С. На втором этапе проводили осаждение путем добавления по каплям 200 мл 6.25%-ного раствора аммиака при постоянном перемешивании и температуре 0°С. Величина рН реакционной смеси в конце процесса осаждения была равна 10. В ходе осаждения образовался осадок ТiO2 белого цвета, который отделяли от маточного раствора фильтрованием с использованием воронки Бюхнера и фторопластового фильтра, а затем промывали дистиллированной водой 3 раза и сушили в сушильном шкафу при 100°С.
Полученный порошок (1) исследовали в сравнении с коммерческими порошками диоксида титана (2 и 3) производства Plasmotherm (Россия), которые существенно отличаются по свойствам. Порошки сравнения были выбраны исходя из характеристик (размер наночастиц и фазовый состав), указанных производителем. Однако структура и свойства этих порошков сравнения были исследованы наряду с синтезированным порошком 1.
Фазовый состав и кристаллическую структуру порошков изучали методом рентгенофазового анализа (РФА) с использованием дифрактометра Bruker D8 Advance (CuKα-излучение, 2θ = 20°–80°, шаг 0.0075°, выдержка 7 с, параметры решетки рассчитывали методом наименьших квадратов с помощью программного комплекса PDWin), а морфологию синтезированных нанопорошков – методом просвечивающей электронной микроскопии (ПЭМ) высокого разрешения на просвечивающем электронном микроскопе Zeiss Libra 120. При расчете размеров областей когерентного рассеяния (ОКР) были использованы рефлексы 101 и 110 для анатаза и рутила соответственно.
Размер частиц, их морфологию и степень агломерации оценивали с помощью сканирующей электронной микроскопии с использованием растрового электронного микроскопа высокого разрешения Carl Zeiss NVision 40 с детектором Oxford Instruments X-MAX (80 мм2) при ускоряющем напряжении 1 кВ.
Удельную поверхность и пористость исследуемых материалов анализировали методом низкотемпературной адсорбции азота с использованием анализатора QuantaChrome Nova 1200e. Перед измерениями проводили дегазацию образца при 150°C в вакууме в течение 15.5 ч. Определение удельной площади поверхности образцов (Sуд) проводили с использованием моделей Брунауэра–Эммета–Теллера (по 7 точкам в диапазоне парциальных давлений азота p/p0 0.07−0.25) и Лэнгмюра. Удельный объем пор измеряли при парциальном давлении азота p/p0 = 0.995.
Кислотно-основные свойства поверхности синтезированных порошков были охарактеризованы по кинетике изменения рН суспензии [12, 13], получаемой при введении навесок порошков массой ~30 мг в 30 мл дистиллированной воды с исходным значением pH ~6.5 при непрерывном перемешивании магнитной мешалкой. Измерения рН суспензии проводили на рН-метре “Мультитест” ИПЛ-301 (НПП “СЕМИКО” Россия) через 5, 10, 20, 30, 40, 50, 60 с и далее через каждые 30 с в интервале от 1 до 5 мин и через каждые 60 с в течение последующих 5 мин после погружения навески порошка.
Агрегативную и седиментационную устойчивость водных суспензий исследовали методами динамического и электрофоретического рассеяния света с использованием прибора NanoBrook 90 Plus Zeta путем измерения среднего значения гидродинамического диаметра и ζ-потенциала частиц в суспензиях. Концентрации нанопорошков в суспензиях (3.0, 1.0, 0.3, 0.1, 0.01, 0.001, 0.0001 г/л) для этих исследований были выбраны из расчета перспективности их использования в агротехнологиях. Было изучено влияние мощности УЗ-диспергирования на исследуемые характеристики. В первом варианте суспензии с концентрацией 1.0 и 0.1 г/л получали методом ультразвукового диспергирования нанопорошков в дистиллированной воде в течение 20 мин с использованием УЗ-ванны (240 Вт, 40 кГц). Измерения проводили через 3 сут после установления равновесия. Второй вариант исследования предусматривал более интенсивное ультразвуковое воздействие с помощью УЗ-диспергатора И100-840 (рабочая частота 22 кГц, 5 мин). Измерения проводили после выдержки в течение 20 мин.
Фотокаталитическую активность исследуемых нанопорошков оценивали по количеству выделяемого под действием ультрафиолетового излучения синглетного кислорода, подавляющего развитие патогенной флоры. Измерения проводили с использованием оборудования фирмы ЗАО “ОПТЭК”, включающего генератор синглетного кислорода ГСК-1 и хемилюминесцентный газоанализатор синглетного кислорода 1О2. Одинаковые навески (по 2 мг) порошка диоксида титана и эталона (нанопорошок TiO2 P-25 Degussa®) по отдельности наносили на пористые фторопластовые мембраны, которые поочередно помещали в генератор ГСК-1, где их освещали светодиодной матрицей фирмы CHANSON (Р = 10 Вт, λ = 365 нм). Предварительно осушенный и очищенный с помощью угольного фильтра от активных форм кислорода воздух прокачивали через мембрану и подавали в газоанализатор синглетного кислорода. Синглетный кислород образовывался в мембране при взаимодействии фотокатализатора, активированного УФ-излучением, с молекулами обычного триплетного кислорода в прокачиваемом воздухе [14].
Бактерицидные и фунгицидные свойства исследуемых веществ с концентрациями 0.003, 0.03, 0.3 и 3.0 г/л оценивали с применением в качестве тест-объектов двух фитопатогенов: возбудителя сосудистого бактериоза капусты Xanthomonas campestris pv. сampestris (штамм 5212) и возбудителя темно-бурой пятнистости ячменя и корневой гнили гриба Cochliobolus sativus (S. Ito & Kurib.) Drechsler ex Dastur по методикам, описанным в [15, 16]. Влияние обработки семян суспензиями нанопорошков на устойчивость растений к поражению фитопатогенными микроорганизмами оценивали с помощью методики, описанной в [16] на примере белокочанной капусты сорта Penca de Povoa. Семена капусты высевали в кассеты (12 семян на 1 ячейку кассеты объемом 150 см3), наполненные субстратом на основе верхового торфа низкой степени разложения, зараженного возбудителями черной ножки капусты грибными патогенами (Pyhtium debaryanum Hesse, Olpidium brassicae Wor., Phizoctonia aderholdii Kolosh., Leptosphaeria maculans (Sowerby) P.Karst., Fusarium sp.). Кассеты обильно поливали и помещали в растильную камеру, в которой поддерживали постоянную температуру воздуха +18°C и режим день/ночь – 16 ч/8 ч. Оценку проводили на 21-е сутки после появления всходов. Учитывали два показателя: число растений и степень поражения по шкале ВИР (1 – отсутствие поражения, 3 – слабые симптомы, 5 – типичные симптомы, 7 – сильно выраженные симптомы, некроз, 9 – отсутствие всходов). Средневзвешенный балл поражения по вариантам вычисляли по формуле:
М = ∑(ab)/N,
где ∑(ab) – сумма произведений числа пораженных вариантов на соответствующий балл (степень) поражения, N – общее число вариантов [17]. Контролем служили растения, выращенные из семян, обработанных водой. При этом часть контрольных семян проращивали на зараженном грибными фитопатогенами субстрате (контроль с заражением), а часть – высевали в кассету с автоклавированным незараженным субстратом (контроль без заражения).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
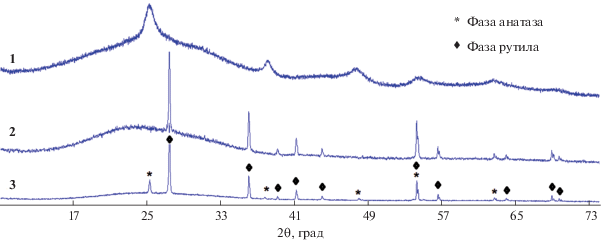
Исследование фазового состава, морфологии и текстуры нанопорошков. Данные РФА для нанопорошков диоксида титана (рис. 1) показывают, что фазовый состав синтезированного образца 1 соответствует плохо окристаллизованной фазе анатаза. Для коммерческих порошков диоксида титана наблюдается более высокая степень кристалличности. Их состав соответствует фазам рутила (образец 2) и смеси анатаз : рутил в массовом соотношении 1 : 4 (образец 3).
Размер ОКР для синтезированного плохо окристаллизованного анатаза (1) составил 7 нм, для коммерческого рутила (2) – 80 нм, а для смеси анатаза и рутила (3) – 70 и 90 нм соответственно.
Анализ морфологии порошков, выполненный по данным СЭМ (рис. 2), показал, что синтезированный нанопорошок 1 (плохо окристаллизованный анатаз) состоит из плотно агрегированных частиц размером от ~20 до ~50–100 нм. Наночастицы коммерческих порошков 2 и 3 образуют плотные агрегаты, имеющие четкие границы. Порошок 2 (рутил) характеризуется несколько большим размером агрегатов (~100–300 нм), в то время как агрегаты порошка 3, состоящего из смеси частиц рутила и анатаза, несколько меньше (~100–200 нм) и имеют более ярко выраженную анизометрическую форму.
Рис. 2.
СЭМ-изображения поверхности нанопорошков: а, а* – синтезированного химическим осаждением (1) и б, в – коммерческих (2 и 3 соответственно).

Результаты, полученные методом низкотемпературной адсорбции азота, приведены в табл. 1. Они показывают, что синтезированный порошок 1 характеризуется значительно более высокими значениями удельной поверхности и объема пор по сравнению с коммерческими порошками 2 и 3, что согласуется с меньшим размером частиц нанопорошка 1 (по данным СЭМ) и соответственно более развитой мезопористой структурой, образующейся в процессе химического синтеза порошка.
Таблица 1.
Текстура нанопорошков TiO2, рассчитанная на основе анализа полных изотерм адсорбции–десорбции азота
| Параметр* | Синтезированный порошок 1 (анатаз) | Порошки сравнения | |
|---|---|---|---|
| 2 (рутил) | 3 (анатаз-рутил) | ||
| SLangmuir, м2/г | – | − | 5.9 ± 0.2 |
| SBET, м2/г | 369 ± 7 | 13.3 ± 0.3 | − |
| ${{V}_{{p{\text{/}}{{p}_{0}}}}}$ ≅ 0.995, cм3/г | 0.270 | 0.044 | 0.031 |
Примечание. Параметры текстуры охарактеризованы на основе полных изотерм адсорбции–десорбции азота с помощью моделей Ленгмюра (Langmuir) и Брунауэра–Эммета–Теллера (Brunauer–Emmett–Teller, BET): SLangmuir и SBET – удельная площадь поверхности, ${{V}_{{p{\text{/}}{{p}_{0}}}}}$ → 0.99 – удельный объем пор.
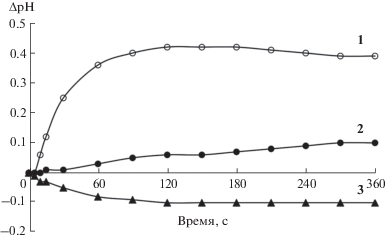
Исследование кислотно-основных свойств. Кинетику изменения рН водных суспензий исследуемых образцов можно проследить на рис. 3. Вид зависимостей для высокопористого слабоокристаллизованного порошка 1 в значительной степени отличается от зависимостей, полученных для коммерческих порошков 2 и 3. Суспензия синтезированного порошка 1 со структурой анатаза характеризуется медленным, но довольно значительным ростом величины pH вплоть до насыщения − приблизительно через 2 мин. Такой слабоосновный характер поверхности может быть обусловлен преобладанием основных центров Бренстеда, по-видимому, образованных группами типа =Ti(OH)2. Для суспензий с порошками 2 и 3 со структурой рутила и смешанной структурой анатаз-рутил наблюдается соответственно слабоосновная и слабокислая реакция с незначительным (не более ±0.1) изменением величины рН, что, по-видимому, отражает конкурирующие процессы гидролиза бренстедовских основных (=Ti(OH)2) и кислотных (≡Ti–OH) групп [18, 19].
Рис. 3.
Кинетика изменения pH водных суспензий синтезированного порошка 1 и порошков сравнения 2 и 3.
Интересно отметить, что степень кристалличности, морфологические и текстурные особенности исследуемых нанопорошков TiO2 оказывают на кислотно-основные свойства поверхности значительно большее влияние, чем фазовый состав. Суспензия коммерческого порошка со структурой хорошо окристаллизованного рутила (2) проявляет слабоосновную реакцию. Использование в составе суспензии порошка (3), состоящего из смеси хорошо окристаллизованных анатаза и рутила, содержащей 20 мас. % анатаза, приводит к изменению реакции водной среды на столь же слабо выраженную кислую. Это может свидетельствовать об образовании на поверхности материала кислотных групп типа ≡Ti–OH. Напротив, поверхность плохо окристаллизованного анатаза (1) обладает выраженной основной реакцией. Этот эффект может быть обусловлен увеличением числа поверхностных атомов, имеющих “свободные” связи, не участвующие в образовании кристаллической структуры и способные к образованию групп типа =Ti(OH)2 или даже –Ti(OH)3, гидролизующихся в водной среде с отщеплением гидроксил-ионов.
Исследование агрегативной устойчивости водных суспензий нанопорошков оксидов титана. Полученные значения размеров агрегатов частиц и ζ-потенциала поверхности исследуемых нанопорошков в водных суспензиях с различной концентрацией приведены в табл. 2.
Таблица 2.
Коллоидные характеристики нанопорошков TiO2 в водных суспензиях, обработанных в УЗ-ванне (240 Вт, 40 кГц, 20 мин), с последующей выдержкой в течение 3 сут
| Характеристика | Средний гидродинамический диаметр частиц (D, нм) в водных суспензиях различной концентрации | ||
|---|---|---|---|
| синтезированный | порошки сравнения | ||
| порошок 1 (анатаз) | 2 (рутил) | 3 (анатаз-рутил) | |
| Концентрация, г/л | |||
| 1.0 | 350 | 1800 | 1500 |
| 0.1 | 290 | 1800 | 700 |
| ζ-потенциал, мВ | −18 | −27 | −18 |
Полученные данные показывают, что для суспензий, полученных на основе исследованных нанопорошков диоксидов титана, размер образованных наночастицами агломератов в целом коррелирует с размерами частиц в исходных порошках. Размеры агломератов частиц на основе коммерческих порошков (2 и 3) существенно больше. При этом образец, имеющий фазовый состав рутила, сохраняет размер агломератов после разбавления неизменным. Кроме того, наночастицы в этой суспензии обладают значением ζ-потенциала, близким к значениям ζ-потенциалов устойчивых суспензий. Размер агрегатов синтезированного нанопорошка диоксида титана (1) в водной суспензии слабо изменяется при разбавлении. Однако малое по абсолютной величине значение ζ-потенциала свидетельствует о его недостаточной стабильности, что подтверждается образованием осадка на дне сосуда, наблюдаемым при длительном хранении. В отличие от остальных порошков, для диоксида титана со смешанным фазовым составом анатаз-рутил (3) наблюдается существенное уменьшение размеров агломератов в водных суспензиях при разбавлении, что указывает на относительно невысокую прочность межчастичных связей, разрушающихся при ультразвуковом воздействии. Исходя из значения ζ-потенциала можно заключить, что суспензия порошка 3 также является недостаточно стабильной.
В табл. 3 проанализировано влияние более интенсивного ультразвукового воздействия с помощью ультразвукового диспергатора (вместо УЗ-ванны) на характеристики поверхности нанопорошков диоксида титана при дальнейшем разбавлении. Коллоидные характеристики нанопорошков – синтезированного плохо окристаллизованного анатаза (1) и смеси хорошо окристаллизованных анатаза и рутила (3), водные суспензии которых в дальнейшем были использованы для обработки семян растений, представлены в табл. 4.
Таблица 3.
Коллоидные характеристики нанопорошков TiO2 (1 и 3) в водных суспензиях, обработанных с помощью УЗ-диспергатора (22 кГц, 5 мин), с последующей выдержкой в течение 20 мин
| С, г/л | Синтезированный порошок 1 (анатаз) | Порошок сравнения 3 (анатаз-рутил) | ||
|---|---|---|---|---|
| D, нм | ζ, мВ | D, нм | ζ, мВ | |
| 3.0 | 841 | −18 ± 3 | 2700 | −11.5 ± 1,5 |
| 0.3 | 800 | −15 ± 2 | 806 | −12 ± 3 |
| 0.1 | 705 | −28 ± 2 | 486 | Не удалось измерить |
| 0.01 | 550 | Не удалось измерить | 403 | −17 ± 4 |
Таблица 4.
Коллоидные наночастицы нанодисперсного порошка 2 (рутил) после обработки с помощью ультразвукового диспергатора (22 кГц, 5 мин) с последующей выдержкой в течение 20 мин
| С, г/л | D, нм | ζ, мВ |
|---|---|---|
| 0.3 | ~40 | +30 ± 6 |
| 0.1 | 226 | Не удалось измерить |
| 0.01 | 296 | 0 |
| 0.001 | 368 | −19 ± 3 |
| 0.0001 | 342 | −27 ± 5 |
Как видно из табл. 3, тенденция к уменьшению размера агрегатов наночастиц по мере разбавления суспензий сохранилась и при более мощном УЗ-воздействии. Однако их размер у более аморфизированного и химически активного нанопорошка 1 стал больше, а у содержащего фазу анатаза кристаллического нанопорошка 3, наоборот, меньше, за исключением суспензии с самой высокой концентрацией 3.0 г/л. Знак заряда наночастиц не изменился.
Совсем другая картина наблюдалась для порошка 2, состав которого отвечает рутилу (табл. 4). Видно, что применение ультразвука высокой интенсивности способствует растворению нанопорошка [20, 21]. В дисперсионной среде появляются положительные полиядерные комплексы, приводящие к перезарядке поверхности. Состав этих комплексов и их заряд зависят от рН и концентрации твердой фазы.
Сравнительное исследование фотокаталитической активности. Результаты измерений фотокаталитической активности нанопорошков показали, что наилучшие фотокаталитические характеристики (200 у.е.) наблюдаются для порошка 3, два других порошка проявляют намного более низкую активность: 17 у. е. для синтезированного порошка 1 и 13 у.е. для порошка 2. Высокая фотокаталитическая активность, достигнутая в случае нанопорошка 3 со смешанной структурой анатаз-рутил, может быть обусловлена присутствием фазы анатаза с высокой степенью кристалличности, в отличие от недостаточно окристаллизованной структуры анатаза у образца 1 или структуры рутила у порошка 2. Кроме того, кислая реакция поверхности образца 3 может отражать некоторое разупорядочение ее функционального состава и присутствие гидроксильных групп кислотного типа, способных вносить вклад в проявляемую материалом фотокаталитическую активность.
Оценка фитопротекторных свойств. Оценка способности изучаемых суспензий нанопорошков диоксида титана подавлять рост и развитие ряда грибных и бактериальных фитопатогенных микроорганизмов показала, что в тестируемых концентрациях, не оказывающих негативного влияния на растения [15], они не обладают фунгицидными и бактерицидными свойствами. Только нанопорошок диоксида титана (3) со смешанной структурой анатаз-рутил и высокой фотокаталитической активностью при концентрации 3 г/л показывает бактериостатический эффект в отношении возбудителя сосудистого бактериоза капусты – бактерий Xanthomonas campestris pv. сampestris, штамм 5212.
Дальнейшие исследования влияния обработки семян суспензиями нанопорошков 1 и 3 с концентрациями 0.3 и 3.0 г/л на развитие растений белокочанной капусты сорта Penca de Povoa в субстрате, зараженном возбудителями заболевания черная ножка – грибными патогенами (Pyhtium debaryanum Hesse, Olpidium brassicae Wor., Phizoctonia aderholdii Kolosh., Leptosphaeria maculans (Sowerby) P. Karst., Fusarium sp.), показали, что суспензии этих нанопорошков диоксида титана проявили выраженный фитопротекторный эффект (табл. 5). При этом более значимым он был у фотокаталитически малоактивного плохо окристаллизованного порошка диоксида титана (1) в варианте с высокой концентрацией 3.0 г/л, а у отличающегося более высокой фотокаталитической активностью порошка 3 (рутил-анатаз) – в варианте с меньшей концентрацией (0.3 г/л). Выживаемость растений под влиянием указанных наиболее эффективных (в уменьшении степени их поражаемости болезнью черная ножка) вариантах обработки семян суспензиями нанопорошков диоксида титана повышалась относительно зараженного контроля, однако имела существенно более низкие значения (на 43 и 54% соответственно) по сравнению с незараженным контролем. Полученные данные свидетельствуют о необходимости качественного и количественного усовершенствования составов синтезированных веществ для повышения их фитопротекторной функции.
Таблица 5.
Выживаемость растений белокочанной капусты и ее поражаемость заболеванием черная ножка при выращивании в зараженном грибными возбудителями корневой гнили субстрате из семян, обработанных изучаемыми веществами
| Вариант обработки семян | Доля живых растений (среднее значение), % |
Средневзвешенный балл поражения, М (шкала ВИР [17]) |
|
|---|---|---|---|
| наименование | концентрация нанопорошка | ||
| Вода | 0 | 38.9 ± 3.4 | 7.9 |
| 1 (плохо окристаллизованный анатаз) | 0.3 | 34.3 ± 2.6 | 6.1 |
| 3.0 | 57.2 ± 4.1 | 5.3 | |
| 3 (хорошо окристаллизованные анатаз-рутил) | 0.3 | 45.7 ± 1.2 | 5.2 |
| 3.0 | 34.3 ± 0.8 | 5.1 | |
| Стерильная почва | 100 | 100 | |
ЗАКЛЮЧЕНИЕ
Химическим осаждением из раствора TiCl4 получен нанопорошок диоксида титана, обладающий высокой пористостью, развитой поверхностью и отвечающий фазовому составу анатаза (ОКР = 7 нм), кристаллиты которого образуют плотноупакованные агломераты размером ~20–100 нм. В качестве порошков сравнения были выбраны два коммерческих низкопористых, хорошо окристаллизованных нанопорошка. Один из них отвечает фазовому составу рутила (ОКР = 90 нм) и образует плотные агрегаты размером ~100–300 нм. Второй состоит из смеси кристаллитов анатаза (ОКР = 70 нм) и рутила (ОКР = 90 нм), образующих агрегаты анизометрической формы размером ~100–200 нм.
Установлено, что фазовый состав, морфология и текстура нанопорошков диоксида титана оказывают сильное влияние на его фотокаталитическую активность, а также на размер агрегатов, заряд и кислотно-основные свойства поверхности порошков в водных суспензиях, что имеет большое значение для их последующего применения в агротехнологиях. Фотокаталитическая активность в наибольшей степени зависит от фазового состава (наличия фазы анатаза) и степени окристаллизованности нанопорошков. Размер агрегатов частиц, образующихся в водных суспензиях, в основном коррелирует с размером наночастиц в порошках. Однако при интенсивном ультразвуковом воздействии может происходить уменьшение размера агрегатов и перезарядка поверхности наночастиц. Агрегативная устойчивость суспензий диоксида титана не зависит от развитости поверхности, а в основном определяется величиной ее заряда, что обеспечивает эффект отталкивания одноименно заряженных частиц. Водные суспензии на основе синтезированного высокопористого нанопорошка диоксида титана с высокоразвитой поверхностью обладают слабоосновной реакцией, благодаря доминирующему процессу гидролиза с образованием бренстедовских основных (=Ti(OH)2) групп, что благоприятно для обработки семян и проростков растений.
Тестируемые нанопорошки диоксида титана проявляют протекторный эффект, обеспечивающий снижение степени развития у белокочанной капусты заболевания черная ножка при выращивании ее в условиях заражения субстрата комплексом фитопатогенных грибов, вызывающих это заболевание. При этом отмечаются различия в концентрационной зависимости проявления указанного эффекта у нанопорошков диоксида титана с разной фотокаталитической активностью. Так, у порошка диоксида титана (плохо окристаллизованный анатаз) с низкой фотокаталитической активностью (17 у. е.) более значимым указанный эффект был в варианте с высокой концентрацией (3.0 г/л), а у порошка, отличающегося более высокой фотокаталитической активностью (200 у. е.) (хорошо окристаллизованные рутил/анатаз), − в варианте с меньшей концентрацией (0.3 г/л).
Список литературы
Soonchul K., Maohong F. // Crit. Rev. Env. Sci. Technol. 2008. V. 38. № 3. P. 197. https://doi.org/10.1080/10643380701628933
Исмагилов З.Р., Цикоза Л.Т., Шикина Н.В. и др. // Успехи химии. 2009. Т. 78. № 9. С. 942. https://doi.org/10.1070/RC2009v078n09ABEH004082
Ruffini Castiglione M., Giorgetti L. // J. Nanopart. Res. 2010. V. 10. P. 24. https://doi.org/10.1007/s11051-010-0135-8
Lai Y., Wang L., Liu D. et al. // J. Nanomater. 2015. Art. 250632. https://doi.org/10.1155/2015/250632
Jukapli N.M., Bagher S. // J. Photochem. Photobiolog. B: Biol. (Inv. Rev.) 2016. V. 163. P. 421. https://doi.org/10.1016/j.jphotobiol.2016.08.046
Жеребцов Д.А., Куликовских С.А., Викторов В.В. и др. // Журн. неорган. химии. 2019. Т. 64. № 2. С. 132. https://doi.org/10.1134/S0044457X19020235
Фаттахова З.А., Захарова Г.С., Андрейков Е.И., Пузырев И.С. // Журн. неорган. химии. 2019. Т. 64. № 7. С. 700. https://doi.org/10.1134/S0044457X19070079
Janmohammadi M., Amanzadeh T., Sabaghia N., Dashti S. // Acta Agriculturae Slovenica. 2016. V. 107. № 2. P. 265. https://doi.org/10.14720/aas.2016.107.2.01
Шилова О.А., Хамова Т.В., Панова Г.Г. и др. // Журн. прикл. химии. 2020. Т. 93. № 1. С. 32. https://doi.org/10.31857/S004446182001003X
Palmqvist N.G.M., Bejai S., Meijer J. et al. // Sci. Rep. 2015. V. 5. P. 10146. https://doi.org/10.1038/srep10146
Shalaby T.A., Bayoumi Y., Abdalla N. et al. Nanoparticles, Soils, Plants and Sustainable Agriculture. In: Nanoscience in Food and Agriculture 1 / Eds. Ranjan S., Dasgupta N., Lichtfouse E. Cham. Springer, 2016. https://doi.org/10.1007/978-3-319-39303-2_10
Нечипоренко А.П. Донорно-акцепторные свойства поверхности твердофазных систем. Индикаторный метод. СПб.: Лань, 2017. 284 с.
Сычев М.М., Минакова Т.С., Слижов Ю.Г., Шилова О.А. Кислотно-основные характеристики поверхности твердых тел и управление свойствами материалов и композитов. СПб.: Химиздат, 2016. 271 с.
Daimon T., Nosaka Y. // Phys. Chem. C. 2007. V. 111. № 11. P. 4420. https://doi.org/10.1021/jp070028y
Панова Г.Г., Семенов К.Н., Шилова О.А. и др. // Агрофизика. 2018. № 3. С. 48. https://doi.org/10.25695/AGRPH.2018.03.09
Shilova O.A., Panova G.G., Nikolaev A.M. et al. // Lett. Appl. NanoBioScience. 2021. V. 10. № 2. P. 2215. https://doi.org/10.33263/LIANBS102.22152239
Сазонова Л.В. и др. Методические указания ВИР. Изучение и поддержание коллекции овощных растений (морковь, сельдерей, петрушка, пастернак, редька, редис). Л., 1981. 190 с.
Diebold U. // Appl. Phys. A. 2003. V. 76. P. 681. https://doi.org/10.1007/s00339-002-2004-5
Wendt S., Matthiesen J., Schaub R. et al. // Phys. Rev. Lett. 2006. V. 96. № 6. P. 066107. https://doi.org/10.1103/PhysRevLett.96.066107
Хмелев В.Н., Попова О.В. Многофункциональные ультразвуковые аппараты и их применение в условиях малых производств, сельском и домашнем хозяйстве. Барнаул: Изд-во АлтГТУ, 160 с.
Tsai W.B., Kao J.Y., Wu T.M. et al. // J. Nanopart. 2016. Art. 6 539 581. https://doi.org/10.1155/2016/6539581
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии