Журнал неорганической химии, 2021, T. 66, № 5, стр. 658-668
Формирование нанокристаллов Bim + 1Fem – 3Ti3O3m + 3 (m = 4–9) при термическом разложении соосажденных гидроксидов
Н. А. Ломанова a, *, М. В. Томкович a, А. В. Осипов b, В. Л. Уголков b, В. В. Панчук c, d, В. Г. Семенов c, d, В. В. Гусаров a
a Физико-технический институт им. А.Ф. Иоффе РАН
194021 Санкт-Петербург, Политехническая ул., 26, Россия
b Институт химии силикатов им. И.В. Гребенщикова РАН
199034 Санкт-Петербург, наб. Макарова, 2, Россия
c Санкт-Петербургский государственный университет
199034 Санкт-Петербург, Университетская наб., 7–9, Россия
d Институт аналитического приборостроения РАН
198095 Санкт-Петербург, ул. Ивана Черных, 31–33, Россия
* E-mail: natus@mail.ioffe.ru
Поступила в редакцию 30.11.2020
После доработки 29.12.2020
Принята к публикации 30.12.2020
Аннотация
Нанокристаллы фаз Ауривиллиуса Bim+ 1Fem– 3Ti3O3m+ 3 (m = 4–9) синтезированы термическим разложением соосажденной смеси гидроксидов висмута, железа и титана. Средний размер кристаллитов в нанопорошках зависит от m и составляет 50–100 нм. Образцы охарактеризованы с помощью синхронного термического и элементного анализа, рентгенодифракционного и мессбауэровского исследований. Установлено, что начало кристаллизации Bim+ 1Fem– 3Ti3O3m+ 3 находится вблизи температуры плавления неавтономной (поверхностной) фазы на основе оксида висмута (450°С). Показано, что соединения Bim+ 1Fem– 3Ti3O3m+ 3 с m ≤ 5 кристаллизуются в одну стадию. На первом этапе образования соединений с m > 5 формируется фаза Ауривиллиуса с m ≈ 5 и аморфная фаза. На втором этапе компоненты аморфной фазы встраиваются в перовскитоподобные блоки фазы Ауривиллиуса с m ≈ 5, скорее всего, через их наружные перовскитоподобные слои. После дальнейшей термообработки происходит перераспределение компонентов между наружными и внутренними слоями перовскитоподобных блоков. Обнаруженная зависимость механизма формирования нанокристаллов Bim+ 1Fem– 3Ti3O3m+ 3 от их состава может быть использована в технологии направленного синтеза нанокристаллических мультиферроиков.
ВВЕДЕНИЕ
Сложные перовскитоподобные оксиды семейства фаз Ауривиллиуса Bim+ 1Fem– 3Ti3O3m+ 3 вызывают большой интерес как потенциальные материалы для магнитоэлектроники, фотовольтаики, катализа и т.д. [1–7]. Элементарная ячейка структуры этих соединений состоит из чередующихся висмут-кислородных слоев (Bi2O2)2+ и перовскитоподобных блоков (Bim+ 1Fem– 3Ti3O3m+ 1)2–, состоящих из m монослоев. Среди известных фаз Ауривиллиуса гомологический ряд Bim+ 1Fem– 3Ti3O3m+ 3 обладает наибольшей вариабельностью состава, так как m может изменяться от 3 до 9, принимая в том числе и дробные значения [5].
В работе [8] указывается на близость структурных параметров перовскитоподобного блока многослойных фаз Ауривиллиуса (m > 7) и перовскитоподобного BiFeO3. Последний поэтому может рассматриваться как некоторый предел, к которому приближается гомологический ряд Bim+ 1Fem– 3Ti3O3m+ 3 при m → ∞. В работах [8, 9] понижение термической устойчивости фаз Bim+ 1Fem– 3Ti3O3m+ 3 при увеличении m связывается с метастабильным характером BiFeO3 [10–13]. Сложность синтеза многослойных фаз Ауривиллиуса (m > 5) обусловлена большим содержанием BiFeO3 в перовскитоподобном блоке их структуры [14].
Особенности формирования нанокристаллов Bim+ 1Fem– 3Ti3O3m+ 3 с m < 5 в условиях методов “мягкой химии” описаны во многих работах [15–25]. В работе [24] описан механизм формирования Bi7Fe3Ti3O21 (m = 6) в гидротермальных условиях через серию промежуточных продуктов с m < 6, имеющих существенные различия в морфологии частиц. Следует отметить, что такая этапность характерна и для синтеза фаз Ауривиллиуса Bim+ 1Fem– 3Ti3O3m+ 3 с большим числом слоев в перовскитоподобном блоке методом твердофазных химических реакций [14, 26]. Однофазный продукт на основе многослойных фаз Ауривиллиуса сложно получить как высокотемпературным методом твердофазного синтеза [8, 26, 27], так и при применении низкотемпературных методов [25]. По-видимому, это связано с потенциальной возможностью формирования при их синтезе многокомпонентной смеси на основе фаз, реализующихся в системе Bi2O3–Fe2O3–TiO2. К ним относятся, например, соединения Bi12TiO20/Bi25FeO39, Bi2Ti2O7, BiFeO3, Bi2Fe4O9 и др. [2, 9, 10, 13, 25]. Изучение особенностей формирования слоистой перовскитоподобной структуры в условиях “мягкой химии” является важной задачей для развития технологии материалов на основе фаз Ауривиллиуса.
Как показано в ряде работ [28–37], для определения механизма химических превращений в сложных железосодержащих перовскитоподобных оксидах полезную информацию дает мессбауэровское исследование состояния железа. В работах [3, 6, 27, 29, 31] установлено, что важным фактором, влияющим на устойчивость фаз Ауривиллиуса, является распределение катионов Fe3+ и Ti4+ по внутренним и внешним позициям перовскитоподобного блока, в частности, показано, что характер распределения ионов Fe3+ в структуре резко изменяется при m ≈ 5, а при m → 9 их распределение по структурно-неэквивалентным позициям приближается к чисто случайному, при этом устойчивость фаз Ауривиллиуса понижается. Связь между процессом образования нанокристаллов Bim+ 1Fem– 3Ti3O3m+ 3 и распределением катионов в структуре ранее не исследовалась.
Целью работы являлось определение механизмов формирования нанокристаллических фаз Ауривиллиуса состава Bim+ 1Fem– 3Ti3O3m+ 3 (m = = 4–9) при термическом разложении соосажденной смеси гидроксидов висмута, железа и титана.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез образцов проводили в несколько этапов. На первом этапе готовили растворы исходных компонентов. В качестве исходных веществ использовали пятиводный нитрат висмута Bi(NO3)3 ⋅ 5H2O квалификации “ч.”, девятиводный нитрат железа(III) Fe(NO3)3 ⋅ 9H2O квалификации “ч.” и тетраизопропоксид титана Ti[OCH(CH3)2] (97%). Нитраты растворяли в разбавленной азотной кислоте с концентрацией 0.1 моль/л (pH < 2), тетраизопропоксид титана для предотвращения гидролиза растворяли в этиловом спирте. Полученные исходные растворы смешивали в пропорциях, обеспечивающих соотношение катионов железа, висмута и титана, отвечающее формулам соединений Bim+ 1Fem– 3Ti3O3m+ 3 (m = 4, 5, 6, 7, 8, 9). Далее растворы медленно вливали в раствор аммиака c постоянным перемешиванием и контролем значения pH > 8. Полученные осадки промывали на фильтре дистиллированной водой и высушивали. Полученные таким образом порошки подвергали термообработке в режиме нагрев–изотермическая выдержка–охлаждение в диапазоне температур 450–890°С в зависимости от степени завершенности процесса образования целевого продукта. Изотермическая выдержка составляла 1 ч при каждой температуре.
Элементный состав образцов определяли методом энергодисперсионного микроанализа (сканирующий электронный микроскоп FEI Quanta 200 с приставкой EDAX).
По данным рентгеновской дифракции (дифрактометр Shimadzu XRD-7000, CuKα-излучение, λ = 15.401 нм) определяли фазовое состояние образцов и рассчитывали параметры элементарных ячеек с использованием программного комплекса PDWin 4.0. Размеры кристаллитов определяли по формуле Шеррера на основании данных об уширении линий рентгеновской дифракции.
Термическое поведение соосажденных гидроксидов исследовали методом дифференциальной сканирующей калориметрии (ДСК) совместно с термогравиметрией (ТГ) в диапазоне температур 25–1250°С в воздушной среде со скоростью нагрева 10 град/мин (анализатор Netzsch STA 429). Анализ проводили в режиме термопрограммируемого нагрева и охлаждения образцов.
Мессбауэровское исследование выполняли на спектрометре Wissel в геометрии на поглощение при комнатной температуре (источник 57Со в матрице родия, величины изомерных сдвигов (IS) определены относительно IS α-Fe).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Нанокристаллические порошки фаз Ауривиллиуса, номинальное соотношение элементов в которых задавалось по стехиометрии соединений Bim+ 1Fem– 3Ti3O3m+ 3 с m = 4, 5, 6, 7, 8 и 9 (табл. 1, образцы 1, 2, 3, 4, 5 и 6 соответственно), получали разложением соосажденых гидроксидов.
Таблица 1.
Состав, условия синтеза, размерные параметры нанокристаллов фаз Ауривиллиуса Bim+ 1Fem– 3Ti3O3m+ 3
| № | Номинальный состав |
m | Состав по данным EDX* | Примесные и промежуточные фазы | Метод синтеза | Ts0**, °С | Tсинт***, °С; t, ч |
d (D)****, нм | Источник |
|---|---|---|---|---|---|---|---|---|---|
| – | Bi4Ti3O12 | 3 | – | – | Соосаждение | 450 | 450; 10/800; 1 | 50/124 | [25] |
| Bi2O3 | Соосаждение | 600 | 750; 2 | 20 | [15] | ||||
| – | Гидротермальный | 100 | 180; 48 | >100 | [16] | ||||
| Bi2Ti2O7 | Соосаждение | 470 | 650; 1 | ~100 | [18] | ||||
| 1 | Bi5FeTi3O15 | 4 | Bi4.9Fe1.1Ti3.0O15 | – | Соосаждение | 450 | 890; 1 | >100 | – |
| – | Гидротермальный | 180 | 900 | >100 | [20] | ||||
| Bi2O2CO3 | Золь-гель | 500 | 180; 72 160; 15 |
>100 (микроцветы) >100 (наноцветы) |
[22] | ||||
| 160; 15 | 20–40 (наночастицы) >100 (наностержни, нанослои) |
[22] | |||||||
| 2 | Bi6Fe2Ti3O18 | 5 | Bi5.6Fe1.4Ti3.0O16.6 | – | Соосаждение | 450 | 890; 1 | >100 | – |
| 3 | Bi7Fe3Ti3O21 | 6 | Bi6.8Fe2.6Ti3.0O20.1 | ф. Аурив. с m < 6 Bi2Fe4O9 |
Соосаждение | 460 | 850; 1 | 86 | – |
| Bi4Ti3O12 Bi5FeTi3O15 Bi25FeO40 |
Гидротермальный | 200 | 200; 48 | >100 (наношельф) | [15] | ||||
| 4 | Bi8Fe4Ti3O24 | 7 | Bi7.6Fe3.9Ti3.0O23.3 | ф. Аурив. с m < 6 Bi2Fe4O9 |
Соосаждение | 460 | 850; 1 | 80 | – |
| 5 | Bi9Fe5Ti3O27 | 8 | Bi9.7Fe5.5Ti3.0O29.0 | ф. Аурив. с m < 6 Bi2Fe4O9 |
Соосаждение | 460 | 850; 1 | 75 | – |
| 6 | Bi10Fe6Ti3O30 | 9 | Bi10.8Fe7.3Ti3.0O33.2 | ф. Аурив. с m < 6 Bi2Fe4O9 |
Соосаждение | 460 | 850; 1 | 53 | – |
| BiFeO3 | ∞ | – | Bi25FeO39 Bi2Fe4O9 |
Соосаждение | 600 | 600; 0.1–0.15 | <50 | [46] | |
| Bi25FeO39 Bi2O2CO3 |
Раств. горен. | 450 | 550; 0.2 420 |
70 20 |
[42] | ||||
| – | Гидротерм. | 420 | 20 | [36] | |||||
| Bi25FeO39 | УЗ-распыление | 500 | 750 | >100 (полые сферы) | [45] |
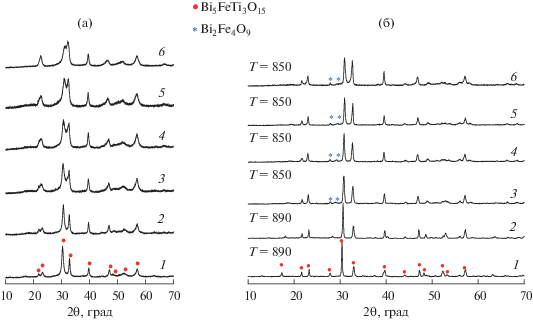
Термограммы (ДСК/ТГ) высушенных осадков показаны на рис. 1, из которого видно, что до 450°С на кривых ТГ фиксируются два накладывающихся эффекта потери массы, связанные, по-видимому, с потерей адсорбированной воды и разложением гидроксидов. На кривых ДСК при ~450°С фиксируется начало хорошо выраженного экзотермического эффекта с экстремумом около 500°С, относящегося к процессу формирования кристаллических фаз Ауривиллиуса в системе Bi2O3–Fe2O3–TiO2 из продуктов дегидратации соосажденных гидроксидов. Это подтверждает анализ приведенных на рис. 2а рентгеновских дифрактограмм, на которых после термообработки соосажденной смеси при 450°С (1 ч) наблюдаются хорошо выраженные рефлексы соединений со структурой фаз Ауривиллиуса. Характер фоновой кривой на дифрактограммах указывает на присутствие в образцах также и аморфной фазы.
Рис. 1.
Кривые ДСК/ТГ образцов исходной композиции в режиме нагрева. На вставке показан режим охлаждения для образца 6.
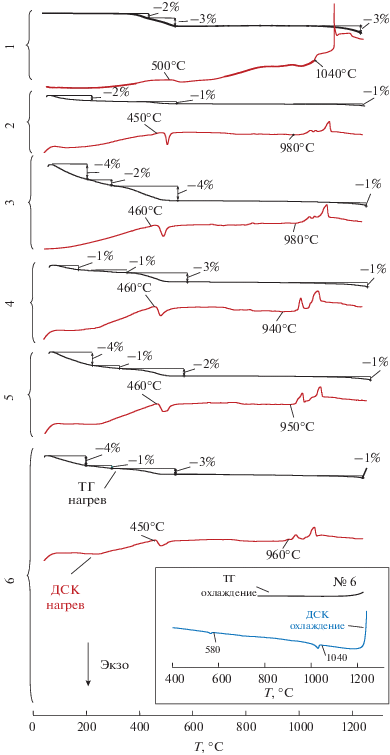
Следует отметить, что несмотря на то, что максимум тепловыделения на термограммах всех образцов находится в одной температурной области, вид зависимости экзотермического эффекта от температуры на термограммах различается (рис. 1). В образце 1, состав которого, как следует из данных элементного анализа (табл. 1), близок к составу четырехслойной фазы Ауривиллиуса, данный эффект размыт и плохо определяется. В образце 2 с номинальным составом, отвечающим m = 5, этот пик достаточно узкий.
Для образцов 3–6 (m > 5) на кривой ДСК наблюдается уширенный пик, растянутый в высокотемпературную область, который можно рассматривать, как наложение двух или большего числа экзотермических эффектов. В высокотемпературной области на термограммах наблюдаются интенсивные эндотермические эффекты с началом около 940–1040°С в зависимости от состава образцов. В соответствии с данными о квазибинарном разрезе BiFeO3–Bi4Ti3O12 [9] диаграммы состояния системы Bi2O3–Fe2O3–TiO2, они отвечают началу перитектического плавления фаз Ауривиллиуса. При этом на термограммах образцов, состав которых соответствует многослойным фазам, можно выделить серию эндотермических эффектов, связанных с последовательным перитектическим плавлением фаз Ауривиллиуса, протекающим с образованием фаз Ауривиллиуса с меньшим числом слоев в перовскитоподобном блоке.
После окончательного расплавления образцов наблюдается небольшая потеря массы на кривых ТГ, связанная с испарением компонентов расплава, главным образом оксида висмута [38–40]. При охлаждении образовавшегося расплава ниже точки его равновесной кристаллизации в образцах наблюдаются экзотермические пики, отвечающие кристаллизации фаз Ауривиллиуса. В соответствии с диаграммой состояния системы Bi4Ti3O12–BiFeO3 [9], эти пики соответствуют кристаллизации соединений с меньшими значениями m. В качестве примера данный процесс показан для образца 6 на вкладке к рис. 1.
В табл. 1 приведены данные об условиях формирования нанокристаллов фаз Ауривиллиуса при использовании разных методов “мягкой химии”. Следует отметить, что температура начала формирования фаз Ауривиллиуса (Ts0) коррелирует во всех рассмотренных случаях с температурой плавления поверхностной (двумерной неавтономной) фазы на основе оксида висмута (460 ± 40°С [41]), при которой стартует процесс формирования сложных висмутсодержащих перовскитоподобных оксидов при использовании низкотемпературных методов синтеза [25, 36, 42–45]. Можно видеть, что, независимо от состава этих фаз, в большинстве систем наблюдаются близкие значения температуры начала их образования Ts0 = = 450–600°С (табл. 1). Некоторый разброс данных в значениях температуры Ts0, по-видимому, может быть связан с формированием примесных фаз в реакционной композиции.
Рентгеновские дифрактограммы образцов после завершающей стадии синтеза приведены на рис. 2б. Анализ данных рентгеновской дифракции показывает, что наряду с целевым продуктом при образовании фаз Ауривиллиуса Bim+ 1Fem– 3Ti3O3m+ 3 с m > 5 в некоторых образцах обнаруживаются небольшие количества примесной фазы Bi2Fe4O9. Наличие примесной фазы потенциально может быть связано либо с нарушением заданной стехиометрии образцов на этапе синтеза, в частности, из-за высокой летучести оксида висмута [38], либо с кинетическими затруднениями образования фаз Ауривиллиуса с большим содержанием BiFeO3 в перовскитоподобном блоке, что подробно анализировалось в работах [14, 26]. Варианты возможных примесных фаз при формировании соединений Bim+ 1Fem– 3Ti3O3m+ 3 в различных условиях приведены в табл. 1.
Полученные в работе (рис. 2б) и литературные (табл. 1) данные показывают, что при синтезе соединений Bim+ 1Fem– 3Ti3O3m+ 3 с m ≤ 5 примесные фазы образуются реже и в меньших количествах, чем при m > 5. Причем в случае синтеза фаз Ауривиллиуса с m < 5 после термообработки выше 700°С примесные компоненты расходуются на формирование основной фазы. При синтезе BiFeO3 примесные фазы, как правило, образуются в большем количестве (табл. 1), что затрудняет формирование однофазного материала. Исключение составляет синтез этого соединения в гидротермальных условиях и при использовании методов высокоинтенсивного смешения реагентов при их соосаждении [46, 47].
На рис. 3 приведены зависимости V = V(m) объема элементарной ячейки V фаз Ауривиллиуса от m после низкотемпературной (1) и высокотемпературной (2) обработки образцов. Можно видеть, что обе зависимости совпадают до значения m ≈ 5. При m > 5 значения V = V(m) зависимости 1 практически не меняются, а зависимость 2 имеет линейный вид на всем интервале изменения величины m и хорошо описывает как полученные в работе экспериментальные результаты, так и данные работ [27, 29, 45]. Из этого можно заключить, что после низкотемпературной обработки соосажденных гидроксидов с соотношением катионов, отвечающим соединению Bim+ 1Fem– 3Ti3O3m+ 3 с m > 5, формируются фазы Ауривиллиуса с m ≈ 5 (рис. 3, кривая 1).
Рис. 3.
Зависимость объема элементарной ячейки V фаз Bim+ 1Fem– 3Ti3O3m+ 3 от номинального значения m на разных этапах термообработки: 1 – 450; 2 – 850–890°С.
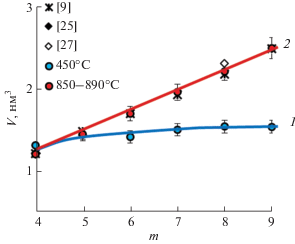
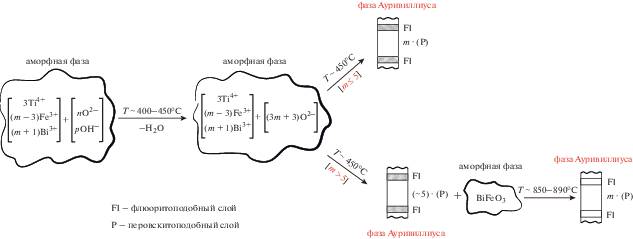
Непрореагировавшие при данных температурах компоненты образуют аморфную фазу. Дальнейшая высокотемпературная обработка этих образцов приводит к образованию фаз Ауривиллиуса с объемом элементарной ячейки, соответствующим целевому продукту (рис. 3, кривая 2). Таким образом, полученные результаты показывают, что по характеру образования фаз Ауривиллиуса соединение Bi6Fe2Ti3O18 (m = 5) является граничным с точки зрения механизма формирования соединений гомологического ряда Bim+ 1Fem– 3Ti3O3m+ 3. При m ≤ 5 эти соединения формируются сразу после дегидратации гидроксидов при ~450°C в один этап, а при m > 5 после дегидратации гидроксидов сначала образуется кристаллическая фаза, состав которой отвечает фазе Ауривиллиуса с m ≈ 5, и аморфная фаза. И только последующая более длительная и высокотемпературная обработка приводит к формированию фазы Ауривиллиуса заданного состава вследствие встраивания в перовскитоподобный блок компонентов из аморфной фазы. Схематически данный процесс представлен на рис. 4.
Отметим, что полученный результат согласуется с данными работ [14, 26], в которых синтез фаз Ауривиллиуса проводили разными методами. Это показывает, что независимо от условий формирования многослойных соединений Bim + 1Fem– 3Ti3O3m+ 3 с m > 5 их синтез проходит через стадию образования фаз Ауривиллиуса с меньшим значением m. В частности, в работе [24] установлено, что формирование нанокристаллов Bi7Fe3Ti3O21 (m = 6) в гидротермальных условиях протекает через серию промежуточных продуктов, основными из которых являются Bi4Ti3O12 (m = 3) и Bi5FeTi3O15 (m = 4) (табл. 1). В работе [26] была описана аналогичная этапность формирования этого соединения при протекании твердофазной химической реакции в смеси оксидных реагентов – от формирования сначала соединений с меньшим числом слоев в перовскитоподобном блоке с последующим встраиванием в него компонентов исходных фаз. Так как этапный механизм формирования соединений Bim+ 1Fem– 3Ti3O3m+ 3 с большими значениями m характерен для различных методов синтеза, можно сделать заключение, что особенности фазообразования в данном случае зависят главным образом от особенностей строения самих фаз Ауривиллиуса в рассматриваемой системе.
Для уточнения связи между особенностями формирования фаз Ауривиллиуса с большим числом слоев в перовскитоподобном блоке (m > 5) и параметрами их строения был проведен мессбауэровский анализ образцов 2 (m = 5) и 4 (m = 7) после их термообработки при 450°С и после высокотемпературной обработки (890°С – образец 2, 850°С – образец 4). Такой выбор связан с тем, что, как показано выше, характер фазообразования при синтезе фаз Ауривиллиуса кардинально изменяется при m ≈ 5. Приведенные на рис. 5 мессбауэровские спектры представлены дублетными линиями, которые в зависимости от состава и температуры обработки образца могут быть разложены на два или три дублета. Параметры мессбауэровских спектров образцов 2 и 4 и размеры кристаллитов соответствующих фаз Ауривиллиуса приведены в табл. 2 в сопоставлении с литературными данными. Сравнение параметров дублетов D1 и D2 (изомерного сдвига IS, квадрупольного расщепления QS) образцов, термообработанных при 450°С, с литературными данными показывает, что состояние ионов Fe3+ в них соответствует состоянию в соединении Bi6Fe2Ti3O18 со структурой фазы Ауривиллиуса (m = 5), т.е. близкие значения параметров имеют оба рассматриваемых образца, хотя их номинальный состав сильно отличается. Этот результат согласуется с описанными выше данными рентгенодифракционного исследования, показывающими, что на начальной стадии синтеза независимо от номинального состава в этих образцах формируется фаза Ауривиллиуса со значением m ≈ 5. Следует отметить, что отличие значений параметров дублетов D1 и D2 от литературных данных состоит только в соотношении долей дублетов, соответствующих ионам Fe3+ на внутренних (B1) и внешних (B2) позициях перовскитоподобных блоков (табл. 2). Параметры (IS и QS) третьего дублета (D3) у образца 4, как следует из их сравнения с литературными данными [36], близки по своим значениям к соответствующим параметрам аморфного BiFeO3. Учитывая, что дублет D2 соединения Bi6Fe2Ti3O18 (m = 5) близок по значению параметров IS и QS к параметрам одного из дублетов аморфного BiFeO3, этот дублет можно рассматривать как наложение соответствующих дублетов фазы Ауривиллиуса и аморфной фазы на основе ортоферрита висмута. Используя данные о соотношении долей дублетов аморфного BiFeO3 [36], можно уточнить соотношение долей дублетов фазы Ауривиллиуса в образце 4 после термообработки при 450°С. После такой корректировки соотношение долей дублетов в образцах 2 и 4 становится приблизительно одинаковым D1 : D2 = 69 : 31. Это соотношение лежит между значениями, характерными для чисто случайного распределения железа по внутренним и наружным слоям перовскитоподобного блока (60 : 40), и случаем, описанным в [29] для фазы Ауривиллиуса состава Bi6Fe2Ti3O18 (m = 5) после ее длительной термообработки, т.е. после установления близкого к равновесному распределению компонентов между структурно-неэквивалентными позициями – 78 : 22 (табл. 2). Следует отметить, что дальнейшая термообработка образцов 2 и 4 при более высокой температуре приводит к уменьшению отношения D1 : D2 в обоих образцах до значений 56 : 44 и 51 : 49 соответственно. Причем в образце 4 это уменьшение выражено больше, чем в образце 2 (табл. 2). Учитывая наличие некоторого количества аморфной фазы в образцах после термообработки при 450°С, которое, как следует из данных рентгенодифракционного и мессбауэровского исследований, невелико при синтезе соединений Bim+ 1Fem– 3Ti3O3m+ 3 с m ≤ 5, но резко возрастает при синтезе фаз Ауривиллиуса с m > 5, указанное выше изменение в распределении ионов железа по позициям можно объяснить следующим образом. При высокотемпературной обработке (850, 890°С) в перовскитоподобные блоки фаз Ауривиллиуса (m ≈ 5), сформировавшихся при 450°С, встраиваются компоненты из аморфной фазы на основе BiFeO3. Причем, как можно заключить на основе данных мессбауэровской спектроскопии, встраивание BiFeO3 происходит, по-видимому, в основном через наружные (B2) слои перовскитоподобных блоков (рис. 5). Более длительная термическая обработка, приводящая к установлению более равновесного распределения компонентов по подрешеткам в фазах Ауривиллиуса, является причиной перераспределения ионов железа и титана между внутренними и внешними слоями в перовскитоподобном блоке. В соответствии с этим ионы железа, как было показано в работе [29], будут иначе распределены по структурно-неэквивалентным позициям. Данный результат показывает, что в зависимости от способа, условий и этапа (продолжительности процесса) синтеза фаз Ауривиллиуса может наблюдаться различное распределение ионов железа и титана между внутренними и наружными слоями перовскитоподобного блока. Это объясняет, по-видимому, наблюдающееся в работах [6, 27, 29] различие в соотношениях компонентов, занимающих позиции В1 и В2.
Рис. 5.
Мессбауэровские спектры образцов с номинальным значением m = 5 и 7 после разных стадий термообработки (в скобках указано реальное значение m, соответствующее параметрам спектров).
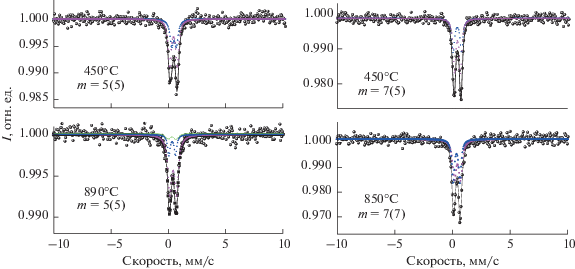
Таблица 2.
Параметры разложения мессбауэровских спектров, фазовое состояние и размер кристаллитов веществ
| Вещество | m/(m0) | Т, °С | Компонент | IS ± 0.02, мм/с |
QS ± 0.03, мм/с |
A, % | Структурная позиция | Фазовое состояние | d, нм | Источник |
|---|---|---|---|---|---|---|---|---|---|---|
| Образец 2 | 5/(5) | 450 | Дуплет 1 | 0.410 | 0.574 | 69 | B(1) | Кристаллическое | 39 | – |
| Дуплет 2 | 0.280 | 0.604 | 31 | B(2) | ||||||
| 890 | Дуплет 1 | 0.406 | 0.603 | 56 | B(1) | Кристаллическое | 116 | – | ||
| Дуплет 2 | 0.314 | 0.615 | 44 | B(2) | ||||||
| Bi6Fe2Ti3O18 | 5 | – | Дуплет 1 | 0.36 | 0.56 | 78 | B(1) | Кристаллическое | >100 | [29] |
| Дуплет 2 | 0.27 | 0.63 | 22 | B(2) | ||||||
| Образец 4 | 7/(5) | 450 | Дуплет 1 | 0.412 | 0.573 | 54 | B(1) | Кристаллическое + + аморфное | 39 | – |
| Дуплет 2 | 0.268 | 0.571 | 35 | B(2) | ||||||
| Дуплет 3 | 0.318 | 1.258 | 11 | – | – | |||||
| 7/(7) | 850 | Дуплет 1 | 0.406 | 0.560 | 51 | B(1) | Кристаллическое | 80 | – | |
| Дуплет 2 | 0.322 | 0.588 | 49 | B(2) | ||||||
| Bi8Fe4Ti3O24 | 7 | – | Дуплет 1 | 0.38 | 0.57 | 73 | B(1) | Кристаллическое | >100 | [29] |
| Дуплет 2 | 0.31 | 0.61 | 27 | B(2) | ||||||
| BiFeO3 | ∞ | – | Дуплет 1 | 0.30 | 1.06 | 50.9 | – | Аморфное | – | [36] |
| Дуплет 2 | 0.32 | 0.65 | 49.1 | – |
Важной составляющей исследования процессов формирования нанокристаллических фаз является анализ изменения размеров кристаллитов в ходе фазообразования. Построенная по экспериментальным данным зависимость размеров кристаллитов (d) от температуры (рис. 6) типична для поведения нанокристаллов, размер которых, как правило, увеличивается с повышением температуры синтеза. Для малослойных соединений (m ≤ 5) с d > 100 нм зависимость d(m) носит оценочный характер, но позволяет охарактеризовать общую тенденцию увеличения размера кристаллитов при нагревании. На рис. 6 можно выделить два вида зависимости d(T) для соединений Bim + 1Fem– 3Ti3O3m+ 3 с 3 ≤ m ≤ 5 и для фаз Ауривиллиуса с номинальными значениями m > 5. В первом случае наблюдается хорошо заметная тенденция к росту размеров кристаллитов с повышением температуры. Это связано, по-видимому, с увеличением скорости массопереноса между нанокристаллами образовавшейся фазы с ростом температуры синтеза. Во втором случае при m > 5 тенденция к росту кристаллитов с повышением температуры менее выражена.
Рис. 6.
Зависимость размера кристаллитов d от температуры синтеза и номинального значения m (голубая область – для m ≤ 5, оранжевая область – для m > 5).
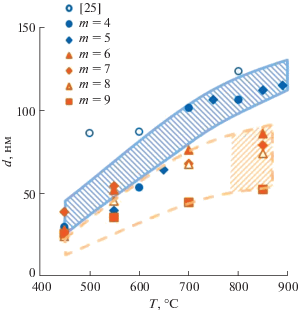
Объяснение подобных различий может быть связано как с затрудненностью процесса перекристаллизации многослойных фаз Ауривиллиуса из-за уменьшения скорости диффузии (так как в сложных оксидных фазах для роста частиц требуется сопряженный массоперенос многих компонентов, чтобы обеспечить постоянство состава кристаллической фазы в процессе диффузии), так и с особенностями описанного выше механизма формирования фаз Ауривиллиуса с большим числом слоев в перовскитоподобном пакете (m > 5). Поскольку при температуре ~450°С, как было показано выше, формируются нанокристаллы Bim+ 1Fem– 3Ti3O3m+ 3 с m ≈ 5 в тех случаях, когда образцы по своему составу соответствуют фазам Ауривиллиуса со значениями m > 5, можно сделать вывод, что рост кристаллитов в большой степени определяется изменением состава образовавшихся на начальном этапе синтеза соединений путем встраивания в их перовскитоподобные блоки компонентов аморфной фазы.
Таким образом, проведенное исследование процесса синтеза фаз Ауривиллиуса при термообработке соосажденных гидроксидов висмута железа и титана позволило предложить и с помощью синхронного термического анализа, рентгенодифракционного и мессбауэровского исследований обосновать механизм их формирования, схематически представленный на рис. 4.
ЗАКЛЮЧЕНИЕ
Показано, что формирование фаз Ауривиллиуса при термообработке смеси соосажденных гидроксидов стартует при 450°С после дегидратации гидроксидов. Соединения Bim+ 1Fem– 3Ti3O3m+ 3 с m ≤ 5 образуются в один этап. Синтез многослойных фаз Ауривиллиуса с m > 5 происходит в два этапа. На первом этапе после разложения соосажденных гидроксидов образуется фаза с m ≈ 5 и аморфная фаза на основе BiFeO3. Дальнейшая более высокотемпературная обработка приводит к встраиванию компонентов аморфной фазы в перовскитоподобный блок фазы Ауривиллиуса, что приводит к увеличению числа слоев m до получения заданного по синтезу соотношения элементов в соединении Bim+ 1Fem– 3Ti3O3m+ 3. При этом встраивание компонентов происходит через наружные слои перовскитоподобного блока. Поскольку такое встраивание не отвечает равновесному распределению компонентов по структурно-неэквивалентным позициям в перовскитоподобных блоках фаз Ауривиллиуса, на следующем этапе идет процесс установления внутрикристаллического равновесия с перераспределением компонентов в решетке фаз Ауривиллиуса.
Список литературы
Keeney L., Smith R.J., Palizdar M. et al. // Adv. Electron. Mater. 2020. V. 6. № 3. P. 1901264. https://doi.org/10.1002/aelm.201901264
Mitrofanova A.V., Fortal’nova E.A., Safronenko M.G. et al. // Russ. J. Inorg. Chem. 2020. V. 65. P. 1654. [Митрофанова А.В., Фортальнова Е.А., Сафроненко М.Г. и др. // Журн. неорган. химии. 2020. Т. 65. № 11. С. 1461.]https://doi.org/10.1134/S0036023620110133
Pikul T., Dzik J., Guzdek P. et al. // Ceram. Int. 2017. V. 43. № 14. P. 11442. https://doi.org/10.1016/j.ceramint.2017.06.008
Steciuk G., Boullay Ph., Pautrat A. et al. // Inorg. Chem. 2016. V. 55. № 17. P. 8881. https://doi.org/10.1021/acs.inorgchem.6b01373
Shujie Sun, Changhui Liu, Guopeng Wang et al. // J. Am. Ceram. Soc. 2016. V. 99. № 9. P. 3033. https://doi.org/10.1111/jace.14312
Birenbaum A.Y., Ederer C. // Phys. Rev. B. 2014. V. 90. P. 214109. https://doi.org/10.1103/PhysRevB.90.21410
Knyazev A.V., Krasheninnikova O.V., Korokin V.Z. // Inorg. Mater. 2014. V. 50. P. 170. [Князев А.В., Крашенинникова О.В., Корокин В.З. // Неорган. материалы. 2014. Т. 50. С. 188.]https://doi.org/10.1134/S0020168514020083
Lomanova N.A., Morozov M.I., Ugolkov V.L. et al. // Inorg. Mater. 2006. V. 42. № 2. P. 189. [Ломанова Н.А., Морозов М.И., Уголков В.Л. и др. // Неорган. материалы. 2006. Т. 42. № 2. С. 225.]https://doi.org/10.1134/S0020168506020142
Lomanova N.A., Gusarov V.V. // Russ. J. Inorg. Chem. 2011. V. 56. P. 616. [Ломанова Н.А., Гусаров В.В. // Журн. неорган. химии. 2011. Т. 56. С. 661.]https://doi.org/10.1134/S0036023611040188
Meera A.V., Ganesan Rajesh, Gnanasekaran T. // J. Alloys Compd. 2019. V. 790. P. 1108. https://doi.org/10.1016/j.jallcom.2019.03.205
Selbach S.M., Einarsrud M.-A., Grande T. // Chem. Mater. 2009. V. 21. № 1. P. 169. https://doi.org/10.1021/cm802607p
Akbashev A.R., Kaul A.R. // Russ. Chem. Rev. 2011. V. 80. P. 1159. [Акбашев А.Р., Кауль А.Р. // Успехи химии. 2011. Т. 80. № 12. С. 1211.]https://doi.org/10.1070/RC2011v080n12ABEH004239
Haumont R., Saint-Martin R., Byl C. // Phase Transitions. 2008. V. 81. P. 881. https://doi.org/10.1080/01411590802328642
Morozov M.I., Gusarov V.V. // Inorg. Mater. 2002. V. 38. № 7. P. 723. [Морозов М.И., Гусаров В.В. // Неорган. материалы. 2002. Т. 38. № 7. С. 867.]https://doi.org/10.1023/A:1016252727831
Chen Zhi-hui, Qiu Jun-fu, Liu Cheng et al. // Ceram. Int. 2010. V. 36. P. 241. https://doi.org/10.1016/j.ceramint.2009.07.022
Chen Zh., Yu Y., Hu J. et al. // J. Ceram. Soc. Jpn. 2009. V. 117. № 3. P. 264. https://doi.org/10.2109/jcersj2.117.264
Kan Y., Wang P., Li Y. et al. // Mater. Lett. 2002. V. 56. P. 910. https://doi.org/10.1016/S0167-577X(02)00636-5
Zhang F., Karaki T., Adachi M. // Jpn. J. Appl. Phys. 2006. V. 45. № 9B. P. 7385. https://doi.org/10.1143/JJAP.45.7385
García-Guaderrama M., Fuentes-Cobas L., Montero-Cabrera M.E. et al. // Integrated Ferroelectrics. 2005. V. 71. № 1. P. 233. https://doi.org/10.1080/10584580590965401
Sun S., Wang W., Xu H. et al. // J. Phys. Chem. C. 2008. V. 112. P. 17835. https://doi.org/10.1021/jp807379c
Hailili R., Wang Zh.-Q., Xu M. et al. // J. Mater. Chem. A. 2017. V. 5. P. 21275. https://doi.org/10.1039/c7ta06618j
Zhang H., Ke H., Ying P. et al. // J. Sol-Gel Sci. Technol. 2018. V. 85. P. 132. https://doi.org/10.1007/s10971-017-4530-9
Thomazinia D., Gelfuso M.V., Eiras J.A. // Powder Technol. 2012. V. 222. P. 139. https://doi.org/10.1016/j.powtec.2012.02.021
Li X., Ju Zh., Li F. et al. // J. Mater.Chem. A. 2014. V. 2. P. 13366. https://doi.org/10.1039/c4ta01799d
Lomanova N.A., Tomkovich M.V., Ugolkov V.A. et al. // Russ. J. Appl. Chem. 2017. V. 90. № 6. Р. 831. [Ломанова Н.А., Томкович М.В., Уголков В.Л. и др. // Журн. прикл. химии. 2017. Т. 90. № 6. С. 673.]https://doi.org/10.1134/S1070427217060015
Lomanova N.A., Gusarov V.V. // Russ. J. Inorg. Chem. 2010. V. 55. № 10. P. 1541. [Ломанова Н.А., Гусаров В.В. // Журн. неорган. химии. 2010. Т. 55. № 10. С. 1634.]https://doi.org/10.1134/S0036023610100086
Mazurek M., Jartych E. // Nukleonika. 2017. V. 62. № 2. P. 153. https://doi.org/10.1515/nuka-2017-0023
Paneva D., Dimitrov M., Velinov N. et al. // J. Phys.: Conf. Ser. 2010. V. 217. P. 012043. https://doi.org/10.1088/1742-6596/217/1/012043
Lomanova N.A., Semenov V.G., Panchuk V.V. et al. // J. Alloys Compd. 2012. V. 528. P. 103. https://doi.org/10.1016/j.jallcom.2012.03.040
Prajapat D., Sagdeo A., Raghavendra Reddy V. // Ceram. Int. 2019. V. 45. № 15. P. 19093.https://doi.org/10.1016/j.ceramint.2019.06.154
Jartych E., Pikula T., Mazurek M. et al. // J. Magn. Magn. Mater. 2013. V. 342. P. 27. https://doi.org/10.1016/j.jmmm.2013.04.046
Saha J., Jana Y.M., Mukherjee G.D. et al. // Mater. Chem. Phys. 2020. V. 240. № 15. P. 122286. https://doi.org/10.1016/j.matchemphys.2019.122286
Albadi Y., Sirotkin A.A., Semenov V.G. et al. // Russ. Chem. Bull. 2020. V. 69. P. 1290. https://doi.org/10.1007/s11172-020-2900-x
Martinson K.D., Ivanov V.A., Chebanenko M.I. et al. // Nanosyst. Phys. Chem. Math. 2019. V. 10. № 6. P. 694. https://doi.org/10.17586/2220-8054-2019-10-6-694-700
Pikula T., Malesa B., Oleszak D. et al. // Solid State Commun. 2016. V. 246. P. 47. https://doi.org/10.1016/j.ssc.2016.08.001
Proskurina O.V., Abiev R.S., Danilovich D.P. et al. // Chem. Eng. Process. – Process Intensif. 2019. V.143. P. 107 598 https://doi.org/10.1016/j.cep.2019.107598
Koval V., Shi Y., Skorvanek I. et al. // J. Mater. Chem. C. 2020. V. 8. P. 8466. https://doi.org/10.1039/D0TC01443E
Stolyarova V.L., Vorozhtcov V.A., Lopatin S.I. et al. // Thermochim. Acta. 2020. V. 685. P. 178531. https://doi.org/10.1016/j.tca.2020.178531
Kargin Yu.F., Ivicheva S.N., Volkov V.V. // Russ. J. Inorg. Chem. 2015. V. 60. № 5. P. 619. [Каргин Ю.Ф., Ивичева С.Н., Волков В.В. // Журн. неорган. химии. 2015. Т. 60. № 5. С. 691.] https://doi.org/10.1134/S0036023615050083
Risold D., Hallstedt B., Gauckler L.J. et al. // JPE. 1995. V. 16. P. 223. https://doi.org/10.1007/BF02667306
Gusarov V.V., Suvorov S.A. // J. Appl. Chem. 1990. V. 63. № 8. P. 1560.
Lomanova N.A., Tomkovich M.V., Sokolov V.V. et al. // J. Nanopart. Res. 2018. V. 20. № 17. https://doi.org/10.1007/s11051-018-4125-6
Matin M.A., Rhaman M.M., Hossain M.N. et al. // Trans. Electr. Electron. Mater. 2019. V. 20. P. 485. https://doi.org/10.1007/s42341-019-00140-8
Egorysheva A.V., Kuvshinova T.B., Volodin V.D. et al. // Inorg. Mater. 2013. V. 49. № 3. P. 310. [Егорышева А.В., Кувшинова Т.В., Володин В.Д. и др. // Неорган. материалы. 2013. Т. 49. № 3. С. 316.] https://doi.org/10.1134/S0020168513030035
Dmitriev A.V., Vladimirova E.V., Kandaurov M.V. et al. // J. Alloys Compd. 2019. V. 777. № 10. P. 586. https://doi.org/10.1016/j.jallcom.2018.10.387
Proskurina O.V., Tomkovich M.V., Bachina A.K. et al. // Russ. J. Gen. Chem. 2017. V. 87. № 11. Р. 2507. [Проскурина О.В., Томкович М.В., Бачина А.К. и др. // Журн. общ. химии. 2017. Т. 87. № 11. P. 1761.]https://doi.org/10.1134/S1070363217110019
Proskurina O.V., Nogovitsin I.V., Il’ina T.S. et al. // Russ. J. Gen. Chem. 2018. V. 88. P. 2139. [Проскурина О.В., Ноговицин И.В., Ильина Т.С. и др. // Журн. общ. химии. 2018. Т. 10. С. 1699.] https://doi.org/10.1134/S1070363218100183
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии