Журнал неорганической химии, 2021, T. 66, № 3, стр. 336-343
Синтез и свойства соединений соинтеркалирования нитрата графита со сложными эфирами карбоновых кислот
А. А. Давыдова a, Е. В. Ракша a, *, В. А. Глазунова b, О. Н. Осколкова a, В. В. Гнатовская a, П. В. Сухов a, В. В. Бурховецкий b, Г. К. Волкова b, Ю. В. Берестнева c, М. В. Савоськин a
a Институт физико-органической химии и углехимии им. Л.М. Литвиненко
283114 Донецк, ул. Р. Люксембург, 70, Украина
b Донецкий физико-технический институт им. А.А. Галкина
283114 Донецк, ул. Р. Люксембург, 72, Украина
c Федеральный научный центр агроэкологии, комплексных мелиораций и защитного лесоразведения РАН
400062 Волгоград, Университетский пр-т, 97, Россия
* E-mail: elenaraksha411@gmail.com
Поступила в редакцию 25.06.2020
После доработки 27.08.2020
Принята к публикации 09.09.2020
Аннотация
С целью расширения ряда возможных предшественников углеродных наночастиц − малослойных графенов и наносвитков – синтезированы бинарные и тройные соединения соинтеркалирования нитрата графита (ССНГ) со сложными эфирами муравьиной и уксусной кислот. Методом рентгенофазового анализа установлено, что полученные ССНГ представляют собой соединения II-ой и IV-ой стадий интеркалирования. Показано, что использование этилформиата или смеси этилацетат/бутилацетат в качестве соинтеркалантов ведет к увеличению высоты заполненного интеркалантами слоя по сравнению с нитратом графита. Путем расслоения ССНГ в этиловом спирте при содействии ультразвука получены дисперсии углеродных наночастиц − малослойных графенов и наносвитков. Морфология полученных наночастиц исследована методом просвечивающей электронной микроскопии.
ВВЕДЕНИЕ
Для получения коллоидных дисперсий графена и других углеродных наночастиц [1] в качестве предшественников можно использовать как природный или высокоориентированный пиролитический графит, так и другие материалы, в структуре которых содержатся графеновые слои, например, соединения интеркалирования графита. Такие соединения образуются при внедрении между слоями кристаллической решетки графита частиц интеркалантов [2–4]. При этом межплоскостные расстояния между соседними слоями графита сильно увеличиваются, что способствует генерированию наночастиц в мягких условиях.
Для расщепления графитовой матрицы необходимо преодолеть силы притяжения, существующие между индивидуальными углеродными слоями в предшественнике, а также стабилизировать образующиеся углеродные наночастицы. На данный момент одним из перспективных методов получения углеродных наночастиц [4, 5] является расслоение графита и его соединений интеркалирования в жидких средах под действием ультразвука [6–8]. Данный подход открывает перспективу получения как однослойных и малослойных графеновых частиц, так и родственных им наносвитков и рассматривается как возможный метод коммерческого производства графена и графеноподобных частиц [9].
В данной работе представлены результаты исследования особенностей структуры новых бинарных и тройных соединений соинтеркалирования нитрата графита (ССНГ) со сложными эфирами карбоновых кислот: этилформиатом, этилацетатом и бутилацетатом (табл. 1), а также способности полученных ССНГ к термическому расширению, показана возможность получения на их основе дисперсий углеродных наночастиц.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали природный чешуйчатый графит Завальевского месторождения (Украина) марки ГТ-1 по ГОСТ 4596-75, исходная зольность которого составляла 4.56%. Предварительно графит обеззоливали обработкой концентрированными соляной и плавиковой кислотами в три этапа: 1 – кипячение в HCl; 2 – обработка HF; 3 – повторное кипячение в HCl. На каждом этапе определяли зольность графита по ГОСТ 17818.4-90. Зольность графита после очистки составила 0.01%.
Синтез ССНГ A–F проводили в термостатируемом реакторе при 20°C. К навеске графита ГТ-1 добавляли азотную кислоту (ρ = 1.505 г/см3) и перемешивали смесь в течение 10 мин. Затем нитрат графита обрабатывали одним (синтез соединений A, B, C) или двумя (синтез соединений D, E, F) соинтеркалантами и перемешивали еще 10 мин. При получении тройных соединений D–F органические соинтеркаланты добавляли последовательно сразу один за другим в равных по объему количествах. Расход дымящей азотной кислоты и соинтеркалантов составлял 0.6 и 6 см3/г соответственно. Образующийся продукт отделяли фильтрованием и сушили при 20°C до постоянной массы.
Особенности структуры графита и ССНГ исследовали методом рентгенофазового анализа (РФА) с помощью дифрактометра ДРОН-3 с использованием CuKα-излучения (λα = 1.54181 Å, U = 30 кВ, I = 20 мА). Для исследований методом РФА использовали свежеприготовленные образцы ССНГ и нитрата графита.
На основе угловых положений пиков на дифрактограммах для нитрата графита и ССНГ определены значения периода идентичности и высоты заполненного интеркалантом слоя [3]. Период идентичности (IС, Å) рассчитывали в соответствии с уравнением: ${{I}_{C}} = l\frac{\lambda }{{2\sin {{\theta }_{i}}}},$ где λ – длина волны излучения (Å), θi – угол скольжения (°), l – порядок отражения под углом θi.
Порядок отражения l максимальной интенсивности связан с номером стадии интеркалирования нитрата графита и ССНГ n соотношением l = n + 1. Высоту заполненного интеркалантами слоя (di, Å) для нитрата графита и ССНГ определяли из соотношения: di = IC – (n – 1) × 3.360, где IС – период идентичности (Å), n – номер стадии интеркалирования (число графитовых плоскостей между соседними слоями интеркаланта), 3.360 Å – межплоскостное расстояние в исходном графите.
Коэффициент термического расширения (KV, см3/г) полученных ССНГ определяли при ударном режиме нагревания (900°C, муфельная печь Fisher Scientific Isotemp ® Model 650 Programmable Muffle Furnace). Величину KV рассчитывали по формуле: ${{K}_{V}} = \frac{V}{m},$ где KV – коэффициент термического расширения (см3/г), V – объем графитовой пены (см3), m – масса навески ССНГ (г).
Морфологию поверхности частиц исходного графита, нитрата графита и ССНГ исследовали с помощью растрового (сканирующего) электронного микроскопа JSM-6490LV (Япония).
Дисперсии углеродных наночастиц получали путем обработки ССНГ ультразвуком на установке И100-6 с рабочими параметрами: 22 кГц, 315, 470 и 630 Вт (ультразвуковая техника Инлаб, Россия) в этаноле в течение 1 ч. Свежеприготовленные дисперсии центрифугировали в течение 5–7 мин (3000 об/мин, центрифуга ОПН-3) и анализировали с использованием спектрофотометра Helios Gamma (Thermo Electron Corporation, США) в диапазоне длин волн 200–600 нм.
Исследования морфологии и внутренней структуры углеродных наночастиц проводили с использованием микроскопа JEM-200А фирмы JEOL. Образцы для просвечивающей электронной микроскопии (ПЭМ) формировали из дисперсий ССНГ на специально покрытых углеродом медных сетках путем помещения капли дисперсии на сетку. Электронно-микроскопическое изображение или картину электронной дифракции для определения кристаллической структуры образца получали путем изменения напряженности поля магнитных линз.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
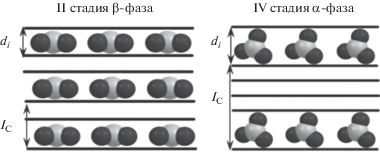
Дымящая азотная кислота при взаимодействии с графитом обладает свойствами как интеркаланта, так и окислителя, т.е. является самостоятельно внедряющимся интеркалантом. Поэтому для получения нитрата графита не требуется дополнительных реагентов. Соединения интеркалирования графита с азотной кислотой имеют специфическую слоистую структуру: двумерные квазижидкие слои интеркаланта не связаны с графитовой матрицей ковалентными связями и обладают высокой лабильностью. На первом этапе образуется кристаллическая α-фаза нитрата графита, которая характеризуется стехиометрией ${\text{C}}_{{24n}}^{ + } \cdot {\text{NO}}_{3}^{ - } \cdot 5{\text{HN}}{{{\text{O}}}_{3}},$ где n – номер стадии интеркалирования, и высотой заполненного слоя 0.780 нм [10]. Со временем она переходит в β-фазу с высотой заполненного слоя 0.655 нм и стехиометрией ${\text{C}}_{{24n}}^{ + } \cdot {\text{NO}}_{3}^{ - } \cdot 2{\text{HN}}{{{\text{O}}}_{3}}$ [11]. В обзоре [12] приведены успехи синтеза, изучения свойств и получения углеродных материалов на основе широкого ряда соединений интеркалирования графита акцепторного типа и нитрата графита в том числе. Известны бинарные [13–15] и тройные [16–18] соединения соинтеркалирования нитрата графита с органическими соединениями. Установлено [3, 13–18], что модификация нитрата графита органическими соединениями ведет к его дополнительной стабилизации и в то же время способствует значительному увеличению способности к термическому расширению. Общая схема синтеза нитрата графита и его соединений соинтеркалирования (1) включает взаимодействие графита с азотной кислотой с образованием нитрата графита и его последующее соинтеркалирование сложными эфирами карбоновых кислот. Как исходный нитрат графита, так и полученные на его основе соединения соинтеркалирования A–F характеризуются структурой, схематически представленной на рис. 1.
(1)
$\begin{gathered} {\text{C}}\xrightarrow{{{\text{HN}}{{{\text{O}}}_{3}}}}{\text{C}}_{{24n}}^{ + } \cdot {\text{NO}}_{3}^{ - } \cdot xHN{{O}_{3}}\xrightarrow{{{\text{Int}}}} \\ \to {\text{C}}_{{24n}}^{ + } \cdot {\text{NO}}_{3}^{ - } \cdot (x - y){\text{HN}}{{{\text{O}}}_{3}} \cdot y{\text{Int}}, \\ \end{gathered} $Морфология поверхности частиц исходного графита, а также полученных ССНГ A–F исследована методом сканирующей электронной микроскопии (СЭМ). Все образцы обладают слоистой структурой (рис. 2). Частицы ССНГ на основе этилформиата (A), высушенные на воздухе при комнатной температуре, демонстрируют подвспученную структуру даже без дополнительной термообработки и еще до помещения в вакуумную камеру электронного микроскопа (рис. 2б). По-видимому, в процессе синтеза этого ССНГ происходит так называемое химическое или реагентное вспучивание. Это можно объяснить частичным гидролизом этилформиата в кислой среде до этанола и муравьиной кислоты (2) и экзотермической реакцией последней с азотной кислотой с выделением большого количества газообразных продуктов – CO2 и NO2 (3). Данный факт открывает новые перспективы использования указанного ССНГ в получении графеноподобных наночастиц на его основе.
(2)
${\text{HCOO}}{{{\text{C}}}_{2}}{{{\text{H}}}_{5}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}}\xrightarrow{{{{{\text{H}}}^{ + }}}}{{{\text{C}}}_{{\text{2}}}}{{{\text{H}}}_{{\text{5}}}}{\text{OH}} + {\text{HCOOH}},$(3)
$HCOOH\,\, + 2{\kern 1pt} {\text{HN}}{{{\text{O}}}_{3}} \to C{{O}_{2}}\,\, + 2{\kern 1pt} N{{O}_{2}}\,\, + 2{{{\text{H}}}_{2}}{\text{O}}.$Рис. 2.
Типичные СЭМ-микрофотографии исходного графита (а) и соинтеркалантов нитрата графита: (б – A, в – D, г – F).

Полученный ряд бинарных и тройных ССНГ характеризуется достаточно высокими значениями коэффициента вспучивания – от 275 до 340 см3/г (табл. 2). Для тройных соединений D–F значение KV превышает величины для соответствующих бинарных ССНГ, что косвенно указывает на повышение мольной доли соинтеркалантов в межслоевом пространстве.
Таблица 2.
Структурные характеристики нитрата графита и его соединений соинтеркалирования (A–F), по данным РФА, и коэффициенты вспучивания ССНГ
| Объект | IV стадия, α-фаза | II стадия, β-фаза | KV, cм3/г | ||||
|---|---|---|---|---|---|---|---|
| 2θ, град | IC, Å | di, Å | 2θ, град | IC, Å | di, Å | ||
| Нитрат графита | 25.00 | 17.809 | 7.729 | 26.76 | 9.994 | 6.634 | 250 |
| ССНГ | |||||||
| A | 25.36 | 17.560 | 7.480 | 26.68 | 10.023 | 6.663 | 320 |
| B | 25.12 | 17.725 | 7.645 | 27.12 | 9.864 | 6.504 | 275 |
| C | 25.12 | 17.725 | 7.645 | 26.76 | 9.994 | 6.634 | 295 |
| D | 25.04 | 17.781 | 7.701 | 27.16 | 9.850 | 6.490 | 340 |
| E | 25.24 | 17.642 | 7.562 | 26.80 | 9.979 | 6.619 | 325 |
| F | 24.72 | 18.007 | 7.927 | 26.96 | 9.921 | 6.561 | 315 |
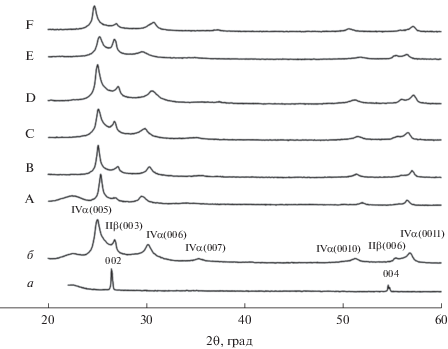
Структурные изменения графита при его взаимодействии с азотной кислотой и последующей обработке сложными эфирами муравьиной и уксусной кислот исследованы методом РФА. Рис. 3 иллюстрирует дифрактограммы исходного графита, нитрата графита и ССНГ в координатах I0.5–2θ в диапазоне значений 2θ = 20°–60°. Анализ дифрактограмм полученных продуктов показал, что все исследуемые эфиры образуют с нитратом графита соединения соинтеркалирования. Дифрактограммы свежеприготовленных образцов ССНГ по своему виду мало отличаются от дифрактограммы нитрата графита, однако наблюдается смещение рефлексов в сторону бóльших или меньших углов. Индицирование дифрактограмм бинарных и тройных ССНГ (A–F), выполненное по аналогии с нитратом графита и бинарными ССНГ [3, 15], выявило наличие в исследуемых соинтеркалантах соединений II-ой (β-фаза) и IV-ой (α-фаза) стадий интеркалирования. Фазовый состав продуктов синтеза соединений интеркалирования графита с азотной кислотой в значительной степени определяется концентрацией кислоты и наличием влаги в окружающей среде [19–21]. Различия в фазовом составе полученных соединений интеркалирования с данными авторов [19–21] обусловлены разными условиями синтеза. В отсутствие инертной атмосферы на первом этапе, по-видимому, образуется соединение II-ой стадии (α-фаза), которое далее реагирует по двум направлениям. Первое – потеря интеркалантов с превращением в соединение IV-ой стадии (α-фаза). Второе – реакция соединения II-ой стадии (α-фаза) с влагой воздуха с образованием β-фазы. При этом в образцах нитрата графита и ССНГ одновременно присутствуют соединения II-ой и IV-ой стадий. Постепенное превращение α → β для соединения IV-ой стадии наблюдалось для нитрата-ацетата графита [3] при хранении образцов, а после обработки водой свежеприготовленного нитрата-ацетата графита в образце присутствовали только β-фазы соединений II-ой и IV-ой стадий [15]. Данные факты согласуются с выводами авторов [19, 20] о необходимости присутствия критического количества влаги для реализации перехода α → β. Отражения в области 2θ = 26.8° и 55.4°, определяемые нами как отражения 003 и 006 соединения II-ой стадии β-фазы для нитрата графита, присутствуют на дифрактограммах и после его обработки органическими соинтеркалантами А–F (рис. 3), уксусной кислотой [3, 15], смесью уксусной кислоты и этилформиата [17], после обработки нитрата-ацетата графита водой [15] и не могут быть обусловлены сорбцией соинтеркалантов на поверхности графита.
На основе данных дифрактограмм для нитрата графита и ССНГ определены значения периода идентичности (IC, Å) и высоты заполненного интеркалантом слоя (di, Å). В табл. 2 представлены соответствующие значения для соединений II-ой и IV-ой стадий интеркалирования. Анализ структурных параметров ССНГ, полученных методом РФА, выявил следующие особенности структурной реорганизации нитрата графита при обработке сложными эфирами карбоновых кислот. При образовании соинтеркалантов A–E для соединений IV-ой стадии интеркалирования наблюдается стабилизация структуры, о чем свидетельствует уменьшение высоты заполненного слоя на 0.03–0.25 Å по сравнению с нитратом графита. Аналогичный эффект наблюдается для соединений II-ой стадии интеркалирования при образовании соинтеркалантов B–F: высота заполненного частицами интеркалантов слоя уменьшается по сравнению с таковой для нитрата графита на 0.02–0.15 Å. Однако для соединений F (IV-ая стадия интеркалирования) и A (II-ая стадия интеркалирования) наблюдается обратный эффект – значение di увеличивается. Этот факт позволяет предложить, что соинтеркаланты A и F могут выступать в качестве эффективных предшественников углеродных наночастиц – малослойных графенов и родственных структур.
Ранее нами показано, что в результате расслоения нитрата графита в этаноле при содействии ультразвука образуются наносвитки [4]. Полученные ССНГ A и F также были испытаны в качестве предшественников углеродных наночастиц путем их обработки ультразвуком в среде этилового спирта. Для получения дисперсий углеродных наночастиц свежеприготовленный ССНГ обрабатывали ультразвуком в этиловом спирте в течение 1 ч и анализировали дисперсию методом УФ-спектроскопии, который используется для количественного определения как однослойного графена, так и малослойных графенов в различных растворителях [22–25]. Для водных дисперсий графена, полученных восстановлением оксида графена гидразингидратом [22], а также расслоением соединений интеркалирования графита [25], максимум поглощения в УФ-спектре наблюдается при 268–269 нм. Для дисперсии графена в этаноле, полученной расслоением графита под действием ультразвука, максимум поглощения наблюдался в области 255–270 нм [24]. В ацетонитриле дисперсии, полученные расслоением различных прекурсоров графена под действием ультразвука, демонстрировали максимум абсорбции при 273 нм [25]. Анализ спектров поглощения дисперсий углеродных наночастиц, полученных ультразвуковой обработкой ССНГ A и F в среде этилового спирта, в диапазоне длин волн 250–350 нм выявил следующие особенности. Увеличение мощности УЗ-обработки ожидаемо ведет к увеличению числа частиц при расслоении ССНГ в среде этилового спирта. УФ-спектры полученных дисперсий наночастиц в этиловом спирте (рис. 4) помимо ожидаемого максимума в области 273–275 нм содержат еще один в области 279–285 нм. Батохромный сдвиг максимума поглощения обусловлен присутствием интеркалантов – азотной кислоты и соответствующих сложных эфиров. Появление двух максимумов поглощения в диапазоне 250–350 нм обусловлено, возможно, как наличием в исследуемых дисперсиях наночастиц с различным типом морфологии, так и присутствием незначительного количества карбонильных групп. При взаимодействии графита с азотной кислотой возможно окисление его поверхности с образованием кислородсодержащих групп, но для получения оксида графита, дисперсии которого имеют подобный характер спектра поглощения, требуется наличие дополнительного окислителя [26]. Образование заметного числа продуктов окисления графита проявилось бы и в виде дополнительных отражений на дифрактограммах в области 2θ = 8°–22° [26–28]. Генерирование углеродных наночастиц разнообразной морфологии наблюдалось в процессе расслоения графита в жидкой среде под действием ультразвука [29]. Продолжительная обработка ультразвуком может индуцировать значительные морфологические изменения графеновых слоев, генерируемых при расслоении графита, с образованием нанолент, нановолокон, скручиванием графенов и нанолент в наносвитки [30–32]. При получении дисперсий ССНГ нельзя исключить и возможного окисления графеновых частиц, вызванного протеканием радикальных реакций в кавитационных полостях при обработке системы ультразвуком [29, 33]. И по аналогии с оксидом графена, дисперсии которого также имеют второй максимум в районе 300 нм [22, 34], можно допустить, что наблюдаемый для дисперсий ССНГ максимум поглощения при 279–285 нм обусловлен наличием С=О-групп. С другой стороны, показано, что наличие в системе небольших органических молекул снижает вероятность протекания реакций с участием графеновых частиц [33].
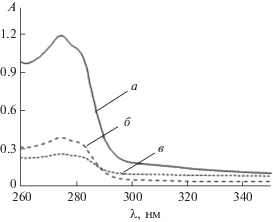
Рис. 4.
Типичные УФ-спектры дисперсий наночастиц, полученных при расслоении ССНГ в среде этилового спирта под действием ультразвука (а – ССНГ A, 315 Вт; б – ССНГ F, 470 Вт; в – ССНГ A, 470 Вт).
Анализ дисперсий, полученных при ультразвуковой обработке ССНГ в этиловом спирте методом ПЭМ показал, что таким образом могут быть получены углеродные наночастицы различной морфологии (рис. 5, 6). Планарные размеры отдельных малослойных графеновых частиц, полученных при расслоении ССНГ A на основе этилформиата (УЗ: 1 ч, 22 кГц, 315 Вт), достигают нескольких микрометров (рис. 5а). Однако в суспензии присутствуют также мелкие аморфные наноуглеродные частицы (рис. 5б). Увеличение мощности УЗ до 470 Вт ведет к уменьшению планарных размеров графеноподобных частиц и образованию в системе наносвитков, диаметр которых составляет 40–85 нм, а длина варьирует от 150 нм до 1 мкм (рис. 5в). В полученных таким образом образцах присутствуют агрегаты более крупных наносвитков (рис. 5г) длиной от 660 нм до 1.6 мкм. Помимо наносвитков суспензия содержит графеновые плоскости (рис. 5г, 5д), плоскостные размеры которых составляют 1–2 мкм. Для малослойных графеновых частиц (рис. 5д) получена типичная микроэлектронограмма, свидетельствующая о том, что анализируемый участок представляет собой кристаллическую структуру.
Рис. 5.
Типичные ПЭМ-микрофотографии наночастиц, полученных расслоением нитрата графита, соинтеркалированного этилформиатом (A), в этаноле при содействии ультразвука мощностью 315 Вт (а, б) и 470 Вт (в–д).

Рис. 6.
Типичные ПЭМ-микрофотографии наночастиц, полученных расслоением нитрата графита, соинтеркалированного этилацетатом и бутилацетатом (F), в этаноле при содействии ультразвука (470 Вт).

Аналогичные результаты получены в случае обработки свежеприготовленного образца соинтеркаланта F ультразвуком в этиловом спирте в течение 1 ч (470 Вт). В дисперсии присутствуют наночастицы различной морфологии − малослойные графены и наносвитки (рис. 6). Плоскостные размеры малослойных графенов достигают 1–2 мкм, края многих частиц подкручены. Длина наносвитков варьирует от 200 нм до 1–4 мкм, а диаметр составляет 15–130 нм.
Наличие в системе соинтеркалантов способствует стабилизации получаемых из ССНГ дисперсий наночастиц. Дисперсия, получаемая в этаноле из графита, неустойчива, и полное оседание частиц (разрушение) наблюдается уже через 4 ч [24]. Дисперсии соединений A и F в этаноле устойчивы в течение не менее 3 сут.
ЗАКЛЮЧЕНИЕ
Получен ряд новых бинарных и тройных соединений соинтеркалирования нитрата графита со сложными эфирами муравьиной и уксусной кислот. Бинарное ССНГ на основе этилформиата и тройное ССНГ на основе этил- и бутилацетата характеризуются бóльшим по сравнению с исходным нитратом графита значением высоты заполненного интеркалантом слоя. Расслоение этих ССНГ в этиловом спирте под действием ультразвука приводит к образованию углеродных наночастиц различной морфологии – малослойных графенов и наносвитков. Увеличение мощности УЗ-обработки от 315 до 470 Вт ведет к уменьшению планарных размеров образующихся наночастиц и способствует формированию наносвитков. Получаемые наночастицы могут быть использованы как армирующие наполнители для полимеров, резин и строительных материалов, а также как сенсоры, сорбционные материалы и подложки различных катализаторов.
Список литературы
Grayfer E.D., Makotchenko V.G., Nazarov A.S. et al. // Russ. Chem. Rev. 2011. V. 80. № 8. P. 784. [Грайфер Е.Д., Макотченко В.Г., Назаров А.С. и др. // Успехи химии. 2011. Т. 80. № 8. С. 784.]https://doi.org/10.1070/RC2011v080n08ABEH004181
Dresselhaus M.S., Dresselhaus G. // Adv. Phys. 2002. V. 51. № 1. P. 1. https://doi.org/10.1080/00018730110113644
Savoskin M.V., Yaroshenko A.P., Whyman G.E. et al. // J. Phys. Chem. Solids. 2006. V. 67. № 5–6. P. 1127. https://doi.org/10.1016/j.jpcs.2006.01.034
Savoskin M.V., Mochalin V.N., Yaroshenko A.P. et al. // Carbon. 2007. V. 45. № 14. P. 2797. https://doi.org/10.1016/j.carbon.2007.09.031
Xin Y., Sun B., Zhu X. et al. // Vacuum. 2018. V. 151. P. 90. https://doi.org/10.1016/j.vacuum.2018.02.006
Hernandez Y., Nikolosi V., Lotya M. et al. // Nat. Nanotechnol. 2008. V. 3. № 9. P. 563. https://doi.org/10.1038/nnano.2008.215
Edwards R.S., Coleman K.S. // Nanoscale. 2013. V. 5. № 1. P. 38. https://doi.org/10.1039/C2NR32629A
Yi M., Shen Z. // J. Mater. Chem. A. 2015. V. 3. № 22. P. 11 700. https://doi.org/10.1039/C5TA00252D
Arao Y., Mori F., Kubouchi M. // Carbon. 2017. V. 118. P. 18. https://doi.org/10.1016/j.carbon.2017.03.002
Touzain P. // Synth. Met. 1979. V. 1. № 1. P. 3. https://doi.org/10.1016/0379-6779(79)90003-1
Fuzellier H., Melin J., Herold A. // Mater. Sci. Eng. 1977. V. 3. P. 191. https://doi.org/10.1016/0025-5416(77)90018-0
Sorokina N.E., Nikol’skaya I.V., Ionov S.G. et al. // Russ. Chem. Bull. 2005. V. 54. № 8. P. 1749. [Сорокина Н.Е., Никольская И.В., Ионов С.Г. и др. // Изв. Академии наук, сер. хим. 2005. Т. 54. № 8. С. 1699.]https://doi.org/10.1007/s11172-006-0034-4
Рудаков Е.С., Савоськин М.В., Рудакова Р.И. и др. // А.с. 1614350 А1 СССР. Опубл. 20.02.1995
Maksimova M.V., Sorokina N.E., Shornikova O.N. et al. // J. Phys. Chem. Solids. 2004. V. 65. № 2–3. P. 177. https://doi.org/10.1016/j.jpcs.2003.10.013
Savoskin M.V., Yaroshenko A.P., Mysyk R.D. et al. // Theor. Experim. Chem. 2004. V. 40. P. 92. [Савоськин М.В., Ярошенко А.П., Мысык Р.Д. и др. // Теорет. и эксперим. химия. 2004. Т. 40. № 2. С. 88.]
Рудаков Е.С., Савоськин М.В., Рудакова Р.И. и др. // А.с. 1476785 А1 СССР. Опубл. 20.02.1995.
Ракша Е.В., Берестнева Ю.В., Вишневский В.Ю. и др. // Хим. физ. и мезоскопия. 2017. Т. 19. № 3. С. 448.
Raksha E.V., Davydova A.A., Berestneva Yu.V. et al. // Advanced Materials, Springer Proceedings in Materials 6 / Ed. Parinov I.A., Chang Sh.H., Long B.T. Springer International Publishing, 2020. P. 41. https://doi.org/10.1007/978-3-030-45120-2_4
Мищенко Н.М. Синтез, физико-химические превращения и диффузионные процессы в интеркалированных соединениях графита с азотной кислотой. Дис. … канд. хим. наук. Владивосток, 2001. 160 с.
Ziatdinov A.M., Mishchenko N.M. // J. Phys. Chem. Solids. 1997. V. 58. № 7. P. 1161. https://doi.org/10.1016/S0022-3697(96)00229-6
Авдеев В.В., Сорокина Н.Е., Тверезовская О.А. и др. // Вестн. Моск. ун-та. Сер. 2. Химия. 1999. Т. 40. № 6. С. 422.
Ciplak Z., Yildiz N., Calimli A. // Fullerenes, Nanotubes and Carbon Nanostructures. 2014. V. 23. № 4. P. 361. https://doi.org/10.1080/1536383X.2014.894025
Hayyan M., Abo-Hamad A., AlSaadi M.A. et al. // Nanoscale Res. Lett. 2015. V. 10. № 324. https://doi.org/10.1186/s11671-015-1004-2
Zhang X., Coleman A.C., Katsonis N. et al. // Chem. Commun. 2010. V. 46. № 40. P. 7539. https://doi.org/10.1039/c0cc02688c
Uran S., Alhani A., Silva C. // AIP Advances. 2017. V. 7. № 3. P. 035 323. https://doi.org/10.1063/1.4979607
Ziatdinov A.M., Saenko N.S., Skrylnik P.G. // Russ. J. Inorg. Chem. 2020. V. 65. № 1. P. 133. [Зиатдинов А.М., Саенко Н.С., Скрыльник П.Г. // Журн. неорган. химии. 2020. Т. 65. № 1. С. 131.]https://doi.org/10.1134/S0036023620010210
Buslaeva E.Yu., Kraevskii S.V., Groshkova Yu.A. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 1. P. 5. [Буслаева Е.Ю., Краевский С.В., Грошкова Ю.А. и др. // Журн. неорган. химии. 2020. Т. 65. № 1. С. 8.]https://doi.org/10.1134/S0036023620010040
Jankovský O., Nováček M., Luxa J. et al. // Chem. Eur. J. 2017. V. 23. P. 1. https://doi.org/10.1002/chem.201700809
Tapia J.I., Quintana M. Handbook of carbon nanomaterials (In 2 Volumes). Volume 5: Graphene – Fundamental Properties. World Scientific Publishing Co. Pte. Ltd., 2014. 549 p. https://doi.org/10.1142/9789814566704_0003
Viculis L.M., Mack J.J., Kaner R.B. // Science. 2003. V. 299. № 5611. P. 1361. https://doi.org/10.1126/science.1078842
Bang J.H., Suslick K.S. // Adv. Mater. 2010. V. 22. № 10. P. 1039. https://doi.org/10.1002/adma.200904093
Wang S., Tang L.A., Bao Q. et al. // J. Am. Chem. Soc. 2009. V. 131. № 46. P. 16832. https://doi.org/10.1021/ja905968v
Tapia J.I., Quintana M. // Mesoporous Biomater. 2016. V. 3. P. 76. https://doi.org/10.1515/mesbi-2016-0010
Stroyuk A.L., Andryushina N.S., Shcherban’ N.D. et al. // Theor. Experim. Chem. 2012. V. 48. P. 2. [Строюк А.Л., Андрюшина Н.С., Щербань Н.Д. и др. // Теорет. и эксперим. химия. 2012. Т. 48. № 1. С. 1.]https://doi.org/10.1007/s11237-012-9235-0
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии