Журнал неорганической химии, 2021, T. 66, № 12, стр. 1779-1791
Минерализация карбоната кальция в композитах поликапролактона с нанокристаллической целлюлозой: структура, морфология и сорбционные свойства
М. И. Воронова a, *, О. В. Суров a, Е. О. Лебедева b, Н. В. Рублева a, А. В. Афинеевский b, А. Г. Захаров a
a Институт химии растворов им. Г.А. Крестова РАН
153045 Иваново, ул. Академическая, 1, Россия
b Ивановский государственный химико-технологический университет
153000 Иваново, Шереметевский пр-т, 7, Россия
* E-mail: miv@isc-ras.ru
Поступила в редакцию 09.03.2021
После доработки 02.07.2021
Принята к публикации 05.07.2021
Аннотация
Изучено влияние нанокристаллической целлюлозы в составе композита с поликапролактоном на минерализацию карбоната кальция с образованием различных полиморфов (кальцит, ватерит). Композиты получены с использованием ацетонового органогеля нанокристаллической целлюлозы, а также нанокристаллической целлюлозы, поверхностно модифицированной поливинилпирролидоном. В качестве растворителей для получения композитов использовали диметилформамид, смесь растворителей диметилформамид-тетрагидрофуран и хлороформ. Наличие нанокристаллической целлюлозы в композите увеличивает его гидрофильность и пористость. Показано, что в пористых пленках кристаллизация карбоната кальция происходит и на поверхности, и в объеме пленки. Нанокристаллическая целлюлоза в составе композита способствует минерализации карбоната кальция в объеме пленки с образованием ватерита. Предложенный подход позволяет получать композиционные материалы биомедицинского назначения с заданными свойствами.
ВВЕДЕНИЕ
Карбонат кальция – широко распространенный в природе минерал. Он входит в состав горных пород, таких как мел, известняк, мрамор и океанические отложения [1], является биоминерализующим компонентом в жемчужинах, коралловых рифах, экзоскелетах членистоногих и моллюсков [2], играет важную роль в живых организмах, включая патогенные образования желчных и почечных камней, используется как наполнитель бумаги, резины, пластика и других материалов, входит в состав цемента, используется в производстве стали и при нейтрализации шлаков сталелитейного производства, находит применение в сельском хозяйстве для удобрения почв и в пищевой промышленности в качестве пищевой добавки.
Карбонат кальция образует несколько полиморфных модификаций: аморфный карбонат кальция, имеющий несколько форм с различным содержанием воды; две гидратированные кристаллические формы – гексагидрат CaCO3 ⋅ 6H2O (икаит) и моногидрокальцит CaCO3 ⋅ H2O; три дегидратированные кристаллические полиморфные модификации – кальцит, арагонит и ватерит [3–6].
Термодинамическая стабильность полиморфов уменьшается от кальцита к ватериту. Кальцит, арагонит и ватерит легко различить по форме кристаллов: кристаллы кальцита имеют кубическую форму, арагонита – игольчатую, ватерит кристаллизуется в виде пористых сфер.
С точки зрения создания систем адресной доставки лекарственных средств на основе неорганических носителей особый интерес представляет ватеритная модификация карбоната кальция [7, 8]. Преимуществом ватерита является его пористая структура, обеспечивающая возможность адсорбции различных веществ и их высвобождения при перекристаллизации [9]. Благодаря простоте получения, дешевизне, мягким условиям растворения, биодеградируемости и высокой биосовместимости высокопористые нано- и микросферы ватерита могут успешно использоваться в качестве контейнеров с целью пролонгированного и контролируемого высвобождения лекарственных соединений [10]. В этой связи актуальным является получение микросфер ватерита контролируемого размера, морфологии и внутренней структуры для дальнейшего биомедицинского применения.
Контроль морфологии и фазового состава карбоната кальция может быть осуществлен с использованием водонерастворимых полимерных каркасов (скаффолдов), используемых в качестве шаблонов при кристаллизации, например, поликапролактона [11].
Поликапролактон (ПКЛ) – гидрофобный, полукристаллический полимер с низкой температурой плавления (55–60°С), имеющий линейно-разветвленную структуру и относящийся к алифатическим сложным полиэфирам: [–(CH2)5–CO–O–]n. ПКЛ обладает хорошими формовочными свойствами и является биосовместимым и биодеградируемым полимером. ПКЛ применяется в качестве материала для изготовления полимерных изделий медицинского назначения, имплантатов для заместительной хирургии, в системах доставки лекарственных средств и в тканевой инженерии [12]. Однако применение чистого ПКЛ ограничено его высокой гидрофобностью, низкой температурой плавления, невысокой механической прочностью. Для улучшения полезных свойств материалов на основе ПКЛ и расширения области его применения используют различные наполнители и армирующие добавки, в том числе нанокристаллическую целлюлозу (НКЦ) [13, 14]. Кроме того, при изучении процессов биоминерализации давно обратили внимание на роль полисахаридов при кристаллизации определенных полиморфов CaCO3 [15]. При этом пористая структура, а также поверхностные функциональные группы (например, карбоксильные или сульфатные) выступают в качестве центров кристаллизации карбонатов и фосфатов кальция [16, 17].
Полученные композиты могут быть использованы при моделировании процессов, протекающих при биоминерализации и имплантации в полимерных скаффолдах, применяемых в тканевой инженерии и регенеративной медицине [18, 19]. Присутствие НКЦ в полимерном композите увеличивает его гидрофильность и механическую прочность за счет водородных связей, в которых участвуют поверхностные гидроксильные группы НКЦ. В свою очередь, улучшенная смачиваемость и наличие поверхностных функциональных групп способствуют процессам минерализации биоактивных солей (фосфаты, карбонаты кальция) и пролиферации клеток (разрастание ткани организма) в пористых полимерных скаффолдах [20], используемых в биоинженерии.
Цель настоящей работы – изучить влияние нанокристаллической целлюлозы в составе композита с поликапролактоном и пористости пленок композитов ПКЛ/НКЦ на кристаллизацию карбоната кальция в определенной полиморфной модификации.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы. В работе применяли ПКЛ (М ~ 80 000), поливинилпирролидон (ПВП, М ~ 40000) производства фирмы Sigma-Aldrich. Для получения НКЦ использовали коммерческую микрокристаллическую целлюлозу (МКЦ) (Cellulose, powder ~20 micron, Sigma-Aldrich), бидистиллированную воду и серную кислоту (х. ч., ГОСТ 4204-77, Химмед).
Использовали CaCl2 и Na2CO3 (х. ч., АО “Химреактив”), а также растворители: диметилформамид (ДМФА), тетрагидрофуран (ТГФ), хлороформ (ХФ, Sigma-Aldrich) и ацетон (Химмед). Все растворители имели квалификацию “х. ч.” или “ос. ч.” и не подвергались дополнительной очистке.
Синтез объектов исследования. Для растворения ПКЛ и получения пленок различной морфологии применяли три растворителя: диметилформамид, смесь диметилформамида и тетрагидрофурана (ДМФА : ТГФ = 6 : 4) [21] и хлороформ. Пленки получали методом налива в стеклянные чашки Петри и сушки при комнатной температуре. Для получения композитов НКЦ/ПКЛ необходимо получить устойчивую суспензию НКЦ в растворителе, смешиваемом с растворителем ПКЛ. Для получения устойчивой суспензии НКЦ в ДМФА и смеси ДМФА-ТГФ использовали ацетоновый органогель НКЦ, в случае ХФ применяли НКЦ, поверхностно модифицированную ПВП [22].
Композиты ПКЛ/НКЦ с использованием различных растворителей получали по следующим методикам. Смешивали 0.5 г ПКЛ, 10 мл растворителя (ДМФА или смесь ДМФА-ТГФ в соотношении 6 : 4) и определенное количество ацетонового геля НКЦ. Полученную смесь перемешивали в течение суток при комнатной температуре, отливали в стеклянные чашки Петри и сушили при комнатной температуре. Аналогичным способом – добавлением модифицированной (ПВП) НКЦ в раствор ПКЛ – получали композиты в ХФ. Содержание НКЦ в высушенной композитной пленке составляло 10%.
Водные суспензии НКЦ были получены сернокислотным гидролизом МКЦ по методике, описанной в [23]. Гидролиз МКЦ проводили в водном растворе серной кислоты (62%) (1 г МКЦ/40 мл раствора) при 50°C в течение 2 ч при интенсивном перемешивании. Полученную в результате гидролиза суспензию отмывали от кислоты дистиллированной водой многократным повторением циклов центрифугирования до достижения постоянного значения pH надосадочной жидкости (~рН 2.4). Далее суспензию НКЦ очищали с помощью ионообменной смолы (ТОКЕМ МВ-50(R), Германия), обрабатывали ультразвуком (Sonorex DT100, Bandelin, Германия) в течение 15–30 мин и использовали для получения композитных пленок ПКЛ/НКЦ.
Ацетоновый органогель НКЦ был получен из гидрозолей НКЦ постепенной заменой воды на ацетон по методике, описанной в [24]. Органический растворитель осторожно добавляли на поверхность водной суспензии НКЦ, чтобы предотвратить перемешивание и обеспечить образование органического слоя над водной суспензией. Ацетон заменяли 1–2 раза в сутки до тех пор, пока НКЦ не собиралась на дне в однородный гель (обычно 5–7 сут). Во время процесса органический слой слегка встряхивали для облегчения обмена растворителей. Содержание НКЦ в ацетоновом геле определяли гравиметрически. Содержание НКЦ в ацетоновом геле составляло 6%.
Поверхностно модифицированную НКЦ получали путем смешивания 0.5 г ПВП, 10 мл воды и необходимого количества водной суспензии НКЦ (концентрация 20.0 г/л) при перемешивании в течение 1 ч. Полученную смесь подвергали лиофильной сушке в течение 48 ч при температуре –54°С и давлении 6 Па. Предварительно образцы были заморожены и выдержаны при –40°С в течение 2 сут. Далее лиофилизированные образцы использовали для приготовления композитов с ПКЛ с использованием ХФ в качестве растворителя.
В зависимости от применяемого растворителя были получены три серии образцов: с использованием ДМФА, ХФ и смеси ДМФА-ТГФ. В первом случае образцы имеют маркировку Д, во втором – ДТ, в третьем – Х. Содержание НКЦ в композитах составляло 10%. Перечень образцов с их маркировкой представлен в табл. 1. Например, образец с маркировкой ПКЛ(Д) – это пленка чистого ПКЛ, отлитого из ДМФА; ПКЛ/НКЦ(ДТ) – пленка композита, отлитого из смеси ДМФА-ТГФ, с содержанием НКЦ 10% и т.д.
Таблица 1.
Перечень изученных образцов и их маркировка
| Образцы ПКЛ, полученные из разных растворителей | Образцы композитов ПКЛ/НКЦ* | Минерализованные образцы | ||
|---|---|---|---|---|
| образцы ПКЦ | растворитель | образцы ПКЛ | образцы композитов ПКЛ/НКЦ | |
| ПКЛ(Д) | Диметилформамид | ПКЛ/НКЦ(Д) | ПКЛ(Д)-М | ПКЛ/НКЦ(Д)-М |
| ПКЛ(ДТ) | Диметилформамид- тетрагидрофуран | ПКЛ/НКЦ(ДТ) | ПКЛ(ДТ)-М | ПКЛ/НКЦ(ДТ)-М |
| ПКЛ(Х) | Хлороформ | ПКЛ/НКЦ(Х) | ПКЛ(Х)-М | ПКЛ/НКЦ(Х)-М |
Минерализацию пленок ПКЛ и ПКЛ/НКЦ проводили по методике, описанной в [25]. Образец пленки размерами 1 × 3 см помещали в 3 мл 1 М раствора CaCl2 и обрабатывали в УЗ-ванне в течение 10 мин. Затем в процессе УЗ-обработки добавляли 3 мл 1 М раствора Na2CO3 и обрабатывали УЗ еще 1 мин. Для кристаллизации СаСО3 пленку оставляли в растворе на 15–20 мин, после чего образец промывали водой 2–3 раза. Для формирования однородного покрытия СаСО3 процедуру повторяли 3 раза. Затем образец сушили при 40°С в течение 30 мин. Для обозначения минерализованных образцов ПКЛ и ПКЛ/НКЦ при маркировке добавляли букву М, например, ПКЛ(Д)-М (табл. 1).
Методы физико-химического анализа
Сканирующая электронная микроскопия (СЭМ), электронная спектроскопия для химического анализа. Морфология образцов изучена с помощью сканирующего электронного микроскопа Vega 3 Tescan (Чехия). Исследование проводили с использованием детектора вторичных электронов при ускоряющем напряжении 5 кВ в режиме высокого вакуума. Элементный состав определяли методом рентгеновского энергодисперсионного анализа с помощью спектрометра X-Max 6 (Oxford Instruments NanoAnalysis) с использованием детектора x-ACT. Диапазон анализируемых элементов: 4Be–94Pu. Данное оборудование обеспечивает высокую точность анализа (разрешающая способность соответствует стандарту ISO156 32:2012), кроме того, оно синхронизировано с электронной пушкой сканирующего электронного микроскопа, что позволяет проводить детальное элементное картирование поверхности.
Поляризационная оптическая микроскопия. Для изучения морфологии пленок ПКЛ и его композитов с НКЦ дополнительно использовали поляризационный оптический микроскоп (ПОМ) Soptop CX40P (Sunny Instruments, Китай).
Пористая структура композитов изучена методом низкотемпературной адсорбции азота (анализатор удельной поверхности и пористости). Образцы выдерживали в вакууме в течение 3 ч при температуре 50°С. Адсорбционные и десорбционные изотермы измеряли при температуре –196°C в интервале относительных давлений p/p0 от 0.01 до 0.95. Удельную поверхность рассчитывали по адсорбционной изотерме методом БЭТ. Распределение пор по размерам и объем пор определяли методом BJH. Относительная ошибка определения объема пор и площади поверхности составляла 2%.
Рентгеноструктурный анализ проводили на дифрактометре фирмы Bruker D2 Phaser (Германия) с использованием CuKα-излучения (λ = 0.1542 нм). Угловой диапазон сканирования составлял 2°–45° с шагом 0.01°.
Степень кристалличности ПКЛ и его композитов рассчитывали с использованием пакета программного обеспечения Diffrac.Suite.
Дифрактограммы СаСО3 использовали для определения фазового состава образцов [26].
ИК-спектры регистрировали на спектрофотометре Vertex 80v (Bruker, Германия) в области частот 4000–400 см–1. Образцы запрессовывали в таблетки, содержащие 1 мг анализируемого вещества и 100 мг бромида калия.
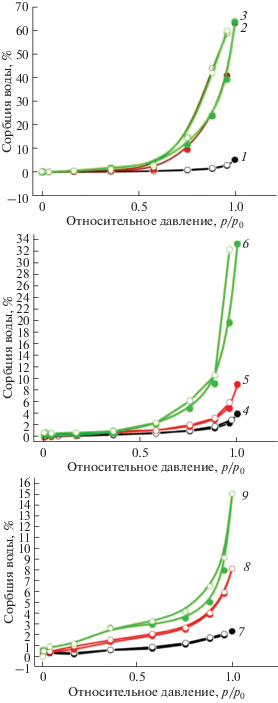
Изотермы адсорбции и десорбции воды были получены при температуре 25°C в условиях контролируемой влажности. Содержание воды в образцах определяли гравиметрически. Относительная ошибка определения сорбции паров воды составляла 5%.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Морфология пленок ПКЛ и композитов ПКЛ/НКЦ, полученных из разных растворителей
Поверхность пленок ПКЛ, отлитых из ДМФА или смеси ДМФА-ТГФ, неоднородная, с ярко выраженной пористостью. Причем, как показывают СЭМ-изображения сколов, пористая структура характерна для всего объема пленки (рис. S1–S3 ). Напротив, поверхность пленки ПКЛ, отлитой из ХФ, достаточно гладкая и однородная, не имеет видимых пор и трещин. В поляризованном свете видно, что при образовании пленки, отлитой из ХФ, ПКЛ кристаллизуется в виде крупных сферолитов (рис. S1 ).
Полученные данные показывают, что пленки ПКЛ, отлитые из ДМФА или смеси ДМФА-ТГФ, имеют бóльшую удельную поверхность, чем пленки, полученные с использованием ХФ. Введение НКЦ в матрицу полимера увеличивает удельную площадь поверхности и пористость полученных композитов. Кроме того, с увеличением содержания НКЦ в композите увеличивается сорбция паров воды, что связано с увеличением гидрофильности композитного материала (табл. 2).
Минерализация пленок ПКЛ и ПКЛ/НКЦ
В результате минерализации пленок ПКЛ и композитов ПКЛ/НКЦ образуются кристаллы СаСО3 различной морфологии и различной полиморфной модификации (кальцит и ватерит).
Морфология кристаллов СаСО3, сформированных на пленке ПКЛ, отлитой из ДМФА, показана на рис. 1. Анализ СЭМ-изображений поверхности (рис. 1а, 1б) и скола (рис. 1в–1д) пленки показывает, что кристаллизация СаСО3 происходит как на поверхности, так и в объеме пленки. Проведенное картирование скола пленки (рис. 1е), а также элементный анализ поверхности и скола пленки на содержание кальция (табл. 3) показывают присутствие кальция в объеме пленки. При этом содержание кальция в объеме пленки приблизительно в 2 раза меньше, чем на поверхности.
Рис. 1.
СЭМ-изображения поверхности (а, б) и скола (в–д) минерализованных образцов пленки ПКЛ(Д)-М; элементное картирование скола пленки по кальцию (е).

Таблица 3.
Элементный состав минерализованных образцов пленок ПКЛ и композитов ПКЛ/НКЦ по данным рентгеновского энергодисперсионного анализа
| Образец | Элементный состав, мас. % | ||
|---|---|---|---|
| C | O | Ca | |
| ПКЛ(Д)-М Поверхность Скол ПКЛ/НКЦ(Д)-М Поверхность Скол ПКЛ(ДТ)-М Поверхность Скол ПКЛ/НКЦ(ДТ)-М Поверхность Скол ПКЛ(Х)-М Поверхность Скол ПКЛ/НКЦ(Х)-М Поверхность Скол |
22.3 ± 0.2 47.1 ± 0.3 22.3 ± 0.2 45.6 ± 0.3 17.7 ± 0.3 51.3 ± 0.3 24.5 ± 0.2 37.7 ± 0.3 63.8 ± 0.2 79.6 ± 0.3 51.1 ± 0.2 85.7 ± 0.3 |
50.7 ± 0.3 41.0 ± 0.3 50.7 ± 0.3 31.5 ± 0.3 47.4 ± 0.3 34.0 ± 0.3 57.2 ± 0.2 41.4 ± 0.3 33.2 ± 0.2 20.4 ± 0.3 39.3 ± 0.3 14.3 ± 0.3 |
26.5 ± 0.2 11.8 ± 0.08 26.5 ± 0.2 22.2 ± 0.1 25.8 ± 0.2 12.7 ± 0.1 17.2 ± 0.1 19.0 ± 0.1 3.0 ± 0.04 – 8.7 ± 0.07 – |
На поверхности пленки видны кристаллы двух видов – ромбические с гладкими гранями, характерные для кальцита, и сферические (овальные), имеющие сложную внутреннюю архитектуру, характерные для ватерита. Размеры кристаллов можно оценить как 0.5–2 мкм. Во внутреннем поровом пространстве пленки ПКЛ(Д) присутствуют кристаллы СаСО3 ромбической формы и сферические частицы, агрегаты и фрагменты сферических частиц.
Аналогичная картина наблюдается при минерализации CaCO3 в пленках ПКЛ, отлитых из смешанного растворителя ДМФА-ТГФ (рис. 2). И на поверхности, и в объеме пленки образуются как кубические кристаллы кальцита, так и сферические – ватерита.
Рис. 2.
СЭМ-изображения поверхности (а, б) и скола (в, д) минерализованных образцов пленки ПКЛ(ДТ)-М; элементное картирование скола пленки по кальцию (г).

Пленка ПКЛ, отлитая из хлороформа, не пористая (табл. 2, рис. S1 ), поэтому кристаллизация СаСО3 происходит только на ее поверхности преимущественно в виде ромбических кристаллов кальцита (рис. 3а, 3б). Элементный анализ (табл. 3) и картирование скола пленки (рис. 3д) показывают отсутствие кальция в объеме пленки.
Рис. 3.
СЭМ-изображения поверхности (а, б) и скола (в, г) минерализованных образцов пленки ПКЛ(Х)-М; элементное картирование скола пленки по кальцию (д).

СЭМ-изображения минерализованных композитов ПКЛ/НКЦ(Д)-М, ПКЛ/НКЦ(Д-Т)-М и ПКЛ/НКЦ(ХФ)-М показаны на рис. 4–6. Элементный анализ сколов композитных пленок, отлитых из ДМФА или ДМФА-ТГФ (табл. 3), показывает, что добавка НКЦ в состав композита приводит к увеличению содержания кальция в поровом объеме пленки. При этом содержание кальция на поверхности и в объеме пленки становится практически одинаковым.
Рис. 4.
СЭМ-изображения поверхности (а, б) и скола (в, г) минерализованных образцов пленки ПКЛ/НКЦ(Д)-М; элементное картирование скола пленки по кальцию (д).

Рис. 5.
СЭМ-изображения поверхности (а, б) и скола (в, г) минерализованных образцов пленки ПКЛ/НКЦ(ДТ)-М; элементное картирование скола пленки по кальцию (д).

Рис. 6.
СЭМ-изображения поверхности (а, б) и скола (в, г) минерализованных образцов пленки ПКЛ/НКЦ(Х)-М; элементное картирование скола пленки по кальцию (д).

В композитах ПКЛ/НКЦ, отлитых из хлороформа, присутствие НКЦ существенно не изменяет процесс кристаллизации СаСО3. Кристаллизация происходит только на поверхности пленки (рис. 6, табл. 3).
В ИК-спектрах чистого ПКЛ (рис. S6 ) наблюдаются характерные основные полосы при 2945 и 2864 см–1 (асимметричные и симметричные вибрационные колебания CH2), 1729 см–1 (колебания С=O), 1240 и 1166 см–1 (асимметричные и симметричные колебания C–O–C). ИК-спектры пленок НКЦ характеризуются интенсивными полосами поглощения в интервалах волновых чисел 3300–3500 и 2800–3000 см–1, что соответствует валентным колебаниям O–H- и C–H-связей целлюлозы. Область поглощения 950–1200 см–1 относится к валентным колебаниям связей С–О и С–С кольцевых структур.
В ИК-спектрах минерализованных образцов ПКЛ и композитов ПКЛ/НКЦ (рис. S6 ) хорошо просматриваются полосы при 1480 и 875 см–1, характерные для СаСО3 в форме ватерита. Полоса при 875 см–1 в спектре относится к деформационным колебаниям C–O карбонатных групп, а полоса при 1480 см–1 – к асимметричным растягивающим колебаниям C–O ватерита [17]. Полосы при 745 и 712 см–1, свидетельствующие о присутствии ватерита и кальцита соответственно, перекрываются полосами, характерными для ПКЛ. Однако для образца ПКЛ(Х)-М, в котором преобладает кальцит, четко проявляется полоса при 712 см–1.
На рис. 7 приведены дифрактограммы минерализованных образцов ПКЛ и композитов ПКЛ/НКЦ. Для дифрактограммы чистого ПКЛ характерны два дифракционных пика (брэгговские углы ~21° и 23°), которые соответствуют кристаллографическим плоскостям (110) и (200) орторомбической решетки ПКЛ [27]. Дифракционные пики НКЦ на рентгенограмме композита не проявляются в силу малого содержания. На рентгенограммах минерализованных образцов отчетливо видны дифракционные пики, соответствующие кальциту и ватериту. Дифрактограммы минерализованных пленок ПКЛ и композитов ПКЛ/НКЦ использовали для определения фазового состава СаСО3, кристаллизующегося в образцах. Анализ полученных результатов (табл. 4) показал, что процесс кристаллизации СаСО3 на композитах ПКЛ/НКЦ происходит с преимущественным образованием ватерита. Таким образом, присутствие НКЦ в составе композита влияет на процесс кристаллизации и способствует образованию ватерита.
Рис. 7.
Дифрактограммы минерализованных пленок ПКЛ и композитов ПКЛ/НКЦ: 1 – ПКЛ(Д)-М, 2 – ПКЛ/НКЦ(Д)-М, 3 – ПКЛ(ДТ)-М, 4 – ПКЛ/НКЦ(ДТ)-М, 5 – ПКЛ(Х)-М, 6 – ПКЛ/НКЦ(Х)-М.
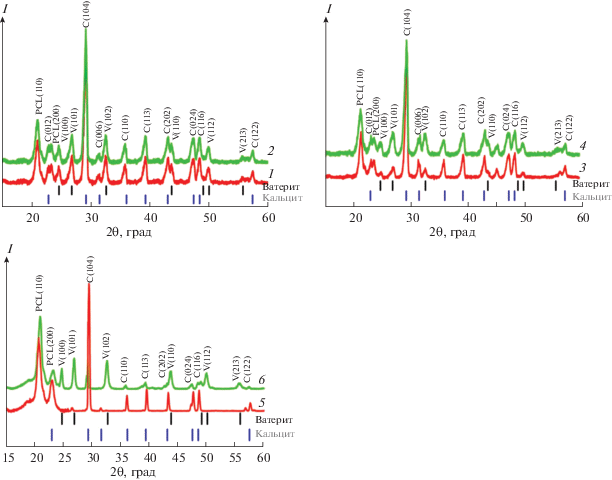
Таблица 4.
Фазовый состав карбоната кальция, кристаллизующегося в пленках ПКЛ и композитов ПКЛ/НКЦ
| Образец | Содержание, % | |
|---|---|---|
| ватерит | кальцит | |
| ПКЛ(Д)-М ПКЛ/НКЦ(Д)-М ПКЛ(ДТ)-М ПКЛ/НКЦ(ДТ)-М ПКЛ(Х)-М ПКЛ/НКЦ(Х)-М |
61 ± 3 61 ± 3 39 ± 2 60 ± 3 22 ± 1 88 ± 4 |
39 ± 2 38 ± 2 61 ± 3 40 ± 2 78 ± 4 12 ± 1 |
Адсорбционные характеристики минерализованных образцов ПКЛ и композитов ПКЛ/НКЦ
Минерализация ПКЛ и композитов ПКЛ/НКЦ приводит к небольшому увеличению удельной поверхности и значительному увеличению сорбции воды (табл. 5, рис. S7 , рис. 8). По форме изотермы адсорбции паров воды на изученных образцах можно отнести к II типу по классификации Брунауэра [28]. Такая форма изотермы присуща макропористым адсорбентам и описывает полимолекулярную адсорбцию. При небольшой площади поверхности и незначительной пористости наблюдается значительное увеличением адсорбции паров воды при увеличении относительного давления. Изотермы адсорбции и десорбции паров воды характеризуются гистерезисом в области достаточно больших относительных давлений. Значительное увеличение адсорбции паров воды и наличие гистерезиса в области повышенных относительных давлений могут свидетельствовать о возникновении капиллярной конденсации. Необходимо отметить, что наибольшее увеличение сорбции воды наблюдается у минерализованных пленок с большим содержанием ватерита. Это связано с пористой структурой ватерита, которая определяет поверхностные и адсорбционные особенности минерализованных образцов.
ЗАКЛЮЧЕНИЕ
С использованием диметилформамида, хлороформа и смеси растворителей диметилформамид-тетрагидрофуран получены композиты поликапролактона с нанокристаллической целлюлозой. Показано, что используемый растворитель значительно влияет на морфологию полученных пленок. Присутствие нанокристаллической целлюлозы в составе композита с поликапролактоном и пористость пленок ПКЛ и композитов ПКЛ/НКЦ оказывают влияние на кристаллизацию CaCO3 с образованием различных полиморфов (кальцит, ватерит). Показано, что в пористых пленках кристаллизация карбоната кальция происходит и на поверхности, и в объеме пленки. Содержание НКЦ в составе композита приводит к увеличению содержания карбоната кальция в поровом объеме пленки и способствует образованию ватерита.
Список литературы
Al Omari M.M.H., Rashid I.S., Qinna N.A. et al. // Profiles of Drug Substances, Excipients and Related Methodology. 2016. V. 41. P. 31. https://doi.org/10.1016/bs.podrm.2015.11.003
Ferral-Pérez H., Galicia-García M., Alvarado-Tenorio B. et al. // AMB Expr. 2020. V. 10. № 174. https://doi.org/10.1186/s13568-020-01111-6
Boyjoo Y., Pareek V.K., Liu J. // J. Mater. Chem. 2014. V. 2. № 35. P. 14270. https://doi.org/10.1039/C4TA02070G
Chen Y., Ji X., Zhao G., Wang X. // Powder Technol. 2010. V. 200. № 3. P. 144. https://doi.org/10.1016/j.powtec.2010.02.017
Grasby S.E. // Geochim. Cosmochim. Acta. 2003. V. 67. № 9. P. 1659. https://doi.org/10.1016/S0016-7037(02)01304-2
Nehrke G., Van Cappellen P., van der Weijden C.H. // J. Cryst. Growth. 2006. V. 287. № 2. P. 528. https://doi.org/10.1016/j.jcrysgro.2005.11.080
Ferreira A.M., Vikulina A.S., Volodkin D. // J. Controlled Release. 2020. V. 328. P. 470. https://doi.org/10.1016/j.jconrel.2020.08.061
Savelyeva M.S., Prikhozhdenko E., Gorin D.A. et al. // Frontiers Chem. 2020. V. 7. Article 888. https://doi.org/10.3389/fchem.2019.00888
Trushina D.B., Bukreeva T.V., Kovalchuk M.V., Antipina M.N. // Mater. Sci. Eng., C. 2014. V. 45. P. 644. https://doi.org/10.1016/j.msec.2014.04.050
Konopacka-Łyskawa D. // Crystals. 2019. V. 9. № 223. https://doi.org/10.3390cryst9040223
Sepulveda F., Butto N., Arias J.L. et al. // Cryst. Growth Des. 2020. V. 20. № 8. P. 5610. https://doi.org/10.1021/acs.cgd.0c00803
Woodruff M., Hutmacher D. // Prog. Polym. Sci. 2010. № 35. P. 1217. https://doi.org/10.1016/j.progpolymsci.2010.04.002
Joshi M.K., Tiwari A.P., Pant H.R. et al. // ACS Appl. Mater. Interfaces. 2015. № 7. P. 19672. https://doi.org/10.1021/acsami.5b04682
Boujemaoui A., Sanchez C., Engström J. et al. // ACS Appl. Mater. Interfaces. 2017. V. 9. № 40. P. 35305. https://doi.org/10.1021/acsami.7b09009
Arias J.L., Fernandez M.S. // Chem. Rev. 2008. V. 108. № 11. P. 4475. https://doi.org/10.1021/cr078269p
Meldrum F.C. // Int. Mater. Rev. 2003. V. 48. № 3. P. 187. https://doi.org/10.1179/095066003225005836
Lu Q., Cai Z., Wang S. et al. // ACS Sustainable Chem. Eng. 2017. V. 5. P. 8456. https://doi.org/10.1021/acssuschemeng.7b02394
Zakharov N.A., Koval E.M., Aliev A.D. et al. // Russ. J. Inorg. Chem. 2021. V. 66. № 3. P. 305. [Захаров Н.А., Коваль Е.М., Алиев А.Д. и др. // Журн. неорган. химии. 2021. Т. 66. № 3. С. 317. https://doi.org/ 10.31857/S0044457X21030211]https://doi.org/10.1134/S0036023621030219
Golovanova O.A. // Russ. J. Inorg. Chem. 2020. V. 65. № 3. P. 305. [Голованова О.А. // Журн. неорган. химии. 2020. Т. 65. № 3. P. 302. https://doi.org/10.31857/S0044457X20030046]https://doi.org/10.1134/S0036023620030043
Fadeeva T.V., Golovanova O.A. // Russ. J. Inorg. Chem. 2019. V. 64. № 7. P. 847. [Фадеева Т.В., Голованова О.А. // Журн. неорган. химии. 2019. Т. 64. № 7. P. 690. https://doi.org/10.1134/S0044457X19070067]https://doi.org/10.1134/S0036023619070064
Nartker S., Hassan M., Stogsdill M. // Mater. Res. Express. 2015. V. 2. № 3. P. 035401. https://doi.org/10.1088/2053-1591/2/3/035401
Singh A., Genovese M., Mancini G. et al. // ACS Sustainable Chem. Eng. 2020. V. 8. № 10. P. 4128. https://doi.org/10.1021/acssuschemeng.9b06760
Bondeson D., Mathew A., Oksman K. // Cellulose. 2006. V. 13. № 2. P. 171. https://doi.org/10.1007/s10570-006-9061-4
Capadona J.R., Shanmuganathan K., Trittschuh S. et al. // Biomacromolecules. 2009. V. 10. № 4. P. 712. https://doi.org/10.1021/bm8010903
Savelyeva M.S., Abalymov A.A., Lyubun G.P. et al. // J. Biomed. Mater. Res. Part. A. 2017. V. 105. № 1. P. 94. https://doi.org/10.1002/jbm.a.35870
Феоктистова Н.А. Микросферы ватерита как основа для создания многофункциональных носителей биологически активных веществ. Дис. … канд. хим. наук. М., 2019. 145 с.
Ahmed F., Saleemi S., Khatri Z. et al. // Carbohydr. Polym. 2015. № 115. P. 388. https://doi.org/10.1016/j.carbpol.2014.09.002
Адамсон А. Физическая химия поверхностей / Пер. с англ. под ред. Зорина З.М., Муллера В.М. М.: Мир, 1979.
Дополнительные материалы
- скачать ESM.docx
- Рис. S1. - Рис. S7.
Инструменты
Журнал неорганической химии