Журнал неорганической химии, 2020, T. 65, № 7, стр. 872-879
Сравнительный анализ солнцезащитных характеристик нанокристаллического диоксида церия
И. В. Колесник a, b, А. Б. Щербаков c, Т. О. Козлова a, b, Д. А. Козлов a, b, В. К. Иванов b, *
a Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
b Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
c Институт микробиологии и вирусологии им. Д.К. Заболотного НАН Украины
03680 Киев, ул. Академика Заболотного, 154, Украина
* E-mail: van@igic.ras.ru
Поступила в редакцию 14.02.2020
После доработки 25.02.2020
Принята к публикации 28.02.2020
Аннотация
Широко используемые в качестве неорганических УФ-фильтров нанокристаллические TiO2 и ZnO, несмотря на хорошие солнцезащитные характеристики, могут оказывать негативное воздействие на кожу. В качестве перспективного компонента солнцезащитной косметики предложен нанокристаллический диоксид церия, однако до настоящего времени количественное сравнение солнцезащитных характеристик CeO2 c другими оксидами металлов не проводилось. В настоящей работе впервые экспериментально определены величины солнцезащитного фактора и фактора защиты от УФ-А излучения для наночастиц CeO2 в соответствии со стандартом ГОСТ ИСО 24443-2016 и проведено их сопоставление с характеристиками TiO2 и ZnO. Установлено влияние размерного фактора на солнцезащитные характеристики CeO2.
ВВЕДЕНИЕ
Ультрафиолетовое излучение солнца имеет чрезвычайно важное значение для здоровья человека, однако длительное воздействие солнечного света на кожу может приводить к развитию острых и хронических заболеваний, включая эритему, дерматозы, фотоиммуносупрессию, фотостарение и карциногенез [1]. В настоящее время для защиты кожи от неблагоприятного воздействия излучения диапазонов УФ-Б (290–320 нм) и УФ-А (320–400 нм) используют солнцезащитные средства (кремы, лосьоны), в состав которых включены УФ-фильтры – органические и неорганические вещества, способные минимизировать вредное воздействие ультрафиолетового излучения. Более трех десятилетий в качестве неорганических УФ-фильтров используют оксид титана (TiO2) и оксид цинка (ZnO). Поскольку TiO2 более эффективен в диапазоне УФ-Б, а ZnO – в диапазоне УФ-А, их сочетание обеспечивает широкополосную защиту от ультрафиолетового излучения [2]. Основным недостатком указанных неорганических пигментов является непрозрачный матовый слой (“эффект белил”), который они в виде макрочастиц оставляют на коже, что приводит к снижению потребительских характеристик солнцезащитных продуктов. Этот визуальный эффект можно устранить, если размер частиц пигментов уменьшить до 100–200 нм, однако у нанодисперсных TiO2 и ZnO проявляются нежелательные побочные свойства. Например, нано-TiO2 имеет высокую фотоцитотоксичность, а нано-ZnO может растворяться с образованием ионов Zn2+, проявляющих токсичность. Наночастицы этих оксидов металлов как неорганические компоненты солнцезащитных препаратов регистрируются в Европе с рядом существенных ограничений [3–5]. В качестве альтернативы TiO2 и ZnO предложено использовать нанодисперсный диоксид церия [6–8]. По данным GEMATRIA Test Lab GmbH, если для нано-TiO2 (<100 нм) фотокаталитическая активность больше 88%, то в случае нано-CeO2 (<50 нм) это значение составляет ∼5% [9]. Более того, в последнее десятилетие нанодисперсный диоксид церия привлекает внимание в качестве неорганического антиоксиданта, способного эффективно защищать живые системы от окислительного стресса [10], в том числе связанного с УФ-излучением [6, 9, 10].
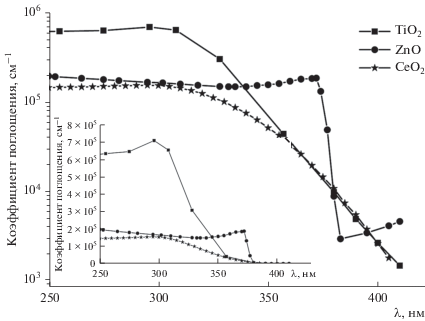
Мерой защиты кожи от воздействия вредных солнечных лучей является солнцезащитный фактор косметического средства (Sun Protection Factor, SPF), который обозначает способность средства продлевать время безопасного нахождения на солнце. SPF определяется как отношение дозы УФ-излучения (290–400 нм), необходимой для получения 1 минимальной эритемной дозы (МЭД) на защищенной солнцезащитным средством коже (после нанесения 2 мг/см2 продукта) по сравнению с дозой излучения для получения 1 МЭД на незащищенной коже. Солнцезащитный фактор рассчитывают исходя из способности компонентов солнцезащитного средства поглощать ультрафиолетовое излучение, поэтому значение коэффициента поглощения в диапазоне 250–400 нм является основной физической характеристикой возможности использования того или иного материала в качестве компонента солнцезащитного средства. Анализ литературных данных [11–14] показывает, что по величине коэффициента поглощения диоксид церия как объемный материал в диапазоне УФ-Б уступает диоксиду титана, а в УФ-А – оксиду цинка (рис. 1).
Помимо солнцезащитного фактора важной характеристикой солнцезащитного средства является критическая длина волны (λкрит) – длина волны, при которой интеграл спектральной кривой поглощения составляет 90% от интеграла поглощения в диапазоне от 290 до 400 нм; λкрит характеризует способность солнцезащитного средства поглощать УФ-А излучение по отношению к общему поглощению в диапазоне 290–400 нм. По мере увеличения критической длины волны увеличивается и защита от УФ-А. При использовании критической длины волны в сочетании с SPF описание фотозащитных характеристик продукта получается более полным [15]. По требованиям Управления по контролю за продуктами и лекарствами США (FDA), фактор защиты от УФ-А излучения должен составлять не менее одной трети от общего солнцезащитного фактора (UVAPF/SPF ≥ 1/3).
Согласно рекомендации Европейской Комиссии от 22 сентября 2006 г., касающейся эффективности солнцезащитных средств [16], минимальная степень защиты, обеспечиваемая солнцезащитными средствами, должна быть следующей: SPF не менее 6, значение должно быть получено с использованием стандартного метода тестирования, такого как ИСО 24444 либо аналогичного [17]; УФ-А-защитный фактор должен составлять не менее 1/3 от солнцезащитного фактора SPF; критическая длина волны должна быть не менее 370 нм.
В настоящей работе впервые проведены стандартизованные исследования солнцезащитных характеристик нанодисперсного диоксида церия, включая величины солнцезащитного фактора и критической длины волны модельного косметического средства, содержащего наночастицы диоксида церия, а также проанализировано влияние размерного эффекта на указанные характеристики.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Нанокристаллический диоксид церия получали в соответствии с опубликованной ранее методикой [18]. Готовили водно-изопропанольный раствор (объемное соотношение 1 : 1) Ce(NO3)3 · 6H2O; концентрация ионов церия в растворе составляла 0.08, 0.4 или 0.8 моль/л. Полученный раствор приливали к 3 М раствору NH4OH. Образовавшуюся бледно-фиолетовую суспензию выдерживали при комнатной температуре при постоянном перемешивании в течение суток. Сформировавшийся осадок промывали дистиллированной водой до нейтрального значения pH и оставляли в виде водной суспензии. Образцы в соответствии с концентрацией ионов церия в растворе обозначали как Ce3-0.08, Ce3-0.4, Ce3-0.8. Образец с обозначением Ce4-0.8 получали аналогичным способом, используя в качестве исходного 0.8 М раствор (NH4)2Ce(NO3)6.
Непосредственно перед проведением эксперимента по определению солнцезащитных характеристик CeO2 суспензии центрифугировали, после чего 0.2 г осадка сразу же смешивали с 1.8 г обратной эмульсии, содержащей 67% воды, 1% NaCl, 0.5% лимонной кислоты, 0.2% гуаровой камеди, 3% глицерина (водная фаза), 4% эмульгатора (смеси полиглицерил-3 полирицинолеата, полиглицерил-3 рицинолеата), 4% цетилового спирта и 22% каприлового триглицерида (масляная фаза). Эмульсию готовили, прибавляя водную фазу к масляной при интенсивном перемешивании. Затем 0.35 г эмульсии наносили на поверхность пленки 3M™ Transpore™ Tape 1527-2 (площадь 27.5 см2) и распределяли по поверхности до достижения равномерного покрытия.
Спектры в диапазоне 290–400 нм регистрировали на спектрометре Perkin Elmer Lambda 950 в режиме диффузного отражения (диаметр интегрирующей сферы 150 мм). В качестве образца сравнения использовали пленку 3M™ Transpore™ Tape 1527-2, на которую была нанесена аналогичная эмульсия, не содержащая оксида церия.
Расчет значений солнцезащитного фактора (SPF) и фактора защиты от УФ-А излучения (UVAPF) проводили в соответствии с международным стандартом ГОСТ ИСО 24443-2016.
Для корректного определения UVAPF0 образцы облучали при помощи источника, имитирующего солнечное излучение, Suntest CPS+ (ATLAS MTS). Дозу излучения рассчитывали, исходя из спектров поглощения образцов, согласно методике, описанной в стандарте ГОСТ ИСО 24443-2016.
Для исследования образцов методами рентгенофазового анализа и просвечивающей электронной микроскопии суспензии CeO2 высушивали при 60°С в течение суток.
Рентгенографические эксперименты проводили на дифрактометре с вращающимся анодом Rigaku D/MAX 2500 (Rigaku, Япония) в режиме отражения (геометрия Брегга–Брентано) с использованием CuKα1, 2-излучения и графитового монохроматора. Съемку дифрактограмм для осуществления фазового анализа проводили в низкофоновых кюветах из ориентированного в направлении [510] кремния с использованием стандартных держателей образцов. Съемку осуществляли в режиме θ−2θ-сканирования с шагом 0.02° по шкале 2θ и временем накопления спектра 3 с в интервале углов 2θ 10°−90°. Полнопрофильный анализ дифрактограмм методом Ле Бейла проводили с использованием программного пакета Jana2006 [19]. Оценку размеров областей когерентного рассеяния (ОКР) выполняли с помощью формулы Шеррера:
где p – размеры ОКР, λ – длина волны рентгеновского излучения, K – форм-фактор, Lx – параметр полнопрофильного анализа в Jana2006.Микроструктуру образцов изучали методом просвечивающей электронной микроскопии на электронном микроскопе Leo912 AB Omega при ускоряющем напряжении 100 кВ. Перед съемкой образцы помещали на покрытые полимерной пленкой медные сетки диаметром 3.05 мм. Изображения в просвечивающем режиме получали при увеличении до ×500 000, при получении изображений электронной дифракции применяли ограничивающую диафрагму диаметром 0.4 мкм.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
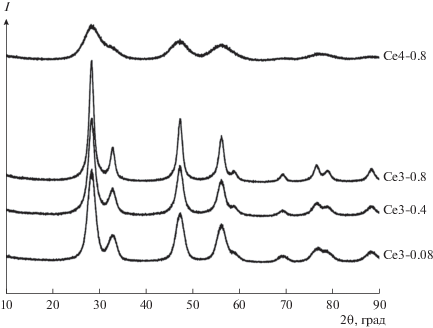
Согласно результатам рентгенофазового анализа, все синтезированные образцы представляют собой однофазный диоксид церия со структурой флюорита (PDF № 34-394) (рис. 2) и в зависимости от условий синтеза имеют размер областей когерентного рассеяния (ОКР) в диапазоне 2–7 нм (табл. 1). Размеры наночастиц CeO2, определенные по данным просвечивающей электронной микроскопии, хорошо согласуются с размерами, рассчитанными из дифрактограмм. Образцы преимущественно состоят из изотропных наночастиц CeO2 с примесью в образцах частиц Ce3-0.4, Ce3-0.8, имеющих форму стержней (рис. 3). Отметим, что обычно в указанных условиях формируются изотропные наночастицы CeO2 [20, 21], а для получения наностержней используют специальные условия синтеза, чаще всего гидро- или сольвотермальную обработку в присутствии поверхностно-активных веществ [22–24]. Тем не менее в единичных работах авторы наблюдали формирование 1D-наночастиц CeO2 и при использовании обычного метода соосаждения. Так, авторы [25] cоосаждали Ce(NO3)3 ∙ 6H2O с CO(NH2)2, выдерживали суспензию сутки при комнатной температуре, а затем в течение 1–6 ч при 85°С. При длительной выдержке реакционной смеси в этих условиях сферические наночастицы CeO2 трансформируются в стержнеобразные. Наблюдаемый эффект был объяснен ориентированным сращиванием наночастиц CeO2. В работе [26] осуществлен синтез CeO2 при комнатной температуре добавлением к раствору Ce(NO3)3 ∙ 6H2O растворов аммиака различной концентрации и установлено, что использование больших концентраций NH4OH (1–2 моль/л) приводит к формированию наностержней CeO2 вместо изотропных наночастиц. Авторы [26] объяснили образование наностержней протеканием топотактических реакций. В [27] получали изотропные наночастицы CeO2, а затем выдерживали их в водных растворах при различных значениях рН в течение месяца. Обнаружено, что в растворе с рН 7.6 наночастицы CeO2 трансформируются в наностержни. По мнению авторов, механизм формирования наностержней включает две стадии: на первой происходит самосборка и агрегация наночастиц, на второй образуются псевдомонокристаллы по механизму растворения-рекристаллизации. Причиной агрегации является уменьшение заряда на поверхности наночастиц CeO2 при повышении рН выше нейтрального. Предложенные объяснения, вероятно, можно распространить и на представленные в настоящей статье результаты. По всей видимости, возможность образования наностержней в двух образцах является следствием сочетания нескольких факторов, а именно: типа прекурсора (соль Ce3+), мольного соотношения реагентов и времени выдержки (1 сут). По данным просвечивающей электронной микроскопии, в образце Ce3-0.4 по сравнению с образцом Ce3-0.8 визуально доля наностержней больше, чем доля изотропных частиц.
Таблица 1.
Солнцезащитный фактор (SPF), фактор защиты от УФ-А излучения (UVAPF) и критическая длина волны (λкрит) для эмульсий, содержащих CeO2
| Образец | SPF | UVAPF | λкрит | UVAPF/SPF | Размер ОКР, нм |
|---|---|---|---|---|---|
| Ce3-0.08 | 2.15 | 1.70 | 375 | 0.79 | 4.5 |
| Ce3-0.4 | 2.25 | 1.95 | 379 | 0.87 | 5.5 |
| Ce3-0.8 | 2.80 | 2.15 | 375 | 0.77 | 7.0 |
| Ce4-0.8 | 2.90 | 2.40 | 375 | 0.83 | 2.0 |
Рис. 3.
Микрофотографии образцов нанодисперсного диоксида церия: а – Ce3-0.08, б – Ce3-0.4, в – Ce3-0.8, г – Ce4-0.8.

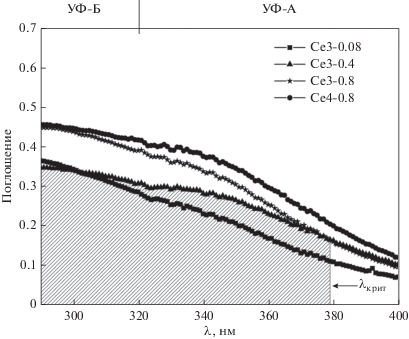
Спектры поглощения в УФ-области эмульсий, содержащих Ce3-0.08, Ce3-0.4, Ce3-0.8, Ce4-0.8, представлены на рис. 4. Для образца Се4-0.8 характерны наибольшие значения поглощения при всех длинах волн, что соответствует наибольшему значению SPF (табл. 1). По всей видимости, это связано с тем, что благодаря наименьшему размеру частиц диоксид церия наиболее равномерно распределяется по поверхности пленки и, как следствие, обеспечивает более высокую экранирующую способность. Для эмульсии, содержащей образец Ce3-0.4, характерно наибольшее значение критической длины волны. Таким образом, Ce3-0.4 обладает наиболее сбалансированными характеристиками с точки зрения соотношения защиты от УФ-А и УФ-Б излучения. Поскольку этот образец, по данным просвечивающей электронной микоскопии, характеризуется наличием большого количества наностержней, можно предположить, что к изменению спектра поглощения приводит размерный эффект и/или особенности электронной структуры наночастиц (примесь Ce3+, кислородные вакансии) [26, 28, 29].
Рис. 4.
Спектры поглощения эмульсий, содержащих образцы Ce3-0.08, Ce3-0.4, Ce3-0.8, Ce4-0.8. Заштрихованная область соответствует 90% площади под графиком для эмульсии, содержащей образец Ce3-0.4. Максимальная длина волны, ограничивающая эту область справа, соответствует λкрит – критической длине волны.
В табл. 1 приведены определенные на основании экспериментальных данных значения солнцезащитного фактора (SPF), фактора защиты от УФ-А излучения (UVAPF) и критической длины волны (λкрит) для эмульсий, содержащих Ce3-0.08, Ce3-0.4, Ce3-0.8, Ce4-0.8.
Из табл. 1 следует, что полученные солнцезащитные композиции, содержащие наночастицы диоксида церия (10%), не обладают требуемым значением солнцезащитного фактора SPF, тогда как значения λкрит и UVAPF/SPF находятся в пределах, рекомендуемых Еврокомиссией [16]. Видно, что для образцов CeO2, синтезированных с использованием в качестве прекурсора соли Ce3+, с увеличением размера наночастиц возрастает SPF и UVAPF. Известно, что для CeO2 характерно существенное изменение физико-химических свойств при изменении размеров наночастиц. Так, с уменьшением размера частиц возрастает параметр элементарной ячейки и ширина запрещенной зоны, увеличивается биологическая и каталитическая активность [30, 31]. Увеличение размера частиц диоксида церия, в свою очередь, приводит к заметному увеличению соотношения УФ-А/УФ-Б и критической длины волны [32], что хорошо согласуется с полученными нами результатами. В то же время на оптические характеристики наночастиц CeO2 влияет не только размерный эффект, но и условия синтеза [33]. Использование в качестве исходного соединения соли Ce4+ может служить еще одной возможной причиной большого значения SPF для образца Се4-0.8, что также не противоречит выявленной закономерности для образцов, полученных из соли Ce3+.
В табл. 2 приведены значения SPF, UVAPF и λкрит для наночастиц диоксида титана и оксида цинка (содержание TiO2, ZnO и CeO2 во всех образцах составляет 10 мас. %), полученные с использованием симулятора BASF для расчета характеристик солнцезащитных препаратов [34]. В основу математического аппарата симулятора BASF положены принципы того же международного стандарта ИСО 24443, поэтому сравнение результатов является корректным.
Таблица 2.
Солнцезащитный фактор (SPF), фактор защиты от УФ-А излучения (UVAPF) и критическая длина волны (λкрит) для солнцезащитных составов, содержащих TiO2 и ZnO [34]
| Образец | SPF | UVAPF | λкрит | UVAPF/SPF |
|---|---|---|---|---|
| ZnO (Z-Cote®) | 3.70 | 3.80 | 384 | 1.01 |
| TiO2 | 11.30 | 3.50 | 376 | 0.31 |
Как видно из табл. 1 и 2, образцы нанодисперсного диоксида церия по величине солнцезащитного фактора существенно уступают диоксиду титана и незначительно – оксиду цинка при одинаковом содержании в рецептуре. При этом по фактору защиты от УФ-А излучения оба традиционных неорганических фильтра превосходят диоксид церия, а оксид цинка – как по абсолютному, так и по относительному показателю (UVAPF/SPF). Отметим, что достижение таких высоких значений солнцезащитного фактора для TiO2 известно из данных [35], однако не обязательно характерно для всех коммерческих образцов. Нами проведены дополнительные измерения солнцезащитного фактора и фактора защиты УФ-А излучения для коммерческих анатаза и рутила. Значения SPF составили 2.70 и 3.10, значения UVAPF – 2.45 и 3.10 для анатаза и рутила соответственно. Видно, что значения SPF в случае TiO2 могут быть даже ниже значений, определенных для CeO2 (табл. 1).
Хорошо известно, что при ультрафиолетовом облучении образуется большое количество активных форм кислорода и свободных радикалов, которые разрушающе действуют как на элементы кожи, так и на компоненты самого средства [36, 37]. По этой причине в состав солнцезащитных средств вводят антиоксиданты и акцепторы свободных радикалов: токоферол, аскорбиновую кислоту, ниацинамид, коэнзим Q-10, ретинол и т.д. В ряде работ [38–44] приводятся данные в пользу того, что нанокристаллический диоксид церия способен выступать в качестве неорганического антиоксиданта. Таким образом, несмотря на тот факт, что в выполненных нами экспериментах наночастицы CeO2 продемонстрировали более низкие значения солнцезащитного фактора и фактора защиты от УФ-А излучения, они способны дополнительно защищать кожу от действия ультрафиолетового излучения за счет непрямых механизмов, например, нейтрализуя активные формы кислорода и свободные радикалы.
ЗАКЛЮЧЕНИЕ
Впервые проведены стандартизованные исследования солнцезащитных характеристик нанодисперсного диоксида церия и выполнено его сравнение с традиционными неорганическими УФ-фильтрами. Показано, что наночастицы диоксида церия в ряде случаев не обладают достаточными оптическими свойствами для обеспечения солнцезащитного фактора и фактора защиты от УФ-А излучения по сравнению с нанокристаллическими TiO2 или ZnO. Выявлено, что предыстория получения CeO2 напрямую определяет его солнцезащитные свойства: увеличение размеров частиц CeO2 внутри одной серии образцов приводит к росту SPF и UVAPF. Использование соли Ce4+ вместо соли Ce3+ в качестве исходного реагента позволило получить продукт, обладающий максимальными солнцезащитными характеристиками. Достигнутые результаты демонстрируют потенциал для дальнейших исследований нанокристаллического диоксида церия и его композиций в качестве компонента солнцезащитной косметики.
Список литературы
González S., Fernández-Lorente M., Gilaberte-Calzada Y. // Clin. Dermatol. 2008. V. 26. № 6. P. 614. https://doi.org/10.1016/j.clindermatol.2007.09.010
Smijs T.G., Pavel S. // Nanotechnol. Sci. Appl. 2011. V. 4. P. 95. https://doi.org/10.2147/NSA.S19419
https://ec.europa.eu/health/sites/health/files/scientific_committees/consumer_safety/docs/sccs_o_202. pdf
https://ec.europa.eu/health/sites/health/files/scientific_committees/consumer_safety/docs/sccs_o_206. pdf
https://ec.europa.eu/health/scientific_committees/consumer_safety/docs/sccs_o_103.pdf
Zholobak N.M., Ivanov V.K., Shcherbakov A.B. et al. // J. Photochem. Photobiol. B. 2011. V. 102. № 1. P. 32. https://doi.org/10.1016/j.jphotobiol.2010.09.002
Caputo F., De Nicola M., Sienkiewicz A. et al. // Nanoscale. 2015. V. 7. № 38. P. 15643. https://doi.org/10.1039/c5nr03767k
Kuznetsova S.A., Gordeev A.A., Fedorishin D.A. // Nanosystems: Phys. Chem. Math. 2019. V. 10. № 4. P. 456. https://doi.org/10.17586/2220-8054-2019-10-4-456-465
Herrling T., Seifert M., Jung K. // SOFW-J. 2013. V. 139. № 5. P. 10. https://doi.org/10.1002/adma.201302511
Shcherbakov A.B., Zholobak N.M., Ivanov V.K. // Cerium Oxide (CeO2): Synthesis. Properties and Applications. Elsevier, 2020. P. 279. https://doi.org/10.1016/C2017-0-02724-6
Popov A.P., Zvyagin A.V., Lademann J. et al. // J. Biomed. Nanotechnol. 2010. V. 6. № 5. P. 432. https://doi.org/10.1166/jbn.2010.1144
Muth J.F., Kolbas R.M., Sharma A.K. et al. // J. Appl. Phys. 1999. V. 85. № 11. P. 7884. https://doi.org/10.1063/1.370601
Edward D.P., Palik I. // Handbook of optical constants of solids. Orlando: Academic Press, 1985. 804 p.
Debnath S., Islam M.R., Khan M.S.R. // Bull. Mater. Sci. 2007. V. 30. № 4. P. 315. https://doi.org/10.1007/s12034-007-0052-3
Antoniou C., Kosmadaki M.G., Stratigos A.J. et al. // JEADV. 2008. V. 22. № 9. P. 1110. https://doi.org/10.1111/j.1468-3083.2007.02580.x
https://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=OJ:L:2006:265:0039:0043:en:PDF
Pissavini M., Tricaud C., Wiener G. et al. // Int. J. Cosmet. Sci. 2018. V. 40. № 3. P. 263. https://doi.org/10.1111/ics.12459
Ivanov V.K., Baranchikov A.E., Polezhaeva O.S. et al. // Russ. J. Inorg. Chem. 2010. V. 55. P. 325. https://doi.org/10.1134/S0036023610030034
Petříček V., Dušek M., Palatinus L. // Z. Kristallogr. 2014. V. 229. № 5. P. 345. https://doi.org/10.1515/zkri-2014-1737
Stoianov O.O., Ivanov V.K., Shcherbakov A.B. et al. // Russ. J. Inorg. Chem. 2014. V. 59. P. 15. https://doi.org/10.1134/S0036023614020181
Ivanov V.K., Polezhaeva O.S., Tret’yakov Y.D. // Russ. J. Gen. Chem. 2010. V. 80. P. 604. https://doi.org/10.1134/S1070363210030412
Chen Y., Liu T., Chen C. et al. // Mater. Lett. 2013. V. 96. P. 210. https://doi.org/10.1016/j.matlet.2013.01.069
Sun C., Li H., Zhang H. et al. // Nanotechnology. 2005. V. 16. № 9. P. 1454. https://doi.org/10.1088/0957-4484/16/9/006
Meng F., Bo Q., Zhang C. et al. // J. Nanosci. Nanotechnol. 2013. V. 13. № 10. P. 6653. https://doi.org/10.1166/jnn.2013.7527
Chen J.Q., Chen Z.G., Wei Y. // Mater. Sci. Forum. 2013. V. 743–744. P. 389. https://doi.org/10.4028/www.scientific.net/msf.743-744.389
Zhang Z., Wang L., Shao M. et al. // Micro Nano Lett. 2012. V. 7. № 8. P. 770. https://doi.org/10.1049/mnl.2012.0406
Plakhova T.V., Romanchuk A.Y. Yakunin S.N. et al. // J. Phys. Chem. C. 2016. V. 120. № 39. P. 22615. https://doi.org/10.1021/acs.jpcc.6b05650
Feng J., Zhang X., Fu J. et al. // Catal. Commun. 2018. V. 110. P. 28. https://doi.org/10.1016/j.catcom.2018.03.001
Chen Y., Liu T., Chen C. et al. // Ceram. Int. 2013. V. 39. № 6. P. 6607. https://doi.org/10.1016/j.ceramint.2013.01.096
Иванов В.К., Полежаева О.С., Третьяков Ю.Д. // Рос. хим. журн. 2009. Т. 53. № 2. С. 56.
Baranchikov A.E., Polezhaeva O.S., Ivanov V.K. et al. // CrystEngComm. 2010. V. 12. № 11. P. 3531. https://doi.org/10.1039/c0ce00245c
Zholobak N.M., Ivanov V.K., Shcherbakov A.B. et al. // J. Photochem. Photobiol., B. 2011. V. 102. № 1. P. 32. https://doi.org/10.1016/j.jphotobiol.2010.09.002
Иванов В.К., Щербаков А.Б., Усатенко А.В. // Успехи химии. 2009. Т. 78. № 9. С. 924.
https://www.carecreations.basf.com/sunscreen-simulator
Kolesnik I.V., Aslandukov A.N., Arkhipin A.S. et al. // Crystals. 2019. V. 9. № 7. P. 332. https://doi.org/10.3390/cryst9070332
Shekunova T.O., Lapkina L.A., Shcherbakov A.B. et al. // J. Photochem. Photobiol., A. 2019. V. 382. P. 111925. https://doi.org/10.1016/j.jphotochem.2019.111925
Amaro-Ortiz A., Yan B., D’Orazio J. // Molecules. 2014. V. 19. № 5. P. 6202. https://doi.org/10.3390/molecules19056202
Schubert D., Dargusch R., Raitano J. et al. // Biochem. Biophys. Res. Comm. 2006. V. 342. P. 86. https://doi.org/10.1016/j.bbrc.2006.01.129
Das M., Patil S., Bhargava N. et al. // Biomaterials. 2007. V. 28. P. 1918. https://doi.org/10.1016/j.biomaterials.2006.11.036
Singh N., Cohen C.A. Rzigalinski B.A. // Ann. N. Y. Acad. Sci. 2007. V. 1122. № 1. P. 219. https://doi.org/10.1196/annals.1403.015
Niu J., Azfer A., Rogers L.M. et al. // Cardiovasc. Res. 2007. V. 73. P. 549. https://doi.org/10.1016/j.cardiores.2006.11.031
Niu J., Wang K., Kolattukudy P.E. // J. Pharmacol. Exp. Ther. 2011. V. 338. P. 53. https://doi.org/10.1124/jpet.111.179978
Hirst S.M., Karakoti A., Singh S. et al. // Environ. Toxicol. 2013. V. 28. P. 107. https://doi.org/10.1002/tox.20704
Colon J., Herrera L., Smith J. et al. // Nanomedicine. 2009. V. 5. P. 225. https://doi.org/10.1016/j.nano.2008.10.003
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии