Журнал неорганической химии, 2020, T. 65, № 7, стр. 950-957
Фазовый комплекс пятикомпонентной взаимной системы Li+,Na+,K+||F–,Cl–,Br– и исследование стабильного тетраэдра LiF–NaF–KCl–KBr
И. К. Гаркушин a, *, А. В. Бурчаков a, У. А. Емельянова a, М. В. Чугунова a
a Самарский государственный технический университет
443100 Самара, ул. Молодогвардейская, 244, Россия
* E-mail: gik49@yandex.ru
Поступила в редакцию 06.02.2020
После доработки 25.02.2020
Принята к публикации 27.02.2020
Аннотация
Впервые исследован фазовый комплекс пятикомпонентной взаимной системы Li+,Na+,K+||F–,Cl–,Br–. Разбиением в соответствии с теорией графов установлено, что древо фаз системы имеет линейное строение и состоит из стабильных пентатопа LiF–NaF–KF–KBr–KCl, гексатопа LiF–NaBr–NaCl–KCl–KBr–NaF и гептатопа NaCl–KCl–KBr–LiBr–LiCl–LiF–NaBr, соединенных стабильным тетраэдром LiF–NaF–KCl–KBr и стабильным пентатопом LiF–KBr–NaBr–NaCl–KCl. С помощью дифференциального термического анализа изучены фазовые равновесия в стабильном тетраэдре LiF–NaF–KCl–KBr и подтверждены методом рентгенофазового анализа. В тетраэдре реализуется моновариантное фазовое равновесие ж ⇄ LiF + α + KClxBr1 –x, где α – ограниченный твердый раствор на основе NaF (система LiF–NaF), KClxBr1 –x – непрерывный ряд твердых растворов на основе KCl и KBr. Построена компьютерная 3D-модель в виде проекции фазового комплекса на концентрационный тетраэдр в программе КОМПАС 3D. Выделены объемы кристаллизующихся равновесных фаз.
ВВЕДЕНИЕ
Современная технология в значительной степени опирается на материалы с заданными свойствами. Новые материалы во многих случаях представляют собой многокомпонентные композиции. Фазовые диаграммы являются инструментом для создания многих новых материалов, в том числе теплоаккумулирующих, электролитов для химических источников тока, для получения металлов из расплавов электролитов. Расчет, моделирование фазовых равновесий и исследование систем позволяют выявить оптимальные составы для синтеза функциональных материалов [1–13].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектом исследования является комплекс – пятикомпонентная взаимная система Li+,Na+,K+||F–,Cl–,Br– и входящий в нее симплекс – стабильный тетраэдр LiF–NaF–KCl–KBr. Система Li+,Na+,K+||F–,Cl–,Br– включает 9 исходных веществ, 18 двухкомпонентных систем, 6 трехкомпонентных систем, 9 трехкомпонентных взаимных систем и 6 четырехкомпонентных взаимных систем [14].
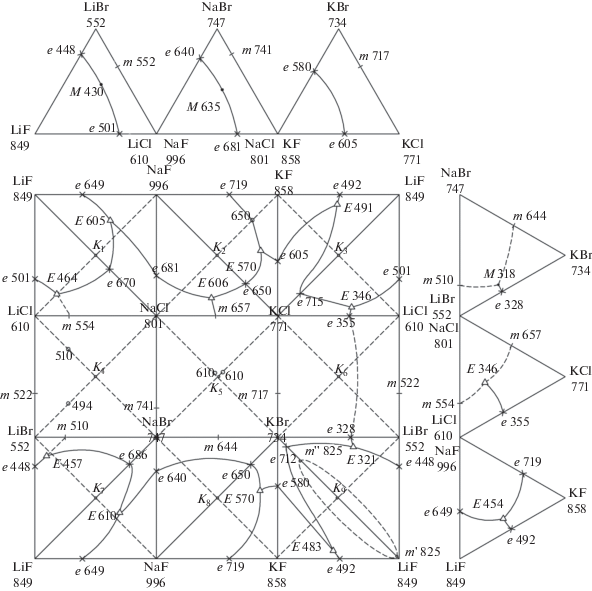
На рис. 1 представлена информация по системам низшей мерности (одно-, двух- и трехкомпонентным взаимным и невзаимным системам), которые являются составными частями остова пятикомпонентной взаимной системы [10–24].
Экспериментальные исследования фазовых равновесных состояний типа жидкость–твердое тело проводили методом дифференциального термического анализа [25]. В работе использовали реактивы марки “ч. д. а.”: LiF (ТУ 6-09-170-77), NaF (ГОСТ 4463-76), KBr (ГОСТ 4160-74), KCl (ГОСТ 4234-77). Все составы выражены в мол. %, температуры – в °С.
Рентгенофазовый анализ образцов проводили на рентгеновском дифрактометре ДРОН-2 (CuKα-излучение, никелевый β-фильтр). Режим съемки стандарта: напряжение на трубке 30 кВ, ток рентгеновской трубки 20 мА, скорость съемки 1 град/мин.
Образцы для РФА отжигали в течение 4 ч в платиновых тиглях при температуре, на 10–20°С ниже температур конечного затвердевания расплавов, закаляли во льду, перетирали в агатовой ступке и запрессовывали в кюветы. Идентификацию фаз осуществляли по межплоскостным расстояниям d (нм) и относительным интенсивностям I/I0 (%) с использованием справочной литературы [26–28].
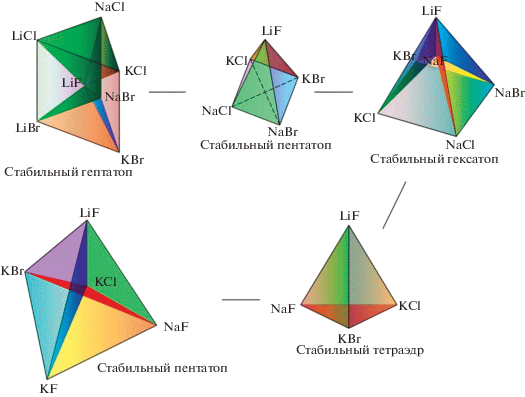
В работе [14] проведено разбиение пятикомпонентной взаимной системы Li+,Na+,K+||F–,Cl–,Br– на стабильные симплексы по теории графов [29]. Получено древо фаз системы Li+,Na+,K+||F–,Cl–,Br– (рис. 2), имеющее линейное строение, которое включает стабильный гептатоп NaCl–KCl–KBr–LiBr–LiCl–LiF–NaBr, гексатоп LiF–NaBr–NaCl–KCl–KBr–NaF и пентатоп LiF–NaF–KF–KBr–KCl, связанные между собой стабильными секущими – пентатопом LiF–KBr–NaBr–NaCl–KCl и тетраэдром LiF–NaF–KCl–KBr.
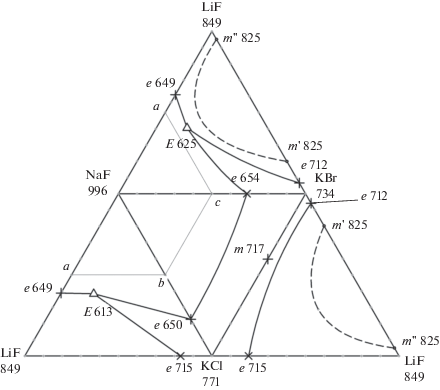
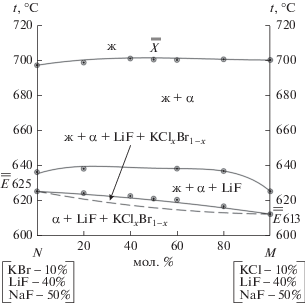
Исследование стабильного тетраэдра LiF–NaF–KCl–KBr методом ДТА. Развертка граневых элементов тетраэдра представлена на рис. 3. На основании анализа развертки граневых элементов для исследования фазового комплекса выбрано двумерное политермическое сечение a[LiF – 50%; NaF – 50%]–b[KCl – 50%; NaF – 50%] – c [KBr – 50%; NaF – 50%] в объеме кристаллизации фторида натрия (рис. 4). В сечении a–b–c экспериментально исследован одномерный политермический разрез N[LiF – 40%; KBr – 10%; NaF – 50%]–M[LiF – 40%; KCl – 10%; NaF – 50%] (рис. 5).
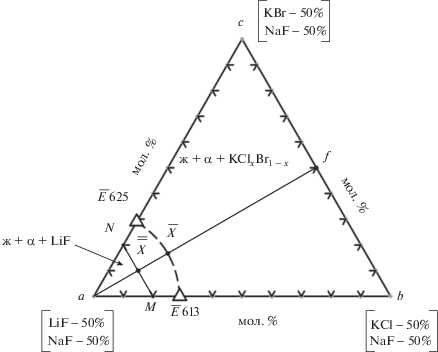
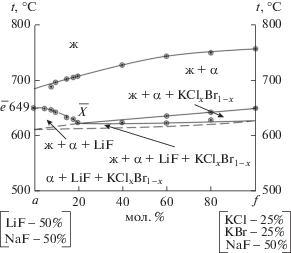
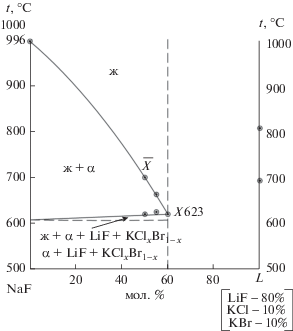
Для дальнейшего исследования был выбран политермический разрез a[LiF – 50%; NaF – 50%]–f[KCl – 25%; KBr – 25%, NaF – 50%], диаграмма состояния которого представлена на рис. 6. Точка $\bar {\bar {X}}$ пересечения ветвей вторичной кристаллизации является проекцией точки Х, принадлежащей линии моновариантного фазового равновесия ж ⇄ α + LiF + KClxBr1 –x, где α – ограниченный твердый раствор (ОТР) на основе NaF (система LiF–NaF), KClxBr1 – x – непрерывный ряд твердых растворов (НРТР) на основе KCl и KBr (рис. 6). Дополнительным разрезом, выходящим из полюса кристаллизации NaF и проходящим через точку $\bar {\bar {X}}$, определены координаты фигуративной точки Х: NaF – 40%, LiF – 48%, KBr – 6%, KCl – 6%, tпл = 623°C (рис. 7).
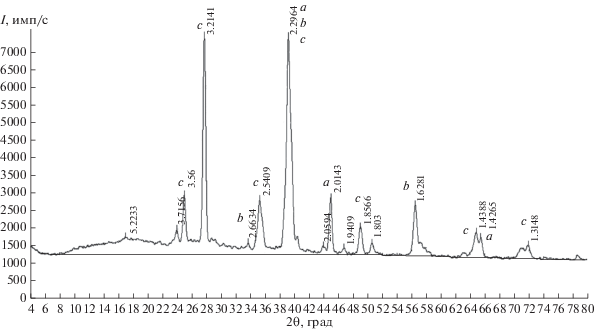
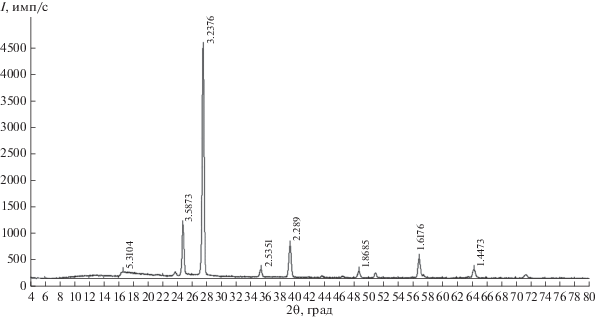
Исследование стабильного тетраэдра LiF–NaF–KCl–KBr методом РФА. Для состава, отвечающего фигуративной точке X на моновариантной кривой, выполнен рентгенофазовый анализ порошка смеси (рис. 8). Дополнительно с целью идентификации фаз твердых растворов KClxBr1 –x в исходной смеси сделан РФА порошка смеси, отвечающей содержанию KCl и KBr в четырехкомпонентной смеси (рис. 9).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На T–x-диаграмме разреза N–M (рис. 5) экспериментально выявлена стабильность фазы твердого раствора KClxBr1 –x и отсутствие четверного минимума на моновариантной линии, соединяющей тройные эвтектики Е625 (стабильный треугольник NaF–LiF–KBr) и E613 (стабильный треугольник LiF–NaF–KCl). При анализе рентгенограммы порошка состава, отвечающего точке Х на линии моновариантного равновесия ж ⇄ LiF + α + KClxBr1 –x, зарегистрированы следующие фазы: LiF, α, KClxBr1 –x (рис. 8) [27, 28]. Таким образом, с помощью РФА подтвержден прогноз кристаллизующихся фаз, выполненный при разбиении системы на симплексы и построении древа фаз. Данное исследование подтверждает точность прогнозирования фаз в многокомпонентных системах, выполненного с помощью разбиения методом графов на симплексы.
На основании экспериментальных результатов и данных элементов огранения построена 3D-модель в виде проекции фазового комплекса на концентрационный тетраэдр LiF–NaF–KCl–KBr (рис. 10) [30].
Рис. 10.
Компьютерная 3D-модель проекции фазового комплекса на концентрационный тетраэдр системы LiF–NaF–KCl–KBr.
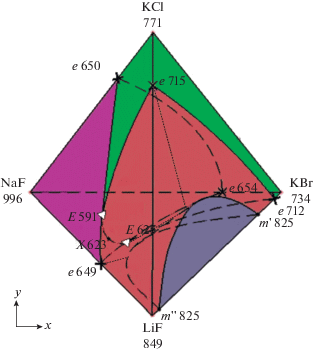
Объемы кристаллизации фаз изображены различными цветами для большей наглядности: красным – фаза LiF, фиолетовым – ограниченный твердый раствор на основе NaF, синим – область расслоения жидких фаз ж1 + ж2, зеленым – НРТР KClxBr1 –x. Базовые геометрические элементы модели представлены в табл. 1.
Таблица 1.
Базовые геометрические элементы модели для системы LiF–NaF–KCl–KBr
| Фазовая область | Число равновесных фаз (Ф) | Степень свободы (С) | Геометрические элементы модели |
|---|---|---|---|
| ж ⇄ α + LiF + KClxBr1 – x | 4 | 1 | Линия E591–X623–E625 |
| ж ⇄ LiF + KClxBr1 – x | 3 | 2 | Поверхность E591–e715–e712–E625–E591 |
| ж ⇄ α + KClxBr1–x | 3 | 2 | Поверхность E591– e650–e654–E625– E591 |
| ж ⇄ α + LiF | 3 | 2 | Поверхность E591–X623–E625–e 649–E591 |
| ж1 = ж2 + LiF | 3 | 2 | Поверхность |
| ж1 = ж2 | 2 | 3 | Локальный объем (синий) |
| ж ⇄ α | 2 | 3 | Локальный объем (фиолетовый) |
| ж ⇄ LiF | 2 | 3 | Локальный объем (красный) |
| ж ⇄ KClxBr1–x | 2 | 3 | Локальный объем (зеленый) |
ЗАКЛЮЧЕНИЕ
1. Проведено разбиение пятикомпонентной взаимной системы на симплексы методом графов. Построено древо фаз, имеющее линейное строение и состоящее из стабильных пентатопа LiF–NaF–KF–KBr–KCl, гексатопа LiF–NaBr–NaCl–KCl–KBr–NaF, гептатопа NaCl–KCl–KBr–LiBr–LiCl–LiF–NaBr, которые соединены стабильным тетраэдром LiF–NaF–KCl–KBr и стабильным пентатопом LiF–KBr–NaBr–NaCl–KCl.
2. Экспериментально изучены фазовые равновесия в стабильном тетраэдре LiF–NaF–KCl–KBr методом ДТА, выявлено образование непрерывных рядов твердых растворов на основе KCl и KBr (KClxBr1 –x). Определены координаты некоторой фигуративной точки Х на моновариантной кривой, отвечающей фазовой реакции: ж ⇄ α + LiF + + KClxBr1 –x.
3. Проведен рентгенофазовый анализ порошка смеси, отвечающей составу точки , мол. %: NaF – 40, LiF – 48, KBr – 6, KCl – 6%, экспериментально подтверждена стабильность кристаллизующихся фаз α + LiF + KClxBr1 –x.
4. Выполнено построение модели фазового комплекса системы, определены объемы кристаллизации фаз.
Список литературы
Chang Y.A., Chen S., Zhang F. et al. // Prog. Mater. Sci. 2004. V. 49. № 3. P. 313. https://doi.org/10.1016/S0079-6425(03)00025-2
Schmid-Fetzer R. // J. Phase Equilib. Diff. 2014. V. 35. № 6. P. 735. https://doi.org/10.1007/s11669-014-0354-2
Fu Taibai, Zheng Zhoushun, Du Yong et al. // Comput. Mater. Sci. 2019. V. 159. P. 478. https://doi.org/10.1016/j.commatsci.2018.12.036
Kang J., Liu B. // J. Alloys Compd. V. 673. 2016. P. 309. https://doi.org/10.1016/j.jallcom.2016.02.200
Nipan G.D. // J. Alloys Compd. V. 371. 2004. P. 160. https://doi.org/10.1016/j.jallcom.2003.08.107
Ардашникова Е.И. // Соросовский образовательный журн. 2004. Т. 8. № 2. С. 30.
Benes O., J.P.M. van der Meer, Konings R.J.M. // Calphad. 2007. V. 31. P. 209. https://doi.org/10.1016/j.calphad.2006.12.004
Андрюнас К., Вишекес Ю., Кабелка В. и др. // Письма в ЖЭТФ. 1985. Т. 42. № 3. С. 333.
Pubin I.I., Thomas R.A. // J. Am. Ceram. Soc. 1969. V. 49. № 2. P. 100.
Минченко В.И., Степанов В.П. Ионные расплавы: упругие и калорические свойства. Екатеринбург: УрО РАН, 2008. 367 с.
Kubota K., Konomura M. // J. Atomic Energy Soc. Jpn. 2002. V. 44. № 5. P. 393.
Басиев Т.Т. // Физика твердого тела. 2006. Т. 47. № 6. С. 1354.
Xie Wei, Morgan D. // Comput. Mater. Sci. 2018. V. 143. P. 505. https://doi.org/10.1016/j.commatsci.2017.11.042
Бурчаков А.В., Емельянова У.А., Гаркушин И.К. // Материалы II съезда химиков респ. Дагестан. Махачкала: Изд-во ДГУ, 2019. С. 120.
Термические константы веществ / Под ред. Глушко В.П. М.: ВИНИТИ ИВТ АН СССР, 1981. Вып. 10. Ч. 1. С. 42.
Термические константы веществ. База данных. Ин-т теплофизики экстремальных состояний РАН Объединенного ин-та высоких температур РАН. Химический факультет МГУ им. М.В. Ломоносова. [Электронный ресурс] URL: http://www.chem.msu.su/cgi-bin/tkv.pl?show=welcom.html (Дата обращения 04.07.19).
Garkushin I.K., Ragrina M.S., Sukharenko M.A. // Russ. J. Inorg. Chem. 2018. V. 63. № 1. P. 98. [Гаркушин И.К., Сухаренко М.А., Рагрина М.С. // Журн. неорган. химии. 2018. Т. 63. № 1. С. 94.]https://doi.org/10.1134/S0036023618010084
Воскресенская Н.К., Евсеева Н.Н., Беруль С.И. и др. Справочник по плавкости систем из безводных неорганических солей. М.: Изд-во АН СССР, 1961. Т. 1. 845 с. Т. 2. 585 с.
Диаграммы плавкости солевых систем. Многокомпонентные системы / Под ред. Посыпайко В.И., Алексеевой Е.А. М.: Химия, 1977. 216 с.
Егорцев Г.Е., Гаркушин И.К., Истомова М.А. // Изв. ВУЗов. Химия и хим. технология. 2005. Т. 48. № 10. С. 86.
Гаркушин И.К., Чугунова М.В., Милов С.Н. Образование непрерывных рядов твердых растворов в тройных и многокомпонентных солевых системах. Екатеринбург: УрО РАН, 2011. 140 с.
Ефимов А.И., Белорукова Л.В., Василькова И.В. и др. Свойства неорганических соединений. Справочник. Л.: Химия, 1983. С. 82, 83.
Sangster J.M., Pelton A.D. // J. Phys. Chem. Ref. Data. V. 16. № 3. 1987. P. 509.
Егорцев Г.Е., Гаркушин И.К., Истомова М.А. Фазовые равновесия и химическое взаимодействие в системах с участием фторидов и бромидов щелочных металлов. Екатеринбург: УрО РАН, 2008. 132 с.
Мощенский Ю.В. // Приборы и техника эксперимента. 2003. № 6. С. 143.
Ковба Л.М., Трунов В.К. Рентгенофазовый анализ. М.: Изд-во МГУ, 1976. 232 с.
База данных Inorganic Material Database (AtomWork) [Электронный ресурс].: https://crystdb.nims.go.jp/index_en.html (Дата обращения 01.06.2019).
Миркин Л.И. Справочник по рентгеноструктурному анализу поликристаллов. М.: Изд-во физ.-мат. литер., 1961. 863 с.
Посыпайко В.И., Алексеева Е.А., Первикова В.Н. и др. // Журн. неорган. химии. 1973. Т. 17. № 11. С. 3051.
Burchakov A.V., Egorova E.M., Kondratyuk I.M., Moshchenskii Yu.V. // Russ. J. Inorg. Chem. 2018. V. 63. P. 950. [Бурчаков А.В., Егорова Е.М., Кондратюк И.М., Мощенский Ю.В. // Журн. неорган. химии. 2018. Т. 63. № 7. С. 909.]https://doi.org/10.1134/S0036023618070033
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии