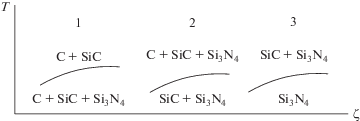Журнал неорганической химии, 2020, T. 65, № 6, стр. 829-836
Обобщенная CVD-диаграмма системы Si–C–N–H–Не(Ar)
В. А. Шестаков a, *, В. И. Косяков a, М. Л. Косинова a
a Институт неорганической химии им. А.В. Николаева СО РАН
630090 Новосибирск, пр-т Академика Лаврентьева, 3, Россия
* E-mail: vsh@niic.nsc.ru
Поступила в редакцию 15.11.2019
После доработки 18.12.2019
Принята к публикации 30.01.2020
Аннотация
Пленки карбонитрида кремния (SiCxNy) благодаря своим свойствам имеют широкие возможности практического применения. Получили интенсивное развитие методы приготовления объемных и пленочных материалов на основе SiCxNy. Рассмотрено получение таких пленок методом химического осаждения из газовой фазы (CVD) с использованием кремнийорганических соединений в качестве исходных веществ. Дополнительными составляющими входных газов являются реагенты NH3, N2 и инертный газ (Не или Ar). Проанализированы основы термодинамических расчетов этого процесса, протекающего в квазиравновесных условиях. Построена обобщенная CVD-диаграмма системы Si–C–N–H–He(Ar) при избытке в ней углерода в области изменения параметров процесса осаждения: p = 0.01–10 Торр, T = 600–1400 K, n(N)/n(Si) = 1–10. Данная диаграмма полезна при экспериментальном исследовании системы Si–C–N–H–He(Ar).
ВВЕДЕНИЕ
Пленки карбонитрида кремния SiCxNy обладают такими функциональными характеристиками, как высокая твердость, низкий коэффициент трения, малое термическое расширение, химическая устойчивость в агрессивных средах и др., что делает их пригодными для использования в качестве защитных покрытий в различных областях техники. В настоящее время существует ряд методик получения пленок SiCxNy с использованием как физических, так и химических методов осаждения. Среди последних особое внимание уделяется методам химического осаждения из газовой фазы (CVD) с использованием летучих кремнийорганических соединений в качестве исходных веществ [1–8]. Пленки получают в проточном реакторе, в который подается газ заданного состава. В рабочей зоне реактора при заданных температуре Т и общем давлении р расположена подложка, на которой осаждается пленка в результате химических реакций в газовой фазе и на границе газ–пленка. Физико-химические и функциональные свойства пленок зависят от их состава и структуры, которые, в свою очередь, определяются технологическими и физико-химическими параметрами процесса осаждения: температурой и давлением в реакторе, скоростью потока газа, неоднородностью температурного поля, методом и параметрами воздействия на газ (ВЧ, лазерное излучение и т.д.) перед его попаданием в рабочую зону реактора или непосредственно в этой зоне и т.д. Например, повышение температуры и уменьшение скорости осаждения должны приводить к появлению нанокристаллических включений в аморфной матрице и образованию композитных и в итоге нано- и микрокристаллических многофазных пленок. В пленках с повышенным содержанием углерода обнаружены наночастицы графита [9, 10].
Сложность проблемы получения пленок SiCxNy с заданными свойствами и многообразие возможных вариантов технологического решения делают актуальной задачу априорного моделирования при разработке лабораторных и технологических методик их получения. На начальном этапе моделирования удобно рассматривать простейшую модель процесса CVD, когда предполагается, что все фазы, находящиеся в рабочей зоне реактора, образуют равновесную термодинамическую систему, состояние которой определяется ее элементным составом, температурой и давлением. В систему вводится поток газа заданного состава, в рабочей зоне реактора осаждается пленка. Газ, находящийся в равновесии с этой пленкой, удаляется из реактора. Для моделирования такого процесса достаточно рассчитать условия равновесия между пленкой и газовой фазой в заданной области варьирования состава газа на входе в реактор, температуры Т и общего давления p в реакторе.
Термодинамическое моделирование процессов CVD с разными исходными летучими кремнийорганическими веществами и дополнительными газообразными реагентами и инертными газами (газ-носитель) проводили в широких пределах условий реализации технологического процесса: p = 0.01–10 Торр, T = 300–1300 K и отношений входных потоков газов и исходных веществ R = 1–50 [1, 11]. Расчеты осуществляли с помощью программного обеспечения термодинамического раздела Банка данных свойств материалов электронной техники (БнД СМЭТ, ИНХ СО РАН) [12]. Состав конденсированных фаз и находящейся в равновесии с ними газовой фазы рассчитывали методом минимизации функции свободной энергии Гиббса при ограничениях, задаваемых условиями материального баланса. В качестве исходной термодинамической информации использовали стандартные термодинамические характеристики индивидуальных веществ: ΔfH0(298 K), S0(298 K), $C_{p}^{0} = f(T).$ К сожалению, в настоящее время отсутствуют термодинамические характеристики для нитрида углерода и тройного соединения карбонитрида кремния, поэтому возможность образования этих фаз не учитывали. Набор согласованных термодинамических свойств для всех соединений был взят из БнД СМЭТ. На основании полученных CVD-диаграмм прогнозировали состав осаждаемых фазовых комплексов в зависимости от типа реагента, условий проведения процесса и среды, в которой происходит осаждение.
Примером работы, посвященной исследованию рассматриваемой системы, является исследование влияния дополнительных составляющих входных газов – He, N2, NH3 – на состав образующейся пленки [13]. По данным [13], увеличение содержания во входном газе гелия не приводит к существенному изменению температурной области существования фазовых комплексов SiC + C и SiC + C + Si3N4. Однако увеличение общего давления в системе от 0.01 до 10 Торр приводит к значительному увеличению температурной области существования трехфазного комплекса. Добавление в систему аммиака приводит к появлению на диаграмме дополнительно области существования двухфазного комплекса C + Si3N4. Аналогичная диаграмма получается, если вместо аммиака добавлять в систему азот. Увеличение общего давления в системе приводит к увеличению температурной области существования комплексов SiC + C + Si3N4 и C + Si3N4.
Рассмотрим особенности используемой в вышеперечисленных работах методологии термодинамического моделирования процесса газофазного осаждения карбонитрида кремния SiCxNy в проточном реакторе.
1. В реактор подается смесь газов (G), компонентами которой могут являться
– кремнийорганические соединения: безазотные SikClHm (КОС1) или азотсодержащие SikClNmHq (КОС2);
– газообразные реагенты: R1 – азотсодержащие (N2, NH3) или R2 – безазотные (H2), эти газы могут участвовать в химических реакциях образования пленки SiCxNy;
– нейтральные газы He, Ar, используемые в качестве газов-носителей и регуляторов общего давления в реакторе.
При конструировании входной газовой смеси из этих газов-компонентов процесс CVD протекает в химических системах с элементным составом Si–C–N–H и Si–C–N–H–(Не или Ar).
2. Состав системы определяется парциальными давлениями (рi) исходного летучего вещества, дополнительных газов-реагентов и газов-носителей на входе в реактор при p = const. Состав газовой смеси удобно задавать через отношения парциальных давлений этих газов ζj. В табл. 1 приведены некоторые примеры моделирования CVD-процессов для системы Si–C–N–H–Не.
Таблица 1.
Примеры моделирования осаждения пленок SiCxNy из смеси кремнийорганического соединения и гелия
| Соединение | Si : N | Тосаж, K | p, Торр | Фазовые комплексы | Литература |
|---|---|---|---|---|---|
| Бис(триметилсилил)этиламин EtN(SiMe3)2 | 2 : 1 | 500–1200 | 0.01 и 10 | SiC + C + Si3N4|SiC + C | [13] |
| Бис(триметилсилил)фениламина PhN(SiMe3)2 | 2 : 1 | ||||
| Гексаметилциклотрисилазан [(CH3)3Si]2NH | 1 : 1 | 300–1300 | 0.01–10 | Si3N4 + SiC + C|SiC + C | [14] |
| Диметил-бис(диэтиламино)силан Me2Si(NEt2)2 | 1 : 2 | 300–1300 | 0.01–10 | Si3N4 + C|Si3N4 + SiC + C|SiC + C | [15] |
| Метил-бис(диэтиламино)силан MeНSi(NEt2)2 | 1 : 2 | ||||
| Трис(диэтиламино)силан НSi(NEt2)3 | 1 : 3 | ||||
| Метил-трис(диэтиламино)силан MeSi(NEt2)3 | 1 : 3 | ||||
| Тетракис(диэтиламино)силан Si(NEt2)4 | 1 : 4 | ||||
| Трис(диэтиламино)силан НSi(NEt2)3 | 1 : 3 | 300–1300 | 0.01–10 | Si3N4 + C|Si3N4 + SiC + C|SiC + C | [16] |
| Триметилфенилсилан PhSiMe3 | 1 : 0 | 300–1300 | 0.01 и 10 | SiC + C | [17] |
| Тетраметилсилан Si(CH3)4 | 1 : 0 | SiC + C | [18] |
3. Для проведения термодинамических расчетов необходимо задать мольный брутто-состав системы CVD. Если газ на входе в реактор рассматривать как идеальную смесь газов-компонентов, величины ζj равны отношению количества молей газов, поступивших в реактор в заданный промежуток времени.
4. В настоящее время сложно построить термодинамическую модель аморфной или частично закристаллизованной пленки, поэтому при термодинамическом анализе равновесного CVD-процесса предполагают, что пленка состоит из смеси кристаллических фаз постоянного состава. Это предельное равновесное состояние пленки, к которому она стремится при уменьшении скорости осаждения или при длительном изотермическом отжиге. В системе Si–C–N–H в условиях моделирования могут существовать более 20 стабильных и метастабильных конденсированных фаз. Расчеты в рамках используемой термодинамической модели системы CVD показали, что в равновесной пленке могут присутствовать только следующие кристаллические фазы: Si (куб.), C (графит), β-SiC (куб.), α-Si3N4 (гекс.). Таким образом, к настоящему времени опубликовано большое количество примеров термодинамических расчетов процессов получения пленок SiCxNy методом CVD в системе Si–C–N–H–(Ar, He). Расчетные диаграммы обладают схожими особенностями их строения, что позволяет предположить возможность построения обобщенной CVD-диаграммы, для которой описанные в литературе результаты моделирования можно рассматривать как ее фрагменты.
ФАЗОВАЯ ДИАГРАММА СИСТЕМЫ Si–C–N–H–(He)
Эксперимент по осаждению пленки SiCxNy из газовой фазы обычно реализуют в стационарных условиях при постоянных температуре, давлении и составе газа. Результаты термодинамического расчета равновесия между пленкой и газовой фазой при заданных значениях p, Т и составе системы удобно отразить в виде фазовых комплексов, образованных из газовой фазы, и находящихся с ней в равновесии твердых фаз. Объединение множества таких комплексов описывают в виде фазовой диаграммы рассматриваемой химической системы в заданной области пространства p–Т–х (х – вектор состава системы). Для системы, образованной из t компонентов, эта диаграмма является геометрической фигурой с размерностью от t – 1 при p, T = = const до t + 1 при переменных p и Т. Компонентами системы являются химические элементы.
Для понимания особенностей CVD-процесса полезно знать строение изобарно-изотермической диаграммы. Для четырехкомпонентной системы она ограничена тетраэдром составов Si–C–N–H. Предполагается, что все твердые фазы системы являются стехиометрическими. Область составов моделируемой пленки является частью грани C–N–Si тетраэдра, ограниченной фигурой С–SiC–Si–C3N4–Si3N4. На рис. 1а показана условная схема тетрангуляции концентрационного тетраэдра Si–C–N–H. На ней газовая фаза обозначена точкой G. Когда газовая фаза содержит все компоненты, соответствующая ей фигуративная точка находится внутри тетраэдра. Если все твердые фазы имеют постоянный состав, область существования пленки занимает участок Si–C–С3N4–Si3N4 на грани Si–C–N исходного тетраэдра. На условной схеме показаны тетраэдрические области четырехфазного равновесия: G–Si–SiC–Si3N4, G–SiC–C–Si3N4, G–C–С3N4–Si3N4. Объединение этих областей схематично описывает фазовые равновесия, которые могут реализоваться в процессе CVD. Точки на ребрах тетраэдров соответствуют равновесию газа с однофазными пленками, точки на гранях тетраэдров описывают равновесие газа с двухфазными пленками, внутренние точки тетраэдров символизируют осаждение трехфазных пленок.
Рис. 1.
Схемы изобарно-изотермической фазовой диаграммы системы Si–C–N–H: а – условная схема тетрангуляции концентрационного тетраэдра Si–C–N–H; б – концентрационный тетраэдр со схематическими изображениями изобарно-изотермических фазовых диаграмм тройных граничных систем.
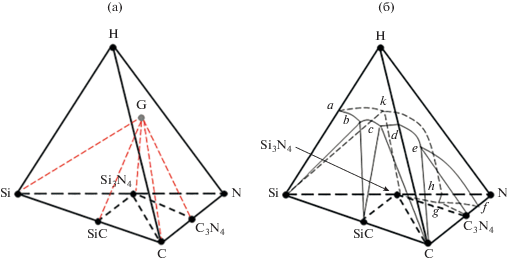
На рис. 1б приведена упрощенная геометрическая схема диаграммы, соответствующей рис. 1а. На ней показан концентрационный тетраэдр со схемами изобарно-изотермических фазовых диаграмм тройных граничных систем. Поверхность, ограниченная линией abcdefghka, отделяет область существования газовой фазы от областей двух- и трехфазных равновесий с ее участием. Точки a, b,… и отрезки ab, bс,… показывают состав газовой фазы, находящейся в равновесии с двумя или одной конденсированной фазой в тройных граничных системах. На рисунке не изображены точки и линии внутри этой поверхности, которые разбивают ее на фрагменты, соответствующие составу газа, находящегося в равновесии с одно-, двух- и трехфазными пленками.
В настоящее время активно исследуются и уже используются функциональные покрытия SiCxNy [1–7], состав которых находится внутри треугольника C–SiC–Si3N4. Рассмотрим детальнее соответствующую область фазовой диаграммы Si–C–N–H. На рис. 2 показаны возможные графы равновесий с участием газовой и твердых фаз в концентрационном тетраэдре в виде проекции из вершины H на грань Si–C–N. На рис. 2а, 2б показаны инвариантные равновесия, которые реализуются при строго определенном составе газа, показанного точкой G. В первом случае проекция фигуративной точки состава газа находится внутри треугольника, во втором – вне его. На рис. 2в, 2г показаны случаи равновесия твердых фаз с газом, существующим в некоторой области тетраэдра составов, в которой не наблюдается инвариантное равновесие. Возможность реализации того или иного случая при заданных p и Т определяется средним составом химической системы.
Рис. 2.
Фрагменты фазовой диаграммы, иллюстрирующие равновесие между газом и кристаллическими фазами C, SiC и Si3N4: a, б – инвариантные равновесия; в, г – равновесия с газовой фазой переменного состава.
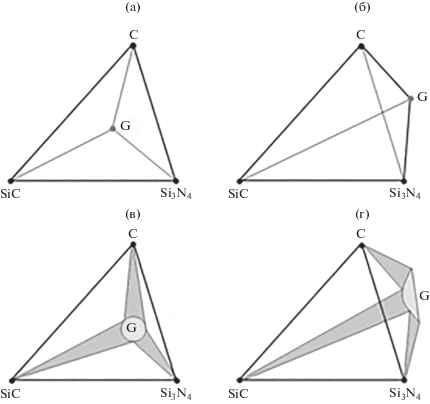
Термодинамическое моделирование позволяет построить необходимый фрагмент фазовой диаграммы или всю диаграмму в интересующей области состава системы и ее параметров состояния Т и p. Результат расчета в сочетании с уравнениями материального баланса компонентов позволяет определить составы равновесных фаз и их относительные количества в любой точке пространства фазовой диаграммы.
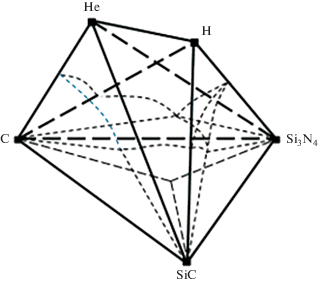
При добавлении инертного газа система становится пятикомпонентной, что затрудняет ее изображение на плоскости. Состав системы ограничен пентатопом в четырехмерном пространстве. Простейший пример проекции диаграммы C–H–N–Si–Не на плоскость показан на рис. 3.
CVD-ДИАГРАММЫ СИСТЕМЫ Si–C–N–H–(He)
При проведении CVD-процесса контролируют состав газа, поступающего в реактор, т.е. состав рассматриваемой химической системы. При термодинамическом моделировании обычно проводят серии термодинамических расчетов, в которых закономерно изменяется координата состава входного газа. Поэтому при построении CVD-диаграмм удобно использовать одну координату состава при построении ζ–Т- или ζ–p-диаграмм либо две координаты состава при построении изобарно-изотермических ζ1–ζ2-диаграмм, как это описано во Введении.
Фрагмент изобарно-изотермической фазовой диаграммы четырех- или пятикомпонентной системы для получения пленок SiCxNy схематично показан на рис. 4. Темно-серым цветом показаны области составов пленки и газовой фазы, находящейся в равновесии с пленкой. Пусть в серии экспериментов составы газа, подаваемого в реактор, лежат на отрезке aa', при этом составы осаждаемых пленок лежат на кривой bb', а соответствующие составы газов, выходящих из реактора, – на кривой сс'. Точки кривых bb' и сс' соединены прямолинейными отрезками (квазиконодами), линия aa' лежит на этой поверхности. Согласно рис. 2, область состава пленок разделена на участки с разным фазовым составом. Если линия составов системы пересекает границу между участками, на линиях bb' и сс' появляются точки излома.
Рис. 4.
Схема соотношения между составами входного газа aa', пленки bb' и газа, выходящего из реактора cc'.
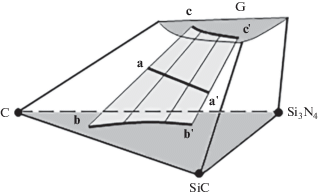
CVD-диаграмму изображают в виде сечения фазовой диаграммы поверхностью φ(ζ1ζ2), где координаты выбираются исследователем для описания результатов CVD-процесса. В этом случае пространство CVD-диаграммы разделено на области, в которых пленка имеет разный фазовый состав. В частности, диаграмма в области C–SiC–Si3N4 может содержать области однофазных пленок C, SiC, Si3N4, двухфазных пленок C–SiC, С–Si3N4, SiC–Si3N4 и трехфазной пленки C–SiC–Si3N4. В литературе описаны расчетные CVD-диаграммы, содержащие следующие фазовые комплексы: С + SiC, Si3N4 + C + SiC, Si3N4 + C, Si3N4. Последовательность выделения фазовых комплексов при понижении температуры может быть связана с величиной давления пара над конденсированными соединениями. Поэтому на CVD-диаграмме присутствуют линии, показанные на рис. 5 (см. также табл. 1) Аналогичные кривые могут реализоваться при выборе вместо Т других координат, например p.
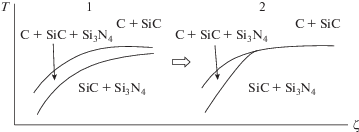
Моновариантные линии на CVD-диаграмме могут объединяться в сети с образованием трех- и четырехвалентных вершин. На рис. 6.1 показан пример близкорасположенных кривых. На рис. 6.2 при больших ζ кривые сливаются. В этом случае на CVD-диаграмме возникает тройная точка.
При избытке в системе углерода, как это обычно бывает при использовании кремнийорганических соединений в качестве прекурсоров, можно составить обобщенную схему диаграммы, которая показывает общие закономерности трансформации CVD-диаграммы при изменении параметров такой системы. На рис. 7 приведена такая схема, полученная для изменения параметров системы11 в интервалах: p = 0.01–10 Торр, Т = 600–1400 K, n(N)/n(Si) = 1–10. При этом граница между областями фазовых комплексов Si3N4 + С и SiС + С определяется равновесием Si3N4 + 3С ↔ 3SiС + 2N2. Например, при n(N)/n(Si) = 10 и p = 0.01 Торр ему соответствует температура 1046 K, а при p = = 10 Торр – 1325 K.
Рис. 7.
Обобщенная схема CVD-диаграммы для системы Si–C–N–H–Ar при изменении ее параметров в интервалах: p = 0.01–10 Торр, Т = 600–1400 K, n(N)/n(Si) = 1–10.
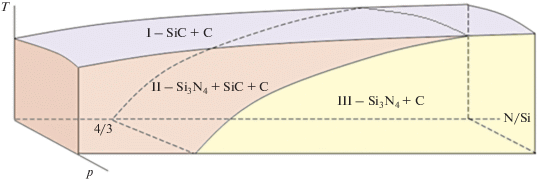
Схемы на рис. 5–7, показывающие взаимное расположение областей существования фазовых комплексов, а также моновариантных линий, получены на основе анализа результатов работ, упомянутых в табл. 1, а также расчетов, выполненных в настоящей работе в указанной области изменения параметров.
Отметим, что в других системах, например в Si–C–N–H–Cl, термодинамические расчеты показывают присутствие полей SiC + Si3N4 и SiC [19–21]. Однако обогащенные углеродом пленки карбонитрида кремния, рассмотренные в данной работе, в настоящее время представляют большой интерес для исследователей [22–26].
ЗАКЛЮЧЕНИЕ
Фазовая диаграмма четверной системы Si–C–N–H при заданных р и Т представляет собой концентрационный тетраэдр, разделенный на области сосуществования кристаллических фаз (С, Si, SiC, Si3N4, C3N4) с газом. В упомянутых выше работах (табл. 1) рассматривали область составов пленки внутри треугольника С–SiC–Si3N4. При варьировании p и Т фазовая диаграмма системы не изменяется, если это стехиометрические фазы, однако элементный состав пленки не остается постоянным. Траектория его изменения определяется температурой и давлением в системе. По результатам исследования CVD-процесса можно построить серию таких траекторий. Каждая из них построена из отрезков, на которых в квазиравновесных рассмотренных условиях выделяются комплексы из C + SiC, C + Si3N4 и С + SiC + + Si3N4. Совокупность таких траекторий позволяет восстановить фазовую диаграмму. Поэтому исследование осаждения пленок CVD и построение фазовых диаграмм дополняют друг друга. Построена обобщенная CVD-диаграмма системы Si–C–N–H–He(Ar) при избытке в ней углерода.
Список литературы
Кузнецов Ф.А., Воронков М.Г., Борисов В.О. и др. Фундаментальные основы процессов химического осаждения пленок и структур для наноэлектроники. Сер. Интеграционные проекты СО РАН. Вып. 37. Новосибирск: Изд-во СО РАН, 2013. 176 с.
Sobczyk-Guzenda A., Oleśko K., Gazicki-Lipman M. et al. // Mater. Res. Express. 2019. V. 6. P. 016410. https://doi.org/10.1088/2053-1591/aae4f9
Khatami Z., Simpson P.J., Mascher P. // Nanotechnology. 2019. V. 30. P. 314003. https://doi.org/10.1088/1361-6528/ab180c
Murano M., Matsutani T., Kawasaki T. // Vacuum. 2018. V. 158. P. 60. https://doi.org/10.1016/j.vacuum.2018.09.005
Fainer N.I., Plekhanov A.G., Asanov I.P. // Glass Phys. Chem. 2017. V. 43. № 5. P. 410. https://doi.org/10.1134/S1087659617050042
Fainer N.I., Plekhanov A.G., Golubenko A.N. et al. // J. Struct. Chem. 2017. V. 58. № 1. P. 119. https://doi.org/10.1134/S0022476617010188
Wu H.-Y., Hsu C.-H., Liu T.-X. et al. // Surf. Coat. Technol. 2019. V. 376. P. 68. https://doi.org/10.1016/j.surfcoat.2018.04.092
Wrobel A.M., Uznanski P., Walkiewicz-Pietrzykowska A., Jankowski K. // Appl. Organomet. Chem. 2017. V. 31. P. e3871. https://doi.org/10.1002/aoc.3871
Reinold L.M., Yamada Y., Graczyk-Zajac M. et al. // J. Power Sources. 2015. V. 282. P. 409. https://doi.org/10.1016/j.jpowsour.2015.02.074
Graczyk-Zajac M., Wimmer M., Neumann C., Riedel R. // J. Solid State Electrochem. 2015. V. 19. P. 2763. https://doi.org/10.1007/s10008-015-2814-y
Rakhlin V.I., Tsirendorzhieva I.P., Voronkov M.G. et al. // Glass Phys. Chem. 2010. V. 36. № 3. P. 376. https://doi.org/10.1134/S1087659610030156
Kuznetsov F.A., Titov V.A., Borisov S.V., Vertoprakhov V.N. // CODATA Bulletin: Abstracts. 11th Int. CODATA Conference, Karlsruhe, Germany, 1988. № 68. P. 9.
Shestakov V.A., Ermakova E.N., Sysoev S.V. et al. // Russ. Chem. Bull. 2018. V. 67. № 6. P. 980. https://doi.org/10.1007/s11172-018-2167-7
Fainer N.I., Golubenko A.N., Rumyantsev Yu.M., Maximovskii E.A. // Glass Phys. Chem. 2009. V. 35. № 3. P. 274. https://doi.org/10.1134/S1087659609030067
Sysoev S.V., Nikulina L.D., Kosinova M.L. et al. // Inorg. Mater. 2011. V. 47. № 12. P. 1324. https://doi.org/10.1134/S0020168511110227
Fainer N.I., Golubenko A.N., Rumyantsev Yu.M. et al. // Glass Phys. Chem. 2012. V. 38. № 1. P. 15. https://doi.org/10.1134/S1087659612010051
Ермакова Е.Н., Сысоев С.В., Никулина Л.Д. и др. // Изв. ВУЗов. Материалы электронной техники. 2014. Т. 17. № 3. С. 199.
Berestenko V.I., Kurkin E.N., Torbov V.I., Domashnev I.A. // High Energ. Chem. 2016. V. 50. № 3. P. 221. https://doi.org/10.1134/S0018143916030036
Xue J., Yin X., Liu X., Zhang L. // J. Eur. Ceram. Soc. 2014. V. 34. P. 3607. https://doi.org/10.1016/j.jeurceramsoc.2014.05.023
Xue J.M., Yin X.W., Ye F., Cheng L.F. // J. Am. Ceram. Soc. 2013. V. 96. P. 979. https://doi.org/10.1111/jace.12115
Liu X.F., Zhang L.T., Liu Y.S. // Ceram. Int. 2013. V. 39. P. 3971. https://doi.org/10.1016/j.ceramint.2012.10.245
Chang W.-Y., Chen W.-Z., Lee H.-T., Leu J. // Jpn. J. Appl. Phys. 2019. V. 58. P. SHHB01. https://doi.org/10.7567/1347-4065/ab1fd5
Storch M., Vrankovic D., Zajac M., Riedel R. // Solid State Ionics. 2018. V. 315. P.59. https://doi.org/10.1016/j.ssi.2017.11.032
Lee W.-J., Choa Y.-H. // Thin Solid Films. 2018. V. 657. P. 32. https://doi.org/10.1016/j.tsf.2018.04.042
Gao Y., Mera G., Nguyen H. et al. // J. Eur. Ceram. Soc. 2012. V. 32. P. 1857. https://doi.org/10.1016/j.jeurceramsoc.2011.09.012
Chang W.-Y., Chung H.-T., Chen Y.-C. et al. // J. Vac. Sci. Technol. B. 2018. V. 36. P. 060601-1. https://doi.org/10.1116/1.5063294
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии