Журнал неорганической химии, 2020, T. 65, № 2, стр. 261-270
Реакционный искровой плазменный синтез пористого биокерамического волластонита
Е. К. Папынов a, b, *, О. О. Шичалин a, И. Ю. Буравлев a, b, А. С. Портнягин a, А. А. Белов a, b, В. Ю. Майоров a, Ю. Е. Скурихина c, Е. Б. Меркулов a, В. О. Главинская a, b, А. Д. Номеровский a, b, А. В. Голуб a, Н. П. Шапкин b
a Институт химии ДВО РАН
690022 Владивосток, пр-т 100-летия Владивостока, 159, Россия
b Дальневосточный федеральный университет
690090 Владивосток, ул. Суханова, 8, Россия
c Тихоокеанский государственный медицинский университет Минздрава России
690002 Владивосток, пр-т Острякова, 2, Россия
* E-mail: papynov@mail.ru
Поступила в редакцию 26.09.2019
После доработки 04.10.2019
Принята к публикации 05.10.2019
Аннотация
Представлен способ реакционного искрового плазменного синтеза (Р-ИПС) пористого (Sуд = 12.7–8.56 м2/г) и конструкционно-прочного (σсж = 201.1–393.2 МПа) биокерамического композитного материала на основе волластонита (CaSiO3) в составе с 20 мас. % гидроксиапатита (ГАП). Способ заключается в использовании в качестве сырьевого компонента аморфного композита на основе ксонотлита (Ca6Si6O17 · 2OH) в смеси с ГАП и порообразователем, полученного золь-гель (темплатным) синтезом. Оригинальность способа состоит в формировании керамического волластонита кристаллической структуры при трансформации его гидратированной формы ксонотлита в условиях искрового плазменного разогрева. Изучена динамика уплотнения, фазообразование и микроструктурные изменения формируемой CaSiO3/ГАП керамики при различных температурах (500–900°С) Р-ИПС с применением РФА, ТГА/ДТА, РЭМ, БЭТ, порометрии. Проведена микробиологическая оценка эффективности формирования бактериальных пленок Pseudomonas aeruginosa на поверхности образцов полученной CaSiO3/ГАП керамики, в том числе в сравнении с некомпозитным составом, в отсутствие ГАП. Предлагаемый способ Р-ИПС обеспечивает создание пористой и конструкционно-прочной композитной керамики, содержащей биосовместимый компонент ГАП, которая может быть перспективна для костно-керамических имплантатов при восстановлении дефектов костной ткани.
ВВЕДЕНИЕ
Современная медицина в значительной степени зависит от биотехнологий, развитие которых определяется качеством современных биоматериалов. Биоматериаловедение изучает физико-химические и механические характеристики биоматериалов: химическую инертность, термостабильность, радиационную устойчивость, конструкционную прочность, пластичность, микроструктурное разнообразие [1], учитывает биосовместимые с живым организмом свойства таких систем, основанные на нетоксичности, биоинертности или биоактивности, биорезистивности [2]. Особый интерес вызывает силикат кальция (CaSiO3) в кристаллической модификации β-волластонит, обладающий всеми требуемыми и указанными выше характеристиками [3–9]. К преимуществам волластонита следует также отнести его универсальность в наборе биосовместимых свойств. Он может выступать как в качестве биоинертного материала в протезировании, так и в виде биоактивной системы в регенеративной импланталогии. Последнее свойство связано с его способностью активизировать рост апатитового слоя на своей поверхности за счет выраженной остеокондуктивности и биорезорбции вследствие обмена (выноса) с биоорганической средой ионами Ca2+ и ${\text{SiO}}_{3}^{{2 - }},$ что делает его перспективным для использования в качестве искусственного заменителя костной ткани [10]. Анализ работ по исследованию биосовместимых свойств волластонита представлен в [11]. Несмотря на это, волластонит, как и практически все известные искусственные биоматериалы, нуждается в повышении биоактивных свойств и структурных характеристик с целью достижения максимального подобия функциональным и структурным параметрам костной ткани. Применяя известные методы мокрого и твердофазного синтеза, ученые стремятся получить биоматериалы, модифицированные гидроксиапатитом (ГАП), который является полным аналогом живой кости [12–14]. Формирование керамических композитов является чрезвычайно сложной задачей. Оно связано с трудностями, обусловленными негативным воздействием термообработки на состав (нестабильность ГАП при температуре >1000°С) и микроструктуру (деструкция пористого объема и рост зерна) конечного материала [12, 15, 16].
Решение указанных проблем и получение керамики высокого качества возможно при использовании передовых и оригинальных технологий синтеза, например, искрового плазменного спекания (ИПС) и его модификаций или комбинаций с другими методами [17–19]. Ранее нами было показано, что высокоскоростной электроимпульсный разогрев нано- и микрокристаллических порошков под давлением прессования, осуществляемый по технологии ИПС, обеспечивает быстрое формирование керамического волластонита с регулируемой микроструктурой и высокими механическими характеристиками [20]. Более того, расширение возможностей данной технологии применительно к синтезу керамического волластонита было исследовано нами в условиях комбинирования ИПС с золь-гель (темплатным) синтезом [21]. Оригинальность такого решения заключается в консолидации дисперсного гидратированного силиката кальция (ксонотлита) аморфной структуры в смеси с порообразующими темплатами при оптимальных условиях электроимпульсной термообработки по технологии ИПС. Такой подход обеспечивает инициирование фазового перехода аморфного ксонотлита в кристаллическую модификацию волластонита с иерархически пористым керамическим каркасом, в том числе функционализированного наноразмерными частицами золота [22].
Описанный способ представляет собой элемент реакционного синтеза, протекающего в условиях ИПС, когда термическое воздействие на исходное сырье инициирует реакцию в твердой фазе и на выходе образуется новый продукт. Успешные примеры реакционного ИПС (Р-ИПС) различных керамик описаны в работах [23–25], демонстрирующих перспективность этого способа.
Исходя из вышеизложенного, в настоящей работе предлагается исследовать ранее нереализованный способ Р-ИПС с целью получения композитной керамики на основе кристаллического волластонита, содержащего ГАП, путем консолидации порошка аморфного композитного материала на основе ксонотлита и ГАП, полученного золь-гель (темплатным) методом. Преимущества предлагаемого способа заключаются в достижении гомогенного распределения ГАП в объеме гидратированного композита в момент его золь-гель синтеза, возможности равномерного введения порообразующего коллоидного темплата в его объем и формировании пористой и конструкционно-прочной CaSiO3/ГАП керамики кристаллического типа за счет высокой скорости консолидации аморфного сырья в условиях искрового плазменного разогрева.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы. Метасиликат натрия (Na2SiO3 · 5H2O “х. ч.”), кальций хлористый (CaCl2 · 2H2O “х. ч.”), гидрофосфат аммония ((NH4)2HPO4 “х. ч.”) использовали как прекурсоры для синтеза силиката кальция. Промышленный силоксан-акрилатный латекс КЭ 13-36 (содержание твердой фазы 50%, средний размер частиц 160 нм) производства ООО “Астрохим” (Электросталь), синтезированный подобно описанному в [26], был применен в качестве порообразующего темплата.
Методика синтеза. Получение композитной CaSiO3(волластонит)/ГАП керамики проводили в две последовательные стадии: золь-гель (темплатный) синтез аморфного композитного материала на основе гидратированного силиката кальция (ксонотлит Ca6Si6O17 · 2OH) в смеси с ГАП и латексным темплатом с последующей консолидацией данного композита по технологии ИПС.
Золь-гель (темплатный) синтез порошка аморфного композита Ca6Si6O17 · 2OH(ксонотлит)/ГАП. К 150 мл водного раствора силоксан-акрилатного латекса (латекс : вода = 1 : 30) при интенсивном перемешивании приливали 50 мл 1.0 M раствора хлорида кальция и 50 мл 1.0 M раствора метасиликата натрия несколькими порциями. Далее раствор перемешивали в течение 3 ч при 100°С до образования густого геля, который после кипячения охлаждали до комнатной температуры (25°С). После этого к полученному гелю приливали 16.6 мл 1.0 M раствора хлорида кальция и 10 мл 1.0 M гидрофосфата аммония, перемешивали на магнитной мешалке в течение 1 ч при комнатной температуре (25°С). Полученный гель отфильтровывали, промывали дистиллированной водой до отрицательной реакции на хлорид-ионы и сушили ∼5 ч при 90°С.
Ниже приведены соответствующие уравнения химических реакций.
Синтез волластонита:
Синтез гидроксиапатита в растворе силиката кальция:
Соотношение CaSiO3 : ГАП (массовое 5 : 1).
Реакционный искровой плазменный синтез керамического CaSiO3(волластонит)/ГАП композита. Формование керамического композита CaSiO3 (волластонит)/ГАП проводили путем консолидации ксерогеля, полученного по методике п.2.2.1, по технологии ИПС по следующей схеме: 3 г порошка композитного материала (фракция 0.1–0.5 мм) помещали в графитовую пресс-форму (диаметр 15.5 мм), подпрессовывали (20.7 МПа), далее заготовку помещали в вакуумную камеру (давление 6 Па), затем спекали. Для предотвращения припекания консолидируемого порошка к пресс-форме и плунжерам, а также для легкого извлечения полученного компаунда использовали графитовую фольгу толщиной 200 мкм. Пресс-форму оборачивали теплоизолирующей тканью для снижения теплопотерь при разогреве. Температуру Р-ИПС процесса контролировали с помощью оптического пирометра, сфокусированного на отверстие, расположенное на середине плоскости внешней стенки пресс-формы при заглублении 5.5 мм. Температуру консолидации образцов варьировали (500, 600, 700, 800 и 900°С) со скоростью разогрева 170 град/мин. Спекаемые образцы выдерживали при максимальной температуре 5 мин, а затем охлаждали до комнатной температуры (25°С). Давление прессования на образец при спекании (24.5 МПа) было постоянным в течение всего процесса. Периодичность генерируемого низковольтового импульса в режиме On/Off составляла 12/2, длительность пакета импульсов 39.6 мс, пауза между пакетом импульсов 3.3 мс. Максимальная сила тока при спекании составляла 500 А, напряжение – 2 В. Выбор режима спекания для экспериментов был основан на оптимальных режимах спекания ксонотлита, установленных нами в предыдущих работах [21, 22]. С целью удаления темплата полученную керамику прокаливали в атмосфере воздуха при 800°С в течение 1 ч со скоростью нагрева 5 град/мин в муфельной печи Nabertherm GmbH (Германия).
Микробиологические исследования основывались на оценке формирования биопленок Pseudomonas aeruginosa на полученных образцах керамического волластонита. Образцы размещали на поверхности твердой питательной среды (МПА), предварительно засеянной бактериальной культурой. Культивирование проводили при 37°С в течение 24 ч. Фиксацию биопленки на образце осуществляли путем промывки в 4%-ном формальдегиде с 1%-ным раствором фосфатного буфера и последующим воздействием 1%-ным раствором тетраоксида осмия в течение 1 ч. Обезвоживание проводили с помощью последовательной обработки в этаноле различной концентрации и при соответствующей экспозиции (30, 50, 70, 96% – по 10 мин; 100% – 20 мин), а затем в ацетоне 20 мин. Морфологию сформированных биопленок изучали с помощью растровой электронной микроскопии (РЭМ).
Методы исследования. Идентификацию кристаллических фаз в исходных порошках и полученных образцах проводили с помощью рентгенофазового анализа (CuKα-излучение, Ni-фильтр, средняя длина волны λ = 1.5418 Å, диапазон углов съемки 10°–80°, шаг сканирования 0.02°, скорость регистрации спектров 5 град/мин) на многоцелевом рентгеновском дифрактометре D8 Advance Bruker AXS (Германия). База данных РФА Powder Diffraction FileTM (Soorya N Kabekkodu, 2007). Номер карточки волластонита: 01-084-0654 (C) Wollastonite 1A – CaSiO3; гидроксиаппатита: 01-074-0566 (C) Hydroxyiapatite – Ca10(PO4)6(OH)2. Дифференциальный термический анализ (ДТА) проводили на дериватографе Q-1500 системы F. Paulik, J. Paulik, L. Erdey (Венгрия) на воздухе в платиновом тигле при скорости нагрева 10 град/мин до предельной температуры 1000°С. Удельную поверхность определяли на анализаторе низкотемпературной адсорбции азота при 77 K на приборе Autosorb IQ фирмы Quantochrome (США), для расчета результатов применяли модель БЭТ. Распределение пор по размерам определяли на ртутном поромере AutoPore IV Micromeritics GmbH (США). Механическую прочность образцов цилиндрической формы (диаметром 15.3 мм и высотой 3–6 мм) определяли путем раздавливания со скоростью 0.5 мм/мин на разрывной машине Autograph AG-X plus 100 kN Shimadzu (Япония). Изображения структуры исследуемых материалов были получены методом РЭМ на приборе Carl Zeiss Ultra 55 (Германия) c катодом на полевой эмиссии при ускоряющих напряжениях 1–5 кВ и токе пучка I ≈ 100 pA.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
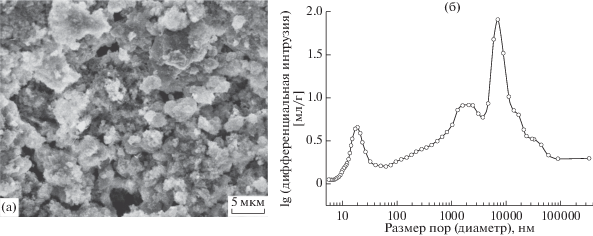
Выбор золь-гель (темплатного) синтеза для получения исходной спекаемой композитной смеси Ca6Si6O17 · 2OH(ксонотлит)/ГАП обосновывается возможностью получения ГАП, гомогенно распределенного во всем объеме гидратированного силиката кальция, а также достижением равномерного введения порообразующего коллоидного темплата. Это связано с преимуществами методов синтеза веществ из растворов (“мокрого”) по сравнению с твердофазным (механическим) перемешиванием компонентов в сухой смеси. Согласно РЭМ-изображению (рис. 1а), синтезированный порошок аморфного композита характеризуется рыхлой пористой структурой. Распределение пор по размерам представлено на дифференциальной интрузионной кривой (рис. 1б).
Рис. 1.
РЭМ-изображение (а) поверхности и дифференциальная зависимость интрузии ртути в образец аморфного композитного материала Ca6Si6O17 · 2OH(ксонотлит)/ГАП в смеси с латексным темплатом.
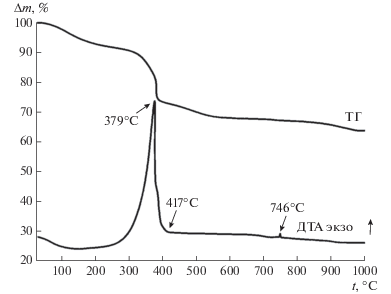
Последующее спекание данного аморфного композита требует его термической обработки, в ходе которой он претерпевает значительные изменения. В частности, по результатам термогравиметрического анализа (рис. 2) установлено, что нагрев композита на воздухе сопровождается несколькими стадиями потери массы. Убыль массы образца (∼10%) при температурах ниже 200°С обусловлена удалением остаточной влаги из гидратированного композита. Далее в температурном интервале 300–400°С происходит окислительная деструкция (выгорание) порообразующего темплата с потерей 13 вес. % и экзоэффектом с максимумом 379°С. В нашем предыдущем исследовании было показано, что последующая потеря массы связана с дегидратацией аморфного ксонотлита. Его кристаллизация с образованием кристаллического волластонита происходит выше 746°С и сопровождается экзоэффектом [22]. В исследуемой композитной системе в присутствии ГАП этот эффект также наблюдается на кривой ДТА (рис. 2). Дальнейшее повышение температуры окислительного прокаливания выше 800°С сопровождается дигидратацией ГАП с его полным разложением выше 1000°С до Ca3(PO4)2 [27].
Рис. 2.
Термогравиметрический анализ образца аморфного композитного материала Ca6Si6O17 · 2OH(ксонотлит)/ГАП в смеси с латексным темплатом.
Дифрактограмма исходного порошка композитного материала системы Ca6Si6O17 · 2OH(ксонотлит)/ГАП подтверждает аморфную природу ксонотлита, наблюдается только несколько рефлексов слабой интенсивности фазы ГАП (рис. 3).
Рис. 3.
Дифрактограммы образцов композитных материалов исходного порошка и керамики на его основе, полученной при различных температурах ИПС.
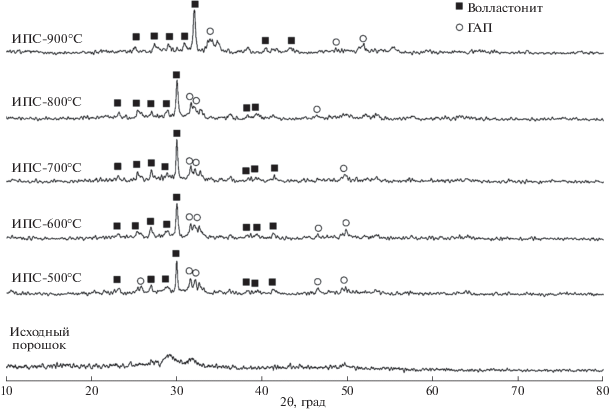
Консолидация аморфного композита по технологии Р-ИПС обеспечивает формирование компактных образцов керамики. Фазовый состав образцов представлен кристаллической модификацией волластонита в смеси с ГАП, который остается неизменным при температуре спекания до 900°С в условиях ИПС, а также после дополнительной термообработки на воздухе при 800°С (рис. 3).
Описанные эффекты термического воздействия, сопровождаемые удалением несвязанной воды, разложением порообразующего темплата и изменением аморфной модификации силиката кальция (ксонотлита) c образованием кристаллического волластонита, также отражаются на динамике спекания и физико-химических характеристиках образцов. В частности, величина уплотнения спекаемого композита значительно изменяется при повышении температуры процесса. По зависимостям на рис. 4 видно, что при разогреве до 700°С (Р-ИПС) значение удельной площади поверхности формируемой керамики увеличивается с 17.91 до 21.09 м2/г. Это связано с частичной деструкцией, деформацией, перегруппировкой при упаковке частиц под воздействием давления прессования (последствия механического воздействия). Увеличение температуры спекания керамического композита свыше 700°С приводит к существенному уплотнению образцов и увеличению их прочности (σсж). Повышение температуры до 900°С приводит к снижению Sуд до 8.56 м2/г, что вызвано прямым спеканием частиц порошка, которое сопровождается пластическим течением и деформацией материала, а также удалением из него свободного пористого пространства (последствия термического воздействия). Механическая прочность спекаемой керамики повышается прямо пропорционально температуре спекания и достигает величины 393.3 МПа при максимально выбранной температуре разогрева 900°С (рис. 4). Плотность образцов линейно возрастает по мере увеличения температуры спекания (рис. 5).
Рис. 4.
Зависимости величин уплотнения, удельной площади поверхности и прочности при сжатии образцов CaSiO3/ГАП керамики, полученных Р-ИПС, от температуры спекания (давление прессования 24.5 МПа).
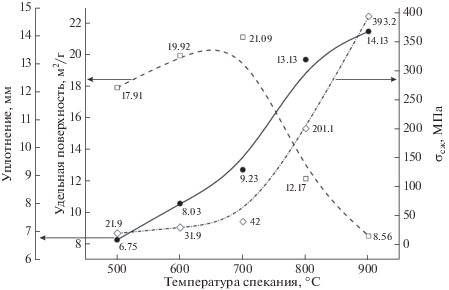
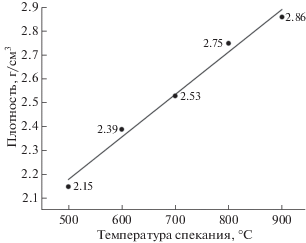
Рис. 5.
Зависимость плотности образцов CaSiO3/ГАП керамики, полученных Р-ИПС, от температуры спекания (давление прессования 24.5 МПа).
На изображениях РЭМ (рис. 6) видно, что в интервале температур 500–700°С микроструктура поверхности образцов керамик пористая и идентичная друг другу. В керамике наблюдается наличие мелких пор, которые образуются вследствие выгорания латексного темплата. При этом ИПС-консолидация при 800°С и выше приводит к значительному снижению открытой пористости из-за активного спекания материала, что согласуется с характеристиками, представленными на рис. 4, 5.
Рис. 6.
РЭМ-изображения образцов композитной керамики на основе CaSiO3/ГАП, полученных Р-ИПС при различных температурах спекания (давление прессования 24.5 МПа).

Проведено микробиологическое исследование по оценке формирования бактериальной биопленки на поверхности образцов керамики композитного CaSiO3/ГАП состава и некомпозитного состава волластонит без добавки ГАП. Для этого использовали синегнойную палочку Pseudomonas aeruginosa, которая активно формирует биопленки, распространена во внешней среде и в то же время является одним из возбудителей инфекционного процесса после хирургических вмешательств. По результатам РЭМ обнаружена заметная разница в формировании биопленки на исследуемых образцах (рис. 7).
Рис. 7.
РЭМ-изображения бактериальной пленки на образцах керамического волластонита: а, а* – в отсутствие ГАП; б, б* – в составе с ГАП.

На керамике без добавки ГАП (рис. 7а, 7а*) преимущественно наблюдаются отдельно расположенные бактериальные клетки. Присутствуют отдельные и редко сосредоточенные по поверхности образцов небольшие плотные участки сформированной биопленки. Бактерии (как отдельные, так и в составе биопленки) покрыты плотным слоем внеклеточного полимерного матрикса, защищающего их от воздействия негативных факторов окружающей среды. Адгезивные пили не сформированы. Это свидетельствует об угнетении жизнедеятельности, размножении бактерий и замедлении формирования биопленки.
На керамике композитного состава CaSiO3/ГАП (рис. 7б, 7б*) слой бактериальной биопленки более выражен. Он толстый и объемный, содержит большое количество матрикса, хорошо видны адгезивные пили. Слой достаточно рыхлый за счет структуры матрикса и отпочковывающихся планктонных форм бактерий, что является признаком зрелости биопленки и активности ее распространения. Это является косвенным подтверждением повышенной биосовместимости данного образца по сравнению с керамикой, не содержащей ГАП. Однако следует учитывать, что при такой бактериальной предрасположенности возрастает риск развития инфекционного процесса при применении данного вида материалов в импланталогии, что требует дополнительной процедуры противобактериальной обработки или повышении антибактериальных свойств изделий на их основе.
ЗАКЛЮЧЕНИЕ
В работе применен оригинальный способ реакционного искрового плазменного синтеза биокерамического волластонита в составе с 20 мас. % гидроксиапатита в качестве биосовместимого компонента. Исходное сырье было получено золь-гель (темплатным) синтезом, который обеспечил формирование аморфного композита в виде гидратированного силиката кальция (ксонотлита) с равномерным распределением ГАП и порообразующего латексного темплата. По данным РФА и ТГА, формирование кристаллической CaSiO3/ГАП керамики может быть инициировано искровым плазменным разогревом аморфного ксонотлита, содержащего ГАП и порообразователь, при температурах процесса 500–900°С. С помощью РФА, РЭМ, БЭТ установлено, что оптимальная температура Р-ИПС для получения исследуемой биокерамики составляет 800–900°С, при этой температуре фаза ГАП устойчива и сохраняется структурная пористость керамического каркаса (Sуд = 12.17–8.56 м2/г). Определено, что биокерамика характеризуется высокой конструкционной прочностью (σсж = 201.1–393.2 МПа) и плотностью (ρуд = 2.75–2.86 г/см3). По результатам микробиологических исследований, наличие ГАП в составе керамики повышает эффективность формирования бактериальных пленок Pseudomonas aeruginosa на поверхности образца, что косвенно указывает на выраженную биосовместимость CaSiO3/ГАП композита. Предлагаемый способ Р-ИПС перспективен для синтеза материала биокерамического класса со структурой и прочностью, подобными костной ткани, который можно применять в качестве имплантатов при восстановлении дефектов натуральной кости.
Список литературы
Stevens M.M. // Mater. Today. 2008. V. 11. № 5. P. 18. https://doi.org/10.1016/S1369-7021(08)70086-5
Dubok V.A. // Powder Metall. Met. Ceram. 2001. V. 39. № 7–8. P. 381. https://doi.org/10.1023/A:1026617607548
Sainitya R., Sriram M., Kalyanaraman V. et al. // Int. J. Biol. Macromol. 2015. V. 80. P. 481. https://doi.org/10.1016/j.ijbiomac.2015.07.016
Bheemaneni G., Saravana S., Kandaswamy R. // Mater. Today. 2018. V. 5. № 1. P. 1807. https://doi.org/10.1016/j.matpr.2017.11.279
Maxim L.D., Niebo R., Utell M.J. et al. // Inhal. Toxicol. 2014. V. 26. № 2. P. 95. https://doi.org/10.3109/08958378.2013.857372
Lin K., Lin C., Zeng Y. // RSC Adv. 2016. V. 6. № 17. P. 13 867. https://doi.org/10.1039/c5ra26916d
Hu Y., Xiao Z., Wang H. et al. // Ceram. Int. 2018. V. 45. № 3. P. 3710. https://doi.org/10.1016/j.ceramint.2018.11.034
Adams L.A., Essien E.R., Kaufmann E.E. // J. Asian Ceram. Soc. 2018. V. 6. № 2. P. 132. https://doi.org/10.1080/21870764.2018.1480685
Tian L., Wang L., Wang K. et al. // Sci. Rep. 2019. V. 9. № 1. P. 2. https://doi.org/10.1038/s41598-019-43918-9
Ni S., Chang J. // J. Biomater. Appl. 2009. V. 24. № 2. P. 139. https://doi.org/10.1177/0885328208094745
Biswas N., Samanta A., Podder S. et al. // J. Mech. Behav. Biomed. Mater. 2018. V. 86. P. 264. https://doi.org/10.1016/j.jmbbm.2018.06.046
Ingole V.H., Sathe B., Ghule A.V. // Fundam. Biomater.: Ceram. 2018. P. 273. https://doi.org/10.1016/B978-0-08-102203-0.00012-3
Golovanova O.A. // Russ. J. Inorg. Chem. 2018. V. 63. № 12. P. 1541. [Голованова О.А. // Журн. неорган. химии. 2018. Т. 63. № 12. С. 1530.] https://doi.org/10.1134/S0036023618120094
Fadeeva T.V., Golovanova O.A. // Russ. J. Inorg. Chem. 2019. V. 64. № 7. P. 847. [Фадеева Т.В., Голованова О.А. // Журн. неорган. химии. 2019. Т. 64. № 7. С. 847.] https://doi.org/10.1134/s0036023619070064
Ergun C. // Ceram. Int. 2011. V. 37. № 3. P. 935. https://doi.org/10.1016/j.ceramint.2010.11.001
Viswanathan V., Laha T., Balani K. et al. // Mater. Sci. Eng. R. 2006. V. 54. № 5–6. P. 121. https://doi.org/10.1016/j.mser.2006.11.002
Orru`R., Licheri R., Locci A.M. et al. // Mater. Sci. Eng. R. 2009. V. 63. № 4–6. P. 127. https://doi.org/10.1016/j.mser.2008.09.003
Simonenko T.L., Kalinina M.V., Simonenko N.P. et al. // Int. J. Hydrogen Energy. 2019. V. 44. № 36. P. 20 345. https://doi.org/10.1016/j.ijhydene.2019.05.231
Simonenko T.L., Kalinina M.V., Simonenko N.P. et al. // Ceram. Int. 2018. V. 44. № 16. P. 19 879. https://doi.org/10.1016/j.ceramint.2018.07.249
Papynov E.K., Mayorov V.Y., Portnyagin A.S. et al. // Ceram. Int. 2015. V. 41. № 1. P. 1171. https://doi.org/10.1016/j.ceramint.2014.09.045
Papynov E.K., Shichalin O.O., Modin E.B. et al. // RSC Adv. 2016. V. 6. P. 34 066. https://doi.org/10.1039/C6RA04956G
Papynov E.K., Shichalin O.O., Mayorov V.Y. et al. // Ceram. Int. 2017. V. 43. № 11. P. 8509. https://doi.org/10.1016/j.ceramint.2017.03.207
Simonenko E.P., Simonenko N.P., Papynov E.K. et al. // J. Sol-Gel Sci. Technol. 2017. V. 82. № 3. P. 748. https://doi.org/10.1007/s10971-017-4367-2
Dudina D.V., Mukherjee A.K. // J. Nanomater. 2013. V. 2013. № 11. P. 1. [Дудина Д.В., Мукерджи А.К. // Наноматер. 2013. Т. 2013. № 11. С. 1.]https://doi.org/10.1155/2013/625218
Kosyanov D.Y., Yavetskiy R.P., Vorona I.O. et al. // AIP Conf. Proc. 2017. V. 1874. P. 040 020. https://doi.org/10.1063/1.4998093
Wang H.H., Li X.R., Fei G.Q. et al. // Express Polym. Lett. 2010. V. 4. № 11. P. 670. https://doi.org/10.3144/expresspolymlett.2010.82
Крутько В.К., Кулак А.И., Мусская О.Н. // Неорган. материалы. 2017. Т. 53. № 4. С. 427. [Krutko V.K., Kulak A.I., Muskaya O.N. // Inorg. Mater. 2017. V. 53. № 4. P. 427. https://doi.org/10.1134/S0020168517040094]
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


