Журнал неорганической химии, 2020, T. 65, № 12, стр. 1697-1704
Экспериментальное моделирование извлечения технеция(VII) из рафинатов после экстракционной переработки ОЯТ
А. М. Сафиулина a, *, А. В. Ананьев a, b, А. В. Лизунов a, М. Туиза b, М. В. Логунов a, К. Н. Двоеглазов a
a АО “Высокотехнологический научно-исследовательский институт неорганических материалов им. А.А. Бочвара”
123060 Москва, ул. Рогова, 5, Россия
b Национальный исследовательский ядерный университет “МИФИ”
115409 Москва, Каширское ш., 31, Россия
* E-mail: amsafiulina@bochvar.ru
Поступила в редакцию 09.07.2020
После доработки 24.07.2020
Принята к публикации 27.07.2020
Аннотация
Дано экспериментальное обоснование возможности экстракционного выделения технеция из рафината технологической схемы аффинажа уран-плутониевого продукта, образующегося при гидрометаллургической переработке отработанного ядерного топлива (ОЯТ). Технеций(VII) из водного раствора Zr(IV) (10 г/л) и 4 моль/л HNO3 с незначительным содержанием оксокатионов ZrOb+ и ${\text{Z}}{{{\text{r}}}_{{\text{2}}}}{\text{O}}_{{\text{3}}}^{{b + }}$ извлекается на 80% в 30% ТБФ в углеводородном разбавителе за семь ступеней противоточного непрерывного каскада при соотношении О : В = 1 : 1. При варьировании отношения потоков фаз для части каскада Тс(VII) экстрагируется в органическую фазу практически полностью за десять ступеней. Технеций(VII) реэкстрагируется селективно из нагруженной органической фазы водой практически полностью за одиннадцать ступеней непрерывного противоточного каскада. Предложена технологическая экстракционная схема выделения технеция(VII) из растворов ОЯТ.
ВВЕДЕНИЕ
Замыкание ядерного топливного цикла является одной из стратегических целей государственной корпорации РФ “Росатом”. Эта проблема решается, в частности, в рамках комплексного проекта “Прорыв”, концепция которого предусматривает создание на одной производственной площадке реактора на быстрых нейтронах со свинцовым теплоносителем, работающего на смешанном нитридном уран-плутониевом (СНУП) топливе и модулей переработки отработанного СНУП-топлива и рефабрикации топлива из регенерированных ядерных материалов. Использование реакторов на быстрых нейтронах (РБН) в “тандеме” с реакторами на тепловых нейтронах типа ВВЭР позволит решить основные проблемы ядерной энергетики, включая прекращение накопления плутония и сокращение объемов радиоактивных отходов (РАО), направляемых на глубинное захоронение, за счет дожигания актинидов в реакторах на быстрых нейтронах. Концепция топливного цикла с РБН подразумевает, что технология переработки СНУП отработанного ядерного топлива (ОЯТ) должна обеспечить переработку топлива с выгоранием 6% и более тяжелых атомов с выдержкой после облучения не более 1 года [1]. Для решения этой задачи в рамках проекта “Прорыв” разрабатывается комбинированная “пиро-гидротехнология” переработки “горячего” СНУП ОЯТ [1–7], позволяющая на стадии пиропередела удалить основную часть тепловыделяющих продуктов деления и выделить делящиеся материалы и МА, окончательная очистка которых производится методами гидрометаллургии. Сочетание этих двух методов позволит получить целевой продукт (смесь оксидов актинидов с коэффициентом очистки от продуктов деления (ПД) ~106), пригодный для воспроизводства новой партии топлива. В то же время дизайн строящегося модуля переработки СНУП ОЯТ предполагает возможность использования только гидрометаллургического метода, но с увеличенной до 2 лет выдержкой топлива перед переработкой.
Особенностью ОЯТ энергетических установок с повышенной степенью выгорания является присутствие в ПД значимых количеств технеция-99. В связи с тем, что период полураспада Тс-99 составляет 212 тысяч лет, выведение его в РАО совместно с относительно короткоживущими (Т1/2 = 30–50 лет), обращение с которыми предполагает приповерхностное хранение, представляется неприемлемым. Поэтому выведение технеция в отдельный поток на гидрометаллургическом переделе является важной технологической задачей.
В соответствии с разработанной схемой гидрометаллургической переработки СНУП ОЯТ с использованием в качестве экстрагента растворов трибутилфосфата (ТБФ) значительная часть технеция остается в рафинате головного блока. Меньшая часть технеция попадает в совместный реэкстракт урана, плутония и нептуния и отделяется от них на стадии аффинажа смеси указанных актинидов. Целесообразно перед передачей растворов, содержащих технеций, на дальнейшую переработку РАО объединять и выделять из них технеций.
К настоящему времени как в России, так и за рубежом разработано множество экстракционных технологических приемов с использованием ТБФ в разбавителях для селективного выделения технеция при переработке оксидного ОЯТ [8–16]. В основе всех известных вариантов лежит способность Tc к комплексообразованию с ТБФ с последующей его экстракцией [17–19], а также к соэкстракции в анионной форме с U(VI) и четырехвалентными элементами, особенно с цирконием [20–23].
Настоящая работа посвящена экспериментальному обоснованию возможности экстракционного выделения технеция из потоков технологической схемы переработки СНУП ОЯТ по гидрометаллургическому варианту.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для проведения экспериментов по экстракции технеция использовали модельный раствор, имитирующий состав объединенного рафината первого цикла экстракционного отделения U–Pu–Np от ПД и рафината операции аффинажа указанной смеси [3]. Для приготовления модельного раствора использовали имитаторы продуктов деления и коррозии в форме нитратов Cs, Sr, Ca, Ba, Ag, Pb, Fe, Pd, La, Ce, Nd, Pr, Gd, Sm. Молибден вводили в виде полимолибдата аммония (NH4)6Mo7O24 · 4H2O. Нитрат циркония Zr(NO3)4 готовили кипячением в течение 72 ч ZrO(NO3)2 · 2H2O в концентрированной азотной кислоте с обратным холодильником с последующим отделением нерастворившегося осадка. В модельный раствор технеций(VII) вводили путем растворения пертехнетата аммония NH4TcO4 (АО “ВО Изотоп”). Растворы готовили объемно-весовым методом.
В качестве экстрагента использовали 30 об. % раствор ТБФ в углеводородном разбавителе марки “Изопар-М”. Экстрагент предварительно очищали от примесей промывкой 5 мас. % раствором карбоната натрия в воде с последующей промывкой водой. Операцию проводили дважды.
Эксперименты по экстракции технеция проводили в статических условиях при соотношении объемов органической и водной фаз 1 : 1 и температуре 20 ± 1°С. Перемешивание фаз осуществляли в течение 3 мин в ротационном смесителе (80 об/мин). Этого времени было достаточно для установления равновесия в системе, что подтверждено контрольным опытом с 20-минутным контактированием фаз. Фазы разделяли центрифугированием. После разделения фаз отбирали пробы на анализ.
Анализ элементного состава растворов проводили методом бесстандартной рентгенофлюоресцентной спектрометрии с дисперсией по длинам волн. Измерения выполняли с использованием спектрометра для РФА ARL Advant’X (Thermo scientific). Для расчета элементного состава пробы использовали программный комплекс UniQuant.
Контроль за распределением технеция(VII) при экстракции в обеих фазах осуществляли методом жидкостной сцинтилляционной спектрометрии (ЖСС) на приборе СКС-50М-Б11. Во всех исследованиях использовали сцинтилляционный коктейль Ultima Gold-AB (Perkin Elmer Inc). Для лучшего эмульгирования пробы Tc(VII) в органической фазе вносили эмульгатор Triton X-100 (Sigma-Aldrich), смесь тщательно перемешивали, получая счетный образец, подготовленный для ЖСС, который измеряли со статистической погрешностью 5%.
Концентрацию азотной кислоты определяли только в водной фазе потенциометрическим титрованием 0.096 моль/л раствором NaOH с использованием автоматического титратора T50 Mettler Toledo.
Для каждой концентрации проводили не менее трех независимых опытов. Погрешность полученных результатов составляла ~20%, учитывая не исключенную и случайную составляющие.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Механизм совместной экстракции пертехнетат-аниона с катионами четырехвалентного циркония исследован и описан в работе [24]:
(1)
$\begin{gathered} {\text{Z}}{{{\text{r}}}^{{{\text{4}} + }}} + {\text{3NO}}_{{\text{3}}}^{--} + {\text{TcO}}_{{\text{4}}}^{--} + {\text{2TБФ}} = \\ = {\text{Zr}}{{\left( {{\text{N}}{{{\text{O}}}_{{\text{3}}}}} \right)}_{{\text{3}}}}\left( {{\text{Tc}}{{{\text{O}}}_{{\text{4}}}}} \right){{({\text{TБФ}})}_{{\text{2}}}}. \\ \end{gathered} $Перед началом экспериментальной работы представлялось целесообразным провести теоретический расчет требуемого количества ступеней экстракции противоточного каскада. Для этого требовались данные по изотерме экстракции технеция в системе Tc(VII)–Zr(IV)–4 моль/л HNO3. Попытка использовать данные по совместной экстракции технеция и циркония из азотнокислых растворов, опубликованные в [24], успеха не имела, поскольку солевой фон растворов, на которых были получены изотермы экстракции технеция в данной работе, сильно отличался от условий поставленной задачи. Вследствие этого был выполнен предварительный эксперимент по получению изотерм экстракции технеция(VII) из азотнокислых растворов, содержащих адекватные количества циркония(IV) и посторонних неэкстрагируемых элементов (нитрат лантана). Экстракционное равновесие технеция(VII) и азотной кислоты при контакте модельного раствора ОЯТ с раствором ТБФ изучали методом изменения объемов фаз. Этот метод позволяет оперировать многокомпонентными растворами, не опасаясь, что по какому-либо компоненту не будет достигнуто равновесие. Однако полученная изотерма будет справедлива только в диапазоне рабочих концентраций.
В качестве водной фазы использовали раствор, содержащий 125 мг/л Tc(VII), 9.94 г/л Zr, 7.58 г/л La, 4.02 моль/л HNO3. Эксперимент проводили по следующей схеме (табл. S1 ).
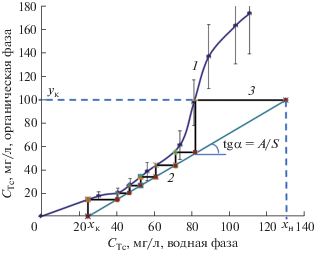
Графический расчет числа теоретических ступеней экстракции проводили методом Тиле–МакКэба, который сводится к построению равновесной и рабочей линии, а затем и ступеней изменения концентрации между этими двумя линиями [26]. На рис. 1 представлена изотерма экстракции технеция(VII) и результат проведенного расчета. Рабочая линия построена по данным состава исходного раствора и отношения потоков органической и водной фаз (О : В = 1 : 1) в экстракционном каскаде.
(2)
$A\left( {{{x}_{{\text{н}}}} - {{x}_{{\text{к}}}}} \right) = S\left( {{{y}_{{\text{к}}}} - {{y}_{{\text{н}}}}} \right),$Рис. 1.
Изотерма экстракции Тс(VII) в 30% ТБФ в углеводородном разбавителе из раствора 125 мг/л Tc(VII) в 4.02 моль/л HNO3 в присутствии 9.94 г/л Zr и 7.58 г/л La при 20°С (1), рабочая линия (2) и ступени экстракции (3).
Преобразуя уравнение рабочей линии (2), получим выражение (3) для концентрации технеция(VII) на выходе из противоточного каскада:
(3)
${{x}_{{\text{к}}}} = {{x}_{{\text{н}}}} - \frac{S}{A}\left( {{{y}_{{\text{к}}}} - {{y}_{{\text{н}}}}} \right).$Согласно уравнению (3) (входящий в противоточный каскад поток с концентрацией технеция(VII) 125 мг/л в водной фазе и выходящий поток с концентрацией 99.8 мг/л в органической фазе, а также отношение потоков 1 : 1), имеем 25.3 мг/л Tc(VII) в выходящем потоке в водной фазе.
В результате приведенного графического расчета было получено семь теоретических степеней. Содержание технеция(VII) на выходе из обычного противоточного каскада с семью ступенями составляет 25 мг/л, что соответствует 80% извлечения от исходного раствора. Дальнейшее увеличение количества ступеней экстракции к росту степени извлечения технеция в рассмотренных условиях не приводит (рис. 1).
В отдельной серии экспериментов было изучено влияние концентрации циркония на распределение технеция и азотной кислоты между водной и органической фазами (рис. 2а и 2б).
Рис. 2.
Влияние концентрации циркония на изотермы технеция (2а) и изотермы азотной кислоты (2б) при экстракции технеция(VII) в 30% ТБФ в углеводородном разбавителе в присутствии 9.94 и 3.64 г/л Zr(IV).
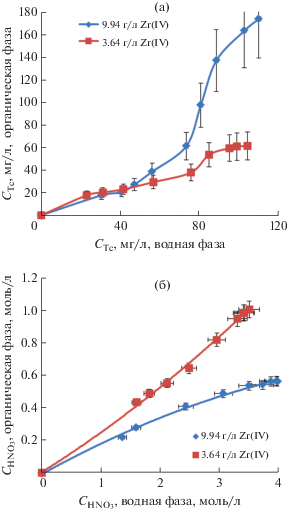
Как видно из рис. 2, уменьшение концентрации циркония(IV) приводит к существенному ухудшению экстракции технеция(VII). В то же время экстракционная способность ТБФ к экстракции азотной кислоты в описанных условиях эксперимента резко возрастает. Этот результат вполне закономерен, так как с уменьшением содержания циркония в экстракционной системе увеличивается концентрация свободного экстрагента, что и приводит к увеличению экстракции азотной кислоты в органическую фазу.
Для подтверждения полученных ранее результатов провели следующую серию экспериментов.
С целью оценки количества ступеней противоточного каскада, при котором достигается стационарное состояние или максимальное приближение к этому состоянию, было проведено моделирование исчерпывающей (первой) ступени противоточного каскада (рис. 1S) или перекрестного тока [27, 28].
Все эксперименты проводили при соотношении объемов фаз О : В = 1 : 1. Начальная концентрация Tc(VII) в модельном растворе составляла 130 мг/л, [HNO3] = 4.02 моль/л.
Как следует из представленной на рис. 1S схемы, порция свежей водной фазы контактирует в ячейке 1 с порцией свежей органической фазы по вышеописанной методике. После разделения фаз в делительной воронке обедненная водная фаза поступает в ячейку 2, где контактирует со свежей порцией органической фазы. После контакта во второй ячейке и разделения фаз обедненная водная фаза поступает в ячейку 3, затем в 4 и т.д. После каждого контакта определяли содержание азотной кислоты и технеция(VII) в водной и органической фазах. Экспериментальные результаты представлены на рис. 3.
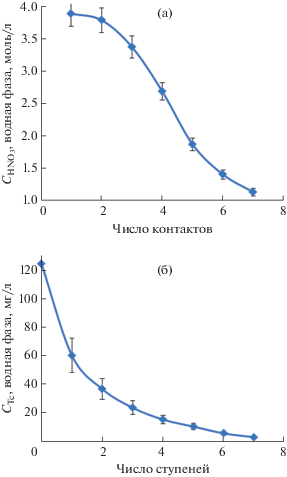
Рис. 3.
Содержание азотной кислоты (3а) и Tc(VII) (3б) в обедненной водной фазе после каждого контакта.
В табл. 2S представлено содержание металлов в модельном растворе после семикратного перекрестного тока (исчерпывания).
Таблица 1.
Содержание технеция(VII) в ступенях противоточного каскада, мг/л
| Фаза | I | II | III | IV | V | VI | VII |
|---|---|---|---|---|---|---|---|
| Водная | 82.3 | 71.5 | 61.2 | 53.5 | 47.9 | 40.5 | 25.1 |
| Органическая | 99.8 | 55.3 | 43.5 | 34.4 | 26.5 | 20.6 | 14.5 |
Таблица 2.
Содержание циркония(IV) и азотной кислоты в ступенях противоточного каскада
| Соединение | I | II | III | IV | V | VI | VII |
|---|---|---|---|---|---|---|---|
| Zr(IV), г/л | 6.27 | 8.45 | 7.35 | 6.0 | 4.23 | 2.98 | 1.96 |
| HNO3, моль/л | 0.82 | 1.67 | 2.41 | 2.78 | 2.95 | 3.02 | 3.07 |
Металлы – имитаторы продуктов деления и коррозии конструкционных материалов (Nd, Ce, Sm, Pr, Gd, La, Ba, Cs, Sr, Ca, Pb, Mo, Fe, Ag, K, Pd), содержащиеся в модельном растворе (табл. 2S), практически не экстрагируются в органическую фазу, за исключением циркония, 70% которого извлекается в ТБФ.
Извлечение технеция(VII) из модельного раствора ОЯТ в 4.02 моль/л HNO3 за семь ступеней в перекрестном токе составило 98%.
После первых двух контактов произошло обеднение водной фазы по Тс(VII) на ~70%, а после следующих пяти контактов – на ~92% (рис. 3б). С последующим увеличением числа контактов переход технеция в органическую фазу становился незначительным. Вследствие этого эксперимент по моделированию противоточного каскада включал семь ступеней.
Поскольку металлы, входящие в состав модельного раствора, за исключением циркония, не экстрагируются в органическую фазу, в серии экспериментов по непрерывной экстракции для поддержания солевого фона использовали только лантан. Состав модельного раствора был следующим: 125 мг/л Tc(VII), 9.94 г/л Zr(IV) и 7.58 г/л La(III) в 4.02 моль/л HNO3.
Моделирование непрерывной экстракции осуществляли с помощью ряда следующих друг за другом операций периодической экстракции. При использовании предложенной схемы (рис. 2S) моделирования принимали, что каждая операция периодической экстракции эквивалентна одной идеальной (теоретической) ступени [27, 28].
В ячейке 1 исходный раствор контактирует со свежей порцией экстрагента, экстракт выбрасывается, а рафинат экстрагируется свежей порцией экстрагента в ячейке 2. После этого экстракт подается в ячейку 1 второй ступени, а рафинат – в ячейку 3 первой ступени и т.д. Экстракты движутся сверху вниз, а рафинаты – слева направо. Соотношение фаз при контактах составляло 1 : 1 и не изменялось на протяжении всего исследования.
Верхний ряд операций рис. 2S представляет собой семь ступеней экстракции в перекрестном токе (исходная смесь семь раз экстрагируется одинаковым количеством экстрагента). Соответственно после указанных операций концентрация металлов в рафинате будет значительно меньше концентрации конечного рафината (после седьмой ступени) при моделировании противоточного каскада (исчерпывающая экстракция). С увеличением числа операций конечная концентрация металлов в рафинате возрастает.
Согласно схеме, представленной на рис. 2S, в табл. 1 и 2 приведены концентрационные профили технеция(VII), циркония(IV) и азотной кислоты в ступенях противоточного каскада.
В результате семи ступеней противоточного каскада технеций(VII) в органическую фазу извлекается более чем на 80% (табл. 1), а цирконий(IV) – на 70% (табл. 2). Лантан(III) в условиях эксперимента в органическую фазу практически не экстрагируется.
Таблица 4.
Параметры рабочей линии для каскада Tc(VII) при реэкстракции
| Параметр | Концентрация, мг/л | |
|---|---|---|
| органическая фаза | водная фаза | |
| Входная в каскад по технецию | 74.9 | 0 |
| Выходная | 2 | 73 |
| О : В = 1 : 1. Коэффициент рабочей линии 1 | ||
В отличие от перекрестного тока, где технеций извлекается в органическую фазу на 98% за семь стадий исчерпывания, противоточный каскад несколько уступает в эффективности. В результате семиступенчатого противоточного каскада в органическую фазу извлекается только 80% технеция. В случае противоточного каскада система стремится к равновесию, а при исчерпывании далека от состояния равновесия, так как на каждой ступени обедненная водная фаза контактирует со свежей (ненагруженной) органической фазой.
Экспериментальные данные вполне согласуются с теоретическими (рис. 1). Концентрация технеция(VII) на выходе из каждой ступени противоточного непрерывного каскада укладывается в рабочую линию (рис. 1), извлечение технеция(VII) в ТБФ (30% в изопаре-М) протекает на 80% за семь ступеней при О : В = 1 : 1. Рабочая линия пересекает ось абсцисс при [Tc(VII)] = 25 мг/л, что соответствует концентрации металла в выходном потоке экстракционного каскада (рис. 1).
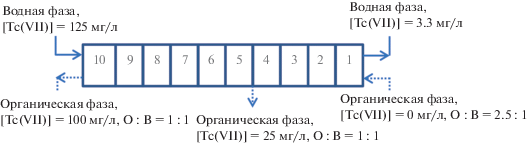
Для более глубокого извлечения технеция из водных растворов одним из вариантов может быть варьирование отношения О : В в части противоточного каскада. Схема эксперимента с изменяемым по каскаду соотношением О : В приведена на рис. 4.
В исчерпывающую часть каскада вводили поток экстрагента в соотношении О : В = 2.5 : 1. После четырех ступеней, обедняющих водную фазу по технецию до 3.3 мг/л, часть органической фазы выводили в соотношении 1.5 : 1 (рис. 4) и далее контактировали с водной фазой в соотношении 1 : 1. На рис. 5 приведена часть изотермы экстракции в области низких концентраций технеция(VII) и рабочие линии, рассчитанные для описанного эксперимента.
Рис. 5.
Изотерма экстракции Тс(VII) в 30% ТБФ в углеводородном разбавителе из раствора 125 мг/л Tc(VII) в 4.02 моль/л HNO3 в присутствии 9.94 г/л Zr и 7.58 г/л La при 20°С (1), расчетная ломаная рабочая линия (2а, 2б) и ступени экстракции (3).
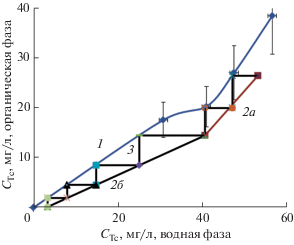
Приведенный процесс характеризует ломаная рабочая линия, состоящая из двух участков, которые можно описать двумя уравнениями. Для участка ступеней 1–4 выражение имеет вид:
где A – поток водной фазы; S – поток органической фазы; F – дополнительный поток органической фазы; xi + 1, xк – концентрация технеция на выходе с четвертой ступени, конечная концентрации технеция в водной фазе, мг/л; yi, yк – концентрация технеция на входе в четвертую ступень, конечная концентрации технеция в органической фазе, мг/л.Для участка ступеней 5–10 уравнение принимает вид:
где xi – концентрация технеция на входе в пятую ступень в водной фазе, мг/л.В табл. 3 приведены параметры ломаной рабочей линии вышеописанного экстракционного непрерывного каскада в 10 ступеней для более глубокого извлечения Тс(VII).
Таким образом, при варьировании отношения потоков водной и органической фаз в экстракционном каскаде можно достичь 97%-ного извлечения технеция(VII) за десять ступеней экстракции.
Потоки органической фазы объединяли и направляли на реэкстракцию технеция.
Исследована возможность реэкстракции технеция из нагруженной технецием и цирконием органической фазы водой при температуре 20°С.
Экстракционное равновесие технеция(VII) и азотной кислоты в системе ТБФ–Tc(VII)–Zr(IV)–HNO3–H2O изучали методом изменения объемов фаз.
В качестве органической фазы использовали 30 об. %-ный раствор ТБФ в изопар-М, содержащий 74.9 мг/л Тс(VII), 4.6 г/л Zr(IV) и 1.6 моль/л HNO3. Реэкстракцию проводили водой. Эксперимент проводили по схеме (табл. 1S), результаты приведены на рис. 6.
Рис. 6.
Распределение Тс(VII) в системе ТБФ–Tc(VII)–Zr(IV)–HNO3–H2O (1), расчетная рабочая линия (2) и ступени (3).
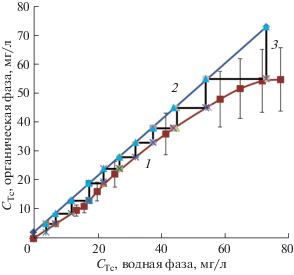
Уравнение рабочей линии при реэкстракции технеция(VII) из нагруженной органической фазы идентично выражению (2). Преобразуя выражение (2), получаем уравнение рабочей линии для реэкстракции технеция(VII) в условиях нашего эксперимента (табл. 4):
(6)
${{y}_{{\text{к}}}} = {{y}_{{\text{н}}}} + \frac{A}{S}({{x}_{{\text{н}}}} - {{x}_{{\text{к}}}}).$В указанных условиях технеций(VII) из нагруженной органической фазы извлекается практически полностью за 11 ступеней.
ЗАКЛЮЧЕНИЕ
При концентрации циркония(IV) ~10 г/л и 4 моль/л HNO3 с незначительным содержанием оксокатионов ZrOb+ и ${\text{Z}}{{{\text{r}}}_{{\text{2}}}}{\text{O}}_{{\text{3}}}^{{b + }}$ в исходном водном растворе извлечение технеция(VII) в ТБФ (30% в углеводородном разбавителе) возможно на 80% за семь ступеней противоточного непрерывного каскада при О : В = 1 : 1.
При варьировании отношения потоков фаз для части каскада достигается более глубокое извлечение технеция (97%) из растворов ОЯТ за десять ступеней.
Возможна реэкстракция Тс из нагруженной органической фазы водой практически полностью за 11 ступеней.
Список литературы
Адамов Е.О., Джалавян А.В., Лопаткин А.В. и др. // Атомная энергия. 2012. Т. 112. № 6. С. 319. [Adamov E.O., Dzhalavyan A.V., Lopatkin A.V. et al. // Atomic Energy. 2012. V. 112. № 6. P. 391. https://doi.org/10.1007/s10512-012-9574-x]
Шадрин А.Ю., Иванов В.Б., Скупов М.В. и др. // Атомная энергия. 2016. Т. 121. № 2. С. 90. [Shadrin A.Yu., Ivanov V.B., Skupov M.V. et al. // Atomic Energy. 2016. V. 121. № 2. P. 119. https://doi.org/10.1007/s10512-016-0171-2]
Шадрин А.Ю., Двоеглазов К.Н., Масленников А.Г. и др. // Радиохимия. 2016. Т. 58. № 3. С. 234. [Shadrin A.Yu., Dvoeglazov K.N., Maslennikov A.G. et al. // Radiochemistry 2016. V. 58. № 3. P. 271. https://doi.org/10.1134/S1066362216030085]
Алексеев П.Н., Гагаринский А.Ю., Кухаркин Н.Е. и др. // Атомная энергия. 2017. Т. 122. № 3. С. 123. [Alekseev P.N., Gagarinskii A.Yu., Kukharkin N.E. et al. // Atomic Energy. 2017. V. 122. № 3. P. 143. https://doi.org/10.1007/s10512-017-0249-5]
Shadrin A.Yu., Dvoeglazov K.N., Kascheev V.A. et al. // Procedia Chemistry. 2016. V. 21. P. 148. https://doi.org/10.1016/j.proche.2016.10.021
Зильберман Б.Я., Пузиков Е.А., Рябков Д.В. и др. // Атомная энергия. 2009. Т. 107. № 5. С. 273. [Zilberman B.Ya., Puzikov E.A., Ryabkov D.V. et al. // Atomic Energy. 2009. V. 107. № 5. P. 333. https://doi.org/10.1007/s10512-010-9233-z]
Решетников Ф.Г. // Атомная энергия. 2001. Т. 91. № 6. С. 453. [Reshetnikov F.G. // Atomic Energy. 2001. V. 91. № 6. P. 998. https://doi.org/10.1023/A:1014811604126]
Голецкий Н.Д., Зильберман Б.Я., Федоров Ю.С. и др. // Радиохимия. 2014. Т. 56. № 5. С. 427. [Goletskii N.D., Zilberman B.Y., Fedorov Y.S. et al. // Radiochemistry. 2014. V. 56. № 5. P. 501. https://doi.org/10.1134/S1066362214050099]
Бугров К.В., Коротаев В.Г., Корченкин К.К. и др. // Химическая технология. 2018. Т. 19. № 10. С. 454.
Кудинов А.С., Голецкий Н.Д., Зильберман Б.Я. и др. // Атомная энергия. 2013. Т. 114. № 5. С. 276. [Kudinov A.S., Goletsky N.D., Zilberman B.Ya. et al. // Atomic Energy. 2013. V. 114. № 5. P. 344. https://doi.org/10.1007/s10512-013-9722-y]
Podrezova L.N., Volk V.I., Dvoeglazov K.N. et al. // Radiation & Applications. 2017. V. 2. № 3. P. 164. https://doi.org/10.21175/RadJ.2017.03.034
Alekseenko V.N., Dvoeglasov K.N., Marchenko V.I. et al. // J. Radioanal. Nucl. Chem. 2015. V. 304. P. 201. https://doi.org/10.1007/s10967-014-3882-7
Durain J., Bourgeois D., Bertrand M. et al. // Solvent Extr. Ion Exch. 2019. V. 37. № 5. P. 328. https://doi.org/10.1080/07366299.2019.1656853
Герман К.Э., Григорьев М.С., Ден Овер К. и др. // Журн. неорган. химии. 2013. Т. 58. № 6. С. 782. [German K.E., Grigoriev M.S., Den Auwer C. et al. // Russ. J. Inorg. Chem. 2013. V. 58. № 6. P. 691. https://doi.org/10.1134/S0036023613060090]
Сергиенко В.С. // Журн. неорган. химии. 2019. Т. 64. № 3. С. 260. [Sergienko V.S. // Russ. J. Inorg. Chem. 2019. V. 64. № 3. P. 317. https://doi.org/10.1134/S0036023619030185]
Сергиенко В.С. // Журн. неорган. химии. 2019. Т. 64. № 5. С. 473. [Sergienko V.S. // Russ. J. Inorg. Chem. 2019. V. 64. № 5. P. 583. https://doi.org/10.1134/S0036023619050164]
Zaitsev A.A., Lebedev I.A., Pirozhkov S.V. et al. // Radiokhimiya. 1964. V. 6. № 4. P. 440.
Lieser K.H., Kruger A., Singh R.N. // Radiochimica Acta. 1981. V. 28. № 2. P. 97. https://doi.org/https://doi.org/10.1524/ract.1981.28.2.97
Pruett D.J. // Radiochim. Acta. 1981. V. 28. № 3. P. 153. https://doi.org/10.1524/ract.1981.28.3.153
Jassim T.N., Liljenzin J.O., Lundqvist R. et al. // Solvent Extr. Ion Exch. 1984. V. 2. № 3. P. 405. https://doi.org/10.1080/07366298408918455
Garraway J., Wilson P.D. // J. Less-Common Met. 1985. V. 106. P. 183. https://doi.org/10.1016/0022-5088[85]90379-0
Pruett D.J., McTaggart D.R. // J. Inorg. Nucl. Chem. 1981. V. 43. № 9. P. 2109. https://doi.org/10.1016/0022-1902[81]80559-3
Kolaric Z., Dressler P. // Solvent Extr. Ion Exch. 1989. V. 7. № 4. P. 625. https://doi.org/10.1080/07360298908962328
Пузиков Е.А., Зильберман Б.Я., Федоров Ю.С. и др. // Радиохимия. 2015. Т. 57. № 3. С. 233. [Puzikov E.A., Zilberman B.Y., Fedorov Y.S. et al. // Radiochemistry. 2015. V. 57. № 3. P. 273. https://doi.org/10.1134/S106636221503008X]
Пузиков Е.А., Зильберман Б.Я., Федоров Ю.С. и др. // Радиохимия. 2013. Т. 55. № 5. С. 402. [Puzikov E.A., Zilberman B.Ya., Fedorov Yu.S. et al. // Radiochemistry. 2013. V. 55. № 5. P. 481. https://doi.org/10.1134/S1066362213050056]
Дытнерский Ю.И. // Основные процессы и аппараты химической технологии. Пособие по проектированию. М.: Химия, 1991. 496 с.
Трейбал Р. // Жидкостная экстракция. М.: Химия, 1966. 724 с.
Альдерс Л. // Жидкостная экстракция. М.: Изд-во иностр. литер., 1962. 258 с.
Дополнительные материалы
- скачать ESM.docx
- Дополнительные материалы
Инструменты
Журнал неорганической химии