Журнал неорганической химии, 2020, T. 65, № 10, стр. 1377-1385
Онлайн-мониторинг адсорбции из сверхкритических растворов на силикагелевых ксеро- и аэрогелях с использованием сверхкритической флюидной хроматографии
М. О. Костенко a, b, К. Б. Устинович a, О. И. Покровский a, *
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
b Московский государственный университет им. М.В. Ломоносова, Химический факультет
119991 Москва, Ленинские горы, 1, Россия
* E-mail: pokrovskiy@terraint.ru
Поступила в редакцию 06.04.2020
После доработки 30.05.2020
Принята к публикации 02.06.2020
Аннотация
Предложен и опробован метод измерения адсорбции низкомолекулярных веществ из растворов в сжиженных газах и сверхкритических флюидах, основанный на онлайн-соединении автоклава высокого давления и сверхкритического флюидного хроматографа. Показана применимость метода для определения сорбционной емкости и построения изотерм адсорбции низкомолекулярных соединений из растворов в сверхкритическом диоксиде углерода на поверхности силикагелевых ксерогелей и аэрогелей. Метод может быть использован для проведения разработок в области использования ксерогелей и аэрогелей как носителей для фармацевтических препаратов адресной доставки и контролируемого релиза.
ВВЕДЕНИЕ
Аэрогели – уникальные сверхлегкие материалы, обладающие высокой удельной площадью поверхности, высокой пористостью, низкой теплопроводностью и рядом других свойств, благодаря которым они нашли применение в самых разнообразных сферах науки и техники – от создания теплоизоляционных покрытий для трубопроводов до изготовления пылеуловителей, используемых в космических аппаратах для сбора звездной пыли [1–3]. Одно из интенсивно развивающихся направлений применения аэрогелей – создание фармацевтических субстанций контролируемого релиза и адресной доставки на базе аэрогелей как носителей [4]. Один из наиболее удобных и часто используемых способов создания таких препаратов – импрегнация заранее сформированных аэрогелей активным фармацевтическим ингредиентом в среде сверхкритического диоксида углерода (СК-СО2). Таким образом снимается необходимость вводить вещество на стадии формирования геля, что может повлиять на процесс формирования структуры, и одновременно обеспечивается сохранность высокой пористости материала на стадии импрегнации из-за отсутствия межфазного натяжения в сверхкритическом растворителе.
Следует отметить, что в целом ряде случаев для создания таких композитных препаратов нет жесткой необходимости формировать именно классические аэрогели, т.е. сверхлегкие материалы с геометрической плотностью <0.1 г/см3. Зачастую возникает необходимость использовать материал с такой же, как у аэрогелей, высокой пористостью и удельной площадью поверхности, но с большей плотностью для обеспечения высокой сорбционной емкости и одновременно компактных размеров. Этого можно добиться через управление параметрами гелирования и сушки гелей [5, 6]. Для таких более плотных материалов применение сверхкритической импрегнации как способа формирования композитных препаратов столь же актуально, как и для аэрогелей, поскольку традиционная пропитка в жидких средах также может привести к уничтожению значительной части их пористой структуры вследствие капиллярных эффектов, а иногда и вовсе к разрушению материала.
Одним из ключевых вопросов при разработке методик формирования лекарственных средств на базе гелей как носителей является адсорбционная емкость геля по выбранному ингредиенту. Измерение адсорбционной емкости при адсорбции из сверхкритических растворов сопряжено с техническими сложностями, поскольку сверхкритические среды существуют только при повышенных давлениях. В случае адсорбции из жидких сред при атмосферном давлении изучение термодинамики и кинетики адсорбции обычно ведется путем отбора пробы маточного раствора над адсорбентом и анализа содержания адсорбтивов в нем любым подходящим методом количественного анализа. При работе со сверхкритическими флюидами и сжиженными газами такой метод обычно не используется, так как отбор пробы, склонной к самопроизвольному расширению и испарению, и ее точный анализ в среде высокого давления весьма проблематичны [7]. При работе с мелкодисперсными сорбентами с узким распределением частиц по размерам и при сравнительно небольших сорбционных нагрузках широко применяются хроматографические методы исследования адсорбции, в которых термодинамические характеристики процессов сорбции-десорбции вычисляются из формы и положения хроматографических пиков, полученных в условиях нелинейной адсорбции [8–13]. В основном используют такие стандартные для жидкостной хроматографии способы, как элюирование по характеристическим точкам, фронтальный анализ, способ времени удерживания и т.д. Недавно для изучения термодинамических характеристик адсорбции на различных силикагелях, в том числе аэрогелях, из двухкомпонентных сверхкритических растворителей был предложен метод инверсионной сверхкритической флюидной хроматографии [14]. Эти методы весьма информативны и позволяют не только вычислить термодинамические характеристики адсорбции, но и установить многие закономерности взаимодействия сорбентов с сорбатами. Однако их реализация требует соблюдения целого ряда весьма специфических условий, как технических, так и физико-химических. Так, далеко не для всех перспективных адсорбентов возможно получение мелкодисперсного порошка, состоящего из сферических частиц с узким распределением по размерам, и его последующая равномерная усадка в хроматографическую колонку, что необходимо для реализации хроматографических способов изучения адсорбции. В частности, эта проблема существенна для аэрогелей, для которых методы формирования устойчивых к сминанию пересыпаемых порошков с размером частиц 1–10 микрон еще не вполне отработаны. Также хроматографические методы всегда осуществляются в рамках какой-либо модели процесса адсорбции, заданной a priori, что позволяет получить достоверный результат только в том случае, если модель угадана верно.
Для исследования сверхкритической адсорбции на сорбентах, полученных методом золь-гель синтеза, чаще всего применяются приемы, основанные на определении содержания фармсубстанции в аэрогеле после исчерпывающей импрегнации. Наиболее простой из них – гравиметрический, основанный на измерении увеличения массы образца аэрогеля в результате его импрегнации в сверхкритической среде. Данный метод пользуется популярностью при проведении пилотных поисковых исследований [15–17], не требующих высокой точности. В более детальных исследованиях применяются методы, основанные на полной десорбции фармсубстанции с аэрогеля подходящим жидким растворителем с последующим анализом элюата спектрофотометрическими [18–20] или хроматографическими методами [21–23]. В случае чисто неорганических силикагелевых аэрогелей и органических фармацевтических субстанций также возможно применение элементного анализа с определением процентного содержания углерода [18, 19]. Известны примеры применения метода баланса магнитного подвеса для исследования адсорбции на неорганических аэрогелях из сверхкритических сред [20].
Методы исследования адсорбции, основанные на оффлайн-анализе образца аэрогеля после импрегнации, достаточно трудоемки и менее производительны по времени, чем хроматографические. На получение одной точки данных в них уходит много времени, так как необходимо, во-первых, гарантированно достичь требуемой степени импрегнации, затем полностью сбросить давление с системы, извлечь образец и провести аналитические измерения. При необходимости получения большого числа данных, например при построении изотерм адсорбции для многих типов гелей или при исследовании кинетики адсорбции в зависимости от параметров состояния сверхкритического растворителя, на проведение такой работы может уйти несколько месяцев. Кроме того, при применении этих методов исследователь сталкивается с необходимостью учитывать возможность депонирования фармацевтической субстанции на поверхности аэрогелей не в результате адсорбции из сверхкритического раствора, а в результате осаждения вещества из раствора в ходе сброса давления. При сбросе давления СО2 переходит из сверхкритического состояния в газообразное и теряет свою растворяющую способность. При этом растворенное в нем вещество резко выпадает в осадок и кристаллизуется на любых доступных поверхностях, в том числе и в порах аэрогеля [17–20]. Такие отложения характеризуются иной кинетикой растворения и иным поведением при хранении, чем адсорбат, и при оценке сорбционной емкости выбранного аэрогеля по заданному веществу необходимо разделять нагрузку, полученную адсорбцией и такой кристаллизацией. Для этого приходится проводить дополнительные опыты с очень плавным сбросом давления после импрегнации в надежде, что при таком сбросе кристаллизация из расширяющегося флюида не будет вносить значимый вклад в увеличение массы импрегнированного аэрогеля [17, 20]. Это существенно обременяет и без того сложную процедуру поиска оптимального типа аэрогеля-носителя и разработку технологии формирования нужного композитного препарата.
В настоящей работе представлены результаты первичной апробации нового метода изучения адсорбции из сверхкритических флюидов и сжиженных газов. Метод основан на онлайн-соединении автоклава высокого давления, в котором происходит адсорбция из сверхкритической среды, со сверхкритическим флюидным хроматографом. В работе дано описание метода и приведены результаты его применения к исследованию адсорбции модельного вещества – кофеина – на силикагелевых ксерогелях и аэрогелях на основе тетраэтоксисилана (ТЭОС) и метилтриметоксисилана (МТМС).
ОПИСАНИЕ МЕТОДА
Суть предложенного метода заключается в следующем. Автоклав высокого давления соединяется с линией подвижной фазы сверхкритического флюидного хроматографа перед колонкой через кран-дозатор. Весь соединительный узел термостатируется. В автоклав загружаются навески сорбента и адсорбируемого вещества, автоклав герметизируется, термостатируется, в него подается СО2, включается перемешивание. Хроматограф выводится на равновесный режим в условиях, заранее отработанных для анализа заданного целевого вещества. После установления требуемых условий в обеих подсистемах и выдержки автоклава в течение определенного времени производится наполнение петли хроматографа раствором из автоклава с помощью крана-дозатора. Объем отбираемой пробы мал по сравнению с объемом автоклава (<0.5 об. %), поэтому отбор оказывает пренебрежимо малое влияние на установившееся равновесие. Далее отобранная проба вводится в хроматографический тракт хроматографа стандартным способом. Концентрация вещества в пробе определяется по площади хроматографического пика с использованием заранее построенных калибровочных кривых. Полученное значение пересчитывается в величины адсорбции с учетом исходных масс вещества и адсорбента.
Данный метод эквивалентен отбору пробы жидкой фазы, используемому при исследовании адсорбции из жидких сред при атмосферном давлении. Хроматограф служит средством анализа содержания вещества в пробе. Онлайн-соединение позволяет избежать всех сложностей, связанных с анализом проб, отбираемых из сжимаемых сред высокого давления. При должном термостатировании отбираемый образец все время находится при одних и тех же параметрах состояния флюида от автоклава до петли хроматографа, что обеспечивает его сохранность. На рис. 1 приведена схема прибора для осуществления данного метода.
Рис. 1.
Схема прибора для исследования адсорбции из сверхкритических сред методом онлайн-соединения автоклава высокого давления и сверхкритического флюидного хроматографа. 1, 7 – насосы СО2; 2 – насос сорастворителя; 3, 10 – краны-дозаторы; 4 – термостатируемая хроматографическая колонка; 5 – детектор хроматографа; 6 – регулятор обратного давления; 8 – сосуд высокого давления; 9 – фильтр; 11 – краны системы ввода пробы; 12 – петля расширения.
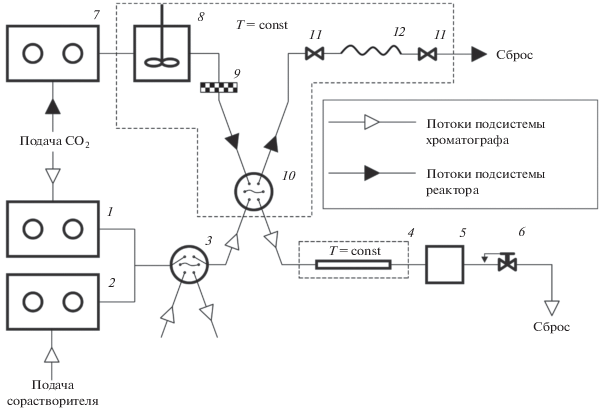
Очевидно, что такой способ анализа применим не только для исследования адсорбции из сверхкритических сред, но и для любых исследований, требующих мониторинга содержания растворенных веществ в сжатых газах и сверхкритических флюидах: измерения растворимости и коэффициентов распределения в многофазных системах с участием сжатых газов, исследования кинетики высвобождения веществ из твердых матриц в сверхкритический растворитель и т.п. В самом общем виде применительно к любым стационарным системам высокого давления и без уточнения вида хроматографии такой метод был теоретически предложен еще в классической монографии Циклиса [24]. Недавно такой подход был реализован для определения растворимости веществ в сверхкритическом СО2 [25–27]. В общем случае для анализа может использоваться любой подходящий для выбранных целевых веществ вид хроматографии, но, на наш взгляд, сверхкритическая флюидная хроматография (СФХ) наиболее удобна, поскольку в ней применяются те же среды, что и в самом автоклавном процессе. Смешение отобранной пробы и хроматографического элюента протекает гладко, без нежелательных неравновесных эффектов, вызванных разницей в давлении, плотности и вязкости между подвижной фазой и пробой, что благотворно сказывается на результатах хроматографического определения.
В целом метод существенно более прост в исполнении, чем чисто хроматографические методы характеризации адсорбции из сверхкритических сред, и обладает большей производительностью, чем методы, основанные на оффлайн-анализе сорбентов после адсорбции. Высокая производительность может быть особенно важна при проведении исследований кинетики адсорбции. Хроматографические методы принципиально неприменимы для такой работы, так как основываются на предположении о моментальном достижении равновесия на каждой теоретической тарелке колонки. Стационарные методы с оффлайн-анализом, во-первых, обладают очень низкой производительностью и, во-вторых, страдают от возможных случайных ошибок при сбросе давления в автоклаве и последующих манипуляциях с образцами. В предлагаемом нами методе процедура извлечения сорбента для анализа отсутствует, и исследование кинетики адсорбции может быть выполнено в рамках одной загрузки. При необходимости аналитическая методика может быть подобрана таким образом, чтобы обеспечивать одновременное количественное определение нескольких веществ. Тем самым возможно исследование конкурирующей адсорбции одновременно нескольких веществ.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы. В работе использовали тетраэтоксисилан, метанол чистоты для ВЭЖХ и водный раствор аммиака “ос. ч.” (Химия XXI, Россия), метил-триметоксилан “ос. ч.” производства Sigma-Aldrich (Химмед, Россия). Дистиллированную воду получали с помощью лабораторного дистиллятора Liston A 1104 (Liston, Россия). Применяли также кофеин “ч. д. а.” (Лаборатория мыла, Россия), пищевой СО2 (99.8%, ГОСТ 8050-85, Линде Газ Рус, Россия), фиксанал HCl и P2O5 “х. ч.” (Мосхимторг, Россия).
Синтез гелей. Для обоих типов прекурсоров – ТЭОС и МТМС – синтез проводили двухстадийным способом по приведенной ниже методике, близкой к методикам, описанным в [5, 6]. На первой стадии проводили кислотный гидролиз прекурсора из расчета получения ∼100 мл геля. Для этого аликвоту прекурсора растворяли в метаноле, после чего добавляли нужное количество водного раствора соляной кислоты заданной концентрации. Полученную гетерогенную смесь при комнатной температуре тщательно перемешивали, используя магнитную мешалку. В случае ТЭОС перемешивание вели в течение 10–15 мин до исчезновения видимой негомогенности. В случае МТМС смешение происходит быстрее. Далее полученный раствор оставляли в закрытой колбе на сутки при комнатной температуре для роста частиц золя. На второй стадии проводили гелирование в щелочных условиях, для чего к ранее полученному раствору прибавляли порцию метанола и аликвоту водного раствора аммиака нужной концентрации. Полученную смесь тщательно перемешивали и быстро переносили в емкости с заданной формой (шприцы на 6 мл). Гелирование с последующим старением проводили в течение 4 сут. Далее сформированные гели помещали в химический стакан на 500 мл с 200 мл чистого метанола на сутки для отмывки от непрореагировавших прекурсоров.
Мольные соотношения реагентов в случае ТЭОС и МТМС несколько различались. Опытным путем было установлено, что для синтеза гелей на основе МТМС необходимо использовать более высокие концентрации аммиака и меньшие концентрации соляной кислоты. В противном случае не удавалось сформировать монолитные гели. Подобранные эмпирическим путем мольные соотношения реагентов, использованные в работе, приведены в табл. 1.
Таблица 1.
Мольные соотношения прекурсоров и реагентов, использованных в синтезе гелей
| Стадия | n(ТЭОС)/n(МТМС) | n(H2O) | n(MeOH) | n(HCl) | n(NH4OH) |
|---|---|---|---|---|---|
| моль | |||||
| ТЭОС | |||||
| 1 | 1 | 3 | 4 | 0.0005 | 0 |
| 2 | 0 | 6 | 36 | 0 | 0.09 |
| Всего | 1 | 9 | 40 | 0.0005 | 0.09 |
| МТМС | |||||
| 1 | 1 | 4 | 10 | 0.001 | 0 |
| 2 | 0 | 4 | 20 | 0 | 0.5 |
| Всего | 1 | 8 | 30 | 0.001 | 0.5 |
Гидратация гелей. Для некоторых гелей на основе ТЭОС проводили дополнительную выдержку в воде в расчете добиться большей доли силанольных групп на единицу поверхности благодаря гидролизу остаточных алкоксильных групп и увеличению за счет этого сорбирующей способности материала. Для этого гель после старения четырехкратно выдерживали в 200 мл дистиллированной воды по 1 ч, каждый раз сливая отработанную воду. В ходе данной процедуры гель терял свою цилиндрическую форму, становился более эластичным и существенно увеличивался в объеме. После гидратации воду сливали, массу геля делили пополам. Одну половину использовали для получения ксерогелей сразу после гидратации, а вторую, предназначенную для сверхкритической сушки, четырехкратно выдерживали в 200 мл метанола в течение 2 ч для обратной замены растворителя на метанол, поскольку прямая сушка сверхкритической экстракцией от воды невозможна.
Сушка гелей. Использовали два способа сушки гелей: высокотемпературную сушку в сушильном шкафу с получением ксерогелей и сверхкритическую сушку с получением аэрогелей.
Получение ксерогелей сушкой в сушильном шкафу. Сушильный шкаф разогревали до 150°С, после чего в него помещали чашку Петри с образцом геля на 24 ч. По окончании процесса образец извлекали из сушильного шкафа, охлаждали в эксикаторе над P2O5 и размалывали в агатовой ступке до получения равномерного порошка.
Для некоторых образцов ксерогелей определяли удельную площадь поверхности методом низкотемпературной адсорбции азота с помощью анализатора текстурных характеристик Катакон АТХ-06 (Новосибирск, Россия).
Получение аэрогелей сверхкритической сушкой. Сверхкритическую сушку проводили с использованием установки для сверхкритической флюидной экстракции SFE-1000 производства Waters Corp. (Милфорд, США). Термостатируемый сосуд высокого давления объемом 100 мл заливали метанолом и аккуратно помещали в жидкость образец алкогеля. Герметизировали сосуд и нагревали его до 75°С, после чего подавали в систему сжиженный СО2. Экстракцию осуществляли в течение 4 ч в проточном режиме с массовой скоростью потока 10 г/мин (согласно показаниям встроенного в систему массового расходомера Кориолиса) при постоянном давлении 15 МПа. По окончании экстракции плавно сбрасывали давление до атмосферного в течение 3–4 ч при помощи автоматического регулятора давления, не прекращая при этом прогрев сосуда, чтобы избежать коллапса пористой структуры геля вследствие формирования жидкой фазы СО2. Полученные таким образом аэрогели досушивали от остатков физически адсорбированной влаги по методике, описанной ранее, после чего гели также измельчали в агатовой ступке.
Измерение адсорбции методом автоклав-СФХ. Опыты по измерению адсорбции кофеина на ксеро- и аэрогелях проводили по описанной выше методике. В качестве автоклава использовали термостатируемый автоклав с магнитной мешалкой R-100 объемом 96 ± 1 мл производства Waters Corp. Нагнетание СО2 в автоклав осуществляли с помощью плунжерного насоса SSI SFC-24, работающего в режиме контроля по давлению. В качестве крана-дозатора использовали 6-портовый кран Valco C6W (Valco corp, США). Для минимизации внутреннего объема узла отбора пробы использовали капилляры внешнего диаметра 1/16'' c ДУ 0.25 мм и игольчатые краны на трубки 1/16'' (HiP, США). Термостатирование всего узла отбора пробы вели с помощью жидкостного термостата M02 (Термэкс, Россия) и самодельной водяной бани объемом 24 л. В качестве аналитического сверхкритического хроматографа использовали прибор Acquity UPC2 производства Waters Corp. Хроматограф был дополнительно модифицирован для обеспечения онлайн-соединения с автоклавом и минимизации мертвого объема. Анализ содержания кофеина в пробе проводили на неподвижной фазе Luna C18 100-5 100 × 4.6 мм (Phenomenex, США). Условия элюирования: подвижная фаза СО2/метанол 99/1, скорость потока подвижной фазы 2 мл/мин (объемная величина потока указывается для жидкой фазы в условиях +2° и 6.5 МПа), температура колоночного термостата +35°С, давление на выходе из колонки 12 МПа. Калибровочную кривую по кофеину строили в интервале концентраций от 0.048 до 2 г/л. Для увеличения набора точек для калибровки стандартные растворы вводили в хроматограф в различных объемах по 3 раза, суммарно для построения кривой было получено 93 точки. Полученную зависимость аппроксимировали линейной функцией с R2 = 0.9997.
Процедура проведения адсорбционных измерений изложена выше в разделе “Описание метода”.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Внешний вид гелей. Внешний вид алкогелей на основе ТЭОС и МТМС представлен на рис. 2.
Гели на основе ТЭОС, в отличие от МТМС, обладают прозрачностью. При последующей сверхкритической сушке гели сохраняют форму и степень прозрачности. Для гелей на основе ТЭОС наблюдается несколько бóльшая линейная и объемная усадка в результате сверхкритической сушки: 16 ± 1 и 41 ± 4% соответственно для гелей на основе ТЭОС по сравнению с 8 ± 1 и 22 ± 3% для гелей на основе МТМС. ТЭОС-аэрогели достаточно хрупкие, легко крошатся в руках. МТМС-аэрогели обладают некоторой упругостью, их можно сгибать, держась за концы полученных цилиндрических образцов, на угол ∼10° без видимых разрушений. Также аэрогели на основе МТМС обладают гидрофобностью. Внешний вид аэрогеля на основе МТМС и демонстрация гидрофобности его поверхности представлены на рис. 3. Такое свойство характерно для гелей на основе МТМС и неоднократно описывалось в литературе.
Рис. 3.
Аэрогели на основе МТМС: а – внешний вид, б – демонстрация гидрофобности (на поверхности геля капля воды объемом 15 мкл).

Ксерогели на основе и ТЭОС, и МТМС представляют собой твердые прозрачные гранулы с линейными размерами 0.5–5 мм. После механического измельчения все образцы представляют собой бесцветный порошок.
Сорбционная емкость гелей. В табл. 2 представлены результаты измерения массы адсорбированного кофеина на силикагелях при загрузке сорбента 30 мг и навеске кофеина 30 мг.
Таблица 2.
Сорбционная способность гелей по кофеину: масса адсорбированного кофеина на единицу массы сорбента*, мг/мг. Масса навески сорбента 30 мг, масса навески кофеина 30 мг
| Тип силикагеля | ТЭОС | МТМС |
|---|---|---|
| Ксерогель | ||
| без гидратации | 0.35 | 0 |
| с гидратацией | 0.20 | – |
| Аэрогель | ||
| без гидратации | 0.21 | 0 |
| с гидратацией | 0.30 | – |
Силикагели на основе МТМС не показали никакой сорбционной способности по отношению к кофеину. Концентрация кофеина в растворе в присутствии этих сорбентов была равна его концентрации в отсутствие сорбента с точностью до погрешности измерения вне зависимости от типа геля, времени выдержки и т.д. Вероятно, этот результат следует считать ожидаемым. Кофеин как третичный алкалоид, предположительно, сорбируется на силикагелях прежде всего по механизму сильной водородной связи, а в гелях на основе МТМС число силанольных групп, доступных для контакта с молекулами кофеина, должно быть мало. МТМС-гели традиционно считаются хорошими сорбентами для липофильных субстанций; в частности, они рассматриваются как одни из перспективных кандидатов на роль материалов для устранения разливов нефти на поверхности воды [28]. Их сорбционная способность по отношению к гидрофильным веществам невелика.
Гели на основе ТЭОС демонстрируют наличие сорбционной способности по кофеину. Их присутствие в системе приводит к заметному понижению концентрации кофеина в растворе. Наиболее существенным для целей настоящей работы выводом, который можно сделать из приведенных величин поглощения кофеина адсорбентами, является то, что предложенный метод исследования сорбционных процессов в сверхкритических средах является достаточно чувствительным для улавливания небольших различий в активности сорбентов. Что касается самих измеренных величин, то обращает на себя внимание факт большей сорбционной способности ксерогеля на основе ТЭОС по сравнению с аналогичным аэрогелем. В приведенных условиях ксерогель адсорбировал ∼0.35 мг кофеина на 1 мг сорбента, а аэрогель – 0.2 мг. Данное наблюдение устойчиво воспроизводилось на качественном уровне в наших опытах. Ксерогели, полученные в настоящей работе, обладают достаточно развитой поверхностью. Так, по данным метода низкотемпературной адсорбции азота, ТЭОС-ксерогель, не подвергшийся гидратации, имеет удельную площадь поверхности порядка 1100 м2/г. Тот факт, что аэрогели, несмотря на гораздо меньшую геометрическую плотность по сравнению с ксерогелями, не продемонстрировали значимых преимуществ в адсорбции выбранного модельного соединения в приведенных условиях, кажется нам любопытным и заслуживающим дальнейшего более детального изучения.
В качестве дополнительной демонстрации результатов применения предложенного метода исследования адсорбции из сверхкритической среды были построены зависимости величин адсорбции кофеина на ТЭОС-ксерогелях двух видов, подвергшихся и не подвергшихся гидратации, от массы исходной загрузки кофеина при постоянной массе сорбента. На рис. 4 приведены соответствующие изотермы адсорбции.
Рис. 4.
Изотермы адсорбции кофеина на ксерогелях на основе ТЭОС из сверхкритического СО2: а – ксерогель, подвергшийся гидратации после гелирования (параметры изотермы: a = 2.1 мкмоль/м2, b = = 4.4 м3/моль, R2 = 0.9984); б – ксерогель, не подвергшийся гидратации (a = 2.0 мкмоль/м2, b = = 3.6 м3/моль, R2 = 0.9995).
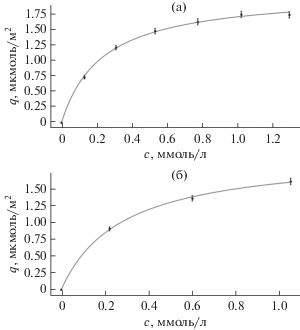
Изотермы имеют схожий вид и хорошо аппроксимируются в рамках простой ленгмюровской модели адсорбции:
где q – избыточная адсорбция по Гиббсу, мкмоль/м2, с – концентрация кофеина в исходном растворе в СК-СО2, ммоль/л, a – емкость адсорбционного монослоя, мкмоль/м2, b – константа адсорбционного равновесия, м3/моль.Примечательно, что значения параметров изотерм адсорбции для обоих ксерогелей близки: емкости монослоя и константы адсорбции составили соответственно 2.1 мкмоль/м2 и 4.4 м3/моль для гидратированного ксерогеля и 2.0 мкмоль/м2 и 3.6 м3/моль для негидратированного. Формально адсорбционная способность по кофеину выше у ксерогеля, который подвергся гидратации. На деле это так только в пересчете на единицу площади поверхности. Удельная площадь поверхности гидратированного геля почти в два раза меньше таковой для негидратированного – 610 против 1100 м2/г. На единицу массы сорбента негидратированный ксерогель на основе ТЭОС показал более высокую сорбционную способность по кофеину, чем все остальные гели.
ЗАКЛЮЧЕНИЕ
Предложенный метод исследования подходит для изучения сорбционных процессов в сверхкритических средах. Он отличается высокой экспрессностью, лишен некоторых ограничений, свойственных статическим оффлайновым методам изучения адсорбции из сверхкритических растворителей, и удобен при исследовании адсорбции на таких непростых для изучения объектах, как аэрогели и ксерогели с развитой поверхностью. Вероятно, метод можно рекомендовать к использованию при проведении исследований, направленных на разработку технологий изготовления лекарств контролируемого релиза на базе аэрогелей.
Список литературы
Pierre A.C., Pajonk G.M. // Chem. Rev. 2002. V. 102. № 11. P. 4243. https://doi.org/10.1021/cr0101306
Smirnova I., Gurikov P. // J. Supercrit. Fluids. 2018. V. 134. P. 228. https://doi.org/10.1016/j.supflu.2017.12.037
Smirnova I., Gurikov P. // Annu. Rev. Chem. Biomol. Eng. 2017. V. 8. № 1. P. 307. https://doi.org/10.1146/annurev-chembioeng-060816-101458
Ulker Z., Erkey C. // J. Controlled Release. 2014. V. 177. P. 51. https://doi.org/10.1016/j.jconrel.2013.12.033
Yorov K.E., Sipyagina N.A., Lermontov S.A. et al. // Russ. J. Inorg. Chem. 2016. V. 61. № 11. P. 1339. https://doi.org/10.1134/S0036023616110048
Lermontov S.A., Baranchikov A.E., Sipyagina N.A. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 2. P. 255. https://doi.org/10.1134/S0036023620020084
Peper S., Dohrn R. // J. Supercrit. Fluids. 2012. V. 66. P. 2. https://doi.org/10.1016/j.supflu.2011.09.021
Brunner G., Johannsen M. // J. Supercrit. Fluids. 2006. V. 38. № 2. P. 181. https://doi.org/10.1016/j.supflu.2006.06.008
Guiochon G., Tarafder A. // J. Chromatogr. A. 2011. V. 1218. № 8. P. 1037. https://doi.org/10.1016/j.chroma.2010.12.047
Vajda P., Guiochon G. // J. Chromatogr. A. 2013. V. 1305. P. 293. https://doi.org/10.1016/j.chroma.2013.06.075
Enmark M., Forssén P., Samuelsson J. et al. // J. Chromatogr. A. 2013. V. 1312. P. 124. https://doi.org/10.1016/j.chroma.2013.09.007
Enmark M., Samuelsson J., Forss E. et al. // J. Chromatogr. A. 2014. V. 1354. P. 129. https://doi.org/10.1016/j.chroma.2014.05.070
Enmark M., Åsberg D., Leek H. et al. // J. Chromatogr. A. 2015. V. 1425. P. 280. https://doi.org/10.1016/j.chroma.2015.11.001
Sun M., Ruiz Barbero S., Johannsen M. et al. // J. Chromatogr. A. 2019. V. 1588. P. 127. https://doi.org/10.1016/j.chroma.2018.12.053
Caputo G., De Marco I., Reverchon E. // J. Supercrit. Fluids. 2010. V. 54. № 2. P. 243. https://doi.org/10.1016/j.supflu.2010.05.003
Caputo G., Scognamiglio M., De Marco I. // Chem. Eng. Res. Des. 2012. V. 90. № 8. P. 1082. https://doi.org/10.1016/j.cherd.2011.11.011
Singh N., Mukhopadhyay M., Vinjamur M. // J. Supercrit. Fluids. 2019. V. 152. P. 104553. https://doi.org/10.1016/j.supflu.2019.104553
Smirnova I., Mamic J., Arlt W. // Langmuir. 2003. V. 19. № 20. P. 8521. https://doi.org/10.1021/la0345587
Gorle B.S.K., Smirnova I., Dragan M. et al. // J. Supercrit. Fluids. 2008. V. 44. № 1. P. 78. https://doi.org/10.1016/j.supflu.2007.08.004
Gorle B.S.K., Smirnova I., Arlt W. // J. Supercrit. Fluids. 2010. V. 52. № 3. P. 249. https://doi.org/10.1016/j.supflu.2010.01.006
Hu X., Zheng S., Zhu L., Tanyi A.R. et al. // J. Supercrit. Fluids. 2013. V. 79. P. 41. https://doi.org/10.1016/j.supflu.2013.02.015
Lovskaya D.D., Lebedev A.E., Menshutina N.V. // J. Supercrit. Fluids. 2015. V. 106. P. 115. https://doi.org/10.1016/j.supflu.2015.07.011
Lovskaya D., Menshutina N. // Materials. 2020. V. 13. № 2. P. 329. https://doi.org/10.3390/ma13020329
Циклис Д.С. Техника физико-химических исследований при высоких и сверхвысоких давлениях. М.: Химия, 1976. 432 с.
Ramsey E.D., Li B., Guo W. et al. // J. Chromatogr. A. 2015. V. 1388. P. 141. https://doi.org/10.1016/j.chroma.2015.02.037
Li B., Guo W., Song W. et al. // J. Supercrit. Fluids. 2016. V. 115. P. 17. https://doi.org/10.1016/j.supflu.2016.04.008
Li B., Guo W., Ramsey E.D. // J. Supercrit. Fluids. 2019. V. 152. P. 104558. https://doi.org/10.1016/j.supflu.2019.104558
Lermontov S.A., Sipyagina N.A., Malkova A.N. et al. // Russ. J. Inorg. Chem. 2014. V. 59. № 12. P. 1392. https://doi.org/10.1134/S0036023614120134
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии



