Журнал неорганической химии, 2019, T. 64, № 8, стр. 862-868
Синтез и строение донорно-акцепторных комплексов ацетата родия(II): Rh2(OAc)4(Diox)2, Rh2(OAc)4(Dmso)2 и Rh2(OAc)4[(4-FC6H4)3Sb]2
В. В. Шарутин 1, *, О. К. Шарутина 1, В. С. Сенчурин 1
1 Национальный исследовательский Южно-Уральский государственный университет
454080 Челябинск, пр-т им. В.И. Ленина, 76, Россия
* E-mail: vvsharutin@rambler.ru
Поступила в редакцию 21.06.2018
После доработки 03.07.2018
Принята к публикации 15.02.2019
Аннотация
Растворением диацетата родия [Rh2(OAc)4] в диоксане (Diox) и диметилсульфоксиде (Dmso) с последующим медленным испарением растворителя получены комплексы диацетата родия с диоксаном Rh2(OAc)4(Diox)2 (I) и диметилсульфоксидом Rh2(OAc)4(Dmso)2 (II). Взаимодействием [Rh2(OAc)4] с трис-4-фторфенилсурьмой в ацетонитриле синтезирован комплекс Rh2(OAc)4[(4-FC6H4)3Sb]2 (III). Методом РСА установлено, что атомы родия в соединениях I–III имеют малоискаженную октаэдрическую координацию: углы ORhRh, ORhO 176.56(6)°–177.72(4)° (I); SRhRh, ORhO 174.79(9)°–179.271(13)° (II) и SbRhRh, ORhO 173.590(19)°–175.48(10)° (III), связи Rh–Rh, Rh–OAc, Rh–ODiox 2.380(3), 2.037(3)–2.046(3), 2.335(3) Å (I), Rh–Rh, Rh–O, Rh–S 2.4288(10), 2.034(3)–2.046(3), 2.7258(10) Å (II), Rh–Rh, Rh–O, Rh–Sb 2.4183(12), 2.033(3)–2.044(3), 2.7113(13)−2.7120(13) Å (III). Структурная организация в кристаллах I и III обусловлена слабыми водородными связями Н…ODiox 2.50–2.72 Å, Н…OAc 2.57 Å (I); Н…ODmso 2.48–2.71 Å, Н…OAc 2.65, 2.66 Å (II) H…F 2.56–2.62 Å, H…O 2.68–2.71 Å (III).
ВВЕДЕНИЕ
Каталитическая способность комплексов родия широко известна, поэтому получение новых соединений этого металла и исследование особенностей их строения являются актуальной задачей, о чем свидетельствует достаточно большое число публикаций, посвященных этим вопросам [1–24]. Среди производных родия ионного типа с галогенсодержащими анионами можно выделить комплексы с моноядерными анионами: [RhHal6], где Hal = Cl [1–4], Br [5, 6], [RhHal4(Dmso-S)2]–, Hal = Cl [7, 8], Br [9, 10], [RhCl4(H2O)2]– [11], а также с биядерными анионами с μ2-мостиковыми атомами галогена: [Rh2(μ2-Cl3)Cl6]3– [12], [Rh2(μ2-I2)I4(CO)2(COMe)2]2– [13, 14], [Rh2(μ2-Cl3)Cl4(i-Pr3P)2]– [15]. Молекулярные галогенсодержащие комплексы родия также представлены моноядерными и биядерными формами: [RhCl3(CH3CN)2(DMF)] [11], [Rh2(μ2-Cl2)Cl4(Te[SiMe3]2)4] [16], [Rh2(μ2-Br2)Br4(Me3P)4] [17].
Известно, что тетраацетат диродия [Rh2(OAc)4] склонен к образованию аддуктов общей формулы [Rh2(OAc)4L2] с n-донорными лигандами. В качестве лигандов L могут выступать молекулы полярных растворителей, таких как вода [18, 19], N,N-диметилформамид [20], метанол [21], диметилсульфоксид [22], пиридин, монооксид углерода, диэтиламин, P(OMe)3, P(OPh)3, PF3 [23], Ph3Sb, Ph3As, S(CH2Ph)2 [24].
В настоящей работе синтезированы ацетатные комплексы родия Rh2(OAc)4(Diox)2, Rh2(OAc)4(Dmso)2 и Rh2(OAc)4[(4-FC6H4)3Sb]2 и методом РСА исследовано их строение.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез Rh2(OAc)4(Diox)2 (I). 50 мг (0.11 ммоль) Rh2(OAc)4 (коммерческий продукт) растворяли в 20 мл диоксана. После испарения растворителя при 24°С в течение недели наблюдали образование крупных темно-коричневых кристаллов, которые отфильтровывали и высушивали. Получили 58 мг (83%) комплекса I (tразл = 240°С). ИК-спектр (ν, см–1): 3447, 2988, 2938, 2920, 2864, 1585, 1435, 1418, 1352, 1418, 1352, 1344, 1263, 1115, 1080, 1045, 891, 870, 829, 696, 623, 594, 449.
Синтез Rh2(OAc)4(Dmso)2 (II). Растворяли 50 мг [Rh2(OAc)4] в 2 мл диметилсульфоксида. После испарения растворителя при 24°С в течение трех недель наблюдали образование крупных кристаллов, которые отфильтровывали и высушивали. Получили 50 мг (75%) комплекса II (tразл > 200°С). ИК-спектр (ν, см–1): 3443, 3053, 3009, 2920, 2855, 1589, 1472, 1431, 1418, 1364, 1346, 1310, 1263, 1211, 1084, 1015, 955, 924, 899, 851, 783, 700, 669, 521, 484, 436.
Синтез Rh2(OAc)4[(4-FC6H4)3Sb]2 (III). Смесь 50 мг (0.11 ммоль) Rh2(OAc)4 и 91 мг (0.22 ммоль) трис-4-фторфенилсурьмы растворяли при перемешивании в 15 мл ацетонитрила. После испарения растворителя при 24°С в течение недели наблюдали образование крупных коричневых кристаллов, которые отфильтровывали и высушивали. Получили 82 мг (58%) комплекса III (tразл = 193°С). ИК-спектр (ν, см–1): 3446, 3088, 3063, 3036, 2930, 1585, 1489, 1433, 1389, 1346, 1302, 1269, 1225, 1161, 1088, 1059, 1020, 818, 696, 625, 592, 575, 507, 415.
ИК-спектры соединений I–III записывали на ИК-Фурье-спектрометре Shimadzu IRAffinity 1S. Образцы готовили таблетированием с KBr (область поглощения 4000–400 см–1).
РСА кристаллов I–III проведен на дифрактометре D8 QUEST фирмы Bruker (MoKα-излучение, λ = 0.71073 Å, графитовый монохроматор) при 293(2) K. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [25]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [26] и OLEX2 [27]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур I–III приведены в табл. 1, основные длины связей и валентные углы – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1840624 (I), 1840627 (II), 1840625 (III), deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Таблица 1.
Кристаллографические данные, параметры эксперимента и уточнения структур комплексов I–III
| Параметр | Значение | ||
|---|---|---|---|
| I | II | III | |
| М | 309.10 | 598.25 | 1256.05 |
| Сингония | Триклинная | Моноклинная | Триклинная |
| Пр. гр. | P1 | P21/c | P1 |
| a, Å | 8.092(12) | 8.379(4) | 11.177(6) |
| b, Å | 8.535(9) | 16.708(9) | 11.840(6) |
| c, Å | 9.160(12) | 14.869(10) | 18.511(11) |
| α, град | 113.76(4) | 90.00 | 90.10(3) |
| β, град | 99.28(5) | 90.13(2) | 89.99(3) |
| γ, град | 105.47(6) | 90.00 | 107.23(2) |
| V, Å3 | 531.5(12) | 2082(2) | 2340(2) |
| Z | 2 | 4 | 2 |
| ρвыч, г/см3 | 1.931 | 1.909 | 1.783 |
| μ, мм–1 | 1.613 | 1.830 | 1.908 |
| F(000) | 310.0 | 1192.0 | 1220.0 |
| Размер кристалла, мм | 0.42 × 0.29 × 0.13 | 0.22 × 0.11 × 0.05 | 0.6 × 0.44 × 0.23 |
| Область сбора данных по θ, град | 5.54–90.8 | 6–65.34 | 5.68–63.28 |
| Интервалы индексов отражений | –16 ≤ h ≤ 16, –17 ≤ k ≤ 17, –18 ≤ l ≤ 18 |
–12 ≤ h ≤ 12, –25 ≤ k ≤ 25, –18 ≤ l ≤ 22 |
–16 ≤ h ≤ 16, –17 ≤ k ≤ 17, –27 ≤ l ≤ 27 |
| Измерено отражений | 40950 | 62749 | 101419 |
| Независимых отражений | 8645 | 7602 | 15656 |
| Rint | 0.0509 | 0.0514 | 0.0323 |
| Переменных уточнения | 139 | 243 | 564 |
| GOOF | 1.096 | 1.055 | 1.072 |
| R-факторы по F2 > 2σ(F2) | R1 = 0.0505, wR2 = 0.0815 |
R1 = 0.0288, wR2 = 0.0533 |
R1 = 0.0404, wR2 = 0.0734 |
| R-факторы по всем отражениям | R1 = 0.0885, wR2 = 0.0965 |
R1 = 0.0580, wR2 = 0.0595 |
R1 = 0.0570, wR2 = 0.0818 |
| Остаточная электронная плотность (min/max), e/A3 | 1.82/–3.17 | 0.42/–1.13 | 1.31/–1.02 |
Таблица 2.
Длины связей и валентные углы в структурах I–III
| Связь | d, Å | Угол | ω, град |
|---|---|---|---|
| I | |||
| Rh(1)–Rh(1a) | 2.380(3) | O(5)Rh(1)Rh(1a) | 177.72(4) |
| Rh(1–O(1) | 2.039(3) | O(3)Rh(1)O(4) | 176.56(6) |
| Rh(1)–O(2a) | 2.039(3) | O(1)Rh(1)O(2a) | 176.61(7) |
| Rh(1)–O(3) | 2.037(3) | O(1)Rh(1)Rh(1a) | 88.43(10) |
| Rh(1)–O(4) | 2.046(3) | O(2a)Rh(1)Rh(1a) | 88.18(10) |
| Rh(1)–O(5) | 2.335(3) | O(3)Rh(1)Rh(1a) | 88.23(7) |
| C(1)–O(1) | 1.269(3) | O(4)Rh(1)Rh(1a) | 88.33(7) |
| C(1)–O(2) | 1.273(3) | O(1)Rh(1)O(3) | 90.36(13) |
| C(3)–O(3a) | 1.269(3) | O(2a)Rh(1)O(3) | 89.64(14) |
| C(3)–O(4) | 1.266(3) | O(2a)Rh(1)O(4) | 90.42(14) |
| C(5)–O(5) | 1.418(3) | O(2a)Rh(1)O(5) | 91.63(11) |
| C(8)–O(5) | 1.433(4) | O(1)Rh(1)O(4) | 89.38(13) |
| C(6)–O(6) | 1.426(4) | O(1)Rh(1)O(5) | 91.75(10) |
| C(7)–O(6) | 1.429(4) | O(3)Rh(1)O(5) | 89.50(8) |
| Преобразования симметрии: a) 1 – x, 1 – y, 1 – z. | O(4)Rh(1)O(5) | 93.94(8) | |
| II | |||
| Rh(1)–Rh(1a) | 2.4069(10) | S(1)Rh(1)Rh(1a) | 176.469(16) |
| Rh(1)–O(2) | 2.0395(16) | O(2)Rh(1)O(3) | 175.57(6) |
| Rh(1)–O(3) | 2.0330(16) | O(4)Rh(1)O(5) | 175.52(6) |
| Rh(1)–O(4) | 2.0417(16) | O(3)Rh(1)S(1) | 88.39(5) |
| Rh(1)–O(5) | 2.0327(17) | O(2)Rh(1)S(1) | 96.04(5) |
| Rh(1)–S(1) | 2.4521(11) | O(2)Rh(1)Rh(1a) | 87.42(5) |
| S(1)–O(1) | 1.4795(17) | O(3)Rh(1)Rh(1a) | 88.15(5) |
| Rh(2)–Rh(2b) | 2.4056(10) | S(2)Rh(2)Rh(2b) | 176.467(16) |
| Rh(2)–O(6) | 2.0427(16) | O(6)Rh(2)O(7) | 175.63(6) |
| Rh(2)–O(7) | 2.0347(17) | O(8)Rh(2)O(9) | 175.64(6) |
| Rh(2)–O(8) | 2.0376(16) | O(9)Rh(2)S(2) | 88.51(5) |
| Rh(2)–O(9) | 2.0335(16) | O(8)Rh(2)S(2) | 95.86(5) |
| Rh(2)–S(2) | 2.4510(11) | O(8)Rh(2)Rh(2b) | 87.61(5) |
| S(2)–O(10) | 1.4787(17) | O(9)Rh(2)Rh(2b) | 88.03(5) |
| Преобразования симметрии: a) 2 – x, 1 – y, 1 – z; b) 1 – x, 1 – y, –z. | |||
| III | |||
| Rh(1)–Rh(1a) | 2.4183(12) | Sb(1)Rh(1)Rh(1a) | 173.620(18) |
| Rh(1)–O(1) | 2.034(3) | O(1)Rh(1)O(3) | 175.38(10) |
| Rh(1)–O(2) | 2.033(3) | O(2)Rh(1)O(4) | 175.29(10) |
| Rh(1)–O(3) | 2.041(3) | O(1)Rh(1)Sb(1) | 86.41(8) |
| Rh(1)–O(4) | 2.044(3) | O(3)Rh(1)Sb(1) | 98.16(8) |
| Rh(1)–Sb(1) | 2.7113(13) | O(4)Rh(1)Rh(1a) | 87.15(8) |
| Sb(1)–C(1) | 2.128(4) | O(2)Rh(1)Rh(1a) | 88.16(8) |
| Sb(1)–C(11) | 2.141(4) | O(2)Rh(1)O(3) | 89.10(12) |
| Sb(1)–C(21) | 2.134(4) | O(3)Rh(1)O(4) | 90.29(12) |
| Rh(2)–Rh(2b) | 2.4183(12) | Sb(2)Rh(2)Rh(2b) | 173.590(19) |
| Rh(2)–O(5) | 2.043(3) | O(5)Rh(2)O(7) | 175.39(11) |
| Rh(2)–O(6) | 2.044(3) | O(6)Rh(2)O(8) | 175.48(10) |
| Rh(2)–O(7) | 2.037(3) | O(7)Rh(2)Sb(2) | 86.35(8) |
| Rh(2)–O(8) | 2.034(3) | O(5)Rh(2)Sb(2) | 98.22(8) |
| Rh(2)–Sb(2) | 2.7120(13) | O(6)Rh(2)Rh(2b) | 87.13(8) |
| Sb(2)–C(31) | 2.133(4) | O(8)Rh(2)Rh(2b) | 88.38(8) |
| Sb(2)–C(41) | 2.129(4) | O(5)Rh(2)O(8) | 89.00(12) |
| Sb(2)–C(51) | 2.138(4) | O(7)Rh(2)O(8) | 90.41(12) |
| Преобразования симметрии: a) 1 – x, 2 – y, 1 – z; b) 1 – x, 1 – y, 2 – z. | |||
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Комплексы тетракис-(μ2-ацетато)-бис-(диоксан)диродий Rh2(OAc)4(Diox)2 (I) и тетракис-(μ2-ацетато)-бис-(диметилсульфоксид)диродий Rh2(OAc)4(Dmso)2 (II) получали растворением тетраацетата диродия в диоксане и ДМСО соответственно, тетракис-(μ2-ацетато)-бис-(три(4-фторфенил)стибин)диродий Rh2(OAc)4[(4-FC6H4)3Sb]2 (III) синтезировали из тетраацетата диродия и трис-4-фторфенилсурьмы в ацетонитриле. Установлено, что во всех случаях при медленном испарении растворителя кристаллизуются устойчивые на воздухе крупные темно-коричневые кристаллы:
В работе [24] для синтеза комплекса родия с трифенилстибиновым лигандом Rh2(OAc)4(Ph3Sb)2 в качестве растворителя использовали метанол, однако мы считаем, что ацетонитрил более предпочтителен, так как в этом случае удается исключить реакцию лигандного обмена между растворителем и триарилсурьмой. В [23] отмечена высокая лабильность аксиальных лигандов в комплексах родия Rh2(OAc)4L2, где L = пиридин, NHEt2, CO, P(OPh)3, PF3, P(OMe)3, которые в избытке метанола способны вступать в реакции обмена, что, по словам авторов, оказалось самым сложным синтетическим препятствием. Следует отметить, что строение комплекса II было исследовано ранее недостаточно точно (R-фактор = 3.6%) [22]. С целью уточнения особенностей кристаллической структуры II нами проведено ее повторное определение.
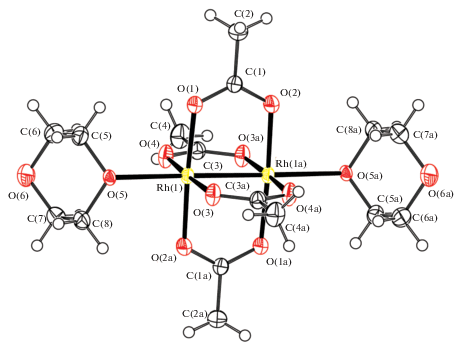
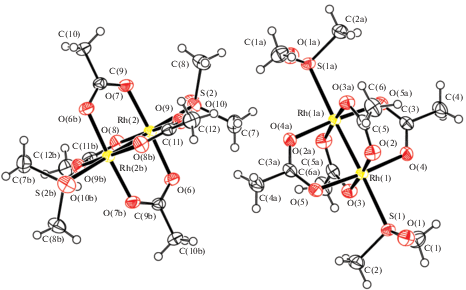
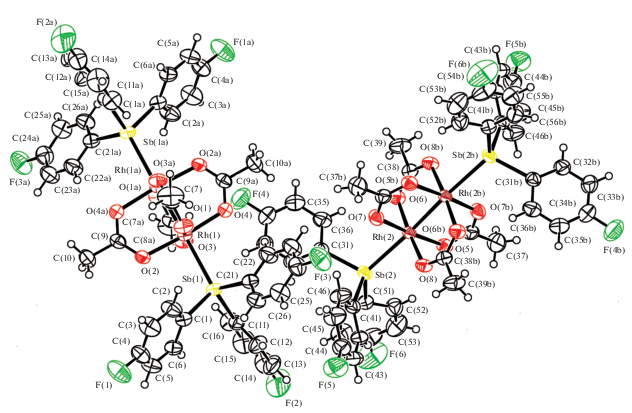
По данным РСА, в центросимметричных комплексах I–III атомы родия имеют малоискаженную октаэдрическую координацию (рис. 1–3). В кристаллах II и III присутствует по два типа кристаллографически независимых молекул, геометрические параметры которых близки друг к другу.
Транс-углы ORhO (О – атом кислорода ацетатных лигандов) равны 176.61(7)°, 176.56(9)° (I), 175.55(7)°−175.61(7)° (II), 175.3(1)°−175.7(1)° (III). Углы RhRhО (177.72(4)°), RhRhS (176.48(2)°, 176.49(2)°), RhRhSb (173.59(1)°, 173.62(1)°) в I, II, III соответственно также близки к теоретическому значению. Связи Rh–Rh 2.380(3) Å (I), 2.4056(10) и 2.4069(10) Å (II), 2.4183(12) Å (III) меньше удвоенного ковалентного радиуса атома родия (2.82 Å [28]). В I аксиальная связь Rh–ODiox (2.335(3) Å) значительно длиннее экваториальных Rh–OAc (2.037(3)–2.046(3) Å) и аналогичных связей Rh–O в структурно охарактеризованных комплексах родия, содержащих O-донорные молекулы растворителей: [Rh2(OAc)4(H2O)2] (2.309 Å) [18], [Rh2(OAc)4(DMF)2] (2.286, 2.308 Å) [20] и [Rh2(OAc)4(CH3OH)2] (2.288 Å) [21], что в целом коррелирует с основностью (донорыми числами) данных растворителей (диоксан – 14.8, вода – 18.0, ДМФА – 26.6, метанол – 19 [29]). В II и III длины связей Rh–S и Rh–Sb составляют 2.4510(11) и 2.4521(11) Å (II), 2.7113(13) и 2.7120(13) Å (III), экваториальные связи Rh–OAc изменяются в интервалах 2.0327(17)–2.044(3) и 2.033(3)–2.044(3) Å соответственно.
Структурная организация в кристаллах I–III обусловлена слабыми водородными связями Н…ODiox 2.50–2.72 Å, Н…OAc 2.57 Å (I); Н…ODmso 2.48–2.71 Å, Н…OAc 2.65, 2.66 Å (II); H…F 2.56–2.62 Å, H…O 2.68–2.71 Å (III), длины которых близки к суммам ван-дер-ваальсовых радиусов атомов водорода и кислорода (2.62 Å), а также водорода и фтора (2.57 Å) [30] соответственно.
Список литературы
Макитова Д.Д., Красочка О.Н., Атовмян Л.О. и др. // Коорд. химия. 1987. Т. 13. С. 383.
Graf J., Frank W. // Z. Anorg. Allg. Chem. 2004. V. 630. № 12. P. 1894. https://doi.org/10.1002/zaac.200400208
Pekhnyo V.I., Orysyk S.I., Bon V.V. et al. // Pol. J. Chem. 2006. V. 80. № 11. P. 1767.
Bujak M., Frank W. // Z. Kristallogr. – New Cryst. Struct. 2014. V. 229. № 2. P. 147. https://doi.org/10.1515/ncrs-2014-0083
Bujak M., Frank W. // Z. Naturforsch., B: Chem. Sci. 2002. V. 57. P. 1391.
Bujak M. // Cryst. Growth Des. 2015. V. 15. № 3. P. 1295. https://doi.org/10.1021/cg501694d
Alessio E., Santi A.S., Faleschini P. et al. // J. Chem. Soc., Dalton Trans. 1994. P. 1849. https://doi.org/10.1039/DT9940001849
Abbasi A., Geranmayeh S., Skripkin M.Y. et al. // Dalton Trans. 2012. V. 41. P. 850. https://doi.org/10.1039/C1DT11698C
Sharutin V.V., Sharutina O.K., Senchurin V.S., Somov N.V. // Russ. J. Coord. Chem. 2014. V. 40. № 11. P. 821. [Шарутин В.В., Шарутина О.К., Сенчурин В.С., Сомов Н.В. // Коорд. химия. 2014. Т. 40. № 11. С. 683.]https://doi.org/10.1134/S1070328414110074
Sharutin V.V., Sharutina O.K., Senchurin V.S. // Russ. J. Gen. Chem. 2016. V. 86. № 9. P. 2141. [Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. общ. химии. 2016. Т. 86. № 9. С. 1579.]https://doi.org/10.1134/S1070363216090309
Varshavskii Yu.S., Cherkasova T.G., Khrustalev V.N. et al. // Russ. J. Coord. Chem. 2007. V. 33. № 3. P. 194. [Варшавский Ю.С., Черкасова Т.Г., Хрусталев В.Н. и др. // Коорд. химия. 2007. Т. 33. № 3. С. 202.]https://doi.org/10.1134/S1070328407030074
Cotton F.A., Ucko D.A. // Inorg. Chim. Acta. 1972. V. 6. P. 161. https://doi.org/10.1016/S0020-1693(00)91778-X
Adamson G.W., Daly J.J., Forster D. // J. Organomet. Chem. 1974. V. 71. № 1. P. C17. https://doi.org/10.1016/S0022-328X(00)93156-5
Nguyen D.H., Lassauque N., Vendier L. et al. // Eur. J. Inorg. Chem. 2014. № 2. P. 326. https://doi.org/10.1002/ejic.201300933
Mura P. // J. Coord. Chem. 1999. V. 48. № 4. P. 503. https://doi.org/10.1080/00958979908023590
Vigo L., Poropudas M.J., Salin P. et al. // J. Organomet. Chem. 2009. V. 694. № 13. P. 2053. https://doi.org/10.1016/j.jorganchem.2009.02.001
Boyd S.E., Field L.D., Hambley T.W. // Acta Crystallogr., Sect. C: Cryst. Struct. Commun. 1994. V. 50. № 7. P. 1019. https://doi.org/10.1107/S010827019201271X
Cotton F.A., DeBoer B.G., LaPrade M.D. et al. // Acta Crystallogr., Sect. B: Struct. Sci. 1971. V. 27. № 8. P. 1664. https://doi.org/10.1107/S0567740871004527
Martin Junior D.S., Webb T.R., Robbins G.A. et al. // Inorg. Chem. 1979. V. 18. № 2. P. 475. https://doi.org/10.1021/ic50192a061
Moszner M., Glowiak T., Ziolkowski J.J. // Polyhedron. 1985. V. 4. № 8. P. 1413. https://doi.org/10.1016/S0277-5387(00)86972-7
Noinville V., Viossat B., Dung N.-H. // Acta Crystallogr., Sect. C: Cryst. Struct. Commun. 1993. V. 49. № 7. P. 1297. https://doi.org/10.1107/S0108270193000022
Cotton F.A., Felthouse T.R. // Inorg. Chem. 1980. V. 19. № 2. P. 323. https://doi.org/10.1021/ic50204a010
Christoph G.G., Koh Y.-B. // J. Am. Chem. Soc. 1979. V. 101. № 6. P. 1422. https://doi.org/10.1021/ja00500a011
Clark R.J.H., Hempleman A.J., Dawes H.M. et al. // J. Chem. Soc., Dalton Trans. 1985. P. I775. https://doi.org/10.1039/DT9850001775
Bruker (1998). SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA.
Bruker (1998). SHELXTL/PC. Vers. 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. № 2. P. 339. https://doi.org/10.1107/S0021889808042726
Batsanov S.S. // Russ. J. Inorg. Chem. 1991. V. 36. № 12. C. 3015.
Фиалков Ю.А. Не только в воде. Л.: Химия, 1989. 88 с.
Mantina M., Chamberlin A.C., Valero R. et al. // J. Phys. Chem. A. 2009. V. 113. № 19. P. 5806. https://doi.org/10.1021/jp8111556
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии