Журнал неорганической химии, 2019, T. 64, № 8, стр. 837-844
Синтез, структурные характеристики и тепловое расширение фосфатов ZnxMg0.5 + xE2 – x(PO4)3 (E = Ti, Zr)
В. И. Петьков 1, *, Д. А. Лавренов 1, М. В. Суханов 1, А. М. Ковальский 2, Е. Ю. Боровикова 3
1 Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, пр-т Гагарина, 23, Россия
2 Национальный исследовательский технологический университет “МИСиС”
119049 Москва, Ленинский пр-т, 4, Россия
3 Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: petkov@inbox.ru
Поступила в редакцию 14.01.2019
После доработки 12.02.2019
Принята к публикации 15.03.2019
Аннотация
Фосфаты ZnxMg0.5 +xE2 –x(PO4)3 (E = Ti, Zr) синтезированы золь-гель методом с последующей термообработкой и исследованы с помощью рентгенографии, электронного микрозондового анализа и ИК-спектроскопии. Установлено, что твердый раствор ZnxMg0.5 +xTi2 –x(PO4)3 (0 ≤ х ≤ 0.5, пр. гр. R$\bar {3}$) кристаллизуется в структурном типе NaZr2(PO4)3 и устойчив до 1050°С. Уточнена структура Zn0.2Mg0.7Ti1.8(PO4)3. Ее основу составляет каркас из соединенных общими вершинами тетраэдров PO4 и октаэдров (Mg,Ti)O6. В полостях каркаса располагаются катионы Mg2+ и Zn2+, имеющие октаэдрическую кислородную координацию. Твердый раствор ZnxMg0.5 +xZr2 –x(PO4)3 (0 ≤ х ≤ 0.5, пр. гр. P21/n), кристаллизующийся в структурном типе Sc2(WO4)3, термически нестоек выше 1000°С. Число полос валентных и деформационных колебаний иона ${\text{PO}}_{4}^{{3 - }}$ в ИК-спектрах ортофосфатов находится в согласии с фактор-групповым анализом для пр. гр. R$\bar {3}$ и P21/n. Изучено тепловое расширение твердых растворов ZnxMg0.5 +xE2 –x(PO4)3 в интервале температур 25–800°С. Регулирование состава этих средне- и высокорасширяющихся материалов позволяет изменять характеристики теплового расширения в желаемом направлении.
ВВЕДЕНИЕ
В плане моделирования новых соединений вызывает интерес структурный тип трифосфата натрия-дициркония (NZP, NASICON) [1]. К этому структурному типу относится природный минерал коснарит KZr2(PO4)3 [2]. Семейство NZP включает соединения и твердые растворы, описываемые кристаллохимической формулой (M1)0 → 1(M2)0 → 3{[L2(PO4)3]p−}3∞, где {[L2(PO4)3]p−}3∞ – каркас структуры (р – заряд каркаса), а (M1)0 → 1, (M2)0 → 3 – типы внекаркасных катионных позиций с обозначением заполнения позиций в каждом типе [3]. Заселение одних и тех же кристаллографических позиций атомами в степенях окисления от +1 до +5, а также широкие вариации изо- и гетеровалентного изоморфизма определяют уникальные свойства этих материалов − способность противостоять тепловым ударам, суперионную проводимость и каталитическую активность [3–9].
Двойные фосфаты M0.5Ti2(PO4)3 (M – катион в степени окисления +2) относятся к структурному типу NZP, кристаллизуются в ромбоэдрической системе, катионы M заселяют половину внекаркасных (M1)-полостей [10]. Фосфаты M0.5Zr2(PO4)3 с каркасными катионами циркония бóльшего размера по сравнению с титаном и крупными ионами M (Cd, Pb, Sr, Ba) в полостях кристаллизуются в структуре NZP, с ионами M меньшего размера − в структуре Sc2(WO4)3 (SW) [10]. Соединение Mn0.5Zr2(PO4)3 существует в виде модификаций SW и NZP [10].
Анализ литературных данных о фосфатах структурных типов NZP и SW, содержащих катионы M только в каркасе: [M1/3Nb5/3(PO4)3] (M = = Mg, Mn, Co, Ni, Cu, Zn) [11], Na1 + 2x[MgxZr2 –x(PO4)3] (0 ≤ x ≤ 1) [12], Na3[MZr(PO4)3] (M = Mn, Mg) [13], показал, что часть позиций каркаса может быть занята сравнительно небольшими катионами Mg, Mn, Co, Ni, Cu или Zn. Попытка синтеза соединения Na3[ZnZr(PO4)3] не увенчалась успехом [13].
Сведения о фосфатах, содержащих элементы в степени окисления +2 одновременно в позициях каркаса и в полостях структуры, ограничены твердыми растворами M0.5 + $_{x}{\text{M}}_{x}^{'}$E2– x(PO4)3 (M, M' = Mg, Co, Mn, Cd, Ca, Sr, Pb, Ba; E = Ti, Zr) [14]. На устойчивость и смену структурного типа таких фосфатов влияют природа и размеры катионов, сочетающихся в каркасе и в полостях. Можно предположить, что структурный тип NZP устойчив, если каркасные позиции заселены катионами E4+ и M2+, радиус которых меньше, чем у Cd2+, а позиции полостей – катионами с радиусом, равным или бóльшим, чем у кадмия. Структурный тип SW предпочтителен для фосфатов, содержащих в полостях небольшие катионы, незначительно отличающиеся по размеру от каркасообразующих катионов.
На изоморфные замещения атомов в описываемых фосфатах определенный отпечаток накладывает стереохимия переходных элементов. Так, в числе потенциальных кристаллохимических родственников титана, лишенного в состоянии Ti4+d-электронов, может быть представлен цинк. Химические связи Zn−O в кристаллических структурах имеют ковалентный характер, прежде всего за счет d10-конфигурации цинка сферической формы, не вносящей специфику, присущую остальным d-состояниям. Однако катион Zn2+, имея относительно большой радиус (0.74 Å), проявляет тенденцию к тетраэдрической координации, в отличие от октаэдрической координации Ti4+ (для которого практически не существует альтернативы), имеющего широкие изоморфные отношения с Zr4+ [15].
Цель настоящей работы заключалась в экспериментальной проверке возможности включения цинка в каркасные и внекаркасные кристаллографические позиции фосфатов, описываемых общей формулой ZnxMg0.5 +xE2 –x(PO4)3 (E = Ti, Zr), изучении их фазообразования, выявлении поля концентрационно-температурной стабильности ожидаемых твердых растворов и определении параметров теплового расширения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Образцы ZnxMg0.5 +xE2 –x(PO4)3 (E = Ti, Zr) c x = 0, 0.1, 0.2, 0.3, 0.4, 0.5, 0.6, 0.7, 0.8, 0.9, 1.0 получали золь-гель методом с последующей термообработкой. Исходными реагентами для синтеза служили реактивы квалификации “х. ч.”: MgO, ZnO, TiOCl2 (получен из TiCl3 путем окисления на воздухе смесью соляной и азотной кислот), ZrOCl2 · 8H2O и H3PO4. Стехиометрические количества растворенных в соляной кислоте оксидов цинка и магния и 1М водного раствора оксихлорида титана или циркония смешивали при комнатной температуре. Затем при перемешивании добавляли раствор ортофосфорной кислоты, взятый также в соответствии со стехиометрией. Реакционные смеси высушивали при 90°C и подвергали термообработке на воздухе при 600–1100°C в течение 24 ч на каждой стадии. Поэтапное нагревание чередовали с диспергированием для обеспечения гомогенизации смесей. Синтезированные образцы представляли собой поликристаллические порошки белого цвета.
Рентгенограммы образцов записывали на дифрактометре Shimadzu XRD-6000 (CuKα-излучение, λ = 1.54178 Å, диапазон углов 2θ = 10°–60°). Рентгенофазовый анализ (РФА) использовали для установления фазового состава образцов в процессе их получения после каждого этапа изотермического обжига. Индицирование рентгенограмм проводили методом структурной аналогии с использованием кристаллографических данных описанных в литературе соединений. Параметры элементарных ячеек полученных фосфатов уточняли методом наименьших квадратов. Погрешности в определении параметров не превышали Δa = ±0.006, Δb = ±0.004, Δc = ±0.006 Å, Δβ = = ±0.04°.
Контроль химического состава и однородности образцов осуществляли с помощью сканирующего электронного микроскопа JEOL JSM-7600F, оснащенного термополевой электронной пушкой (катод Шоттки), с пространственным разрешением до 1 нм. Микроскоп оснащен системой микроанализа − энергодисперсионным спектрометром OXFORD X-Max 80 (Premium) с полупроводниковым кремний-дрейфовым детектором с безазотным охлаждением.
Рентгенодифракционный спектр Zn0.2Mg0.7Ti1.8(PO4)3 (x = 0.2) для структурного исследования записывали в интервале углов 2θ = = 10°–110° с шагом сканирования 0.02° и экспозицией в точке 15 с. Обработку рентгенограммы и уточнение структуры фосфата проводили методом Ритвельда [16] с использованием программы RIETAN-97 [17]. Аппроксимирование профилей пиков осуществляли согласно модифицированной функции псевдо-Войта (Mod-TCH pV [18]). В качестве базовой модели для уточнения кристаллической структуры фосфата использовали координаты атомов NaGeTi(PO4)3 [19].
Функциональный состав образцов подтверждали методом ИК-спектроскопии. ИК-спектры поглощения записывали на ИК-Фурье-спектрометре Shimadzu FTIR-8400S в диапазоне волновых чисел 400–1400 см−1.
Высокотемпературную съемку осуществляли в температурном интервале 25–800°С с использованием приставки HA-1001 фирмы Shimadzu. Скорость нагревания составляла 10 град/мин. Перед началом съемки образец выдерживали при заданной температуре в течение 10 мин.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При изучении процессов фазообразования в системах ZnxMg0.5 +xE2 –x(PO4)3 образцы в процессе синтеза подвергали изотермическому обжигу при 600, 800, 900, 1000, 1050 и 1100°C. Время выдержки при каждой температуре составляло 24 ч. В конце каждой стадии обжига часть образца подвергали воздушной закалке и анализировали. Оставшуюся часть продолжали нагревать, так поступали на протяжении всего ступенчатого обжига.
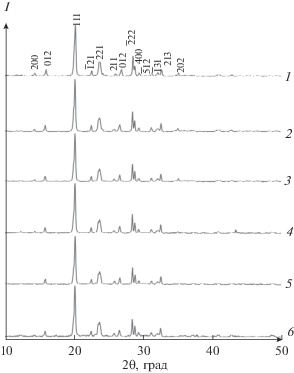
В системе ZnxMg0.5 +xTi2 – x(PO4)3 образуется ограниченный твердый раствор в области составов 0 ≤ х ≤ 0.5. Однофазные продукты со структурой NZP кристаллизуются при 800°C.
На рис. 1 представлено влияние температуры на формирование фазы состава Zn0.5Mg1.0Ti1.5(PO4)3 (x = 0.5). При 600°С методом РФА фиксируется смесь фаз: целевого продукта, Mg2P2O7, ZnP4O11 и Mg3(PO4)2. С повышением температуры доля примесных фаз уменьшается, а кристалличность целевой фазы возрастает. Тройной фосфат устойчив до 1050°C, последующее повышение температуры ведет к его разложению.
Рис. 1.
Рентгенограммы фосфатов ZnxMg0.5 + xTi2 ‒ x(PO4)3: х = 0 (1), 0.1 (2), 0.3 (3), 0.4 (4), 0.5 (5).
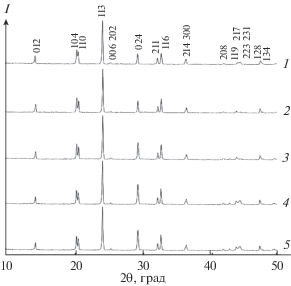
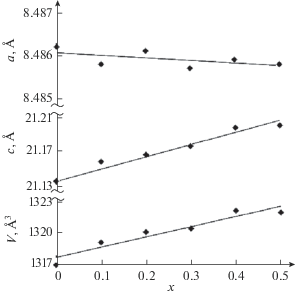
На рентгенограммах образцов твердого раствора ZnxMg0.5 +xTi2 –x(PO4)3 присутствуют интенсивные рефлексы фаз NZP-строения (рис. 2). По данным электронной микроскопии, образцы гомогенные, химический состав, по результатам микрозондового анализа, соответствует теоретическим значениям. Параметры элементарных ячеек образцов твердого раствора монотонно изменяются с ростом x (рис. 3). При х > 0.5 образцы системы ZnxMg0.5 +xTi2 –xP3O12 представляют собой смесь фаз (рис. 1).
Рис. 2.
Зависимость интенсивности максимальных рефлексов отражения фаз, образующихся при синтезе фосфата Zn0.5Mg1.0Ti1.5P3O12, от температуры. Обозначения фаз: 1 – Zn0.5Mg1.0Ti1.5(PO4)3 (2θ = = 24.5°), 2 – Mg2P2O7 (2θ = 30.1°), 3 – ZnP4O11 (2θ = = 27°), 4 – Mg3(PO4)2 (2θ = 25.6°).
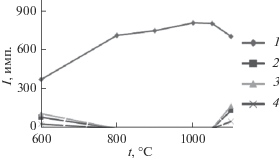
ИК-спектры изученных образцов ZnxMg0.5 +xTi2 –x (PO4)3 (0 ≤ х ≤ 0.5) имеют вид, типичный для ортофосфатов NZP-строения с пр. гр. R$\bar {3}$ (рис. 4а). В ИК-спектрах фосфатов с пр. гр. R$\bar {3}$ правилами отбора разрешено по шесть полос асимметричных валентных νas и асимметричных деформационных δas колебаний иона ${\text{PO}}_{4}^{{3 - }},$ а также четыре полосы симметричных деформационных δs колебаний и две полосы симметричных валентных νs колебаний этого иона. Полосы в области 1270−1040 см−1 отнесены к валентным асимметричным колебаниям νas иона ${\text{PO}}_{4}^{{3 - }}.$ Весьма большие значения волновых чисел (1270−1240 см−1) объясняются тем, что при большом значении угла POTi в структурах электронная плотность поляризованного иона Ti4+, имеющего малый размер и большой заряд, частично локализуется в связи P−O; это приводит к более высоким значениям силовых постоянных связи P−O. К валентным симметричным νs колебаниям относятся полосы в области 990−880 см−1. Полосы при 680−540 см−1 соответствуют деформационным асимметричным δas, а при 460−440 см–1 − деформационным симметричным δs колебаниям иона ${\text{PO}}_{4}^{{3 - }}.$
Рис. 4.
ИК-спектры фосфатов ZnxMg0.5 +xE2 –x(PO4)3: E = Ti (а), Zr (б), x = 0 (1), 0.1 (2), 0.2 (3), 0.3 (4), 0.4 (5), 0.5 (6).
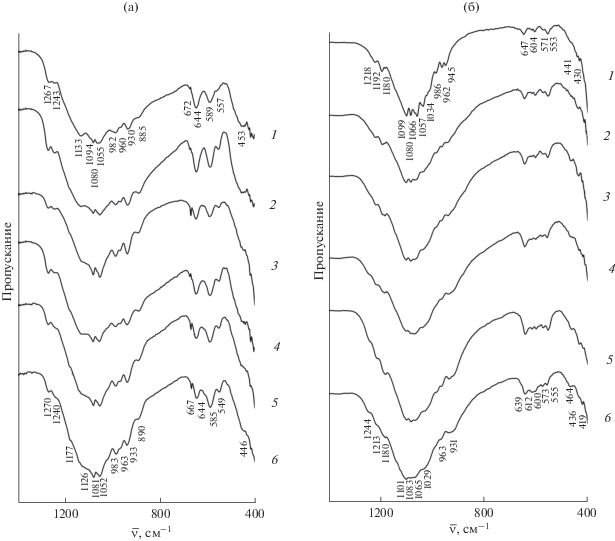
Для подтверждения строения твердого раствора ZnxMg0.5 +xTi2 –x(PO4)3 проведено уточнение его структуры (x = 0.2) при комнатной температуре методом Ритвельда. Условия съемки, параметры ячейки и основные данные по уточнению структуры приведены в табл. 1. На рис. 5 показаны экспериментальная, вычисленная, штрих- и разностная рентгенограммы Zn0.2Mg0.7Ti1.8(PO4)3. Координаты, параметры атомных смещений и заселенности базисных атомов фосфатов приведены в табл. 2.
Таблица 1.
Условия съемки, параметры ячейки и основные данные по уточнению структуры фосфата Zn0.2Mg0.7Ti1.8(PO4)3
| Параметр | Zn0.2Mg0.7Ti1.8(PO4)3 |
|---|---|
| Пр. гр., Z | R$\bar {3},$ 6 |
| a, Å | 8.4885(4) |
| c, Å | 21.191(1) |
| V, Å3 | 1322.3(1) |
| ρрентг, г/см3 | 2.973(1) |
| Интервал углов 2θ, град | 10.00–110.00 |
| Шаг сканирования | 0.02 |
| Число рефлексов отражения | 187 |
| Число уточняемых параметров | Структурные – 11 Прочие – 18 |
| Факторы достоверности: | |
| Rwp, % | 5.9 |
| RP, % | 3.96 |
| S | 2.03 |
Рис. 5.
Экспериментальная (1), вычисленная (2), разностная (3) и штрих- (4) рентгенограммы фосфата Zn0.2Mg0.7Ti1.8(PO4)3.
Таблица 2.
Координаты, параметры атомных смещений и заселенности (q) базисных атомов в структуре фосфата Zn0.2Mg0.7Ti1.8(PO4)3
| Атом | x | y | z | Bизо | q |
|---|---|---|---|---|---|
| Mg(1) Zn Mg(2) Ti(1) Mg(3) Ti(2) |
0.0 0.0 0.0 0.0 0.0 0.0 |
0.0 0.0 0.0 0.0 0.0 0.0 |
0.5 0.0 0.1377(6) 0.1377(6) 0.6476(5) 0.6476(5) |
1.2(1) 1.2(1) 1.2(1) 1.2(1) 1.2(1) 1.2(1) |
1.0 0.2 0.1 0.9 0.1 0.9 |
| P | 0.279(1) | –0.005(2) | 0.2556(6) | 1.2(1) | 1.0 |
| O(1) | 0.163(2) | –0.035(3) | 0.1971(8) | 1.2(1) | 1.0 |
| O(2) O(3) O(4) |
0.037(3) 0.201(3) 0.851(3) |
0.799(2) 0.172(3) 0.820(3) |
0.6817(8) 0.0831(8) 0.5913(8) |
1.2(1) 1.2(1) 1.2(1) |
1.0 1.0 1.0 |
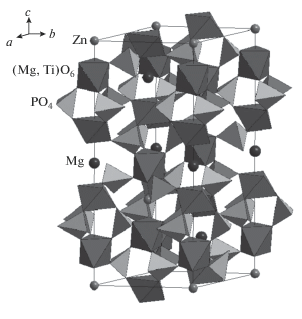
Фрагмент структуры фосфата Zn0.2Mg0.7Ti1.8(PO4)3, кристаллизующегося в структурном типе NZP, приведен на рис. 6. Ее основу формирует каркас {Mg0.2Ti1.8(PO4)3}3∞, образованный сочленением изолированных октаэдров (Mg,Ti)O6 и тетраэдров PO4. Каждый из октаэдров связан вершинами с шестью тетраэдрами PO4, которые, в свою очередь, соединены с четырьмя разными октаэдрами. Два (Mg,Ti)-октаэдра и три заселенных атомами фосфора тетраэдра, объединяясь через вершины, образуют характерный фрагмент каркаса – “фонарик”. Эти группировки связаны в трехмерную решетку. В полостях каркаса между ребрами двух октаэдров располагаются катионы Zn2+ и Mg2+, имеющие октаэдрическую кислородную координацию (рис. 6). Межатомные расстояния Mg(Ti)−O в двух независимых октаэдрах смешанного типа (Mg,Ti)O6 распределены в интервалах 1.87−1.99 и 1.85−1.99 Å, средние расстояния Mg(Ti)−O в координационных полиэдрах составляют 1.93 и 1.92 Å. Соотношение длин связей и валентных углов в тетраэдрах PO4 типично для этого аниона. Тетраэдры деформированы, длины связей P−O в полиэдрах PO4 изменяются в пределах 1.49−1.72 Å. Во внекаркасных позициях расстояния Zn−O и Mg−O до шести ближайших атомов O равны 2.32 и 2.42 Å соответственно. В твердом растворе Zn-xMg0.5 +xTi2 –x(PO4)3 с ростом x происходит заселение внекаркасных полостей катионами цинка. Кроме того, в координационных полиэдрах каркаса (Mg,Ti)O6 увеличивается содержание бóльших по размеру ионов магния. Расположение координационных полиэдров ZnO6 и (Mg,Ti)O6 вдоль направления оси c элементарной ячейки (рис. 6) приводит к расширению структуры вдоль этой оси и увеличению параметра с ячейки с ростом x (рис. 3). При этом происходит деформация РО4-тетраэдров. Внутренний угол ОРО увеличивается вдоль оси с, что сокращает расстояние между параллельными колонками и приводит к уменьшению параметра а.
Как следует из приведенных данных, кристаллохимическая формула твердого раствора – Mg0.5Znx[MgxTi2 –x(PO4)3]3∞, где [MgxTi2 –x(PO4)3]3∞ − каркас структуры, в котором Mg и Ti заселяют позиции с КЧ = 6, а внекаркасные позиции частично заполнены Znx и Mg0.5 (КЧ = 6).
В ряду фосфатов ZnxMg0.5 +xZr2 –x(PO4)3 при 900°C образуется ограниченный твердый раствор. Анализ рентгенограмм образцов ZnxMg0.5 + xZr2 –x(PO4)3 в области составов 0 ≤ х ≤ ≤ 0.5 позволил установить их однофазность и кристаллизацию в структурном типе Sc2(WO4)3 (SW) (рис. 7).
Рис. 7.
Рентгенограммы образцов ZnxMg0.5 +xZr2– x(PO4)3: х = 0 (1), 0.1 (2), 0.2 (3), 0.3 (4), 0.4 (5), 0.5 (6).
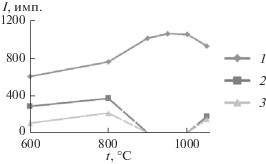
Влияние температуры на формирование твердого раствора Zn0.5Mg1.0Zr1.5(PO4)3 представлено на рис. 8. При 600°C методом РФА фиксируется смесь фаз: целевого продукта, ZrP2O7 и Zn2Mg(PO4)2. С повышением температуры доля примесных фаз уменьшается, а кристалличность целевой фазы возрастает. Целевой продукт устойчив до 1000°С.
Рис. 8.
Зависимость интенсивности максимальных рефлексов отражения фаз, образующихся при синтезе фосфата Zn0.5Mg1.0Zr1.5P3O12, от температуры. Обозначения фаз: 1 – Zn0.5Mg1.0Zr1.5(PO4)3 (2θ = = 20.0°), 2 – ZrP2O7 (2θ = 21.4°), 3 – Zn2Mg(PO4)2 (2θ = 25.7°).
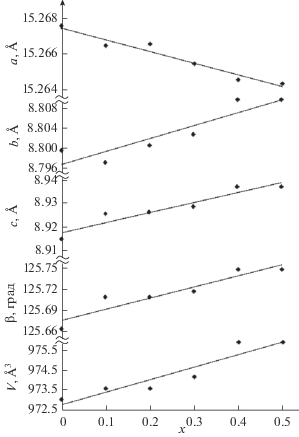
В твердом растворе ZnxMg0.5 +xZr2 –x(PO4)3 в каркасе структуры [MgxZr2 –x(PO4)3]3∞ магний и цирконий заселяют позиции с КЧ = 6, внекаркасные позиции заняты Zn и Mg с КЧ = 4. Рассчитанные параметры элементарных ячеек монотонно изменяются с увеличением содержания катиона в степени окисления +2 в составе твердого раствора (рис. 9).
ИК-спектры ZnxMg0.5 +xZr2 –x(PO4)3 (0 ≤ х ≤ 0.5) имеют вид, типичный для ортофосфатов SW-строения с пр. гр. P21/n (рис. 4б). В ИК-спектрах фосфатов с пр. гр. P21/n правилами отбора разрешено по девять полос асимметричных валентных νas и асимметричных деформационных δas колебаний иона ${\text{PO}}_{4}^{{3 - }},$ а также шесть полос симметричных деформационных δs колебаний и три полосы симметричных валентных νs колебаний этого иона. Полосы в области 1250−1025 см−1 соответствуют валентным асимметричным колебаниям νas иона ${\text{PO}}_{4}^{{3 - }}.$ К валентным симметричным νs колебаниям относятся полосы в интервале 990−930 см−1. Полосы при 660−540 см−1 соответствуют деформационным асимметричным δas, а при ~450 см−1 − деформационным симметричным δs колебаниям иона ${\text{PO}}_{4}^{{3 - }}.$
Результаты исследования твердых растворов ZnxMg0.5 +xTi2 –x(PO4)3 и ZnxMg0.5 +xZr2 –x(PO4)3 расширяют картину фазообразования известных фосфатов с октаэдро-тетраэдрическими каркасами {[L2(PO4)3]p–}3∞: с одной стороны, они характеризуют общие тенденции зависимости строения фосфатов от размерного фактора, описанные во введении, а с другой – отражают стереохимические возможности цинка, накладывающие отпечаток на характер изоморфных замещений атомов. Близкие значения радиусов катионов Ti4+, Zr4+ и Mg2+ с часто наблюдаемой в фосфатах октаэдрической координацией способствуют их изоморфному замещению в кристаллических постройках. Для Zn2+ в кислородных соединениях характерна прежде всего тетраэдрическая координация, значительно реже − октаэдрическая.
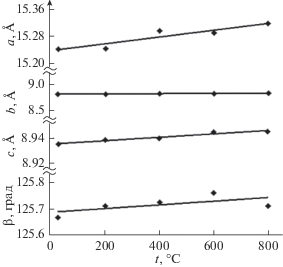
Поскольку практически важной характеристикой материалов является тепловое расширение [20], методом высокотемпературной рентгенографии исследованы образцы твердых растворов ZnxMg0.5 + xE2 – x(PO4)3. Температурные зависимости параметров ячейки фосфатов описываются линейными функциями (рис. 10). Значения коэффициентов теплового расширения, представленные в табл. 3, позволяют отнести фосфаты к средне- (αV = (4–6) × 10−6 K−1) и сильно расширяющимся (αV = (9–10) ×10−6 K−1) веществам. За счет изменения состава твердых растворов можно регулировать характеристики теплового расширения материалов в требуемом направлении.
Таблица 3.
Коэффициенты теплового расширения фосфатов ZnxMg0.5 +xE2 –x(PO4)3 (E = Ti, Zr)
| Фосфат | Коэффициенты теплового расширения (α × 106, K−1) | ||||
|---|---|---|---|---|---|
| αa | αb | αc | αβ | αV | |
| Mg0.5Ti2(PO4)3 | 5.9 | 7.3 | 6.4 | ||
| Zn0.3Mg0.8Ti1.7(PO4)3 | 3.9 | 7.4 | 5.1 | ||
| Zn0.5MgTi1.5(PO4)3 | 4.7 | 4.8 | 4.7 | ||
| Mg0.5Zr2(PO4)3 | –2.3 | 7.8 | 0.1 | –0.2 | 5.7 |
| Zn0.3Mg0.8Zr1.7(PO4)3 | 5.9 | 3.4 | 1.4 | 0.8 | 9.5 |
| Zn0.5MgZr1.5(PO4)3 | 6.4 | 2.6 | 2.2 | 4.5 | 10.0 |
ЗАКЛЮЧЕНИЕ
Исследовано фазообразование в системах Zn-xMg0.5 +xE2 –x(PO4)3 (E = Ti, Zr). Синтезированы твердые растворы Mg0.5Znx[MgxE2 –x(PO4)3] (0 ≤ x ≤ 0.5) с кристаллическими структурами NZP и SW. Показано, что их основой является трехмерный каркас из соединяющихся общими вершинами тетраэдров PO4 и октаэдров (Mg, E)O6, атомы цинка заселяют внекаркасные позиции, а атомы магния – каркасные и внекаркасные позиции. Изменение состава твердых растворов ZnxMg0.5 +xE2 –x(PO4)3 позволяет регулировать в желаемом направлении значения их коэффициентов теплового расширения (αV) от 1 × 10−5 до 5 × 10−6 K−1.
Список литературы
Naqash S., Tietz F., Guillon O. // Solid State Ionics. 2018. V. 319. P. 13. https://doi.org/10.1016/j.ssi.2018.01.048
Brownfield M.E., Foord E.E., Sutley S.J. et al. // Am. Mineral. 1993. V. 78. P. 653.
Pet'kov V.I. // Russ. Chem. Rev. 2012. V. 81. № 7. P. 606. [Петьков В.И. // Успехи химии. 2012. Т. 81. № 7. С. 606.]https://doi.org/10.1070/RC2012v081n07ABEH004243
Wang Y., Zhou Y., Song Y. et al. // Ceram. Int. 2018. V. 44. № 14. P. 16698. https://doi.org/10.1016/j.ceramint.2018.06.097
Иванов-Шиц А.К., Мурин И.В. Ионика твердого тела. Т. 1. СПб.: Изд-во СПбГУ, 2001. 616 с.
Lu X., Wang S., Xiao R. et al. // Nano Energy. 2017. V. 41. P. 626. https://doi.org/10.1016/j.nanoen.2017.09.044
Lee W., Yamauchi S., Tamura S., Imanaka N. // Mater. Lett. 2019. V. 234. P. 261. https://doi.org/10.1016/j.matlet.2018.09.095
Asabina E.A., Orekhova N.V., Ermilova M.M. et al. // Inorg. Mater. 2015. V. 51. № 8. P. 793. [Асабина Е.А., Орехова Н.В., Ермилова М.М. и др. // Неорган. материалы. 2015. Т. 51. № 8. С. 864.]https://doi.org/10.1134/S002016851508004X
Ilin A.B., Ermilova M.M., Orekhova N.V. et al. // J. Alloys Compd. 2018. V. 748. P. 583. https://doi.org/10.1016/j.jallcom.2018.03.099
Pet’kov V.I., Lavrenov D.A., Sukhanov M.V. et al. // Russ. J. Inorg. Chem. 2019. V. 64. № 2. P. 137. [Петьков В.И., Лавренов Д.А., Суханов М.В. и др. // Журн. неорган. химии. 2019. Т. 64. № 2. С. 137.]https://doi.org/10.1134/S0036023619020165
Pet'kov V.I., Orlova A.I., Sukhanov M.V. et al. // J. Mater. Sci. Lett. 2002. V. 21. № 6. P. 513. https://doi.org/10.1023/A:1015355228098
Jaeger C., Barth S., Feltz A. et al. // Phys. Status Solidi A. 1987. V. 102. № 2. P. 791. https://doi.org/10.1002/pssa.2211020242
Feltz A., Barth S. // Solid State Ionics. 1983. V. 9−10. P. 817. https://doi.org/10.1016/0167-2738(83)90094-2
Asabina E., Pet’kov V., Mayorov P. et al. // Pure Appl. Chem. 2017. V. 89. № 4. P. 523. https://doi.org/10.1515/pac-2016-1005
Пятенко Ю.А., Воронков А.А., Пудовкина З.В. Минералогическая кристаллохимия титана. М.: Наука, 1976. 155 с.
Rietveld H.M. // Acta Crystallogr. 1967. V. 22. № 1. P. 151. https://doi.org/10.1107/S0365110X67000234
Kim Y.I., Izumi F. // J. Ceram. Soc. Jpn. 1994. V. 102. P. 401. https://doi.org/10.2109/jcersj.102.401
Izumi F. The Rietveld Method. N.Y.: Oxford Univ. Press, 1993. 298 p.
Carrasco M.P., Guillem M.C., Alamo J. // Mater. Res. Bull. 1993. V. 28. P. 793. https://doi.org/10.1016/0025-5408(93)90020-E
Pet’kov V.I., Shipilov A.S., Dmitrienko A.S. et al. // J. Ind. Eng. Chem. 2018. V. 57. P. 236. https://doi.org/10.1016/j.jiec.2017.08.029
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии