Журнал неорганической химии, 2019, T. 64, № 6, стр. 613-622
Теоретическое исследование структуры и стабильности послойно гидрированных алюминиевых кластеров Al44Hn и Al89Hm
О. П. Чаркин 1, *, Н. М. Клименко 2
1 Институт проблем химической физики РАН
142432 Московской обл., Черноголовка, пр-т Академика Семенова, 1, Россия
2 Московский государственный технологический университет им. М.В. Ломоносова
119571 Москва, пр-т Вернадского 86, Россия
* E-mail: charkin@icp.ac.ru
Поступила в редакцию 02.11.2018
После доработки 06.12.2018
Принята к публикации 15.03.2019
Аннотация
В рамках метода функционала плотности (DFT) рассчитаны структурные, энергетические и спектроскопические характеристики двух серий послойно гидрированных алюминиевых кластеров Al44Hn (n = 27–44) и Al89Hт (т = 15, 24, 39 и 63). Показано, что при увеличении числа атомов Н в обеих сериях происходит быстрое нарастание структурных деформаций вплоть до кооперативных перегруппировок с изменением формы и состава поверхностного слоя и внутреннего ядра кластеров. В конце первой серии Al44Hn несколько поверхностных атомов смещается во внешнюю сферу каркаса с образованием валентно-ненасыщенных “надповерхностных” фрагментов AlHn и Al2Hn, которые могут быть активными центрами на стадиях более глубокого гидрирования. Одновременно внутреннее ядро [Al]5 распадается и его атомы внедряются в поверхностный слой. Локализовано семейство “инвертированных” изомеров Al42H42 с каркасом [Al42], которые содержат эндоэдральную группу AlH4 и “внутренние” связи Al−H, направленные водородным концом к центру внутренней полости. В конце второй серии во внешней сфере кластера ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{{63}}^{ - }$ образуются пять аланатных групп AlH4 и два фрагмента Al3H2, связанных с поверхностью водородными мостиками. Результаты представляют интерес при DFT-моделировании гидрирования наноразмерных алюминиевых кластеров на молекулярном уровне.
ВВЕДЕНИЕ
Поиск и исследование структуры новых гидридов алюминия с высоким содержанием водорода, а также изучение механизмов гидрирования легких элементов остаются важной задачей из-за перспектив использования этих соединений в качестве эффективных накопителей водорода, источников водорода для топливных элементов, восстанавливающих агентов и т.д. (например, [1–5]). Благодаря развитию методов молекулярных пучков, масс-спектрометрии, фотоэлектронной спектроскопии (ФЭС) и колебательной спектроскопии в инертных матрицах в сочетании c квантово-химическими расчетами было обнаружено более двухсот новых кластеров и молекулярных ионов гидридов алюминия различного состава и рассчитаны их молекулярные характеристики [6–17]. В работе [18] в рамках метода теории функционала плотности (ТФП/DFT) были выполнены расчеты структурных, энергетических и спектроскопических характеристик серии гидрированных кластеров серии ${\text{A}}{{{\text{l}}}_{{44}}}{\text{H}}_{n}^{ - }$ с последовательно увеличивающимся числом атомов водорода в интервале n = 1−24. Согласно расчетам, в этой серии алюминиевый каркас сохраняет замкнутую форму матрешки с поверхностным слоем [Al39] и пятиатомным внутренним “ядром” [Al5], но при увеличении n происходит быстрое нарастание асимметричных деформаций как поверхностного слоя, так и ядра. Поверхность гофрируется, часть двухцентровых терминальных связей Al−H трансформируется в трехцентровые водородные мостики Al−H−Al, и часть ее атомов Al смещается из поверхностного слоя во внешнюю сферу. Внутреннее ядро [Al5] при n = 24 теряет бипирамидальную форму и смещается к поверхностному слою так, что один или два его атома встраиваются в вогнутые участки поверхностного слоя. Рассчитанные энергии реакций распада Al44Hn → Al44Hn– 2 + Н2 с отщеплением молекулы водорода имеют порядок ~5−6 ккал/моль и свидетельствуют о небольшой эндотермичности этих реакций.
Настоящее работа является продолжением [18] и ставит целью исследование эволюции структурных и энергетических свойств субнаноразмерных гидрированных кластеров AlmHn при увеличении числа каркасных атомов алюминия m и атомов водорода n. Проблемы структурной перестройки поверхности кластера Alm по мере ее последовательного насыщения атомами Н; знание состава и структуры поверхностных дефектов, которые могут выражаться в образовании надповерхностных реакционноспособных фрагментов типа AlHn, Al2Hn и их ассоциатов или в виде многоатомных поверхностных “окон”; понимание механизмов обновления поверхности, разрушающейся при гидрировании за счет внедрения в нее атомов из подповерхностных слоев; знание критических значений n*, для которых характерны радикальные трансформации с изменениями формы и состава поверхностного слоя и ядра и др., представляются важными и интересными во многих аспектах, но на молекулярном уровне они остаются малоизученными. На наш взгляд, систематические DFT-расчеты наиболее интересных участков поверхности потенциальной энергии гидрированных кластеров AlmHn с разными m и n могут быть в этой области весьма полезными. В настоящей работе мы попытались проиллюстрировать это на примере расчетов двух серий послойно гидрированных субнаноразмерных кластеров Al44Hn и ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{n}^{ - }$ (см. также [19]).
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Как и в [18], стартовые структуры выбирали добавлением n внешних связей Al−H к равновесной структуре свободного кластера Al44 с последовательным заполнением его поверхностных, промежуточных и экваториального слоев II, I и O шестью и девятью атомами Н. Оптимизацию геометрических параметров и частот нормальных колебаний кластеров Al44Hn проводили с использованием программы GAUSSIAN-09 [20] в рамках приближения B3LYP [21, 22] с базисом 6-31G и серии оптимизационных процедур при последовательном понижении симметрии до С1. Энергетические характеристики уточняли с базисом 6-31G*. К сожалению, расчеты частот нормальных колебаний кластера ${\text{Al}}_{{89}}^{ - }$ и гидридов ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{n}^{ - }$ выходят за рамки возможностей нашего компьютера, поэтому мы ограничились оптимизацией их геометрии на уровне B3LYP с поляризованным базисом 6-31G* без ограничений по симметрии (С1) и повторной реоптимизацией умеренно деформированных структур, в которых атомы Al были смещены из равновесных позиций на 0.10–0.15 Å. В большинстве случаев результаты оптимизации и последующих реоптимизаций оказывались близкими, и мы полагаем, что оптимизированные структуры соответствуют локальным минимумам ППЭ. Как обычно, основное внимание уделяется тенденциям и относительным изменениям рассчитанных структурных и энергетических характеристик при изменении n. Оптимизированные структуры и характеристики рассмотренных систем приведены на рис. 1−4 и в табл. 1.
Рис. 1.
Оптимизированные структуры послойно гидрированных изомеров кластеров Al44Hn (n = 27–43).

Рис. 1.
Окончание.
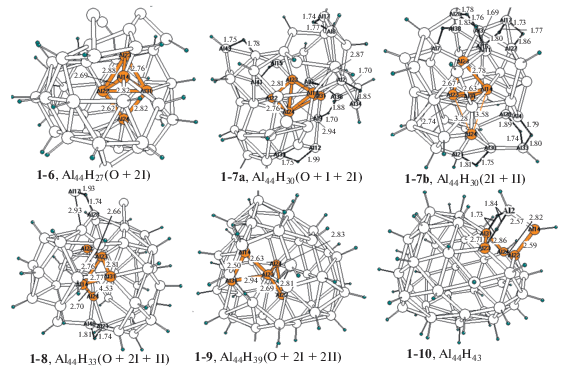
Таблица 1.
Рассчитанные энергетические характеристики послойно гидрированных изомеров кластеров Al44Hn (n = 6−43) в ккал/мольа
| Кластер, cтруктура | D(nH) | D(H) | ΔD | D | ||||
|---|---|---|---|---|---|---|---|---|
| HII | HI | HO | HII | HI | HO | |||
| Al44H6 (II) | 329 | 54.7 | 329 | 54.7 | ||||
| Al44H9 (O), (1-1a) Al44H9 (I), (1-1b) |
499 499 |
55.4 55.4 |
499 | 499 | 55.4 | 55.4 | ||
| Al44H12 (2II), | 663 | 55.3 | 334 | 55.6 | ||||
| Al44H15 (O+II), (1-2a) Al44H15 (I+II), (1-2b) |
817 824 |
54.5 54.9 |
318 325 |
498 495 |
53.0 54.2 |
54.2 55.0 |
||
| Al44H18 (O+I), (1-3a) Al44H18 (2I), (1-3b) |
993 1018 |
55.2 56.5 |
494 519 |
494 | 54.9 56.5 |
54.9 | ||
| Al44H21 (O+2II), (1-4a) Al44H21(I+2II), (4-4b) |
1165 1163 |
55.5 55.4 |
348 339 |
505 | 507 | 58.0 56.5 |
56.1 | 56.3 |
| Al44H24 (O+I+II), (1-5a1) Al44H24 (O+I+II), (1-5a2) |
1319 | 50.0 | 326 | 502 | 495 | 54.3 | 55.8 | 55.0 |
| Al44H24 (2I+II), (1-5b) | 1356 | 56.5 | 338 | 513 | 57.5 | 57.0 | ||
| Al44H27 (O+2I), (1-6) | 1467 | 54.3 | 474 | 449 | 52.7 | 50.0 | ||
| Al44H30 (O+I+2II), (1-7a) Al44H30 (2I+II), (1-7b) |
1652 1650 |
55.1 55.0 |
333 | 487 | 489 | 55.5 | 54.1 | 54.3 |
| Al44H33 (O+2I+II), (1-8b) | 1792 | 54.3 | 325 | 473 | 54.2 | 54.1 | ||
| Al44H39 (O+2I+2II), (1-9) | 2163 | 55.5 | ||||||
| Al44H43 (O+2I+2II), (1-10) | 2335 | 54.3 | ||||||
| Al44H44, (3-2) | 2403 | 54.6 | ||||||
а Расчеты в приближении B3LYP/6-31G* + ЭНК(B3LYP/6-31G). Оптимизированные структуры изомеров Al44Hn изображены на рис. 1.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
“Послойно” гидрированные кластеры Al44Hn с n = 27, 33, 39 и 43
Тенденция к нарастанию деформаций гидридов Al44Hn с увеличением n, отмеченная в [18], быстро усиливается в интервале с n = 24−43 и достигает апогея в конце серии. Если в первой половине серии каркас Al44 сохраняет замкнутую форму, то уже у изомера Al44H30 (1-8a) аксиальные атомы ядра Al(23) и Al(24) приближаются почти на 2 Å, а экваториальные атомы Al(14), Al(22) и Al(21), напротив, удаляются друг от друга, встраиваются в поверхностные позиции и становятся стерически открытыми для образования новых внешних связей Al−H (рис. 1). Кроме того, два фрагмента состава Al3H3 с координационно-ненасыщенными атомами Al отдаляются от поверхности на 0.15−0.20 Å, смещаясь во “внешнюю” сферу каркаса, и могут служить активными центрами на последующих стадиях глубокого гидрирования. В отличие от гидридов первой половины серии, у которых алюминиевый каркас в большинстве случаев покрыт двухцентровыми терминальными связями Al−H, у изомера Al44H30 (1-8a) поверхностный слой содержит десять трехцентровых водородных мостиков Al(i)−H−Al(j), в том числе 4 квазисимметричных и 6 несимметричных. У первых расстояния R(Al(i)−H) и R(Al(j)−H) близки (~1.75−1.78 Å), а у последних их разница лежит в интервале ~0.15−0.20 Å. У симметричных мостиков частоты продольных и поперечных колебаний атома водорода лежат в существенно отстоящих интервалах ~1500−1650 и ~750−810 см–1, а у несимметричных − в более близких интервалах ~1350−1450 и ~900−1050 см–1. У второго изомера Al44H30 (1-8b) сильнее всего деформированы области внешних слоев II+ и II–. В их надповерхностную сферу смещаются фрагменты Al2H2, Al2H и AlH. Ядро принимает форму изогнутой цепочки, у которой атомы Al(14) и Al(31) внедряются в поверхностный слой и тоже открыты для образования новых связей Al−H.
У гидрида Al44H33 cо структурой 1-9 атомы ядра Al(14) и Al(23) остаются во внутренней полости каркаса, а остальные (Al(22), Al(24) и Al(31)) встраиваются в поверхностный слой. Алюминиевый каркас приобретает пятиатомные “окна” и теряет закрытую форму. Атом Al(17) смещается из поверхностной позиции, приобретает большой положительный заряд и выполняет роль внешнесферного катиона. Аналогично, у изомера Al44H39 (1-10) биядерный фрагмент Al2H2 и несколько групп AlH смещаются во внешнюю сферу, в каркасе появляется несколько “окон”, частично закрытых атомами Н, расположенными над ними в шапочных позициях. Три атома ядра – Al(14), Al(22) и Al(31) – встроены в каркас и открыты для образования новых связей Al−H.
У гидрида Al44H43 (1-11) все пять атомов “бывшего” ядра выходят из внутренней полости. Четыре из них встраиваются в поверхность в виде согнутого ромба, а пятый Al(14) переходит в состав внешнесферного фрагмента Al2H2, соединенного с каркасом связью Al(14)−Al(31) и двумя внешними Н-мостиками. Опустевший каркас [Al42] имеет фуллереноподобную форму, в которой все атомы алюминия окружены двухцентровыми терминальными связями Al−Н.
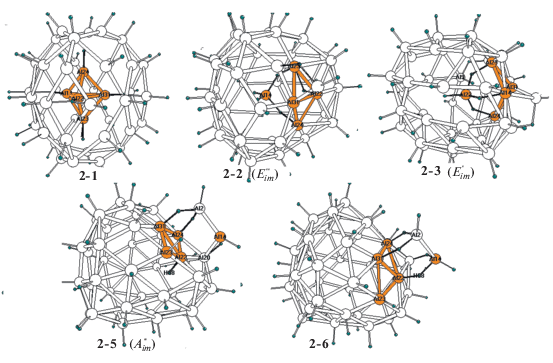
Изомеры кластера Al44H44
Равновесные структуры изомеров последнего члена серии Al44H44 рассчитывали с использованием стартовой симметричной структуры 2-1 (рис. 2) с гидрированным ядром [Al5H5] внутри оболочки [Al39Н39] после серии повторных оптимизаций с понижением симметрии до С1 и поправками на векторы смещений атомов, отвечающих мнимым частотам. На рис. 2 изображены структуры наиболее выгодных изомеров, имеющих только действительные значения колебательных частот. Как и Al44H43 (1-11), они имеют фуллереноподобный алюминиевый каркас с встроенными в него четырьмя атомами ядра в виде согнутого ромба. У экзоэдральных изомеров 2-4 и 2-5 имеется фрагмент Al2H2, вытесненный из поверхности во внешнюю сферу и связанный с поверхностью внешними Н-мостиками, а у эндоэдральных 2-2 и 2-3 во внутренней полости каркаса остаются лишь атом Al(14) и близкая к электронейтральной бидентатная или тридентатная группа AlH4, которая связана с поверхностными атомами Al внутренними Н-мостиками. Их мостиковые атомы Н имеют отрицательный заряд −0.22е. Внутренний мостик Al(22)−Hb−Al(23) с пятым эндоэдральным атомом H характеризуется длинами фрагментов ~1.76 и 1.79 Å и частотами ~1380 (Al(22)H) и 1090 см–1 (Al(23)H). Согласно расчетам, все четыре изомера лежат в пределах ~7 ккал/моль, остальные структуры менее выгодны и здесь не рассматриваются.
В структурах эндоэдральных (2-2 и 2-3) и экзоэдральных (2-2 и 2-3) изомеров внутренние связи Al−H и мостики Al−H−Al не сильно отличаются от своих внешних аналогов, расположенных на поверхности. Внутренние фрагменты слегка удлинены по сравнению с внешними, но отличия в их длинах не превышают 0.02 Å у терминальных и 0.04 Å у мостиковых связей, а различия в колебательных частотах составляют ~50−80 см–1. Изомеры 2-3 и 2-5 близки по энергии, а 2-4 лежит на ∼7 ккал/моль выше, чем 2-5.
Экзоэдральные и эндоэдральные фуллереноподобные изомеры AlnHm
На рис. 3 изображены структуры нескольких фуллереноподобных изомеров AlnHn с действительными колебательными частотами, которые были локализованы при серийных расчетах кластеров AlnHm. При оптимизации изомера Al39H39 (3-1) в качестве стартовой использовали эндоэдральную структуру одного из изомеров Al44H39, из которой удалены атомы внутреннего ядра [Al5]. Такую же структуру 3-1 получили в расчетах ионов ${\text{A}}{{{\text{l}}}_{{39}}}{\text{H}}_{{39}}^{ + }$ и ${\text{A}}{{{\text{l}}}_{{39}}}{\text{H}}_{{39}}^{ - }.$ При оптимизации изомера Al42H42 (3-2) в качестве стартовой выбрали экзоэдральную структуру Al44H44 (2-5), из которой удалена внешнесферная группа Al2H2. Согласно расчетам, обе клетки (3-1 и 3-2) имеют по два десятка деформационных частот <100 см–1 и напоминают эластичные и легко деформируемые сетки.
Рис. 3.
Структуры фуллереноподобных изомеров Al44H39 и Al44H42 с внешними и внутренними связями Al−H.
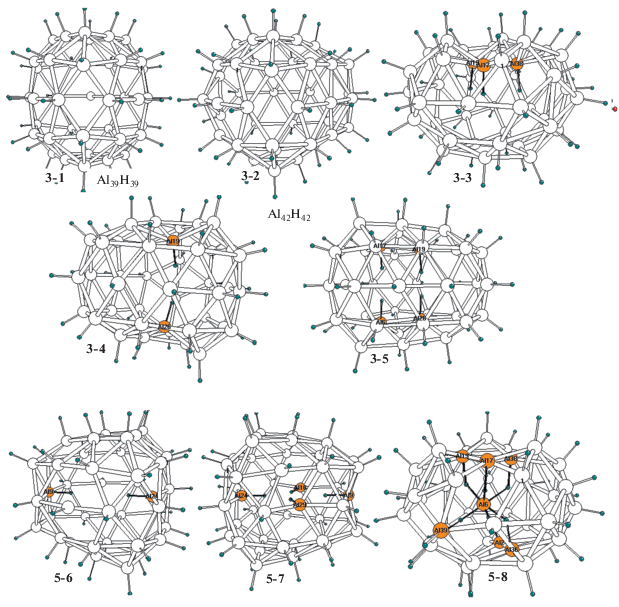
Помимо “нормальной” структуры 3-2, у которой полый алюминиевый каркас окружен внешними связями Al−H, на рис. 3 приведены структуры 3-3−3-8 “инвертированных” фуллереноподобных изомеров кластера Al42H42, имеющих только действительные значения колебательных частот и содержащих “внутренние” связи Al−H, водородные концы которых направлены к центру полого каркаса (ниже атомы внутренних связей обозначены звездочкой). У изомеров 3-3 и 3-4 имеются одна и три параллельные, а у 3-5 и 3-6 − две и четыре антипараллельные (“встречные”) связи Al*−H* при атомах алюминия, занимающих промежуточные позиции m внешних слоев II+ и II−. Изомеры 3-7 и 3-8 содержат две и четыре встречные связи Al*−H* при атомах алюминия экваториального слоя О.
Особенность инвертированных структур 3-3−3-8 (по сравнению с “правильной” 3-2) состоит в том, что их связи Al*−H* втянуты во внутреннюю полость вместе с атомами Al*, в результате чего рельеф отвечающего им участка поверхности каркаса Al42 приобретает характер вогнутых “впадин”, а при наличии нескольких соседних внутренних связей эти индивидуальные “впадины” сливаются в довольно глубокие и широкие “долины”. При этом, как и у изомеров Al44H44 (см. выше), отличия между внутренними и внешними связями не превышают 0.01–0.02 Å и нескольких десятков см–1 для расстояний R(AlH) и частот ν(AlH) соответственно. Подчеркнем, что, согласно расчетам, инвертированные изомеры энергетически более выгодны по сравнению с “правильным” 3-2. Так, изомеры 3-4, 3-5 и 3-6 лежат ниже, чем 3-2, на 28 и 20–22 ккал/моль, а у изомеров 3-5 и 3-6 разница уменьшается до 7.5 и 18 ккал/моль. Отметим еще, что оптимизация стартовой структурой с тремя парами встречных аксиальных связей Al*−H* приводит к образованию необычной структуры 3-7 (рис. 3), в которой атомы фрагмента ${\text{Al}}_{{(6)}}^{*} - {\text{H}}_{{(42)}}^{*}$ перемещаются во внутреннюю полость, а атом ${\text{Al}}_{{(6)}}^{*}$ занимает позицию в центре эндоэдрального октаэдра $[{\text{Al}}_{{(6)}}^{*}{{({\text{H}}*)}_{6}}]$ и связан с каркасом пятью внутренними асимметричными мостиками ${\text{Al}}_{{(6)}}^{*}$−${\text{H}}_{{\text{b}}}^{*}$−Al. Длины мостиковых фрагментов R(${\text{Al}}_{{(6)}}^{*} - {\text{H}}_{{\text{b}}}^{*}$) и R(${\text{H}}_{{\text{b}}}^{*}$−Al) лежат в интервалах 1.75−1.80 и 1.68−1.72 Å соответственно, а углы φ(${\text{Al}}_{{(6)}}^{*}$−${\text{H}}_{{\text{b}}}^{*}$−Al) − в интервале 125°−130°. Частоты валентных колебаний коротких фрагментов ${\text{Al}}_{{(6)}}^{*} - {\text{H}}_{j}^{*}$ лежат в интервале 1500−1750 см–1. Согласно расчетам, изомер 3-7 лежит почти на 68 ккал/моль ниже, чем 3-2, и оказывается самым выгодным среди инвертированных структур.
В заключение кратко остановимся на энергетических характеристиках гидридов Al44Hn, В табл. 1 помимо формулы кластеров указаны гидрированные внешний, промежуточный и экваториальный слои II, I и O. Энергии D(Al44Hn) образования кластеров по схеме Al 44 + nH → → Al44Hn рассчитаны по разности полных энергий продукта и реагентов с учетом энергий нулевых колебаний. В третьей колонке даны энергии ${{\bar {D}}_{n}}({\text{H}})$ связей Al−H, усредненные по полной совокупности атомов водорода (Dn(H) = 1/n D(Al44Hn)). В четвертой колонке приведены энергии D(II), D(I) и D(O) “послойного” гидрирования с присоединением шести атомов Н к внешнему слою и девяти атомов Н к промежуточному или экваториальному слою. В последующих колонках даны “послойные” энергии связей Al−H (D(HII) = 1/6 D(II), D(HI) = 1/9 D(I) и D(HO) = 1/9 D(O)), усредненные по совокупностям связанных атомов Н соответствующего заполненного слоя.
Из табл. 1 следует, что “полностью усредненные” энергии ${{\bar {D}}_{n}}({\text{H}})$ варьируются в пределах 55.5 ± ± 2.5 ккал/моль во всем интервале изменения n = = 2−39. Усредненные “послойные” энергии $\bar {D}({{{\text{H}}}_{{{\mathbf{II}}}}}),$ $\bar {D}({{{\text{H}}}_{{\mathbf{I}}}})$ и $\bar {D}({{{\text{H}}}_{{\mathbf{O}}}})$ также укладываются в тех же пределах, хотя у разных слоев они могут различаться на несколько ккал/моль в зависимости от присутствия других гидрированных слоев, их числа и положения. Энергии присоединения молекул Н2 по схеме Al 44Hn + H2 → Al44Hn+ 2 составляют ~3−8 ккал/моль, так что на полуколичественном уровне эти реакции можно полагать слабоэкзотермичными. Из-за вычислительных трудностей потенциальные барьеры реакций Al44Hn + H2 → Al44Hn+ 2 не рассчитывали, но поскольку барьер аналогичной простой реакции ${\text{Al}}_{{13}}^{ - }$ + H2 → ${\text{A}}{{{\text{l}}}_{{13}}}{\text{H}}_{2}^{ - },$ рассчитанный в [23, 24], составляет ~39 ккал/моль, можно полагать, что у более сложных алюмогидридов барьеры также останутся высокими и что кластеры Al44Hn могут существовать и быть экспериментально обнаружены в изолированном состоянии или в инертных матрицах.
Согласно расчетам, во второй половине серии Al44Hn однослойное бипирамидальное ядро Al5 оказывается малостабильным и при большом числе атомов Н может разрушаться с внедрением его атомов в поверхностную оболочку. Разрушение ядра сопровождается одновременным выходом нескольких атомов алюминия из поверхности и образованием внешнесферных валентно-ненасыщенных фрагментов типа AlHn и Al2Hn. Возникает вопрос, в какой степени эта картина сохранится или изменится у родственных кластеров с большим числом атомов алюминия во внутреннем ядре и на поверхности.
Послойно гидрированные кластеры Al89Hn
Кластер ${\text{Al}}_{{89}}^{ - }$, структура которого изображена в верхней части рис. 4, представляет собой горизонтально расширенную модификацию кластера Al44. Как и Al44, он имеет пятислойную структуру, но число атомов в его экваториальном (O), промежуточных (I) и внешних (II) слоях увеличивается до 27, 19 и 12 соответственно (в структуре 4-1а эти слои выделены красным, серым и желтым цветом). В кластере ${\text{Al}}_{{89}}^{ - }$ можно выделить двухслойное внутреннее “ядро”, состоящее из 26 атомов, пять из которых входят в состав центральной бипирамиды [Al5] (выделены синим цветом в структуре 4-1b), а остальные 21 образуют промежуточную (подповерхностную) оболочку [Al21] (выделены оранжевым цветом). Оптимизированные структуры послойно гидрированных производных Al89Hn с 15, 24, 39 и 63 атомами Н изображены в нижней части рис. 4.
Рис. 4.
Структуры кластера ${\text{Al}}_{{89}}^{ - }$ и гидридов ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{{24}}^{ - },$ Al89H29 и Al89H63.
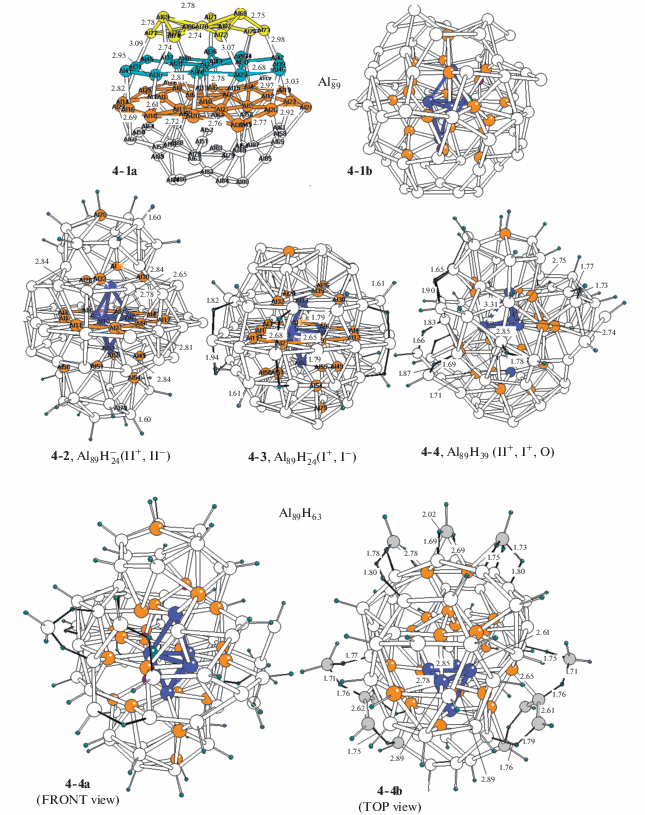
Из рис. 4 видно, что при присоединении 24 атомов Н к внешним слоям (структура ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{{24}}^{ - }$ (4-2)) оба слоя II+ и II− “надуваются” и приобретают форму купола с одновременным смещением нескольких атомов подповерхностной оболочки [Al21], которые встраиваются в граничные области, отделяющие куполы от центрального массива каркаса. При гидрировании промежуточных слоев I+ и I− (структура ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{{24}}^{ - }$ (9-3)) половина присоединившихся атомов Н образует терминальные связи Al−H, а другая половина включается в мостики AlI–Hb–AlO, связывающие промежуточные слои I с экваториальным O. Гидрирование экваториального слоя О сопровождается образованием девяти терминальных связей Al−H и шести мостиков AlО–Hb–AlO между соседними экваториальными атомами. Бипирамидальное ядро [Al5] деформируется слабо. Средние энергии связей DII(H), DI(H) и DO(H), рассчитанные по разностям полных энергий реагентов и продуктов реакций типа ${\text{Al}}_{{89}}^{ - }$ + 24H → ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{{24}}^{ - }$ и усредненные по числу атомов водорода во внешних, промежуточных и экваториальном слоях, лежат в интервале 53.5−57.0 ккал/моль. При послойном гидрировании наиболее предпочтительными оказываются позиции у внешних слоев II± и наименее выгодными – позиции у средних слоев I±. Энергии D(2H) присоединения пары атомов Н у всех трех структур лежат в интервале ~107−114 ккал/моль, что на ~4−10 ккал/моль больше энергии диссоциации свободной молекулы Н2.
При одновременном гидрировании соседних слоев II+, I+ и O помимо деформаций, отмеченных выше, у кластера Al89H39 (4-4) происходит распад бипирамидального ядра [Al5] → [Al4] + + Al(52). При этом аксиальный атом Al(52) смещается вдоль молекулярной оси и удаляется более чем на 1 Å от группы [Al4], которая принимает форму сильно искаженного тетраэдра. У кластера Al89H51, который получается из Al89H39 (4-4) при заполнении второго промежуточного слоя I−, начинаются серьезные перестройки поверхности в области между экваториальным и промежуточными слоями с появлением внешнесферных фрагментов AlHn и Al3Hn, а также с распадом ядра [Al5] → [Al4] + Al) и смещением атома Al(5) в экваториальной плоскости на ~1.4 Å.
Наиболее значительные деформации характерны для структур с несимметричным расположением атомов водорода. У симметрично гидрированной структуры ${\text{A}}{{{\text{l}}}_{{89}}}{\text{H}}_{{63}}^{ - }$ (4-5) ядро сохраняет бипирамидальную форму с умеренным сжатием и укорочением длины связей Al−Al на 0.10−0.15 Å по сравнению с их длинами в голом кластере ${\text{Al}}_{{89}}^{ - }$. При этом существенно возрастает число внешнесферных фрагментов AlН, AlH2 и Al3H2, связанных с поверхностью в основном водородными мостиками. Простейшие фрагменты AlН с их мостиками образуют пять координированных аланатных групп AlH4, три из которых пространственно разделены, а две связаны с трехъядерными фрагментами Al3H2. Как и в предыдущих случаях, атомы внешних слоев II± покрыты терминальными связями Al−H и выгибаются в виде полусфер с образованием шароподобных фрагментов, встроенных сверху и снизу в основной центральный блок. Группа атомов промежуточной оболочки Al21 встраивается в поверхностную оболочку кластера и может присоединять дополнительно еще восемь атомов водорода. Атомы экваториальной плоскости остаются в составе ядра и смещаются к центру кластера на умеренные 0.05−0.10 Å.
Хотя наше рассмотрение ограничивается изомерами “однослойных” кластеров AlmHn, в которых число атомов H не превышает числа атомов Al в поверхностных позициях, полученные результаты иллюстрируют большое разнообразие изомеров, структурных форм и сложных перегруппировок, характерных для этих нежестких систем, следовательно, работа может рассматриваться как первый шаг в DFT-моделировании гидридов наноразмерных алюминиевых кластеров на молекулярном уровне. При дальнейшем увеличении n, несомненно, будут найдены новые низколежащие изомеры с необычными структурами, дефектами и перегруппировками. Поиск критических значений n и конфигураций, соответствующих наиболее “драматическим” перегруппировкам, может быть важным для понимания механизмов реакций на стадиях более глубокого гидрирования.
Мы надеемся, что полученные результаты будут способствовать исследованиям ряда общих вопросов, включая а) деформации и последовательное разрушение гидрируемой поверхности с ростом n; б) ассоциации и организацию алановых фрагментов в надповерхностной области; в) миграцию и внедрение атомов подповерхностного слоя в поверхностную оболочку; г) роль многоатомных “окон” и родственных поверхностных дефектов в качестве “калиток” для миграции внешних атомов Н во внутреннюю область каркаса с образованием внутренних связей и мостиков и др. Нетривиальные фуллероидные структуры с внешними и внутренними связями могут представлять особый интерес для структурной химии алюмогидридов.
Список литературы
Orimo S., Nakamori Y., Eliseo J.R. et al. // Chem. Rev. 2007. V. 107. № 10. P. 4111.
Graetz J., Reilly J.J., Yartys V.A. et al. // J. Alloys Compd. 2011. V. 509S. P. 5517. https://doi.org/https://doi.org/ 10.1016/j.jallcom2010.11.115
Jeon K.-J., Moon H.R., Ruminski A.M. et al. // Nature Mat. 2011. V. 10. P. 286. https://doi.org/10.1038/NMAT2978
Francombe T.J. // Chem. Rev. 2012. V. 112. P. 2164.
Charkin O.P., Klimenko N.M., Charkin D.O. et al. // Faraday Discuss. 2003. V. 124. P. 215.
Andrews L., Wang X. // J. Phys. Chem. A. 2004. V. 2004. P. 4202.
Lai Q., Paskevicius M., Sheppard D.A. et al. // Chem. Sus. Chem. 2015. V. 8. P. 2789. https://doi.org/ https://doi.org/10.1002/cssc.201500231
Li X., Grubisich A., Stokes S.T. et al. // Science. 2007. V. 315. P. 356. https://doi.org/10126/science/1133767
Jung J., Han Y.-K. // J. Chem. Phys. 2006. V. 125. P. 064306.
Roach P.J., Reber A.C., Hoodwaed W.H. et al. // Proc. Natt. Acad. Sci. US. 2007. V. 104. № 37. P. 14565. https://doi.org/https://doi.org/10.1073/PNAS.07066113104
Li X., Grubistich A., Bowen K.H. et al. // J. Chem. Phys. 2010. V. 132. P. 241103. https://doi.org/ https://doi.org/10.1063/1.3458912
Kiran B., Kandalam A.K., Xu J. et al. // J. Chem. Phys. 2012. V. 137. № 13. P. 134303. https://doi.org/https://doi.org/ 10.1063/1.4754506
Zhang X., Wang H., Collins E. et al. // J. Chem. Phys. 2013. V. 138. P. 124303. https://doi.org/https://doi.org/10.1063/ 1.47962000
Wang H., Zhang X., Ko Y. et al. // J. Chem. Phys. 2014. V. 140. № 16. P. 164317. https://doi.org/https://doi.org/10.1063/ 1.4871884
Grubisic A., Li X., Stokes S.T. et al. // J. Am. Chem. Soc. 2007. V. 129. P. 5969.
Moc J. // Chem. Phys. Lett. 2008. V. 116. P. 466.
Goldberg A., Yarovsky I. // Phys. Rev. B. 2007. V. 75. P. 195403.
Henry D.J., Yarovsky I. // J. Phys Chem. A. 2009. V. 113. P. 2565.
Charkin O.P., Klimenko N.M., Charkin D.O. // Chem. Phys. 2019. V. 523. P. 112. https://doi.org// 10.1016/j.chemphys.2019.02.007
Charkin O.P., Klimenko N.M. // Russ. J. Inorg. Chem. 2018. V. 63. № 4. P. 479. [Чаркин О.П., Клименко Н.М. // Журн. неорган. химии. 2018. Т. 63. № 4. С. 448.]
Frisch M.J., Trucks G.W., Schlegel H.B. et al. Gaussian 09, Revision C.01. Gaussian, Inc., Wallingford CT, 2013.
Becke A.D. // J. Chem. Phys. 1993. V. 98. P. 5648.
Lee C., Yang W., Parr R.G. // Phys. Rev. 1988. V. 37B. P. 785.
Charkin O.P., Klimenko N.M. // Russ. J. Inorg. Chem. 2007. V. 53. № 12. P. 1925. [Чаркин О.П., Клименко Н.М. // Журн. неорган. химии. 2007. Т. 52. № 12. С. 2033.]
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии