Журнал неорганической химии, 2019, T. 64, № 6, стр. 594-602
Структура и газочувствительные свойства композиции WO3–Co3O4, полученной золь-гель методом
Ю. С. Гайдук 1, *, А. А. Савицкий 1, А. А. Хорт 2
1 Белорусский государственный университет
220030 Минск, пр-т Независимости, 4, Беларусь
2 Институт тепло- и массообмена им. А.В. Лыкова НАН Республики Беларусь
220072 Минск, ул. Петруся Бровки, 15, Беларусь
* E-mail: j_hajduk@bk.ru
Поступила в редакцию 24.09.2018
После доработки 25.12.2018
Принята к публикации 10.01.2018
Аннотация
Методами рентгенофазового анализа, ИК-спектроскопии, сканирующей электронной микроскопии и термогравиметрии, а также определением удельной поверхности по низкотемпературной адсорбции азота в интервале температур 200–800°С изучены структурно-фазовые особенности композиции WO3–Co3O4, полученной золь-гель методом. Обнаружено существенное возрастание газовой чувствительности композиции по сравнению с исходными оксидами. Установлен характер зависимости чувствительности к СO и NO2 от состава двухфазной композиции и предложено объяснение выявленной зависимости. Изготовлены маломощные полупроводниковые сенсоры, обеспечивающие определение низких концентраций диоксида азота (<1 ppm) с хорошими временами срабатывания и восстановления.
ВВЕДЕНИЕ
Интерес к изучению твердофазной системы WO3–Co3O4 вызван тем, что она является исходным материалом для получения ультра- и нанодисперсных карбидов вольфрама с кобальтовой связующей фазой, а также вольфрамата кобальта и сложных композиций на его основе, известных уникальными механическими, термическими, электрохимическими и электрокаталитическими свойствами [1–3]. Ранее уже были исследованы структура и физико-химические свойства композиции WO3–Co3O4, полученной по стандартной керамической технологии [4], гидротермальным методом [5] и методом распылительного пиролиза [6]. Разработаны методы синтеза нанопроволочных гетероструктур, представляющих собой нанопроволоки WO3 и WCoO4, декорированные наночастицами Co3O4 [7], нановолоконные структуры типа “ядро–оболочка” (ядро – нановолокна Co3O4) [8]. В то же время информация о физико-химических свойствах системы WO3–Co3O4, полученной золь-гель методом, отсутствует, не исследовано влияние добавки Со3О4 на газовую чувствительность оксида вольфрама, несмотря на то что газочувствительные свойства индивидуальных оксидов WO3 [9–11] и Co3O4 [12, 13] изучались неоднократно.
Образование оксидных композиций с различными активными добавками приводит к повышению чувствительности и селективности полупроводниковых датчиков. Изучается влияние добавок Pt, Pd, Au, Ag, обладающих высокой каталитической активностью при окислении восстановительных газов, на газоадсорбционную активность оксидов [14]. Кроме того, некоторые оксиды переходных металлов, например Co3O4 или CuO, также являются катализаторами окисления различных газов. Доказана связь между газочувствительными и каталитическими свойствами этих и некоторых других оксидов переходных металлов. Известно также, что Co3O4 и CuO обладают газочувствительными свойствами как полупроводники p-типа [15, 16]. В литературе есть работы по изучению активирующего действия Co3O4 на обнаружение СО сенсором на основе In2O3 [17]. Исследовались также газочувствительные свойства композиции SnO2–Co3O4 [17, 18].
Цель настоящей работы – изучение особенностей образования WO3, его композиций с оксидом кобальта Co3O4, полученных золь-гель методом (совместным отжигом ксерогелей оксидов вольфрама и кобальта), а также влияния температуры отжига на структурные, электрические и газочувствительные свойства композиции.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Оксид вольфрама WO3 получали из 1.23 М водного раствора Na2WO3 · 2H2O капельным введением в 12 М раствор азотной кислоты при постоянном перемешивании, выдержке его в течение 6 ч в маточном растворе и отмывании декантацией от примесей электролитов. Оксид кобальта Co3O4 получали аналогично из 2.3 М водных растворов CoSO4 · 7H2O путем добавления 9.24 М водного раствора аммиака. Наиболее полное осаждение Co(OH)2 происходило при pH 8–10. В интервале рН 10–12 наблюдалась минимальная растворимость гидроксида кобальта, которая при дальнейшем повышении pH резко возрастала. Выбранные условия осаждения Co(OH)2 соответствовали типичным условиям проведения золь-гель синтеза Co(OH)2 [19].
Образцы для физико-химических исследований готовили сушкой приготовленных ранее золей при комнатной температуре, последующим смешиванием образующихся ксерогелей в различных массовых соотношениях (1.0, 3.0, 5.0, 15.0, 25.0, 50.0 мас. % Co3O4) и термической обработкой полученных таким образом композиций в интервале температур 200–800°С в течение 2 ч на воздухе. Электрическое сопротивление в режиме нагревания и охлаждения измеряли цифровым мультиметром B7-40, температуру контролировали хромель-алюмелевой термопарой, закрепленной непосредственно вблизи образца.
Рентгеноструктурные исследования проводили на дифрактометре ДРОН-3 (CoKα-излучение) на порошках состава WO3–Co3O4 (5.0, 15.0, 25.0, 50.0 мас. % Co3O4). Размер кристаллитов (области когерентного рассеяния) определяли по дифрактограмме методом аппроксимации. Инфракрасные спектры образцов, высушенных при 20, 300 и 600°C, регистрировали на спектрометре Avatar 330 (Thermo Nicolet) в области волновых чисел (ν) 400–700 см–1 диффузным отражением с использованием приставки Smart Diffuse Reflectance. Порошки ксерогелей, высушенные при 20°С, исследовали на приборе синхронного термического анализа Netzsch STA 449C “Jupiter” в диапазоне температур 20–600°C на воздухе со скоростью нагревания 5 град/мин. Масса навесок составляла 2.47–2.92 мг. Изменение микроструктуры образцов исследовали с помощью сканирующего электронного микроскопа Leo 1420. Электрическое сопротивление образцов (таблеток) WO3, Co3O4, а также композиций оксида вольфрама с Co3O4 (1.0, 3.0, 5.0, 15.0, 25.0, 50.0 мас. %) в диапазоне 100–250°C измеряли двухэлектродным методом в корундовой ячейке, помещенной в трубчатую печь, соединенную с терморегулятором.
Образцы в виде таблеток (диаметр 10.0 мм, толщина 3.0 мм, масса 0.7–0.8 г) прессовали из предварительно отожженных порошков оксидов (400°С, 2 ч) с использованием органического связующего (канифоль) на гидравлическом прессе (давление 150 кПа) и спекали на воздухе при 450°C (5 ч). Для улучшения электрического контакта на обе стороны образца наносили серебряные электроды. Для изготовления двухэлектродных маломощных сенсоров слои WO3 и композиции WO3–Co3O4 осаждали на микропластины из анодированного алюминия (1.3 × 1.3 мм) с платиновыми электродами (фотолитография), которые затем отжигали на воздухе при 450°C в течение 12 ч.
Удельную поверхность порошков определяли методом низкотемпературной адсорбции азота на установке Клячко-Гурвича [20].
Сенсорный отклик (S, отн. ед.) определяли по формуле S = Ra/Rog, где Ra и Rog – электрическое сопротивление таблетки или сенсора на воздухе и при воздействии NO2 в качестве газа-окислителя, или S = Rrg/Ra, где Rа и Rrg − электрическое сопротивление на воздухе и при воздействии СО в качестве газа-восстановителя соответственно. Во всех случаях при исследовании газочувствительных свойств сенсоров использовали поверочные газовые смеси, содержащие диоксид азота (производство РУП “Белорусский государственный институт метрологии”) или оксид углерода (производство ОАО “Минский НИИ радиоматериалов”). Для исследования газовой чувствительности оксидов и оксидных композиций к диоксиду азота в виде газопроницаемых таблеток газовые смеси готовили согласно [21].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
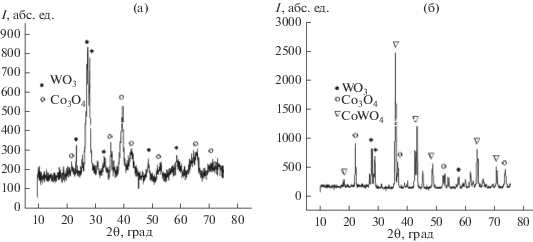
По данным РФА, воздушно-сухие образцы WO3–Co3O4 (20°С, 24 ч), содержащие 5.0, 15.0, 25.0 и 50.0 мас. % Co3O4, рентгеноаморфны. При отжиге в интервале температур 200–600°С композиция состояла из индивидуальных фаз WO3 и Co3O4. В процессе термообработки при 600–650°С (2 ч) происходила твердофазная реакция с образованием соединения CoWO4 (PDF15-867). В частности, при содержании в исходной смеси 15.0 мас. % Co3O4 в качестве второй фазы выступал WO3, а Co3O4 полностью вступал в реакцию [22].
Спектры РФА образцов после термообработки при 450°С не содержат рефлексов CoWO4 (рис. 1). Размер области когерентного рассеяния для образца WO3–Co3O4, содержащего 15.0 мас. % Co3O4 (отжиг при 450°С, 2 ч), составил ~50 нм, т.е. меньше, чем для образцов индивидуальных оксидов вольфрама (~100 нм) и кобальта (~200 нм), отожженных в аналогичных условиях. Это явление может быть связано с образованием в комплексных оксидных системах с различными структурами кристаллов с искаженными неровными гранями, что термодинамически затрудняет их рост [23]. Таким образом, совместный отжиг ксерогелей вольфрамовой кислоты и гидроксида кобальта приводит к замедлению роста зерен по сравнению с индивидуальными соединениями.
На рис. 2а–2в представлены ИК-спектры образцов композиции WO3–Co3O4, содержащей 15.0, 25.0 и 50.0 мас. % Co3O4. ИК-спектры подтверждают выводы, сделанные на основании РФА, об образовании в интервале температур 600–650°С соединения CoWO4. В спектрах образцов, термообработанных при 600°С, в области частот 500–600 см–1, где находятся характеристические полосы оксидов металлов, полосы пропускания Сo3O4 не зафиксированы. В то же время в спектре образца, термообработанного при 450°С, присутствуют два выраженных пика при 567 и 657 см–1, соответствующих колебаниям тетраэдрически координированных ионов Со2+ и октаэдрически координированных ионов Co3+ в Co3O4. Полосу поглощения вблизи 1000 см–1 можно отнести к колебаниям деформированных связей Со–О, W–O и W–O–W. Наиболее явно проявляется полоса поглощения при 500 см–1, отвечающая связям W–O в октаэдрах WO6. Полосы при 821 и 620 см–1 соответствуют валентным колебаниям О–W–O и W–O, полосы при 1635 и 3300 см–1 – колебаниям О–Н координационно связанных и физически адсорбированных молекул воды. Полученные ИК-спектры свидетельствуют о наличии в порошках обособленных фаз оксидов вольфрама и кобальта и согласуются с литературными данными по индивидуальным оксидам вольфрама и кобальта [22, 24–27].
Рис. 2.
ИК-спектры образцов WO3–Co3O4: а – 15.0 мас. % Co3O4, 600°C, 2 ч; б –25,0 мас. % Co3O4, 600°C, 2 ч; в – 50.0 мас. % Co3O4, 600°C, 2 ч; г – 15.0 мас. % Co3O4, 450°C, 2 ч.
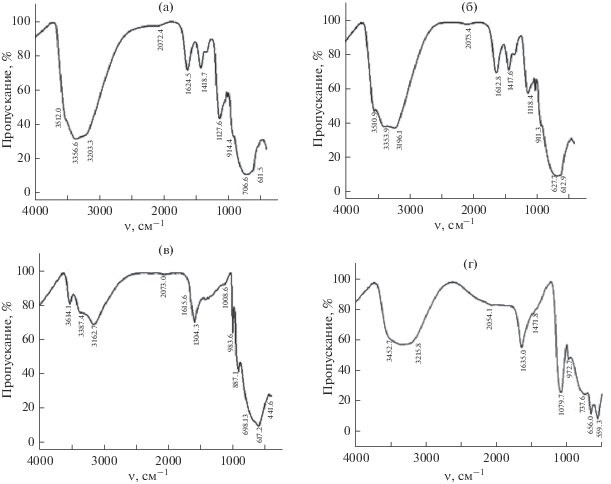
На рис. 2г представлен ИК-спектр образца композиции WO3–Со3O4, содержащего 15.0 мас. % Co3O4, прошедшего термообработку (2 ч) при 450°С. В области колебаний 900–3700 см–1, к которой относятся симметричные и асимметричные колебания О–Н координационно связанной воды, колебания О–Н в молекуле воды, а также W–OH2 и другие колебания, поглощение выражено сильнее, чем в соответствующих данным условиям отжига образцах индивидуальных оксидов вольфрама и кобальта (рис. 3в, 3г). Такой результат может быть получен в результате замедления дегидратации и кристаллизации оксидов вольфрама и кобальта в совместной композиции по сравнению с индивидуальными оксидами. Повышенная концентрация поверхностных OH-групп (кислотных центров по Бренстеду) может способствовать более высокой адсорбционной и каталитической способности композиции по сравнению с исходными оксидами, в частности, адсорбции и окислению газов восстановительной природы [28].
Рис. 3.
ИК-cпектры: а – WO3–Co3O4, 15.0 мас. % Co3O4, 450°C, 2 ч, после воздействия газовоздушной смеси, содержащей 3.6 ppm NO2 (t = 187°C, τ = 30 мин); б – CoWO4, синтез 650°С, 2 ч, после воздействия газовоздушной смеси, содержащей 3.6 ppm NO2 (t = 187°C, τ = 30 мин); в – WO3, 450°C, 2 ч; г – Co3O4, 450°С, 2 ч.
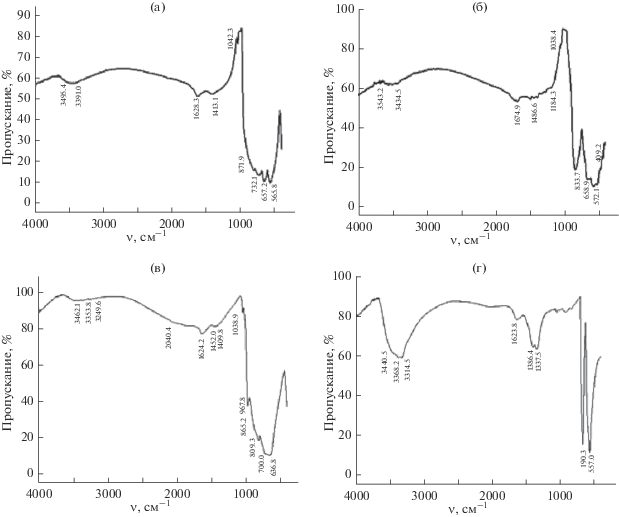
Образцы композиции WO3–Co3O4, обработанные в газовоздушной среде, содержащей NO2, демонстрируют более интенсивное поглощение в области частот 1100–1700 см–1 по сравнению с необработанными образцами. Поглощение в этой области объясняется поглощением различных адсорбированных форм диоксида азота. Так, в области 1500–1700 см–1 находится максимум поглощения NO2, в области 1250–1350 см–1 – максимум поглощения N2O. На рис. 3а приведен ИК-спектр образца композиции WO3–Co3O4 (15.0 мас. %).
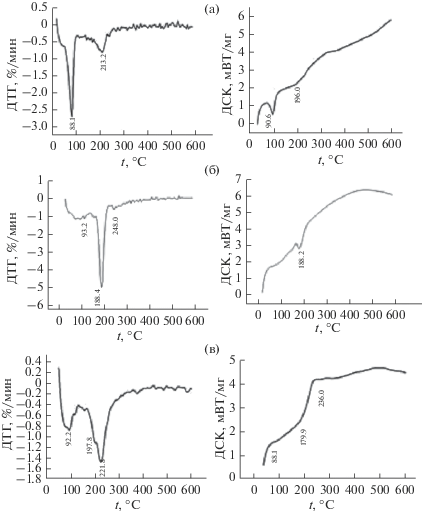
На рис. 4 представлены кривые ДТГ–ДТА термолиза ксерогелей композиции WO3–Co3O4 с содержанием 15.0 и 25.0 мас. % Co3O4. Удаление связанной воды начинается при ~50°С и завершается термодеструкцией вольфрамовой кислоты и гидроксида кобальта с образованием соответствующих оксидов при 270–280°С. На ДСК-кривой оксида вольфрама имеются два пика (при 90.6 и 196°С), соответствующих ступенчатой дегидратации вольфрамовой кислоты и переходу оловых связей в оксоловые. На кривых, соответствующих композиционному материалу, содержащему 15.0 мас. % Co3O4, указанные пики проявляются при 88.1 и 179.9°С соответственно. В композиции с содержанием Co3O4 25.0 мас. % первый пик отсутствует, а второй проявляется при температуре 179.9°С и перекрывается с пиком, характеризующим дегидратацию гидроксида кобальта (236°С для образца с содержанием 15.0 мас. % Co3O4).
Наблюдаемое при сравнении кривых ДТГ и ДТА, относящихся к индивидуальным оксидам вольфрама и кобальта и к композиции WO3–Co3O4, смещение пиков, отражающих процессы разложения гидроксидов, в сторону низких температур может указывать на увеличение дисперсности и структурной дефектности материала и (или) на изменение морфологии и поверхностного состояния частиц оксидов в совместной композиции. Сравнение указанных кривых позволяет также обнаружить различие в протекании процессов дегидратации в индивидуальных оксидах и в композиции. Тепловой эффект дегидратации образцов WO3–Co3O4 (15.0 и 25.0 мас. % Co3O4) ниже, чем индивидуального WO3. Полученные методом ТГ–ДТА результаты подтверждают данные ИК-спектроскопии, указывающие на зависимость количества адсорбированной воды от мольного соотношения оксидов (уменьшается с увеличением содержания Co3O4).
На рис. 5 представлены фазово-контрастные СЭМ-изображения оксидной композиции WO3–Co3O4, содержащей 15.0 мас. % Co3O4, после термической обработки на воздухе (2 ч) при 600°С. По сравнению с оксидом вольфрама, не содержащим добавки оксида кобальта, прошедшим термическую обработку в тех же условиях, порошок смешанной композиции характеризуется заметно меньшими размерами частиц и более развитой удельной поверхностью (0.2–0.3 мкм и 12.2–12.6 м2/г соответственно для смешанной композиции, 0.2–2.0 мкм и 2.9–3.5 м2/г для оксида вольфрама). Таким образом, рост частиц WO3 и Со3О4 при термической обработке в смешанной композиции замедляется по сравнению с индивидуальными оксидами, аналогичное явление наблюдалось при сопоставлении данных РФА по размерам областей когерентного рассеяния.
Образцы оксида вольфрама проявляли n-тип отклика к газовым смесям, содержащим СО, образцы оксида кобальта – p-тип отклика. Все смешанные образцы с содержанием оксида кобальта от 1.0 до 25.0 мас. % показали n-тип отклика к указанной газовой смеси, а образцы, содержащие 50.0 мас. % Co3O4, – p-тип отклика. Чувствительность композиции к СО заметно возрастала уже при небольшом содержании добавки Co3O4 и была максимальной при содержании добавки 5.0 мас. %. Как следует из рис. 6a, при увеличении рабочей температуры от 187 до 243°С величина сенсорного отклика увеличивается более чем вдвое.
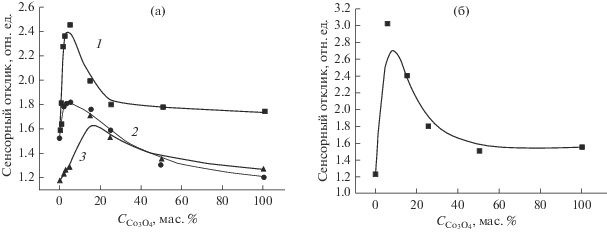
Рис. 6.
Сенсорный отклик образцов WO3–Co3O4 к газовоздушным смесям (время воздействия 10 мин): а – 3000 ppm CO/N2, 243°C (1); – 3000 ppm CO/возд., 243°C (2); – 3000 ppm CO/N2, 187°C (3), б – 1.1 ppm NO2/возд.
Наблюдаемое увеличение чувствительности к СО связано с каталитической активностью оксидов кобальта при окислении СО, H2 и углеводородов. Такая активность впервые была обнаружена японскими исследователями [10–12]. Авторы [12] объясняли исключительно высокую чувствительность композиции SnO2–Co3O4 к СО и H2 изменением окислительно-восстановительного состояния Co3O4.
Кроме того, для композиции WO3–Co3O4, как и для других смешанных оксидных систем, имеет место формирование p–n-гетеропереходов, наличие которых способствует активации диссоциации молекул газа. Предполагается, что в системах, содержащих оксидные полупроводники n- и p-типа, возможен частичный перенос электронов между оксидами, как это наблюдается на границе металл/оксид в оксидах, содержащих металлические наноразмерные кластеры [11]. При образовании гетероконтактов WO3–Co3O4 электроны проводимости из зерен WO3 переходят в зерна Co3O4. Этот процесс должен приводить к росту удельного электрического сопротивления композиции на воздухе, что и наблюдается в действительности. В газовоздушной среде, содержащей газы-восстановители (СО, H2), электрическое сопротивление Co3O4 снижается в большей степени, чем WO3, т.е. электроны проводимости возвращаются к Co3O4, что приводит к увеличению чувствительности сенсоров. Такой механизм действия добавки называется электронной сенсибилизацией [15]. Оптимальное количество добавки p-полупроводника в подобных случаях невелико и составляет несколько процентов, что и наблюдалось в нашем случае. При увеличении содержания добавки чувствительность снижалась, поскольку большое количество высокореактивных участков препятствует диффузии молекул газа в массивных образцах и толстопленочных чувствительных элементах. Таким образом, возрастание чувствительности композиции WO3–Co3O4 к восстановительным и окислительным газам при небольших концентрациях добавки Co3O4 происходит, по-видимому, за счет механизма электронной сенсибилизации, в котором помимо высокой реакционной способности Co3O4 к CO и NO2 важную роль играет электронное взаимодействие между оксидами вольфрама и кобальта.
В случае СО сенсибилизирующее действие Co3O4 заключается в протекании газоадсорбционных реакций, в которых происходит восстановление Co3O4 и разрыв p–n-переходов. Образование при отжиге бинарной композиции WO3–Co3O4 выше 600°С в значительном количестве соединения СоWO4 является причиной снижения эффективного количества Co3O4 и, следовательно, причиной падения газовой чувствительности.
Сенсорный отклик к СО при 242°С проходит через максимум вблизи 15.0–20.0 мас. % добавки (рис. 6а). Сенсорный отклик к NO2 при 187°С достигает максимума при содержании в композиции 5.0 мас. % Co3O4, затем монотонно снижается. При 187°С сенсорный отклик образца WO3 в виде газочувствительной таблетки к 1.1 ppm NO2 на воздухе составил S = 1.29, а отклик образца композиции WO3–Co3O4 (5.0 мас. % Co3O4) – S = = 3.03 (рис. 6б).
С применением композиции WO3–Co3O4 в ОАО “Минский НИИ радиоматериалов” были изготовлены маломощные двухэлектродные газовые сенсоры (подложки на основе Al2O3, 1.3 × 1.3 мм) [22, 29], которые обладают существенно более высокой чувствительностью к CO и NO2 по сравнению с сенсорами, содержащими в составе чувствительного элемента оксид вольфрама без добавки. Материалы на основе композиции WO3–Co3O4 обладают хорошей адгезией к Al2O3 и пригодны для изготовления чувствительных полупроводниковых сенсоров с рабочей температурой <200°С.
Газочувствительный слой сенсора из WO3 показал чувствительность к NO2 и СО S = 1.5 и 1.1 соответственно при токе нагрева 41 мА. Сенсоры с добавкой 5.0 мас. % Co3O4 показали более высокую чувствительность к СО и исключительно высокую чувствительность к 2.0 ppm NO2 (S ≤ 6), что позволило детектировать данный газ в ppb-диапазоне. При этом время достижения максимального сигнала и время восстановления не превышало 120 с, а потребляемая мощность сенсоров составляла 85 мВт (ток нагрева 31 мА).
Чувствительные элементы сенсоров на основе композиции WO3–Co3O4 отжигали при 400–600°С. Установлено, что отжиг при более высоких температурах приводит к образованию фазы СоWО4, которая практически не проводит электрический ток. Наличие фазы СоWО4 отрицательно сказывается на газовой чувствительности композиции, несмотря на сохранение высокой удельной поверхности материала.
С целью определения причин резкого падения газовой чувствительности в образцах композиции, отожженных при 650°С и содержащих фазу CoWO4, данное соединение было синтезировано в чистом виде отжигом при 650°С эквивалентной смеси гидроксидов (золей) вольфрама и кобальта. Заметного поглощения в области частот, сопоставляемой с колебаниями связей адсорбированного NO2, в спектре CoWO4 не наблюдается (рис. 3б), что подтверждает более низкую газоадсорбционную активность CoWO4 по сравнению с двухфазной композицией, содержащей WO3 и Со3О4. Вероятно, инертность CoWO4 в газоадсорбционных реакциях наряду с ростом средних размеров частиц в процессе отжига при 650°С по сравнению с отжигом при 450°С является основной причиной снижения газовой чувствительности.
Установлено, что соединение CoWO4, а также отожженные при температурах 650°С порошки композиции WO3–Co3O4, содержащие в качестве третьей фазы CoWO4, не обладают удовлетворительной адгезией к подложкам из поликора (Al2O3).
Удельная поверхность (отжиг 600°С, 2 ч) порошков WO3–Co3O4 заметно выше (10.0–11.0 м2/г для композиции, содержащей 15.0 мас. % Co3O4, 12.0–13.0 м2/г для композиции, содержащей 25.0 мас. % Co3O4), чем индивидуального WO3 (2.9–3.5 м2/г).
Таким образом, в системе WO3–Co3O4 наибольшая газовая чувствительность к CO наблюдается при содержании добавки Co3O4 5.0–15.0 мас. % (242°С), а к NO2 – при содержании добавки Co3O4 3.0–5.0 мас. % (187°С).
Механизм детектирования газов различной химической природы сенсорами на основе композиции WO3–Co3O4 можно связывать с частичным разделением рецепторной и преобразовательной функций сенсора между фазами WO3 и Co3O4, которые при температуре отжига 400–600°С сохраняются в неизменной форме. Увеличение чувствительности и снижение рабочей температуры происходят за счет структурного разупорядочения и снижения размеров кристаллитов в композициях по сравнению с исходными оксидами и увеличения удельной поверхности, а также, вероятно, за счет формирования p–n‑переходов, наличие которых предполагает расширение обедненной зоны на границе зерен [18]. Проведенное исследование не позволяет определить количественно вклад каждого из рассмотренных факторов (особенности микроструктуры, различие в удельной поверхности, дефектность кристаллов, наличие поверхностных ОH-групп и вероятное формирование p–n-переходов) в величину сенсорного отклика, однако в литературе имеется предположение о более значительной роли дефектности кристаллов и состояния поверхности (наличие поверхностных ОН-групп) по сравнению с другими факторами [29].
ЗАКЛЮЧЕНИЕ
Добавка к оксиду вольфрама 3–20 мас. % Co3O4 приводит к заметному увеличению газочувствительности по сравнению с таковой для индивидуального WO3, в частности, к 3000 ppm СO в воздухе и в азоте. Композиция WO3–Co3O4 обладает хорошей адгезией к анодированному оксиду алюминия и пригодна для изготовления чувствительных элементов полупроводниковых газовых сенсоров.
Установлена возможность получения стабильной микроструктуры в наногетерогенных композициях WO3–Co3O4. Рост размера зерен WO3 и Co3O4 при термической обработке при 450°С в смешанной композиции замедляется по сравнению с индивидуальными оксидами при всех исследованных методом РФА соотношениях оксидов (5, 15, 25, 50 мас. % Co3O4). Установлено, что образование CoWO4 в качестве третьей фазы нарушает электронное взаимодействие между оксидом вольфрама и оксидом кобальта и подавляет газоадсорбционную активность (чувствительность к СО, CH4, NO2) оксидной композиции WO3–Co3O4.
Высокая газовая чувствительность (S ≤ 6 к 2 ppm NO2 в воздухе) оксидной композиции WO3–Co3O4, полученной золь-гель методом, позволяет изготавливать сенсоры NO2 с низким порогом чувствительности (<1.0 ppm), рабочей температурой <200°С и удовлетворительным временем срабатывания и восстановления [30].
Список литературы
Feizpoor S., Habibi-Yangjeh A. // J. Colloid Interface Sci. 2018. V. 524. https://doi.org/10.1016/j.jcis.2018.03.069
Андреев И.В., Бондаренко В.П., Савчук И.В. и др. // Породоразрушающий и металлообрабатывающий инструмент – техника и технология его изготовления и применения: Сб. науч. тр. Киев: ІНМ им. В.М. Бакуля НАН Украины, 2009. Вып. 12. С. 389.
Li Y., Li X., Wang J. et al. // RSC Advantes. 2017. V. 7. № 5. P. 2919.
Pullar R.C., Alford N.M., Farrah S. // J. Eur. Ceram. Soc. 2007. V. 27. № 2–3. P. 1059. https://doi.org/10.1016/j.jeurceramsoc.2006.05.085
Song Xu Ch., Yang E., Ma R., Chao Y. // J. Nanopart. Res. 2008. V. 10. № 4. P. 709.
Gang-qin Sh., Jing-kun G., Ji-ren X. et al. // J. Wuhan University of Technology – Mater. Sci. 2004. V. 19. № 2. P. 1. https://doi.org/10.1007/BF03000154
Li Y., Chopra N. // J. Catal. 2015. V. 329. P. 514. https://doi.org/10.1016/j.jcat.2015.06.015
Chopra N., Li Y., Kumar K. // Symp. K/RR – Synthesis, Char. Appl. Fun. Mat. – Thin Films Nanostr. 2014. V. 1675. P. 191. https://doi.org/10.1557/opl.2014.863
Rhushikesh G., Vedpathak A., Godbole V., Bhagwat S. // Mater. Res. Express. 2017. V. 4. № 7. P. 076401. https://doi.org/10.1088/2053-1591/aa72a8
Hu L., Hu P., Chen Y. et al. // Front. Chem. V. 6. P. 452. https://doi.org/10.3389/fchem.2018.00452
Shimizu Y., Matsunaga N., Hyodo T., Egashira M. // Sens. Actuators, B. 2001. V. 77. P. 35. https://doi.org/10.1016/S0925-4005(01)00669-4
Wöllenstain J., Burgmair M., Plescher G. et al. // Sens. Actuators. B. 2003. V. 93. P. 442. https://doi.org/10.1016/S0925-4005(03)00168-0
Xu J.M., Cheng J.P. // J. Alloys and Compounds. 2016. V. 686. P. 753.
Yamazoe N., Kurokawa Y., Seiyama T. // Sens. Actuators, B. 1983. V. 4. P. 283.
Choi J.-S., Sakai Go, Shimano K., Yamazoe N. // Sens. Actuators, B. 2004. V. 98. P. 166. https://doi.org/10.1016/ j.snb.2003.09.033
Maekawa T., Tamaki J., Miura N., Yamazou N. // Chem. Lett. 1991. V. 20. № 4. P. 575.
Yamaura H., Tamaki J., Moriya K. et al. // J. Electrochem. Soc. 1977. V. 144. P. L158.
Choi J.-S., Sakai Go, Shimano K., Yamazoe N. // Sens. Actuators, B. 2005. V. 107. № 1. P. 397. https://doi.org/10.1016/ j.snb.2004.10.033
Пятницкий И.В. Аналитическая химия кобальта. М., 1965. 256 с.
Клячко-Гурвич А.Л. // Изв. АН СССР. Сер. хим. наук. 1961. № 10. С. 1884.
Кричмар С.И., Безпальченко В.М., Мишекин А.А. // Заводская лаборатория. Диагностика материалов. 2008. Т. 74. № 1. С. 21.
Гайдук Ю.С., Ломоносов В.А., Савицкий А.А. // Изв. НАН Беларуси. Сер. хим. 2014. № 2. С. 9.
Kang Suk-Jong L. Sintering: densification, grain growth and microstructure. Elsevier Butterworth-Heinemann, 2005. 266 p.
Kumar V.Bh., Mochanta D. // Bull. Mater. Sci. 2011. V. 34. № 3. P. 435.
Noguera H., Cavalerio A., Rocha J. et al. // Mater. Res. Bull. 2004. V. 39. P. 683. https://doi.org/10.1016/j.materresbull.2003.11.004
Sharifi S.L., Shakur H.R., Mirzaei A., Hosseini M.H. // Int. J. Nanosci. Nanotechnol. 2013. V. 9. № 1. P. 51.
Salavati-Niasari M., Mir N., Davar F. // J. Phys. Chem. Solids. 2009. V. 70. № 5. P. 847. https://doi.org/10.1016/ j.ica.2009.07.023
Liu Y., Ma X., Wang Sh., Gong J. // Appl. Catal., B. 2007. V. 77. P. 125. https://doi.org/10.1016/j.apcatb.2007.07.011
Пронин И.А., Аверин И.А., Александрова О.А., Мошников В.А. // Датчики и системы. 2013. № 3. С. 13.
Гайдук Ю.С., Таратын И.А. Сенсор диоксида азота: заявл. на изобр. Респ. Беларусь, МПК G01N 27/407; заявитель ОАО “Минский НИИ радиоматериалов”. № а 20140371; заявл. 08.07.2014; опубл. 28.02.2016 // Афiцыйны бюл. / Нац. цэнтр iнтэлектуал. уласнасцi. 2016. № 1. С. 44.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии