Журнал неорганической химии, 2019, T. 64, № 6, стр. 643-645
Оптические спектры ионов Gd(III) в расплавленных фторидах щелочных металлов
А. А. Хохряков 1, *, А. С. Пайвин 1, М. А. Самойлова 1
1 Институт металлургии УрО РАН
620016 Екатеринбург, ул. Амундсена, 101, Россия
* E-mail: 9221717036@mail.ru
Поступила в редакцию 02.08.2018
После доработки 12.10.2018
Принята к публикации 14.11.2018
Аннотация
Приведены оптические спектры расплавленных систем МF–GdF3 (M = Li, Na, K, Cs) и NaF–CsF–GdF3. На основании спектральных данных установлено, что в этих расплавах образуются устойчивые комплексные группировки ${\text{GdF}}_{{\text{6}}}^{{{\text{3-}}}}{\text{.}}$ В расплавленной системе LiF–GdF3 наряду с комплексной группировкой ${\text{GdF}}_{{\text{6}}}^{{{\text{3-}}}}$ обнаружена группировка ${\text{GdF}}_{{\text{4}}}^{{\text{-}}}{\text{,}}$ распадающаяся со временем. Высказано предположение, что число катионов во второй координационной сфере группировок ${\text{GdF}}_{{\text{6}}}^{{{\text{3-}}}}$ уменьшается при переходе от расплава LiF, NaF к KF, CsF c 14 до 13.
ВВЕДЕНИЕ
Оптические спектры Gd(III) хорошо известны в низкотемпературных средах, таких как водные растворы [1–3], нитраты, перхлораты, расплавы хлоридов щелочных металлов [4, 5]. Значительные сложности возникают при регистрации спектров ионов гадолиния в высокотемпературных и химически агрессивных фторидных расплавах. В настоящей работе методом отражательно-абсорбционной электронной спектроскопии получены спектры ионов Gd(III) в индивидуальных расплавленных фторидах и в эвтектике NaF–CsF.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Спектры фторидных расплавов, содержащих ионы гадолиния, регистрировали на спектрально-аналитическом комплексе производства ООО “СОЛ-инструмент” (Минск) в диапазоне 42 000–6050 см–1 с разрешением ~1 нм. Методы регистрации спектров высокотемпературных расплавов, синтез фторидных соединений РЗЭ, подготовка солей фторидов щелочных металлов подробно изложены в работах [6, 7].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рис. 1 приведены оптические спектры ионов Gd(III) в расплавленных фторидах щелочных металлов. Сложные по профилю спектральные полосы разложены на гауссовы компоненты с помощью программы Origin 8.1. Разложение возможно только для литиевых и натриевых расплавов. В остальных системах разложение невозможно из-за низкой интенсивности полос поглощения ионов гадолиния в диапазоне (36–42) × × 10–3 см–1. На спектрограммах наблюдаются характерные для ионов Gd(III) электронные переходы с основного состояния 8S на три различные мультиплетные группы: 6P, 6I, 6D [1, 2], которые не расщепляются в поле лигандов. Наиболее интенсивной полосой поглощения во всех фторидных расплавах является полоса, связанная с электронным переходом 8S → 6P. В работе [8] методом спектроскопии КР установлено, что координационные числа (КЧ) ионов РЗЭ в расплавленном фториде калия постоянны для всего лантанидного ряда и равны 6, т.е. проявляется изовалентный изоморфизм. Это позволяет отнести полосы поглощения к комплексным группировкам ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}{\text{.}}$ Такое отнесение подкрепляется общей тенденцией комплексообразования ионов легких лантанидов в расплавленных фторидах щелочных металлов, изученных ранее [7, 9]. Квантово-химическое моделирование комплексов ${\text{LnF}}_{{\text{6}}}^{{{\text{3--}}}}$ выполнено в работах [9–14], где были рассчитаны структурные, энергетические и электронные характеристики [10–12]. Необходимо отметить отличие оптических спектров расплава LiF–GdF3 от спектров фторидных систем, содержащих ионы легких РЗЭ. Интегральная интенсивность полос поглощения ионов гадолиния в этом расплаве уменьшается со временем и стабилизируется в течение 1 ч. Из диаграмм состояния систем MF–LnF3 известно, что в них образуются соединения состава M3LnF6, которые плавятся конгруэнтно, тогда как соединения состава MLnF4 плавятся с разложением [15, 16]. Это позволяет предположить, что в расплавах LiF–GdF3 присутствуют комплексные группировки двух типов: ${\text{GdF}}_{{\text{4}}}^{{\text{--}}}$ и ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}{\text{.}}$ Спектр поглощения расплава LiF–GdF3, измеренный сразу после плавления, разлагается на несколько гауссовых компонент, часть из которых имеет сильный батохромный сдвиг по отношению к гауссовым компонентам устойчивой спектрограммы (табл. 1). Такой сдвиг возможен при условии увеличения ковалентности связи Gd–F, связанного с понижением КЧ ионов Gd(III). Это позволило отнести полосы поглощения с центрами тяжести 29 630, 35 520, 38 970 см–1 к группировке ${\text{GdF}}_{{\text{4}}}^{{\text{--}}}{\text{.}}$ Данная группировка неустойчива, и снижение концентрации гадолиния связано с высоким давлением пара GdF3, образующегося при ее распаде.
Рис. 1.
Электронные спектры поглощения ионов Gd(III) в расплавленных фторидах щелочных металлов. Расплавы: LiF–[GdF3] = 0.9 мол. %, 1 – без выдержки, 2 – выдержка расплава >1 ч; NaF–[GdF3] = = 1.4 мол. %; KF–[GdF3] = 2 мол. %; CsF–[GdF3] = = 5 мол. %; эвтектическая смесь NaF–CsF–[GdF3] = = 3.9 мол. %, Т = 1273 K.
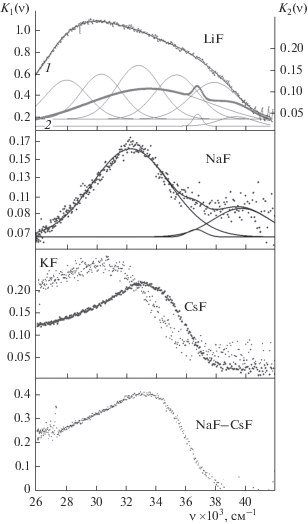
Таблица 1.
Положение полос поглощения ионов Gd(III) в расплавленных фторидах щелочных металлов
| Расплав | 6P3/2, см–1 | 6I7/2, см–1 | 6D7/2, см–1 | Группи-ровка |
|---|---|---|---|---|
| LiF(1) | 29 630 | 35 520 | 38 970 | [GdF4]– |
| 33 800 | 37 168 | – | [GdF6]3– | |
| LiF(2) | 33 591 | 36 821 | 39 391 | [GdF6]3– |
| NaF | 32 345 | 36 693 | 39 727 | [GdF6]3– |
| KF | 32 490 | – | – | [GdF6]3– |
| CsF | 32 169 | – | – | [GdF6]3– |
| NaF–CsF | 31 190 | – | – | [GdF6]3– |
Неустойчивость соединений LiLnF4 подтверждается их низкой энергией диссоциации по отношению к другим соединениям MLnF4 (M = Na, K, Cs) [17–19].
Следует отметить, что изменение центра тяжести полосы поглощения 8S → 6P происходит последовательно в парах расплавов LiF, NaF и KF, CsF. Скачок наблюдается при переходе от расплава NaF к KF. Сравнение спектров расплавов, содержащих ионы гадолиния, со спектрами легких лантанидов позволило связать скачок центра тяжести электронных переходов с изменением состава второй координационной сферы [8]. Одинаковые изменения спектральных характеристик дают возможность приписать для группировок ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}$ те же значения для состава второй координационной сферы, которые ранее были установлены для ионов легких лантанидов. Для литиевых и натриевых расплавов КЧ = 14, а для калиевых и цезиевых –13.
Сдвиг в парах расплавов LiF, NaF и KF, CsF центра тяжести в область более низких значений волновых чисел связан с увеличением ковалентности связей в группировках ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}$ (нефелоксетический эффект).
Наибольшую интенсивность и наименьшее значение волновых чисел полоса поглощения электронного перехода 8S → 6P имеет в расплаве NaF–CsF. В этом расплаве ионы легких лантанидов формируют полиэдры, близкие по симметрии к Oh. [9]. Отметим, что изменение интенсивности полос поглощения ионов Gd(III) в расплавленных фторидах щелочных металлов указывает на зависимость спектральных характеристик от симметрии группировок ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}{\text{.}}$ Наименьшую деформацию геометрия группировок ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}$ испытывает в эвтектике NaF–CsF.
ЗАКЛЮЧЕНИЕ
Ионы Gd(III) образуют в расплавленных фторидах щелочных металлов устойчивые группировки ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}{\text{.}}$ Центры тяжести полос поглощения этих группировок смещаются в область более низких волновых чисел в следующем порядке LiF → NaF и KF → CsF. Это указывает на увеличение в каждой паре растворителей ковалентности связей Gd–F. Высказано предположение, что число катионов второй координационной сферы в группировках ${\text{GdF}}_{{\text{6}}}^{{{\text{3--}}}}$ уменьшается при переходе от расплавов LiF, NaF к KF, CsF с 14 до 13 [8].
Список литературы
Carnall W.T., Fields P.R., Rajnak K. // J. Chem. Phys. 1968. V. 49. № 10. P. 4412. https://doi.org/10.1063/1.1669892
Carnall W.T., Fields P.R., Rajnak K. // J. Chem. Phys. 1968. V. 49. № 10. P. 4443. https://doi.org/10.1063/1.1669893
Banks C.V., Klingman D.W. // Analyt. Chim. Acta. 1956. V. 15. P. 356.
Смит Г.А. Электронные спектры поглощения расплавленных солей / Под ред. Укше Е.А. М.: Мир, 1966.
Angervaks A.E., Shcheulin A.S., Ryskin A.I. et al. // Inorg. Mater. 2014. V. 50. P. 733. https://doi.org/10.1134/ S0020168514070024
Хохряков А.А., Пайвин А.С., Норицын С.И. // Расплавы. 2014. Т. 1. С. 62.
Хохряков А.А., Вершинин А.О., Пайвин А.С., Шишкин В.Ю. // Расплавы. 2017. Т. 2. С. 175.
Photiadis G.M., Brresen B., Papatheodorou G.N. // J. Chem. Soc., Faraday Trans. 1998. V. 94. № 17. P. 2605. https://doi.org/10.1039/a802813c
Хохряков А.А., Вершинин А.О., Пайвин А.С. и др. // Расплавы. 2017. № 3. С. 226.
Gutowski M., Boldyrev A.I., Simons J. et al. // J. Am. Chem. Soc. 1996. V. 118. P. 1173. doi https://doi.org/10.1021/ ja952412r
Buz'Ko V.Y., Chuiko G.Y., Kushkhov K.B // Russ. J. Inorg. Chem. 2012. Т. 57. № 12. С. 1588. doi 10.1134/ S0036023612120066 [Бузько В.Ю., Чуйко Г.Ю., Кушхов Х.Б. // Журн. неорган. химии. 2012. Т. 57. № 12. С. 1687.]
Groen P., Oskam A., Kovács A. // J. Mol. Struct. (Theochem.). 2000. V. 531. P. 23. https://doi.org/10.1016/S0166-1280(00)00393-6
Takeda K., Tsuchiya T., Nakano H. et al. // J. Mol. Struct. (Theochem.). 2001. № 537. P.107. doi.org/ https://doi.org/10.1016/S0166-1280(00)00667-9
Delpech S., Merle-Lucotte E., Heuer D. et al. // J. Fluor. Chem. 2009. V. 130. № 1. P. 11. https://doi.org/10.1016/ j.jfluchem.2008.07.009
Координационная химия редкоземельных элементов / Под ред. Синицына В.И., Мартыненко Л.И. М., 1979. С. 254.
Thoma R.E. // Prog. Sci. Technol. Rare Earths. 1966. V. 2. P. 90.
Groen C.P., Kovacs A., Varga Z., Hargittai M. // Inorg. Chem. 2012. V. 51. P. 543. https://doi.org/10.1021/ic202009v
Groen C.P., Oskam A., Kovacs A. // Inorg. Chem. 2000. V. 39. P. 6001. https://doi.org/10.1021/ic000581t
Groen C.P., Oskam A., Kovacs A. // Inorg. Chem. 2003. V. 42. № 3. P. 851. https://doi.org/10.1021/ic0260973
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


