Журнал неорганической химии, 2019, T. 64, № 3, стр. 251-259
Кристаллохимические особенности и сорбционные свойства природных и синтетических смектитов
Н. А. Пальчик 1, *, Л. И. Разворотнева 1, Т. Н. Мороз 1, Л. В. Мирошниченко 1
1 Институт геологии и минералогии им. В.С. Соболева СО РАН
630090 Новосибирск, пр-т Академика Коптюга, 3, Россия
* E-mail: nadezhda@igm.nsc.ru
Поступила в редакцию 30.05.2018
После доработки 15.08.2018
Принята к публикации 26.07.2018
Аннотация
Методами рентгенографии, ИК-спектроскопии и масс-спектрометрии с индуктивно-связанной плазмой высокого разрешения изучена сорбция уранил-ионов из растворов уранилнитрата UO2(NO3)2 · 6H2O природными и синтетическими слоистыми силикатами. Изменения некоторых структурных параметров исследуемых объектов после взаимодействия с уранил-ионами обусловлены частичным внедрением уранила в межслоевое пространство структуры смектита или разворотом тетраэдров тетраэдрической сетки и деформацией октаэдров в октаэдрическом слое. Наилучшими сорбционными показателями обладают образцы природных глин со дна Тихого океана и Охотского моря. Это связано с дефектами структуры и образованием комплексов урана с ионами железа, входящими в структуру смектитов. Присутствие железа в глинистых минералах повышает их сорбционный потенциал.
ВВЕДЕНИЕ
Для предотвращения неконтролируемой миграции радионуклидов в окружающей среде используют природные геохимические барьеры [1], для создания которых чаще всего применяются наиболее распространенные в природе глинистые минералы (смектиты, каолинит, иллиты и др.) и торф. Высокой сорбционной активностью обладают также слоистые марганцевые минералы, в огромных количествах присутствующие на дне океанов, морей и озер. Как правило, эти материалы находятся в форме гидроксидов низкой степени кристалличности с множеством дефектов, позволяющих эффективно связывать элементы из морской воды (до трех четвертых всех известных элементов) [2, 3]. Смектиты – группа глинистых минералов, обладающих способностью к сорбции, ионному обмену, а также к набуханию при внутрикристаллическом внедрении органических молекул. Характер этих взаимодействий определяется природой поверхности смектитов, которая, в свою очередь, обусловлена условиями их кристаллизации, составом и кристаллическим строением силикатных слоев [4]. Наиболее устойчивый компонент структуры смектитов представлен двумя кремнекислородными тетраэдрическими сетками, соединенными между собой октаэдрической сеткой. Все вершины тетраэдров каждого слоя повернуты к центру октаэдрического слоя. Характерной особенностью этих минералов является возможность изоморфных замещений практически по всем кристаллографическим позициям. Так, в высокожелезистых смектитах, нонтронитах, присутствует трех- и двухвалентное железо в тетраэдрических и октаэдрических позициях соответственно. Такие замещения являются нестехиометрическими и создают в слое дефицит положительных зарядов, компенсируемый межслоевыми катионами. Величина слоевого заряда и его локализация в октаэдрической и/или тетраэдрических сетках определяют характер взаимодействия между слоями и, соответственно, ионообменные и сорбционные свойства минералов, зависящие также и от свойств катионов в межслоевом пространстве: их размера, заряда, координационного числа, строения внешних электронных оболочек и т.д. [5].
Благодаря лабильности кристаллической структуры смектиты широко используются для создания эффективных барьеров при угрозе загрязнения окружающей среды радионуклидами, которые связываются и долговременно удерживаются либо в межслоевом пространстве, либо на поверхности минералов [1, 6, 7]. Поверхностные реакции смектитов играют существенную роль в биогеохимических и экологических процессах в почвах, водах, используются в индустриальных технологиях, в клинической практике, для утилизации отходов и т.п. Известно, что сорбция урана глинистыми минералами происходит главным образом за счет ионного обмена между алюмосиликатной матрицей и растворимыми формами урана [8].
Цель работы – исследование сорбционных свойств и структурных преобразований природных смектитов разного генезиса, состава и степени кристалличности, а также синтетических литийсодержащих слоистых силикатов при взаимодействии с уранил-ионом ${\text{UO}}_{2}^{{2 + }}$ из азотнокислых водных растворов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектами исследования служили образцы минералов группы смектита (Ge99-43), поднятые со дна Охотского моря в районе Курильской островной дуги и имевшие явные признаки поствулканических гидротермальных изменений [9, 10], а также образцы, поднятые со дна Тихого океана в районе выхода рудоносных гидротерм в пределах осевой рифтовой долины Хуан-де-Фука (образец 930/10). Эти образцы представляют собой высокожелезистые нонтрониты, в структуре которых практически во всех октаэдрических позициях Mg2+ и/или Al3+ замещены на Fe3+, изредка на Fe2+, а в тетраэдрических сетках Si4+ частично замещен на Fe3+ (табл. 1) [11]. Отметим, что богатые Fe смектиты широко распространены в почвах и связаны с “судьбой” и подвижностью опасных следовых количеств металлов, в частности, с изменениями биогеохимических окислительно-восстановительных реакций структурного Fe, определяющих сорбционные и десорбционные свойства глинистых минералов [12]. Синтетические образцы представлены литийсодержащими фтористыми соединениями, полученными в автоклавах при различных температуре и давлении. Авторами [13] было показано, что в смектитах даже при частичном внедрении лития в позиции катионов межслоевого пространства и/или октаэдров изменяется отрицательный заряд основного слоя, что сопровождается изменением свойств минерала (например, проявлением гидрофобных свойств) и отражается на механизме сорбции катионов в межслоевом пространстве.
Таблица 1.
Химический состав природных и синтетических слоистых силикатов по результатам микрозондового анализа и атомно-абсорбционной спектрометрии, %
| Образец | SiO2 | Al2O3 | MgO | CaO | FeO | Na2O | K2O | Li* | F | Сумма** |
|---|---|---|---|---|---|---|---|---|---|---|
| Ge99-43 | 44.2 | 1.56 | 2.69 | 0.52 | 36.2 | 0.334 | 3.76 | Не опр. | 89.34 | |
| 930/10 | 46.0 | 0.4 | 2.1 | 0.3 | 33 | 1.1 | 3.5 | » | 86.34 | |
| 196 | 55.6 | 0.182 | 21.53 | 1.68 | – | 0.948 | 0.457 | 2.4 | 8.26 | 91.07 |
| 198 | 51.8 | 0.61 | 22.57 | 0.696 | 0.33 | 1.21 | 0.877 | 2.8 | 8.93 | 89.85 |
Исходные и обработанные раствором уранилнитрата синтетические смектитоподобные соединения, природные смектиты (исходные и после насыщения органическими жидкостями с последующей температурной обработкой (при 550°С)) анализировали методом порошковой рентгеновской дифрактометрии. Рентгенофазовый анализ (РФА) проводили на порошковом дифрактометре ARL X’TRA фирмы Thermo Fisher Scientific (Ecublens) SARL (Швейцария), CuKα-излучение, интервал углов 2θ 2°–64°, шаг 0.02°, время сканирования в точке 3 с.
Состояние минеральных объектов, форму вхождения и тип “воды” в них исследовали методом ИК-спектроскопии на Фурье-спектрометре VERTEX 70 FT IR Bruker в области 400–4000 см–1. Образцы для ИК-спектроскопии готовили прессованием таблеток с KBr.
Исследования проводили также методом электронного парамагнитного резонанса (ЭПР) на радиоспектрометре Radiopan, fмод = 100 кГц, t = = 293°С. Метод ЭПР-спектроскопии позволил выявить в образцах даже очень низкие концентрации иона Fe2+.
Эксперименты по сорбции уранила синтетическими образцами и нонтронитами проводили из растворов уранилнитрата UO2(NO3)2 · 6H2O с исходной концентрацией (2.4–3.6) × 10–4 г/л (в пересчете на уран) и 0.01 М NaCl. Соотношение вода : порода составляло 50 : 1, время сорбции – от 30 мин при рН 6.8 (с применением магнитных мешалок). Ранее было показано, что слоистые силикаты сохраняют сорбционную способность в отношении урана в достаточно широком диапазоне рН 4–9, характерном для большинства природных вод, и что сорбция уранил-иона природными смектитами происходит в основном на их поверхности [7]. Разделение фаз после сорбции проводили центрифугированием при 15 000 об/мин.
Сорбционную активность определяли по изменению начальной концентрации ионов уранила в исходных растворах в жидкой фазе после контакта с навеской образца в течение фиксируемых промежутков времени. Концентрацию уранила измеряли методом масс-спектрометрии с индуктивно-связанной плазмой (ICP MS) высокого разрешения на приборе ELEMENT фирмы FINNIGAN MAT (Germany) с магнитным сектором и двойной фокусировкой ${\text{UO}}_{2}^{{2 + }}$ в диапазоне концентраций 10–1–10–4 г/л. Оптимизированные инструментальные параметры получены при использовании стандартного раствора 10090а977 фирмы Merck. Погрешность определения 1–5%.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Изучение кинетики сорбции уранил-иона из разбавленных растворов урана показало, что подвижное равновесие на поверхности исследуемых материалов достигается за 20 мин. Увеличение концентрации урана в растворе приводит к возрастанию времени достижения равновесия, что указывает на высокую степень насыщения ионами уранила химически активных групп поверхности, а также на участие в процессе сорбции поверхностного порового пространства [6]. Значимый вклад в иммобилизацию урана сорбентами вносят поверхностные дефекты структуры. Это особенно важно учитывать при изучении ландшафтной миграции урана, поскольку под действием различных природных факторов происходит не только измельчение минералов-сорбентов со значительным увеличением их удельной поверхности, но и глубокие структурные нарушения [1, 8].
Для исследования свойств и структурных преобразований синтезированных смектитоподобных образцов и природных смектитов при взаимодействии с уранил-ионом были взяты два образца фтористых литийсодержащих синтетических (196а и 198б) и два природных: один из Охотского моря (серия Ge99-43), второй из центральной части Тихого океана (930/10), оба последних практически не содержали примесей других минералов.
Дифрактограмма исходного образца 930/10 приведена на рис. 1 (кривая 1). После насыщения его этиленгликолем рефлекс d001 = 11.35 Å исходного минерала значительно уширился и весьма слабо проявился в области малых углов (d ∼ 18.3 Å) (рис. 1, кривая 2). Ранее показано, что у нонтронитов серии Ge99 рефлекс d001 после насыщения этиленгликолем практически исчезает, т.е. не происходит его сдвига в сторону меньших углов, что является характерным свойством для смектитов в целом [11, 14]. Можно предположить, что структурные особенности и свойства океанического образца близки к таковым для образца из Охотского моря серии Ge99-43. Исчезновение или уширение и ослабление без выраженного рефлекса d001 при внедрении органических молекул в межслоевое пространство обусловлено высокой степенью разупорядоченности структуры смектитов и малыми размерами доменов перпендикулярно направлению 00l. При внедрении молекул этиленгликоля в межслоевое пространство таких структур, характеризующихся несколькими типами дефектов, нарушается последовательность упаковки слоев, между которыми возможны еще и непрерывные переходы. Рефлекс d001 либо не регистрируется вовсе, либо размывается от 5° до 2° по углу 2θ. Разные структурные преобразования при внедрении органических молекул в межслоевое пространство смектитов обусловлены большим или меньшим количеством структурных дефектов, что отражается и на сорбционной способности минералов.
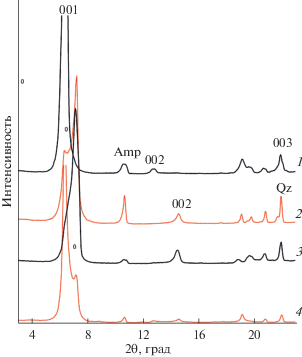
Рис. 1.
Дифрактограммы образца 930/10: 1 – исходный, 2 – насыщенный этиленгликолем, 3 – после взаимодействия с уранил-ионом, 4 – с уранилом и насыщенный этиленгликолем, 5 – с уранилом после термической обработки при 550°С. На вставке – фрагмент дифрактограмм в области рефлекса d060.
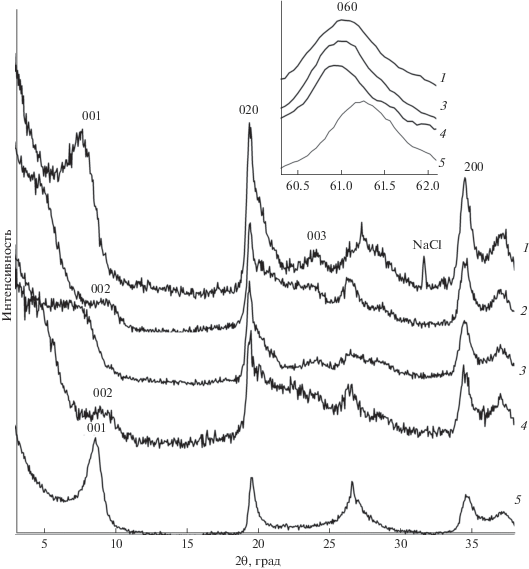
На рис. 1 приведены рентгенограммы образца 930/10, исходного (рис. 1, кривая 1) и после сорбции уранил-иона ${\text{UO}}_{2}^{{2 + }}$ (рис. 1, кривая 3). Обнаружено, что рефлекс d001 = 11.35 Å исходного минерала уширился в сторону меньших углов до значений от 11.73 до 18 Å. Такое преобразование обусловлено частичным внедрением уранил-иона в межслоевое пространство структуры смектита, а также разворотом тетраэдров тетраэдрической сетки и деформацией октаэдров в октаэдрической сетке в результате взаимодействия с уранил-ионом. Таким образом, образовались нонтронит урансодержащий и нонтронит с деформированным алюмосиликатным слоем, т.е. структурными полиэдрами. Присутствие этих фаз в смектите после его взаимодействия с раствором соли урана подтверждается также уширением рефлекса 060 (рис. 1, вставка) с небольшими вариациями параметра b: 9.108 Å в исходном образце, 9.102 и 9.132 Å после эксперимента. Уменьшение параметра b, скорее всего, обусловлено разворотом и деформацией структурных полиэдров, а увеличение – внедрением уранил-иона в структуру минерала. Элементарная ячейка нонтронита, обработанного азотнокислым раствором урана, после насыщения этиленгликолем заметно увеличилась по параметрам с и b (рис. 1, кривая 4) и существенно уменьшилась после температурной обработки при 550°С в течение 1 ч (рис. 1, кривая 5). В последнем случае структурные преобразования обусловлены удалением молекул воды из межслоевого пространства и исчезновением дефектов упаковки в алюмосиликатном слое.
Синтезированные слоистые Li-содержащие силикаты в ходе взаимодействия с раствором уранилнитрата UO2(NO3)2 · 6H2O также частично поглощают уранил-ион (внедрение в межслоевое пространство), но в большей степени происходит искажение структурных полиэдров. В результате в образце 196 исходный рефлекс d001 = 13.472 Å с относительной интенсивностью I = 100 (рис. 2, кривая 1) раздваивается: 13.792 Å с I = 30 и 12.156 Å c I = 60, при этом параметр b = 9.084 Å остается практически неизменным, происходит лишь уширение рефлекса 060 (рис. 2, кривая 2) [15]. Структурные преобразования в образце 198 практически идентичны вышеописанным: исходный рефлекс 12.305 Å с I = 25 (рис. 2, кривая 3) делится на два – 13.792 с I = 100 и 12.228 Å с I = 24, но с незначительным уменьшением параметра b от 9.084 до 9.06 Å (рис. 2, кривая 4). Уменьшение параметра b в этом случае, очевидно, обусловлено деформацией структуры при взаимодействии с уранил-ионами. Незначительные различия структурных преобразований в синтетических слоистых силикатах при их взаимодействии с уранил-ионом объясняются спецификой заполнения кристаллографических позиций в тетраэдрах, октаэдрах и, что наиболее важно, межслоевого пространства. Кристаллохимические формулы синтетических образцов рассчитаны по результатам микрозондового анализа (табл. 1) по катионам для триоктаэдрического типа структуры смектита [16]:
Рис. 2.
Фрагменты дифрактограмм образцов: 1 – 196 исходный, 2 – 196 после обработки уранинитратом, 3 – 198 исходный, 4 – 198 после обработки уранилнитратом. Примеси кварца – Qz, амфибола – Amp.
196: (K0.04Na0.14Li0.12Ca0.13)0.43(Mg2.41Li0.56Al0.03)3Si4O10(F1.89O0.11)2.nH2O,
198: (K0.07Na0.15Li0.24Ca0.06)0.52(Mg2.46Li0.51Fe0.03)3(Si3.95Al0.05)4О10(F1.9O0.1)2.nH2O.
Сравнивая относительные интенсивности перечисленных рефлексов, можно заключить, что в образце 198 происходит более активная сорбция ${\text{UO}}_{{\text{2}}}^{{2 + }}$ в межслоевое пространство, чем в образце 196, что подтверждается значениями концентрации урана в растворах до и после взаимодействия с исследуемыми образцами (табл. 2). Подобное явление можно объяснить тем, что в межслоевом пространстве образца 198 в два раза больше легких и малых по размеру атомов Li и в два раза меньше более крупных атомов Са.
Таблица 2.
Концентрация урана(VI) в растворе до и после сорбции на природных и синтетических образцах при рН 6.8, время сорбции 30 мин (в присутствии 0.01 М NaCl)
| Образец | СU, г/л | |
|---|---|---|
| в исходном азотнокислом растворе | в растворе после взаимодействия с исследуемыми образцами | |
| Ge 99-43 | 2.4 × 10–4 | 6.4 × 10–6 |
| 930/10 | 2.4 × 10–4 | 1.5 × 10–6 |
| 196 | 3.6 × 10–4 | 7.8 × 10–5 |
| 198 | 3.6 × 10–4 | 3.1 × 10–5 |
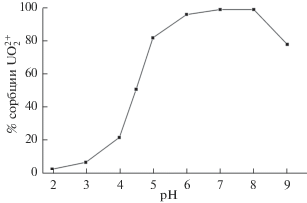
Как видно из табл. 2, природные нонтрониты со дна Тихого океана и Охотского моря обладают лучшими сорбционными показателями, чем синтетические образцы (196 и 198). Это связано не только с наличием дефектов структуры, но и с образованием комплексов уранил-иона с ионами железа, входящими в структуру смектитов. Присутствие железа в глинистых осадках усиливает их сорбционный потенциал, однако процесс существенно зависит и от рН водной фазы [17–19]. Экспериментально показано, что оптимальным является диапазон рН 5.5–8.2 (рис. 3). При этом образование поверхностных комплексов происходит по схеме:
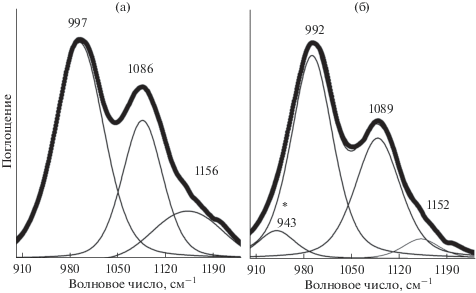
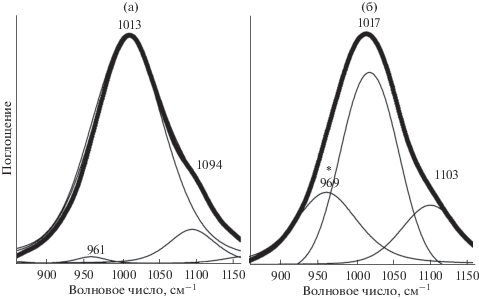
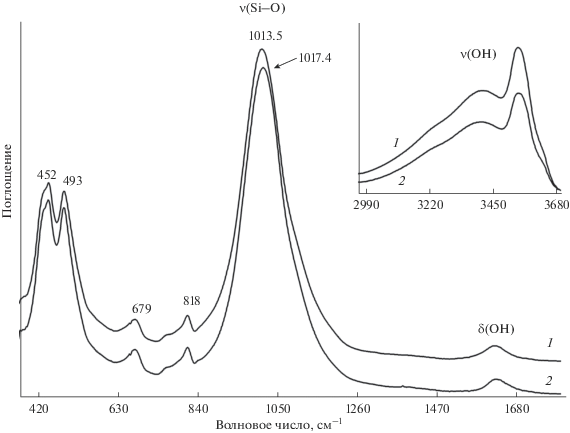
Данные ИК-спектроскопии подтверждают подобные выводы. В спектрах синтетических образцов присутствуют полосы поглощения смектита и слюды с примесью кварца (рис. 4, кривая 1, 6а) [15]. Природные образцы представлены высокожелезистыми смектитами – нонтронитами [20–23] (рис. 5, кривая 1). Характеристическими полосами в ИК-спектрах нонтронита являются полосы валентных колебаний Si–O связей в области волновых чисел 1013, 1100 см–1, деформационных колебаний Si–O–Fe в области 493 см–1, деформационных колебаний Si–O–Si в области 452 см–1, а также валентных колебаний Fе–ОН в области 3545 см–1 (рис. 5, кривая 1, вставка) [14, 23]. ИК-спектры соединений, содержащих уранил-ион, характеризуются полосами поглощения антисимметричных валентных колебаний катиона уранила с волновыми числами около 915–940 cм–1 и слабыми полосами симметричных валентных колебаний 850–865 cм–1 [24, 25]. В ИК-спектрах синтетических образцов после взаимодействия с азотнокислым раствором урана наблюдается увеличение интенсивности и уширение полосы в области 910–990 см–1 за счет внедрения в межслоевое пространство уранил-ионов (рис. 4, кривая 2). ИК-спектры природных нонтронитов, обработанных раствором с катионом уранила (${\text{UO}}_{2}^{{2 + }}$), показаны на рис. 5 (кривая 2). Наблюдается небольшой сдвиг полос колебаний Si–O–Si, что, вероятно, является следствием взаимодействия раствора уранил-иона с атомами кислорода из мостиков Si–O–Si. В синтетическом и природном смектитах полоса, соответствующая колебанию ${\text{UO}}_{2}^{{2 + }}$ ∼ 930 см–1 (на рис. обозначена звездочкой), перекрывается с колебанием SiOSi-группы и проявляется ее уширением. Для определения полосы уранила необходимо разложение как исходных спектров (рис. 6а, 7а), так и спектров образцов, обработанных уранилнитратом (рис. 6б, 7б). Разложение фрагментов ИК-спектров проведено методом математического моделирования с использованием функции Фогта. В сравнении с синтетическими образцами сорбционные показатели природных глин со дна Тихого океана и Охотского моря существенно лучше (табл. 2, рис. 5, 7б). После разложения полосы в области валентных колебаний уранил-иона интенсивность полосы (обозначенной звездочкой) в природном образце в 2 раза выше, чем в синтетическом. ИК-спектроскопия более наглядно демонстрирует взаимодействие и внедрение ${\text{UO}}_{2}^{{2 + }}$ в структуры таких сорбентов, как, например, мох (рис. 4, кривая 3), где полоса уранил-иона не накладывается на полосу исследуемого образца и проявляется явно.
Рис. 4.
ИК-спектры синтетического образца 198: 1 – исходный, 2 – обработанный уранилнитратом, 3 – обработанный уранилнитратом мох, звездочкой отмечена полоса валентного колебания уранил-иона. На вставке – область валентных колебаний ОН-группы.
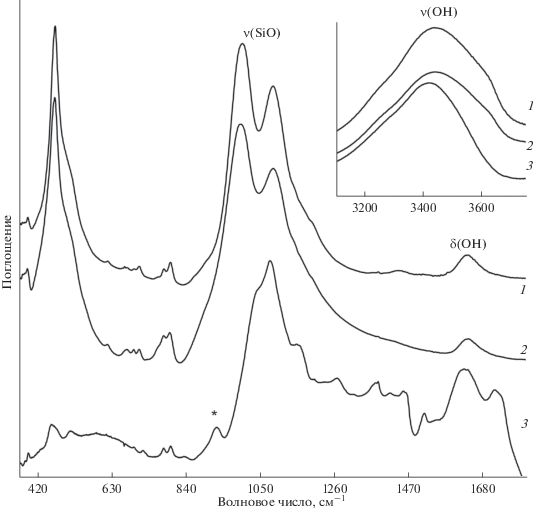
Рис. 5.
ИК-спектры природного образца нонтронита 930/10: 1 – исходный, 2 – после обработки уранилнитратом. На вставке – область валентных колебаний ОН-группы.
ЗАКЛЮЧЕНИЕ
Проведенные исследования позволяют сделать вывод, что основными причинами связывания радионуклидов являются не только обменные процессы, но и образование поверхностных комплексов [26–28]. Взаимодействие иона уранила с поверхностью природных минералаов, содержащих ионы железа, изучено методом ЭПР [29, 30]. В исходных образцах ионы Fe3+ регистрируются преимущественно в октаэдрических позициях. В ЭПР-спектрах после сорбции уранила фиксируется широкая (80–120 мТл) симметричная линия комплексов с железом в области g = = 2.05. Как видно из табл. 3, после сорбции урана количество парамагнитных центров (ПМЦ) увеличивается, что свидетельствует об окислении железа(II), входящего в структуру нонтронитов океанических осадков, до железа(III). В местах разрывов связей освобождаются краевые атомы кислорода и металла, что приводит к возникновению некомпенсированных парамагнитных центров с повышенной энергетикой, обеспечивающих устойчивое связывание уранила [7].
Таблица 3.
Изменение количества ПМЦ после сорбции урана из растворов с содержанием урана(VI) 2.4 × × 10–4 г/л (тип центров Fe3+ структурный)
| Образец | Количество ПМЦ, отн. ед | |
|---|---|---|
| исходный образец | после сорбции урана | |
| Ge 99-43 | 359 | 532 |
| 930/10 | 482 | 633 |
Показано, что в процессе взаимодействия природных нонтронитов и синтетических слоистых силикатов с раствором, содержащим уранил-ион, меняются структурные параметры как природных, так и синтетических материалов. Это происходит в результате вхождения уранил-ионов в межслоевое пространство, а также вследствие деформации структурных полиэдров. Методами ЭПР- и ИК-спектроскопии, масс-спектрометрии с индуктивно-связанной плазмой высокого разрешения выявлено, что лучшими сорбционными характеристиками обладают природные железосодержащие нонтрониты донных отложений. Полученные результаты позволят наметить пути модификации материалов геохимических барьеров в зависимости от нужд конкретных производств.
БЛАГОДАРНОСТЬ
Авторы выражают признательность сотруднику Тихоокеанского океанологического института им. В.И. Ильичева ДВО РАН д.г.-м.н. А.Н. Деркачеву за предоставленные природные образцы и сотруднику ИГМ СО РАН Т.Н. Григорьевой за обсуждение результатов. Инструментальные исследования проведены в ЦКП многоэлементных и изотопных исследований СО РАН. Работа выполнена в рамках государственного задания, проекты № 0330-2016-0017 и 0330-2016-0010.
Список литературы
Ковалев В.П., Мельгунов С.В., Пузанков Ю.М., Раевский В.П. Предотвращение неуправляемого распространения радионуклидов в окружающую среду (геохимические барьеры на смектитовой основе). Новосибирск: Изд-во СО РАН, 1996.
Palchik N.A., Grigorieva T.N., Moroz T.N. // Russ. J. Inorg. Chem. 2013. V. 58. № 2. P. 138. doi 10.1134/S0036023 [Пальчик Н.А., Григорьева Т.Н., Мороз Т.Н. // Журн. неорган. химии. 2013. Т. 58. № 2. С. 172.]
Palchik N.A., Grigorieva T.N., Moroz T.N. et al. // Russ. J. Inorg. Chem. 2014. V. 59. № 5. P. 511. doi 10.1134/ S0036023614050131 [Пальчик Н.А., Мороз Т.Н., Григорьева Т.Н.и др. // Журн. неорган. химии. 2014. Т. 59. № 5. С. 681.]
Дриц В.А., Коссовская А.Г. Кн. Глинистые минералы: смектиты, смешанослойные образования. М.: Наука, 1990.
Sakharov B.A., Drits V.A. // Lithol. Miner. Resour. 2015. V. 50. P. 50. doi 10.1134/S0024490215010058 [Сахаров Б.А., Дриц В.А. // Литология и полезные ископаемые. 2015. № 1. С. 55]
Timacher R.M., Holmhoe M., Tournassat S. et al. // Geochim. Cosmochim. Acta. 2016. V. 171. 130.
Разворотнева Л.И., Богуславский А.Е., Ковалев В.П. и др. // Экология промышленного производства. 2007. № 3. С. 33.
Kampos B., Aguilar-Carillo J., Algarra M. et al. // Appl. Clay Sci. 2013. V. 85. P. 53.
Горбаренко С.А., Деркачев А.Н., Астахов А.Н. и др. // Тихоокеанская геология. 2000. Т. 19. № 2. С. 58.
Деркачев А.Н., Баранов Б.В., Карп Б.Я. и др. // Докл. РАН. 2009. Т. 426. № 6. С. 782.
Palchik N.A., Moroz T.N., Grigorieva T.N. et al. // Crystallogr. Rep. 2017. V. 62. № 1. P. 91. doi 0.1134/S1063774517010163 [Пальчик Н.А., Мороз Т.Н., Григорьева Т.Н. и др. // Кристаллография. 2017. Т. 62. № 1. С. 86.]
Koo Tae-hee, Kim Jee-young, Choi Jong-woo, Kim Jin-wook // Clays and Clay Minerals. 2017. V. 65. № 6. P. 410. doi 10.1346/CCMN.2017.064080
Trillo J.M., Poyato J., Tobías M.M., Castro M.A. // Clay Minerals. 1990. V. 25. № 4. P. 485.
Palchik N.A., Grigorieva T.N., Moroz T.N. // Crystallogr. Rep. 2013. V. 58. № 2. P. 302. doi 10.1134/S1063774513020193 [Пальчик Н.А., Григорьева Т.Н., Мороз Т.Н. // Кристаллография. 2013. Т. 58. № 2. С. 275.]
Пальчик Н.А., Разворотнева Л.И., Мороз Т.Н. и др. // Вопросы естествознания. 2018. № 4 (18). С. 33.
Булах А.Г. Руководство и таблицы для расчета формул минералов. М.: Недра, 1967.
Разворотнева Л.И., Богуславский А.Е., Маркович Т.И. // Радиохимия. 2016. Т. 58. № 3. С. 274.
Zhang C., Liu X., Tinnacher R.M. // Environ. Sci. Technol. 2018. Article ASAP. doi 10.1021/ acs.est.8b02504
Jones A.M., Murphy C.A., Waite T.D., Collins R.N. // Environ. Sci. Technol. 2017. V. 51. P. 12573. doi 10.1021/acs.est.7b01793
Frost R.L., Kloprogge T., Ding Z. // Spectrochim. Acta. Part A. 2002. V. 58. P. 1881.
Kuligiewicz A., Derkowski A., Marek S. et al. // Clays and Clay Minerals. 2015. V. 63. № 1. P. 15. doi 10.1346/CCMN.2015.0630102
Farmer V.C. // Infrared Spectra of Minerals / Ed. Farmer V.C. L.: The Mineralogical Society, 1974. P. 331.
Frost R.L. // Spectrochim. Acta. Part A. Molec. Biomolec. Spectrosc. 2004. V. 60. № 7. P. 1469.
Cejka J., Muck Jr.A., Cejka J. // Phys. Chem. Minerals. 1984. V. 11. P. 172.
Tsarev T., Waite T.D., Collins R.N. // Environ. Sci. Technol. 2016. V. 50. № 15. P. 8223. doi 10.1021/ acs.est.6b02000
Liu X., Lu X., Cheng J. et al. // Geochim. Cosmochim. Acta. 2013. V. 117. P. 180.
Liu X., Lu X., Cheng J. et al. // Geochim. Cosmochim. Acta. 2015. V. 168. P. 293.
Milodowski A.E., Norris S., Alexander W.R. // Appl. Geochem. 2016. V. 66. P. 184.
Worasith N., Goodman B.A., Deng W. // J. Appl. Sci. 2018. V. 17. № 1. P. 12. doi 10.14416/j.appsci.2018.05.002
Balena S.P., Messerschmidt I., Tomazoni J.C. et al. // J. Brazil. Chem. Soc. 2011. V. 22. № 9. P. 1788. doi 10.1590/S0103-50532011000900023
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии