Химическая физика, 2022, T. 41, № 8, стр. 74-80
Инициирование горения водородовоздушных смесей металлическим родием и смесей водород–метан/этан/этилен–воздух родием и палладием при давлениях 1–2 атм
К. Я. Трошин 1, *, Н. М. Рубцов 2, Г. И. Цветков 2, В. И. Черныш 2, И. О. Шамшин 1
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова Российской академии наук
Москва, Россия
2 Институт структурной макрокинетики и материаловедения Российской академии наук
Черноголовка, Россия
* E-mail: troshin@chph.ras.ru
Поступила в редакцию 25.10.2021
После доработки 23.11.2021
Принята к публикации 21.12.2021
- EDN: CQVSHN
- DOI: 10.31857/S0207401X22080131
Аннотация
Экспериментально определены температуры воспламенения и эффективные энергии активации смесей (5÷40% Н2 – воздух над поверхностью металлического родия и стехиометрических смесей 70% H2 + 30% метана и (30÷70%) H2 + (70÷30%) этана (или этилена) с воздухом над поверхностями родия и палладия при давлениях 1–2 атм и начальной температуре 20–300 °С. Было показано, что поверхность металлического родия является более эффективным катализатором данных процессов горения, чем поверхность металлического палладия; величины эффективных энергий активации воспламенения зависят не только от природы катализатора, но и от химической природы углеводорода в исследуемой смеси. Полученные данные указывают на то, что каталитическое воспламенение инициируется экзотермической поверхностной реакцией окисления водорода в присутствии катализатора, углеводород на поверхности расходуется в реакциях с участием промежуточных продуктов окисления водорода, не приводящих к разветвлению цепей, и затем горение переходит в объем. Установлено, что в не обработанном воспламенениями исследуемой смеси реакторе температура воспламенения смеси 70% H2 + 30% метана с воздухом над поверхностью палладия при давлении 1.75 атм составляет 310 °С, а над поверхностью родия – 105 °С. В обработанном воспламенениями реакторе температура воспламенения смеси 70% H2 + 30% метана с воздухом над поверхностью палладия при давлении 1.75 атм составляет 270 °С, а над поверхностью родия – 62 °С. Полученный результат указывает на перспективность использования родиевого катализатора для существенного понижения температуры воспламенения топлив на основе метана и водорода.
ВВЕДЕНИЕ
Для широкого использования водорода в качестве топлива в “зеленой” энергетике необходимо решить ряд проблем по безопасности производства, транспортировке и хранению водорода. Одной из основных проблем является нештатное воспламенение, поскольку водород имеет гораздо более широкие концентрационные пределы воспламенения, чем углеводороды, обычно используемые в качестве топлив [1]. Одним из возможных источников воспламенения является горячая поверхность. Таким образом, необходимо иметь возможность предотвращать или надежно контролировать условия, при которых смесь водорода и окислителя контактирует с горячей поверхностью, особенно если поверхность обладает каталитическими свойствами.
Каталитическое горение водорода представляет интерес, поскольку устройства, например котлы, использующие этот принцип, работают при относительно низких температурах и могут генерировать тепло для бытовых приложений без выбросов CO2 и NOx [2]. В реакции горения водорода катализаторы должны обладать термической стабильностью, а также должны быть обеспечены условия, при которых окисление водорода происходило без взрыва. Эти требования могут быть удовлетворены при использовании благородных металлов, которые, кроме того, эффективно поглощают H2 и O2 при сравнительно низких температурах [3].
В качестве альтернативы наряду с водородом повышенное внимание привлекают более безопасные смесевые водородно-углеводородные топлива, концентрационные пределы воспламенения которых существенно уже, чем в случае водорода. Поэтому горение этих топлив позволит удовлетворить современную потребность в ограничении выбросов NOx в производстве энергии, в том числе в двигателях внутреннего сгорания [4–6].
Благородные металлы по-разному влияют на воспламеняемость горючих газов и их смесей. Мы ранее показали, что температура зажигания смеси 40%H2 – воздух над металлическим Pd (70 °C, 1 атм) на ~200 °С меньше, чем над поверхностью Pt (260 °C, 1 атм) [6], т.е. Pd каталитически более эффективен, чем Pt. Таким образом, Pd более удобен для использования в рекомбинаторах водорода на АЭС в том числе и потому, что в газовой фазе не появляются образованные при разложении летучего оксида каталитические частицы металла в качестве центров зажигания, как это имеет место в случае Pt [7]. Экспериментальное значение эффективной энергии активации каталитического воспламенения водорода над Pd составляет ~3.5 ккал/моль, что характерно для поверхностных процессов [6]. Это указывает на заметную роль темновой каталитической реакции окисления водорода, называемой также “беспламенным горением”, которое наблюдается при низких давлениях [8]. Осуществление такой реакции снижает вероятность нештатного воспламенения за счет расходования водорода и, соответственно, выхода смеси из области воспламенения.
Горение водорода над поверхностями Rh, Ru, Pd и Pt при общих давлениях до 200 Торр и начальных температурах до 500 °С исследовали в работе [9] с целью установления как зависимостей пределов каталитического воспламенения над поверхностями благородных металлов от температуры, так и управляющих факторов процесса зажигания газа каталитической поверхностью. Было показано, что Rh является наиболее эффективным катализатором воспламенения 2H2 + O2, при этом самая низкая температура зажигания наблюдается при использовании Rh и составляет 210 °C, для Ru и Pd – 300 °C, для Pt – 410 °C.
В работах [10, 11] показано, что при горении смесей (70÷40%) водорода + (30÷60%) пропана с воздухом (коэффициент избытка горючего ϕ = 1) над палладием при общих давлениях 1–2 атм периоды задержки воспламенения (τ) сначала уменьшаются с понижением температуры, а затем увеличиваются, до тех пор пока не достигается предел каталитического воспламенения, т.е. наблюдается явление отрицательного температурного коэффициента (ОТК). Эффективная энергия активации процесса составляет Eef = (2.2 ± 1.0) ккал/моль, что характерно для поверхностного процесса. Таким образом, явление ОТК непосредственно связано с состоянием поверхности катализатора.
В работе экспериментально определены значения температуры воспламенения и эффективных энергий активации воспламенения смесей (5÷40%) Н2 – воздух над поверхностью металлического родия и стехиометрических смесей 70% H2 + 30% метана и (30÷70%) H2 + (70÷30%) этана (или этилена) с воздухом над поверхностями родия и палладия при давлениях 1–2 атм и начальной температуре 20–300 °С в статических условиях с целью сравнения каталитической эффективности Rh и Pd, установления факторов, определяющих закономерности инициирования каталитического воспламенения и выяснения наличия ОТК при воспламенении водорода над Rh.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Эксперименты проводили с газовыми смесями (5÷40%) Н2 – воздух над поверхностью металлического родия и стехиометрических (стехиометрический состав рассчитывали для суммы топлив) смесей 70% H2 + 30% метана и (30÷70%) H2 + (70÷30%) этана (или этилена) с воздухом над поверхностями родия и палладия при давлениях 1–2 атм и начальной температуре 20–300 °С в статических условиях. Использовали нагреваемый цилиндрический реактор из нержавеющей стали длиной 25 см и диаметром 12 см, снабженный съемными крышками и оптическим сапфировым окном в одной из крышек [8]. Точность измерения температуры составляла 0.3 °С. Регистрацию воспламенения и распространения пламени осуществляли с помощью цветной высокоскоростной камеры Casio Exilim F1 Pro (Japan) с частотой кадров – 600 с–1. Видеофайл сохраняли в памяти компьютера и затем проводили его покадровую обработку [10, 11]. Откачанный и нагретый реактор быстро заполняли газовой смесью из буферного объема высокого давления до необходимого давления. Для открытия и закрытия газовых коммуникаций использовали электромагнитный клапан. Давление в процессе напуска газа и горения регистрировали прецизионным датчиком давления “Карат-ДИ” (Россия). Для осуществления термического/каталитического зажигания использовали палладиевую проволоку толщиной 0.3 мм и длиной 80 мм, а также образец Rh, который был получен путем электрохимического осаждения слоя Rh толщиной 15 мкм на эту проволоку. Палладий был выбран, так как его коэффициент теплового расширения наиболее близок к Rh [12]. Проволоки из Pd или Rh/Pd использовали для воспламенения газовой смеси; при этом температуру проволоки измеряли, включая ее в качестве плеча в цепь моста Уитстона и калибруя предварительно по температуре. Перед каждым экспериментом реактор откачивали до 0.1 Торр. Верхний предел каталитического воспламенения определяли как среднее значение двух температур при заданном давлении при подходе со стороны низких температур в не обработанном воспламенениями сосуде: при более низкой температуре воспламенение отсутствовало, при более высокой – воспламенение происходило. Нижний предел каталитического воспламенения определяли аналогично, но при “подходе” со стороны высоких температур в обработанном воспламенениями сосуде. Общее давление в реакторе контролировали с помощью образцового вакуумметра, а давление в буферном объеме – с помощью образцового манометра. Использовали химически чистые газы и Pd чистотой 99.85%.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Эксперименты по высокоскоростной регистрации каталитического воспламенения на примере смеси 40% H2 – воздух и стехиометрической смеси (70% Н2 + 30% СН4) – воздух над поверхностью проволоки из Rh/Pd показали, что первичный центр воспламенения возникает у поверхности металла (рис. 1); в последующих экспериментах в тех же условиях место возникновения первичного центра воспламенения изменялось. Такое же изменение места локализации первичного центра мы наблюдали ранее при воспламенении над поверхностью платины [6, 7, 9].
Рис. 1.
Последовательность кадров высокоскоростной съемки (600 с–1) каталитического воспламенения смесей 40% H2 + воздух (а) над поверхностью родия при T0 = 80 °С, P0 = 1.7 атм и 70% H2 + 30% СН4 + воздух (б) над той же поверхностью при тех же значениях T0 и P0 (все кадры на рис. 1б увеличены в 4 раза по сравнению с рис. 1а). Первый кадр соответствует моменту возникновения первичного очага воспламенения.
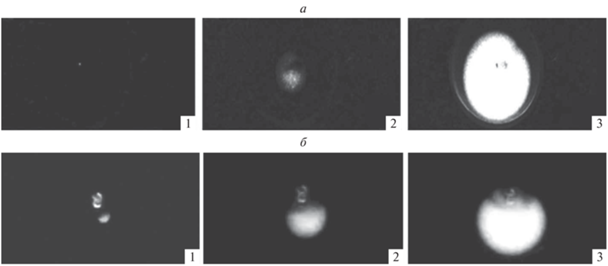
Таким образом, воспламенение над поверхностью благородного металла связано с реакциями адсорбированных активных центров на поверхности, поведение которых определяется как поверхностными дефектами с избытком свободной энергии, так и природой катализатора. Воспламенение включает стадии прогрева, локального зажигания и распространения пламени. Химическая активность различных участков поверхности изменяется от одного воспламенения к другому.
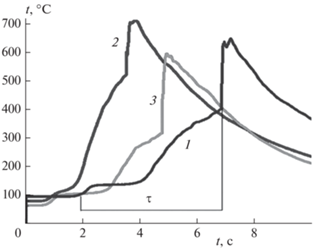
Зависимости температуры разогрева проволоки из Rh/Pd от времени при каталитически инициированном воспламенении смеси 40% H2 – воздух при P0 = 1.75 атм и T0 = 98, 80, 68 °C представлены на рис. 2. Эти зависимости соответствуют последовательным значениям температуры, при которых горючая смесь напускается в обработанный воспламенениями реактор ниже верхнего предела каталитического воспламенения, измеренного в необработанном сосуде при “подходе” снизу вверх по температуре (при более низких температурах воспламенение не происходит, при более высоких воспламенение наблюдается) [10]. Таким образом, в этой серии опытов первое воспламенение соответствует превышению верхнего предела каталитического воспламенения, осциллограммы второго и третьего воспламенений приведены на рис. 2. Как видно из этого рисунка, периоды задержки воспламенения τ сначала уменьшаются с понижением температуры. Затем значения τ увеличиваются, пока не достигается нижний предел каталитического воспламенения (при более высоких температурах происходит воспламенение, при более низких воспламенение отсутствует). Напомним, что нижний предел каталитического воспламенения соответствует поверхности реактора или поверхности катализатора, обработанной воспламенениями; верхний предел каталитического воспламенения соответствует “свежему” реактору, в котором до этого не происходило воспламенений. Таким образом, над поверхностью родия мы наблюдаем явление отрицательного температурного коэффициента, подобное описанному в работе [10]. Явление ОТК, очевидно, вызвано изменением состояния поверхности родия. Как показано в работе [9], в образцах, обработанных зажиганиями, проявляются дефекты в виде отверстий (см. рис. 5 из [9]), располагающихся на фигурах травления. В реакциях травления, очевидно, участвуют активные промежуточные продукты окисления водорода.
Рис. 2.
Изменение температуры разогрева проволоки Rh/Pd при воспламенении смеси 40% H2 + воздух; при следующих значениях T0: 1 – 98 °C, 2 – 80 °C, 3 – 68 °C; Р = 1.75 атм; время задержки воспламенения (τ) показано на рисунке.
Чтобы выявить влияние химической природы как катализатора (Pd и Rh/Pd), так и углеводорода на поверхностные процессы, использовали газы метан, этилен и этан в смесях с водородом и экспериментально измеряли температурные зависимости концентрации водорода на нижнем пределе каталитического воспламенения. В данной работе приводится наиболее практически важный результат по воспламенению смесей водород–метан–воздух. Он заключается в том, что в не обработанном воспламенениями исследуемой смеси реакторе температура воспламенения смеси 70% H2 + 30% метана с воздухом над поверхностью палладия при давлении 1.75 атм составляет 310 °С, а над поверхностью родия – 105 °С (верхний предел каталитического воспламенения). В обработанном воспламенениями реакторе температура воспламенения смеси 70% H2 + 30% метана с воздухом над поверхностью палладия при давлении 1.75 атм составляет 270 °С, а над поверхностью родия – 62 °С (нижний предел каталитического воспламенения), т.е. родиевый катализатор обеспечивает снижение как нижнего, так и верхнего пределов каталитического воспламенения в разы по сравнению с палладием. Полученный результат, требующий дальнейших исследований, указывает на перспективность использования родиевого катализатора для существенного понижения температуры воспламенения топлив на основе метана и водорода.
Экспериментальные зависимости температуры на нижних пределах каталитического воспламенения для стехиометрических смесей H2–этан–воздух (темные кружки) и H2–этилен–воздух (светлые кружки) над поверхностью Pd от содержания H2 в смеси при 1.7 атм представлены на рис. 3a. На рис. 4a представлены зависимости нижних пределов каталитического воспламенения над поверхностями Pd и Rh/Pd от содержания H2 в смесях: H2–воздух над Rh/Pd (темные кружки), H2–воздух над Pd (квадраты), H2–этилен–воздух над Rh/Pd (светлые кружки) при P0 = 1.7 атм.
Рис. 3.
а – Экспериментальные зависимости температуры на нижнем пределе каталитического воспламенения на поверхности Pd от содержания H2 в смеси: ⚫ – смесь H2–этан–воздух, ⚪ – смесь H2–этилен–воздух; б – эти же зависимости в координатах Аррениуса. Эффективные энергии активации Еef: горючее H2–этан – (1.25 ± 0.50) ккал/моль; горючее H2–этилен – (2.8 ± 1.0) ккал/моль.
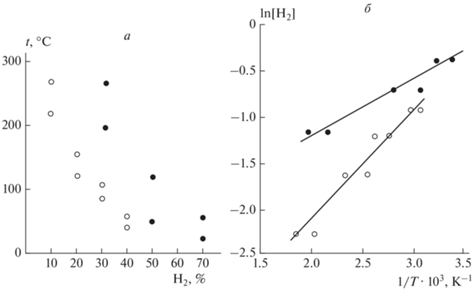
Рис. 4.
а – Экспериментальные зависимости температуры на нижнем пределе каталитического воспламенения на поверхностях Pd и Rh/Pd от содержания H2 в смеси: ⚫ – смесь H2–воздух над Rh/Pd, ◻ – смесь H2–воздух над Pd, ⚪ – смесь H2–этилен–воздух над Rh/Pd при P0 = 1.7 атм; б – аррениусовские зависимости содержания H2 в смеси на нижнем пределе каталитического воспламенения от температуры на поверхности Rh/Pd: ⚫ смесь – H2–этилен–воздух, Еef = (2.4 ± 1.0) ккал/моль; ⚪ – смесь 40% H2–воздух, Еef = (3.5 ± 1.1) ккал/моль; в – аррениусовские зависимости нижнего предела воспламенения (PI) смесей 2H2 + O2 (рис. 6, 7 из [9]) от температуры: ◻ – над Pd, Еef = (3.9 ± 1.0) ккал/моль; ◆ – над Rh/Pd, Еef = (3.6 ± 1.1) ккал/моль.
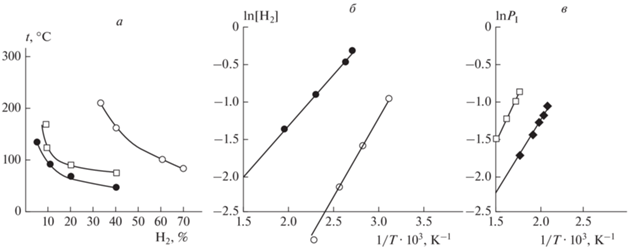
Из рис. 3a видно, что смесь H2–этан–воздух воспламеняется при более низких температурах, чем смесь H2–этилен–воздух, т.е. этан более эффективно взаимодействует с активными центрами на каталитической поверхности палладия. Рисунок 4a показывает, что поверхность Rh/Pd воспламеняет смесь H2–воздух при более низких температурах, чем поверхность Pd. Этот результат согласуется с рис. 4 из работы [9], где установлено, что Rh является наиболее активной поверхностью при катализе реакции H2 + O2, а поверхности Ru и Pd менее активны при общих давлениях <200 Торр. Следует отметить, что при давлениях >1 атм и последовательных каталитических воспламенениях смесей H2–углеводород–воздух над поверхностью Rh/Pd вблизи нижнего предела каталитического воспламенения при тех же условиях период задержки воспламенения увеличивается, т.е. нижний предел каталитического воспламенения увеличивается. Это можно предотвратить путем каталитического воспламенения смеси 40% H2–воздух перед каждым каталитическим воспламенением смесей H2–углеводород– воздух. Как указано выше, изменение каталитической активности благородного металла определяется изменением состояния его поверхности. Таким образом, поверхность родия более эффективно ингибируется (травится) углеводородом, чем поверхность палладия; этот углеводород удаляется с поверхности при ее обработке воспламенением смеси H2–воздух.
Зависимости содержания водорода в исследованных смесях от температуры на нижнем пределе каталитического воспламенения в координатах Аррениуса представлены на рис. 3б и 4б. Величины эффективной энергии активации берутся из тангенсов углов наклона прямых на этих рисунках. Укажем также, что в качестве значения концентрации в ln[H2] на рис. 3б и 4б берется доля водорода, а не проценты, как на рис. 3а. Как видно из этих рисунков, эти зависимости аппроксимируются прямыми линиями (коэффициенты корреляции ≥0.98). Данные обрабатывали с помощью программного пакета Statistica 9 (Statsoft). Приведенное в работе [6] обоснование использования таких координат основано на том, что в отсутствие водорода в смесевом горючем воспламенение в присутствии катализатора в использованном в работе интервале давлений и температур не происходит; именно процесс окисления водорода обеспечивает нагрев катализатора за счет поверхностной экзотермической реакции.
Из рис. 3б видно, что эффективная энергия активации нижнего предела каталитического воспламенения смеси H2–этан–воздух составляет (1.25 ± 0.5) ккал/моль; она заметно меньше значения аналогичного параметра для смеси H2–этилен–воздух (2.8 ± 1.0 ккал/моль), т.е. при каталитическом воспламенении углеводороды на поверхности расходуются каждый по своему специфическому механизму [13]. Для обеспечения воспламенения должна быть реализована совокупность реакций (звено цепи), в которых происходит разветвление (увеличение числа свободных валентностей) [6]. Активированная (E = 16.7 ккал/моль [14]) гомогенная реакция разветвления H + O2 → → O + OH является самой медленной стадией в звене цепи окисления водорода. Следовательно, энергия активации разветвления должна определять температурную зависимость всего процесса, как это наблюдается в аналогичных экспериментах с поверхностью металлической платины [15]. Это означает, что в случае каталитической поверхности Pd некоторые стадии, входящие в цикл реакций, приводящих к разветвлению, имеют гетерогенную природу [9], поскольку эффективная энергия активации составляет <3 ккал/моль. Таким образом, полученные в работе экспериментальные данные указывают на то, что каталитическое воспламенение инициируется экзотермической поверхностной реакцией окисления водорода в присутствии катализатора, углеводород на поверхности расходуется в реакциях с участием промежуточных продуктов окисления водорода, не приводящих к разветвлению цепей, и затем горение переходит в объем.
На рис. 4б приведены зависимости Аррениуса логарифма доли H2 в смеси на нижнем пределе каталитического воспламенения от обратной температуры на поверхности Rh/Pd для смеси H2–этилен–воздух. Величина эффективной энергии активации составляет (2.4 ± 1.0) ккал/моль. Эта величина меньше, чем при воспламенении над Pd, что указывает на бóльшую каталитическую эффективность родия по сравнению с палладием.
Величина эффективной энергии активации в аррениусовских координатах на нижнем пределе каталитического воспламенения на поверхности Rh/Pd для смеси H2–воздух составляет (3.5 ± 1.1) ккал/моль (рис. 4в). Эта величина близка к значению, взятому из зависимости Аррениуса для нижнего предела по давлению каталитического воспламенения смеси 2H2 + O2 над Rh/Pd: (3.6 ± 1.1) ккал/моль (рис. 6 из [9]). Величина эффективной энергии активации, определенная для нижнего предела каталитического воспламенения по давлению смеси 2H2 + O2 над Pd ((3.9 ± 1.0) ккал/моль, рис. 6 из [9]), также удовлетворительно согласуется со значением, полученным из зависимости Аррениуса для смеси 2H2 + O2 над Pd: ∼(3.5 ± 1.1) ккал/моль [6] (рис. 4в). Полученные значения эффективной энергии активации взаимно согласуются и свидетельствуют в пользу поверхностной природы отдельных реакций, входящих в процесс разветвления на поверхности Rh, как мы предположили ранее в работе [9]; при этом Rh более каталитически активен, чем Pd.
ЗАКЛЮЧЕНИЕ
Установлено, что Rh является более эффективным катализатором изученных процессов горения, чем Pd. Величины эффективных энергий активации каталитического воспламенения зависят не только от природы катализатора, но и от химической природы углеводорода в смеси. Таким образом, каталитическое воспламенение инициируется экзотермической поверхностной реакцией окисления водорода в присутствии катализатора, углеводород на поверхности расходуется в реакциях с участием промежуточных продуктов окисления водорода, не приводящих к разветвлению цепей, затем горение переходит в объем.
Установлено, что в не обработанном воспламенениями реакторе температура воспламенения смеси 70% H2 + 30% метана с воздухом над поверхностью Pd при давлении 1.75 атм составляет 310 °С, а над поверхностью Rh – 105 °С. В обработанном воспламенениями реакторе температура воспламенения этой смеси над поверхностью Pd при давлении 1.75 атм составляет 270 °С, а над поверхностью Rh – 62 °С. Полученный результат указывает на перспективность использования родиевого катализатора для понижения температуры воспламенения топлив на основе метана и водорода.
В части изучения горения над поверхностью металлических родия и палладия при использовании скоростной цветной киносъемки работа выполнена в рамках госзадания АААА-А17-117011910011-09 и в рамках госзадания ИСМАН; в части изучения горения смесей водород–метан–воздух – в рамках госзаданий ФИЦ ХФ РАН № 0082 (регистрационный номер АААА-А21-121011990037-8) и ИСМАН (регистрационный номер АААА-А19-119010990034-5).
Список литературы
Lewis B., Von Elbe G. Combustion, Explosions and Flame in Gases. New York, London: Acad. Press, 1987.
Persson K., Pfefferle L.D., Schwartz W., Ersson A., Jaras S.G. // Appl. Catal. B: Environmental. 2007. V. 74. P. 242.
ernández A., Arzac G.M., Vogt U.F. et al. // Appl. Catal. B. 2016. V. 180. P. 336
Cho E.-S., Chung S.H. // J. Mech. Sci. Technol. 2009. V. 23. P. 650.
Razali H., Sopian K., Mat S. // ARPN J. Eng. Appl. Sci. 2015. V. 10. P. 7780.
Борисов А.А., Рубцов Н.М., Скачков Г.И., Трошин К.Я. // Хим. физика. 2012. Т. 31. № 8. С. 30.
Трошин К.Я., Рубцов Н.М., Цветков Г.И., Черныш В.И. // Хим. физика. 2022. Т. 41. № 1. С. 23.
Рубцов Н. М., Виноградов А. Н., Калинин А. П. и др. // Хим. физика. 2019. Т. 38. № 4. С. 53.
Rubtsov N.M., Tsvetkov G.I., Chernysh V.I., Troshin K.Ya. // Combust. and Flame. 2020. V. 218. P. 179.
Борисов А.А., Кнорре В.Г., Кудряшова Е.Л., Скачков Г.И., Трошин К.Я. // Хим. физика. 1998. Т. 17. № 7. С. 80.
Калинин А.П., Рубцов Н.М., Виноградов А.Н. и др. // Хим. физика. 2020. Т. 39. № 2. С.23.
Engineering ToolBox, Coefficients of Linear Thermal Expansion, 2003, https://www.engineeringtoolbox.com/ linear-expansion-coefficients-d_95.html
Репинский С.М. Введение в химическую физику поверхности твердых тел. Новосибирск: Наука; Сиб. изд. фирма, 1993.
Семенов Н.Н. О некоторых проблемах химической кинетики и реакционной способности. М.: АН СССР, 1958.
Родионов И.Д., Рубцов Н.М., Виноградов А.Н. и др. // Хим. физика. 2021. Т. 40. № 8. С. 82.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


