Экология, 2019, № 4, стр. 263-269
Внутривидовая изменчивость металлоустойчивости семенного потомства Taraxacum officinale Wigg. S.L.: анализ на основе зависимостей “доза–эффект”
В. С. Безель a, *, Т. В. Жуйкова b, **, О. В. Дуля a, Н. С. Балыбердина b
a Институт экологии растений и животных УрО РАН
620144 Екатеринбург, ул. 8 Марта, 202, Россия
b Нижнетагильский государственный социально-педагогический институт (филиал) ФГАОУ ВО
“Российский государственный профессионально-педагогический университет”
622031 Нижний Тагил, ул. Красногвардейская, 57, Россия
* E-mail: bezel@ipae.uran.ru
** E-mail: hbfnt@rambler.ru
Поступила в редакцию 20.08.2018
После доработки 27.11.2018
Принята к публикации 05.12.2018
Аннотация
На основе анализа зависимостей “доза–эффект” при воздействии широкого диапазона концентраций сульфата меди по корневому тесту оценена металлоустойчивость семенного потомства двух морфологических форм Taraxacum officinale Wigg. s.l., произрастающих в фоновых условиях и при техногенной трансформации среды (промышленные отвалы). Поскольку на исследованных участках ранее были установлены различия в обилии и соотношении в ценопопуляциях этих форм, а также в уровнях накопления ими меди, то предполагалось, что они различаются и по металлоустойчивости семенного потомства. Показано, что средние значения эффективных концентраций сульфата меди, угнетающих рост корня проростков на 10, 50 и 90%, не различались между исследуемыми участками и морфологическими формами одуванчика.
Способность растительных популяций поддерживать численность при загрязнении среды тяжелыми металлами (ТМ) широко известна [1–4 и др.]. Несмотря на то, что продолжительность функционирования промышленных предприятий как источников загрязнения среды пренебрежимо мала по сравнению с эволюционными масштабами времени, результаты исследований этой проблемы свидетельствуют об адаптации растений к антропогенной трансформации среды обитания [5, 6]. Такая адаптация основана на снижении проницаемости корневого барьера при поступлении токсикантов в растительный организм [7, 8], увеличении фертильности, плодовитости и др. Многие работы [9–11] посвящены поиску различий между фоновыми и металлоустойчивыми популяциями и проверке гипотезы о том, что загрязнение может приводить к морфологической или физиологической дифференциации за счет репродуктивной изоляции, эффекта основателя или отбора. Однако мало работ, в которых сравнивают пути адаптации внутривидовых форм [10, 14], что свидетельствовало бы о возможных микроэволюционных процессах в ценопопуляциях при экстремальных условиях среды.
Более 20 лет мы исследуем ценопопуляции Taraxacum officinale Wigg. s.l. на техногенно трансформированных территориях. Возникает вопрос, что лежит в основе их длительного функционирования, которое проявляется в стабильности таких популяционных параметров, как численность, плотность и возрастной состав? Возможно, имеет место определенная коррекция физиологических параметров, связанных с устойчивостью к избытку ТМ и отбор по признаку металлоустойчивости.
Цель настоящей работы – на основе анализа зависимостей “доза–эффект” выявить различия между морфологическими формами и ценопопуляциями одуванчика по реакции на концентрации сульфата меди, угнетающие рост корня на 10, 50 и 90% (ЕСх). Обсуждаются две гипотезы: 1) в градиенте техногенной трансформации происходит увеличение металлоустойчивости (т.е. увеличение ECx); 2) металлоустойчивость различается между морфологическими формами T. officinale. Вторая гипотеза основана на том, что соотношение численности форм одуванчика в пределах исследуемых ценопопуляций различается между техногенно трансформированными и фоновыми местообитаниями.
МАТЕРИАЛ И МЕТОДЫ
Объект исследования. В качестве модельного вида рассмотрен одуванчик лекарственный (Taraxacum officinale Wigg. s.l.), семейство Asteraceae Dumort. (Compositae Giseke). По типу полового размножения – факультативный апомикт, триплоид [15]. Как рудеральный вид имеет высокую семенную продуктивность и жизнеспособность потомства. Исследуемые ценопопуляции представлены двумя морфологическими формами: одуванчиками Дальштедта (T. off. f. dahlstedtii Lindb. fil.) и гребенчатовидным (T. off. f. pectinatiforme Lindb. fil.).
Характеристика участков исследования. Семенной материал собран в зоне аэрогенных выбросов предприятий черной металлургии г. Нижний Тагил (Средний Урал). Ценопопуляции произрастают на участках, представляющих градиент техногенной трансформации и различающихся рядом физико-химических параметров почв, в том числе содержанием подвижных форм ТМ [16]. Химический состав почв изучен в соответствии с аттестованными методами анализа в аккредитованной лаборатории ИЭРиЖ УрО РАН (Аттестат аккредитации № РОСС RU. 0001.515630). На основе концентраций тяжелых металлов в почвах и расчетного индекса загрязнения (суммарного коэффициента концентрации Z, выраженного в относительных к фоновым значениям единицах) были выделены зоны техногенной нагрузки с расположенными в их пределах участками исследования: фоновая (уч. Ф: Z = 1.0 отн. ед.), буферная (уч. Б: Z = 6.2 отн. ед.) и импактная (уч. И: Z = 22.8 отн. ед.). Названия зон даны в соответствии с номенклатурой ЮНЕП [17].
По ландшафтным и почвенным условиям участок Ф относится к агроземам, расположен в агроландшафтах с агродерново-подзолистыми почвами (залежь возрастом более 20 лет), характеризуется средним плодородием и насыщенностью основаниями, низкой и средней обеспеченностью подвижными соединениями фосфора и калия, содержание легкогидролизуемого азота в агроземах среднее и низкое. Техноземы (участки Б, И) расположены в техногенных ландшафтах (на промышленных отвалах возрастом более 45 лет). Это молодые почвы, формируемые по буроземному и литоземному типам, обладают более высоким плодородием. Насыщенность почв основаниями высокая, в обменном комплексе преобладает кальций. Обеспеченность обменными формами фосфора и калия высокая и очень высокая, обеспеченность азотом при слаборазвитой дернине низкая, при наличии дернины – высокая. Подробная характеристика ландшафтов, агрохимических свойств почв и грунтов исследованных участков, а также содержание тяжелых металлов в почве опубликованы ранее [16].
Синтаксономическая характеристика сообществ: Ф – безранговое сообщество Elytrigia repens [Stellarietea mediae/Molinio-Arrhenatheretea]; Б – безранговое сообщество Trifolium pratense-Festuca pratensis [Arrhenatheretalia]; И – безранговое сообщество Tussilago farfara-Calamagrostis arundinacea [Dauco-Melilotion/Agropyrion repentis]. Травяные сообщества являются серийными, развивающимися на залежах и отвалах. Видовое богатство (шт.) сообществ: Ф – 25, Б – 47, И – 42. Суммарное проективное покрытие (%) видов: Ф – 103.1, Б – 148.4, И – 82.9. По флористическому составу сообщество участка Б относится к луговой стадии, сообщества И относятся к злаковой стадии сукцессии. Различия в видовом богатстве и покрытии сообществ исследуемых участков, видимо, связаны не только с сукцессионным возрастом, но и неблагоприятными эдафическими условиями участка И. Таким образом, исследованные ценопопуляции произрастают на территориях, различающихся по эдафическим и фитоценотическим условиям.
Оценка металлоустойчивости. Семена собраны в июне 2015 г. с 20 растений (потомство одного растения – семья) каждой морфологической формы одуванчика, произрастающих в пределах исследуемых ценопопуляций (всего 120 растений). Проращивание семянок выполнено по прошествии латентного периода в рулонной культуре [18] с 8-го месяца после сбора семян. Опыты проводили в емкостях (50 мл) с растворами сульфата меди при температуре 22–24°С и освещении лампами дневного света в течение 12 ч.
Из-за большого объема работа разделена на два эксперимента (март и май 2016 г.): в первом участвовало 5 семей каждой формы и ценопопуляции (всего 30) – при этом каждый вариант воздействия (семья × концентрация сульфата меди) представлен одной емкостью с 40 семянками; во втором – по пять семей каждой формы и ценопопуляции (всего 30). Каждый вариант представлен тремя емкостями с 15 семянками. Девять семей включены в оба эксперимента (для оценки возможной систематической ошибки).
В качестве контрольного раствора использовали 5 × 10–4 М Са(NO3)2 + 1 × 10–3 M KCl, на котором все потомство культивировали первые семь дней, после чего измеряли максимальную длину корня. Затем все растения переносили на контрольный и опытные растворы. Опытные растворы готовили с добавлением СuSO4 в концентрациях: 0.08; 0.10; 0.13; 0.18; 0.26; 0.31; 0.34; 0.45; 0.51 мг/л. После 10 дней культивирования у каждого проростка была измерена максимальная длина корня. В качестве результирующего параметра принят прирост корня за 10 дней. Всего было исследовано 12 539 проростков.
Статистический анализ выполнен в ПО R v.3.2.3. Поскольку любая математическая модель – это приближение реального биологического процесса, то один и тот же массив данных может быть одинаково хорошо аппроксимирован разными моделями, каждая из которых способна описывать разные участки диапазона концентраций токсиканта. Вследствие этого стандартом в современной токсикологии стал мультимодельный подход, в котором используют несколько конкурирующих моделей, строго оценивая их соответствие исходным данным, например с помощью информационного критерия Акаике (AIC). На основе токсикометрических параметров, рассчитанных с помощью каждой модели, определяли среднее значение этих параметров с учетом доброкачественности (goodness) каждой из них. Использование только одной модели для описания разных массивов данных может быть ошибочным, поскольку форма зависимости “доза–эффект”, как правило, индивидуальна.
В нашем случае зависимость прироста корня от концентрации сульфата меди для каждой семьи аппроксимировали следующими функциями: модели Вейбулла c разными формами асимметрии, лог-нормальная модель, модели Цедергрин-Рица-Штрайбига, модель Брэйна-Козенса и модель экспоненциального затухания [19] с использованием пакета drc v.2.2-1 [20]. Нижний предел прироста корня приравнивали нулю. Соответствие каждой модели исходным данным оценивали с помощью информационного критерия AIC, который трансформирован в AIC-вес, интерпретируемый как вероятность того, что модель лучшая из всего набора исследованных [21]. По результатам моделирования в список лучших для 42 семей вошли частные случаи модели Цедергрин-Рица-Штрайбига, модель экспоненциального затухания, а также модели Вейбулла c разными формами асимметрии. Для семи семей успешная аппроксимация зависимости была возможна только с помощью линейной модели.
На основе каждой из моделей для семьи рассчитывали EC10, EC50 и EC90 (пример на рис. 1), затем их усредняли для отдельной семьи с учетом AIC-весов использованных моделей. Поскольку в каждую выборку ECx вошло 9–10 семей, что недостаточно для использования параметрических методов анализа, то ECx разных форм и ценопопуляций одуванчика сравнивали с помощью теста Манна-Уитни с контролем вероятности ложных отклонений FDR при множественных проверках гипотез.
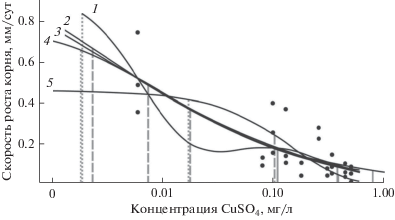
Рис. 1.
Пример зависимости “рост корня–концентрация сульфата меди” и ее аппроксимация моделями (1 – Цедергрин-Рица-Штрайбига, 2 – линейная, 3 – Вейбулла I, 4 – Вейбулла II, 5 – экспоненциального затухания) для одной из семей T. officinale. На ось Х спроецированы EC10 (пунктирная линия), EC50 (штриховая линия) и EC90 (сплошная линия), полученные с помощью разных моделей.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Стабильное существование Taraxacum officinale Wigg. s.l. на исследуемых участках свидетельствует о его достаточной семенной продуктивности во всех ценопопуляциях, позволяющей поддерживать необходимое обилие вида. Средняя многолетняя плотность особей этого вида, оцененная по количеству особей на 0.25 м2, в ценопопуляциях варьирует: Ф – от 14.22 ± 1.87 до 44.67 ± 5.77; Б – от 13.67±1.94 до 85.89±17.1; И – от 11.44 ± 2.88 до 56.78 ± 4.52. Независимо от уровня загрязнения на протяжении длительного периода (11 лет наблюдений) ценопопуляции характеризуются как молодые нормальные [22]. Циклические изменения возрастного состава, как правило, не сопровождаются переходом ценопопуляций из одного класса в другой и носят характер осцилляций. Лишь в некоторые годы отмечены флуктуационные колебания возрастного состава, приводящие к переходу ценопопуляций из класса молодых в класс зреющих. Стабильное преобладание молодых онтогенетических групп и сохранение онтогенетических спектров, близких к базовому, независимо от уровня техногенной трансформации почв свидетельствует о высокой устойчивости онтогенетической структуры ценопопуляций как к разным эдафическим условиям, так и погодным факторам.
В структуре всех ценопопуляций более многочисленна форма T. off. f. dahlstedtii. В градиенте изменения качества среды происходит уменьшение ее доли: Ф – 84.3 ± 1.2%; Б – 70.7 ± 3.0%; И – 62.5 ± 3.7%. Морфологические формы различаются по уровням накопления ТМ, в т.ч. меди (табл. 1). Хотя концентрации ионов меди в подземных и надземных органах T. officinale и не максимальны для данного вида, но сопоставимы с концентрациями в растениях из местообитаний, загрязненных выбросами автотранспорта [23, 24; и др.], а также сталелитейного и коксохимического заводов [25]. При изучении внутривидовой дифференциации растений по накопительным особенностям установлено, что при низких концентрациях меди в почве (0–100 мкг/г) ее содержание в корнях у исследуемых форм одуванчика статистически значимо не различается. При высоком содержании меди в почве (более 100 мкг/г) данный показатель значимо выше у f. pectinatiforme (p < 0.05) как в корнях, так и в листьях.
Таблица 1.
Содержание меди в почве и органах T. officinale f. dahlstedtii (1) и f. pectinatiforme (2), мкг/г
| Форма | Участок | ||
|---|---|---|---|
| фоновый | буферный | импактный | |
| 57°57′50″ с.ш., 60°15′11″ в.д. | 57°58′13″ с.ш., 59°58′35″ в.д. | 57°54′14″ с.ш., 59°54′41″ в.д. | |
| Почва, мкг/г | |||
| Cu2+ | 12.6 ± 0.9 | 101.6 ± 11.13 | 951.49 ± 236.10 |
| Корни (n = 20) | |||
| 1 | 20.04 ± 1.86 | 29.54 ± 0.64 | 95.02 ± 6.25 |
| 2 | 15.23 ± 1.41 | 25.11 ± 0.54 | 190.04 ± 2.80 |
| Листья (n = 20) | |||
| 1 | 13.2 ± 1.71 (0.65) | 11.3 ± 1.41 (0.38) | 46.34 ± 1.43 (0.49) |
| 2 | 11.3 ± 2.62 (0.74) | 10.9 ± 3.14 (0.43) | 83.62 ± 1.23 (0.44) |
| Семянки (n = 10) | |||
| 1 | 20.66 ± 0.67 | – | 20.65 ± 1.45 |
| 2 | 20.12 ± 1.19 | – | 20.44 ± 1.11 |
Различия в накоплении ТМ растениями в градиенте техногенно трансформированной среды отражают реакцию популяционной системы в целом на изменение качества среды обитания. Поскольку исследуемые территории различаются по уровню ТМ в почвах, то остается открытым вопрос существует ли отбор семян по металлорезистентности?
Ранее (1997–1998 гг.) в той же Притагильской зоне на аналогичных участках с различным уровнем загрязнения почв ТМ были исследованы показатели жизнеспособности и металлоустойчивости семенного потомства Taraxacum officinale Wigg. s.l. [26]. Методом корневого теста в рулонной культуре при одной, подобранной в предварительном эксперименте дозе CuSO4 (100 мг/л) в водном растворе были обнаружены статистически значимые различия в длине корней проростков у морфологических форм этого вида, произрастающих в градиенте загрязнения почв металлами. Однако более корректная оценка металлоустойчивости растений возможна при экспериментальном исследовании зависимости “доза–эффект” методом корневого теста проростков при широком диапазоне концентраций металлов [6, 27, 28]. Данный метод позволяет оценить гетерогенность семенного потомства по доле металлорезистентных семян в потомстве.
На примере 9 семей показано отсутствие систематической ошибки оценок эффективных концентраций, которая могла быть вызвана возможными отличиями между условиями разных экспериментов (непараметрический критерий знаков: Z = 0.76; p = 0.44). С увеличением концентрации сульфата меди, вплоть до максимальной, число выживших проростков не изменялось. Средние значения одноименных эффективных концентраций обеих форм T. officinale не различались между разными по уровню трансформации участками (p > 0.91; рис. 2). Это свидетельствует о том, что даже на максимально загрязненном участке семенное потомство растений не обладает повышенной устойчивостью к избытку меди. Этому соответствует и равный уровень накопления меди семянками на фоновом и импактном участках у обеих форм T. оfficinale (см. табл. 1).
Рис. 2.
EC10, EC50, EC90 форм T. off. f. dahlstedtii (а) и T. off. f. pectinatiforme (б) в ценопопуляциях участка Ф (сплошная линия, черные круги), Б (пунктирная линия, белые ромбы), И (пунктирная линия, серые квадраты); представлены медиана и размах.
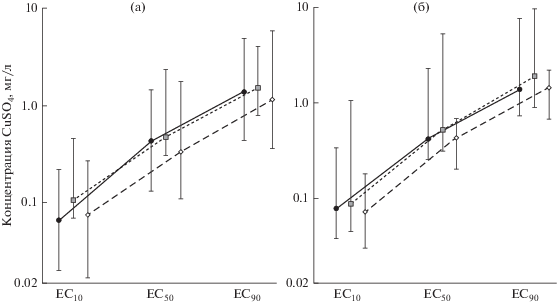
Не установлено также значимых различий в металлоустойчивости разных форм T. officinale в пределах каждого участка (p > 0.94), несмотря на разное содержание меди в подземных и надземных органах в импактных условиях (см. табл. 1, рис. 2). Возможно, отсутствие различий в реакции корневой системы проростков у обеих форм одуванчика связано с тем, что предельная в нашем случае доза (EC90) почти на порядок меньше, чем использованная ранее [26]. Не исключено, что различия в корневых тестах могут проявиться при существенно более высоких концентрациях металла, превышающих его реальные уровни в почвах. Надо иметь в виду, что высокая вариабельность реакций корневых систем одуванчика была отмечена и другими авторами, согласно которым репродуктивные показатели этого вида в зависимости от погодных и временных параметров могут изменяться в десятки раз [29].
Не исключено также, что при исследуемых уровнях загрязнения почв важную роль в формировании устойчивости к избытку ТМ играют микоризные ассоциации со стресс-устойчивыми видами микобионтов. Это предположение выдвигалось ранее [30] на основании данных по микроскопии корня T. officinale из загрязненных местообитаний.
ЗАКЛЮЧЕНИЕ
Анализ результатов на основании мультимодельного подхода показал, что высокие концентрации меди (до 900 мкг/г и выше) в почвах не оказывают прямого влияния на развитие повышенной металлоустойчивости (ECx) семенного потомства Taraxacum officinale к этому металлу. Возможно, соотношения двух морфологических форм Taraxacum officinale f. dahlstedtii и T. off. f. pectinatiforme в ценопопуляциях, произрастающих в градиенте техногенной трансформации среды, не являются следствием различий только в металоустойчивости их семенного потомства. Изменение внутривидовой структуры популяций, вероятно, обусловлено сменой эдафических и ценотических условий, в том числе опосредованно вызванных повышенными уровнями ТМ в почвах. Это определяет необходимость дальнейших исследований внутривидовой изменчивости T. officinale, в частности по показателям ценотической конкурентности и толерантности к абиотическим факторам среды (увлажнение, плодородие почвы и др.).
Работа выполнена в рамках государственного задания Института экологии растений и животных УрО РАН, а также частично поддержана Комплексной программой УрО РАН (проект № 18-4-4-9). Авторы подтверждают отсутствие конфликта интересов.
Список литературы
Позолотина В.Н., Антонова Е.В., Безель В.С. и др. Пути адаптации одуванчика лекарственного к длительному химическому и радиационному воздействию // Экология. 2006. № 6. С. 440–450. [Pozolotina V.N., Antonova E.V., Bezel’ V.S. et al. Pathways of adaptation of common dandelion coenopopulations to long-term chemical and radiation effects // Rus. J. of Ecology. 2006. V. 37. № 6. P. 402–407. doi 10.1134/S1067413606060063]
Трубина М.Р. Стратегия выживания Crepis tectorum L. в условиях хронического атмосферного загрязнения // Экология. 2011. № 2. С. 1–8. [Trubina M.R. The survival strategy of Crepistectorum L. under conditions of chronic atmospheric pollution // Rus. J. of Ecology. 2011. V. 42. № 2. P. 103–109. doi 10.1134/S1067413611020135]
Казнина Н.М., Титов А.Ф., Батова Ю.В., Лайдинен Г.Ф. Устойчивость растений Setaria viridis (L.) Beauv. к воздействию кадмия // Изв. РАН. Сер. биол. 2014. V. 41. № 5. С. 474–480. [Kaznina N.M., Titov A.F., Batova Y.V., Laidinen G.F. The resistance of plants Setariaveridis (L.) Beauv. to the influence of cadmium // Biology Bulletin. 2014. V. 41. № 5. P. 428–433. doi 10.7868/S000233291405004.х]
Позолотина В.Н., Антонова Е.В., Шималина Н.С. Адаптация Plantago major L. к длительному радиационному и химическому воздействию // Экология. 2016. № 1. С. 3–13. [Pozolotina V.N., Antonova E.V., Shimalina N.S. Adaptation of greater plantain, Plantago major L., to long-term radiation and chemical exposure // Rus. J. of Ecology. 2016. V. 47. № 1. Р. 1–10. doi 10.1134/S1067413616010124]
Ernst W.H.O. Evolution of metal tolerance in higher plants // For. Snow Landsc. Res. 2006. V. 80. № 3. P. 251–274.
Дуля О.В., Микрюков В.С., Воробейчик Е.Л. Стратегии адаптации Deschampsia caespitosa и Lychnis flos-cuculi к загрязнению тяжелыми металлами: анализ на основе зависимости доза–эффект // Экология. 2013. № 4. С. 243–253. [Dulya O.V., Mikryukov V.S., Vorobeichik E.L. Strategies of adaptation to heavy metal pollution in Deschampsia caespitosa and Lychnis flos-cuculi: analysis based on dose–response relationship // Rus. J. of Ecology. 2013. V. 44. № 4. P. 271–281. doi 10.1134/S1067413613040036]
Безель В.С., Жуйкова Т.В., Позолотина В.Н. Структура ценопопуляций одуванчика и специфика накопления тяжелых металлов // Экология. 1998. № 5. С. 376–382. [Bezel V.S., Zhuikova T.V., Pozolotina V.N. The structure of dandelion cenopopulations and specific features of heavy metal accumulation // Rus. J. Ecology. 1998. V. 29. № 5. P. 331–337.]
Jin X.F., Yang X.O., Islam E. et al. Effects of cadmium on ultrastructure and antioxidative defense system in hyperaccumulator and non-hyperaccumulator ecotypes of Sedum alfredii Hance // J. Hazard Mater. 2008. V. 156. № 1–3. P. 387–397. https://doi.org/10.1016/j.jhazmat.2007.12.064
Baker A.J.M., Dalby D.H. Morphological variation between some isolated populations of Silene maritima with in the British-Isles with particular reference to inland populations on metalliferous soils // New Phytologist. 1980. V. 84. № 1. P. 123–138.
Жуйкова Т.В., Безель В.С., Позолотина В.Н., Северюхина О.А. Репродуктивные возможности растений в градиенте химического загрязнения среды // Экология. 2002. № 6. С. 431–436. [Zhuikova T.V., Bezel’ V.S., Pozolotina V.N., Severyukhina O.A. The reproductive capacity of plants in a gradient of chemical environmental pollution // Rus. J. of Ecology. 2002. V. 33. № 6. P. 407–412. doi 10.1051/radiopro/2002193]
Jimenez-Ambriz G., Petit C., Bourrie I. et al. Life history variation in the heavy metal tolerant plant Thlaspi caerulescens growing in a network of contaminated and noncontaminated sites in southern France: role of gene flow, selection and phenotypic plasticity // New Phytologist. 2007. V. 173. № 1. P. 199–215.
Abratowska A., Wasowicz P., Bednarek P.T. et al. Morphological and genetic distinctiveness of metallicolous and non-metallicolous populations of Armeria maritima s.l. (Plumbaginaceae) in Poland // Plant Biology. 2012. V. 14. № 4. P. 586–595. https://doi.org/10.1111/j.1438-8677.2011.00536.x
Дуля О.В., Микрюков В.С. Изменение формы и размера листьев Lychnis flos-cuculi L. в градиенте полиметаллического загрязнения // Вестник ТГУ. 2013. V. 18. № 3. С. 778–782.
Воробьев Г.В., Алябьев А.Ю., Огородникова Т.И. и др. Адаптивные возможности одуванчика лекарственного в условиях загрязнения атмосферы автомобильным транспортом // Экология. 2014. № 2. С. 91–96. [Vorobyev G. V., Alyabyev A.Y., Ogorodnikova T.I. et al. Adaptive properties of the dandelion (Taraxacum officinale Wigg. s.l.) under conditions of air pollution by motor vehicle exhausts // Rus. J. of Ecology. 2014. V. 45. № 2. P. 90–94. doi 10.7868/S0367059714020103]
Жуйкова Т.В., Северюхина О.А., Безель В.С., Прушинская Н.М. Реакция мужского гаметофита Taraxacum officinale s.l. на химическое загрязнение среды // Сибирский экологич. журн. 2007. № 3. С. 511–516.
Жуйкова Т.В., Мелинг Э.В., Кайгородова С.Ю. и др. Особенности почв и травянистых растительных сообществ в условиях техногенеза на Среднем Урале // Экология. 2015. № 3. С. 163–172. [Zhuikova T.V., Me-ling E.V., Kaigorodova S.Y. et al. Specific features of soils and herbaceous plant communities in industrially polluted areas of the Middle Urals // Rus. J. of Ecology. 2015. V. 46. № 3. P. 213–221. doi 10.7868/S0367059715030130]
Global Environmental Monitoring System (GEMS): Action Plan for Phase I. SCOPE Rep. 3, Toronto, Canada, 1973. 132 p.
Школьник М.Я., Алексеева-Попова Н.В. Растения в экстремальных условиях минерального питания: эколого-физиологические исследования. Л.: Наука, 1983. 176 с.
Ritz C. Toward a unified approach to dose–response modeling in ecotoxicology // Environmental Toxicology and Chemistry. 2010. V. 29. № 1. P. 220–229. https://doi.org/10.1002/etc.7
Ritz C., Streibig J.C. Bioassay analysis using R // J. Stat. Softw. 2005. V. 12. № 5. P. 1–22.
Burnham K.P., Anderson D.R. Model selection and multimodel inference: A practical information-theoretic approach. NewYork: Springer, 2002. 488 p.
Жуйкова Т.В. Реакция ценопопуляций и травянистых сообществ на химическое загрязнение среды: Автореф. дис. … докт. биол. наук. Екатеринбург, 2009. 40 с.
Petrova S., Yurkova L., Velcheva I. Taraxacum officinale as a biomonitor of metals and toxic elements (Plovdiv, Bulgaria) // Bulgarian J. of Agricultural Science. 2013. V. 19. № 2. P. 241–247.
Giacomino A., Malandrino M., Colombo M.L. et al. Metal content in dandelion (Taraxacum officinale) leaves: influence of vehicular traffic and safety upon consumption as food // J. of Chemistry. 2016. V. 2016. P. 9. https://doi.org/10.1155/2016/9842987
Królak E. Accumulation of Zn, Cu, Pb and Cd by dandelion (Taraxacum officinale Web.) in Environments with various degrees of metallic contamination // Polish J. of Environmental Studies. 2003. V. 12. № 6. P. 713–721.
Жуйкова Т.В., Позолотина В.Н., Безель В.С. Разные стратегии адаптации растений к токсическому загрязнению среды тяжелыми металлами (на примере Taraxacum officinale s.l.) // Экология. 1999. № 3. С. 189–196. [Zhuikova T.V., Pozolotina V.N., Bezel’ V.S. Different strategies of plant adaptation to toxic environmental pollution with heavy metals: An example of Taraxacum officinale s.l. // Rus. J. of Ecology. 1999. V. 30. № 3. P. 189–196.]
Шитиков В.К., Терехова В.А., Узбеков Б.А. и др. Модели “доза–эффект” для оценки экологического риска при техногенном загрязнении почвы // Принципы экологии. 2015. № 3. С. 73–88.
Kopittke P.M., Blamey F.P., Asher C.J., Menzies N.W. Trace metal phytotoxicity in solution culture: a review // J. Exp. Botany. 2010. V. 61. № 4. P. 945–954.
Pozolotina V.N., Antonova E.V. Temporal variability of the Taraxacum officinale seed progeny from the East-Ural radioactive trace: is there an interaction between low level radiation and weather condition? // Internat. J. of Radiation Biology. 2017. V. 93. № 3. P. 330–339.
Maleci L., Buffa G., Wahsha M., Bini C. Morphological changes induced by heavy metals in dandelion (Taraxacum officinale Web.) growing on mine soils // J. of Soils and Sediments. 2014. V. 14. № 4. P. 731–743. https://doi.org/10.1007/s11368-013-0823-y
Дополнительные материалы отсутствуют.


