Доклады Российской академии наук. Науки о жизни, 2022, T. 502, № 1, стр. 10-14
ВЛИЯНИЕ НАНОЧАСТИЦ ЗОЛОТА НА УСТОЙЧИВОСТЬ ПШЕНИЦЫ К НИЗКОЙ ТЕМПЕРАТУРЕ
Ю. В. Венжик 1, *, А. Н. Дерябин 1, В. Н. Попов 1, Л. А. Дыкман 2, член-корреспондент РАН А. Ф. Титов 3, И. Е. Мошков 1
1 Институт физиологии растений им. К.А. Тимирязева Российской академии наук
Москва, Россия
2 Институт биохимии и физиологии растений
и микроорганизмов Российской академии наук
Саратов, Россия
3 Институт биологии – обособленное подразделение Федерального исследовательского центра “Карельский научный центр Российской академии наук”
Петрозаводск, Россия
* E-mail: jul.venzhik@gmail.com
Поступила в редакцию 05.07.2021
После доработки 31.08.2021
Принята к публикации 03.09.2021
- EDN: LVKDFA
- DOI: 10.31857/S2686738922010218
Аннотация
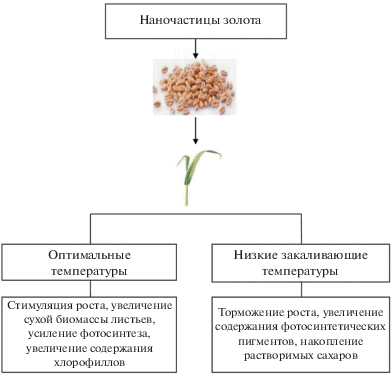
Впервые показано, что обработка семян озимой пшеницы (Triticum aestivum L.) наночастицами золота (средний диаметр 15.3 нм; концентрация раствора 20 мкг/мл) увеличивает устойчивость проростков к низкой температуре. Установлено, что увеличение устойчивости растений под влиянием наночастиц сопровождается рядом изменений, зависящих от температурных условий. Если в условиях оптимальных температур наночастицы золота стимулировали рост пшеницы и активность фотосинтетического аппарата, то в условиях низкой закаливающей температуры (2°С, 7 сут) они ингибировали рост, но поддерживали фотосинтетическую активность, способствуя накоплению в листьях растворимых сахаров – криопротекторов. Сделан вывод, что наночастицы золота могут рассматриваться в качестве адаптогенов, повышающих устойчивость растений к низким температурам, однако их эффективность в этом качестве и тонкие механизмы действия требуют дальнейшего изучения.
Проблема поиска адаптогенов, способных увеличивать стрессоустойчивость растений, является одной из важнейших в биологии и сельском хозяйстве. Мощное развитие нанотехнологий наряду с возрастающим интересом к эффектам наночастиц на живые организмы открыли большие перспективы для использования наноматериалов в этом направлении [1, 2].
Золотые наночастицы (ЗНЧ) обладают уникальными физическими, оптическими и химическими свойствами, благодаря которым легко проникают в растительный организм и перемещаются внутри него, накапливаясь в клетках и тканях [3, 4]. Показано, что ЗНЧ в низких концентрациях стимулируют ростовые процессы [5], усиливают водный обмен [6], интенсивность фотосинтеза и скорость электронного транспорта [7, 8], увеличивают содержание фотосинтетических пигментов и активность антиоксидантных ферментов [9, 10], а также влияют на экспрессию генов, ответственных за рост и развитие растений [6]. К настоящему времени разработан ряд протоколов для получения искусственных ЗНЧ различных размеров, формы и свойств [11, 12], а доступность этих методов позволяет широко использовать ЗНЧ в экспериментальных исследованиях [1]. Однако сведения о влиянии ЗНЧ на стрессоустойчивость растений в литературе не обнаружены. Опираясь на экспериментальные данные о влиянии ЗНЧ на метаболизм растений, мы предположили, что они способны модулировать их устойчивость к низким температурам.
В данном исследовании впервые установлено, что обработка семян пшеницы ЗНЧ увеличивает холодоустойчивость проростков, а также влияет на рост, активность фотосинтетического аппарата (ФСА) и накопление растворимых сахаров в листьях, причем характер этих адаптивных изменений определяется температурными условиями опыта.
Золотые наносферы были получены цитратным методом с использованием реакции восстановления золотохлористоводородной кислоты цитратом натрия [11]. Полученные ЗНЧ были охарактеризованы методами трансмиссионной электронной микроскопии (ТЭМ), спектрофотометрии и динамического светорассеяния [13]. По данным измерений, средний диаметр золотых наносфер составил 15.3 нм, а число наночастиц в 1 мл – 1.6 × 1012 [13]. В опытах использовали водный раствор с концентрацией ЗНЧ 20 мкг/мл.
Семена пшеницы (Triticum aestivum L.) морозостойкого сорта Московская 39 замачивали в растворе ЗНЧ на 24 ч, после чего проращивали на дистиллированной воде при 22°С, относительной влажности воздуха 60–70%, освещенности 100 мкмоль/(м2с) и 16-часовом фотопериоде. Через 10 сут часть проростков закаливали в климатической камере KBW-240 (Binder, Германия) при 2°С в течение 7 сут, сохраняя прочие условия неизменными. Устойчивость закаленных и незакаленных проростков к низким температурам оценивали по выходу электролитов из тканей листа [14], после их 24 ч промораживания в климатической камере MIR-153 (Sanyo, Япония) при температуре –3, –5, –7 и –9°С. Среднюю скорость роста первого листа определяли по формуле: (S2–S1)/T, где S1 – результат первого замера длины листа; S2 – результат последнего замера; T – количество дней между замерами. Изучение СО2-газообмена растений проводили на установке открытого типа с инфракрасным газоанализатором URAS2T (Германия) при 22°C и 2°C. Содержание пигментов в листьях определяли спектрофотометрически по Wellburn [15]. Для оценки содержания глюкозы в листьях использовали набор Глюкоза-Ольвекс (Ольвекс диагностикум, Россия). Содержание сахарозы и фруктозы определяли методом Рое с модификациями [16]. Все эксперименты проводили в 3–6 биологических и 3–4 аналитических повторностях. В таблицах представлены среднеарифметические значения опыта и их стандартные ошибки. Статистическую значимость различий между средними оценивали на основании t-критерия Стьюдента. В статье обсуждаются только величины, статистически значимые при р ≤ 0.05.
В результате исследования установлено, что обработка семян пшеницы ЗНЧ увеличивала холодоустойчивость как незакаленных, так и закаленных проростков. У незакаленных растений, обработанных ЗНЧ, выход электролитов из тканей листьев после промораживания при –3°C и –5°C был на 10–15% ниже, чем у необработанных проростков (табл. 1).
Таблица 1.
Влияние наночастиц золота (ЗНЧ) на выход электролитов (%) из тканей листьев незакаленных и закаленных (2°С, 7 сут) проростков пшеницы после 24 ч промораживания при заданной температуре
| Температура, оС | Незакаленные проростки | Закаленные проростки | ||
|---|---|---|---|---|
| контроль | ЗНЧ | контроль | ЗНЧ | |
| –3 | 35.4 ± 5.3 | 20.0 ± 1.6 | 11.0 ± 1.2 | 12.7 ± 0.6 |
| –5 | 57.3 ± 3.3 | 47.2 ± 2.2 | 16.3 ± 0.6 | 16.3 ± 2.0 |
| –7 | 70.3 ± 3.1 | 67.7 ± 2.3 | 20.3 ± 1.2 | 16.5 ± 1.3 |
| –9 | –* | –* | 35.2 ± 1.2 | 26.6 ± 1.7 |
Снижение температуры промораживания до –7°C и –9°C приводило к гибели незакаленных растений (выход электролитов из тканей составлял 70% и более). Закаленные растения отличались большей устойчивостью, и выход электролитов из тканей листьев даже после промораживания при –9°C у них оставался на уровне 26–35% от полного, что свидетельствует о сохранении ими жизнеспособности (табл. 1). При этом обработка ЗНЧ повышала устойчивость закаленных проростков, по сравнению с необработанными (табл. 1).
Обработка ЗНЧ влияла на рост первого листа пшеницы, причем характер изменения роста зависел от температурных условий опыта. У незакаленных проростков в обычных температурных условиях ЗНЧ увеличивали среднюю скорость роста листа на 60% (табл. 2). В условиях охлаждения (2°С, 7 сут) средняя скорость роста обработанных ЗНЧ проростков снижалась на 30% по сравнению с закаленными, но необработанными проростками (табл. 2). Анализ накопления сухой биомассы побегов показал, что обработка ЗНЧ усиливала этот процесс в оптимальных температурных условиях, а низкотемпературное закаливание приводило к значительному увеличению этого показателя вне зависимости от обработки ЗНЧ (табл. 2).
Таблица 2.
Влияние наночастиц золота (ЗНЧ) на рост, фотосинтез, содержание пигментов и сахаров в листьях незакаленных и закаленных (2°С, 7 сут) проростков пшеницы
| Показатели | Незакаленные проростки | Закаленные проростки | ||
|---|---|---|---|---|
| контроль | ЗНЧ | контроль | ЗНЧ | |
| Средняя скорость роста листа, мм/сут | 5.2 ± 0.6a | 8.3 ± 1.0b | 4.2 ± 0.3a | 2.9 ± 0.4с |
| Сухая масса листьев, % | 14.1 ± 0.3a | 15.9 ± 0.5b | 18.3 ± 0.6с | 18.5 ± 0.5с |
| Фотосинтез, мг СО2/г сухой массы ч | 7.2 ± 0.5a | 10.8 ± 0.5b | 3.7 ± 0.2c | 4.5 ± 0.2c |
| Хлорофиллы (a+b), мг/г сухой массы | 7.7 ± 0.1a | 8.5 ± 0.1b | 8.5 ± 0.1b | 9.1 ± 0.1c |
| Каротиноиды, мг/г сухой массы | 1.2 ± 0.1a | 1.3 ± 0.1a | 1.5 ± 0.03b | 1.6 ± 0.03с |
| Сахароза, мг/г сухой массы | 31.4 ± 2.0a | 28.0 ± 1.7a | 108.8 ± 5.5b | 122.9 ± 1.8c |
| Фруктоза, мг/г сухой массы | 6.0 ± 0.6a | 9.0 ± 0.8b | 24.6 ± 2.7c | 26.5 ± 2.2c |
| Глюкоза, мг/г сухой массы | 79.8 ± 1.7a | 77.6 ± 2.1a | 104.3 ± 3.0b | 96.3 ± 2.4b |
| Сумма сахаров, мг/г сухой массы | 117.2 ± 4.2a | 114.6 ± 2.6a | 234.3 ± 2.9b | 245.7 ± 3.8c |
В литературе встречаются сходные сведения о влиянии ЗНЧ на рост и развитие растений в условиях оптимальных температур. В частности, ЗНЧ размером до 50 нм и в концентрациях до 200 мкг/мл стимулировали рост арбуза [9], горчицы [5], арабидопсиса [6] и кукурузы [10]. Более того, на примере арабидопсиса показано, что ЗНЧ (диаметр 24 нм; концентрации растворов 10 и 80 мкг/мл) не только усиливали темпы роста растений, но и изменяли уровень экспрессии ряда микроРНК, участвующих в регуляции их развития [6].
Изучение активности фотосинтетического аппарата (ФСА) выявило, что ЗНЧ увеличивают интенсивность фотосинтеза незакаленных проростков примерно на 50% (табл. 2). Закаливание тормозило фотосинтез, однако у обработанных ЗНЧ растений этот показатель был несколько выше, чем у необработанных (табл. 2). Кроме того, обработка ЗНЧ приводила к увеличению содержания хлорофиллов в листьях как незакаленных, так и закаленных проростков (табл. 2). Содержание каротиноидов также несколько возрастало под влиянием ЗНЧ, но только у закаленных растений (табл. 2).
Способность ЗНЧ влиять на ФСА растений связывают с эффектом плазмонного резонанса, который характерен для этих наночастиц [3]. Суть эффекта заключается в том, что высокая активность электронов на поверхности ЗНЧ многократно увеличивается за счет коллективных колебаний под влиянием света определенной длины волны [3]. Благодаря этому эффекту активные электроны на поверхности ЗНЧ способны “улавливать” фотоны света и облегчать передачу энергии в светособирающем комплексе [7, 8]. При этом более чем в 10 раз увеличивается количество возбужденных электронов и многократно усиливается абсорбция света [7, 8]. Увеличение содержания фотосинтетических пигментов (табл. 2), происходящее под влиянием ЗНЧ, с одной стороны, может быть связано с усилением интенсивности процесса фотосинтеза, а с другой стороны, со способностью ЗНЧ влиять на экспрессию генов, контролирующих работу ФСА. Показано, например, что наночастицы оксида титана изменяли экспрессию генов, включенных в синтез основного фотосинтетического фермента рибулозобифосфаткарбоксилазы, а также модифицировали белки светособирающего комплекса [17]. Наночастицы оксида цинка влияли на экспрессию генов синтеза хлорофиллов, каротиноидов и структурных белков фотосистемы I [18].
Согласно полученным данным о накоплении растворимых сахаров в листьях пшеницы, незакаленные проростки существенно не различались по их суммарному содержанию, хотя в варианте с ЗНЧ количество фруктозы было выше (табл. 2). Низкотемпературное закаливание более чем в 2 раза увеличивало суммарное содержание растворимых сахаров в листьях обработанных и необработанных ЗНЧ растений, причем в обоих вариантах накопление сахаров происходило в результате повышения содержания всех их форм, но особенно за счет накопления сахарозы (табл. 2). Следует отметить, что содержание глюкозы и фруктозы в листьях пшеницы в период закаливания также возрастало, однако достоверных различий по их содержанию между вариантами не выявлено (табл. 2).
Полученные нами данные свидетельствуют о том, что благодаря своим уникальным свойствам ЗНЧ способны оказывать регулирующее воздействие на интенсивность таких важных процессов в растительном организме, как рост и фотосинтез (табл. 2). Известно, что именно баланс между ними во многом обеспечивает выживаемость и устойчивость растений в неблагоприятных условиях среды [19]. В условиях низких закаливающих температур этот баланс необходим для накопления совместимых осмолитов и резервных веществ, важнейшими из которых являются углеводы. Накапливаясь в цитоплазме и строме пластид, углеводы не только снижают водный потенциал, предотвращая дегидратацию тканей, но и выступают в качестве своеобразных “криопротекторов”, а также являются резервными веществами, необходимыми для энергоемкого процесса адаптации [19]. Под влиянием ЗНЧ в условиях низкотемпературного закаливания увеличивается не только содержание хлорофиллов, но и каротиноидов (табл. 2), которые, как известно, защищают хлорофиллы и липиды мембран от фотодеструкции, участвуя в рассеивании тепловой энергии, избыточной в условиях охлаждения [20]. Увеличение содержания всех форм фотосинтетических пигментов свидетельствует о стабильности структуры фотосинтетических мембран и об отсутствии повреждений в работе ФСА в период закаливания.
Таким образом, впервые показано, что обработка семян пшеницы ЗНЧ повышает холодоустойчивость растений. Увеличение устойчивости пшеницы под влиянием ЗНЧ сопровождалось рядом адаптивных изменений, зависящих от температурных условий опыта (см. рис. 1). В условиях оптимальных температур ЗНЧ усиливали интенсивность роста и фотосинтеза, тогда как в условиях низкотемпературного закаливания поддерживали программу холодовой адаптации, а именно усиливали торможение роста растений, сохраняя активность ФСА и обеспечивая накопление растворимых сахаров, играющих очень важную роль в процессе формирования устойчивости к низкотемпературному стрессу. Полученные данные свидетельствуют о способности ЗНЧ выступать в качестве адаптогенов, увеличивающих стрессоустойчивость растений, а их эффективность в этом качестве и тонкие механизмы действия требуют дальнейшего изучения.
ИСТОЧНИКИ ФИНАНСИРОВАНИЯРабота выполнена в рамках государственного задания Министерства науки и высшего образования Российской Федерации (темы № 121040800153-1 и 121031100266-3).
Список литературы
Венжик Ю.В., Мошков И.Е., Дыкман Л.А. Наночастицы золота в физиологии растений: основные эффекты и перспективы использования // Физиология растений. 2021. Т. 68. № 3. С. 245–257.
Tarrahi R., Mahjouri S., Khataee A. A review on in vivo and in vitro nanotoxicological studies in plants: A headlight for future targets // Ecotoxicol. Environ. Saf. 2021. V. 208. P. 111697.
Sarfraz N., Khan I. Plasmonic gold nanoparticles (AuNPs): properties, synthesis and their advanced energy, environmental and biomedical applications // Chem. Asian J. 2021. V. 16. № 7. P. 720–742.
Siddiqi K.S., Husen A. Engineered gold nanoparticles and plant adaptation potential // Nanoscale Res. Let. 2016. V. 11. P. 400.
Arora S., Sharma P., Kumar S., et al. Gold-nanoparticle induced enhancement in growth and seed yield of Brassica juncea // Plant Growth Regul. 2012. V. 66. № 3. P. 303–310.
Kumar V., Guleria P., Kumar V., et al. Gold nanoparticle exposure induces growth and yield enhancement in Arabidopsis thaliana // Sci. Total Environ. 2013. V. 461–462. P. 462–468.
Das S., Debnath N., Pradhan S., et al. Enhancement of photon absorption in the light-harvesting complex of isolated chloroplast in the presence of plasmonic gold nanosol – a nanobionic approach towards photosynthesis and plant primary growth augmentation // Gold Bull. 2017. V. 50. P. 247–257.
Torres R., Diz V., Lagorio M.G. Effects of gold nanoparticles on the photophysical and photosynthetic parameters of leaves and chloroplasts // Photochem. Photobiol. Sci. 2018. V. 17. № 4. P. 505–516.
Wan Y., Li J., Ren H., et al. Physiological investigation of gold nanorods toward watermelon // J. Nanosci. Nanotechnol. 2014. V. 14. № 8. P. 6089–6094.
Mahakham W., Theerakulpisut P., Maensiri S., et al. Environmentally benign synthesis of phytochemicals-capped gold nanoparticles as nanopriming agent for promoting maize seed germination // Sci. Total Environ. 2016. V. 573. P. 1089–1102.
Дыкман Л.А., Хлебцов Н.Г. Методы химического синтеза коллоидного золота // Успехи химии. 2019. Т. 88. № 3. С. 229–247.
Qiao J., Qi L. Recent progress in plant-gold nanoparticles fabrication methods and bio-applications // Talanta. 2021. V. 223. Pt. 2. P. 121396.
Khlebtsov N.G., Dykman L.A. Optical properties and biomedical applications of plasmonic nanoparticles // J. Quant. Spectrosc. Radiat. Transfer. 2010. V. 111. № 1. P. 1–35.
Гришенкова Н.Н., Лукаткин А.С. Oпределение устойчивости растительных тканей к абиотическим стрессам с использованием кондуктометрического метода // Поволжский экологический журнал. 2005. № 1. С. 3–11.
Wellburn A.R. The spectral determination of chlorophyll a and b, as well as total carotenoids, using various solvents with spectrophotometers of different resolution // J. Plant Physiol. 1994. V. 144. № 3. P. 307–313.
Nakamura M. Determination of fructose in the presence of a large excess of glucose. Part IV. A modified resorcinol-thiourea-hydrochloric acid reaction // Agr. Biol. Chem. 1967. V. 32. № 6. P. 696–700.
Hasanpour H., Maali-Amiri R., Zeinali H. Effect of TiO2 nanoparticles on metabolic limitations to photosynthesis under cold in chickpea // Russ. J. Plant Physl. 2015. V. 62. № 6. P. 779–787.
Wang X., Yang X., Chen S., et al. Zinc oxide nanoparticles affect biomass accumulation and photosynthesis in Arabidopsis // Plant Sci. 2016. V. 6. P. 1243.
John R., Anjum R.A., Sopory S.K., et al. Some key physiological and molecular processes of cold acclimation // Biol. Plant. 2016 V. 60. № 4. P. 603–618.
Маслова Т.Г., Марковская Е.Ф., Слемнев Н.Н. Функции каротиноидов в листьях высших растений (обзор) // Журнал общей биологии. 2020. Т. 81. № 4. С. 297–310.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о жизни