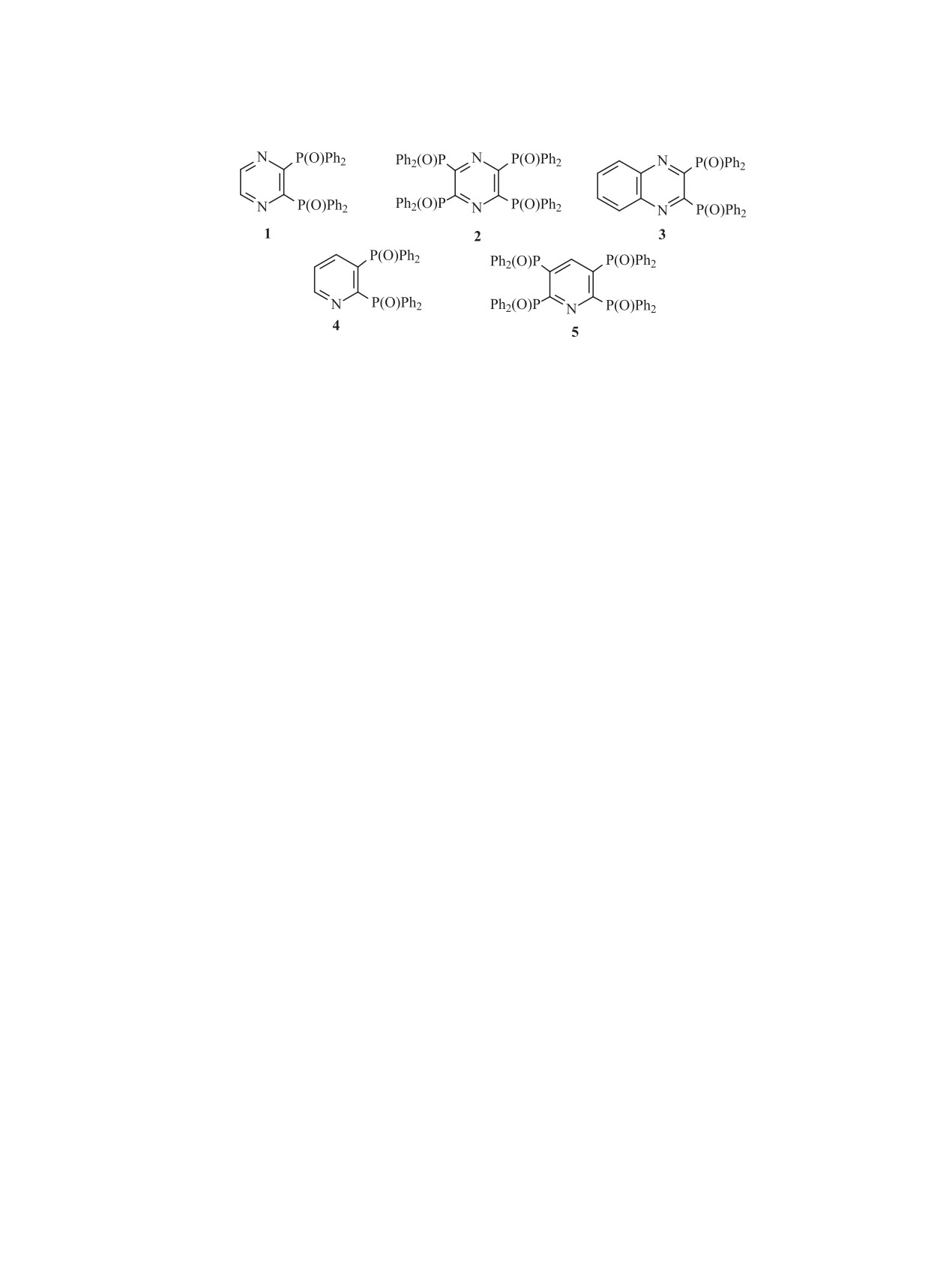
РАДИОХИМИЯ, 2023, том 65, № 6, с. 532-537
УДК 542.61:546.442
ЭКСТРАКЦИЯ АКТИНИДОВ И ЛАНТАНИДОВ
ИЗ АЗОТНОКИСЛЫХ РАСТВОРОВ
ФОСФОРИЛИРОВАННЫМИ ПИРАЗИНАМИ
© 2023 г. А. Н. Туранова, В. К. Карандашевб, О. И. Артюшинв,
Е. В. Смирновав, Г. В. Костиковаг, А. М. Федосеевг, В. К. Брельв,*
а Институт физики твердого тела им. Ю. А. Осипьяна РАН,
142432, Черноголовка Московской обл., ул. Академика Осипьяна, д. 2
б Институт проблем технологии микроэлектроники и особо чистых материалов РАН,
142432, Черноголовка Московской обл., ул. Академика Осипьяна, д. 6
в Институт элементоорганических соединений им. А. Н. Несмеянова РАН,
119334, Москва, ул. Вавилова, д. 28, стр. 1
г Институт физической химии и электрохимии им. А. Н. Фрумкина РАН,
119991, Москва, Ленинский пр., д. 31, корп. 4
* e-mail: v_brel@mail.ru
Поступила в редакцию 30.06.2023, после доработки 14.11.2023, принята к публикации 15.11.2023
Изучена экстракция U(VI), Th(IV), Am(III) и лантанидов(III) из растворов азотной кислоты растворами
фосфорилированных пиразинов в органических растворителях. Определена стехиометрия извлекаемых
комплексов, рассмотрено влияние строения экстрагента и концентрации HNO3 в водной фазе на
эффективность извлечения ионов металлов в органическую фазу. Установлено, что среди изученных
соединений наиболее высокой экстракционной способностью по отношению к актинидам и лантанидам
в азотнокислых средах обладает диоксид бис(дифенилфосфин)хиноксалина.
Ключевые слова: экстракция, уран(VI), торий(IV), америций(III), лантаниды(III), фосфорилированные
пиразины.
DOI: 10.31857/S0033831123060059, EDN: NZEFZO
В процессах переработки отработанного ядер-
и пиридиновый атом азота, который является «мяг-
ного топлива для концентрирования и разделения
ким» донором, показал высокую селективность при
актинидов и лантанидов широко используются экс-
разделении пар Am/Eu и Am/Cm [11].
тракционные методы [1]. Высокой экстракционной
Ранее нами были исследованы экстракционные
способностью по отношению к актинидам и ланта-
свойства 2,3-(дифенилфосфорил)пиридина в азот-
нидам в азотнокислых средах обладают полифунк-
нокислых средах [14, 15]. Это соединение содер-
циональные фосфорорганические реагенты [2-5].
жит две фосфорильные группы, присоединенные
Опубликовано большое число работ, посвященных
к N-гетероциклическому фрагменту. Известно, что
использованию амидов N-гетероциклических кар-
диоксиды алкилендифосфинов обладают высокой
боновых и дикарбоновых кислот для разделения
экстракционной способностью по отношению к
актинидов и лантанидов [6-10]. В последнее вре-
актинидам и лантанидам. Природа мостика между
мя возрос интерес к исследованию экстракцион-
двумя дифенилфосфорильными группами молеку-
ных свойств N,О-донорных лигандов, имеющих в
лы диоксидов дифосфинов существенно влияет на
своем составе фосфиноксидные фрагменты, закре-
их экстракционную способность [16]. Диоксид те-
пленные на N-гетероциклическом каркасе [11-13].
трафенилэтилендифосфина экстрагирует актиниды
Например, 2,6-(дифенилфосфорил)пиридин, содер-
и лантаниды из азотнокислых растворов значитель-
жащий как «жесткие» Р=О-донорные центры, так
но менее эффективно, чем диоксид тетрафенилме-
532
ЭКСТР
АКЦИЯ АКТИНИДОВ И ЛАНТАНИДОВ
533
Схема 1.
тилендифосфина (ТФМДФО) [16]. Это связано с
ки х.ч. Растворы экстрагентов в органических рас-
тем, что увеличение длины алкиленового мостика в
творителях готовили по точным навескам.
молекуле ТФМДФО приводит к разрушению систе-
Распределение Ln(III), U(VI) и Th(IV) в экстрак-
мы сопряженных связей, возникающих при образо-
ционных системах изучали в интервале концентра-
вании шестичленного хелатного цикла в результате
ции HNO3 0.3-7.0 моль/л. Исходные водные раство-
комплексообразования ТФМДФО с ионами акти-
ры с концентрацией каждого элемента 2 × 10-6 моль/л
нидов и лантанидов [16]. В то же время замена в
готовили растворением соответствующих нитратов
молекуле диоксида этиленового мостика между
в воде с последующим добавлением HNO3 до тре-
фосфорильными группами на виниленовый приво-
буемой концентрации. Все Ln(III) (кроме Pm) при-
дит к восстановлению системы сопряженных свя-
сутствовали в исходных водных растворах. Исполь-
зей, несмотря на образование семичленного цикла
зуемые реактивы соответствовали марке х.ч.
при комплексообразовании этого лиганда с ионами
Опыты по экстракции проводили в пробирках с
металлов [17-19]. Это приводит к значительному
притёртыми пробками при температуре 21 ± 1°С и
повышению коэффициентов распределения U(VI) и
соотношении объёмов органической и водной фаз
Am(III) при их экстракции из азотнокислых раство-
1 : 1. Контакт фаз осуществляли на роторном аппа-
ров [17-19]. По этой же причине замена этилено-
рате для перемешивания со скоростью 60 об/мин в
вого мостика на о-фениленовый [20, 21] или пири-
течение 1 ч. Предварительно установлено, что этого
диновый [15] фрагменты приводит к резкому повы-
времени достаточно для установления постоянных
шению коэффициентов распределения актинидов и
значений коэффициентов распределения (D).
лантанидов.
Содержание Ln(III), U(VI) и Th(IV) в исходных
Цель данной работы - исследование влияния
и равновесных водных растворах определяли ме-
строения фосфорилированных пиразинов на эф-
тодом масс-спектрометрии с ионизацией пробы в
фективность экстракции актинидов и лантанидов
индуктивно связанной плазме с использованием
из азотнокислых растворов. Для этого рассмотрено
масс-спектрометра XSeries 2 (Thermo Scientific,
межфазное распределение U(VI), Th(IV), Am(III) и
США). Содержание элементов в органической фазе
Ln(III) между растворами HNO3 и органической фа-
определяли по разнице концентраций в водном рас-
зой, содержащей соединения 1-3. Эффективность
творе до и после экстракции. Коэффициенты рас-
экстракции ионов металлов этими экстрагентами
пределения элементов рассчитывали как отношение
сопоставлена с данными по экстракции фосфори-
их концентраций в равновесных фазах. Погреш-
лированными пиридинами 4 и 5 [15] (Схема 1).
ность определения коэффициентов распределения
не превышала 10%. Коэффициенты распределения
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
241Am(III) определяли как отношение γ-активности
аликвот равновесных органической и водной фаз.
Синтез соединений 1-3 описан в работе [22]. В
Концентрацию HNO3 в равновесных водных фазах
качестве органических растворителей использова-
определяли потенциометрическим титрованием
ли 1,2-дихлорэтан, нитробензол и хлороформ мар-
раствором NaOH.
РАДИОХИМИЯ том 65 № 6 2023
534
ТУРАНОВ и др.
2.0
1
3
1.5
2
3
1
1.0
4
2
2
3
4
0.5
5
1
6
0.0
0
-0.5
-1.0
-1
-1.5
-1.0
-0.5
0.0
0.5
1.0
-4.5
-4.0
-3.5
-3.0
-2.5
-2.0
lg[HNO3]
lg[L]
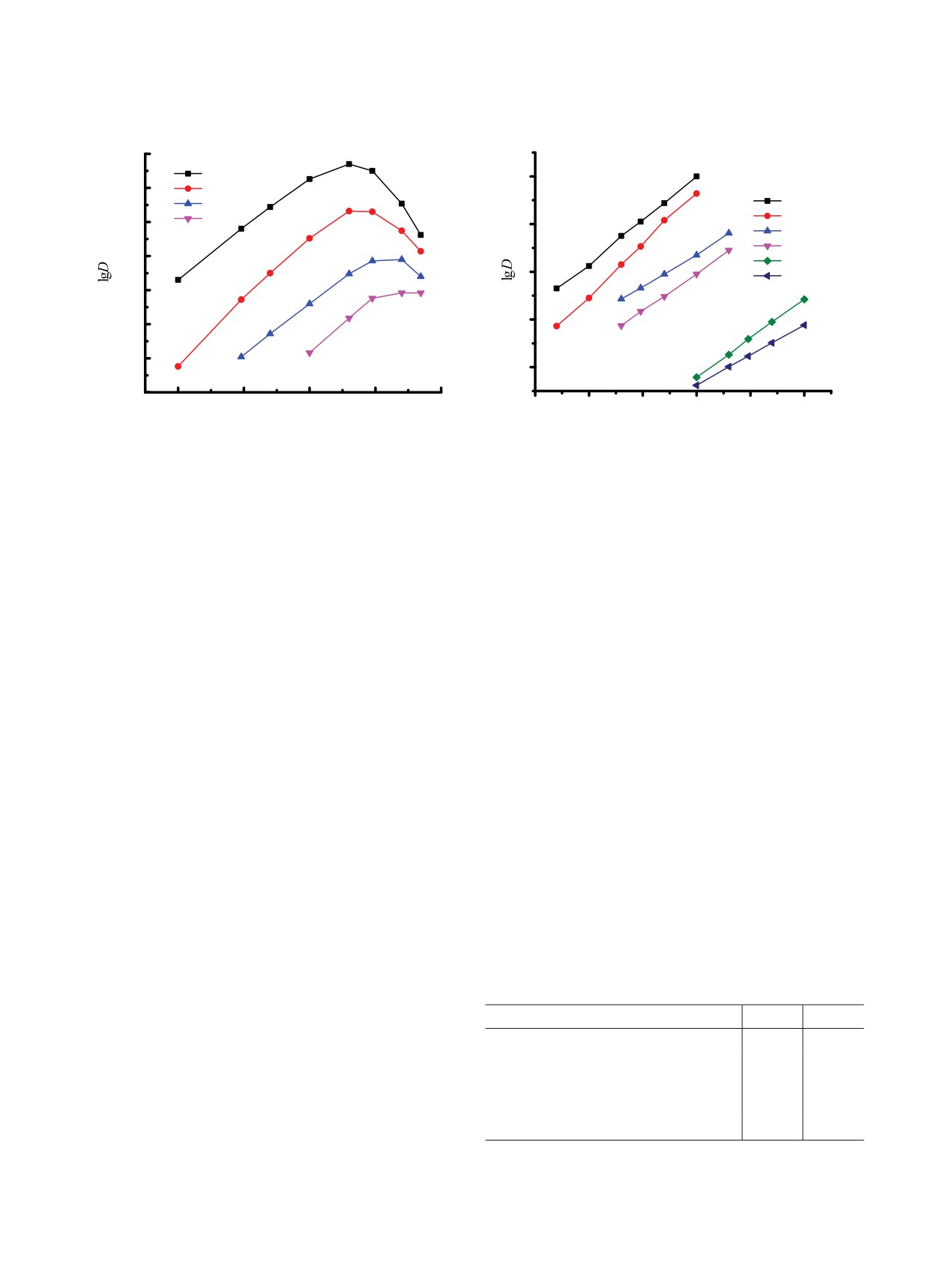
Рис. 1. Зависимость коэффициентов распределения U (1,
Рис. 2. Зависимость коэффициентов распределения U (1,
3) и Th (2, 4) от концентрации HNO3 в водной фазе при
3, 6) и Th (2, 4, 5) от концентрации соединений 1 (5, 6),
экстракции растворами 0.0002 моль/л соединений 3 (1, 3)
2 (3, 4) и 3 (1, 2) в дихлорэтане при экстракции из раство-
и 2 (2, 4) в дихлорэтане.
ра 3 моль/л HNO3.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
соответственно) (рис. 2). Соединение 3 экстрагиру-
ет Th(IV) в виде ди- и трисольватов, а соединения 1 и
Рассмотрено влияние концентрации HNO3 в рав-
2 - в виде моно- и дисольватов (тангенс угла накло-
новесной водной фазе на коэффициенты распреде-
на зависимости lgDTh-lg[L] составляет 1.64 ± 0.1,
ления U(VI) и Th(IV) при экстракции растворами
1.57 ± 0.11 и 2.25 ± 0.1 для соединений 1, 2 и 3 со-
соединений 1 и 3 в дихлорэтане (рис. 1). Наблюдае-
ответственно).
мая при этом зависимость D-[HNO3] с максимумом
Сопоставление данных по экстракции ио-
соответствует экстракции координационно-сольва-
нов Ln(III) из азотнокислых растворов реагента-
тированных нитратов U(VI) и Th(IV) и связана с вы-
ми 1-4 (рис. 3) показало, что соединение 1 с пира-
саливающим действием ионов NO– и связыванием
экстрагентов азотной кислотой.
зиновым фрагментом между Р(О)-группами экстра-
гирует ионы Ln(III) значительно менее эффективно,
Сопоставление данных по экстракции U(VI) и
чем соединение 4 с пиридиновым фрагментом.
Th(IV) реагентами 1-5 (табл. 1) показало, что сое-
динения 1 и 2 с пиразиновыми фрагментами между
Увеличение числа фосфорильных групп в моле-
Р(О)-группами экстрагируют эти ионы значительно
куле соединения 2 по сравнению с соединением 1
менее эффективно, чем диоксиды 4 и 5 с пириди-
приводит к увеличению его экстракционной спо-
новыми группами. Из рассмотренных фосфорили-
собности по отношению к легким и тяжелым ланта-
рованных пиразинов экстрагент 3, в молекуле ко-
нидам(III). При экстракции Eu(III)-Tb(III) значения
торого две Р=О-группы связаны хиноксалиновым
DLn несколько больше в системе с 1, чем с 2.
циклом, извлекает U(VI) и Th(IV) в органическую
Таблица
1. Коэффициенты распределения U(VI) и
фазу наиболее эффективно. Отметим, что соеди-
Th(IV) при экстракции растворами соединений 1-5 в
нения 2-5 экстрагируют U(VI) более эффективно,
дихлорэтане из раствора 3 моль/л HNO3
чем Th(IV), тогда как при экстракции диоксидом 1,
Соединение, концентрация (моль/л)
lgDU
lgDTh
а также ТФМДФО DTh > DU.
1, 0.01
-0.12
0.42
Методом сдвига равновесия показано, что сое-
2, 0.001
1.35
0.95
динения 1-3 экстрагируют U(VI) из азотнокислых
3, 0.001
3.0
2.64
растворов в виде моно- и дисольватов (тангенс угла
4, 0.001 [15]
3.15
2.25
наклона зависимостей lgDU-lg[L] составляет 1.26 ±
5, 0.001 [15]
3.0
1.81
0.1, 1.37 ± 0.11 и 1.74 ± 0.1 для соединений 1, 2 и 3
РАДИОХИМИЯ том 65 № 6 2023
ЭКСТР
АКЦИЯ АКТИНИДОВ И ЛАНТАНИДОВ
535
2.5
1.5
2.0
1.5
1.0
3
1.0
4
0.5
2
0.5
1
1
0.0
2
0.0
3
4
-0.5
-0.5
-1.0
-0.6
-0.4
-0.2
0.0
0.2
0.4
0.6
0.8
La Ce Pr Nd Sm Eu Gd Tb Dy Ho Er TmYb Lu
lg[HNO3]
Ln
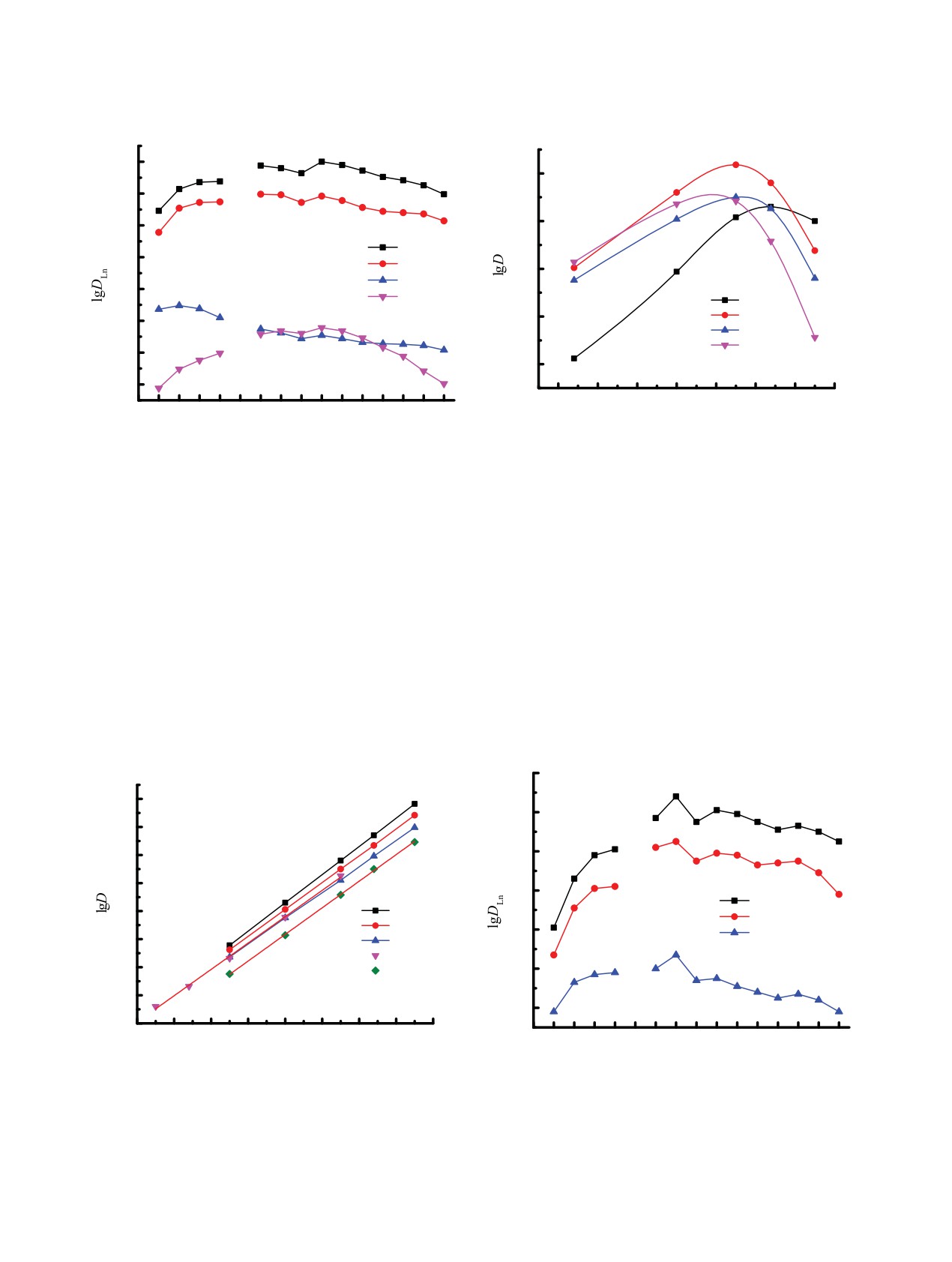
Рис.
4. Зависимость коэффициентов распределения
Рис. 3. Коэффициенты распределения Ln(III) при экс-
Lu(III) (1), Eu(III) (2), La(III) (4) и Am(III) (3) от концен-
тракции растворами
0.05 моль/л соединений
1-4 в
трации HNO3 в водной фазе при экстракции растворами
дихлорэтане из растворов 3 моль/л HNO3.
0.02 моль/л соединения 3 в дихлорэтане.
Соединение 3, в молекуле которого две Р=О-груп-
ние максимума на кривой зависимости D-[HNO3]
пы связаны хиноксалиновым циклом, экстрагирует
смещается в область большей кислотности водной
Ln(III) наиболее эффективно. Ранее методами ИК,
фазы по мере увеличения атомного номера ланта-
ЯМР 31Р спектроскопии и рентгеноструктурно-
нида от La(III) к Lu(III). Во всем исследованном
го анализа установлено, что в комплексах Ce(III)
диапазоне концентрации HNO3 Am(III) экстра-
и Nd(III) координация лиганда 3 осуществляется
гируется соединением 3 менее эффективно, чем
только за счет Р=О-групп по хелатному типу [23].
Eu(III) (рис. 4). При экстракции Am(III) и Ln(III)
При изучении влияния концентрации HNO3 в
из раствора 3 моль/л HNO3 растворами 0.02 моль/л
водной фазе на экстракцию Ln(III) и Am(III) раство-
ром соединения 3 в дихлорэтане получены зависи-
соединения 3 в дихлорэтане коэффициент разделе-
мости D-[HNO3] с максимумом (рис. 4). Положе-
ния Am(III) и Eu(III) составляет 0.48. Ранее было
1.0
2.5
0.8
2.0
1.5
0.6
1.0
0.4
1
0.5
Eu(III)
2
Ho(III)
0.2
3
0.0
Lu(III)
Am(III)
-0.5
La(III)
0.0
-1.0
-0.2
-1.5
-2.8
-2.8
-2.4
-2.2
-2.0
-1.8 -1.8 -1.4
-1.2
La Ce Pr Nd Sm Eu Gd Tb Dy Ho Er Tm Yb Lu
lg[L]
Ln
Рис. 6. Коэффициенты распределения Ln(III) при экс-
Рис.
5. Зависимость коэффициентов распределения
тракции растворами 0.01 моль/л соединения 3 в нитро-
Ln(III) и Am(III) от концентрации соединения 3 в дихлорэ-
бензоле (1), дихлорэтане (2) и хлороформе (3) из раство-
тане при экстракции из растворов 3 моль/л HNO3.
ров 3 моль/л HNO3.
РАДИОХИМИЯ том 65 № 6 2023
536
ТУРАНОВ и др.
показано, что соединение 4 также экстрагирует
КОНФЛИКТ ИНТЕРЕСОВ
Am(III) из растворов HNO3 менее эффективно, чем
Eu(III) [15].
Авторы заявляют об отсутствии конфликта ин-
тересов
Стехиометрическое соотношение Ln(III), Am(III):
СПИСОК ЛИТЕРАТУРЫ
экстрагент 3 в экстрагируемых комплексах опреде-
лено методом сдвига равновесия. Полученные дан-
1.
Myasoedov B.F., Kalmykov S.N., Kulyako Yu.M.,
ные (рис. 5) показали, что соединение 3 в дихлорэ-
Vinokurov S.E. // Geochem. Int. 2016. Vol. 54, N 13.
тане экстрагирует Ln(III) и Am(III) из азотнокислых
P. 1156.
растворов в форме ди- и трисольватов.
2.
Leoncini A., Huskens J., Verboom W. // Chem. Soc. Rev.
Природа органического растворителя оказывает
2017. Vol. 46. P. 7229.
существенное влияние на эффективность экстрак-
ции Ln(III) соединением 3 из азотнокислых раство-
3.
Wilson A.M., Bailey P.J., Tasker P.A. // Chem. Soc. Rev.
ров. Значения DLn возрастают в ряду хлороформ <
2014. Vol. 43. P. 123.
дихлорэтан < нитробензол по мере увеличения
их полярности и сольватирующей способности
4.
Werner E. J., Biros S. M. // Org. Chem. Front. 2019.
Vol. 6. P. 2067.
(рис. 6). Следует отметить, что в системе с соеди-
нением 3 величина DEu увеличивается при переходе
5.
Аляпышев М.Ю., Бабаин В.А., Устынюк Ю.А. // Успе-
от дихлорэтана к нитробензолу в 1.9 раза, тогда как
хи химии. 2016. Т. 85. N 9. С. 943; Alyapyshev M Yu.,
такой переход в системе с ТФМДФО сопровождает-
Babain V.A., Ustynyuk Yu.A. // Russ. Chem. Rev. 2016.
ся увеличением DEu в 33.6 раза [24].
Vol. 85, N 9. P. 943.
Представленные данные показали, что экстрак-
6.
Бабаин В.А., Аляпышев М.Ю., Смирнов И.В. // Ради-
ционная способность фосфорилированных пира-
охимия. 2006. Т. 48. С. 369.
зинов по отношению к актинидам и лантанидам в
7.
Аляпышев М.Ю., Бабаин В.А., Ткаченко Л.И. // Ради-
азотнокислых средах ниже, чем у фосфорилиро-
охимия. 2014. Т. 56. С. 481.
ванных пиридинов и бензолов. Возможной при-
8.
Ustynyuk Yu.A., Gloriozov I.P., Kalmykov S.N.,
чиной этого является изменение электроноакцеп-
Mitrofanov A.A., Babain V.A., Alyapyshev M.Yu.,
торных свойств гетероароматического фрагмента
Ustynyuk N.A. // Solvent Extr. Ion Exch. 2014. Vol. 32.
P. 508.
между фосфорильными группами молекул этих
соединений. В отличие от 2,6-(дифенилфосфорил)
9.
Alyapyshev M., Babain V., Borisova N., Eliseev I.,
пиридина соединения 1-3 не проявляют заметной
Kirsanov D., Kostin A., Legin A., Reshetova M.,
селективности при экстракции Am(III) и Eu(III).
Smirnova Z. // Polyhedron. 2010. Vol. 29. P. 1998.
Наиболее высокой экстракционной способностью
по отношению к рассмотренным ионам обладает
10. Alyapyshev M., Ashina J., Dar’in D., Kenf E.V.,
диоксид бис(дифенилфосфин)хиноксалина. Этот
Kirsanov D., Tkachenko L., Legin A., Starova G.,
Babain V. // RSC Adv. 2016. Vol. 6. P. 68642.
экстрагент может найти применение для эффектив-
ного извлечения актинидов и лантанидов из азотно-
11. Matveev P.I., Borisova N.E., Andreadi N.G., Zaki-
кислых растворов.
rova G.G., Petrov V.G., Belova E.V., Kalmykov S.N.,
Myasoedov B.F. // DaltonTrans. 2019. Vol. 48. P. 2554.
ФОНДОВАЯ ПОДДЕРЖКА
12. Konopkina E.A., Matveev P.I., Huang P.W.,
Kirsanova A.A., Chernysheva M.G., Sumyanova T.B.,
Работа выполнена в рамках Государственного за-
Domnikov K.S., Shi W.-Q., Kalmykov S.N., Petrov V.G.,
дания 2023 г. ИФТТ РАН, ИПТМ РАН, ИФХЭ РАН
Borisova N.E. // Dalton Trans. 2022. Vol. 51. P. 11180.
и ИНЭОС РАН. Синтез исследуемых соединений
выполнен при финансовой поддержке Российского
13. Konopkina E.A., Matveev P.I., Kharcheva A.V.,
научного фонда (грант № 20-13-00329).
Sumyanova T.B., Rozdeev A.S., Novichkov D.A.,
РАДИОХИМИЯ том 65 № 6 2023
ЭКСТР
АКЦИЯ АКТИНИДОВ И ЛАНТАНИДОВ
537
Trigub A.L., Kalle P., Kirsanova A.A., Kalmykov S.N.,
19. Розен А.М., Николотова З.И., Карташева Н.А. // Ра-
Petrov V.G., Borisova N.E. // Solvent Extr. Ion Exch.
диохимия. 1983. Т. 25, № 5. С. 609.
2023. Vol. 41. P. 627.
20. Туранов А.Н., Карандашев В.К., Артюшин О.И., Ко-
стикова Г.В., Федосеев А.М., Брель В.К. // ЖОХ. 2022.
14. Artyushin O.I., Vologzhanina A.V., Turanov A.N.,
Т. 92, № 8. С. 1289; Turanov A.N., Karandashev V.K.,
Karandashev V.K., Brel V.K. // Mendeleev Commun.
Artyushin O.I., Kostikova G.V., Fedoseev A.M.,
2021. Vol. 31. P. 306.
Brel V.K. // Russ. J. Gen. Chem. 2022. Vol. 92. P. 1479.
15. Туранов А.Н., Карандашев В.К., Артюшин О.И., Ко-
21. Turanov A.N., Karandashev V.K., Artyushin O.I.,
стикова Г.В., Федосеев А.М., Брель В.К. // Радиохи-
Brel V.K. // Solvent Extr. Ion Exch. 2020. Vol. 38. P. 166.
мия. 2023. Т. 65, № 6. С. 526-531.
16. Розен А.М., Крупнов Б.В. // Успехи химии. 1996.
22. Smirnova E.V., Artyushin O.I., Vologzhanina A.V.,
Т. 65, № 11. С. 1052; Rozen A.M., Krupnov B.V. // Russ.
Turanov A.N., Karandashev V.K., Brel V.K. // Mendeleev
Chem. Rev. 1996. Vol. 65, № 11. P. 973.
Commun. 2022. Vol. 32. P. 664.
https://doi.org/10.1070/RC1996v065n11ABEH000241
17. Беркман З.А., Бертина Л.Э., Кабачник М.И., Кос-
23. Матросов Е.И., Старикова З.А., Ходак А.А., Нифан-
сых В.Г., Медведь Т.Я., Нестерова Н.П., Розен А.М.,
Юдина К.С. // Радиохимия. 1975. Т. 17, № 2. С. 210.
тьев Э.Е. // ЖНХ. 2003. Т. 48. С. 2008.
18. Розен А.М., Николотова З.И., Карташева Н.А.,
24. Шадрин А.Ю., Смирнов И.В., Киселева Р.Н., Несте-
Медведь Т.Я., Нестерова Н.П., Юдина К.С., Кабач-
рова Н.П., Поликарпов Ю.М., Кабачник М.И. // Ради-
ник М.И. // Радиохимия. 1976. Т. 18, № 6. С. 846.
охимия. 1993. Т. 35, № 1. С. 50.
Extraction of Actinides and Lanthanides from Nitric Acid
Solutions with Phosphorylated Pyrazines
A. N. Turanova, V. K. Karandashevb, O. I. Artyushinc,
E. V. Smirnovac, G. V. Kostikovad, A. M. Fedoseevd, and V. K. Brel*c
a Osip’yan Institute of Solid State Physics, Russian Academy of Sciences,
Chernogolovka, Moscow oblast, 142432 Russia
b Institute of Microelectronics Technology and High Purity Materials, Russian Academy of Sciences,
Chernogolovka, Moscow oblast, 142432 Russia
c Nesmeyanov Institute of Organoelement Compounds, Russian Academy of Sciences,
Moscow, 119334 Ruissia
d Frumkin Institute of Physical Chemistry and Electrochemistry, Russian Academy of Sciences,
Moscow, 119991 Russia
* e-mail: v_brel@mail.ru
The extraction of U(VI), Th(IV), Am(III), and lanthanides(III) from nitric acid solutions with solutions of
phosphorylated pyrazines in organic solvents has been studied. The stoichiometry of the extracted complexes
was determined, and the influence of the structure of the extractant and the concentration of HNO3 in the
aqueous phase on the efficiency of the extraction of metal ions into the organic phase was considered. It has
been established thatm among the studied compounds, bis(diphenylphosphine)quinoxaline dioxide has the
highest extraction ability with respect to actinides and lanthanides in nitric acid media.
Keywords: extraction, uranium(VI), thorium(IV), americium(III), lanthanides(III), phosphorylated pyrazines.
РАДИОХИМИЯ том 65 № 6 2023