РАДИОХИМИЯ, 2023, том 65, № 1, с. 61-69
УДК 541.183+544.58
СИНТЕЗ, ФИЗИКО-ХИМИЧЕСКИЕ И
АДСОРБЦИОННЫЕ СВОЙСТВА
ФОСФАТОВ Ti-Ca-Mg
© 2023 г. А. И. Иванеца,*, И. Л. Шашковаа, Н. В. Китиковаа,
М. В. Масловаб, Н. В. Мудрукб, В. В. Милютинв
а Институт общей и неорганической химии НАН Беларуси, 220072, Минск, ул. Сурганова, д. 9/1
б Институт химии и технологии редких элементов и минерального сырья
им. И.В. Тананаева Кольского научного центра РАН,
184209, Апатиты Мурманской обл., ул. Ферсмана, д. 26а
в Институт физической химии и электрохимии им. А.Н. Фрумкина РАН,
119071, Москва, Ленинский пр., д. 31, корп. 4
*e-mail: Andreiivanets@yandex.ru
Поступила в редакцию 25.07.2022, после доработки 05.12.2022, принята к публикации 12.12.2022
Синтезированы сорбенты на основе фосфатов Ti-Ca-Mg, изучены их физико-химические и сорбционные
свойства по отношению к Cs(I), Sr(II), Co(II) (в виде как стабильных ионов, так и радионуклидов
137Cs, 60Co, 90Sr). Образцы TiCaMg-1 и TiCaMg-2 получали путем гетерогенного взаимодействия
кислых и средних фосфатов Ca-Mg с раствором сульфата титанил-диаммония, а образец TiCaMg-3 -
термообработанного доломита с предварительно осажденной суспензией кислого фосфата титана.
Показано, что полученные образцы обладают высоким сродством к ионам Cs+, Sr2+, Co2+ и их
радионуклидам. Образец TiCaMg-3 имеет наиболее высокие значения коэффициента распределения
радионуклидов 137Cs, 60Co и 90Sr (>105 см3/г). Установлено, что различие в свойствах композитов
обусловлено их фазовым и химическим составом, а также текстурными характеристиками (удельная
поверхность, сорбционный объем и размер пор). Сорбент TiCaMg-3 характеризуется наибольшим
сорбционным объемом (0.410 см3/г) и средним диаметром пор (10.2 нм), что обеспечивает лучшую
доступность ионогенных групп при обменных реакциях.
Ключевые слова: фосфаты титана-кальция-магния, радионуклиды, сорбция.
DOI: 10.31857/S0033831123010094, EDN: OHNVNG
ВВЕДЕНИЕ
карбонатные соединения радионуклидов
[8,
9].
Ионный обмен эффективен при выделении радио-
Развитие атомной энергетики неразрывно свя-
нуклидов, не склонных к комплексообразованию и
зано с образованием и накоплением огромных ко-
присутствующих в растворе в виде гидратирован-
личеств жидких радиоактивных отходов (ЖРО) [1].
ных ионов [10]. Мембранные методы могут приме-
Это обусловливает необходимость разработки но-
няться на различных стадиях переработки ЖРО как
вых эффективных технологий и материалов для
отдельно, так и в комбинации с другими методами
их безопасной переработки [2-4]. Одной из важ-
[11, 12]. Особое место среди вышеуказанных мето-
нейших проблем очистки ЖРО является миними-
дов занимает сорбция, поскольку этот метод не тре-
зация их объемов путем селективного извлечения
бует сложного оборудования, процесс легко управ-
радионуклидов, в частности 137Cs, 90Sr, и 60Co, ко-
ляем, правильно подобранные сорбенты способны
торые вносят основной вклад в дозовую нагрузку
селективно извлекать опасные загрязнители в сколь
ЖРО [5-7]. Традиционно методы осаждения и коа-
угодно малых концентрациях из ЖРО сложного
гуляции широко применяются для удаления гидро-
химического и радионуклидного состава [13]. При
лизующихся либо образующих малорастворимые
этом большое преимущество имеют неорганиче-
61
62
ИВАНЕЦ и др.
ские сорбенты благодаря возможности получения
рактеризующихся высоким сродством к трем ради-
полусинтетических материалов на основе дешевого
онуклидам 137Cs, 60Co, 90Sr.
природного сырья, их химической и радиационной
Цель работы - синтез сорбентов на основе фос-
устойчивости [14]. Среди них выделяются цеолиты
фатов Ti-Ca-Mg и исследование влияния способа
[15], оксиды и гидроксиды металлов [16, 17], тита-
получения на их фазовый и химический состав, тек-
носиликаты [18].
стурные характеристики и сорбционные свойства
Большую группу сорбционных и ионообменных
по отношению к Cs(I), Sr(II), Co(II), в том числе при
материалов составляют неорганические фосфаты
использовании стабильных ионов металлов и ради-
многовалентных металлов, которые характеризу-
онуклидов 137Cs, 60Co, 90Sr.
ются высокой эффективностью в процессах извле-
чения ионов многовалентных металлов и радиону-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
клидов из водных растворов [19-21], радиационной,
термической и химической стойкостью [22]. Боль-
Исходным сырьем для синтеза композиционных
шим сорбционным потенциалом обладают фосфа-
фосфатов Ti-Ca-Mg являлись термически активи-
ты переходных металлов, включая титан и цирко-
рованный при 800°С природный доломит, фосфор-
ний [23, 24]. Одной из особенностей сорбентов на
ная кислота H3PO4 (ч.д.а), концентрированная азот-
основе фосфатов титанов является большое раз-
ная кислота HNO3 (х.ч.), гидрофосфат диаммония
нообразие структурных и морфологических моди-
(NH4)2HPO4, дигидрофосфат аммония NH4H2PO4,
фикаций, которые существенным образом зависят
карбонат аммония (NH4)2CO3 (все ч.д.а.), сульфат
от условий синтеза [24-26]. Как правило, практи-
титанил-диаммония (NH4)2TiO(SO4)2·H2O (водный
ческая емкость ионитов данного класса составляет
раствор 4 мас%). На первом этапе из активиро-
около 4 ммоль/г, достигая лишь в отдельных случа-
ванного доломита получали фосфаты CaMg-1 и
ях 7 ммоль/г - близкую к теоретически рассчитан-
CaMg-2. Для получения CaMg-1 проводили фосфа-
ной. Это обусловлено стерической недоступностью
тирование активированного доломита при соотно-
части ионогенных групп [27].
шении m/V, равном 1 : 3, где m - навеска активиро-
Одним из современных направлений улучше-
ванного доломита (г), V - объем раствора 20%-ной
ния сорбционных характеристик известных мате-
фосфорной кислоты (мл). В этих условиях полу-
риалов, включая фосфаты, является создание ком-
чается фосфатированный доломит валового соста-
позиционных материалов путем внедрения в их
ва Ca0.7Mg0.3HPO4∙2H2O, представляющий собой
структуру органических молекул или примесных
смесь гидрофосфатов кальция и магния. Для по-
катионов, которые могут способствовать созданию
лучения CaMg-2 активированный доломит раство-
более развитой пористой структуры, увеличению
ряли в азотной кислоте, а затем фосфаты кальция
межслоевого расстояния либо аморфизации веще-
и магния осаждали из полученного раствора при
ства [28-33]. Такие композиты могут быть полу-
рН 10 с помощью раствора гидрофосфата диаммо-
чены двумя различными методами: гетерогенным
ния. CaMg-2 представляет собой смесь аморфных
методом путем обработки поверхности фосфата
средних фосфатов кальция и магния и кристалли-
раствором соли другого металла [31, 32] либо мето-
ческого магнийаммонийфосфата [34].
дом гомогенного соосаждения фосфатов различных
Образцы TiCaMg-1 и TiCaMg-2 получали путем
металлов из раствора [33].
взаимодействия твердых навесок кислых (CaMg-1)
Ранее нами было показано, что сорбенты на ос-
и средних фосфатов Ca-Mg (CaMg-2) с 4%-ным во-
нове смешанных фосфатов Ca-Mg эффективно сор-
дным раствором сульфата титанил-диаммония при
бируют радионуклиды 90Sr и 60Co из водных и соле-
массовом соотношении Ti/(Ca + Mg) в реакционной
вых растворов [34, 35]. При этом данные сорбенты
смеси 1.5/1 [37]. В раствор сульфата титанил-диам-
малоактивны при сорбции радионуклидов 137Cs.
мония прибавляли навеску фосфатов CaMg-1 или
Учитывая известную высокую селективность сор-
CaMg-2 при постоянном перемешивании на маг-
бентов на основе фосфатов титана при извлечении
нитной мешалке. Синтез проводили при комнатной
137Cs [36], представляется перспективным синтез
температуре в течение 4 ч, полученную дисперсию
фосфатов Ti-Ca-Mg для получения сорбентов, ха-
оставляли на ночь, затем фильтровали на воронке
РАДИОХИМИЯ том 65 № 1 2023
СИНТЕЗ, ФИЗИКО-ХИМИЧЕСКИЕ И АДСОРБЦИОННЫЕ СВОЙСТВА ФОСФАТОВ Ti-Ca-Mg
63
Бюхнера, промывали несколько раз водой и сушили
ред анализом образцы вакуумировали в течение 1 ч
на воздухе.
при температуре 130-150°С и остаточном давлении
Осаждение фосфатов титана и фосфатов каль-
133.3 × 10-3 Па.
ция и магния наблюдается в различных диапазонах
Сорбционную емкость исследуемых образцов
рН, что не позволяет провести их соосаждение. По-
по стабильным ионам Cs+, Sr2+ и Co2+ определяли
этому для получения композиционного сорбента на
из модельных растворов Sr(NO3)2, Co(NO3)2 и CsCl
основе фосфатов Ti-Ca-Mg методом осаждения из
концентрацией 1000 мг/л. Навеску сорбента 0.20 г
раствора (TiCaMg-3) проводили последовательное
заливали 50.0 мл модельного раствора, выдержи-
осаждение сначала фосфата титана, а затем фосфа-
вали в течение 24 ч до установления равновесия
тов кальция и магния. Процесс осуществляли сле-
при постоянном перемешивании растворов. Содер-
дующим образом. 10.0 г сульфата титанил-диаммо-
жание ионов металлов в растворах определяли на
ния смешивали с соответствующим количеством
атомно-абсорбционном спектрометре Contr AA 300
раствора 1 М фосфорной кислоты для обеспечения
(Analytik Jena, Германия). Сорбционную емкость
молярного соотношения Ti/P = 1/1.2. Полученную
q (мг/г) рассчитывали по формуле
суспензию нагревали до 60°С и выдерживали в те-
чение 3 ч при перемешивании. После полного осаж-
q = (C0 - Cр)Vр/mс,
(1)
дения фосфата титана, 54 мл раствора 1 М дигидро-
где C0, Cр - соответственно исходная и равновесная
фосфата аммония прибавляли в горячую суспензию
концентрация ионов металлов в растворе, мг/л; Vр -
до достижения pH 2.0. Затем прибавляли порошок
объем жидкой фазы, л; mс - масса сорбента, г.
термообработанного при 850°С доломита до соот-
Сорбционные характеристики образцов фос-
ношения Ti/(Ca + Mg) = 1/1. Смесь выдерживали
фатов Ti-Ca-Mg по отношению к радионуклидам
при 60°C в течение 6 ч при перемешивании, затем
137Cs, 90Sr и 60Со также определяли в статических
отделяли полученный сорбент TiCaMg-3 фильтро-
ванием, промывали водой, сушили при 60°C и об-
условиях по разности удельной активности рас-
рабатывали раствором 1 М карбоната аммония при
творов изотопов до и после сорбции. После непре-
соотношении массы TiCaMg-3 к объему раствора
рывного перемешивания навески воздушно-сухого
карбоната аммония m/V (г/мл) = 1/10 для перевода в
сорбента с аликвотой раствора радионуклида до
аммонийную форму. Суспензию выдерживали 24 ч
установления равновесия смесь фильтровали через
при встряхивании, промывали деионизированной
бумажный фильтр «белая лента». Значения коэффи-
водой до достижения pH промывной воды 6.0 и су-
циента распределения Kd (мл/г) рассчитывали по
шили образец при 60°C.
формуле
Данные о фазовом составе исходных фосфатов
,
(2)
Ca-Mg и синтезированных фосфатов Ti-Ca-Mg
были получены с помощью рентгенофазового ана-
где А0, Ар - соответственно удельная активность
лиза (РФА), осуществленного на рентгеновском
радионуклида в исходном растворе и в фильтрате,
дифрактометре Advanced D8 (Bruker, Германия) и
Бк/л; Vр - объем жидкой фазы, мл; mс - масса сор-
D6000 (Shimadzu, Япония) с использованием излу-
бента, г.
чения CuKα (λ = 1.5418 Å) в диапазоне 2θ 5°-60°.
Для образцов TiCaMg-1 и TiCaMg-2 данные
Текстурные свойства образцов оценивали из дан-
по сорбции радионуклидов 137Cs получены при
ных низкотемпературной (-196°С) физической ад-
V/m 200 мл/г, pH 6.0 и солесодержании раство-
сорбции-десорбции азота, измеренных объемным
методом на анализаторе площади поверхности и по-
ра 8.5 г/л (0.1 М NaNO3), по сорбции 90Sr - при
V/m 200 мл/г, рН 6.0 и солесодержании раство-
ристости ASAP 2020 МР и ASAP 2000 (Micromeritics,
США). Удельную поверхность рассчитывали мето-
ра 1.11 г/л (0.01 М CaCl2), по сорбции 60Co - при
дом БЭТ (AБЭТ, м2/г), объем пор (V, см3/г) и средний
V/m 400 мл/г, рН 7.3-7.8 и солесодержании 0.31-
диаметр пор (D, нм) - по десорбционным ветвям
0.33 г/л. Данные по сорбции радионуклидов 137Cs,
изотерм. Распределение пор по размерам рассчи-
90Sr и 60Со для образца TiCaMg-3 получены при V/m
тывали методом Баррета-Джойнер-Халенды. Пе-
250 мл/г, pH 6.3 и солесодержании раствора 4.3 г/л.
РАДИОХИМИЯ том 65 № 1 2023
64
ИВАНЕЦ и др.
0 CaHPO4·2H2O
(а)
(г)
x MgHPO4·3H2O
(б)
(д)
MgNH4PO4·6H2O
0
0
0 CaHPO4·2H2O
0 CaHPO4·2H2O
(в)
0
(е)
0
0
x
x MgHPO4·3H2O
x MgHPO4·3H2O
x
MgNH4PO4·6H2O
MgNH4PO4·6H2O
x
0
0
x
0
0
x
00
x
x
0
0
0
x xx
0
0x
0
x x0
0
0
0
30
2θ, град
60
20
2θ, град
40
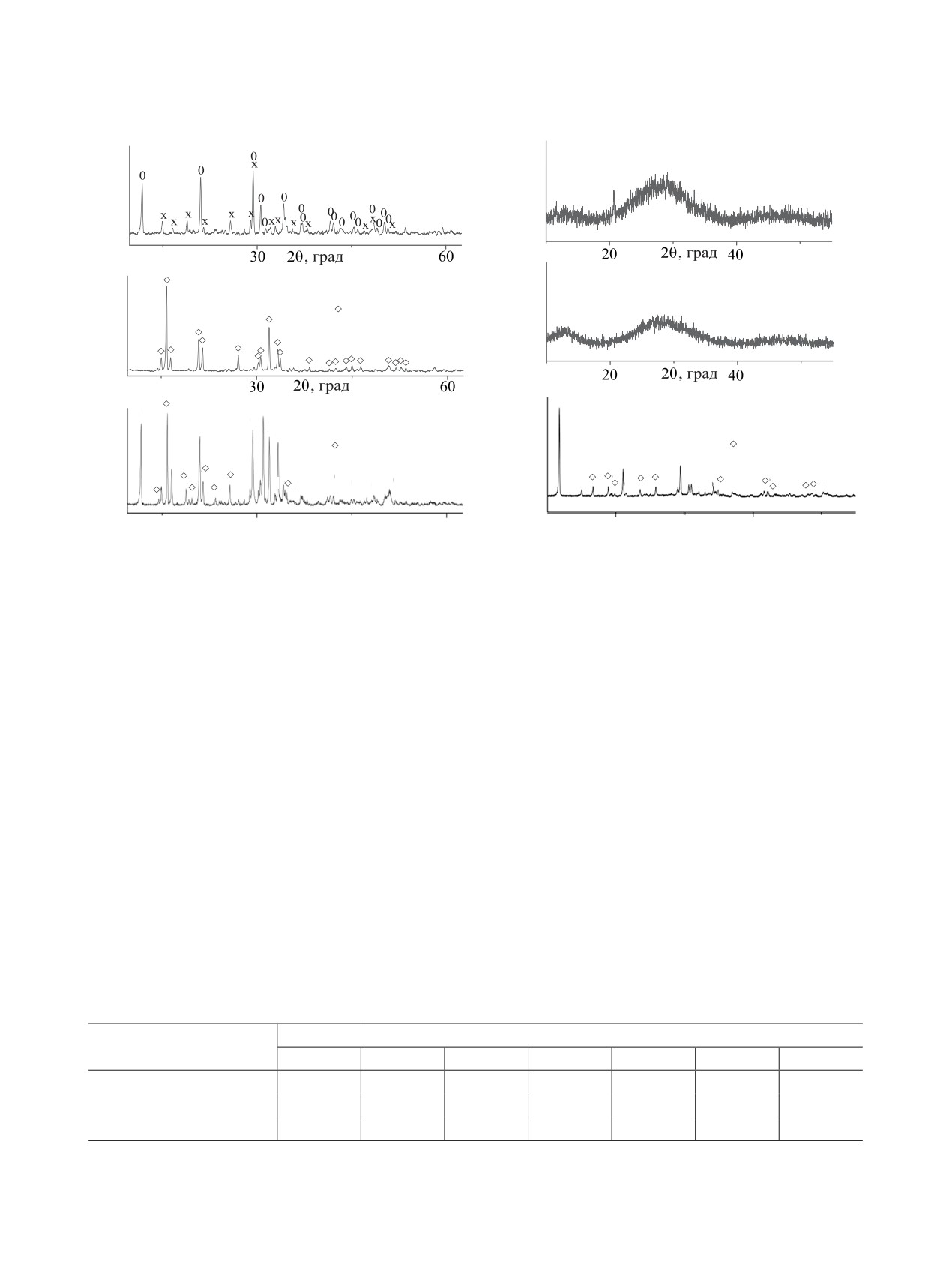
Рис. 1. РФА образцов фосфатированного доломита CaMg-1 (а), CaMg-2 (б), CaMg-3 (в) и полученных на их основе фосфатов
TiCaMg-1 (г), TiCaMg-2 (д) и TiCaMg-3(е).
Удельную активность радионуклидов 137Cs, 90Sr
рошо окристаллизованных гидрофосфатов кальция
и 60Со в растворах определяли прямым радиометри-
CaHPO4·2H2O и магния MgHPO4·3H2O. На рентге-
ческим методом с использованием спектрометри-
нограмме продукта взаимодействия с титанил-иона-
ческого комплекса СКС-50М («Грин стар технолод-
ми (TiCaMg-1) рефлексы исходных гидрофосфатов
жиз», Москва) и γ-спектрометра Canberra (США) с
не обнаруживаются, а рефлексы новых титансодер-
германиевым детектором.
жащих фаз не появляются. Замещение ионов каль-
Исходная удельная активность 137Cs, 90Sr и 60Со
ция и магния на титанил-ионы в исходном образце
в экспериментах составляла (1.5-3.0) × 105 Бк/л.
CaMg-1 сопровождается разрушением кристалли-
Химический состав образцов исследовали по-
ческой решетки кислых фосфатов кальция и магния
средством энергодисперсионной рентгеновской
и формированием аморфного соединения, о чем
спектроскопии - ЭДРС (AZtecLive Advanced with
свидетельствует появление на рентгенограмме ха-
UltimMax 40 detector (Oxford Instruments, Bognor
рактерного гало. Химический состав образуемого
Regis, UK).
соединения (табл. 1) позволяет предположить, что
этим соединением является аморфный гидрофос-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
фат титана с включениями кальция и магния, как
это объяснено в работе [37]. Аналогичным являет-
Анализ данных РФА (рис. 1) показал, что ис-
ся результат взаимодействия с титанил-ионами об-
ходный образец CaMg-1 представлен смесью хо- разца CaMg-2, исходная рентгенограмма которого
Таблица 1. Химический состав фосфатов Ti-Ca-Mg, по данным ЭДРС-анализа
Содержание элемента, ат%
Образец
Mg
Ca
Ti
P
O
Si
S
TiCaMg-1
0.06
1.33
23.60
6.89
66.05
0.68
0.27
TiCaMg-2
0.73
1.69
22.00
7.25
66.55
0.59
-
TiCaMg-3
4.51
7.92
4.01
14.02
37.95
2.82
3.13
РАДИОХИМИЯ том 65 № 1 2023
СИНТЕЗ, ФИЗИКО-ХИМИЧЕСКИЕ И АДСОРБЦИОННЫЕ СВОЙСТВА ФОСФАТОВ Ti-Ca-Mg
65
(а)
(г)
p/p0
(д)
p/p0
(е)
(в)
0.018
140
120
0.014
100
80
0.010
60
0.06
40
20
0.02
0.00
00.0
0.2
0.4
0.6
0.8
1.0
1
5
10
50 100
p/p0
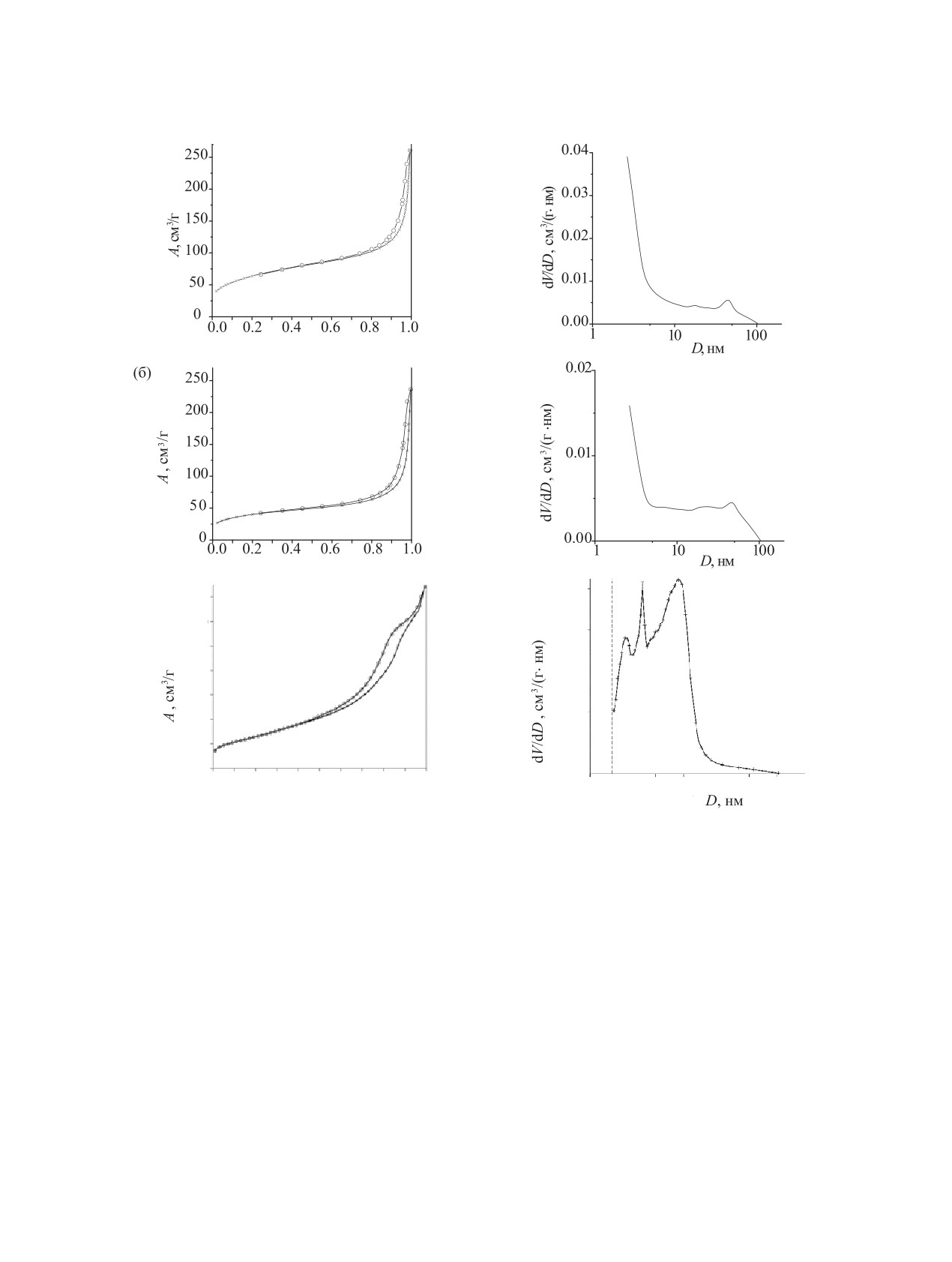
Рис. 2. Изотермы адсорбции-десорбции азота (а-в) и распределение пор по размерам (г-е) для образцов фосфатов TiCaMg-1
(а, г), TiCaMg-2 (б, д) и TiCaMg-3 (в, е). Крестики - адсорбция, кружки - десорбция.
представлена рефлексами магнийаммонийфосфата.
TiCaMg-2 и TiCaMg-3 при 850-1000°С. Дифрак-
После взаимодействия с титанил-ионами в соста-
тограммы термически обработанных образцов со-
ве продукта TiCaMg-2 также не обнаруживается
держат рефлексы фосфатных соединений кальция,
образования новых кристаллических фаз фосфа-
магния, титана сложного состава, включая фосфаты
та титана, и исчезают рефлексы магнийаммоний-
кальция-магния, CaTiPO4, CaTi4(PO4)6, (TiO)2P2O7, а
фосфата. Рентгенограмма осажденного TiCaMg-3
на дифрактограмме образцов TiCaMg-1 и TiCaMg-2
представлена пиками кристаллических фосфатов
обнаруживается также оксид титана [37, 38]. Дан-
CaHPO4·2H2O, MgНPO4·3H2O и MgNH4PO4·6H2O.
ные элементного анализа (табл. 1), полученные
Образование аморфных фосфатов титана при ге-
методом ЭДРС, также подтверждают присутствие
терогенном взаимодействии CaMg-1, CaMg-2 с ти-
титана в составе полученных сорбентов TiCaMg-1,
танил-ионами и последовательном осаждении под-
тверждают данные РФА продуктов, образующихся
TiCaMg-2, TiCaMg-3 и предположение об аморфно-
при термической обработке образцов TiCaMg-1,
сти формируемых фосфатов Ti-Ca-Mg.
РАДИОХИМИЯ том 65 № 1 2023
66
ИВАНЕЦ и др.
Таблица 2. Текстурные характеристики образцов фосфа-
Таблица 3. Коэффициенты распределения радионукли-
тов TiCaMg-1, TiCaMg-2 и TiCaMg-3
дов 137Cs, 90Sr и 60Co
Текстурные характеристики
Коэффициент распределения Kd, мл/г
Образец
Образец
AБЭТ, м2/г
V, см3/г
D, нм
137Cs
90Sr
60Co
TiCaMg-1
232
0.371
6.7
TiCaMg-1
1600
600
600
TiCaMg-2
144
0.336
9.6
TiCaMg-2
900
4200
1400
TiCaMg-3
95
0.410
10.2
TiCaMg-3
400 000
770 000
*
*Активность радионуклида 60Co в растворе после контакта с
сорбентом ниже предела обнаружения.
Изотермы адсорбции-десорбции азота, а также
Как видно из табл. 2, образец TiCaMg-3, полу-
кривые распределения пор по размерам для син-
ченный методом последовательного осаждения
тезированных композиционных фосфатов пред-
титана, кальция и магния, превосходит фосфаты
ставлены на рис. 2. Как видно из рассчитанных
Ti-Ca-Mg, синтезированные гетерогенным спо-
текстурных характеристик (табл. 2), синтезирован-
собом, по суммарному объему пор (0.410 см3/г)
ные фосфаты Ti-Ca-Mg являются мезопористыми
и значению среднего диаметра пор (10.2 нм), при
сорбентами с характерным для данного класса по-
этом уступая им по величине удельной поверхности
ристых тел изотермами типа IV по классификации
(95 м2/г). Это может быть обусловлено различием
IUPAC. Значения удельной поверхности составляют
размеров первичных частиц фосфата титана, об-
95-232 м2/г, удельный объем пор 0.336-0.410 см3/г
разующихся в растворе при осаждении, и частиц,
при их среднем диаметре 7-10 нм.
образующихся на поверхности твердых фосфатов
CaMg-1 и CaMg-2 при взаимодействии с раствором
Природа исходного фосфата Ca-Mg и способ
получения фосфатов Ti-Ca-Mg оказывают суще-
сульфата титанил-диаммония.
ственное влияние на их текстурные характеристи-
Данные РФА и низкотемпературной адсорб-
ки. Наибольшие изменения наблюдаются для об-
ции-десорбции азота свидетельствуют о том, что
разца TiCaMg-1, полученного путем гетерогенного
синтезированные различными способами сорбенты
взаимодействия CaMg-1 с водным раствором суль-
Ti-Ca-Mg имеют различный химический и фазо-
фата титанил-диаммония. Узкие петли гистерезиса
вый состав, а также пористую структуру. Установ-
при высоких относительны давлениях р/р0 > 0.45
ленные структурно-фазовые отличия оказывают
для TiCaMg-1 относятся к типу Н1. При этом удель-
влияние на сорбционные характеристики получен-
ная поверхность TiCaMg-1 (232 м2/г) и объем пор
ных образцов по отношению к Cs(I), Sr(II), Co(II)
(0.371 см3/г) увеличивается более чем на порядок
как при сорбции стабильных ионов металлов, так и
по сравнению с исходными кислыми фосфатами
радионуклидов 137Cs, 60Co, 90Sr.
кальция и магния - 11 м2/г и 0.025 см3/г соответ-
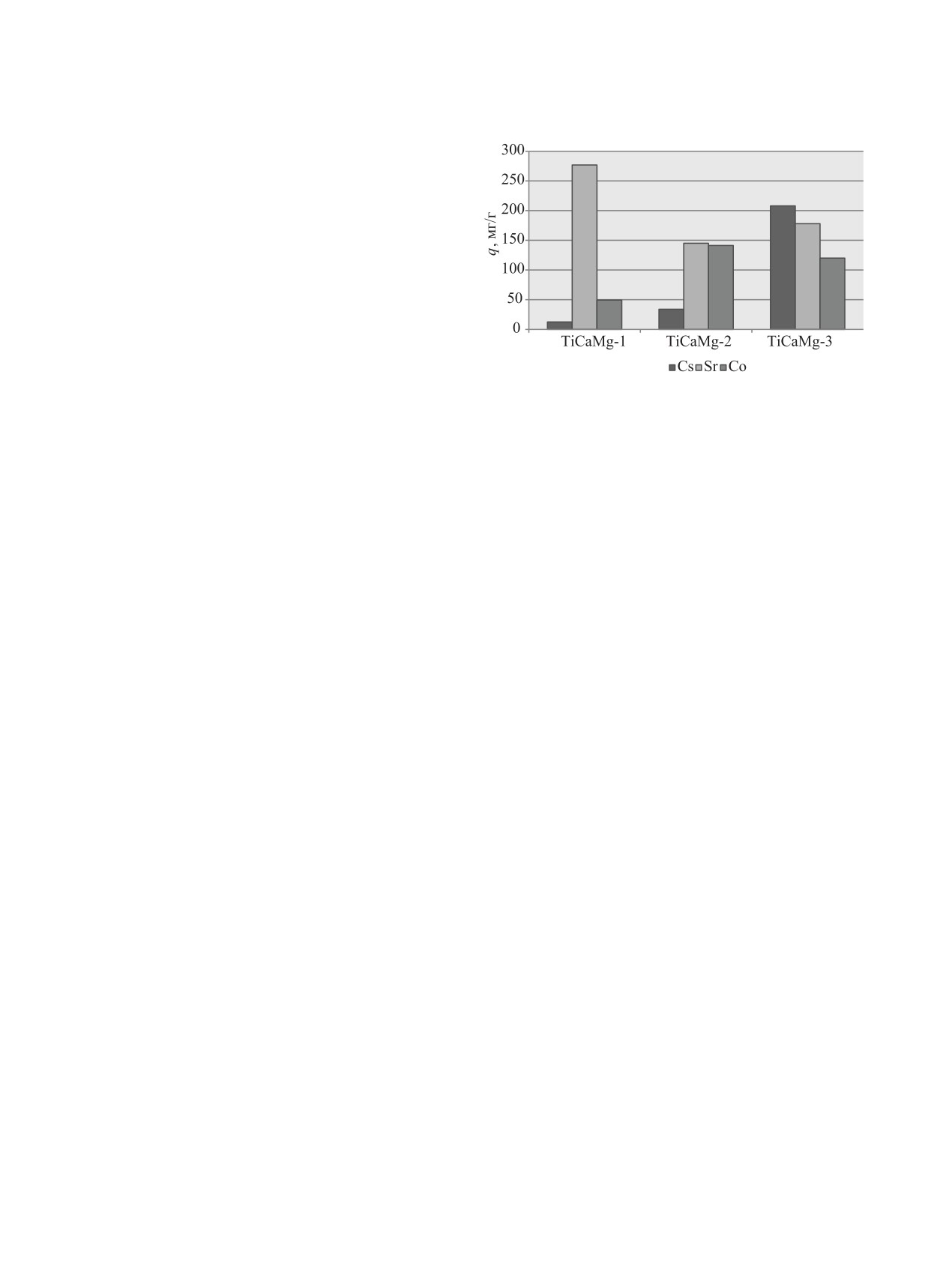
Данные о влиянии способа получения на сорб-
ственно [37], что может быть обусловлено образо-
ционную емкость смешанных фосфатов Ti-Ca-Mg
ванием аморфных титансодержащих продуктов.
по отношению к стабильным ионам Cs+, Sr2+ и Co2+
Изотермы адсорбции-десорбции азота для об-
в водных растворах представлены на рис. 3. Об-
разца TiCaMg-2 имеют схожий вид с изотермой со-
разец TiCaMg-1 имеет минимальную емкость по
рбента TiCaMg-1 и относятся к IV типу изотерм c
ионам Cs+ (q = 13 мг/г). Наиболее высокой емко-
капиллярно-конденсационным гистерезисом типа
стью к Cs+ характеризуется образец TiCaMg-3 (q =
Н1. Важно отметить, что при схожей структуре пор
205 мг/г). Образец TiCaMg-2 занимает промежуточ-
образец TiCaMg-2 по сравнению с TiCaMg-1 харак-
ное положение по сродству к Cs+ (35 мг/г). Более
теризуется значительно более низкой удельной по-
высокая емкость TiCaMg-3 по отношению к ионам
верхностью 144 м2/г при сопоставимом объеме пор
Cs+ может быть обусловлена несколькими факто-
0.336 см3/г, что обусловлено различием в среднем
рами. Этот образец, согласно данным ЭДРС-ана-
диаметре пор 9.6 и 6.7 нм для TiCaMg-2 и TiCaMg-1
лиза (табл. 1), содержит максимальное количество
соответственно.
сорбционно-активных фосфатов, в то время как в
РАДИОХИМИЯ том 65 № 1 2023
СИНТЕЗ, ФИЗИКО-ХИМИЧЕСКИЕ И АДСОРБЦИОННЫЕ СВОЙСТВА ФОСФАТОВ Ti-Ca-Mg
67
образцах TiCaMg-1 и TiCaMg-2 очевидна примесь
нефосфатных соединений титана, в частности ги-
дроксида, о чем свидетельствует высокое содержа-
ние титана при низком содержании фосфора. При
этом, как нами ранее было показано, механизм по-
глощения цезия фосфатом титана ионообменный.
Адсорбции наиболее крупных ионов Cs+ образцом
TiCaMg-3 способствует более крупный размер пор
и их суммарный объем.
Иная зависимость эффективности сорбции от
способа получения наблюдается для катионов Sr2+
и Co2+, что может быть обусловлено различными
Рис. 3. Сорбционная емкость стабильных ионов Cs+, Sr2+
механизмами сорбции, а также различными величи-
и Co2+ для образцов фосфатов TiCaMg-1, TiCaMg-2 и
нами атомных радиусов. Так, для образца TiCaMg-1
TiCaMg-3.
сорбционная емкость по ионам Sr2+достигает
TiCaMg-2 > TiCaMg-1; TiCaMg-1 > TiCaMg-3 >
275 мг/г, что значительно превосходит данную ха-
TiCaMg-2 и TiCaMg-2 > TiCaMg-3 > TiCaMg-1 со-
рактеристику для TiCaMg-2 (145 мг/г). Более высо-
ответственно.
кая сорбционная активность образца TiCaMg-1 по
Исследование сорбции радионуклидов 137Cs, 60Co
отношению к стронцию может быть обусловлена
и 90Sr композитами, полученными различными спо-
наиболее высокой удельной поверхностью при со-
собами, показало, что они характеризуются высоки-
поставимом объеме мезопор по сравнению с дру-
ми коэффициентами распределения (103-105 см3/г)
гими сорбентами, поскольку механизм сорбции
(табл. 3). Сорбент TiCaMg-3, полученный методом
стронция ионообменно-хемосорбционный, а раз-
последовательного осаждения фосфата титана и
мер пор для менее крупного по сравнению с цезием
фосфата кальция-магния, превосходит по значе-
атома стронция не имеет решающего значения. Все
нию коэффициента распределения радионуклидов
образцы достаточно эффективно сорбируют строн-
образцы, полученные методом гетерогенного взаи-
ций.
модействия фосфатов кальция-магния с сульфатом
Аналогичные закономерности наблюдаются при
титанил-диаммония. Образец TiCaMg-3 характе-
сорбции ионов Co2+. Наибольшую сорбционную ем-
ризуется максимальными значения объема пор и
кость демонстрирует образец TiCaMg-2 - 141 мг/г.
их диаметра, что способствует доступности ионо-
Аналогичные характеристики для TiCaMg-1 и
генных групп сорбента для поглощаемых радиону-
TiCaMg-3 составляют 50 и 120 мг/г соответствен-
клидов. Это является важным параметром с учетом
но. Механизм связывания кобальта также ионооб-
предельно низкой их концентрации в растворе в
менно-хемосорбционный. В отличие от сорбентов
отличие от стабильных ионов. Коэффициент рас-
TiCaMg-1 и TiCaMg-2, сорбент TiCaMg-3 содержит
пределения всех трех радионуклидов для этого со-
в своем составе наряду с аморфной фазой кристал-
рбента имеет максимальные значения. При этом в
лические кислые фосфаты кальция, магния и маг-
зависимости от способа получения сорбенты име-
нийаммонийфосфат, обладающие высокой сорб-
ют различное сродство к радионуклидам: TiCaMg-1
ционной активностью по отношению к Sr2+и Co2+
137Cs > 60Co ≈ 90Sr, TiCaMg-2 90Sr > 60Co > 137Cs,
и сорбирующие эти ионы по хемосорбционному
TiCaMg-3 60Co > 90Sr > 137Cs.
механизму. Таким образом, в зависимости от спо-
соба получения сорбента меняется соотношение
компонентов композиционных материалов, селек-
ЗАКЛЮЧЕНИЕ
тивных к различным ионам и определяющих итого-
вую величину сорбционной емкости. В результате
Таким образом, проведенные исследования пока-
сорбенты на основе фосфатов Ti-Ca-Mg по уве-
зали, что фосфаты Ti-Ca-Mg, полученные различ-
личению сорбционной емкости к ионам Cs+, Sr2+,
ными методами, существенно отличаются по фазо-
Co2+ располагаются в различные ряды: TiCaMg-3 >
вому и химическому составу, а также текстурным
РАДИОХИМИЯ том 65 № 1 2023
68
ИВАНЕЦ и др.
свойствам. Как следствие, они существенно отли-
5.
Yasunari T.J., Stohl A., Hayano R.S., Burkhart J.F.,
чаются по сорбционной активности по отношению
Eckhardt S., Yasunari T. // Proc. Nat. Acad. Sci. USA.
к ионам Cs(I), Sr(II), Co(II) как при использовании
2011. Vol. 108, N 49. P. 19530.
6.
Mertz J.L., Fard Z.H., Malliakas C.D., Manos M.J.,
стабильных ионов металлов, так и радионуклидов
Kanatzidis M.G. // Chem. Mater. 2013. Vol. 25, N 10.
137Cs, 60Co, 90Sr. Образец TiCaMg-3, полученный
P. 2116.
методом последовательного осаждения из раство-
7.
Aguila B., Banerjee D., Nie Z., Shin Y., Ma S.,
ра, имеет наиболее высокие значения коэффициен-
Thallapally P.K. // Chem. Commun. 2016. Vol. 52, N 35.
та распределения радионуклидов 137Cs, 60Co и 90Sr
P. 5940.
(>105 см3/г), характеризуется наибольшим объемом
8.
Ojovan M.I., LeeW.E., Kalmykov S.N. An Introduction to
(0.410 см3/г ) и средним диаметром пор (10.2 нм),
Nuclear Waste Immobilisation. Elsevier, 2019. P. 119-
что обеспечивает лучшую доступность ионогенных
143.
групп и отсутствие диффузионных затруднений
9.
Mahmoud M.R., Othman S.H. // Radiochim. Acta. 2018.
при обменных реакциях. Данный сорбент является
Vol. 106, N 6. P. 465.
перспективным материалом для изучения односта-
10. Narbutt J., Bilewicz A., Bartoś B. // J. Radioanal. Nucl.
дийной сорбции радионуклидов 137Cs, 90Sr, 60Co из
Chem. 1994. Vol. 183. P. 27.
водных и малосоленых растворов, а также в про-
11. Милютин В.В, Некрасова Н.А., Каптаков В.О. //
цессах очистки низкоактивных ЖРО. Заслуживает
Радиохимия. 2016. Т. 58, № 1. С. 30. (Milyutin V.V.,
дальнейшего внимания и возможность использова-
Nekrasova N.A., Kaptakova V.O. // Radiochemistry.
ния этих сорбентов не только для сорбции, но и для
2016. Vol. 58, N 1. P. 30.)
последующего захоронения, поскольку при терми-
12. Chon K., Kim S.J., Moon J., Cho J. // Water Res. 2012.
ческой обработке гидратированных фосфатов об-
Vol. 46, N 6. P. 1803.
13. Vellingiri K., Kim K.-H., Pournara A., Deep A. // Prog.
разуются высокоустойчивые безводные фосфаты,
Mater. Sci. 2018. Vol. 94. P. 1.
характеризующиеся прочной связью с сорбирован-
14. Alby D., Charnay C., Heran M., Prelot B., Zajac J. // J.
ными ионами и обладающие высокой термической
Hazard. Mater. 2018. Vol. 344. P. 511.
и радиационной устойчивостью.
15. Jiménez-Reyes M., Almazán-Sánchez P.T., Solache-
Ríos M. // J. Environ. Radioact. 2021. Vol. 233. 106610.
ФОНДОВАЯ ПОДДЕРЖКА
16. Ma J., Wang C., Xi W., Zhao Q., Wang S., Qiu M.,
Wang J., Wang X. // ACS ES&T Eng. 2021. Vol. 1, N 4.
Работа выполнена при финансовой поддержке
P. 685.
БРФФИ (грант Х18Р-026) и РФФИ (грант N18-53-
17. Gu P., Zhang S., Li X., Wang X., Wen T., Jehan R.,
00003).
Alsaedi A., Hayat T., Wang X. // Environ. Pollut. 2018.
Vol. 240. P. 493.
КОНФЛИКТ ИНТЕРЕСОВ
18. Oleksiienko O., Wolkersdorfer Ch., Sillanpää M. //
Chem. Eng. J. 2017. Vol. 317. P. 570.
Авторы заявляют об отсутствии конфликта ин-
19. Hafsteinsdottir E.G., Camenzuli D., Rocavert A.L.,
тересов.
Walworth J., Gore D.B. // Appl. Geochem. 2015. Vol. 59.
P. 47.
СПИСОК ЛИТЕРАТУРЫ
20. Ibrahim M., Labaki M., Giraudon J.-M., Lamonier J.-F. //
J. Hazard. Mater. 2020. Vol. 383. 121139.
1.
Hossain F. // J. Environ. Radioact. 2020. Vol. 225.
21. Balasooriya I.L., Chen J., Korale Gedara S.M., Han Y.,
106423.
Wickramaratne M.N. // Nanomaterials. 2022. Vol. 12.
2.
Wang L., Liang T. // J. Adv. Ceram. 2012. Vol. 1, N 3.
2324.
P. 194.
22. Rigali M.J., Brady P.V., Moore R.C. // Am. Mineral.
3.
Kumar P., Kumar B., Singh D. // Hazardous Waste
Management: An Overview of Advanced and Cost-
2016. Vol. 101. P. 2611.
Effective Solutions / Eds D. Yadav, P. Singh, P. Kumar,
23. Lin R., Ding Y. // Materials. 2013. Vol. 6. P. 217.
D. Vallero. Elsevier, 2022. P. 289-301.
24. Shahadat M., Teng T.T., Rafatullah M., Arshad M. //
4. Abdel Rahman R.O., El Kamash A.M., Ali H.F.,
Colloids Surf. B. 2015. Vol. 126. P. 121.
Hong Y.T. // Int. J. Environ. Eng. Sci. 2011. Vol. 2, N 1.
25. Amghouz Z., García J.R., Adawy A. // Eng. 2022. Vol. 3,
P. 1.
N 1. P. 161.
РАДИОХИМИЯ том 65 № 1 2023
СИНТЕЗ, ФИЗИКО-ХИМИЧЕСКИЕ И АДСОРБЦИОННЫЕ СВОЙСТВА ФОСФАТОВ Ti-Ca-Mg
69
26. Petersen H., Stegmann N., Fischer M., Zibrowius B.,
33. Иваненко В.И., Корнейков Р.И., Локшин Э.П. // Ра-
Radev I., Philippi W., Schmidt W., Weidenthaler C. //
диохимия. 2016. Т. 58, № 2. С. 140. (Ivanenko V.I.,
Inorg. Chem. 2022. Vol. 61, N 5. P. 2379.
Korneikov R.I., Lokshin E.P. // Radiochemistry. 2016.
27. Ярославцев А.Б.
// Успехи химии.
1997. Т.
66.
Vol. 58. No. 2. P. 159).
34. Kitikova N.V., Ivanets A.I., Shashkova I.L., Radkevich A.V.,
№ 7. С. 641. (Yaroslavtsev A.B. // Russ. Chem. Rev.
Shemet L.V., Kul’bitskaya L.V., Sillanpää M.
//
1997. Vol. 66, N 7. P. 579).
J. Radioanal. Nucl. Chem. 2017. Vol. 314. P. 2437.
28. Claverie M., Garcia J., Prevost T., Brendlé J., Li-
35. Ivanets A., Kitikova N., Shashkova I., Radkevich A.,
mousy L. // Materials. 2019. Vol. 12. 1399.
Shemet L., Sillanpää M. // J. Radioanal. Nucl. Chem.
29. Abegunde S.M., Idowu K.S., Adejuwon O.M., Adeyemi-
2018. Vol. 318. P. 2341.
Adejolu T. // Resour. Environ. Sustain. 2020. Vol. 1.
36. Маслова М.В., Иваненко В.И., Герасимова Л.Г., Вил-
100001.
кова Н.Л. // Физикохимия поверхности и защита
30. Kaushal S., Mittal S.K., Singh P. // Orient. J. Chem.
материалов. 2019. Т. 55, № 5. С. 479. (Maslova M.V.,
2017. Vol. 33, N 4. P. 1726.
Ivanenko V.I., Gerasimova L.G., Vilkova N.L. // Prot.
31. Metwally S.S., Ahmed I.M., Rizk H.E. // J. Alloys Compd.
Met. Phys. Chem. 2019. Vol. 55, N 5. P. 833).
2017. Vol. 709. P. 438.
37. Ivanets A.I., Shashkova I.L., Kitikova N.V., Maslova M.V.,
32. Thakkar R., Chudasama U. // J. Hazard. Mater. 2009.
Mudruk N.V. // J. Taiwan Inst. Chem. Eng.
2019.
Vol. 172. P. 129.
Vol. 104. P. 151.
РАДИОХИМИЯ том 65 № 1 2023