РАДИОХИМИЯ, 2022, том 64, № 3, с. 241-247
УДК 544.723.2:546.657+546.795
СОРБЦИЯ NdF3 И ThF4 АКТИВНЫМИ УГЛЯМИ И
ЦЕОЛИТАМИ ИЗ РАСПЛАВА LiF-NaF-KF
© 2022 г. Ю. С. Федоровa,*, В. В. Самонинa, А. С. Зотовa, Е. Д. Хрыловаa,
Е. А. Спиридоноваa, А. Е. Мирославовб, А. А. Акатовa
a Санкт-Петербургский государственный технологический институт (технический университет),
190013, Санкт-Петербург, Московский пр., д. 26
б Радиевый институт им. В.Г. Хлопина,
194021, Санкт-Петербург, 2-й Муринский пр., д. 28
*e-mail: fys54@mail.ru
Поступила в редакцию 07.07.2021, после доработки 02.09.2021, принята к публикации 09.09.2021
Исследована сорбция фторидов неодима и тория различными марками активированных углей и
цеолитов из расплава фторидов щелочных металлов LiF-NaF-KF. Показано, что фторид неодима
сорбируется более эффективно по сравнению с фторидом тория как цеолитами, так и активированными
углями. Экспериментальные данные изотермы сорбции Nd(III) цеолитом NaX аппроксимируются
уравнением Фрейндлиха в отличие от сорбции углем АГ-3, где данные описываются уравнением
Ленгмюра. Рассмотрены возможные варианты механизмов сорбции для различных сорбентов. Для
Nd(III) выявлена корреляция сорбционных свойств углей различных марок для отношения кислых и
основных окислов на единицу поверхности.
Ключевые слова: фториды, расплавы, щелочные металлы, неодим, торий, сорбция, активированный
уголь, цеолиты.
DOI: 10.31857/S0033831122030066, EDN: FQGFSU
ВВЕДЕНИЕ
Сорбционные процессы могут использоваться
и для очистки солевых топливных эвтектик от про-
В последние годы во всем мире возрос интерес
дуктов деления в жидкосолевых реакторах. Такие
к использованию расплавов солей применительно к
методы оказались бы полезными при использова-
ториевому топливному циклу [1]. Новые концепции
нии эвтектик LiF-NaF-KF [5, 6] и LiF-BeF2 [7, 8],
по наработке 233U связаны с использованием ги-
рассматриваемых в качестве топливных солей для
бридного термоядерного реактора синтез-деление
разного типа жидкосолевых реакторов.
[2, 3]. В качестве ториевого бланкета целесообразно
Работ по исследованию сорбции из расплавов
использовать расплав фторидов солей, содержащий
солей очень мало. Цеолит NaA использовали в ди-
сырьевой изотоп, т.е. фторид тория; в этом случае в
намических условиях для очистки от РЗЭ и оско-
данной системе может быть реализована непрерыв-
лочных элементов хлоридных эвтектик [9, 10] и для
ная и быстрая очистка вновь наработанного изотопа
фторидной эвтектики LiF-CaF2 [11].
и продуктов деления [1]. При таком подходе обра-
В настоящей работе изучена сорбция NdF3 и
зование нежелательного изотопа 232U будет мини-
ThF4 из расплава эвтектики LiF-NaF-KF с исполь-
мальным. Возможными эвтектиками, пригодными
зованием различных типов активированных углей и
для бланкета, являются расплавы фторидов солей,
цеолитов в статических условиях.
например эвтектика LiF-ThF4 или LiF-NaF-KF, в
которой растворяется 32.8 мол% ThF4 при темпе-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
ратуре 650°С [4]. Непрерывное выделение целевых
компонентов из расплава фторидов может осущест-
Для исследований процессов в расплавах фто-
вляться с использованием сорбционных методов.
ридов требуется использовать особо чистые ком-
241
242
ФЕДОРОВ и др.
поненты, поскольку небольшие примеси могут зна-
1
2
3
4
6
чительно исказить результаты экспериментов. Так,
7
для эвтектики фторидов щелочных металлов важно
8
отсутствие воды, так как в противном случае из фто-
ридов редкоземельных элементов (РЗЭ) и актини-
9
дов, хорошо растворимых в эвтектике LiF-NaF-KF,
10
образуются соответствующие малорастворимые
оксифториды и HF. Используемые в работе NdF3
и ThF4 не должны содержать значимых количеств
оксифторидов и гидратной воды, поэтому особые
11
требования были к составу полученных продуктов.
Рис. 1. Фотография установки для изучения сорбции из
Фторид неодима получали смешением водных
расплавов солей. 1 - баллон с аргоном, 2 - лабораторный
растворов нитрата неодима и фторида натрия
автотрансформатор, 3 - мембранный регулятор давления
(в мольном соотношении 1 : 3) при перемешивании
с манометром, 4 - ротаметр, 5 - потенциометр-измери-
без нагревания в течение 2 ч. После выпадения си-
тель температуры, 6 - ручка устройства ввода адсор-
бента, 7 - система вентилей регулирования разряжения
реневого хлопьеобразного осадка его промывали,
и подачи аргона, 8 - реактор с расплавом эвтектики, 9 -
отделяли, сушили на фильтре Шотта и переносили
термопара, 10 - печь, 11 - вакуум-насос.
в герметичный бюкс. Непосредственно перед сме-
шением с расплавом фторидов щелочных металлов
ботки при 130°С. Массовая доля модификатора,
фторид неодима сушили в вакууме при температуре
наносимого на углеродную поверхность, составила
350°С в течение 3 ч.
0.004%. Раствор фуллерена готовили путем диспер-
гирования рассчитанного количества фуллерена с
Для получения фторида тория Th(NO3)4 грели
при 200°С в течение 1 ч, потом при 400 °С еще 2 ч.
использованием ультразвука. Состав фуллерена:
С60 - 95.5%, остальные - высшие фуллерены. Про-
Полученный ThO2 обрабатывали восьмикратным
избытком NH4HF2, нагревали до 500°С в течение
изводитель - ЗАО «ИЛИП», Санкт-Петербург.
2 ч [12].
Все использованные в работе активированные
Рентгенофазовый анализ (РФА) выполнялся
угли и цеолиты перед опытом сушили в течение 2 ч
на дифрактометре D2 Phaser (Bruker, Германия)
при 200 и 400°С соответственно.
с использованием СuKα-излучения (напряжение
Фотография установки для исследования сорб-
рентгеновской трубки 30 кВ, сила тока 10 мА),
ции фторидов неодима и тория активированными
съемку проводили в диапазоне углов 2θ = 7°-70°
углями и цеолитами в статических условиях из рас-
в режиме сканирования с шагом 0.02° со скоро-
плава эвтектики LiF-NaF-KF при 650°С представ-
стью 0.5 град/мин. Обработку результатов про-
лена на рис. 1. Подробная схема приведена в работе
водили с использованием программы DIFFRAC.
[14].
EVA.V5.0 и картотеки PDF-2 ICDD (NdF3 - PDF
Фториды лития, калия и натрия (ч.д.а.) исполь-
01-078-1859, ThF4 - 00-015-0413).
зовали в мольном соотношении LiF (46.5)-NaF
Результаты рентгенофазового анализа получен-
(11.5)-KF (42.0) и перед опытами сушили в течение
ного фторида неодима и фторида тория указывают
3 ч под вакуумом при 400°С. Качество полученной
на соответствие полученных фторидов данным кар-
соли проверяли по точке плавления на дериватогра-
тотек.
фе; она составила 456°С, что практически соответ-
Окисленные угли получали по методике [13] об-
ствует литературным данным [1]. К высушенной
работкой перекисью водорода, затем переводили в
соли добавляли фторид неодима или фторид тория
Na-форму обработкой раствором щелочи.
и повторно проводили сушку в течение 2 ч под ва-
Методика модифицирования активного угля
куумом. Опыты проводили в среде аргона при тем-
фуллеренами состояла из стадий приготовления
пературе 650°С и значительном (в 200 и более раз)
водного раствора фуллерена, пропитки активного
избытке эвтектики, содержащей фториды неодима
угля, выдерживания и последующей термообра-
и тория, по отношению к исследуемым образцам
РАДИОХИМИЯ том 64 № 3 2022
СОРБЦИЯ NdF
3
И ThF4 АКТИВНЫМИ УГЛЯМИ
243
сорбента. Непосредственно сорбцию проводили в
Таблица 1. Величины сорбционной емкости активиро-
колбе (реакторе) из пирографита. Высушенный ак-
ванных углей и цеолитов по Nd(III) и Th(IV) при сорбции
из расплава фторидов LiF-NaF-KF. Температура 650°С,
тивированный уголь или цеолит помещали в специ-
время сорбции 1.5 ч. Равновесная концентрация элемен-
альную корзину из металлической меди с отверсти-
тов в расплаве 0.068 ммоль/л
ями и опускали в расплав солей. Корзину с сорбен-
Концентрация в сорбенте, мг/г
тами периодически подвергали вертикально-посту-
Марка сорбента
пательному движению для перемешивания соли.
Nd(III)
Th(IV)
После извлечения корзины проводили анализ на
ФАС
1.4
-
содержание Nd(III) или Th(IV) в угле или цеолите и
СКТ-6А
3.4
-
в солевой эвтектике. Величину сорбции определяли
СКТ-6А окисленный,
0.41
-
по отношению концентрации элемента в сорбенте
в Na-форме
к массе сорбента. Из-за избытка эвтектики, содер-
АГ-5
2.4
-
жащей фториды неодима и тория, по отношению
АГ-5 (с фуллереном)
2.8
-
к исследуемым образцам сорбента концентрация
АГ-3
8.4
0.17
фторидов неодима и тория в эвтектике практически
АГ-3 окисленный,
5.6
-
не менялась.
в Na-форме
Пробы с углем, цеолитом и эвтектики обраба-
АГ-3П
1.7
0.28
тывали серной кислотой для удаления HF и после
АГ-ПР
0.31
0.39
упаривания разбавляли водой и анализировались с
Цеолит NaA
10.6
0.88
использованием арсеназо III в среде соляной кис-
Цеолит NaX
9.5
0.92
лоты на спектрофотометре ПЭ-5300ВИ на длине
волны 650 нм по методике [15]. Предварительно по
Оба образца цеолитов после воздействия рас-
используемой методике определяли фоновые значе-
плава эвтектики получили повреждения шаровой
ния, которые оказались близкими к нулю.
формы, набухли и впитали некоторое количество
расплава (в среднем около 40%). Для цеолитов ис-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
пользуемых марок эффект адгезии оказался весьма
велик, что привело к затруднениям для отделения
Результаты экспериментов по сорбции Nd(III) и
налипших солей эвтектики. Для определения коли-
Th(IV) из эвтектики LiF-NaF-KF при температуре
чества поглощенных солей фторидов щелочных ме-
650°С приведены в табл. 1, из которой следует, что
таллов использовали подобранные по одинаковой
Nd(III) сорбируется в основном гораздо эффектив-
массе гранулы высушенного при 400°С исходного
нее, чем Th(IV). При этом наилучшие сравнитель-
цеолита и сравнивали с массой после сорбции в эв-
ные результаты по сорбции Nd(III) получены для ак-
тектике и механического отделения солей с поверх-
тивированного угля АГ-3 и цеолитов. Активирован-
ности гранул по специальной методике.
ные угли, за исключением СКТ-6А, после нахожде-
Для сорбции Th(IV) наилучшие результаты ока-
ния в расплаве эвтектики практически не изменили
зались у цеолитов, хотя и существенно ниже по
внешний вид, при этом не выявлено налипания или
сравнению с Nd(III). Из табл. 1 следует, что Th(IV)
попадания солей эвтектики внутрь сорбентов. Это
цеолитами сорбируется лучше, чем активирован-
установлено в результате того, что масса проб акти-
ными углями.
вированных углей, взятых из расплава для анализа
и после извлечения сорбированных компонентов в
При окислении углей увеличивается число кис-
ходе анализа, практически не изменилась, как внеш-
лых оксидов, что способствует увеличению ионо-
ний вид гранул угля. Активированный угль СКТ-6А
обменных свойств [13, 16]. Некоторые активиро-
после сорбции в расплаве фторидов щелочных ме-
ванные угли подвергали окислению для того, чтобы
таллов претерпел разрушение и терял форму гра-
усилить ионообменные свойства углей, однако уве-
нул с образованием спекшихся комков, содержание
личения извлечения Nd(III) окисленными сорбен-
Nd(III) в нем определяли так же, как для цеолитов,
тами не произошло, и даже сорбционная емкость
с учетом поглощенной эвтектики.
уменьшилась. При этом следует учесть, что окис-
РАДИОХИМИЯ том 64 № 3 2022
244
ФЕДОРОВ и др.
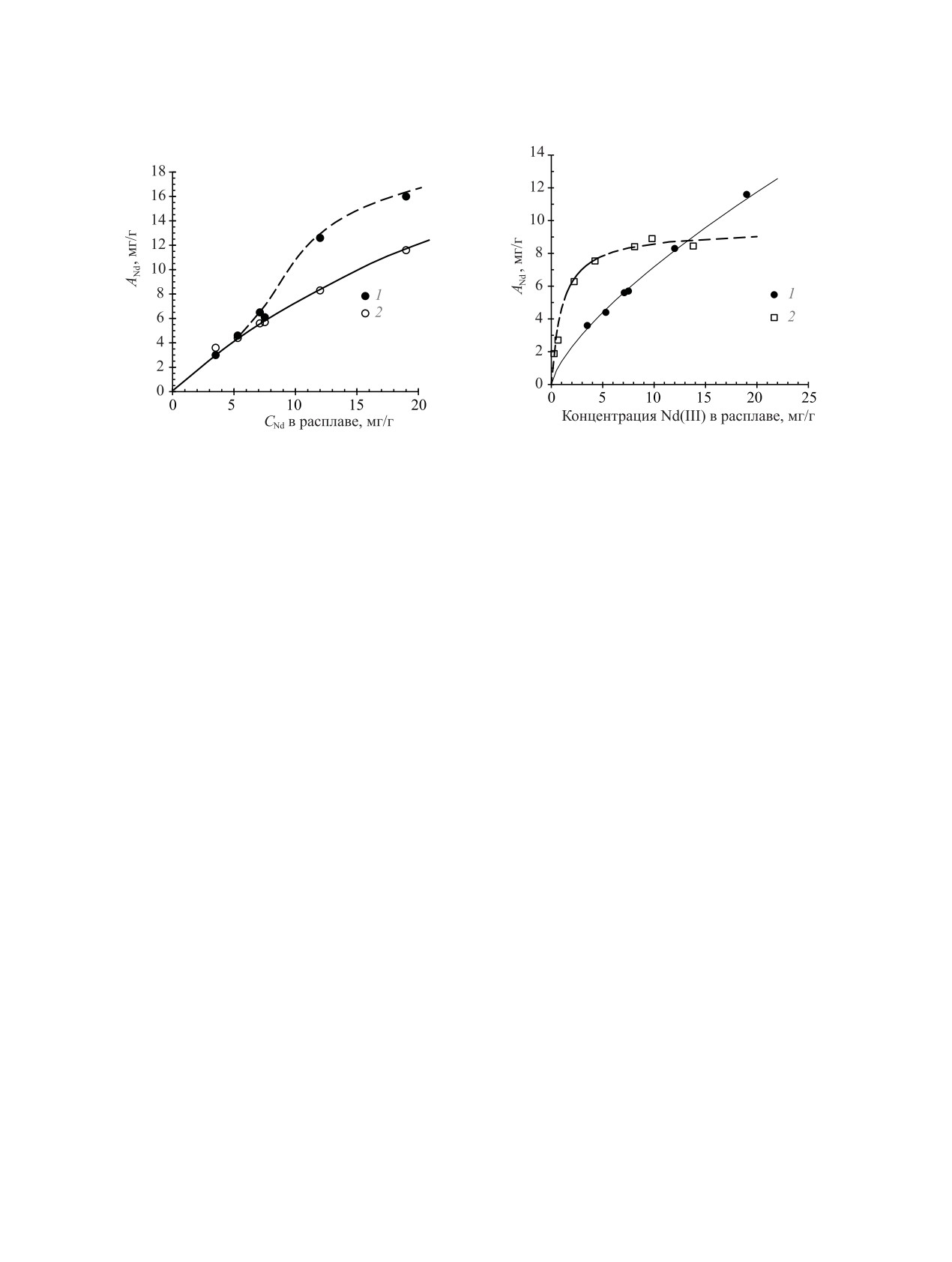
Рис. 3. Изотерма сорбции Nd(III) цеолитом NaX (1) и
активированным углем АГ-3 (2) при 650°C: сплошная
линия - аппроксимация экспериментальных результатов
Рис. 2. Изотерма сорбции Nd(III) цеолитом NaX при
уравнением Фрейндлиха для цеолита NaX (за вычетом
650°C: 1 - суммарное содержание Nd(III) в цеолите и по-
доли эвтектики в сорбенте), штриховая - аппроксимация
глощенной эвтектике, 2 - содержание Nd(III) в цеолите за
экспериментальных результатов уравнением Ленгмюра
вычетом содержания Nd(III) в эвтектике внутри цеолита.
для АГ-3.
ленные угли использовались для сорбции в натрие-
бции Nd(III) активированным углем АГ-3 и цеоли-
вой форме для исключения образования фтористого
том имеют различный характер, при этом экспери-
водорода. Введение фуллерена в АГ-5 привело к не-
ментальные результаты описываются уравнениями
большому увеличению сорбции.
Ленгмюра (АГ-3) и Фрейндлиха (NaX):
На рис. 2 представлены изотерма сорбции Nd(III)
ANd = 1.4 C 0.802,
цеолитом NaX при температуре 650°C с суммарным
где ANd - величина сорбции цеолитом NaX, мг/г; C -
содержанием неодима в цеолите и эвтектике, погло-
концентрация Nd(III) в эвтектике, мг/г.
щенной цеолитом, а также содержание неодима в це-
Таким образом, можно предположить, что сорб-
олите за вычетом его содержания в эвтектике внутри
ция Nd(III) углем АГ-3 происходит, по-видимому, на
цеолита. Доля Nd(III) в поглощенной цеолитом эв-
поверхности угля (вероятно, имеет место процесс
тектике определяли следующим образом. Поскольку
хемосорбции), а сорбция цеолитом осуществляется
увеличение массы цеолитов после контакта с распла-
в объеме за счет ионного обмена, как предполагают
вом возрастало на известную величину (в среднем
некоторые исследователи [9, 10].
на 40%), концентрацию Nd(III) в поглощенной цео-
литом эвтектике приравнивали к его концентрации
Сравнение сорбционной способности цеолита
равновесной фазе расплава LiF-NaF-KF. Как видно
NaX и активного угля АГ-3 по результатам постро-
из рис. 2, влияние поглощенной эвтектики начина-
енных изотерм адсорбции показывает, что в обла-
ет сказываться на поглощении Nd(III) при его кон-
сти малых концентраций, характерных для реали-
центрациях в эвтектике более 5 мг/г. Это связано
зации сорбционных процессов, значительное преи-
с тем, что концентрация в поглощенной цеолитом
мущество имеет активный уголь. При этом энергия
эвтектике больше количества, поглощенного непо-
взаимодействия неодима с углеродной поверхно-
средственно самим цеолитом, поэтому учет доли
стью, содержащей ионогенные группы, достаточно
Nd(III), поглощенного эвтектикой, приводит с сни-
высока в отличие от энергии связывания катиона
жению величины сорбции самим цеолитом.
с матрицей цеолита по механизму обмена. Поэто-
На рис. 3 представлены сравнительные изотер-
му при малых концентрациях неодима в расплаве
мы сорбции Nd(III) цеолитом NaX, полученной в
(в данном примере ниже 5 мг/г) изотерма адсорб-
ходе данной работы, и активированным углем АГ-3
ции для активного угля идет круче по сравнению
из работы [14]. Из рис. 3 видно, что изотермы сор-
с цеолитом и сорбционная емкость активного угля
РАДИОХИМИЯ том 64 № 3 2022
СОРБЦИЯ NdF
3
И ThF4 АКТИВНЫМИ УГЛЯМИ
245
Таблица 2. Параметры активированных углей
Объем пор, см3/г
Содержание оксидов, мг-экв/г
Vми
Образец АУ
Sуд, м2/г
V
ме
Vма
кислые
основные
V01ми
V02ми
АГ-ПР
1100
0.26
0.11
0.11
0.45
0.22
0.49
ФАС
1770
0.53
-
0.49
0.015
0.04
0.28
АГ-3П
1000
0.24
0.25
0.37
0.64
0.13
0.27
АГ-5
1250
0.22
0.11
0.12
0.45
0.09
0.39
АГ-5+F
710
0.24
0.11
0.12
0.47
0.10
0.28
СКТ-6А
1670
0.59
-
0.20
0.20
0.34
0.82
АГ-3
1500
0.20
0.13
0.10
0.45
0.19
0.35
в данной области превышает аналогичную характе-
рованных углей. В процессе сорбции играют роль
ристику цеолита более чем в два раза.
как кислые оксиды, так и основные [13], которые,
С другой стороны, возможно и другое обоснова-
например, могут поглощать анионные комплексы
ние процесса сорбции. Цеолиты NaA и NaX состоят
из водных сред [20], а также большая поверхность
из тетраэдров SiO2 и Al2O3, образующих открытую
сорбента, на которой располагаются оксиды. Опре-
каркасно-полостную структуру [AlSiO]– с отрица-
деленная роль оксидов на поверхности углей может
тельным зарядом, который компенсируется катио-
быть связана с образованием оксидов или оксифто-
нами металлов. Вероятно, следует учитывать воз-
ридов с NdF3 аналогично тому, как это происходит
можность реакций, протекающих с оксидами алю-
при добавлении оксида натрия [21] или оксида ли-
миния и кремния. В расплавах фторидов методом
тия [22, 23] в расплав LiF-NaF-KF.
рентгенофазового анализа идентифицировано обра-
Для установления возможной корреляции на
зование AlNdO3 и Al2O3 в присутствии LiF и NdF3
рис. 4 представлена зависимость величины сорб-
[17]. Оксид кремния в расплаве LiF-NaF-KF может
ции Nd(III) от относительного содержания кислых
взаимодействовать при температуре 600°C с иона-
оксидов (отношение кислых окислов к основным)
ми фтора, образуя небольшое количество [SiO3F]3-,
на единицу поверхности сорбента.
а также [Si2O5]2- за счет разрушения мостиковой
Из рис. 4 видно, что исследуемые угли располо-
связи Si-O-Si [18]. Этим же, по-видимому, можно
жились в две группы. В первой группе адсорбентов
объяснить частичное разрушение цеолитов в ходе
находятся газовые угли ФАС, АР-5, СКТ-6 и АГ-3,
сорбции и сильный эффект адгезии с расплавом.
которые отличаются высокой характеристической
Для оценки сравнительной сорбционной ак-
энергией адсорбции в микропорах [19]. Ко второй
тивности активированных углей в табл. 2 приве-
группе относятся рекуперационные угли АГ-ПР и
дены некоторые ключевые параметры используе-
АГ-3П, которые предназначаются для выделения
мых углей. Усредненные данные по размерам пор
поглощенных компонентов после адсорбции, об-
и удельной поверхности (за исключением АГ-5 и
АГ-5+F) взяты из справочника [19], остальные па-
ладают более низкой характеристической энерги-
раметры получены в ходе данной работы.
ей [19]. Вследствие этого при равных значениях
плотности активных групп на поверхности газовые
В табл. 2 образцы активированных углей пред-
угли, вероятно, обладают более высокой сорбцион-
ставлены в порядке увеличения сорбционных
ной емкостью по Nd(III). И наоборот, равная сорб-
свойств по отношению к Nd(III). Как видно из
ционная емкость по неодиму достигается при гораз-
представленной таблицы, не отслеживается влия-
ние объема характерных типов пор на сорбционную
до более низкой плотности ионогенных групп для
способность данных активных углей на их сорбци-
газовых углей. Ко второй группе также относится
онную способность по неодиму. Определенная за-
газовый уголь АГ-5, модифицированный фуллере-
кономерность сорбции Nd(III) связана с содержани-
нами (АГ-5F), что, по-видимому, происходит вслед-
ем как кислых, так и основных оксидов, которые,
ствие того, что его удельная поверхность в резуль-
как правило, расположены на поверхности активи-
тате модифицирования существенно уменьшилась.
РАДИОХИМИЯ том 64 № 3 2022
246
ФЕДОРОВ и др.
AND, мг/г
процесс присоединения за счет образования хелат-
9
ных соединений.
8
1
Следует отметить, что можно с достаточной до-
7
лей уверенности исключить влияние на сорбцию
2
6
потенциально не удаляемой при длительной сушке
5
под вакуумом воды, так как в случае наличия воды
4
образование оксифторида тория происходило бы
3
эффективнее по сравнению с фторидом неодима,
2
чего не наблюдалось в ходе работы.
1
0
0.0
0.1
0.2
0.3
0.4
0.5
06
ЗАКЛЮЧЕНИЕ
(Скисл/Сосн
)/S, ммоль/м2
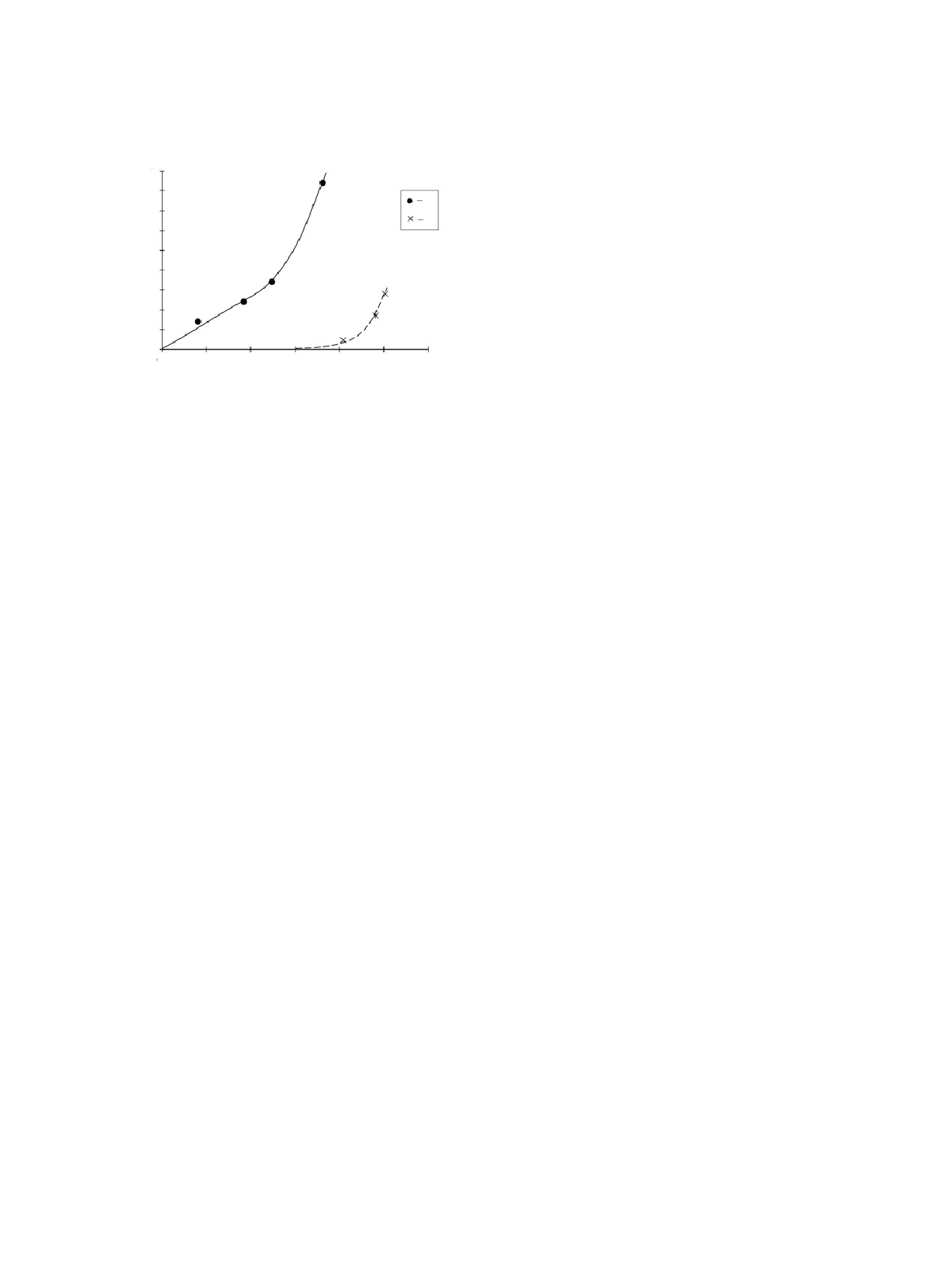
Рис. 4. Корреляционная зависимость величины сорбции
В статических условиях исследована сорбция
Nd(III) от соотношения кислых и основных оксидов на
единицу поверхности. Данные из табл. 1 и 2. Угли по
Nd(III) и Th(IV), вводимых в виде соответствую-
мере возрастания величины ANd
: 1 - ФАС, АГ-5, СКТ-6,
щих фторидов, из расплавов фторидов щелочных
АГ-3; 2 - АГ-ПР, АГ-3П, АГ-5F.
элементов с использованием активированных углей
и цеолитов. Для всех исследуемых сорбентов вели-
Чем выше плотность кислых групп относитель-
чина сорбции Nd(III) значительно выше по сравне-
но основных, тем более эффективно проходит из-
нию с Th(IV). Цеолиты NaA и NaX в ходе сорбции
влечение Nd(III). Следует отметить, что не получа-
частично разрушаются, по-видимому, за счет взаи-
ется разумных корреляций при использовании толь-
модействия алюминия и кремния с анионом фтора.
ко кислых или только щелочных оксидов. Вероятно,
При этом сорбционная емкость по Nd(III) состави-
оксиды обоих типов влияют на процесс извлечения
ла примерно 10 мг/г для концентрации в эвтектике
Nd(III), при этом Th(IV) активными углями извле-
0.068 ммоль/л, а по Th(IV) - менее 1 мг/г для такой
кается слабо. Разница в величинах сорбционного
же концентрации в эвтектике. Экспериментальные
извлечения Nd(III) и Th(IV) может быть связана как
изотермы сорбции Nd(III) цеолитом NaX аппрок-
с бóльшими размерами последнего, так и с большей
симируются уравнением Фрейндлиха. Возможный
прочностью его фторидных комплексов. Извест-
механизм сорбции может быть связан либо с ион-
но, что Nd(III) в расплавах LiF-NaF-KF образует
ным обменом, либо с образованием соединения
анионные комплексы NdF3- [24], а Th(IV) образует
AlNdO3.
более сложные фторидные комплексы с преоблада-
Проведено сравнение извлечения Nd(III) и Th(IV)
нием [ThF8]4- [25]. Кислые оксиды, содержащиеся
различными марками активированных углей. Наи-
на поверхности активных углей, могут участвовать
большей сорбционной емкостью для Nd(III) обла-
в образовании оксифторидов NdOF [26], которые
дает уголь АГ-3, при этом Th(IV) слабо извлекается
фиксируются в порах угля, или более сложных ком-
углями, исследованными в ходе работы. Отмечено,
плексов по аналогии с сорбцией активированными
что экспериментальные данные для изотермы сорб-
углями из водных растворов анионных комплексов
ции Nd(III) углем АГ-3 аппроксимируются уравне-
платины и других элементов [20].
нием Ленгмюра. Обнаружена корреляция величины
При этом следует учесть, что окисленные угли
сорбции Nd(III) различными марками углей с отно-
использовали для сорбции в натриевой форме для
сительной величиной содержания кислых оксидов
исключения образования фтористого водорода. По
на единицу поверхности углей. Сделано предполо-
всей вероятности, процесс поглощения крупного
жение, что сорбция углями Nd(III) происходит, ве-
катиона Nd(III) происходит не за счет ионного об-
роятно, за счет образования окифторидов, которые
мена на катион натрия, а по хорошо известному в
фиксируются в порах углей.
технике применения ионитов механизму хелато-
Различие сорбционных свойств Nd(III) и Th(IV)
образования. В этом случае замена протона в кисло-
при использовании активных углей и цеолитов ука-
родных группах на натрий полностью нивелирует
зывает на возможность разработки сорбционных
РАДИОХИМИЯ том 64 № 3 2022
СОРБЦИЯ NdF
3
И ThF4 АКТИВНЫМИ УГЛЯМИ
247
процессов очистки расплавов фторидных эвтектик,
Minimization of Wastes». Scottsdale, Arizona,
основанных на селективности сорбции.
NCLCollectionStore/_Public/28/019/28019520.pdf
10. Кузин М.А., Макаров А.О. // Экология и пром-сть
ФОНДОВАЯ ПОДДЕРЖКА
России. 2014. № 12. С. 8.
11. Cassayre1 L., Malmbeck R., Harrison M., De Angelis G.,
Исследование выполнено при финансовой
Caravaca C., Bourg S. // Int. Conf. Pyroprocessing
поддержке Российского фонда фундаменталь-
ных исследований в рамках научного проекта
ne.anl.gov/nce/pyroprocess-conference/presentations/
№ 19-29-02010\19.
Tuesday_PM/Cassayre_Pyrochemical%20Separation.
pdf
12. Руководство по неорганическому синтезу / Под ред.
КОНФЛИКТ ИНТЕРЕСОВ
Г. Брауэра. М.: Мир, 1985. С. 1225.
13. Тарковская И.А. Окисленный уголь. Киев: Наук.
Авторы заявляют об отсутствии конфликта ин-
думка, 1981. 200 с.
тересов.
14. Федоров Ю.С., Самонин В.В., Зотов А.С., Хрыло-
ва Е.Д., Спиридонова Е.А., Мирославов А.Е., Ака-
тов А.А. // Радиохимия. 2021. Т. 63, № 6. С. 525.
СПИСОК ЛИТЕРАТУРЫ
15. Савин С.Б. Органические реагенты группы арсеназо
III. М.: Атомиздат, 1971. 348 с.
1.
Molten Salt Reactors and Thorium Energy / Ed. T. J.
16. Jaramillo. J., Alvarez P. M., Gomez-Serrano V. // Fuel
Dolan. Elsevier, 2017. 815 p.
Process. Technol. 2010. Vol. 91. P. 1768.
2.
Велихов Е.П., Ковальчук М.В., Ильгисонис В.И., Иг-
17. Abbasalizadeh, A., Malfliet, A., Seetharaman, S.,
натьев В.В., Цибульский В.Ф., Андрианова Е.А. //
Sietsma, J., Yang, Y. J. Sustain. Metall. 2017. Vol. 3, N 3.
Энергетическая политика. 2017. № 3. С. 12.
P. 627.
3.
Velikhov E.P., Kovalchuk M.V., Azitov E.A., Ignatiev V.V.,
Subbotin S.A., Tsibulskiy V.F. // At. Energy.
2013.
18. Suzuki Y., Inoue Y., Yokota M., Takuya Goto T. //
Vol. 114, N 3. P. 193.
J. Electrochem. Soc. 2019. Vol. 166, N 13. P. 564.
19. Активные угли, эластичные сорбенты, катализаторы,
4.
Lizin A.A., Tomilin S.V., Gnevashov O.E., Gazizov R.K.,
осушители и химические поглотители на их основе:
Osipenko A.G., Kormilitsyn M.V., Nezgovorov N.Y.,
Номенклатурный каталог / Под ред. В.М. Мухина.
Naumov V.S., Ponomarev L.I. // At. Energy.
2013.
М.: Руда и металлы, 2003. 278 с.
Vol. 115, N 1. P. 22.
20. Воробьев-Десятовский Н.В., Кубышкин С.А., Ибра-
гимова Р.И., Каичев В.В., Дубровский Я.А., Баба-
5.
Ponomarev L.I., Belonogov M.N., Volkov I.A.,
ков В.Н., Пичугина Д.А. // ЖОХ. 2012. Т. 82, № 3.
Simonenko V.A., Sheremet’eva U.F. // At. Energy. 2019.
Vol. 126, N 3. P. 139.
С. 390.
21. Ponomarev L.I., Fedorov Y.S., Miroslavov A.E.,
6.
Ponomarev L.I., Belonogov M.N., Volkov I.A,
Degtyarev A.M. // At. Energy. 2016. Vol. 121, N 1. P. 63.
Simonenko V.A, Sheremet’eva U.F. // At. Energy. 2019.
Vol. 126, N 3. P. 150.
22. Мирославов А.Е., Степанова Е.С., Федоров Ю.С.,
Легин Е.К., Хохлов М.Л., Кольцов В.В., Тюпина М.Ю.
7.
Ignatiev V.V., Feynberg O.S, Zagnitko A.V,
Патент RU 2637256 C1. 2016 // Б.И. 2017. № 34.
Merzlyakov A.V., Surenkov A.I., Panov A.V.,
23. Rollet A.L., Veron E., Bessada C. // J. Nucl. Mater. 2012.
Subbotin V.G., Afonichkin V.K., Khokhlov V.A.,
Vol. 429. P. 40.
Kormilitsyn M.V. // At. Energy. 2012. Vol. 112, N 3.
P. 157.
24. Хохряков А.А., Вершинин А.О., Пайвин А.С., Ли-
зин А.А. // Расплавы. 2015. № 4. С. 3.
8.
Delpech S., Merle E., Heuer D., Allibert M., Ghetta V.,
25. Dai J., Long D., Huai P., Li Q // J. Mol. Liq. 2015.
Le-Brun C., Doliger X., Picard G. // J. Flourine Chem.
Vol. 211. P. 747-753.
2009. Vol. 130, N 1 . P. 11.
26. Fergus J.W. // Mater. Res. Bull. 1996. Vol. 31, N. 11.
9.
Pereira C., Babcock B.D. // Proc. Second Int. Symp.
P. 1317.
«Extraction and Processing for the Treatment and
РАДИОХИМИЯ том 64 № 3 2022