РАДИОХИМИЯ, 2022, том 64, № 3, с. 213-216
УДК 621.039.59
ИЗВЛЕЧЕНИЕ ПАЛЛАДИЯ ИЗ АЗОТНОКИСЛЫХ
РАСТВОРОВ ПЕРЕРАБОТКИ ОТРАБОТАВШЕГО
ЯДЕРНОГО ТОПЛИВА
© 2022 г. П. В. Давыдова*, Ю. И. Корнейко, В. А. Королев,
Л. В. Красников, Ю. Л. Крецер
Радиевый институт им. В. Г. Хлопина, 194021, Санкт-Петербург, 2-й Муринский пр., д. 28
*e-mail: davydova@khlopin.ru
Поступила в редакцию 03.08.2021, после доработки 12.11.2021, принята к публикации 18.11.2021
Исследована возможность извлечения палладия из азотнокислых растворов одновременно с синтезом
гексацианоферрата(II) (ГЦФ) железа(III) in situ. Найдено молярное отношение реагентов Pd : ЖКС :
Fe(III) = 1 : 2 : 2 (ЖКС - желтая кровяная соль), обеспечивающее полное извлечение палладия в диапазоне
концентраций азотной кислоты 1-5 моль/дм3. Из раствора, моделирующего ВАО от переработки ОЯТ,
вместе с палладием извлекаются полностью цезий и в значительных количествах молибден и серебро.
Ключевые слова: палладий, степень извлечения, гексацианоферраты, высокоактивные отходы,
отработавшее ядерное топливо, азотнокислые растворы
DOI: 10.31857/S0033831122030029, EDN: FPNLXX
ВВЕДЕНИЕ
калия и солей различных металлов-осадителей (Fe,
Cu, Ni, Al, Zn, Cr, Co). Авторы работы [3] отметили
Палладий входит в состав азотнокислых высоко-
как невозможность получения стехиометрического
активных отходов (ВАО) переработки отработавше-
Pd2[Fe(CN)6], так и полного извлечения палладия
го ядерного топлива (ОЯТ). Общепринятой концеп-
без введения в раствор металла-осадителя. В той же
цией обращения с жидкими ВАО является их вклю-
работе была показана возможность извлечения пал-
чение в стеклянные матрицы. Попадание металлов
ладия из отработанных электролитических раство-
платиновой группы (МПГ) вместе с ВАО в стекло-
ров с помощью in situ образования гексацианофер-
плавильные печи может привести к возникновению
ратов металлов, содержащихся в этих растворах.
эксплуатационных проблем [1]. Например, в США
Нам представляется актуальным распростра-
оседание МПГ на дно плавителя привело к полной
нить этот подход на растворы ВАО с существенно
остановке установки остекловывания и сложному
большей кислотностью 1-5 моль/дм3, так как кон-
ремонту оборудования [2]. Таким образом, извлече-
центрация азотной кислоты в растворах ВАО может
ние МПГ, в том числе палладия, из ВАО, направ-
меняться в значительном диапазоне в зависимости
ляемых на остекловывание, способно существенно
от технологии переработки ОЯТ, а также найти ус-
снизить эксплуатационные расходы.
ловия максимального извлечения палладия. В ка-
Среди многих работ, посвященных извлечению
честве металла-осадителя выбрано железо, так как
палладия из азотнокислых растворов различны-
оно входит в состав ВАО.
ми методами (экстракционными, сорбционными и
др.), встречаются работы, связанные с использова-
нием для этой цели ферроцианидов различных ме-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
таллов (см., например, [3-6]). В работах [3, 4] для
извлечения благородных металлов из слабокислых
В работе использовали порошки гексацианофер-
сред (pH 1-5) исследовали ферроцианиды, полу-
рата(II) калия (K4[Fe(CN)6]·3Н2О, ЖКС) и нитрата
ченные из растворов гексацианоферратов(II) и (III)
железа (Fe(NO3)3∙9H2O).
213
214
ДАВЫДОВА и др.
трация металла в растворе после окончания экспе-
римента.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Извлечение металлов гексацианоферратами
k
общей формулы
MelMe
Fe(CN)
про-
m
n
6
(nklm)/4
текает за счет ионного обмена с металлами (Me)
[7]. На степень извлечения металлов с помощью
нерастворимых гексацианоферратов металлов вли-
яют многие факторы, в том числе условия синтеза,
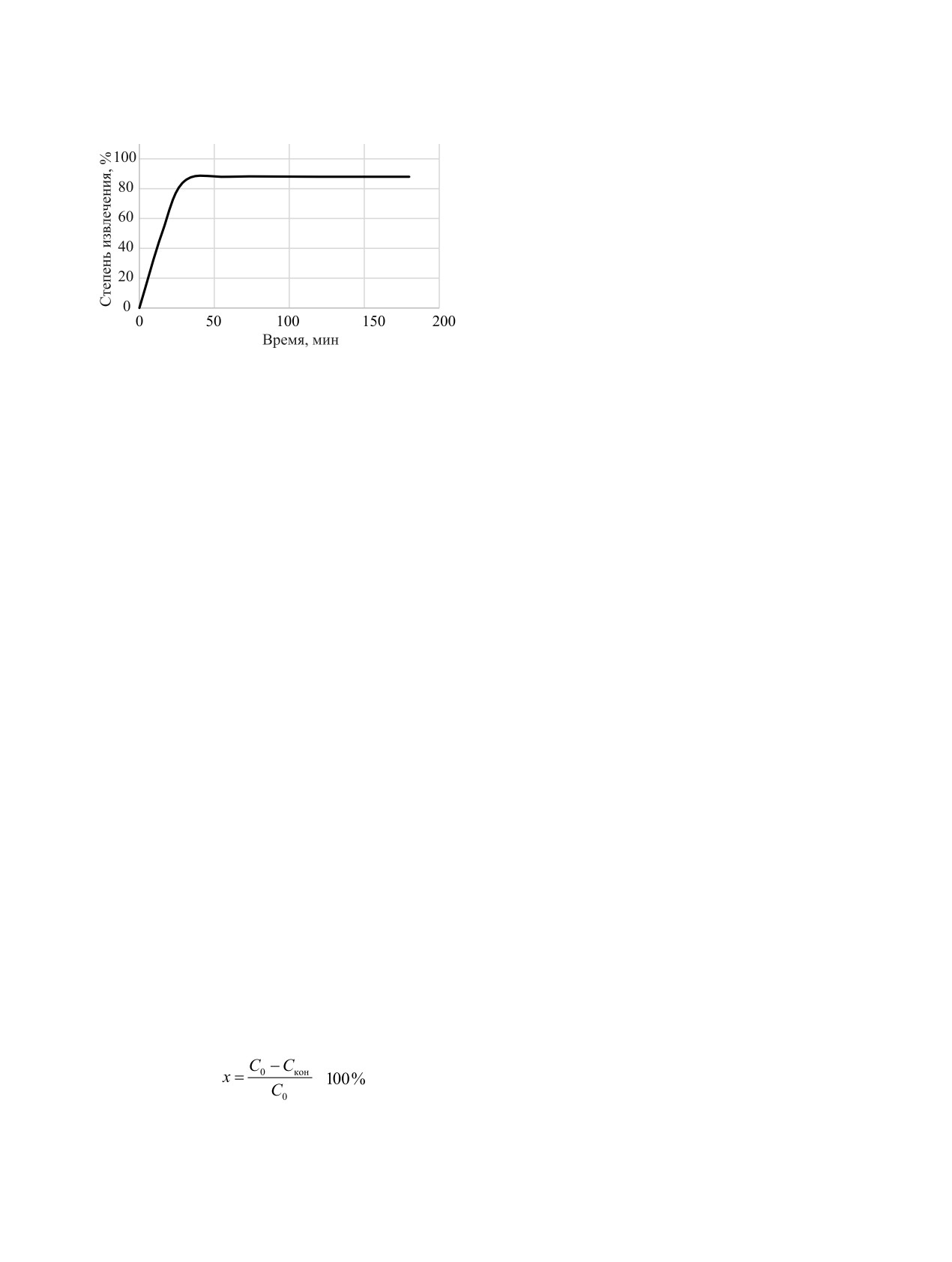
Рис. 1. Зависимость степени извлечения Pd от времени.
мольные соотношения реагентов и извлекаемых
Рабочие растворы азотнокислого палладия с
металлов [8]. В случае синтеза гексацианоферратов
концентрацией металла 100 мг/дм3 готовили из
in situ, т.е. добавления ЖКС в раствор, содержа-
раствора с концентрацией палладия по метал-
щий и палладий, и железо(III), механизм извлече-
лу 25,0 г/дм3 и концентрацией азотной кислоты
ния палладия существенно осложняется, поскольку
4 моль/дм3.
одновременно протекает несколько конкурентных
Концентрации металлов в растворах определя-
процессов: образование ГЦФ железа(III), образова-
ли методом атомно-эмиссионной спектрометрии с
ние комплексных ГЦФ как палладия, так и разнока-
индуктивно-связанной плазмой на приборе Varian
тионных ГЦФ. Образующиеся соединения, в свою
725-OES. Погрешность измерений 10%.
очередь, взаимодействуют с растворенным палла-
Рентгенофазовый анализ (РФА) выполняли на
дием, извлекая его. Таким образом, для достижения
дифрактометре D2 Phaser (Bruker, Германия) с ис-
полноты извлечения палладия требуется опреде-
пользованием CuKα-излучения. Обработку резуль-
лить влияние на процесс различных факторов: вре-
мени завершения процесса, отношения палладия к
татов проводили с использованием программы
вводимым реагентам и их друг к другу, а также кис-
DIFFRAC.EVA.V5.0 и картотеки PDF-2 ICDD.
лотности раствора.
Морфологию частиц и их элементный состав
определяли с помощью сканирующего электрон-
При определении времени, необходимого для
ного микроскопа MIRA3 FE-SEM фирмы TESCAN
завершения процесса извлечения, опыт проводили
Brno, оснащенного системой для рентгеноспек-
при комнатной температуре и мольном отношении
трального микроанализа AZtec. Для повышения
Pd : Fe3+ : ЖКС = 1 : 1 : 1, концентрация азотной
точности анализа легких элементов анализ прово-
кислоты 1 моль/л. Пробоотбор проводили каждые
дили при ускоряющем напряжении 5 кВ.
15 мин в течение часа, затем каждые 30 мин в тече-
Эксперименты проводили следующим обра-
ние 2 ч. Максимальная степень извлечения при дан-
ных условиях (~85%) доcтигалась в течение 30 мин
зом: к аликвоте азотнокислого раствора палладия
(рис. 1). Для дальнейших экспериментов 45 мин
добавляли навеску нитрата железа, раствор пе-
посчитали временем, достаточным для завершения
ремешивали до растворения вносимого реагента и
извлечения палладия.
при заданной температуре вносили навеску ЖКС.
Полученную суспензию перемешивали заданное
Для определения мольных отношений, обеспе-
время при определенной температуре. Полученный
чивающих полноту извлечения палладия, провели
осадок (композит) отделяли центрифугированием.
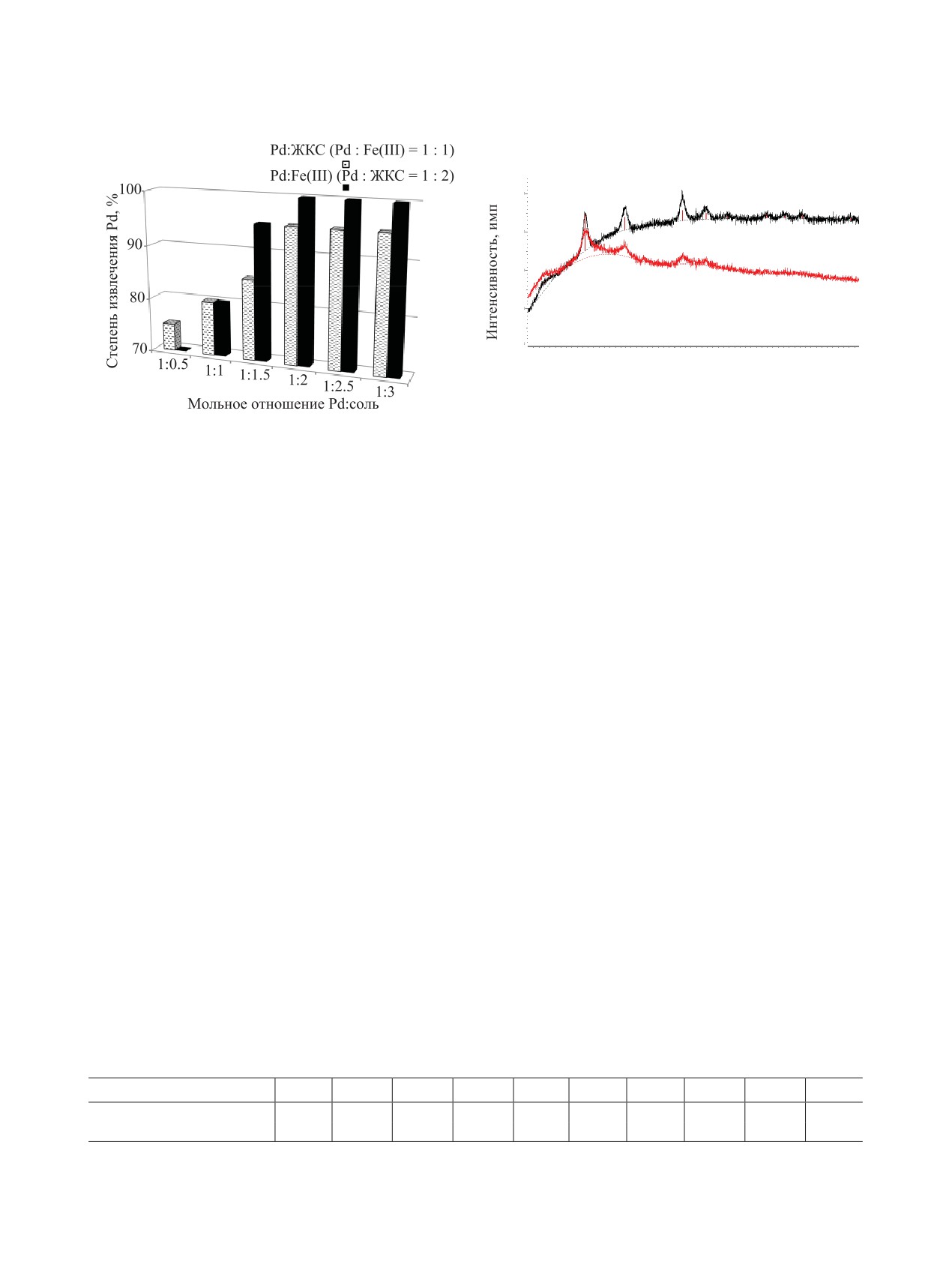
серию экспериментов, в которых варьировали отно-
шения Pd : ЖКС и Pd : Fe(III) (рис. 2). При постоян-
Степень извлечения палладия в композит рас-
ном отношении Pd : Fe(III) (1 : 1) максимальное из-
считывали по формуле
влечение палладия начинается при отношении Pd :
ЖКС = 1 : 2. Дальнейшее увеличение доли ЖКС не
×
,
(1)
приводит к увеличению степени извлечения пал-
где x - степень извлечения палладия, С0 - концен-
ладия. Увеличение доли Fe(III) в растворе при от-
трация металла в исходном растворе, Скон - концен-
ношении Pd : ЖКС = 1 : 2 до 2 моль на 1 моль Pd
РАДИОХИМИЯ том 64 № 3 2022
ИЗВЛЕЧЕНИЕ ПАЛЛАДИЯ ИЗ АЗОТНОКИСЛЫХ Р
АСТВОРОВ
215
4000
3000
2
2000
1
1000
0
10
20
30
40
50
60
2θ, град
Рис. 2. Степень извлечения палладия при различных
Рис. 3. Дифрактограммы образцов ГЦФ палладия (1) и
мольных отношениях Pd : ЖКС.
ГЦФ железа(III) (2).
позволяет извлечь палладий практически нацело.
чения цезия из растворов переработки ОЯТ [8-10]).
Таким образом, количественное извлечение палла-
С учетом этого количество вносимой ЖКС было пе-
дия достигается при мольном отношении Pd : Fe3+ :
ресчитано (2 моль на моль каждого из извлекаемых
K4Fe(CN)6 = 1 : 2 : 2.
металлов).
Так как концентрация азотной кислоты в раство-
В результате весь палладий был выведен в ком-
рах ВАО, направляемых на остекловывание, может
позит. Также в значительной степени из раствора
меняться в значительном диапазоне, мы проверили
были удалены молибден и железо (табл. 1).
ее влияние на полноту извлечения палладия. Как
Рентгенофазовый анализ синтезированного ГЦФ
оказалось, степень извлечения палладия (>99%)
железа(III) (образец 2) (рис. 3) выявил наличие
при мольном отношении исходных реагентов Pd :
только одной фазы с параметрами, соответствую-
Fe3+ : K4Fe(CN)6 = 1 : 2 : 2 не зависит от кислотно-
щими литературным данным [11]. Кристаллическая
сти раствора в диапазоне от 1 до 5 моль/дм3.
фаза палладийсодержащего композита (образец 1),
Поскольку в составе реальных ВАО присутству-
полученного в оптимальных условиях, оказалась
ют в значительных количествах металлы, которые
изоструктурна с ГЦФ железа(III), средний размер
могут оказать существенное влияние на взаимодей-
частиц составил ~80 Å. Однако, судя по величине
ствие палладия с ЖКС, мы провели ряд экспери-
фона (рис. 3), процентное содержание железа в ком-
ментов по извлечению палладия из модельного рас-
позите меньше.
твора с концентрацией азотной кислоты 1 моль/л.
Анализ состава отдельных областей частиц, со-
При использовании найденного оптимального от-
ставляющих композит (рис. 4, табл. 2), с помощью
ношения в композит были полностью извлечены
электронного микроскопа, оснащенного системой
палладий и серебро, около 80% молибдена и в не-
рентгеноспектрального микроанализа, подтвердил
которой степени (~10 %) цирконий. Под «компози-
присутствие палладия в композите. Металл в компо-
том» авторы понимают порошок гексацианоферра-
зите распределен неравномерно, но не выделяется в
та железа с сорбированными на нем металлами. Как
самостоятельные фазы. Отношение палладия к же-
и ожидалось, степень извлечения цезия составила
лезу и железа к углероду приблизительно соответ-
>99% (ферроцианиды металлов применяются в ра-
ствует фазам брутто-соcтава от Fe3Pd1.5[Fe(CN)6]3
диохимической технологии в основном для извле-
до Fe(2.66)Pd2[Fe(CN)6]3.
Таблица 1. Степень извлечения металлов из модельного раствора с концентрацией азотной кислоты 1 моль/л
Металл
Pd
Cs
Ce
Nd
Zr
Ag
Sr
Ba
Mo
Fe
Концентрация, мг/ дм3
350
760
1675
2095
560
45
540
1920
1150
1000
Степень извлечения, %
>99
>99
0
0
10
85
0
0
80
60
РАДИОХИМИЯ том 64 № 3 2022
216
ДАВЫДОВА и др.
(а)
(б)
Таблица 2. Относительный состав (ат%) отдельных
областей композита и расчетные значения для некоторых
составов
Область (рис. 3)
Fe/C
Pd/Fe
C/N
20
43%
24%
1.1
21
35%
26%
1.2
22
32%
38%
1.2
(в)
(г)
25
35%
30%
1.3
26
31%
34%
1.1
27
29%
38%
1.3
28
36%
20%
1.2
Fe4[Fe(CN)6]3
39%
-
1
Pd2[Fe(CN)6]
17%
200%
1
Fe3Pd1.5[Fe(CN)6]3
33%
25%
1
Рис. 4. СЭМ (BSE)-изображение поверхности образца
гексацианоферрата железа-палладия при различных уве-
Fe3-1/3Pd2[Fe(CN)6]3
31%
35%
1
личениях (а-г). Нумерованными квадратами обозначены
области анализа.
ЗАКЛЮЧЕНИЕ
СПИСОК ЛИТЕРАТУРЫ
Получение ГЦФ железа(III) in situ в азотнокис-
1.
Harrison M. // Procedia Metar. Sci. 2014. Vol. 7. P. 10.
лых растворах, содержащих палладий, позволяет
2.
Goel A., McCloy J., Pokorny R., Krugel A.A. // Solids:
полностью извлечь палладий в образующийся ком-
Journal of Non-Crystalline Solids: X, Volume 4, 2019,
позит. Экспериментально найдено оптимальное
100033.
мольное отношение Pd : ЖКС : Fe(III) (1 : 2 : 2) и
3.
Loos-Neskovic C., Dierkes M.H., Jackwerth E.,
показано, что степень извлечения палладия не за-
Fedoroff M., Garnier E. // Hydrometallurgy.
1993.
висит от кислотности раствора вплоть до 5 моль/л
Vol. 32. P. 345.
HNO3. При извлечении палладия из раствора, мо-
4.
Onishi T., Sekioka K., Suto M., Tanaka K., Koyama Sh.,
делирующего ВАО от переработки ОЯТ, в образую-
Inaba Yu., Takahashi H., Harigai M., Takeshita K. //
щийся композит также извлекаются в значительном
Energy Procedia. 2017. Vol. 131. P. 15.
количестве цезий, молибден, серебро. Таким обра-
5.
Rozowski J., Mojski M. // J. Radioanal. Nucl. Chem.
зом, предложенный способ извлечения палладия
может служить основой для разработки технологии
1991. Vol. 148. N 2. P. 373.
извлечения МПГ из азотнокислых ВАО переработ-
6.
Mishima R., Inaba I., Tachioka S., Harigai M. // Chem.
ки ОЯТ.
Lett. 2019. P. 1.
7.
Malik M., Safdar M. // Adsorption Sci. Technol. 1999.
ФОНДОВАЯ ПОДДЕРЖКА
Vol. 17. N 8. P. 689.
8.
Воронина А.В., Семенищев В.С., Ноговицына Е.В.,
Данная работа проведена при финансовой под-
Бетенеков Н.Д. // Радиохимия. 2012. Т. 54, № 1.
держке АО «Наука и инновации».
С. 66.
9.
Mimura H., Lehto J., Harjula R. // Nucl. Sci. Technol.
КОНФЛИКТ ИНТЕРЕСОВ
1997. Vol. 34. P. 607.
10. Haas P.A. // Sep. Sci. Technol. 1993. Vol. 28. Р. 2479.
Авторы заявляют об отсутствии конфликта ин-
11. Weiser H.B., Milligan W.O., Bates J.B. // J. Phys. Chem.
тересов.
1942. Vol. 46. P. 99.
РАДИОХИМИЯ том 64 № 3 2022