РАДИОХИМИЯ, 2020, том 62, № 3, с. 195-201
УДК 539.26+546.798.21
НИТРАТНЫЕ КОМПЛЕКСЫ НЕПТУНИЯ(V) С
ОРГАНИЧЕСКИМИ ОДНОЗАРЯДНЫМИ КАТИОНАМИ
ВО ВНЕШНЕЙ СФЕРЕ
© 2020 г. И. А. Чарушникова*, М. С. Григорьев, А. М. Федосеев
Институт физической химии и электрохимии им. А. Н. Фрумкина РАН, 119071, Москва, Ленинский просп., д. 31, корп. 4
*e-mail: charushnikovai@ipc.rssi.ru
Получена 05.03.2019, после доработки 15.04.2019, принята к публикации 23.04.2019
Выделены в кристаллическом виде и исследованы методом рентгеноструктурного анализа нитратные
комплексы пятивалентного нептуния с однозарядными органическими катионами во внешней сфере
состава [H3O][C(NH2)3]2[NpO2(NO3)2]3 (I), [N(CH3)4][NpO2(NO3)2(H2O)2] (II), [HIm][NpO2(Im)5](NO3)2
(III), где Im - имидазол, C3H4N2. В комплексе с гуанидинием (I) осуществляется катион-катионное (КК)
взаимодействие ионов NpO2+, приводящее к образованию тригонально-гексагональных катионных сеток.
В соединениях II и III КК взаимодействие отсутствует.
Ключевые слова: нептуний(V), синтез, кристаллическая структура, катион-катионное взаимодействие
DOI: 10.31857/S0033831120030028
В работе [1] был описан синтез, строение и
него ~0.5-1.0 моль/л и оставляли при комнатной
некоторые свойства нитратных комплексов неп-
температуре для медленной кристаллизации.
туния(V) со щелочными катионами Li+, Na+, Rb+
Цвет образовавшихся кристаллов можно описать
и Cs+ во внешней сфере. Оказалось, что для этих
как зеленоватый с желтым оттенком (I) и светло-
комплексов характерно образование катион-ка-
зеленый (II). В случае комплекса с имидазолом III
тионных (КК) связей между диоксокатионами
водный раствор ~1 моль/л имидазола нейтрализо-
NpO2+, приводящее к образованию в структуре
вали 1 моль/л HNO3 до рН полученного раствора
квадратных (соединения Li[NpO2(NO3)2]·2H2O и
не выше 6.5-7.0. В результате медленной кристал-
Na[NpO2(NO3)2]·2H2O) или тригонально-гекса-
лизации при комнатной температуре образовались
гональных (соединения Cs 3[NpO2(NO3)2]3·H2O и
кристаллы ярко-зеленого цвета.
NaRb5[NpO2(NO3)2]6·4H2O) катионных сеток.
Рентгенодифракционные эксперименты про-
В продолжение исследования нитратных ком-
ведены на автоматическом четырехкружном диф-
плексов Np(V) выделены кристаллы нитратов
рактометре с двумерным детектором Bruker Kappa
Np(V) с органическими однозарядными катио-
Apex II (излучение MoKα) при 100 K. Измерены
нами гуанидиния C(NH2)3+, тетраметиламмония
интенсивности рефлексов в полусфере обратно-
N(CH3)4+ и имидазолия HIm+ (Im - C3H4N2) во
го пространства. Параметры элементарных яче-
внешней сфере. Были получены соединения соста-
ек уточнены по всему массиву данных. В экспе-
ва [H3O][C(NH2)3]2[NpO2(NO3)2]3 (I), [N(CH3)4]·
риментальные интенсивности введены поправки
[NpO2(NO3)2(H2O)2] (II), [HIm][NpO2(Im)5](NO3)2
на поглощение с помощью программы SADABS
(III).
[2]. Структуры расшифрованы прямым методом
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
(SHELXS97 [3]) и уточнены полноматричным ме-
Cоединения I, II были синтезированы по
тодом наименьших квадратов (SHELXL-2014 [4])
методике, описанной в работе [1]: к раствору
по F2 по всем данным в анизотропном приближе-
~0.05 моль/л NpO2NO3 прибавляли нитрат соот-
нии для всех неводородных атомов. Структура III
ветствующего катиона до концентрации послед-
уточнялась как рацемический двойник с вкладом
195
196
ЧАРУШНИКОВА и др.
Таблица 1. Кристаллографические данные и характеристики рентгеноструктурного эксперимента
Параметр
I
II
III
Формула
C2H15N12O25Np3
C4H16N3O10Np
C18H25N14O8Np
М
1318.26
503.20
802.52
Сингония
Гексагональная
Моноклинная
Ромбическая
Пространственная группа
P63/m
P2/c
Pna21
a, Å
8.2179(2)
10.9081(7)
33.650(3)
b, Å
8.2179(2)
5.6601(4)
7.2445(6)
c, Å
21.3408(12)
11.6195(7)
11.6471(10)
β, град
90
113.622(1)
90
V, Å3; Z
1248.14(9); 2
657.29(7); 2
2839.3(4); 4
ρвыч, г/см3
3.518
2.543
1.877
μ(MoKα), мм-1
8.149
5.159
3.727
Количество измеренных/независимых
20513/1812
11024/2915
33162/8184
отражений
Количество независимых отражений с
1336
2217
6224
I > 2σ(I)
Количество уточняемых параметров
73
108
371
R(F); wR(F2) [I > 2σ(I)]
0.0492; 0.1223
0.0130; 0.0268
0.0341; 0.0518
R(F); wR(F2) [весь массив]
0.0741; 0.1388
0.0221; 0.0296
0.0560; 0.0578
GOOF
1.067
1.0290
1.011
Δρmax и Δρmin, e·Å-3
10.783; -5.497
0.399; -0.903
0.863; -1.250
второго домена 0.24(2). Атомы H катиона оксония
В структуре I атом Np1 катиона NpO2+ локализу-
(I) и молекул воды (II) локализованы из разност-
ется на плоскости m в позиции 6h. Координацион-
ного Фурье-синтеза и уточнены с UН = 1.5Uэкв(O)
ное окружение атома Np1 - гексагональная бипи-
и ограничением расстояний O-H и углов H-O-H.
рамида, и длины связей внутри координационного
Атомы H органических катионов гуанидиния
полиэдра (КП) (табл. 2) такие же, как в структурах
C(NH2)3+ (I), тетраметиламмония N(CH3)4+ (II),
со щелочными катионами. Максимальное откло-
имидазолия C3H5N2+ и молекулярного лиганда
нение атомов кислорода от среднеквадратичной
имидазола (III) введены на геометрически рассчи-
экваториальной плоскости бипирамиды не пре-
танные позиции с UН = 1.5Uэкв(С) для II и UН =
вышает ±0.071(8) Å. Бидентатно-циклические ни-
1.2Uэкв(N,С) для I, III.
трат-ионы располагаются по обе стороны триго-
нально-гексагональной катионной сетки, образуя
Основные кристаллографические данные и ха-
слои состава [NpO2(NO3)2]nn-, перпендикулярные
рактеристики рентгеноструктурного эксперимен-
направлению [001] в кристалле, между ними рас-
та приведены в табл. 1. Длины связей и валентные
полагаются катионы оксония и гуанидиния.
углы в структурах I-III приведены в табл. 2, 3. Ко-
ординаты атомов депонированы в Кембриджский
Катион оксония в структуре I (атом кислорода
O1w) локализуется на инверсионной оси третьего
центр кристаллографических данных, депозиты
порядка, позиция 2b. Три атома водорода у кати-
CCDC 1896401-1896403.
она оксония разупорядочены по двум позициям
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИE
и образуют шесть коротких контактов [Ow···O
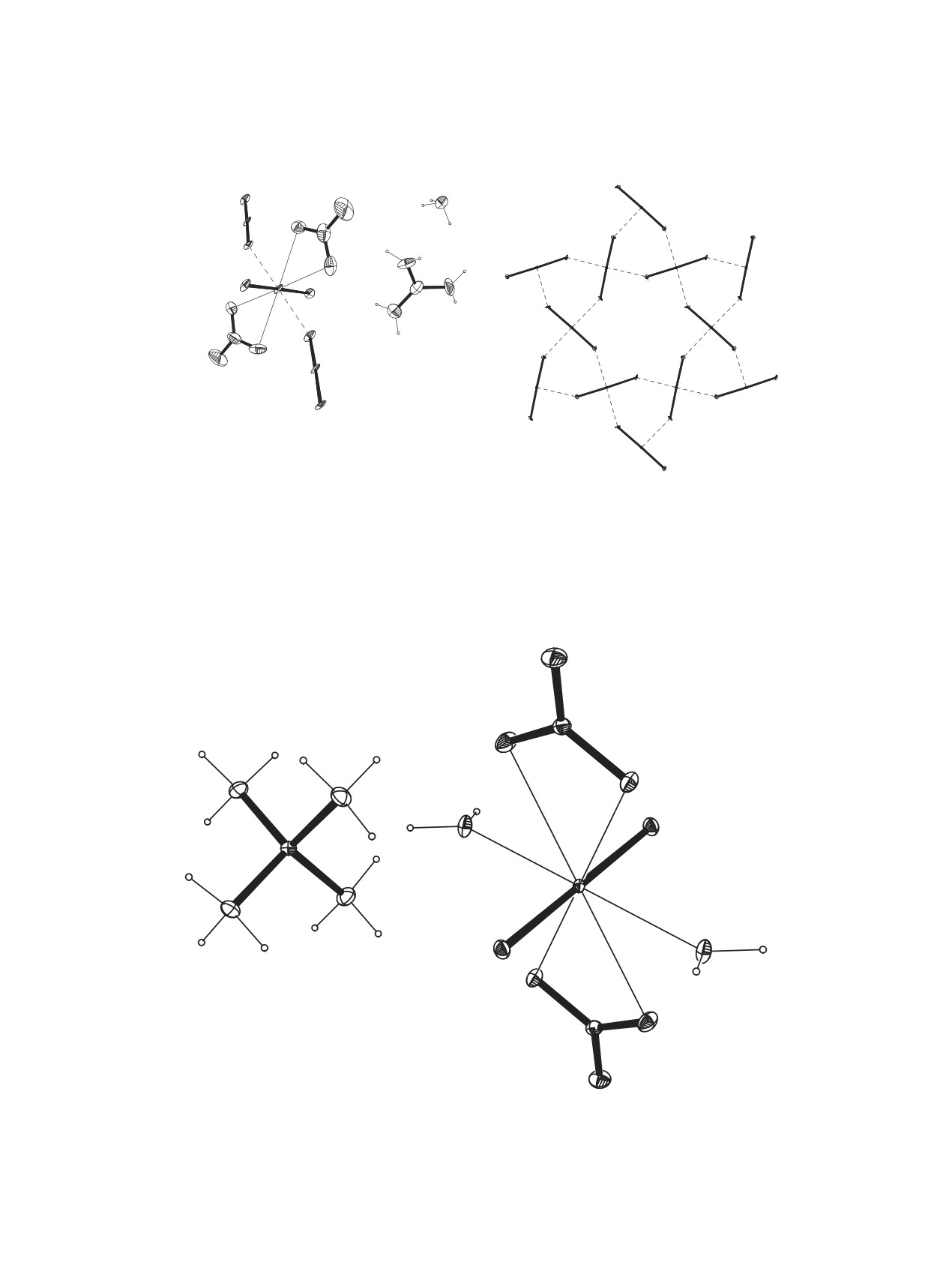
Структура I состоит из комплексных анионов
2.701(16) Å] с концевыми атомами O5 нитрат-
[NpO2(NO3)2]- и однозарядных катионов H3O+
анионов соседних слоев, которые можно отнести к
и C(NH2)3+ (рис. 1а). Катионы NpO2+ связывают-
сравнительно прочным водородным связям.
ся в плоские тригонально-гексагональные сет-
Катион C(NH2)3+ в структуре I локализуется в
ки (рис. 1а), подобные найденным в структурах
позиции 4f. При этом атомы C1 и N2 располага-
Cs3[NpO2(NO3)2]3·H2O и NaRb5[NpO2(NO3)2]6·
ются на оси 3, а атомы N3 и N4 разупорядочены
4H2O [1] или La(NpO2)3(NO3)6∙nH2O [5].
относительно этой оси. Аминогруппы гуаниди-
РАДИОХИМИЯ том 62 № 3 2020
НИТР
АТНЫЕ КОМПЛЕКСЫ НЕПТУНИЯ(V)
197
ɚ
ɛ
O5
O1w
O2b
O3
O2b
Np1b
N1
O1b
N4
Np1
Np1b
O2
O4
N3
O3a
O1
C1
1
O1b
O
N1a
N2
Np1
O2c
O2
2c
O
4a
Np1c
O
O5a
O1c
Np1c
O1c
Рис. 1. Фрагмент структуры [H3O][C(NH2)3]2[NpO2(NO3)2]3 (I) (а) и тригонально-гексагональная катионная сетка в кристалле
I (б). Эллипсоиды температурных смещений показаны с 30% вероятностью (разупорядоченность катионов H3O+ и C(NH2)3+
не показана). Операции симметрии: a - (x, y, 1/2-z); b - (1-y, 1+x-y, z); c - (2-y, 1+x-y, z).
ния участвуют в водородном взаимодействии типа
лорода нитрат-ионов, причем концевой атом O5
N-H···O, объединяющем слои
[NpO2(NO3)2]nn-.
задействован по крайней мере в четырех сравни-
Акцепторами протонов выступают атомы кис-
тельно прочных связях (табл. 4). Контакты N···O
ɚ
ɛ
O4
N1
O2
ɋ1b
ɋ2
O3
O1a
N2
O1w
Np1
ɋ2b
ɋ1
O1wa
O1
O3a
O2a
N1a
O4a
Рис. 2. Фрагмент структуры [N(CH3)4][NpO2(NO3)2(H2O)2] (II). Эллипсоиды температурных смещений даны с 50% веро-
ятностью. Операции симметрии: a - (-x, 1-y, 1-z); b - (-x-1, y, -z+1/2).
РАДИОХИМИЯ том 62 № 3 2020
198
ЧАРУШНИКОВА и др.
Таблица 2. Длины связей (d, Å) и валентные углы (ω, град) в структурах [H3O][C(NH2)3]2[NpO2(NO3)2]3 (I) и [N(CH3)4]
[NpO2(NO3)2(H2O)2] (II)*
I
II
Связь
d
Связь
d
Связь
d
Связь
d
Np1=O1
1.864(7)
N1-O4
1.264(17)
Np1=O1
1.8227(12)·2
Np1-O4
1.2283(18)
Np1=O2
1.829(7)
N1-O5
1.22(2)
Np1=O2
2.6318(12)·2
N2-C1
1.490(2)·2
Np1-O1a
2.422(6)
C1-N2
1.33(3)
Np1-O3
2.6033(12)·2
N2-C2
1.499(2)·2
Np1-O2b
2.424(7)
C1-N3
1.34(4)
Np1-O1w
2.4734(13)·2
Np1···Np1с
5.8097
Np1-O3
2.535(8)·2
C1-N4
1.29(3)
Np1-O2
1.2647(18)
Np1···Np1d
5.6601
Np1-O4
2.568(9)·2
Np1···Np1с
4.1107
Np1-O3
1.2725(19)
N1-O3
1.218(15)
Np1···Np1d
4.1072
Угол
ω
Угол
ω
Угол
ω
Угол
ω
O1Np1O2
178.5(3)
O4N1O5
119.6(14)
O1Np1O1a
180.0
O2N1O4
122.25(15)
O1aNp1O3
64.7(2)·2
N2C1N3
119.9(18)
O2Np1O1w
65.76(4)·2
O3N1O4
121.75(14)
O2bNp1O4
66.5(3)·2
N2C1N4
121(2)
O3aNp1O1w
66.45(4)·2
C1N2C1b
110.26(19)
O3Np1O4
49.0(3)·2
N3C1N4
119(3)
O2Np1O3
48.53(4)·2
C1N2C2
109.41(10)
O3N1O4
116.9(14)
Np1O1Np1c
146.9(4)
O2N1O3
115.98(13)
C1N2C2b
109.34(10)
O3N1O5
123.3(16)
Np1O1Np1d
149.6(4)
a Операции симметрии: I: a - (1 - y, 1 + x - y, z); b - (2 - y, 1 + x - y, z); с - (-x + y, 1 - x, z); d - (1 - x + y, 2 - x, z); II: a - (-x, 1 - y,
1 - z); b - (-x - 1, y, -z + 1/2); c - (x, -y + 1, z - 1/2); d - (-x + 1, -y, 1 - z).
Таблица 3. Длины связей (d, Å) и валентные углы (ω, град) в структуре [HIm][NpO2(Im)5](NO3)2 (III)
Связь
d
Связь
d
Угол
ω
Угол
ω
Np1=O1
1.842(5)
C4-C5
1.350(10)
O1=Np1=O2
179.4(2)
C7N7C9
105.2(7)
Np1=O2
1.829(5)
N7-C7
1.374(9)
N3Np1N5
71.6(4)
C8N8C9
107.5(8)
Np1-N3
2.548(7)
N7-C9
1.317(11)
N3Np1N11
73.0(2)
C8C7N7
110.0(9)
Np1-N5
2.540(4)
N8-C8
1.355(12)
N5Np1N7
74.5(4)
C7C8N8
106.4(8)
Np1-N7
2.542(7)
N8-C9
1.347(11)
N7Np1N9
71.7(2)
N7C9N8
110.9(7)
Np1-N9
2.583(6)
C7-C8
1.341(13)
N9Np1N11
70.19(17)
C10N9C12
104.5(7)
Np1-N11
2.580(7)
N9-C10
1.360(10)
O3N1O4
118.5(7)
C11N10C12
106.2(7)
N1-O3
1.248(8)
N9-C12
1.307(11)
O3N1O5
120.8(7)
N9C10C11
109.7(9)
N1-O4
1.271(7)
N10-C11
1.344(11)
O4N1O5
120.6(7)
N10C11C10
106.4(8)
N1-O5
1.235(8)
N10-C12
1.346(10)
O6N2O7
122.0(7)
N9C12N10
113.2(8)
N2-O6
1.230(8)
C10-C11
1.379(12)
O6N2O8
119.2(7)
C13N11C15
104.2(7)
N2-O7
1.240(8)
N11-C13
1.385(11)
O7N2O8
118.8(7)
C14N12C15
107.9(8)
N2-O8
1.278(8)
N11-C15
1.307(11)
C1N3C3
104.4(7)
C14C13N11
110.2(10)
N3-C1
1.381(10)
N12-C14
1.356(11)
C2N4C3
108.0(7)
C13C14N12
105.5(8)
N3-C3
1.310(9)
N12-C15
1.329(10)
C2C1N3
110.7(7)
N11C15N12
112.0(8)
N4-C2
1.353(11)
C13-C14
1.343(13)
C1C2N4
105.4(8)
C16N13C18
107.8(7)
N4-C3
1.343(11)
N13-C16
1.365(10)
N3C3N4
111.5(8)
C17N14C18
107.8(7)
C1-C2
1.347(11)
N13-C18
1.302(10)
C4N5C6
105.4(6)
C17C16N13
106.8(8)
N5-C4
1.376(10)
N14-C17
1.351(10)
C5N6C6
107.0(6)
C16C17N14
107.6(7)
N5-C6
1.317(11)
N14-C18
1.311(10)
C5C4N5
109.2(7)
N13C18N14
110.0(8)
N6-C5
1.353(10)
C16-C17
1.336(12)
C4C5N6
107.1(6)
N6-C6
1.346(9)
N5C6N6
111.3(7)
с атомом N2 гуанидиния превышают 3.4 Å. Боль-
Соединения II и III с соотношением NpO2+ :
шие температурные смещения атома O5, вероятно,
NO3- = 1 : 2 отличаются от других исследованных
обусловлены влиянием водородного связывания с
нами нитратных комплексов с однозарядными ка-
разупорядоченными катионами оксония и гуани-
тионами во внешней сфере тем, что в их кристал-
диния.
лической структуре нет КК взаимодействия.
РАДИОХИМИЯ том 62 № 3 2020
НИТР
АТНЫЕ КОМПЛЕКСЫ НЕПТУНИЯ(V)
199
Таблица 4. Водородные связи в структурах I-III
D-H…A
D-H, Å
H…A, Å
D…A, Å
D-H…A, град
Операция симметрии для A
[H3O][C(NH2)3]2[NpO2(NO3)2]3 (I)
N3-H3···O3
0.88
1.99
2.85(4)
165.2
x, y - 1, z
N3-H3···O5
0.88
2.37
2.98(4)
125.8
x, y - 1, z
N3-H4···O5
0.88
2.37
3.03(4)
131.4
y, -x + y, -z
N4-H5···O5
0.88
2.05
2.75(4)
135.4
1 + x - y, x, -z
N4-H6···O4
0.88
2.25
2.86(4)
126.0
N4-H6···O5
0.88
2.36
3.12(4)
144.9
[N(CH3)4][NpO2(NO3)2(H2O)2] (II)
O1w-H1···O1
0.88(2)
1.83(2)
2.7094(18)
173(3)
1 - x, -y, 1 - z
O1w-H2···O3
0.80(2)
2.00(2)
2.7730(17)
164(2)
x, 1 - y, z - 1/2
[HIm][NpO2(Im)5](NO3)2 (III)
N4-H1···O4
0.88
2.00
2.848(8)
161.6
x, y + 1, z + 1
N6-H2···O8
0.88
1.98
2.835(8)
162.5
N8-H3···O4
0.88
2.02
2.889(10)
170.5
N10-H4···O1
0.88
1.91
2.785(9)
170.8
1 - x, 1 - y, z - 1/2
N12-H5···O2
0.88
1.90
2.777(9)
173.9
1 - x, 2 - y, z + 1/2
N13-H6···O8
0.88
1.89
2.771(8)
175.3
-x + 3/2, y + 1/2, z - 1/2
N14-H7···O3
0.88
1.95
2.818(8)
167.0
-x + 3/2, y - 1/2, z + 1/2
Структура II является островной и состоит из
Молекула воды O1w, включенная в координаци-
комплексных анионов [NpO2(NO3)2(H2O)2]- и ка-
онное окружение атома Np1, образует водородные
тионов N(CH3)4+.
связи, акцепторами протонов в которых являют-
ся атом кислорода O1 катиона NpO2+ и O3 аниона
Атом Np1 находится в центре инверсии в по-
NO3- (табл. 4, рис. 3). Водородные связи объеди-
зиции 2b и имеет координационное окружение
няют комплексные анионы [NpO2(NO3)2(H2O)2]-
в виде гексагональной бипирамиды с двумя би-
в слои, параллельные плоскости [100] в кри-
дентатно-циклическими анионами NO3- и двумя
сталле. Слабое водородное взаимодействие типа
молекулами воды в экваториальной плоскости. В
Csp3-H···O [6], в котором акцепторами протонов
результате образуется центросимметричный ани-
являются атом O1 катиона NpO2+, атомы O2 и O4
он [NpO2(NO3)2(H2O)2]- (рис. 2). Длины связей
аниона NO3-, дополнительно стабилизирует кри-
и валентные углы в КП атома Np1 приведены в
сталлическую упаковку. Контакты C···O лежат в
табл. 2, максимальное отклонение атомов кисло-
пределах 3.309(2)-3.464(2) Å, контакты H···O - в
рода от экваториальной плоскости бипирамиды
пределах 2.55(3)-2.65(2) Å.
составляет 0.1325(7) Å. В гексагональной бипи-
рамиде атома Np1 структуры II связи с анионами
Катион тетраметиламмония N(CH3)4+ локализо-
NO3- заметно длиннее, чем в КП атомов нептуния
ван на оси второго порядка в позиции 2e, он распо-
структуры I и в структурах нитратных комплек-
лагается между слоями из комплексных анионов
сов с щелочными катионами во внешней сфере с
[NpO2(NO3)2(H2O)2]-.
квадратными (комплексы Li[NpO2(NO3)2]·2H2O
Причиной отсутствия КК взаимодействия в
и Na[NpO2(NO3)2]·2H2O) или тригонально-гекса-
структуре II являются, по-видимому, стерические
гональными (комплексы Cs3[NpO2(NO3)2]3·H2O и
затруднения, вызванные размерами внешнесфер-
NaRb5[NpO2(NO3)2]6·4H2O) катионными сетками
ного катиона. В слоях из комплексных анионов
[1]. Отметим, что средние для этих соединений
[NpO2(NO3)2(H2O)2]-, объединенных водородны-
длины связей в экваториальной плоскости гекса-
ми связями, расстояние Np···Np превышает 5 Å
гональных бипирамид равны: Np-Onitr 2.559 Å,
(табл. 2), тогда как в соединениях с КК связями
Np-Oyl 2.418 Å.
это расстояние не может превышать 4.3 Å, если
РАДИОХИМИЯ том 62 № 3 2020
200
ЧАРУШНИКОВА и др.
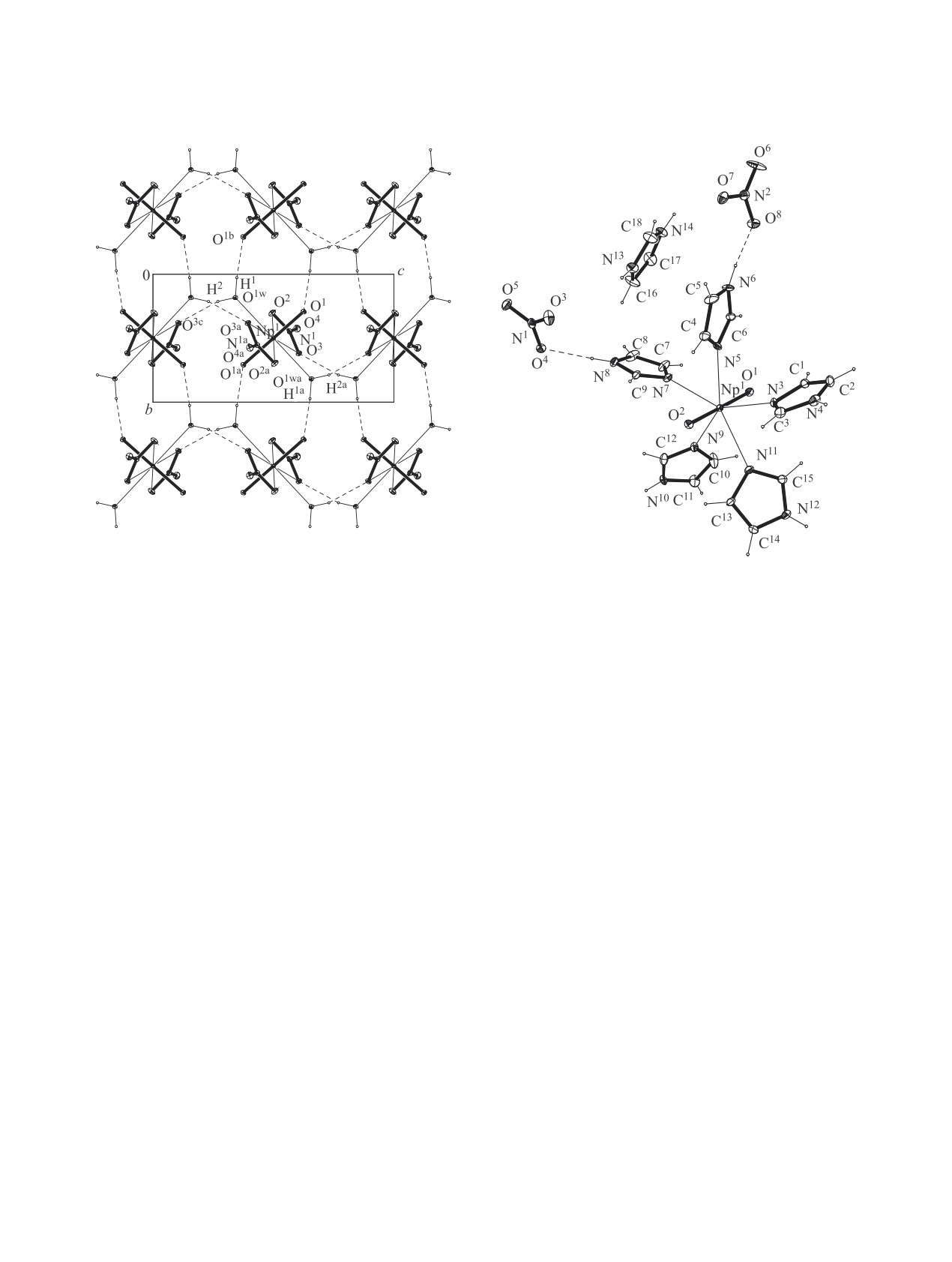
Рис.
3. Водородные связи в структуре
Рис. 4. Фрагмент структуры [HIm][NpO2(Im)5](NO3)2
[N(CH3)4][NpO2(NO3)2(H2O)2] (II). Проекция в
(III). Эллипсоиды температурных смещений даны с
направлении [100]. Операции симметрии: a - (-x, 1 -
50%-ной вероятностью. Пунктирными линиями пока-
y, 1 - z); b - (-x, -y, 1 - z); с - (x, 1 - y, z - 1/2).
заны водородные связи.
рассматривать его как сумму длин связей Np=O
имодействие типа N-H···O. Комплексные катионы
и Np-Oyl, так как усредненные длины этих связей
[NpO2(Im)5]+ связываются между собой водород-
примерно равны 1.85 и 2.45 Å [7].
ными связями, акцепторами протонов в которых
выступают «ильные» атомы кислорода катионов
Структура III состоит из катионов NpO2+ и
NpO2+, а доноры протонов - иминные группы ими-
имидазолия C3H5N2+, молекул имидазола и нитрат-
дазола с атомами азота N10 и N12 (табл. 4). В ре-
анионов. Атом Np1 катиона NpO2+ находится в об-
зультате образуются слои, в которых комплексные
щем положении, в экваториальной плоскости его
катионы [NpO2(Im)5]+ располагаются таким обра-
окружают пять молекул имидазола (рис. 4), обра-
зом, что молекулы имидазола, задействованные в
зуя комплексный катион [NpO2(Im)5]+. КП атома
H-связях с группами NpO2, располагаются внутри
Np1 - пентагональная бипирамида с «ильными»
слоя из комплексных катионов (рис. 5). Плоскости
атомами кислорода группы NpO2 в апикальных
этих молекул имидазола образуют с экваториаль-
позициях (средняя длина связей Np=O 1.836 Å,
ной плоскостью пентагональной бипирамиды дву-
табл. 3). Средняя длина связей Np-N в эквато-
гранные углы 55.4(2)° (атомы [N9C12N10C11C10],
риальной плоскости бипирамиды равна 2.559 Å,
рис. 4) и 50.3(2)° (атомы [N11C15N12C14C13]). Крат-
максимальное отклонение атомов азота от сред-
чайшее межатомное расстояние Np···Np в слое
неквадратичной плоскости экватора не превышает
равно 7.244 Å.
0.197(4) Å.
Анионы NO3- располагаются на внешних по-
Два независимых нитрат-иона не входят в коор-
верхностях слоев и связываются водородными
динационное окружение нептуния. Избыток отри-
связями с комплексными катионами [NpO2(Im)5]+.
цательного заряда компенсируется включением в
Катионы имидазолия C3H5N2+ располагаются в
структуру III катиона имидазолия.
межслоевом пространстве и как доноры прото-
В формировании кристаллической упаковки со-
нов связываются с анионами NO3-. При этом ани-
единения III важную роль играет водородное вза-
он с атомом азота N1 связывается водородными
РАДИОХИМИЯ том 62 № 3 2020
НИТР
АТНЫЕ КОМПЛЕКСЫ НЕПТУНИЯ(V)
201
буются дополнительные элементы. В данном слу-
a
чае в роли таких элементов выступают как катион
имидазолия, так и дополнительный анион NO3-.
Они вносят в структуру вклады как кулоновского,
N14dN13c
так и водородного взаимодействий.
O8
N5
O7 O6
Таким образом, исследовано строение нитрат-
N3
N7
Np1
O4
ных комплексов пятивалентного нептуния с одно-
N12b
N10a
N9
N11
зарядными органическими катионами во внешней
сфере. В комплексе с гуанидинием I осуществляет-
ся КК взаимодействие ионов NpO2+ с образовани-
ем тригонально-гексагональных катионных сеток.
В соединении II с катионом N(CH3)4+ во внешней
сфере КК взаимодействие отсутствует из-за стери-
ческих затруднений, и в КП атома Np вместо ка-
тионов NpO2+ включены молекулы воды. В струк-
0
c
туре III наличие крупных комплексных катионов
[NpO2(Im)5]+ также препятствует возникновению
Рис. 5. Слои из комплексных катионов [NpO2(Im)5]+,
КК связей в кристалле. КП атомов Np - гексаго-
анионов NO3- и катионов C3H5N2+ в структуре III, про-
екция на плоскость [010]. Пунктирными линиями пока-
нальная (I, II) и пентагональная бипирамида (III).
заны водородные связи. Операции симметрии: a - (1 -
x, 1 - y, 1/2 + z); b - (1 - x, 2 - y, -1/2 + z); c - (x, y - 1,
ФОНДОВАЯ ПОДДЕРЖКА
z); d - (3/2x, 1/2 + y, -1/2 + z).
Работа выполнена при частичном финан-
сировании Министерством науки и высше-
го образования Российской Федерации (тема
связями через атом O4 с комплексным катионом
№ АААА-А18-118040590105-4).
[NpO2(Im)5]+ одного слоя и через атом O3 с кати-
оном имидазолия. Анион с атомом азота N2 свя-
Рентгенодифракционные эксперименты выпол-
зывается относительно прочной водородной свя-
нены в Центре коллективного пользования физи-
зью типа C-H···O (контакты С9···O6 3.052(11) Å,
ческими методами исследования ИФХЭ РАН.
H16···O6 2.28 Å, угол D-H···A 138°) с комплекс-
КОНФЛИКТ ИНТЕРЕСОВ
ным катионом этого же слоя, а через атомы O8 -
Авторы заявляют об отсутствии конфликта
с комплексным катионом соседнего слоя и кати-
интересов.
оном имидазолия. Двугранные углы между эква-
ториальной плоскостью пентагональной бипи-
СПИСОК ЛИТЕРАТУРЫ
рамиды и плоскостями задействованных в этих
1. Чарушникова И.А., Григорьев М.С., Федосеев А.М.,
связях молекул имидазола равны: 78.9(3)° (атомы
Бессонов А.А., Лысенко К.А. // Радиохимия. 2020.
[N3C3N4C2C1]), 78.6(2)° (атомы [N5C6N6C5C4]) и
Т. 62, № 2. С. 114.
77.3(3)° (атомы [N7C9N8C8C7]).
2. Sheldrick G.M. SADABS. Madison, Wisconsin (USA):
В трехмерной системе водородных связей име-
Bruker AXS, 2008.
ет место и взаимодействие типа Csp2-H···O с уча-
3. Sheldrick G.M. // Acta Crystallogr., Sect. A. 2008.
стием C-H групп имидазола. Контакты C···O ле-
Vol. 64, N 1. P. 112.
жат в пределах 3.052(11)-3.380(10) Å, контакты
4. Sheldrick G.M. // Acta Crystallogr., Sect. C. 2015.
H···O - в пределах 2.28-2.53 Å. Эти H-связи более
Vol. 71, N 1. P. 3.
прочные, чем связи типа Csp3-H···O в структуре II.
5. Григорьев М.С., Чарушникова И.А., Крот Н.Н. //
Образование «громоздких» комплексных ка-
Радиохимия. 2005. Т. 47, № 6. С. 504.
тионов [NpO2(Im)5]+, по-видимому, и определяет
6. Steiner T. // Chem. Commun. 1997. N 8. P. 727.
структуру соединения III, так как для заполнения
7. Крот Н.Н., Григорьев М.С. // Успехи химии. 2004.
пространства кроме маленького нитрат-иона тре-
Т. 73, № 1. С. 94.
РАДИОХИМИЯ том 62 № 3 2020