РАДИОХИМИЯ, 2020, том 62, № 1, с. 11-19
УДК 539.26+546.798.21
КАТИОН-КАТИОННОЕ ВЗАИМОДЕЙСТВИЕ
В КОМПЛЕКСАХ БЕНЗОАТА И САЛИЦИЛАТА
Np(V) С N-СОДЕРЖАЩИМИ МОЛЕКУЛЯРНЫМИ
ЛИГАНДАМИ
© 2020 г. И. А. Чарушниковаа,*, Н. Н. Крота, В. П. Перминова
а Институт физической химии и электрохимии им. А. Н. Фрумкина РАН,
119071, Москва, Ленинский пр., д. 31, корп. 4
*e-mail: charushnikovai@ipc.rssi.ru
Получена 27.12.2018, после доработки 27.12.2018, принята к публикации 22.01.2019
Гидротермальным методом получены два новых соединения Np(V): бензоат состава [(NpO2)3(py)
(C7H5O2)3(H2O)2] (1) и салицилат состава [(NpO2)(phen)(HOC7H4O2)] (2), где py = пиридин, phen =
1,10-фенантролин. Исследование их строения методом рентгеноструктурного анализа показало, что
катионы NpO2+ связываются между собой катион-катионными связями, образуя искаженные квадратные
сетки в соединении 1 и зигзагообразные цепочки в 2.
Ключевые слова: нептуний(V), бензойная кислота, салициловая кислота, пиридин, 1,10-фенантролин,
синтез, кристаллическая структура, катион-катионное взаимодействие
DO1: 10.31857/S0033831120010025
При изучении свойств бензоатов пятивалент-
с bipy состава [(NpO2)2(bipy)2(o-FC7H4O2)2] [7],
ного нептуния NpO2(C7H5O2)·nH2O (n = 1-4) [1]
или с phen состава [(NpO2)2(phen)2(o-FC7H4O2)2]
на основании электронных спектров поглощения
и
[(NpO2)2(phen)2(p-FC7H4O2)2]
[8]. Однако в
(ЭСП) твёрдых соединений был сделан вывод о
м-нитробензоате Np(V) состава
[(NpO2)(bipy)-
присутствии в их структуре специфического, так
(NO2C7H4O2)(H2O)]·0.5bipy КК взаимодействие
называемого катион-катионного (КК) взаимо-
отсутствует [9].
действия диоксокатионов NpO2+, в котором они
В продолжение исследования КК взаимодей-
выступают одновременно как лиганды и как ко-
ствия в комплексах бензоатов Np(V) и их про-
ординирующие центры. Расшифровка структуры
изводных с N-содержащими лигандами были
дигидрата бензоата Np(V), точный состав которо-
синтезированы бензоат состава
[(NpO2)3(py)·
го описывается формулой [(NpO2)(C7H5O2)(H2O)]·
(C7H5O2)3(H2O)2] (py = пиридин C5H5N, 1) и сали-
3/4H2O [2, 3], показала, что в кристалле диок-
цилат состава [(NpO2)(phen)(HOC7H4O2)] (2).
сокатионы связываются в квадратные сетки.
Включение в состав бензоата N-донорных ли-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
гандов, таких как 2,2'-бипиридин C10H8N2 (bipy)
и 1,10-фенантролин C12H8N2 (phen) [4, 5], со-
Для синтеза соединений 1 и 2 был использован
провождается образованием димерных катионов
нейтральный раствор 0.14 моль/л NpO2Cl, полу-
Np2O42+, в которых ионы NpO2+ попарно связаны
ченный растворением гидроксида Np(V) в раз-
друг с другом КК связями. Такой тип КК взаимо-
бавленной HCl без избытка. Нептуний перед ис-
действия впервые наблюдался в структуре мелли-
пользованием очищали ионообменным методом,
тата Np(V) состава Na4[(NpO2)2C6(СOO)6]∙8H2O
концентрацию Np(V) определяли спектрофото-
[6]. Димерные катионы Np2O42+ найдены также и
метрически по его светопоглощению при 980 нм.
в комплексах фторпроизводных бензоатов Np(V)
Растворы бензоата лития и салицилата лития по-
11
12
ЧАРУШНИКОВА и др.
Таблица 1. Кристаллографические данные и характеристики рентгеноструктурного эксперимента
Параметр
1
2
Формула
C26H24NO14Np3
C19H13N2O5Np
М
1285.46
586.31
Сингония
Моноклинная
Ромбическая
Пространственная группа
P21/n
Pbca
Параметры ячейки:
a, Å
5.6319(7)
21.4066(15)
b, Å
17.146(2)
6.3217(4)
c, Å
31.559(4)
26.1875(18)
β, град
95.119(1)
90
V, Å3; Z
3035.3(6); 4
3543.9(4); 8
ρвыч, г/см3
2.813
2.198
μ(MoKα), мм-1
6.648
3.818
Количество измеренных/независимых отражений
18089/8037
48137/6478
Количество независимых отражений с I > 2σ(I)
5672
4680
Количество уточняемых параметров
398
249
R(F); wR(F2) [I > 2σ(I)]
0.0845; 0.2195
0.0300; 0.0834
R(F); wR(F2) [весь массив]
0.1108; 0.2314
0.0529; 0.1033
GOOF
1.063
0.878
Δρmax и Δρmin, e·Å-3
8.515; -6.232
2.294; -1.690
лучали растворением в стехиометрических коли-
твора 0.25 моль/л Li(HOC7H4O2), 0.04 мл раствора
чествах LiOH соответствующих кислот марки ч.,
0.25 моль/л phen и 0.1 мл воды. После запаивания
дополнительно очищенных перекристаллизацией.
ампулу выдерживали 3 сут при 140°С. В результа-
Использовали также водные растворы пиридина,
те были получены друзы светло-зелёных пластин-
нитрата пиридина и раствор фенантролина в эта-
чатых кристаллов. Один из них был выбран для
ноле. Растворы готовили из реагентов марки ч.д.а.
структурных исследований.
Вода была дважды перегнанной.
Рентгенодифракционные эксперименты вы-
Соединение 1 синтезировали следующим обра-
полнены на автоматическом четырехкружном
зом. К 0.1 мл раствора 0.14 моль/л NpO2Cl, поме-
дифрактометре с двумерным детектором Bruker
щённого в стеклянную ампулу, добавляли 0.04 мл
Kappa Apex II (излучение MoKα, графитовый мо-
раствора 0.5 моль/л Li(C7H5O2), 0.1 мл раствора
нохроматор) при 100 K. Измерены интенсивно-
0.5 моль/л py и 0.1 мл раствора 0.1 моль/л pyHNO3.
сти рефлексов в полусферах обратного простран-
Ампулу запаивали и выдерживали при 115°С 3 сут.
ства. Параметры элементарных ячеек уточнены
В итоге на стенках ампулы образовались большие
по всему массиву данных. В экспериментальные
пластинчатые кристаллы зелёного цвета, пригод-
интенсивности введены поправки на поглощение
ные для рентгеноструктурных исследований.
с помощью программы SADABS [10]. Структуры
В случае приготовления 2 в стеклянную ампу-
расшифрованы прямым методом (SHELXS97 [11])
лу помещали 0.1 мл раствора Np(V), 0.04 мл рас-
и уточнены полноматричными методами наимень-
РАДИОХИМИЯ том 62 № 1 2020
КАТИОН-КАТИОННОЕ ВЗАИМОДЕЙСТВИЕ В КОМПЛЕКСАХ БЕНЗОАТА И САЛИЦИЛАТА
13
Таблица 2. Длины связей (d, Å) и валентные углы (ω, град) в структуре 1a
Связь
d
Угол
ω
Np1=O11
1.825(12)
O11Np1O12
176.4(5)
Np1=O12
1.844(12)
O1Np1O32A
68.2(4)
Np1-O32A
2.434(12)
O22BNp1O1
74.1(4)
Np1-O22B
2.398(12)
O6ANp1O32A
75.0(5)
Np1-O1
2.423(12)
O6ANp1O1w
71.9(5)
Np1-O6A
2.380(15)
O22BNp1O1w
70.9(5)
Np1-O1w
2.546(14)
Np2=O21
1.844(12)
O21Np2O22
176.8(5)
Np2=O22
1.841(12)
O2Np2O11
72.7(5)
Np2-O11
2.432(12)
O31CNp2O3
74.5(4)
Np2-O31C
2.330(11)
O11Np2O3
70.8(4)
Np2-O2
2.404(13)
O31CNp2N1
72.7(5)
Np2-O3
2.495(13)
O2Np2N1
69.4(5)
Np2-N1
2.599(16)
Np3=O31
1.881(12)
O31Np3O32
177.8(5)
Np3=O32
1.858(12)
O12DNp3O5
77.9(5)
Np3-O12D
2.359(12)
O5Np3O21
74.7(4)
Np3-O21
2.432(12)
O21Np3O4
72.5(5)
Np3-O4
2.446(15)
O12DNp3O2w
70.4(4)
Np3-O5
2.387(14)
O4Np3O2w
65.4(4)
Np3-O2w
2.620(13)
Np1···Np2
4.0658(9)
Np1O11Np2
145.2(6)
Np1···Np3A
4.0955(9)
Np1O12Np3D
158.4(6)
Np2···Np3
4.0233(9)
Np2O21Np3
140.0(7)
Np2O22Np1C
159.1(7)
Np3O31Np2B
155.0(7)
Np3O32Np1A
144.9(6)
a Операции симметрии: A - (1/2 - x, -1/2 + y, 3/2 - z); B - (x + 1, y, z); C - (x - 1, y, z); D - (3/2 - x, -1/2 + y, 3/2 - z).
ших квадратов (SHELXS-2014 [12]) по F2 по всем
Результаты уточнения и основные кристалло-
данным в анизотропном приближении для всех
графические данные для структур 1 и 2 приведе-
неводородных атомов. Атомы H у кольцевых ато-
ны в табл. 1, длины связей и валентные углы - в
мов углерода анионов C6H5COO- и HOC6H4COO-,
табл. 2 и 3. Координаты атомов депонированы в
молекул пиридина (1) и фенантролина (2) введены
Кембриджский центр кристаллографических дан-
ных, депоненты CCDC 1857134, 1857135.
на геометрически рассчитанные позиции с UН =
1.2Uэкв(С). Атомы H у молекулы воды в 1 найдены
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
с использованием программы [13]. Атом H у ги-
дроксогруппы аниона HOC6H4COO- локализован
Структура 1 слоистого типа состоит из кати-
на разностном синтезе Фурье. Все атомы H уточ-
онов NpO2+, анионов C6H5COO-, координацион-
нены с UН = 1.5Uэкв(О) и ограниченными межа-
но-связанных молекул пиридина и воды.
томными расстояниями O-H и валентными углами
Три кристаллографически независимых ато-
H-О-Н.
ма Np имеют окружение в виде пентагональных
РАДИОХИМИЯ том 62 № 1 2020
14
ЧАРУШНИКОВА и др.
Таблица 3. Длины связей (d, Å) и валентные углы (ω, град) в структуре 2a
Связь
d
Угол
ω
Np1=O11
1.877(3)
O11Np1O12
175.34(13)
Np1=O12
1.808(3)
O11ANp1O1
78.58(10)
Np1-O11A
2.428(3)
O2BNp1O1
71.66(10)
Np1-O1
2.450(3)
O2BNp1N1
75.60(10)
Np1-O2B
2.429(3)
O11ANp1N2
73.50(10)
Np1-N1
2.618(3)
N1Np1N2
62.13(10)
Np1-N2
2.666(3)
C13-O1
1.240(5)
O1C13O2
125.0(4)
C13-O2
1.284(5)
O1C13C14
118.7(4)
C15-O3
1.347(5)
O2C13C14
116.3(4)
C13-C14
1.495(6)
O3C15C14
123.2(4)
Среднее (C-C)цикл
1.393(8)
O3C15C16
117.8(4)
Средн. (CCC)
120.0(5)
Np1···Np1A
4.0418(3)
Np1ANp1Np1B
102.895(8)
a Операции симметрии: A - (-x + 1/2, y - 1/2, z); B - (-x + 1/2, y + 1/2, z).
Таблица 4. Водородные связи в структурах
D-H···A
D-H, Å
H···A, Å
D···A, Å
D-H···A, град
Операция симметрии для A
[(NpO2)3(py)(C7H5O2)3(H2O)2] (1)
O1w-H1···O4
0.85
2.36
3.12(2)
148.0
O1w-H2···O3
0.86
2.09
2.879(18)
152.7
x + 1, y, z
O2w-H3···O1
0.85(2)
1.99(8)
2.814(18)
163(24)
-x + 3/2, y + 1/2, -z + 3/2
O2w-H4···O3
0.85(2)
2.30(18)
2.921(18)
130(19)
x + 1, y, z
C26-H24···O21
0.95
2.64
3.21(2)
119.1
[NpO2(phen)(HOC7H4O2)] (2)
O3-H1···O2
0.85(2)
1.78(4)
2.572(5)
154(8)
C1-H2···O2
0.95
2.40
3.016(5)
122.1
-x + 1/2, y + 1/2, z
C1-H2···O12
0.95
2.38
3.075(5)
129.3
x, y + 1, z
C12-H9···O11
0.95
2.29
2.965(5)
127.8
-x + 1/2, y - 1/2, z
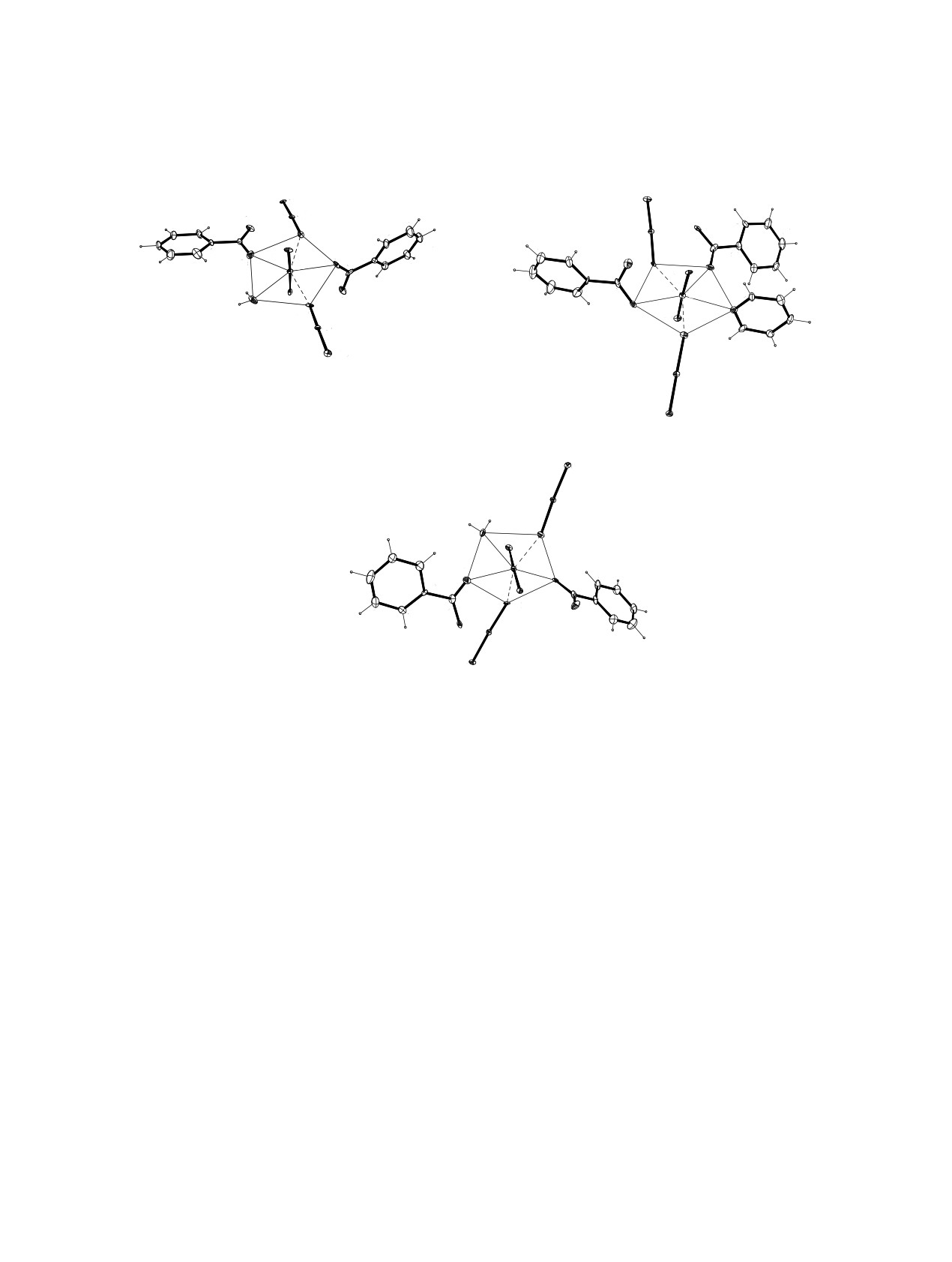
бипирамид (рис. 1). Экваториальные плоскости
Три независимых бензоат-иона являются би-
координационных полиэдров (КП) атомов Np1 и
дентатно-мостиковыми лигандами и связывают
между собой соседние катионы NpO2+. Они имеют
Np3 формируют атомы кислорода двух анионов
обычные для анионов C6H5COO- геометрические
C6H5COO-, двух катионов NpO2+ и молекулы воды.
характеристики. Длины связей в карбоксилатных
В координационном окружении атомам Np2 место
группировках COO лежат в пределах 1.23(2)-
молекулы воды занимает молекула пиридина. КК
1.35(2) Å и здесь явно просматривается тенден-
взаимодействие катионов NpO2+ приводит к об-
ция к удлинению связи C=O с атомом кислорода,
разованию квадратных катионных сеток (рис. 2,
включённым в качестве акцептора протона в водо-
табл. 2).
родную связь с молекулой воды. Средние для трёх
РАДИОХИМИЯ том 62 № 1 2020
КАТИОН-КАТИОННОЕ ВЗАИМОДЕЙСТВИЕ В КОМПЛЕКСАХ БЕНЗОАТА И САЛИЦИЛАТА
15
(а)
(б)
O31A
O12
O5A
Np3A
C4
C4
O1
C20A
C21A
O32A
Np1
C3
C5
C15A
C3
C13C14
C1
C5
O1
C2
O4
C16A
O11
O11
C2
C7
C19A
O21
C6
O6A
C6
C9
C18AC17A
Np1
C1
C74
C12
Np
2C
C25
O11
C8
O2
C11 C10
O22
C24
O1w
O22B
C26
N1
Np2B
O31C
C22
C23
O21B
Np3C
O32C
(в)
O11A
Np1A
O2w
O12A
C
13
O31
C14
C12
Np3
C21
C
9
O
32
C15
C20
C1
O4
O5
C19
O21
6
C10C8
O
C
16
C17
C18
Np2
O22
Рис. 1. Координационное окружение атомов Np в структуре [(NpO2)3(py)(C7H5O2)3(H2O)2] (1): (а) атом Np1; (б) атом Np2;
(в) атом Np3. Эллипсоиды температурных смещений даны с 30% вероятностью. Пунктирными линиями показаны КК связи.
Операции симметрии: A - (1/2-x, -1/2+y, 3/2-z); B - (x+1, y, z); C - (x-1, y, z); D - (3/2-x, 1/2+y, 3/2-z).
анионов длины связей Csp3-Csp2 равны 1.50(3) Å,
Сравним строение 1 со строением бензоата неп-
циклические связи C-C равны 1.40(4) Å.
туноила состава
[(NpO2)(C7H5O2)(H2O)]·3/4H2O
Пиридин в качестве молекулярного лиганда
[2, 3].
входит в координационное окружение атома Np2.
Структура [(NpO2)(C7H5O2)(H2O)]·3/4H2O сло-
Его усреднённые длины связей имеют следую-
истого типа содержит четыре кристаллографиче-
щие значения: длина связей N-C равна 1.30(3) Å,
ски независимые формульные единицы, при этом
циклической связи C-C - 1.40(3) Å. Валентный
все атомы Np имеют координационное окружение
угол CNC равен 119.7(18)°, среднее значение для
одинакового состава. Экваториальная плоскость
углов NCC равно 124(2)°, для углов CCC - 118(2)°.
пентагональных бипирамид всех четырёх атомов
Лиганды - пиридин и бензоат-ионы - распола-
Np содержат два атома кислорода соседних ка-
гаются по обе стороны от катионных сеток (рис. 3),
тионов NpO2+, два атома кислорода двух бензоат-
образуют нейтральные слои, перпендикулярные
ионов и молекулу воды. Разница в строении КП
направлению [001] в кристалле. Две независимые
атомов нептуния заключается лишь в том, что для
молекулы воды, включённые в координационное
атома Np3 наблюдается иной порядок располо-
окружение атомов Np1 и Np3, являются донорами
жения атомов кислорода в экваториальном поясе
протонов в водородных связях (табл. 4), дополни-
бипирамиды, здесь молекула воды располагается
тельно связывающих составные части структуры
между двумя группировками NpO2. В КП других
в слоях.
атомов Np молекула воды располагается между
РАДИОХИМИЯ том 62 № 1 2020
16
ЧАРУШНИКОВА и др.
a
0
c
O22
b
0
O32
O11
O21
Np2
Np3
Np1
O12
O31
a
b
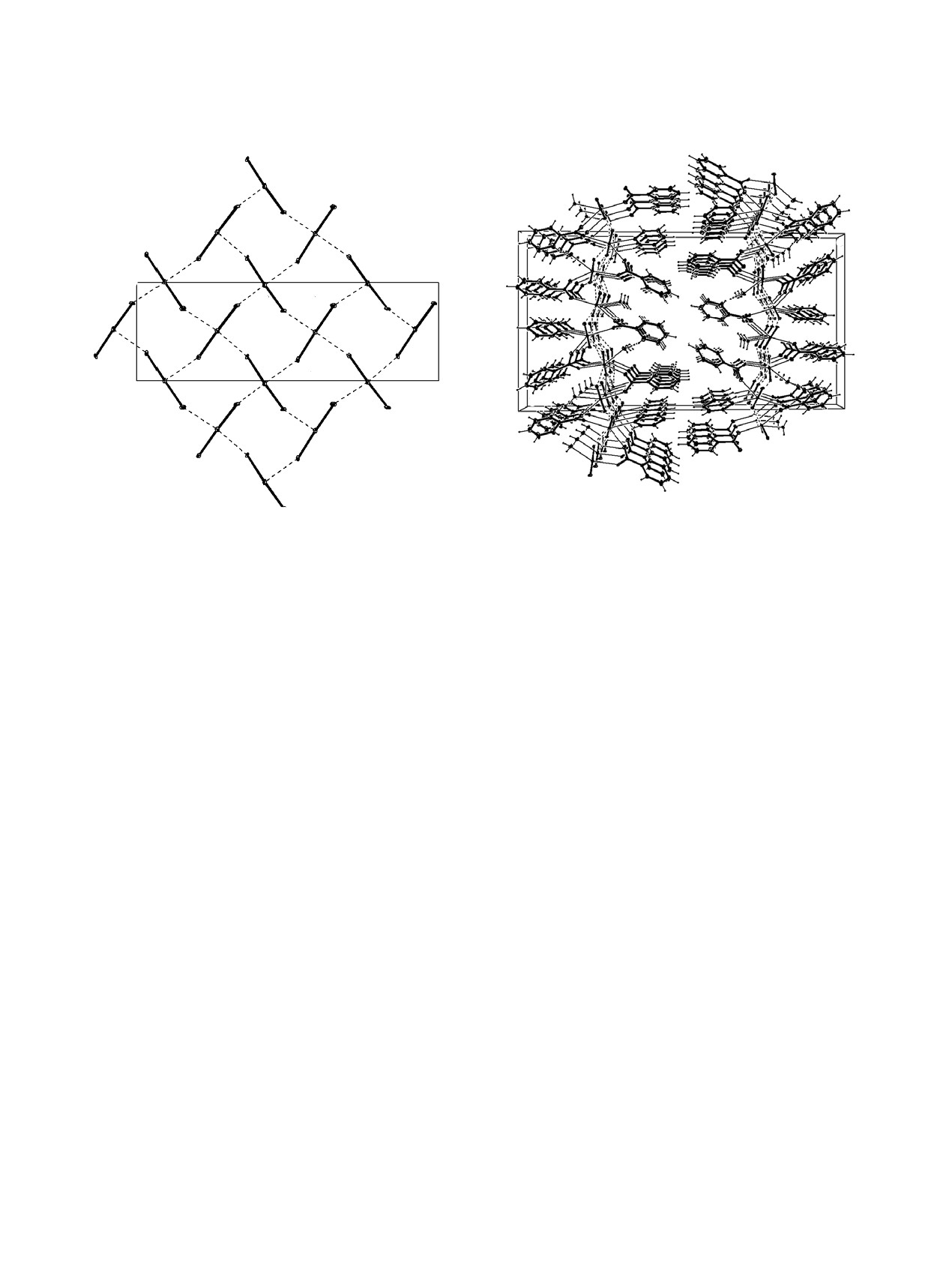
Рис. 2. Катионная сетка в структуре 1. Проекция на
Рис. 3. Упаковка молекул в структуре 1. Пунктирными
плоскость (110).
линиями показаны КК связи.
группировкой NpO2 и анионом. Расстояния Np=O
сетка сильно искажена и среднеквадратичная пло-
в группировках NpO2 находятся в пределах от
скость, рассчитанная через все атомы Np, непло-
1.82(1) до 1.87(1) Å, а углы O=Np=O - от 179.0(6)
ская в пределах ±0.892 Å.
до 175.1(6)°. В экваториальных плоскостях КП
Кристаллическая структура соединения
2
атомов Np расстояния Np-O изменяются от 2.40(1)
состоит из катионов NpO2+, салицилат-ионов
до 2.50(1) Å для «ильных» атомов кислорода, от
HOC6H4COO- и молекул фенантролина, связан-
2.39(1) до 2.53(1) Å для атомов кислорода бен-
ных в электронейтральные бесконечные цепочки
зоат-ионов и от 2.52(1) до 2.58(2) Å для молекул
[(NpO2)(phen)(HOC7H4O2)]n.
воды. КК взаимодействие приводит к образованию
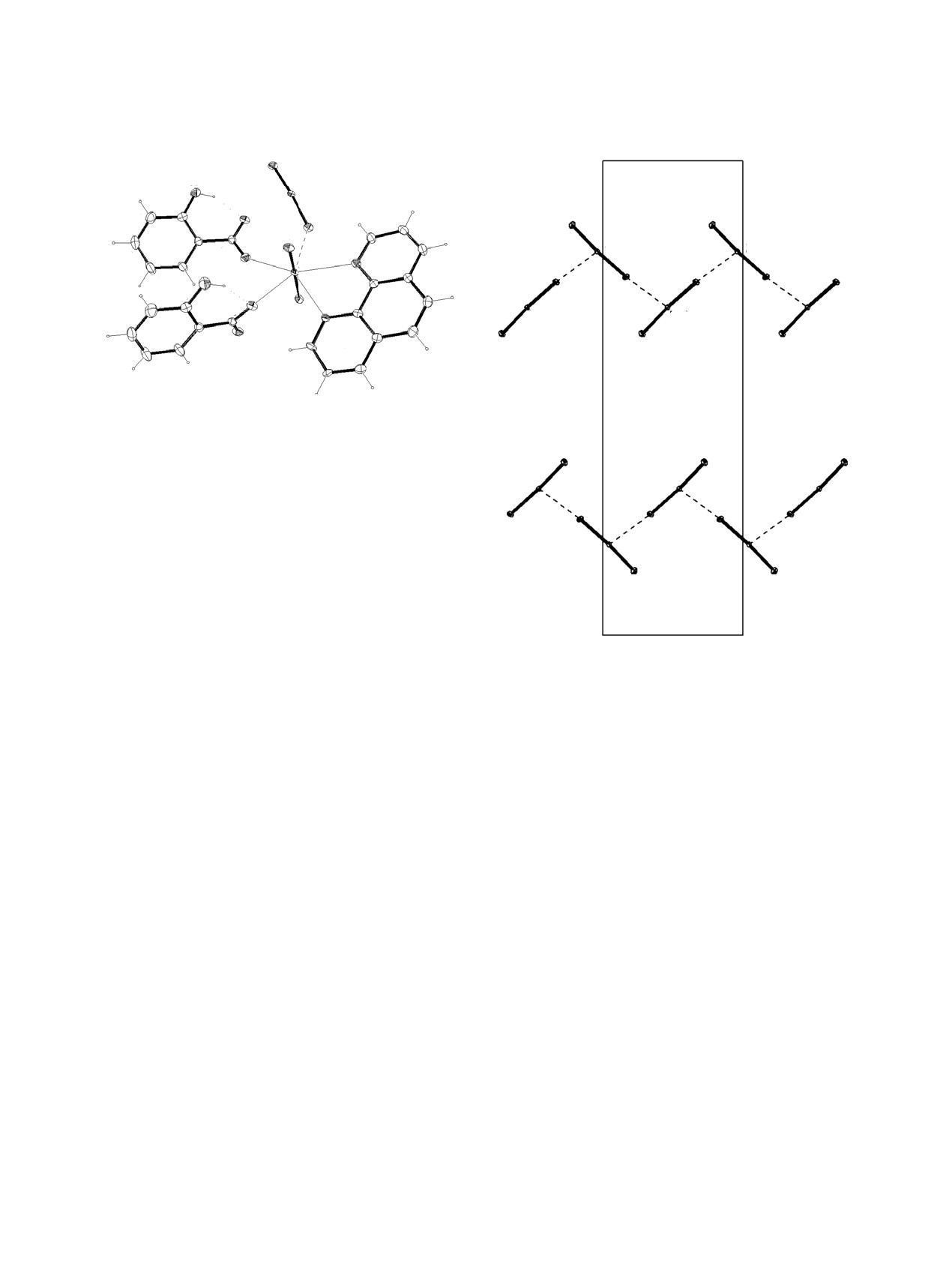
Атом Np1 в структуре имеет координационное
искаженных квадратных катионных сеток, парал-
окружение в виде пентагональной бипирамиды, в
лельных (010). Расстояния Np···Np находятся в
экваториальную плоскость которой включены два
пределах от 4.015(1) до 4.238(1) Å.
атома кислорода от двух салицилат-ионов, один
В исследованном соединении
1 координа-
атом кислорода от соседнего катиона NpO2+ и два
ционное окружение атомов Np1 и Np3 та-
атома азота фенантролина (рис. 4). Длины связей
кое же, как у атомов Np1, Np2 и Np4 в бензоате
внутри КП атома Np1 приведены в табл. 3. КК вза-
[(NpO2)(C7H5O2)(H2O)]·3/4H2O. Замена одной мо-
имодействие связывает катионы NpO2+ в цепочки,
лекулы воды на N-донорный лиганд пиридин не
вытянутые вдоль направления [010] в кристалле.
приводит к изменению характера КК взаимодей-
ствия, однако разброс в межатомных расстояниях
Анион HOC6H4COO- является бидентатно-мо-
Np···Np в 1 меньше (табл. 2), чем в бензоате. В
стиковым лигандом и связывает соседние в ка-
1 катионная сетка гофрирована и условная пло-
тионной цепочке группы NpO2. Длины связей
скость, объединяющая все атомы Np, имеет пере-
и валентные углы в анионе приведены в табл. 3.
гибы ~143°, как это видно на рис. 3. Гофрировка
Длины связей в карбоксилатной группе COO силь-
возникает под влиянием двух факторов: «стягива-
но различаются из-за включения атома кислорода
ния» мостиковыми анионами и дополнительного
O2 в качестве акцептора протона в очень прочную
наложения водородного взаимодействия. В бен-
внутримолекулярную водородную связь с OH-
зоате
[(NpO2)(C7H5O2)(H2O)]·3/4H2O катионная
группой (рис. 4, табл. 4). Группа СОО повёрнута
РАДИОХИМИЯ том 62 № 1 2020
КАТИОН-КАТИОННОЕ ВЗАИМОДЕЙСТВИЕ В КОМПЛЕКСАХ БЕНЗОАТА И САЛИЦИЛАТА
17
O12A
0
b
O3
Np1A
C15
O2
C16
O11A C12
C14
O12
C11
C13
Np1A
Np1B
C
17
C19
C9
O1
C18
N2
C8
O11
C15B
O3B
O
2B
C7
C16B
O11
Np1C
C17B
N1
C4
Np1
Np1D
C5
O1B
C19B
C14B
C6
O12
C18B
C2
C1
C3
Рис. 4. Координационное окружение атома Np1 в струк-
туре [NpO2(phen)(HOC7H4O2)] (2). Эллипсоиды тем-
пературных смещений даны с 50%-ной вероятностью.
Пунктирными линиями показаны КК и водородные
связи. Операции симметрии: A - (-x + 1/2, y - 1/2, z);
B - (-x + 1/2, y + 1/2, z).
относительно плоскости фенольного остатка на
угол 19.7(4)°.
Молекулярный лиганд фенантролин имеет дли-
ны связей и валентные углы такие же, как в дру-
гих структурах, например в исследованных ранее
a
комплексах бензоата, о-фторбензоата и п-фторбен-
зоата Np(V) с фенантролином [8]. Молекулярный
Рис. 5. Катионные цепочки в структуре 2, проекция на
лиганд плоский в пределах ±0.103(4) [отклоне-
плоскость (110).
ние атома C2], средняя длина связей C-N равна
1.342(5) Å, связей (C-C)цикл - 1.403(6) Å.
дроксо-группы, хотя в бензоате [(NpO2)2(phen)2(o-
FC7H4O2)2] наличие атома фтора в орто-положе-
Салицилат-ионы, связывая соседние в катион-
нии безольного кольца не приводит к изменению
ной цепочке группы NpO2, способствуют тому, что
структуры, димерные катионы Np2O42+ сохраня-
цепочки становятся неплоскими. Иными словами,
ются. Внутри КП атомов Np1 в соединениях 2,
катионы NpO2+ с атомами Np1A и Np1B (рис. 5) ле-
[(NpO2)2(phen)2(C7H4O2)2] и фторпроизводных
жат в плоскости, которая образует с плоскостью
бензоата Np(V)
[(NpO2)2(phen)2(o-FC7H4O2)2]
катионов с атомами Np1, Np1C и Np1D двугранный
не наблюдается сколько-нибудь заметной раз-
угол ~116°. Салицилат-ионы располагаются с вну-
тренней стороны цепочек, а молекулы координа-
ницы в средних длинах связей Np-O с аниона-
ционно-связанного фенантролина - с наружной
ми HOC6H4COO-, C6H5COO-, o-FC6H4COO- и
стороны (рис. 6).
p-FC6H4COO-.
Сопоставим строение салицилата 2 со строени-
Как уже отмечалось выше, влияние внутримо-
ем бензоатов и фторпроизводных бензоатов непту-
лекулярного водородного связывания с гидрок-
ноила в комплексах с фенантролином [8].
согруппой в структуре 2 проявляется в заметном
Сравнение
строения
бензоата
различии длин связей в карбоксилатной группе
[(NpO2)2(phen)2(C7H4O2)2] [8] и салицилата 2 по-
аниона (табл. 3). Нарушение делокализации от-
казало, что при переходе от бензоата к салицила-
рицательного заряда в группе СОО приводит к
ту КК сохраняется, но димерные катионы Np2O42+
некоторому упрочнению связи Np1-O в экватори-
размыкаются и образуются катионные цепочки.
альном поясе бипирамиды с атомом кислорода O2,
По-видимому, это происходит под влиянием ги-
задействованным в водородном взаимодействии
РАДИОХИМИЯ том 62 № 1 2020
18
ЧАРУШНИКОВА и др.
носительно друг друга равен 1.485 Å, т.е. они пере-
крываются на треть.
a
Следует отметить, что в цепочечных кристалли-
ческих структурах, в которых также присутствует и
КК взаимодействие, в зависимости от того, как ос-
новные структурообразующие элементы (анионы
и катионы) связываются друг с другом, либо кати-
онные цепочки могут быть плоские, либо катионы
NpO2+ располагаются в параллельных плоскостях,
либо в плоскостях под углом друг к другу, как в
структуре 2. Например, в структуре гликолята неп-
туноила
[NpO2(bipy)(OOC2H2OH)]·1.5H2O
[15],
0
c
основной структурообразующий мотив - нептуно-
b
илгликолятные цепочки, в которых катионы также
объединяются через КК связи. КК цепочки рас-
Рис. 6. Упаковка молекул в структуре 2. Цепочки
полагаются в плоскостях, двугранный угол меж-
вытянуты вдоль оси b
[(NpO2)(phen)(HOC7H4O2)]n
ду которыми равен 145.5(1)°. Наклон плоскостей
кристалла.
возникает из-за объединения анионами катионов
+ из разных плоскостей, так же как и в кри-
NpO2
(рис. 1). Поворот группы СОО относительно пло-
сталле 2. В структуре гликолята возникает взаимо-
скости бензольного кольца, по-видимому, обуслов-
действие между π-системами колец бипиридина из
лен мостиковой функцией аниона, связывающего
соседних цепочек. Кольца перекрываются на треть
два соседних в цепочке катиона NpO2+. Салицилат-
и расстояние между центрами колец равно 3.53 Å.
анион (связь Np1-O1) практически лежит в эква-
Возможно, взаимодействие между π-системами
ториальной плоскости бипирамиды [двугранный
колец из соседних цепочек в какой-то мере влия-
угол 20.0(2)°], второй анион (связь Np1-O2A) рас-
ет на то, что двугранный угол между плоскостями
положен почти перпендикулярно [угол 82.4(1)°]. В
из катионов NpO2+ в структуре гликолята гораздо
бензоатах и фторбензоатах анионы плоские и об-
больше, чем в структуре 2, так как в салицилате
разуют с экваториальной плоскостью бипирамид
π-стекинг возникает вдоль цепочек.
углы ~53°.
В КП атома Np1 гликолята разница в длинах
Сравнение геометрических характеристик ка-
связей Np=O (Δ = 0.048 Å) меньше, чем в струк-
тионных связей показало, что большая разница в
туре 2, угол O=Np=O равен 176.1(2)°, а дли-
длинах связей Np=O, найденная в димерных ка-
на катионной связи Np-Oyl равна 2.458(4) Å.
тионах Np2O42+, сохраняется и в цепочках 2: Δ =
Наблюдается заметная разница в длинах свя-
0.060 Å в [(NpO2)2(phen)2(C7H4O2)2], Δ = 0.064 Å
зей Np-N в КП атомов нептуния в структрах
в [(NpO2)2(phen)2(o-FC7H4O2)2], Δ = 0.063 Å в
2 и гликолята: Δ = 0.048 Å для фенантролина
[(NpO2)2(phen)2(p-FC7H4O2)2] и Δ = 0.069 Å в
в 2 и 0.071(6) Å для бипиридина в гликоляте
2. Угол O=Np=O практически не меняется, зато
[NpO2(bipy)(OOC2H2OH)]·1.5H2O. Поскольку в
катионная связь Np-Oyl в экваториальной пло-
структурах бензоатов [(NpO2)2(phen)2(C7H4O2)2]
скости изменяется заметно. Самая слабая связь
и [(NpO2)2(phen)2(o-FC7H4O2)2] связи Np-N вы-
[(2.4956(16) и 2.498(4) Å] в o- и п-фторбензоатах,
равнены, можно полагать, что большой разброс в
самая прочная - в салицилате [2.428(3) Å].
длинах связей в 2 и гликоляте происходит под вли-
Вдоль цепочек
[(NpO2)(phen)(HOC7H4O2)]n
янием π-стекинга.
в структуре 2 возникает взаимодействие между
Таким образом, исследовано строение двух
π-системами колец A и C фенантролина (рис. 1).
новых соединений Np(V) с молекулярными
Расчёты, проведенные с использованием программ
N-донорными лигандами
- пиридином и фе-
OLEX2 [14], показали, что расстояние между цен-
нантролином: бензоата состава
[(NpO2)3(py)·
трами колец составляет ~3.60 Å и сдвиг колец от-
(C7H5O2)3(H2O)2] (1) и о-оксибензоата (салици-
РАДИОХИМИЯ том 62 № 1 2020
КАТИОН-КАТИОННОЕ ВЗАИМОДЕЙСТВИЕ В КОМПЛЕКСАХ БЕНЗОАТА И САЛИЦИЛАТА
19
лата) состава [(NpO2)(phen)(HOC7H4O2)] (2). В
5. Charushnikova I.A., Krot N.N., Starikova Z.A. //
структуре 1 образуются квадратные катионные
Radiochim. Acta. 2007. Vol. 95, N 3. P. 495.
6. Cousson A., Dabos S., Abazli H. et al. // J. Less-
сетки, как в простом бензоате Np(V). Замена бен-
Common Met. 1984. Vol. 99, N 2. P. 233.
зоат-иона на салицилат-ион, гидроксогруппа ко-
7. Grigoriev M.S., Krot N.N., Bessonov A.A., Suponits-
торого образует прочную внутримолекулярную
ky K.Yu. // Acta Crystallogr. Sect. E. 2007. Vol. 63,
водородную связь с одним из атомов кислорода
N 2. P. m561.
карбоксильной группы, приводит к образованию
8. Чарушникова И.А., Крот Н.Н., Григорьев М.С. //
цепочечной структуры 2.
Радиохимия. 2019. Т. 61, № 3. С. 223.
9. Charushnikova I.A., Grigoriev M.S., Krot N.N. //
КОНФЛИКТ ИНТЕРЕСОВ
Radiochim. Acta. 2011. Vol. 99, N 4. P. 197.
10. Sheldrick G.M. SADABS. Madison, Wisconsin (USA):
Авторы заявляют об отсутствии конфликта
Bruker AXS, 2008.
интересов.
11. Sheldrick G.M. // Acta Crystallogr. Sect. A. 2008.
Vol. 64, N 1. P. 112-122.
СПИСОК ЛИТЕРАТУРЫ
12. Sheldrick G.M. // Acta Crystallogr. Sect. C. 2015.
1. Чарушникова И.А., Афонасьева Т.В., Перминов В.П.,
Vol. 71, N 1, P. 3-8.
Крот Н.Н. // Радиохимия. 1992. Т. 34, № 6. С. 7.
13. Nardelli M. // J. Appl. Crystallogr. 1999. Vol. 21, N 3.
2. Krot N.N., Charushnikova I.A., Grigoriev M.S. //
P. 563-571.
22émes Journées des Actinides (Program and Abstracts).
14. Dolomanov O.V., Bourhis L.J., Gildea R.J., Ho-
Méribel, France, 1992. P. 35.
ward J.A.K., Puschmann H. // J. Appl. Crystallogr. 2009.
3. Григорьев М.С. Дис
д.х.н. М.: ИФХ РАН, 1995.
Vol. 42, N 2. P. 339.
4. Бессонов АА., Крот Н Н., Григорьев М.С., Макарен-
15. Charushnikova I.A., Krot N.N., Starikova Z.A. //
ков В.И. // Радиохимия. 2009. Т. 51, № 3. С. 202.
Radiochim. Acta. 2009. Vol. 97, N 10. P. 587.
РАДИОХИМИЯ том 62 № 1 2020