Радиохимия, 2019, т. 61, N 6, c. 523-528
523
Модификация анионообменной методики концентрирования
изотопа 68Ga и автоматический синтез радиофармпрепарата
[68Ga]Ga-ПСМА-11
© Д. О. Антуганова, Д. В. Рыжковаа, В. В. Тимофеева, Т. А. Зыковаа, Ю. О. Антугановаа,
К. Ю. Тимофееваа, О. П. Самбурова, М. П. Зыков*а
а Национальный медицинский исследовательский центр им. В. А. Алмазова Министерства здравоохранения РФ,
197341, Санкт-Петербург, ул. Аккуратова, д. 2; *e-mail: zykovm@ya.ru
Получена 26.11.2018, после доработки 17.12.2018, принята к публикации 17.12.2018
УДК 661.879
Систематически изучена анионообменная методика концентрирования изотопа 68Ga, полученного из
генератора 68Ga/68Ge ЗАО «Циклотрон». Описана методика синтеза [68Ga]Ga-ПСМА-11, позволяющая
получать с высоким выходом (58 ± 3%, n = 10, от активности, элюированной с генератора) продукт,
удовлетворяющий всем требованиям для клинического применения. Синтез [68Ga]Ga-ПСМА-11 осуществ-
лялся на автоматизированном модуле, сконструированном в НМИЦ им. В. А. Алмазова.
Ключевые слова: позитронная эмиссионная томография, [68Ga]Ga-ПСМА-11, [68Ga]Ga-PSMA-
HBED-CC, радиофармпрепарат, генератор галлия-68.
DOI: 10.1134/S0033831119060145
Рак предстательной железы (РПЖ) занимает вто-
ции методом ядерной медицины, среди которых
рое место в структуре заболеваемости онкологиче-
наиболее широкое применение получила ацикличе-
скими заболеваниями у мужчин [1], поэтому поиск
ская N,N'-бис[2-гидрокси-5-(карбоксиэтил)бензил]-
новых высокоэффективных методов визуализации
этилендиамин-N,N'-диуксусная кислота (PSMA-
первичного опухолевого очага, стадирования и рес-
HBED-CC; ПСМА-11), способная образовывать
тадирования РПЖ является актуальной проблемой
комплексы с 68Ga (T1/2 = 68 мин) [5]. Этот комплекс
здравоохранения. Наиболее перспективными пред-
успешно используется в медицине для диагностики
ставляются методы функциональной визуализации,
рака предстательной железы [6, 7]. Однако этот ли-
в том числе гибридные технологии ядерной медици-
ганд оказался не способен связываться с терапевти-
ны - ПЭТ-КТ и ПЭТ-МРТ с мечеными лигандами к
ческими радионуклидами (177Lu или 225Ac), поэтому
простат-специфическому мембранному антигену
в последние годы широкое применение находит мо-
(ПСМА).
дифицированный
1,4,7,10-тетраазациклододекан-
N,N',N'',N'''-тетрауксусной кислотой (ДОТА) хелатор
Простат-специфический мембранный антиген
также известен как фолатгидролаза I, глутаматкар-
ПСМА-617. [68Ga]Ga-ПСМА-617 показывает схожее
накопление в тканях, но требует более длительного
боксипептидаза II - это интегральный мембранный
протокола сканирования [8, 9]. Структуры обоих
протеин, впервые обнаруженный в клетках РПЖ
линии LNCaP [2]. Антиген в норме экспрессируется
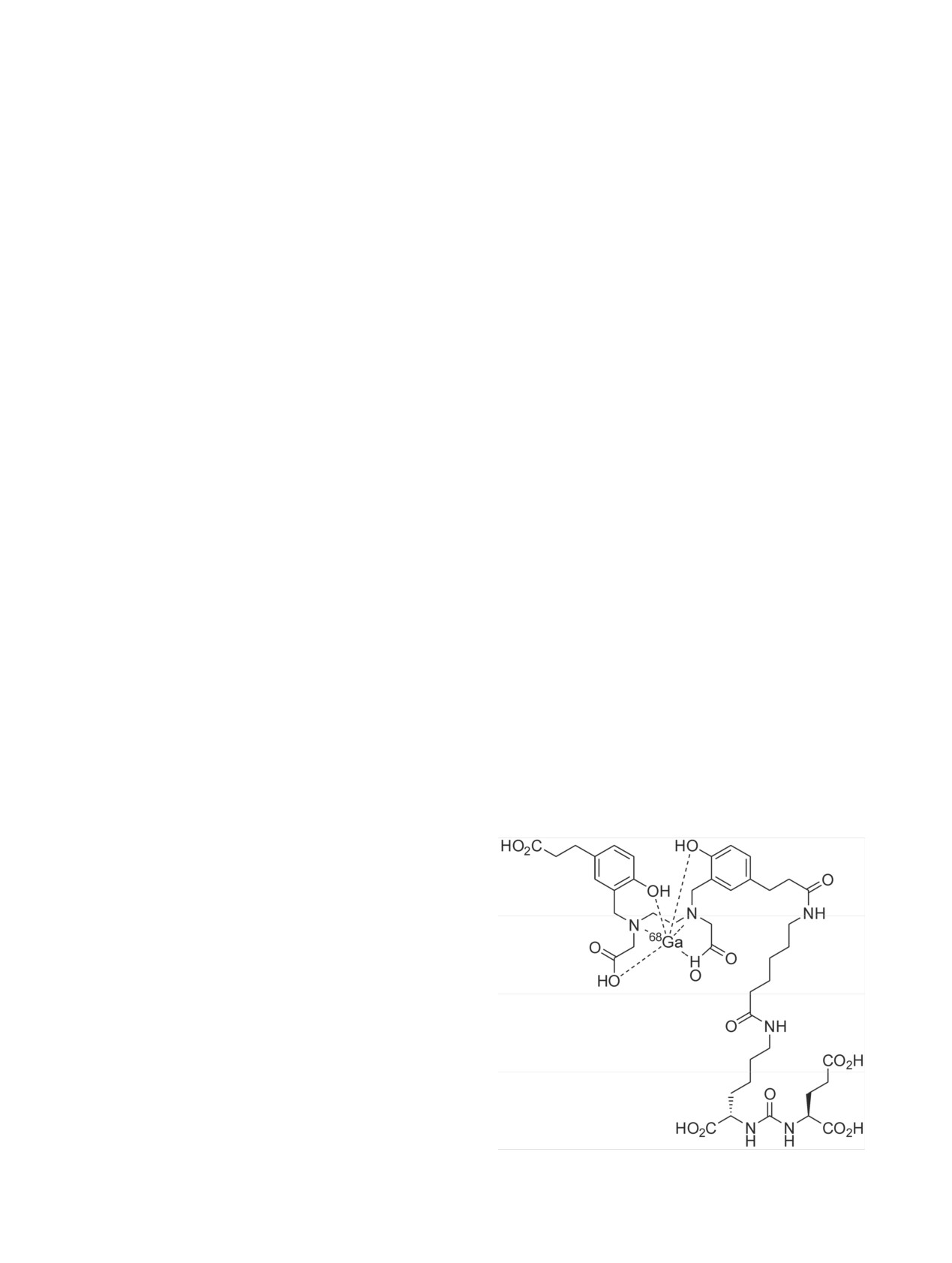
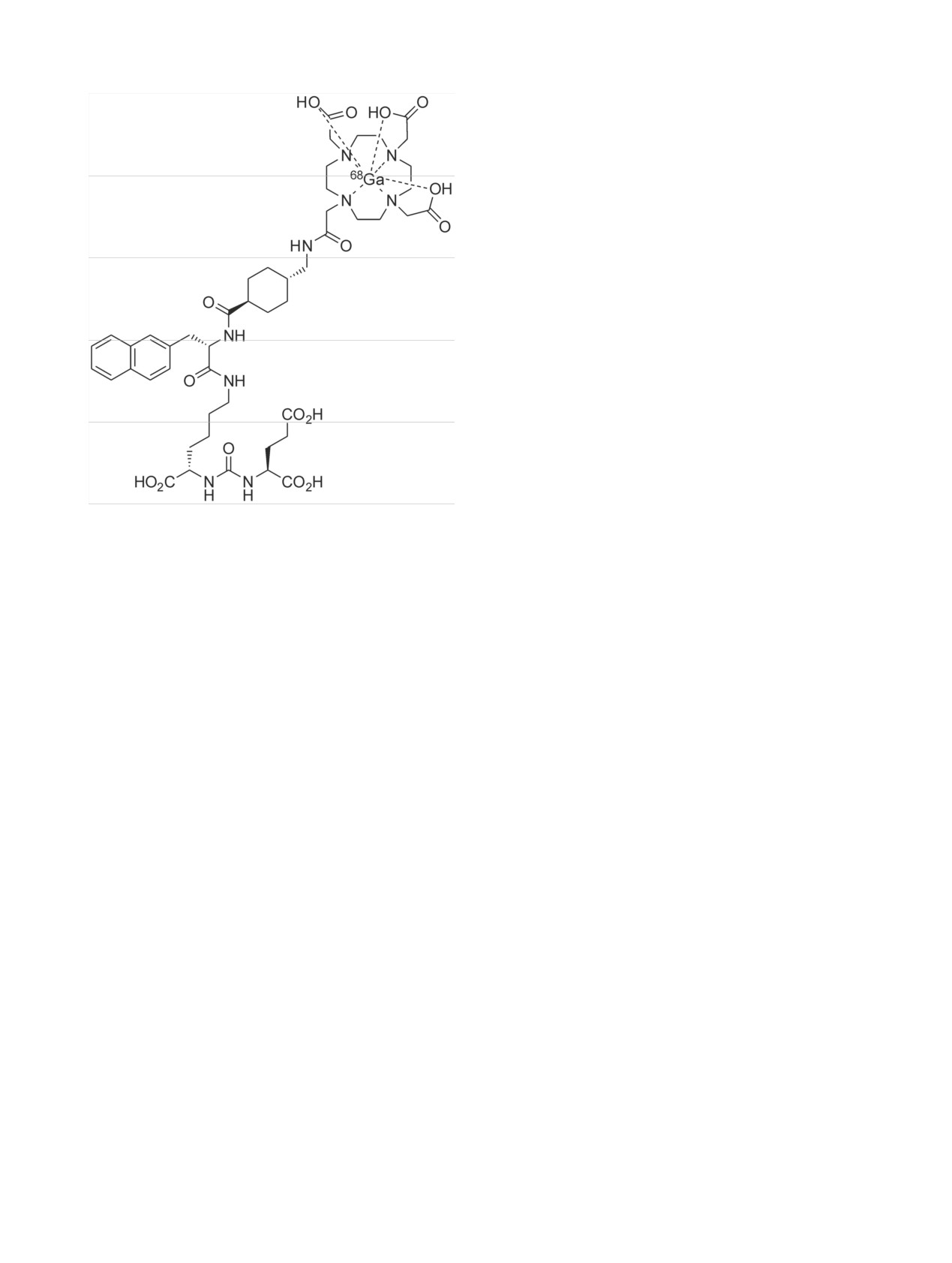
комплексов показаны ниже.
на мембранах всех клеток предстательной железы.
Гиперэкспрессия ПСМА наблюдается в опухолевых
клетках РПЖ. Многочисленные исследования про-
демонстрировали прямую корреляционную зависи-
мость между гиперэкспрессией ПСМА на поверхно-
сти клеток РПЖ и степенью анаплазии первичной
опухоли, появлением отдаленных метастазов и пе-
реходом заболевания в кастрационно-резистентную
форму [3]. Уровень экспрессии данного антигена
может служить прогностическим фактором возник-
новения рецидива заболевания [4]. Следует отме-
тить, что ПСМА не только является тканевым био-
маркером РПЖ, но и мишенью для таргетной тера-
пии с помощью лигандов, меченных β- или
α-эмиттерами.
В настоящее время предложено множество ли-
гандов к ПСМА, предназначенных для визуализа-
68Ga-ПСМА-11
524
Д. О. Антуганов и др.
в ПСМА-11 в автоматическом режиме на модуле,
сконструированном в НМИЦ им. В. А. Алмазова.
Экспериментальная часть
Оборудование: генератор 68Ga/68Ge ЗАО «Цик-
лотрон» (50 мКи, N 11-17, изготовлен 09.10.2017 г.,
Обнинск); горячая камера Manuela (Comecer, Ита-
лия); дозкалибратор Capintec; жидкостный хрома-
тограф Dionex ICS-300, оснащенный ультрафиоле-
товым и радиометрическим детектором; сканер для
тонкослойной хроматографии, оснащенный радио-
метрическим детектором, EZ-Scan (Carroll & Ram-
sey Associates, США); прибор для определения со-
держания бактериальных эндотоксинов (БЭ) En-
dosafe™ PTS (Charles River Endosafe, США); рН-
метр Seven Multi; автоматический криоскопиче-
ский осмометр Osmjmat 030 (Gonotec, Германия);
γ-спектрометр ORTEC GEM20P4-70 с полупровод-
никовым детектором HPGe.
Реагенты и материалы: хлорид натрия, ацетат
натрия, соляная кислота (1 моль/л), отвечающие
68Ga-ПСМА-617
требованиям фармакопейных стандартов качества;
пластины для ТСХ Silica gel 60 F254 (Merck, Гер-
Важную роль в производстве радиофармпрепа-
мания); метанол (Fisher Chemical, Великобрита-
ратов (РФП) на основе 68Ga играет очистка элюата,
ния); трифторуксуская кислота, тринатрия цитрат
полученного из генератора
68Ga/68Ge (произво-
(Sigma-Aldrich, США); ацетонитрил (НПО
дитель - ЗАО «Циклотрон»), который не может
«Криохром», Россия); лиганд ПСМА-11 и стандарт
быть напрямую использован для синтеза радиоли-
Ga-ПСМА-11 (ABX, Германия); картриджи QMA
гандов. В литературе описано три методики, полу-
Accell Light, Oasis WAX 1cc, Oasis WAX Short
чившие широкое распространение. Наиболее про-
(Waters, США); картриджи Alltech SАХ, PS-HCO3-,
стой способ - отбор той фракции, где наблюдается
сорбент SB (Marcherey-Nagel, Германия); вода для
максимальный выход
68Ga (фракционирование)
инъекций (Solopharm, Санкт-Петербург); колонки и
[10]. Этот подход уменьшает металлические и ра-
фриты для твердофазной экстракции (ТФЭ) объе-
дионуклидные примеси, но не исключает их. Вто-
мом 1 и 3 мл (Carlroth, Германия); стерилизующий
рая группа методов основана на сорбции изотопа в
фильтр для растворов PES 0.20 мм (Corning Inc.,
виде иона 68Ga3+ на катионообменных смолах с по-
Германия); стерилизующий фильтр для газов
следующими промывкой и элюированием. Методы
0.20 мм (Millipore, Германия); картриджи для ЛАЛ-
хорошо себя зарекомендовали в плане очистки от
теста (Charles River Endosafe, США). Все реагенты
химических примесей Ti4+, Zn2+ и Fe3+, а также от
использовали без очистки и других модификаций.
материнского 68Ge, но имеют недостаток из-за не-
обходимости использовать органические раствори-
Методы анализа. Подлинность
[68Ga]Ga-
тели в синтезе РФП [11-15]. Группа методов анио-
ПСМА-11 и радиохимическую чистоту препарата
нообменной очистки основана на способности гал-
определяли методом высокоэффективной жидкост-
лия образовывать комплексы [GaCl4]- и [GaCl6]3-
ной хроматографии (ВЭЖХ) и методом тонкослой-
при смешивании с концентрированными раствора-
ной хроматографии (ТСХ).
ми HCl или NaCl. Эти комплексы можно сорбиро-
Для ВЭЖХ анализа использовали хроматограф
вать на анионообменных смолах, а затем разру-
Dionex ICS-300, оснащенный двумя детекторами,
шать их путем пропускания через сорбент неболь-
соединенными последовательно: по поглощению в
шого количества воды [16-19].
УФ спектра (280 нм) и радиоактивности. Разделе-
В настоящей работе рассмотрена модификация
ние компонентов препарата регистрировали с по-
ранее описанной в статье [20] методики, включаю-
мощью программного обеспечения Chromeleon.
щая пропускание раствора 68Ga3+ через слой сухого
Идентификацию [68Ga]Ga-ПСМА-11 осуществляли
NaCl с последующим элюированием водой для
путем сопоставления времени удерживания основ-
инъекций. Помимо этого подобраны условия для
ного пика радиоактивности на хроматограмме, по-
максимального выхода очистки и введения изотопа
лученной с помощью радиометрического детекто-
Модификация анионообменной методики концентрирования изотопа 68Ga
525
ра, и времени удерживания его нерадиоактивного
Автоматический синтез
[68Ga]Ga-ПСМА-11.
аналога Ga-ПСМА-11 на ВЭЖХ хроматограмме с
68Ga3+ получали элюированием из генератора
учетом времени прохождения пробы между детек-
68Ge/68Ga 8 мл 0.1 моль/л HCl со скоростью 1.5-
торами.
1.6 мл/мин. Очистку 68Ga проводили на картридже
Oasis® WAX (ТФЭ колонка, 1 мл, 40 мг, размер час-
Условия хроматографирования: колонка YMC-
тиц 60 мкм) по методике, описанной в предыдущем
Park Polymer C18 6 мкм (4.6 × 250 мм), градиентный
разделе. Элюат смешивали с 20 мкг пептида ПСМА-
режим элюирования (ацетонитрил + вода, подкислен-
11, растворенного в 0.5 мл раствора 1.5 моль/л ацета-
ные 0.1% CF3COOH): 0-0.5 мин - 5% CH3CN, 0.5-
та натрия, и инкубировали без перемешивания при
13 мин - 5 → 45% CH3CN, 13-17 мин - 45 → 5%
95°C в течение 7 мин. Полученный раствор [68Ga]Ga-
CH3CN, 17-20 мин - 5% CH3CN. Скорость потока
ПСМА-11 передавали во флакон для сбора продукта,
элюента 0.9 мл/мин. В таких условиях время удержи-
предварительно наполненный 5 мл воды для инъек-
вания Ga-ПСМА-11 составляло 10.7 мин.
ций. Реактор дополнительно промывали 3 мл воды
В методе ТСХ использовали сканер для пластин
для инъекций, которую также передавали во флакон
ТСХ EZ-Scan, оснащенный детектором по радиоак-
для сбора продукта. Полученный продукт пропуска-
тивности. Элюирование проводили на двух под-
ли через стерильный фильтр с размером пор
вижных фазах восходящим способом. Элюент N 1:
0.20 мкм в пенициллиновый флакон для сбора препа-
1 моль/л CH3COONa : метанол = 1 : 1. В этих
рата. Время синтеза 23 мин. Радиохимический выход
условиях Rf составляет 0.0 для 68Ga3+ и 68Gaколлоид,
58 ± 3% (n = 10) от активности, элюированной с ге-
0.7 для [68Ga]Ga-ПСМА-11. Элюент N 2: раствор
нератора.
0.2 моль/л цитрата натрия. В этих условиях Rf со-
ставляет 0.9 для 68Ga3+, 0.05 для 68Gaколлоид, 0.2 для
Результаты и обсуждение
[68Ga]Ga-ПСМА-11.
Изотоничность готового препарата оценивали
[68Ga]Ga-ПСМА-11 синтезировали по односта-
по значению осмолярности криоскопическим мето-
дийной (one-pot) реакции из коммерчески доступно-
дом. Полученные значения - от 290 до 340 мОсм/л.
го предшественника (ПСМА-11). Для производства
pH препарата составлял от 6.0 до 6.5. Измерения
РФП использовали модуль, сконструированный в
проводили потенциометрическим методом.
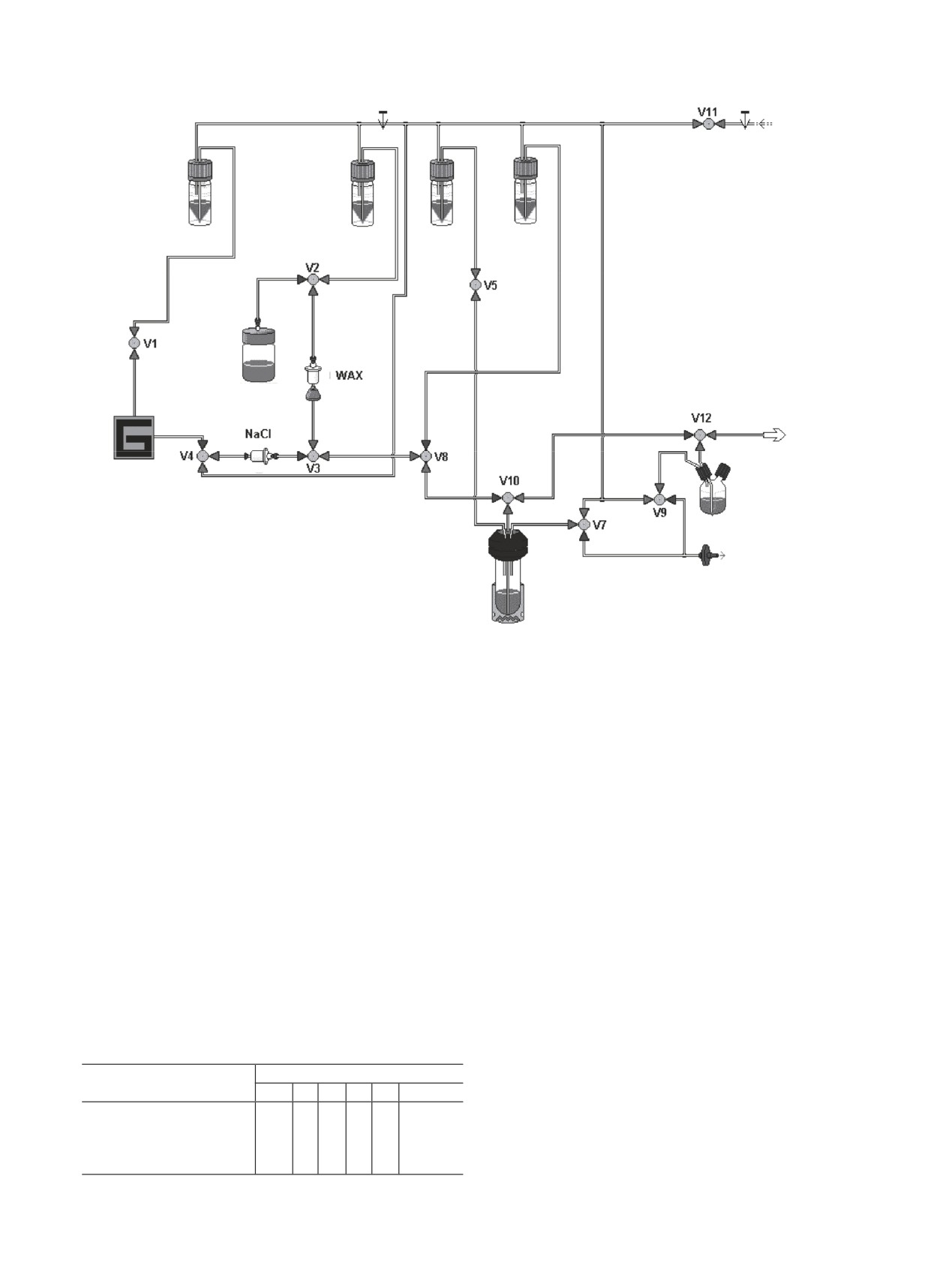
НМИЦ им. В. А. Алмазова (рис. 1). Данный модуль
адаптировали для проведения синтезов радиофарма-
Измерения 68Ge [проскока и радионуклидной
цевтических препаратов на основе 68Ga. Прибор
примеси (РНП)] проводили на γ-спектрометре
сконструирован с использованием мембранных кла-
ORTEC GEM20P4-70 с полупроводниковым детек-
панов Burkert 0127, фторопластовых капилляров с
тором HPGe; объем пробы 400 мкл, время измере-
внутренним диаметром 1/16 и 1/8", а также стан-
ния 3600 с. Измеряемую пробу ставили непосред-
дартных соединений с резьбами 1/4"-28 UNF. Все
ственно на окно детектора из-за очень малой актив-
компоненты широко используются производителя-
ности пробы. Растворы перед измерением выдер-
ми автоматических модулей синтеза. Ближайшие
живали не менее 7 сут. При этом устанавливалось
аналоги нашего устройства - модули Syntra Peptide
равновесие, и активность 68Ge соответствовала ак-
(Synthra GmbH, Германия) и Gerat13-68Ga (РНЦРХТ
тивности 68Ga. Расчет содержания в пробе 68Ga
им. акад. А. М. Гранова, Россия) [21]. В качестве
производили по γ-линии 1077.34 кэВ (3.22).
флаконов для реагентов использовали пробирки со
Определение БЭ проводили кинетическим хромо-
стандартным резьбовым соединением GL14 и GL18
генным методом с использованием портативной
(Duran, Германия). Реакция мечения проводили в
тест-системы Endosafe™ PTS. Испытание препарата
стандартном флаконе объемом 5 мл с V-образным
на стерильность проводили по ОФС.1.2.4.0003.15
дном и скручивающейся крышкой (Wheaton, США).
«Стерильность» методом прямого посева.
Первый этап экспериментов был связан с подбо-
Изучение сорбции 68Ga на анионообменных
ром оптимальных условий очистки 68Ga (активность
смолах. 68Ga3+ получали элюированием из генерато-
300-800 МБк) на анионообменных сорбентах, при
ра 68Ge/68Ga 5 мл 0.1 моль/л HCl. Полученный рас-
которых достигался бы максимальный выход очи-
твор пропускали через картридж, наполненный твер-
щенного изотопа. Нами были опробованы пять вари-
дым NaCl (ТФЭ-колонка, 3 мл, 3.2-3.8 г), и картридж
антов анионообменных сорбентов: QMA light Waters
с анионитом, на котором происходило извлечение
(1, 130 мг), Alltech SAX (2, 600 мг), Chromafix PS-
анионных комплексов галлия. Анионит промывали
HCO– (3, 45 мг), SB Marcherey Nagel (4, 45 мг) и Oa-
2 мл 5 моль/л NaCl и элюировали галлий 1.5 мл воды
sis® WAX 1 см3 (5, 30 мг), однако только для сор-
для инъекции в направлении, противоположном за-
бента 5 удалось достичь высоких значений сорбции
грузке изотопа на сорбент. Активность на каждом
[GaCl4]- - около 80% (см. таблицу). Мы попытались
этапе измеряли с помощью дозкалибратора.
увеличить это значение путем изготовления кар-
526
Д. О. Антуганов и др.
Азот
0.1 моль/л HCl
Вода
Вода
5 моль/л
NaCl
Отходы
В вентиляцию,
фильтр 0.2 мкм
Рис. 1. Конфигурация сконструированного модуля синтеза.
триджей увеличенной массы с использованием сор-
препарата определяли методом ВЭЖХ путем сопос-
бента Oasis® WAX и стандартных ТФЭ колонок
тавления времен удерживания [68Ga]Ga-ПСМА-11 и
объемом 1 см3 с полиэтиленовыми фритами. Увели-
его нерадиоактивного аналога. Радиохимическая
чение массы сорбента до 40 мг (картридж 6) ведет не
чистота (РХЧ) основного продукта [68Ga]Ga-ПСМА-
только к увеличению выхода сорбции, как видно из
11 по ВЭЖХ во всех случаях была >99%, и помимо
таблицы, но и к увеличению суммарного выхода
пика основного продукта на радиометрическом де-
очищенного изотопа до 80%.
текторе не было ни одного значимого пика примеси
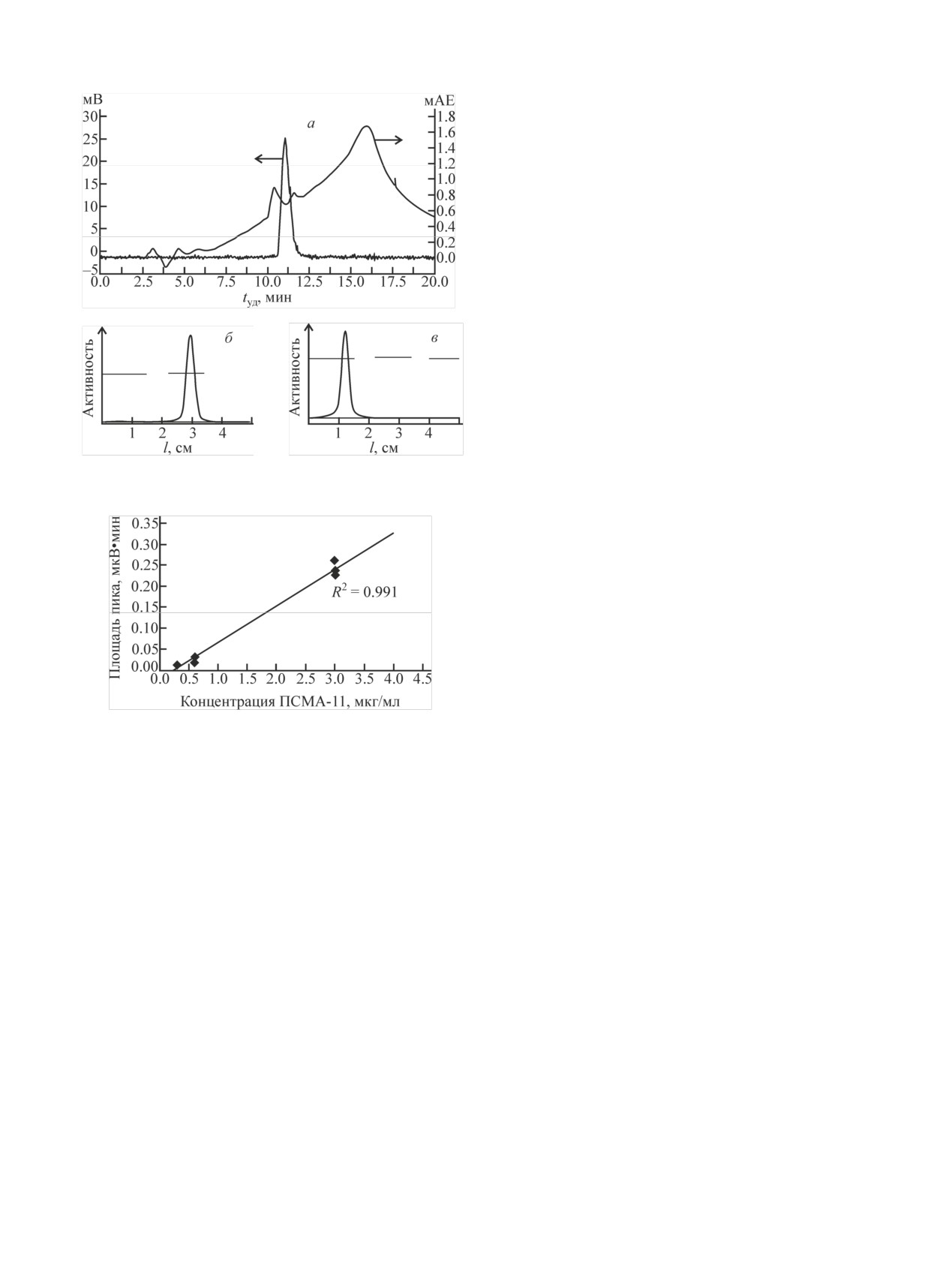
(рис. 2, а). Методом радио-ТСХ [25] (рис. 2, б, в)
Основные условия мечения молекулы пептида
определяли содержание несвязанного
68Ga3+ и
ПСМА-11 во всех случаях оставались неизменными:
«коллоидного» 68Ga (получаемого из-за неизотопно-
95°С, 7 мин. Эти условия были выбраны нами исхо-
го осаждения 68Ga). По данным радио-ТСХ, содер-
дя из многочисленных литературных данных. Кон-
жание основного продукта [68Ga]Ga-ПСМА-11 было
версию определяли методом радио-ТСХ; она состав-
98 ± 2% (n = 10), а содержание примесей несвязан-
ляла более 97% во всех случаях [22, 23].
ного 68Ga3+ и «коллоидного» 68Ga - не более 1 ± 1 и
Контроль качества проводили в соответствии с
2 ± 1% соответственно.
требованиями Европейской фармакопеи [24] для
Содержание непрореагировавшего ПСМА-11 в
аналогичных препаратов на основе 68Ga с использо-
препарате определяли методом ВЭЖХ. Было уста-
ванием методик, описанных выше. Подлинность
новлено, что зависимость площади пика ПСМА-11
от концентрации является линейной в диапазоне от
Очистка изотопа 68Ga на анионообменных сорбентах
0.3 до 3 мкг/мл. На рис. 3 представлен калибровоч-
Сорбент
Параметр
ный график. Среднее содержание ПСМА-11 в пре-
1
2
3
4
5
6 (n = 5)
парате не превышало 0.3-0.6 мкг/мл. Это значение
Сорбция, %
6
54
54
12
78
96 ± 3
Потеря при промывке, %
90
4
5
60
1
1 ± 1
ниже предела по методическим рекомендациям Ев-
Десорбция, %
66
65
54
53
81
82 ± 4
ропейской ассоциации ядерной медицины (EANM)
Суммарный выход, %
0.4
33
28
3
54
78 ± 3
и Сообщества ядерной медицины и молекулярной
Модификация анионообменной методики концентрирования изотопа 68Ga
527
ставляла не более 1·10-4%. Как в элюате галлия с
генератора, так и в продукте содержание 68Ge в каче-
стве РНП не превышает допустимого предела в со-
ответствии с требованиями фармакопеи (<5·10-3%)
[24]. Таким образом, предложенная методика очист-
ки элюата позволяет снизить содержание примеси
68Ge в препарате не менее чем в 50 раз.
Содержание остаточных растворителей (этанола)
не анализировали, так как в отличие от всех других
способов очистки изотопа для изготовления РФП
были использованы только водные растворы. Осмо-
лярность препарата в диапазоне от 239 до 376 мОсм/
л [27]. Содержание бактериальных эндотоксинов
менее 5.0 ЕЭ/мл. Испытание препарата на стериль-
ность проводили по ОФС.1.2.4.0003.15
«Сте-
рильность» методом прямого посева. Во всех случа-
ях препарат был стерильным [28]. Показана стабиль-
ность препарата в течение 4 ч. По показателям каче-
ства синтезированный препарат [68Ga]Ga-ПСМА-11,
раствор для инъекций отвечает требования проекта
Рис. 2. ВЭЖХ (а) и ТСХ (б, в) конечного продукта. Элюент
статьи Европейской фармакопеи на данный РФП.
для ТСХ: б - 1, в - 2.
Таким образом, улучшенная методика очистки
элюата из генератора 68Ga от примесей позволяет
быстро, в автоматическом режиме и с воспроизводи-
мым выходом получать препарат [68Ga]Ga-ПСМА-
11, пригодный для клинического использования.
Методика синтеза не является эксклюзивной и легко
может быть адаптирована к любым системам для
синтеза РФП на основе 68Ga.
Авторы признательны сотрудникам Радиевого
института им. В. Г. Хлопина С. А. Родионову и
Б. К. Куделину за неоценимую помощь в анализе
Рис. 3. Калибровочный график пептида ПСМА-11 (R2 = 0.991).
растворов на содержание 68Ge.
визуализации (SNMMI) - не более 6 мкг во вводи-
Список литературы
мой дозе для стандартного пациента массой 70 кг
[26]. Сумма площадей пиков возможных химиче-
[1] Torre L. A., Bray F., Siegel R. L. et al. // CA Cancer J. Clin.
2015. Vol. 65, N 2. P. 87-108.
ских примесей на УФ хроматограмме препарата с
[2] Israeli R. S., Powell C. T., Fair W. R., Heston W. D. // Cancer
относительным временем выхода в интервале от 0.8
Res. 1993. Vol. 53, N 2. P. 227-230.
до 1.3 от времени выхода ПСMA-11 не превышала
[3] Ghosh A., Heston W. D. // J. Cell Biochem. 2003. Vol. 91,
площадь пика ПСMA-11 (3 мкг/мл) в растворе срав-
N 3. P. 528-539.
нения.
[4] Ross J. S., Sheehan C. E., Fisher H. A. et al. // Clin. Cancer
Res. 2003. Vol. 9, N 17. P. 6357-6362.
Было проанализировано содержание радионук-
[5] Eder M., Schäfer M., Bauder-Wüst U. et al. // Bioconjugate
лидных примесей в элюате из генератора без очист-
Chem. 2012. Vol. 23, N 4. P. 688-697.
ки и в готовом препарате на трех параллельных се-
[6] Afshar-Oromieh A., Haberkorn U., Eder M. et al. // Eur. J.
риях. Измерения проводили на γ-спектрометре
Nucl. Med. Mol. Imag. 2012. Vol. 39, N 6. P. 1085-1086.
[7] Afshar-Oromieh A., Malcher A., Eder M. et al. // Eur. J. Nucl.
ORTEC GEM20P4-70 с полупроводниковым детек-
Med. Mol. Imag. 2013. Vol. 40, N 4. P. 486-495.
тором HPGe. До этого на данном генераторе было
[8] Benešová M., Bauder-Wüst U., Schäfer M. et al. // J. Nucl.
проведено около 200 элюирований. В результате
Med. 2015. Vol. 56, N 6. P. 914-920.
содержание 68Ge в неочищенном элюате было (4.5 ±
[9] Benešová M., Schäfer M., Bauder-Wüst U. et al. // J. Nucl.
0.4)·10-3% на момент элюирования, что соответству-
Med. 2016. Vol. 59, N 5. P. 1761-1775.
ет техническим условиям на данный генератор -
[10] Velikyan I., Beyer G. J., Langstrom B. et al. // Bioconjugate
Chem. 2004. Vol. 15, N 3. P. 554-560.
проскок 68Ge в элюат не более 5·10-3% (ТУ 95 821-
[11] Zhernosekov K. P., Filosofov D. V., Baum R. P. et al. //
06, ЗАО «Циклотрон»). Во всех трех сериях готово-
J. Nucl. Med. 2007. Vol. 48, N 10. P. 1741-1748.
го препарата активность 68Ge была меньше предела
[12] Asti M., De Pietri M., Fraternali A. et al. // Nucl. Med. Biol.
обнаружения при данных условиях измерений и со-
2008. Vol. 35, N 6. P. 721-724.
528
Д. О. Антуганов и др.
[13] Ocak M., Antretter M., Knopp R. et al. // Appl. Radiat. Isot.
и др. // Соврем. технологии в медицине. 2016. T. 8, N 4,
2010. Vol. 68, N 2. P. 297-302.
C. 51-58.
[14] Belosi F., Cicoria G., Lodi F. et al. // Curr. Radiopharm.
[22] Eder M., Neels O., Müller M. et al. // Pharmaceuticals. 2014.
2013. Vol. 6, N 2. P. 72-77.
Vol. 7, N 7. P. 779-796.
[15] Schultz M. K., Mueller D., Baum R. P. et al. // Appl. Radiat.
[23] Migliari S., Sammartano A., Scarlattei M. et al. // ACS
Isot. 2013. Vol. 76. P. 46-54.
Omega. 2017. Vol. 2, N 10. P. 7120-7126.
[16] Schuhmacher J., Maier-Borst W. // Int. J. Appl. Radiat. Isot.
[24] European Pharmacopoeia. Strasbourg: Council of Europe,
1981. Vol. 32, N 1. P. 31-36.
2017. 9th ed. Vol. 1. P. 1150-1152.
[17] Meyer G. J., Macke H., Schuhmacher J. et al. // Eur. J. Nucl.
[25] Larenkov A. A., Maruk A. Ya. // World Acad. Sci., Eng. Tech-
Med. Mol. Imag. 2004. Vol. 31, N 8. P. 1097-1104.
nol., Int. J. Chem., Mol., Nucl., Mater. Metall. Eng. 2016.
[18] De Blois E., Sze Chan H., Naidoo C. et al. // Appl. Radiat.
Vol. 10, N 9. P. 1120-1127.
Isot. 2011. Vol. 69, N 2. P. 308-315.
[26] Fendler W. P., Eiber M., Beheshti M. et al. // Eur. J. Nucl.
[19] Müller D., Klette I., Baum R. P. et al. // World J. Nucl. Med.
Med. Mol. Imag. 2017. Vol. 44, N 6. P. 1014-1024.
2011. Vol. 10. P. 77-78.
[27] ОФС.1.2.1.0003.15: Осмолярность
// Государственная
[20] Ben Azzouna R., Alshoukr F., Leygnac S. et al. // J. Label.
фармакопея Российской Федерации. 2015. XIII изд. Т. 1.
Compd. Radiopharm. 2015. Vol. 58, N 10. P. 403-410.
[28] ОФС.1.2.4.0003.15: Стерильность // Государственная фар-
[21] Тлостанова М. С., Ходжибекова М. М., Панфиленко А. А.
макопея Российской Федерации. 2015. XIII изд. Т. 1.