512
Радиохимия, 2019, т. 61, N 6, c. 512-515
Сорбция радионуклидов на гидроортофосфате церия(IV)
Ce(PO4)(HPO4)0.5(H2O)0.5
© А. Ю. Романчук*а, Т. О. Шекуноваа,б, А. И. Ларинаа, О. С. Ивановаб, А. Е. Баранчикова,б,
В. К. Иванова,б, С. Н. Калмыкова,в
а Московский государственный университет им. М. В. Ломоносова, 119991, Москва, Ленинские горы, д. 1;
*e-mail: romanchuk.anna@gmail.com
б Институт общей и неорганической химии им. Н. С. Курнакова РАН, 119991, Москва, Ленинский пр., д. 31
в Институт геохимии и аналитической химии им. В. И. Вернадского РАН, 119991, Москва, ул. Косыгина, д. 19
Получена 10.12.2018, после доработки 13.02.2019, принята к публикации 13.02.2019
УДК 546.655.4’185:544.723+546.79
Впервые изучены сорбционные свойства гидроортофосфата церия(IV) состава Ce(PO4)(HPO4)0.5·
(H2O)0.5 по отношению к радионуклидам. Показано, что степень сорбции из водных растворов превос-
ходит 95% для Np(V) при рН > 7, для Sr(II) при рН > 9, для Am(III) и U(VI) при рН > 5 и для Th(IV) при
рН > 2. Также обнаружено быстрое и количественное выщелачивание радионуклидов с поверхности
сорбента в кислой среде, что свидетельствует об обратимости сорбции.
Ключевые слова: радионуклиды, сорбция, выщелачивание, гидроортофосфат церия(IV).
DOI: 10.1134/S00338311190600121
Одной из важных задач ядерной энергетики яв-
(PO4)1.1·0.5H2O
(2), Ce(OH)0.27(PO4)0.27(HPO4)1.46·
ляется разработка эффективных методов обраще-
0.55H2O (3), Ce(OH)0.45(PO4)0.45(HPO4)1.1·0.33H2O (4),
ния с радиоактивными отходами (РАО) и их после-
Ce(NH4PO4)0.44(HPO4)1.56
(5), Ce(OH)0.375(PO4)0.375·
дующего долговременного хранения. В качестве
(NH4)0.09H1.16(PO4)1.25·0.25H2O
(6), CeO0.21(PO4)·
перспективных материалов для изоляции компо-
(NH4HPO4)0.45(H2PO4)0.13 (7). Было обнаружено, что
нентов РАО в настоящее время рассматривают
только соединения 1 и 3 проявляют ионообменные
фосфатные керамики, в первую очередь со струк-
свойства в кислой среде, соединение 7 не способно
турой природного минерала монацита (Ce,La,
к ионному обмену, в то время как другие изученные
Y,Ca,Th)PO4 [1]. Такие материалы представляют
соединения проявили ионообменные свойства в ще-
интерес благодаря высокой химической стабильно-
лочной среде.
сти и устойчивости к действию ионизирующего
В качестве материалов для сорбции катионов
излучения [2]. Существует множество синтетиче-
металлов из водных растворов наиболее перспек-
ских соединений со структурой монацита (моно-
тивны соединения, имеющие туннельную или
клинная сингония, пространственная группа P21/n),
слоистую структуру. В работе [13] был синтезиро-
в том числе материалы на основе фосфатов церия
ван гидроортофосфат состава Сe(PO4)1.5(H2O)·
(III) и (IV) [3]. Известно, что Ce(IV) является хими-
(H3O)0.5(H2O)0.5 с туннельной структурой, проявив-
ческим аналогом U(IV), Th(IV) и Pu(IV) [4-8] вви-
ший высокую сорбционную емкость по отноше-
ду близости ионных радиусов (для КЧ 8 ионный
нию к ионам щелочных металлов. Авторами была
радиус составляют 97 пм для Ce(IV) и 100, 105 и
отмечена селективность ионного обмена
[14]
96 пм для U(IV), Th(IV) и Pu(IV) соответственно
(предпоч-тение катионам с малым ионным радиу-
[9]). Исходя из этого можно предположить, что
сом, Li+ > Na+ = K+ > Rb+ > Cs+). В работе [15] син-
фосфаты Ce(IV) должны быть эффективными мате-
тезировали кристаллический смешанный фосфат
риалами для извлечения актинидов, как, например,
церия K2Ce(PO4)2 со структурой, включающей в
фосфат Th(IV) β-Th4(PO4)4P2O7 является известной
себя одномерные каналы. Было показано, что ка-
матрицей для иммобилизации U и Pu [10].
тионы калия способны обмениваться на другие ка-
тионы (например, Sr2+, имеющего близкий ионный
В настоящее время известно ограниченное коли-
радиус) [16]. Отмечено, что катионы калия способ-
чество кристаллических фосфатов Ce(IV), их структу-
ны также обмениваться на ионы гидроксония и
ра подробно описана в работе [11], однако данные об
другие однозарядные катионы.
ионообменных и сорбционных свойствах таких со-
единений весьма ограничены. Так, в работе [12] син-
Ранее нами была разработана методика синтеза
тезировали ряд кристаллических фосфатов Ce(IV),
церийсодержащего фосфорнокислого геля [17] и
которым были приписаны составы Ce(OH)1.62·
предложен эффективный способ иммобилизации
(NH4HPO4)0.35(H2PO4)0.68(PO4)0.45·0.6H2O (1), Ce(OH)0.7·
Th(IV) из жидких РАО с использованием подобных
Сорбция радионуклидов на гидроортофосфате церия(IV) Ce(PO4)(HPO4)0.5(H2O)0.5
513
материалов [18]. Было показано, что при гидротер-
Сорбционные эксперименты проводили при ком-
мальной обработке церийсодержащего фосфорно-
натной температуре. В качестве фонового электро-
кислого геля формируется соединение состава
лита использовали 0.1 или 0.01 моль/л NaClO4 (х.ч.).
Ce(PO4)(HPO4)0.5(H2O)0.5, на котором сорбция ра-
Сорбцию проводили в пластиковых флаконах. При
дионуклидов до сих пор не была изучена [17]. В то
этом параллельно проводили эксперимент в отсут-
же время этот гидроортофосат Ce(IV) является пер-
ствие твердой фазы для определения сорбции ра-
спективным материалом для иммобилизации РАО,
дионуклидов на стенках флаконов. При проведении
поскольку при термической обработке он транс-
экспериментов во флакон с суспензией Ce(PO4)·
формируется в CePO4 с структурой монацита [19].
(HPO4)0.5(H2O)0.5 с концентрацией 0.27 г/л добавля-
ли аликвоту растворов радионуклидов (239Np, 241Am,
В настоящей работе нами была изучена сорбция
233,232U, 234Th, 90Sr, 137Cs). 234Th предварительно вы-
различных радионуклидов на кристаллическом гид-
деляли из раствора 238U методом ионного обмена на
роортофосфате церия(IV) состава Ce(PO4)(HPO4)0.5·
хроматографической колонке, заполненной Dowex
(H2O)0.5 (далее ГОФ-Ce).
1×8 (Serpa), а 239Np - путем экстракции триоктила-
мином в толуоле из солянокислого раствора 243Am.
Экспериментальная часть
Необходимое значение pH в диапазоне от 1 до 11
устанавливали с помощью разбавленных растворов
В работе использовали следующие реактивы:
NaOH и HClO4. Разделение фаз проводили центри-
Ce(NO3)3·6H2O
(99.9%, Ланхит), ортофосфорную
фугированием при
40000 g в течение
15 мин
кислоту
(85%, ч.д.а, Лабтех), водный раствор
(Beckman Allegra, США). Активность растворов из-
NH4OH (25%, ос.ч., ХИММЕД), изопропанол (ос.ч.,
меряли методом жидкостной сцинтилляционной
ХИММЕД), деионизованную воду (18 MΩ). Синтез
спектрометрии (Perkin Elmer Quantulus 1220, США).
ГОФ-Ce проводили по методике, аналогичной опи-
Для исследования кинетики выщелачивания ра-
санной нами ранее [17]. Навеску 0.7 г нанокристал-
дионуклида с поверхности Ce(PO4)(HPO4)0.5(H2O)0.5
лического CeO2, полученного по способу, изложен-
в образцах с сорбцией более 90% раствор подкисля-
ному в работах [20-22], растворяли в 5 мл концен-
ли до pH 1.3 путем добавления разбавленной HClO4.
трированной H3PO4 (85 мас%, ρ = 1.689 г/см3) при
Через определенные промежутки времени отбирали
80°С в течение 4 ч. Мольное соотношение Ce : P
аликвоты раствора, в которых после центрифугиро-
составляло 1 : 18. После остывания раствора к нему
вания определяли содержание радионуклидов. Сте-
при интенсивном перемешивании добавляли 35 мл
пень растворения Ce(PO4)(HPO4)0.5(H2O)0.5 в услови-
деионизованной воды. При этом в течение первых
ях эксперимента по выщелачиванию определяли
минут взаимодействия формировался гель, который
путем масс-спектрометрического измерения содер-
вместе с маточным раствором помещали в тефлоно-
жания церия в растворах (Agilent 7500C, Agilent
вый автоклав (степень заполнения ~40%) и подвер-
Technologies, Япония).
гали гидротермальной обработке при 180°С в тече-
ние суток. В результате получали кристаллический
Результаты и обсуждение
порошок светло-желтого цвета, который очищали
от избытка ортофосфорной кислоты многократной
Дифрактограмма синтезированного исходного
декантацией относительно деионизованной воды,
церийсодержащего фосфорнокислого геля представ-
после чего высушивали при 60°С на воздухе.
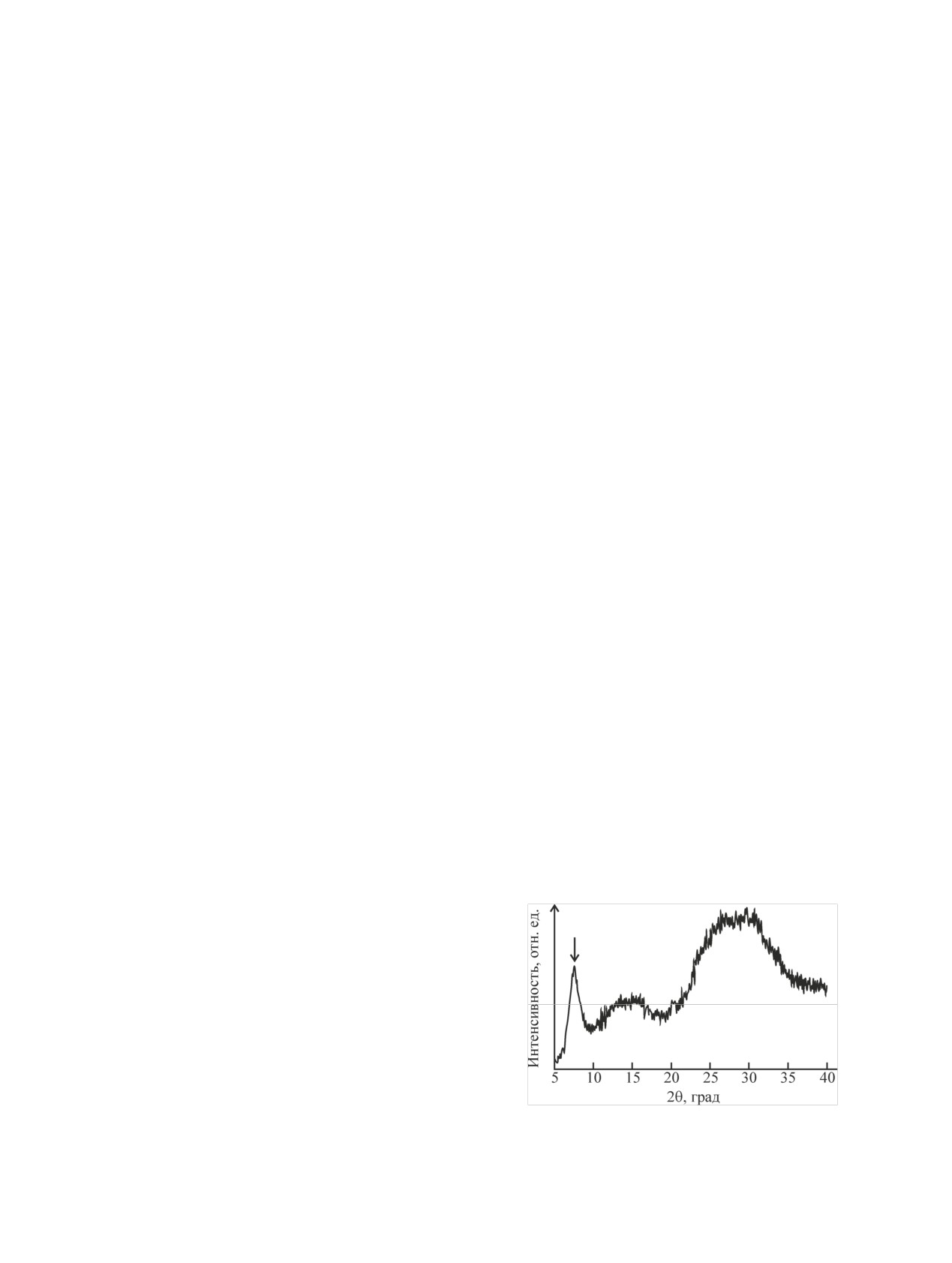
лена на рис. 1. Из рис. 1 видно, что гель является
преимущественно рентгеноаморфным, однако при
Фазовый состав синтезированных геля и порош-
ка ГОФ-Сe анализировали на дифрактометре Bruker
D8 Advance (CuKα-излучение, θ-2θ-геометрия) в
диапазоне углов 2θ 5-60° с шагом 0.01-0.02° и вре-
менем накопления сигнала не менее 0.3 с на точку.
Микроструктуру анализировали с помощью растро-
вого электронного микроскопа Carl Zeiss NVision
40, оснащенного микрозондовым анализатором Ox-
ford Instruments X-MAX, при ускоряющем напряже-
нии 1 кВ. Удельную площадь поверхности ГОФ-Сe
определяли методом низкотемпературной адсорб-
ции азота на анализаторе АТХ-06 (Катакон, Россия)
в интервале относительных давлений азота 0.05-
Рис. 1. Дифрактограмма исходного церийсодержащего фос-
0.25 с использованием модели Брунауэра-Эммета-
форнокислого геля, полученного при смешивании раствора
Теллера по 5 точкам.
CeO2 в концентрированной H3PO4 с деионизованной водой.
514
А. Ю. Романчук и др.
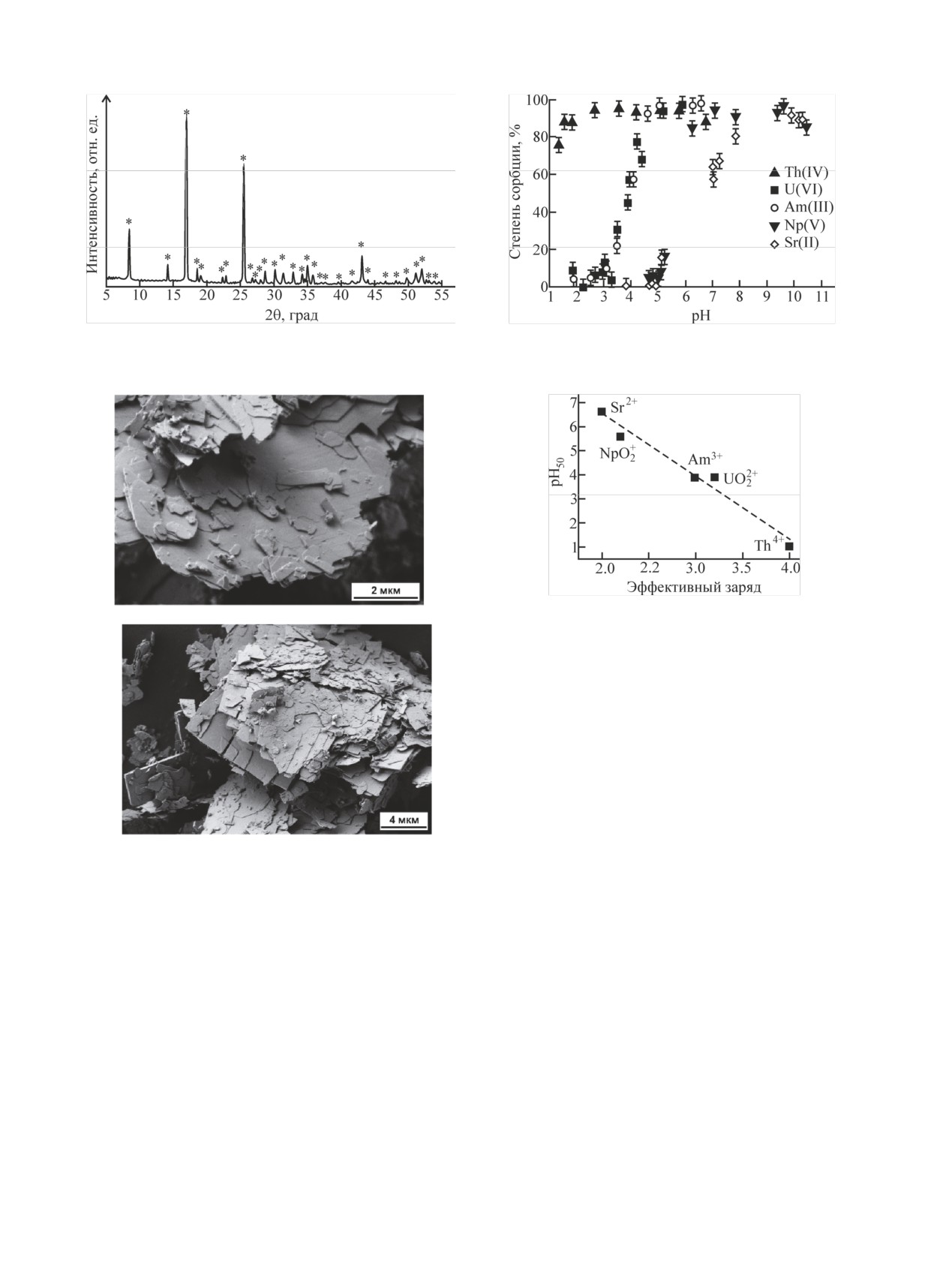
Рис. 2. Дифрактограмма Ce(PO4)(HPO4)0.5(H2O)0.5 (его пики
Рис. 4. Зависимость сорбции 239Np, 241Am, 233,232U, 234Th, 90Sr от
рН суспензии Ce(PO4)(HPO4)0.5(H2O)0.5 (концентрация твердой
отмечены звездочкой), полученного из геля при гидротермаль-
ной обработке.
фазы 0.27 г/л, электролит 0.1 моль/л NaClO4).
Рис. 5. Зависимость pH50 от эффективного заряда катиона при
сорбции различных радионуклидов на Ce(PO4)(HPO4)0.5(H2O)0.5.
пластинчатой морфологией. При этом ГОФ-Ce ха-
рактеризуется относительно низкой удельной пло-
щадью поверхности, составляющей 6 м2/г.
При изучении сорбционных свойств полученно-
го порошка ГОФ-Ce на первоначальном этапе были
получены зависимости сорбции радионуклидов
239Np,
241Am, 233,232U,
234Th,
90Sr от pH суспензии
(рис. 4). Из рис. 4 видно, что ГОФ-Ce обладает высо-
кой сорбционной способностью по отношению к ис-
Рис. 3. Микрофотографии частиц синтезированного порошка
следуемым радионуклидам. Так, несмотря на относи-
Ce(PO4)(HPO4)0.5(H2O)0.5.
тельно низкое содержание твердой фазы (0.27 г/л) с
низкой удельной площадью поверхности, сорбция
2θ = 7.5° находится ярко выраженный уширенный
свыше
95% наблюдается для Th(IV) при
максимум, который может свидетельствовать о су-
рН > 2, для Am(III) и U(VI) при рН > 5, для Np(V)
ществовании в церийсодержащем фосфорнокислом
при рН > 7 и для Sr(II) при рН > 9. Из рис. 4 следует,
геле ближнего порядка с характеристическим рас-
что значения рН, соответствующие сорбции 50%
стоянием ~1.2 нм. Ранее было показано, что схожие
радионуклида (рН50), существенно различаются.
по составу соединения имеют слоистую структуру с
Сорбционная активность катионов зависит от их
межслоевым расстоянием 1.45-1.80 нм [23].
заряда, а эффективный заряд актинидов, согласно
В результате гидротермальной обработки геля
Чоппину [26], возрастает в зависимости от степени
формируется кристаллическое соединение Ce(PO4)·
окисления в ряду An(V) < An(III) ~ An(VI) < An(IV)
(HPO4)0.5(H2O)0.5, что подтверждают данные дифрак-
и составляет +2.2, +3, +3.3 и +4 соответственно.
тограммы на рис. 2. Согласно данным работ [24, 25],
Важно отметить, что свойства катионов уранила и
это соединение обладает слоистой структурой. По
нептуноила определяются именно эффективным
данным растровой электронной микроскопии
зарядом катиона, а не его формальным зарядом. На
(рис. 3), полученный ГОФ-Ce состоит из частиц с
рис. 5 приведена зависимость рН50 от эффективного
Сорбция радионуклидов на гидроортофосфате церия(IV) Ce(PO4)(HPO4)0.5(H2O)0.5
515
ном хранении РАО требует дальнейших исследова-
ний.
Эксперименты по сорбции радионуклидов вы-
полнены за счет средств РНФ (проект N 14-13-
01279). Эксперименты по синтезу, анализу церийсо-
держащего фосфорнокислого геля и порошка вы-
полнены при поддержке РФФИ (проект N 18-33-
00275).
Список литературы
Рис. 6. Кинетика выщелачивания радионуклидов с поверхно-
[1] Логинова Е. Е., Орлова А. И., Михайлов Д. А. и др. // Ра-
сти Ce(PO4)(HPO4)0.5(H2O)0.5 при pH 1.3.
диохимия. 2011. Т. 53, N 6. C. 500-508.
[2] Neumeier S., Arinicheva Y., Ji Y. et al. // Radiochim. Acta.
2017. Vol. 115. P. 961-984.
заряда катиона актинида, которая удовлетворитель-
[3] Clavier N., Podor R., Dacheux N. // J. Eur. Ceram. Soc. 2011.
но объясняет экспериментальные результаты по
Vol. 31. P. 941-976.
сорбции: наблюдается линейная корреляция между
[4] Dacheux N., Clavier N., Wallez G., et al. // Mater. Res. Bull.
эффективным зарядом и значением рН50.
2005. Vol. 40. P. 2225-2242.
[5] Iglesias I., Alfonso B. F., Amghouz Z. et al. // Ceram. Int.
Были также проведены эксперименты по сорб-
2017. Vol. 43. P. 10776-10783.
ции 137Cs в широком диапазоне рН при ионной силе
[6] Qin D., Gausse C., Szenknect S. et al. // J. Chem. Thermodyn.
2017. Vol. 114. P. 151-164.
раствора 0.01 и 0.1 моль/л, однако величина сорб-
[7] Orlova M. P., Kitaev D. B., Spiridonova M. L. et al. // Crys-
ции во всех случаях не превысила 5%. Варьирова-
tallogr. Rep. 2005. Vol. 50. P. 918-922.
ние ионной силы также не привело к увеличению
[8] Dacheux N., Clavier N., Wallez G. et al. // Solid State Sci.
сорбции Sr(II) на ГОФ-Ce.
2007. Vol. 9. P. 619-627.
[9] Shannon R. D., Prewitt C. T. // Acta Crystallogr., Sect. B.
Для уточнения механизмов сорбции радионукли-
1969. Vol. 25. P. 925-946.
дов поверхностью ГОФ-Ce были проведены экспе-
[10] Schlenz H., Neumeier S., Hirsch A. et al. // Highlights in Ap-
рименты по их выщелачиванию при pH 1.3. Раство-
plied Mineralogy / Eds S. Heuss-Aßbichler, G. Amthauer, M.
римость сорбента при этом оказалась крайне низкой
John. De Gruyter, 2018. P. 171-196.
[11] Achary S. N., Bevara S., Tyagi A. K. // Coord. Chem. Rev.
и не превышала 1 мг/л. Кинетические зависимости
2017. Vol. 340. P. 266-297.
выщелачивания приведены на рис. 6. Видно, что в
[12] Herman R. G., Clearfield A. // J. Inorg. Nucl. Chem. 1976.
течение нескольких часов наблюдается количест-
Vol. 38. P. 853-858.
венное выщелачивание всех исследуемых радио-
[13] Nazaraly M., Chaneac C., Ribot F. et al. // J. Phys. Chem.
нуклидов [Sr(II), Am(III), Np(V), U(VI)] с поверхно-
Solids. 2007. Vol. 68. P. 795-798.
[14] Nazaraly M., Quarton M., Wallez G. et al. // Solid State Sci.
сти ГОФ-Ce, что свидетельствует об обратимости
2007. Vol. 9. P. 672-677.
сорбции, и это необходимо учитывать при его при-
[15] Bevara S., Achary S. N., Patwe S. J. et al. // Dalton Trans.
менении в качестве сорбента радионуклидов. Иная
2016. Vol. 45. P. 980-991.
картина наблюдалась нами ранее при анализе кине-
[16] Bevara S., Achary S. N., Patwe S. J. et al. // AIP Conf. Proc.
тики выщелачивания Am(III) с поверхности орто-
2016. Vol. 1731. Paper 140040.
фосфатов РЗЭ со структурой монацита [27]: данный
[17] Shekunova T. O., Baranchikov A. E., Ivanova O. S. et al. //
J. Non-Cryst. Solids. 2016. Vol. 447. P. 183-189.
процесс протекал крайне медленно, что свидетель-
[18] Романчук А. Ю., Шекунова Т. О., Петров В. Г. и др. //
ствовало в пользу частичного встраивания радио-
Радиохимия. 2018. Т. 60, N 6. С. 525-529.
нуклида в кристаллическую структуру сорбента. В
[19] Brandel V., Clavier N., Dacheux N. // J. Solid State Chem.
то же время полученные нами данные указывают на
2005. Vol. 178. P. 1054-1063.
то, что при использовании в качестве сорбента
[20] Ivanov V. K., Baranchikov A. E., Polezhaeva O. S. et al. //
Russ. J. Inorg. Chem. 2010. Vol. 55. P. 325-327.
ГОФ-Ce реализуется лишь сорбция радионуклидов
[21] Polezhaeva O. S., Yaroshinskaya N. V., Ivanov V. K. // Russ.
на его поверхности, и их встраивания в кристалли-
J. Inorg. Chem. 2007. Vol. 52. P. 1184-1188.
ческую структуру данного соединения не происхо-
[22] Ivanov V. K., Polezhaeva O. S., Tret’yakov Y. D. // Russ. J.
дит. Можно ожидать, что при дальнейшей высоко-
Gen. Chem. 2010. Vol. 80. P. 604-617.
температурной обработке ГОФ-Ce будет происхо-
[23] Tsuhako M., Danjo M., Baba Y. et al. // Bull. Chem. Soc. Jpn.
1997. Vol. 70. P. 143-148.
дить встраивание радионуклидов в структуру обра-
[24] Nazaraly M., Wallez G., Chaneac C. et al. // Angew. Chem.
зующегося при этом монацита.
Int. Ed. 2005. Vol. 44. P. 5691-5694.
[25] Nazaraly M., Wallez G., Chaneac C. et al. // J. Phys. Chem.
Таким образом, нами была подтверждена эффек-
Solids. 2006. Vol. 67. P. 1075-1078.
тивная сорбция Sr(II), Am(III), Th(IV), Np(V), U(VI)
[26] Choppin G. R. // Marine Chem. 2006. Vol. 99. P. 83-92.
на поверхности ГОФ-Ce. Оценка эффективности
[27] Romanchuk A. Y., Gracheva N. N., Bryukhanova K. I. et al. //
применения данного материала при долговремен-
Mendeleev Commun. 2018. Vol. 28. P. 303-305.